рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
Обращение времен.
Обращение времен. - Лекция, раздел Медицина, Энтропия ...
 Если обратить время, то полная энтропия замкнутой системы стала бы убывать, тепло потекло бы от холодного тела к горячему.
Если обратить время, то полная энтропия замкнутой системы стала бы убывать, тепло потекло бы от холодного тела к горячему.
V1=V2=1см3, P=1атм. Число частиц в
первом равно числу Авогадро делённому на количество кубических сантиметров в 22,4 л., т.е. 2,7 * 1019 . Второй сосуд пуст. Убрали перегородку. Примерно 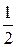 частиц перейдёт во второй сосуд. Сколько бы мы не ждали, обратного процесса не будет. Будут лишь незначительные флуктуации. 70% времени и частиц в каждом объёме от
частиц перейдёт во второй сосуд. Сколько бы мы не ждали, обратного процесса не будет. Будут лишь незначительные флуктуации. 70% времени и частиц в каждом объёме от 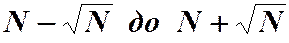 , где N – среднее число частиц.
, где N – среднее число частиц. 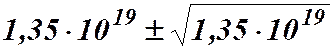 , флуктуации настолько малы.
, флуктуации настолько малы.
Предположим, что время пошло вспять. При этом второй сосуд опустеет и в нём - вакуум. При наблюдении обратного хода, заснятого на плёнке мы не обнаружили ничего неестественного, ни один физический закон не будет нарушен. Но существует бесчисленное множество других конфигураций, когда во втором сосуде и в первом число частиц почти одинаково. Поэтому на практике такой случай допустим, но его вероятность стремится к нулю. Дальнейший обратный ход привёл бы к постепенному заполнению второго сосуда, энтропия возрастает.
– Конец работы –
Эта тема принадлежит разделу:
Энтропия
План лекции... Энтропия... Закон возрастания...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Обращение времен.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов