рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Военное дело
- /
- ВОЕННАЯ ТОКСИКОЛОГИЯ, РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ ЗАЩИТА
Реферат Курсовая Конспект
ВОЕННАЯ ТОКСИКОЛОГИЯ, РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ ЗАЩИТА
ВОЕННАЯ ТОКСИКОЛОГИЯ, РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ ЗАЩИТА - раздел Военное дело, Военная Токсикология, Радиобиология И Медици...
ВОЕННАЯ ТОКСИКОЛОГИЯ, РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ
ЗАЩИТА
Военно-медицинская академия имени С. М. Кирова
ВОЕННАЯ ТОКСИКОЛОГИЯ,
РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ ЗАЩИТА
Учебник
Под редакцией профессора С. А. Куценко
Рекомендуется Учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для студентов медицинских вузов
Санкт-Петербург ФОЛИАНТ 2004
УДК 615.9+612.014.482:614 ББК58; 52.84+53.6:51.26
Рецензенты:
Начальник кафедры военной токсикологии и медицинской защиты Государственного института усовершенствования врачей МО РФ доктор медицинских наук, профессор В. Б. Иванов
Председатель межведомственного совета
по токсикологии РАМН и МЗ РФ, Главный токсиколог МЗ РФ,
директор Института токсикологии МЗ РФ
доктор медицинских наук, профессор А. Н. Петров
Начальник кафедры военной и экстремальной медицины
Санкт-Петербургской государственной медицинской академии имени И. И. Мечникова доктор медицинских наук, профессор Н. А. Смирнов
Заведующий кафедрой общей и клинической токсикологии Сенкт-Петербургской медицинской академии последипломного образования доктор медицинских наук, профессор В. В. Шилов
Куценко С. А., Бутомо Н. В., Гребенюк А. Н. и др.
Военная токсикология, радиобиология и медицинская защита:
Учебник / Под ред. С. А. Куценко. —
СПб: ООО «Издательство ФОЛИАНТ», 2004. — 528 с: ил.
ISBN 5-93929-082-5
Учебник подготовлен и составлен в соответствии с учебной программой по военной токсикологии, радиобиологии и медицинской защите. В нем рассматриваются предмет и задачи учебной дисциплины, вопросы общей токсикологии и радиобиологии, дается подробная характеристика поражающих факторов химической и радиационной природы, актуальных для военной медицины, и мероприятий медицинской противохимической и противорадиационной защиты. Учебник предназначен для студентов медицинских вузов, но может быть использован и в практической деятельности врачей различных специальностей.
Авторский коллектив учебника - сотрудники кафедры военной токсикологии и медицинской защиты Военно-медицинской академии имени С. М. Кирова
КУЦЕНКО Сергей Алексеевич — начальник кафедры — Главный токсиколог-радиолог МО РФ, доктор медицинских наук, профессор БУТОМО Николай Викторович — профессор кафедры, Заслуженный работник высшей школы РФ, доктор медицинских наук, профессор ГРЕБЕНЮК Александр Николаевич — заместитель начальника кафедры, доктор
медицинских наук, профессор ИВНИЦКИЙ Юрий Юрьевич — профессор кафедры, доктор медицинских наук, профессор
МЕЛЬНИЧУК Валерий Павлович — доцент кафедры, кандидат медицинских наук, доцент
ПРЕОБРАЖЕНСКАЯ Татьяна Николаевна — преподаватель кафедры, кандидат биологических наук
РЫБАЛКО Виктор Михайлович — профессор кафедры, Заслуженный работник высшей школы РФ, доктор медицинских наук, профессор
САВАТЕЕВ Николай Васильевич — профессор кафедры, Лауреат Госудерствен-ной премии СССР, Заслуженный работник высшей школы РФ, доктор медицинских наук, профессор
Печатается согласно редакционно-издательскону плану Военно-медицинской академии имени С. М. Кирова, утвержденному начальником Главного военно-медицинского управления
Министерства обороны РФ
ISBN 5-93929-082-5
© Коллектив авторов, 2004
© Военно-медицинская академия, 2004
©Оформление ООО «ИздательствоФОЛИАНТ», 2004
ОГЛАВЛЕНИЕ
Предисловие............................................................................................................................... 10
Часть I. Токсикология............................................................................................... .. 15
Раздел I. Общая токсикология................................................................................ 17
Глава 1. Предмет, цель, задачи и структура токсикологии (С. А. Куценко)............................ 17
1.1. Предмет токсикологии...................................................................................... 17
1.2. Цель и задачи токсикологии............................................................................. 20
1.3. Структура токсикологии.................................................................................... 21
Глава 2. Основные понятия токсикологии (С. А. Куценко,)..................................................... 23
2.1. Токсикант (яд).................................................................................................... 23
2.2. Токсический процесс........................................................................................ 29
Глава 3. Токсикометрия (С. А. Куценко)................................................................................... .. 37
Глава 4. Токсикокинетика (С. А. Куценко)................................................................................ 42
4.1. Общие понятия токсикокинетики.................................................................... .. 42
4.2. Резорбция......................................................................................................... .. 47
4.3. Распределение.................................................................................................. .. 50
4.4. Элиминация....................................................................................................... 52
4.4.1. Экскреция...................................................................................................... 53
4.4.2. Метаболизм ксенобиотиков (биотрасформация)......................................... 54
4.5. Количественные характеристики токсикокинетики....................................... 58
Глава 5. Токсикодинамика (С. А- Куценко)............................................................................... .. 63
5.1. Механизм токсического действия.................................................................... 63
5.1.1. Химизм реакции токсикант — рецептор........................................................ 65
5.1.2.Взаимодействие токсикантов с белками................................................ 67
5.1.3.Взаимодействие токсикантов с нуклеиновыми кислотами................... 68
5.1.4.Взаимодействие токсикантов с липидами мембран.............................. 68
5.1.5. Взаимодействие с реактивными структурами возбудимых мембран........ 69
5.2. Общие механизмы цитотоксичности............................................................... 71
5.2.1. Нарушение процессов биоэнергетики........................................................... . 71
5.2.2. Активация свободнорадикальных процессов в клетке................................ 73
5.2.3. Повреждение мембранных структур............................................................. ... 76
5.2.4. Нарушение гомеостаза внутриклеточного кальция..................................... ... 78
5.2.5. Повреждение процессов синтеза белка и клеточного деления................... ... 80
5.3. Развитие токсического процесса.................................................................... ... 83
Глава 6. Антидоты. Общие принципы оказания неотложной помощи отравленным
(С. А. Куценко, В. П. Мельничук)............................................................................. ... 84
6.1. Характеристика современных антидотов........................................................ 86
6.2. Применение противоядий................................................................................ 89
6.3. Разработка новых антидотов........................................................................... 91
6.4. Основные принципы оказания первой, доврачебной и первой врачебной
помощи при острых отравлениях.................................................................. 92
Раздел II. Военная токсикология............................................................................. 95
Глава 7 Основные понятия военной токсикологии (С. А. Куценко)...................................... ..... 95
7.1. Предмет, цели, задачи военной токсикологии................................................ ..... 95
7.2. Отравляющие и высокотоксичные вещества (ОВТВ)..................................... 96
7.3. Химическая обстановка................................................................................... ... 103
7.4. Медицинская противохимическая защита...................................................... ... 105
Глава 8. Отравляющие и высокотоксичные вещества раздражающего действия
(С. А. Куценко).......................................................................................................... 107
8.1. Общая характеристика..................................................................................... 107
8.2. Физико-химические свойства. Токсичность.................................................... 110
8.3. Методы изучения раздражающего действия................................................... 111
8.4. Основные проявления поражения................................................................... 111
8.5. Патогенез токсического процесса. Механизм действия................................. 113
8.6. Оказание помощи. Медицинская защита........................................................ 117
Глава 9. Отравляющие и высокотоксичные вещества пульмонотоксического
действия (С. А. Куценко, Т. Н. Преображенская).................................................... 119
9.1. Основные формы патологии дыхательной системы химической этиологии. 120
9.2. ОВТВ удушающего действия............................................................................. 132
9.2.1. Характеристика отдельных представителей ОВТВ удушающего действия 132
9.2.1.1. Фосген.......................................................................................................... 132
9.2.1.2. Хлор.............................................................................................................. 134
9.2.1.3. Оксиды азота............................................................................................... 136
9.2.1.4. Паракват...................................................................................................... 137
9.2.2. Диагностика поражения ОВТВ удушающего действия................................. 139
9.2.3. Медицинская защита...................................................................................... 139
Глава 10. Отравляющие и высокотоксичные вещества общеядовитого действия
(С. А. Куценко).......................................................................................................... 144
10.1. ОВТВ, нарушающие кислородтранспортные функции крови....................... 147
10.1.1. ОВТВ, нарушающие функции гемоглобина................................................ 147
10.1.1.1. ОВТВ, образующие карбоксигемоглобин................................................ 149
10.1.1.1.1. Карбонилы металлов............................................................................. 149
10.1.1.1.2. Оксид углерода (СО)................................................................................ 150
10.1.1.2. ОВТВ, образующие метгемоглобин.......................................................... 157
10.1.1.2.1. Нитро-и аминосоединения ароматического ряда................................ 162
10.1.1.2.2. Нитриты................................................................................................... 165
10.1.1.2.3. Взрывные (пороховые) газы................................................................. 170
10.1.2. ОВТВ, разрушающие эритроциты (гемолитики).......................................... 172
10.1.2.1. Мышьяковистый водород (Арсин - AsH3)................................................. 173
10.2. ОВТВ, нарушающие тканевые процессы биоэнергетики............................. 178
10.2.1. Ингибиторы ферментов цикла Кребса........................................................ 178
10.2.1.1. Фторорганические соединения................................................................ 178
10.2.1.2. Фторуксусная кислота............................................................................... 179
10.2.2. Ингибиторы цепи дыхательных ферментов................................................. 181
10.2.2.1. Синильная кислота и ее соединения........................................................ 182
10.2.3. Разобщители тканевого дыхания............................................................... 191
10.2.3.1. Динитро-орто-крезол................................................................................. 192
Глава 11. Отравляющие и высокотоксичные вещества цитотоксического действия
(С. А Куценко)........................................................................................................... 195
11.1. Ингибиторы синтеза белка и клеточного деления......................................... 197
11.1.1. Ингибиторы синтеза белка и клеточного деления, образующие аддукты
ДНК и РНК.................................................................................................... 197
11.1.1.1. Иприты....................................................................................................... . 197
11.1.2. Ингибиторы синтеза белка, не образующие аддукты ДНК и РНК............. . 213
11.1.2.1. Рицин......................................................................................................... . 214
11.2. Тиоловые яды.................................................................................................. . 218
11.2.1. Соединения мышьяка................................................................................. . 219
11.2.1.1. Неорганические соединения мышьяка................................................... . 220
11.2.1.2. Галогенированные алифатические арсины............................................. . 223
11.2.1.3. Галогенированные ароматические арсины............................................ 228
11.3. Токсичные модификаторы пластического обмена....................................... 234
11.3.1. Диоксины...................................................................................................... 235
11.3.2. Полихлорированые бифенилы (ПХБ)........................................................... 239
Глава 12. Отравляющие и высокотоксичные вещества нейротоксического действия
(С. А. Куценко, Н. В. Саватеев)................................................................................ 243
12.1. Вещества, вызывающие преимущественно функциональные нарушения
со стороны нервной системы 244
12.1.1. Отравляющие и высокотоксичные веществе нервно-паралитического
действия........................................................................................................ 246
12.1.1.1. Отравляющие и высокотоксичные вещества судорожного действия . . 248
12.1.1.1.1. Конвульсанты, действующие на холинореактивные синапсы............. 248
12.1.1.1.1.1. Ингибиторы холинэстеразы................................................................ 250
Фосфорораанические соединения.............................................................................. 250
Карбаматы................................................................................................................ 278
12.1.1.1.2. Конвульсанты, действующие на ГАМК-реактивные синапсы.............. 282
12.1.1.1.2.1. Ингибиторы синтеза ГАМК.................................................................. 284
Гидразин.................................................................................................................... 285
12.1.1.1.2.2. Пресинаптические блокаторы высвобождения ГАМК...................... 290
Тетанотоксин........................................................................................................... 290
12.1.1.1.2.3. Антагонисты ГАМК............................................................................... 292
Бициклические фосфорорганочяские соединения (БЦФ).......................................... 293
12.1.1.2. Отравляющие и высокотоксичные вещества паралитического
действия.................................................................................................... 300
12.1.1.2.1. Пресинаптические блокаторы высвобождения ецетилхолина............ 300
Ботулотоксин.......................................................................................................... 300
12.1.1.2.2. Блокаторы №+-ионных каналов возбудимых мембран....................... 305
Сакситоксин. Тетродотоксин................................................................................. 305
12.1.2. Отравляющие и высокотоксичные вещества психодислептического
действия........................................................................................................ ЗЮ
12.1.2.1. Галлюциногены 312
12.1.2.1.1, Диэтиламид лизергиновой кислоты (ДЛК)............................................. 313
12.1.2.2. Делириогены 318
12.1.2.2.1, Вещество BZ........................................................................................... 319
12.1.2.2.2, Фенциклидин (сернил)............................................................................ 324
12.2. Вещества, вызывающие органические повреждения нервной системы ... 327
12.2.1. Таллий........................................................................................................... 328
12.2.2. Тетраэтилсвинец (ТЭС).................................................................................. 332
Часть II. Радиобиология........................................................................................... 337
Раздел III. Общая радиобиология............................................................................ 339
Глава 13. Предмет, цель и задачи радиобиологии (Н. В. Бутомо)........................................... 339
| 14.1. Электромагнитные ионизирующие излучения.............................................. 341 |
Глава 14 Виды ионизирующих излучений и их свойства (Ю. Ю. Ивницкий).......................... 341
................................... 341
................................. 344
14.2. Корпускулярные ионизирующие излучения.........................................
14.3. Плотноионизирующие и редкоионизирующие излучения............................ 346
14.4. Количественная оценка ионизирующих излучений. Основы дозиметрии. . 348
14.5. Основные источники ионизирующих излучений........................................... 350
Глава 15. Радионуклиды как источник радиационной опасности (Ю. Ю. Ивницкий) .. 353
15.1. Радиоактивность. Параметры радиоактивного распада............................... 353
15.2. Количество редиоактивных веществ. Радиометрия..................................... 354
15.3. Источники радионуклидов. Радионуклиды в природе и народном хозяйстве 355
Глава 16. Радиобиологические эффекты (Н. В. Бутомо, Ю. Ю. Ивницкий)............................ 358
16.1. Классификация радиобиологических эффектов............................................ 358
16.1.1. Уровень формирования............................................................................... 358
16.1.2. Сроки появления.......................................................................................... 359
16.1.3. Локализация................................................................................................. 359
16.1.4. Характер связи с дозой облучения.............................................................. 360
16.1.5. Значение для судьбы облученного организма............................................ 362
16.2. Начальные этапы биологической стадии в действии ионизирующих
излучений......................................................................................................... 363
16.2.1. Первичные стадии в действии излучений................................................... 363
16.2.2. Молекулярные механизмы лучевого повреждения биосистем................. 364
16.3. Реакции клеток на облучение........................................................................ 365
16.3.1. Биологическое усиление радиационного поражения................................ 366
16.3.2. Репарация лучевых повреждений.............................................................. 367
16.3.3. Судьба облученной клетки........................................................................... 368
16.3.4. Количественные характеристики лучевого поражения клеток................. 371
16.4. Действие излучений на ткани, органы и системы. Радиочувствительность ,
тканей............................................................................................................... 373
16.4.1. Радиационное поражение системы крови................................................. 374
16.4.2. Радиационное поражение органов желудочно-кишечного тракта........... 377
16.4.3. Лучевое поражение центральной нервной системы.................................. 378
Раздел IV. Военная радиобиология......................................................................... 380
Глава 17. Факторы, вызывающие поражения личного состава войск при ядерных
взрывах и радиационных авариях (Ю. Ю. Ивницкий)........................................... 380
17.1. Поражающие факторы ядерного взрыва...................................................... 380
17.1.1. Радиационные поражающие факторы ядерного взрыва.......................... 381
17.1.2. Нерадиационные поражающие факторы ядерного взрыва...................... 382
17.2. Характеристика лучевых поражений............................................................. 384
Глава 18. Лучевые поражения в результате внешнего облучения (Н. В. Бутомо)_________ 385
18.1. Классификация лучевых поражений от внешнего облучения в зависимости от вида и условий воздействия 385
18.2. Зависимость эффекта облучения от его продолжительности........................ 387
18.3. Зависимость эффекта облучения от распределения поглощенной дозы в объеме телв 389
ГЛава 19. Лучевые поражения в результате общего (тотального) облучения
(Ю. Ю. Ивницкий, Н. В. Бутомо).............................................................................. .. 391
19.1. Острая лучевая болезнь...................................................................... .......... 391
19.1.1. Костномозговая форма острой лучевой болезни....................................... 392
19.1.2. Кишечная форма острой лучевой болезни................................................ .. 396
19.1.3. Токсемическая форма острой лучевой болезни........................................ .. 397
19.1.4. Церебральная форма острой лучевой болезни.......................................... .. 397
19.2. Особенности поражений нейтронами............................................................ .. 398
19.3. Отдаленные последствия общего (тотального) облучения............................. 399
19.3.1. Неопухолевые отдаленные последствия облучения................................... 399
19.3.2. Канцерогенные эффекты облучения.......................................................... 400
19.3.3. Сокращение продолжительности жизни...................................................... 401
с-'
Глава 20. Медицинская защита от внешнего облучения (А. Н. Гребенюк,
Ю. Ю. Ивницкий)...................................................................................................... 403
20.1. Радиопротекторы............................................................................................ 403
20.1.1. Показатели защитной эффективности радиопротекторов......................... .. 404
20.1.2. Механизмы радиозащитного действия....................................................... .. 405
20.1.3. Краткая характеристика и порядок применения радиопротекторов, имеющих наибольшее практическое значение 406
20.2. Средства длительного поддержания повышенной радиорезистентности организма 408
20.3. Средства профилактики общей первичной реакции на облучение............. 413
20.4. Средства профилактики ранней преходящей недееспособности................. 414
20.5. Средства раннего (догоспитального) лечения острой лучевой болезни. .. 416
Глава 21. Местные лучевые поражения (А. Н. Гребенюк, Н. В. Бутомо)................................ 418
21.1. Местные лучевые поражения кожи............................................................... 418
21.2. Местные лучевые поражения слизистых оболочек...................................... 423
21.3. Особенности местных лучевых поражений в результате наружного заражения кожных покровов радионуклидами 424
Глава 22. Поражения в результате внутреннего радиоактивного заражения
(Н. В. Бутомо, А. Н. Гоебенюк)................................................................................. 426
22.1. Кинетика радионуклидов в организме.......................................................... 426
22.1.1. Поступление радионуклидов в организм..................................................... 426
22.1.2. Судьба радионуклидов, проникших в кровь............................................... . 429
22.1.3. Выведение радионуклидов из организма................................................... 429
22.2. Биологическое действие радиоактивных веществ....................................... 430
22.2.1. Влияние на развитие поражения особенностей распределения инкорпорированных радионуклидов 430
22.2.2. Влияние на развитие поражения активности инкорпорированных радионуклидов и продолжительности их пребывания в организме 432
22.2.3. Последствия поступления в организм отдельных радионуклидов.............. 433
22.2.4. Лучевые поражения в результате алиментарного и ингаляционного поступления продуктов ядерного деления 438
22.3. Профилактика поражений радионуклидами. Медицинские средства
звщиты и раннего лечения............................................................................. 44"I
22.3.1. Специальные санитарно-гигиенические и профилактические медицинские мероприятия 44"l
22.3.2. Медицинские средства защиты и раннего (догоспитального) лечения
при внутреннем заражении радиоактивными веществами..................... 442
22.4. Ранняя диагностика и эвакуационные мероприятия при внутреннем
заражении радиоактивными веществами..................................................... 446
Глава 23. Сочетанные и комбинированные радиационные поражения
(А. Н. Гребенюк)........................................................................................................ 448
23.1. Сочетанные радиационные поражения......................................................... 448
23.2. Комбинированные радиационные поражения............................................. 450
Часть III. Средства и методы профилактики химических
и радиационных поражений 457
Глава 24. Технические средства индивидуальной и коллективной защиты
(В. М. Рыбалко, А. Н. Гоебенюк).............................................................................. 459
24.1. Средства индивидуальной защиты.................................................................. 459
24.1.1. Средства индивидуальной защиты органов дыхания................................. 460
24.1.1.1. Эксплуатационная характеристика.......................................................... 460
24.1.1.2. Факторы, определяющие порядок использования средств защиты органов дыхания 4^9
24.1.1.3. Использование СИЗОД для защиты раненых и больных......................... 471
24.1.2. Средства индивидуальной защиты кожи...................................................... 473
24.1.2.1. Эксплуатационная характеристика.......................................................... 474
24.1.2.2. Факторы, определяющие порядок использования средств защиты кожных покровов 476
24.1.3. Средства индивидуальной защиты глаз........................................................ 477
24.2. Коллективные средства защиты..................................................................... 477
Глава 25. Специальная обработка в подразделениях и частях медицинской службы
(В. М. Рыбалко, А. Н. Гребенюк).............................................................................. 481
25.1. Основные понятия.......................................................................................... 48''
25.2. Частичная специальная обработка................................................................ 485
25.2.1. Средства, используемые для частичной специальной обработки.............. 486
25.2.2. Организация и проведение частичной специальной обработки в медицинском пункте батальона 488
25.2.3. Организация и проведение частичной специальной обработки в медицинском пункте полка 489
25.3. Полная специальная обработка. Организация работы отделения
специальной обработки (ОСО)......................................................................... 492
Глава 26. Радиационная и химическая разведка в частях и подразделениях
медицинской службы (А. Н. Гоебенюк, В. М. Рыбалко).......................................... 506
26.1. Средства и методы радиационной разведки и контроля.............................. 506
26.2. Средства и методы химической разведки и контроля.................................. 511
26.3. Организация и проведение радиационной и химической разведки в подразделениях и частях медицинской службы 515
26.4. Организация и проведение контроля доз облучения личного состава, раненых и больных на этапах медицинской эвакуации 518
26.5. Организация и проведение экспертизы воды и продовольствия на зараженность отравляющими, высокотоксичными радиоактивными веществами........................................................................ 520
ПРЕДИСЛОВИЕ
Бурным развитием химической промышленности во второй половине XIX в. были созданы материальные предпосылки для использования высокотоксичных веществ с военными целями.
22 апреля 1915 г. в ходе Первой мировой войны с применения газообразного хлора войсками Германии началась эпоха современных средств массового уничтожения. Всего за годы войны было применено около 130 тыс. тонн высокотоксичных соединений примерно 40 наименований. В итоге, 1,3 млн человек получили поражения, из них более 100 тыс. — погибли. Важно отметить, что, создав химическое оружие и применив его, воюющие страны оказались практически не подготовленными к оказанию помощи пораженным. Это послужило поводом для быстрого формирования уже в ходе войны нового направления военной медицины — санитарно-химической защиты, призванной создать систему профилактики и оказания помощи пораженным отравляющими веществами. У истоков этой работы в нашей стране стояли выдающиеся химики и медики: Н. Д. Зелинский, Г. В. Хлопин, Н. П. Кравков, В. И. Глинчиков, А. А. Лихачев, И. Ф. Пожарисский, М. Д. Тушинский, Н. И. Лепорский. В процессе планомерного изучения токсических свойств боевых отравляющих веществ и медицинских средств защиты от них сформировалось новое направление науки — военная токсикология. Большой вклад в становление и развитие военной токсикологии в России на первом этапе внесли специалисты различного профиля. Это и организаторы здравоохранения (Б. К. Леонардов, позже — Б. С. Синтюрин), и клиницисты (Н. Н. Савицкий), гигиенисты (В. И. Виноградов-Волжинский, И. П. Ласточкин), патологоанатомы (С. С. Вайль), фармакологи (С. В. Аничков, М. Д. Машковский), и ветеринары (Н. А. Сошественский) и др.
В годы Второй мировой войны химическое оружие применяли в крайне ограниченных масштабах. Тем не менее работы по созданию новых образцов ОВ не прекращались. В фашистской Германии, а позже и других странах, были созданы чрезвычайно токсичные боевые отравляющие вещества, что вновь стимулировало военно-токсикологические исследования, к которым подключились большие коллективы ученых, крупные научно-исследовательские центры нашей страны. Большой вклад в решение проблем военной токсикологии во второй половине XX в. внесли видные цеятели отечественной медицинской науки: Ю. В. Другое, С. Н. Голиков, М. Я. Михельсон, Б. Д. Ивановский, А. И. Черкес и многие другие.
Научным итогом многолетней работы по изучению действия на организм боевых отравляющих веществ явилось не только создание эффективных медицинских средств защиты от высокотоксичных соединений, но и существенный вклад в решение ряда фундаментальных проблем
1 □
биологии и медицины. Это — учение о генотоксичности ксенобиотиков; представления о механизмах синаптической передачи нервного импульса; законы процессов биоэнергетики; явление метаболизма чужеродных веществ в организме человека и животных и др. На базе проведенных исследований сложилась система организации медицинской защиты войск от химического оружия.
Вместе с развитием военной токсикологии как науки шло и формирование соответствующей учебной дисциплины. Первоначально это был курс обучения медицинского персонала вопросам санитарно-химической защиты (Аничков С. В., Лихачев А. А., Предтеченский Б. И. «Медико-санитарные основы военно-химического дела», 1933; Лубоцкий М. Н. «Са-нитарно-химическая защита», 1935 и др.). По мере накопления научных данных, курс все более трансформировался в учебную дисциплину — «Военная токсикология». В курсе «Военной токсикологии» практические вопросы рассматривались на основе изучения механизмов токсического действия, патогенеза, проявлений поражений ОВ («Руководство по токсикологии отравляющих веществ» под ред. Черкеса А. Н., 1964; «Руководство по токсикологии отравляющих веществ» под ред. Голикова С. Н., 1972; «Военная токсикология, радиология и медицинская защита» под ред. Саватеева Н. В., 1987 и др.).
В 1993 г. в Париже была принята «Конвенция о запрещении применения, разработки и накопления химического оружия». В настоящее время конвенцию подписали более 150 государств. В соответствии с принятыми документами предполагается уничтожить запасы химического оружия на планете.
«Конвенция», безусловно, является большим шагом вперед в направ-
лении избавления человечества от угрозы массового истребления. Тем не
менее пока существует вероятность возникновения военных конфликтов,
договорные акты едва ли смогут полностью устранить возможность мас-
совых поражений людей химическими веществами. Так, оружие будет
находиться в распоряжении государств еще в течение 10-15, а может
быть и более лет, пока не будут уничтожены все его запасы. Кроме того,
отравляющими веществами могут обладать государства, не присоединив-
шиеся к Конвенции. Не запрещенными являются разработка и накопле-
ние оружия несмертельного действия (полицейские газы). '
Однако основной причиной, побуждающей говорить о сохранении высокого уровня химической опасности в современном мире, являются беспрецедентный рост масштабов химического производства в мирных целях, достижения химии в области органического синтеза, огромное разнообразие синтезированных и вновь синтезируемых веществ, многие из которых обладают высокой токсичностью. Так, в Европе ежегодно производится 0,5 млрд смертельных для человека доз мышьяка, 100 млрд доз фосгена, аммиака, синильной кислоты, 10 000 млрд доз хлора. По данным ВОЗ, широко распространены и находятся в ежедневном обращении более 40 000 химических соединений. Согласно некоторым оценкам, в мире насчитываются десятки тысяч объектов, на которых производят или используют токсичные соединения. Это — предприятия нефтепе-
1 1
рерабатывающей, фармацевтической, химической индустрии, заводы по выпуску пестицидов, продуктов бытовой химии и т. д. Количество изученных на сегодняшней день физиологически активных веществ (ФАВ), свойства которых позволяют рассматривать их как потенциальные средства химической агрессии, составляет не один десяток. Источником таких веществ и информации об их биологической активности являются исследования в области фармакологии, поиск новых высокоэффективных пестицидов (инсектицидов, гербицидов, микоцидов, ратицидов и др.), токсикологические исследования по оценке опасности новых промышленных веществ, появляющихся в ходе внедрения новых технологических процессов и т. д.
Одним из пагубных следствий «химизации» всех сфер человеческой
деятельности является и то, что к угрозе применения химических веществ
(в том числе и оружия) в военных конфликтах добавляются проблемы хи-
мической опасности мирного времени: растет вероятность аварий на хи-
мически опасных объектах, увеличивается возможность химического тер-
роризма. 1
Не менее драматична история «контакта» людей с источниками ионизирующих излучений. Значительные лучевые повреждения живых тканей, в частности тяжелые ожоги кожи, выявились уже в первые месяцы после открытия в конце 1895 г. рентгеновых лучей (В. К. Рентген) и в начале 1896 г. явления радиоактивности (А. Беккерель). Это послужило поводом для проведения экспериментальных исследований биологического действия ионизирующих излучений. Уже в конце 1896 г. была опубликована статья профессора Военно-медицинской академии И. Р. Тарханова, в которой на основании проведенных экспериментов автор впервые предсказал перспективы применения ионизирующих излучений в лечебных целях.
Значительно расширились исследования биологического действия ионизирующих излучений после первых взрывов ядерных бомб в августе 1945 г. над японскими городами Хиросима и Нагасаки. Массовая гибель и заболевания людей в результате воздействия нового, ранее не применявшегося поражающего фактора, опасность появления новых многочисленных жертв в случае повторного применения ядерного оружия заставили развернуть в большинстве развитых стран крупномасштабные работы по изучению биологического действия ионизирующих излучений, характера возникающих поражений, способов предупреждения и лечения этих поражений. Ряд научных центров был организован для решения этих задач в конце 40-х — начале 50-х годов прошлого столетия в Советском Союзе. В частности, в Военно-медицинской академии работы возглавил в специально созданной для этих целей лаборатории академик АН СССР Л. А. Орбели.
Из числа многих ученых, участвовавших в разработке проблем военной радиобиологии на самых ранних этапах ее становления, следует упомянуть сотрудников Военно-медицинской академии А. В. Лебединского, Т. К. Джаракьяна, Н. С. Молчанова, А. Н. Беркутова, А. С. Мозжухина и др.
Накапливающиеся при изучении радиобиологических феноменов факты привели к ряду важных открытий и обобщений, значение которых далеко выходит за рамки радиобиологии. Назовем лишь некоторые из них. Это выявление связи между радиочувствительностью клеток и их пролиферативной активностью (Бергонье и Трибондо). К двадцатым годам XX в. относится обнаружение мутагенного эффекта излучения — способности вызывать такие изменения генетического аппарата, которые приводят к появлению новых, передающихся по наследству признаков (Г. Меллер, Г. С. Филиппов, Г. А. Надсон). С именами Ф. Дессауэра, Н. В. Тимофеева-Рессовского, Д. Ли и других ученых связана разработка «принципов мишеней», объяснивших вероятностный характер проявлений лучевого поражения на клеточном и молекулярном уровнях. Должны быть названы также установление возможности репарации молекулярных повреждений в клетках, в частности, репарации ядерной ДНК и повреждений хромосом (В. Н. Лучник), доказательство способности клеток ре-парировать возникшие сублетальные радиационные повреждения (Д. Эл-кинд), установление возможности химической защиты от радиационных воздействий (3. Бак, X. Патт) и т. д.
В настоящее время ядерное оружие находится на снабжении армий развитых в экономическом отношении государств. Более того, несмотря на договоры о запрещении распространения этого вида оружия, его обладателями становятся все новые государства. Однако проблема радиационной опасности этим обстоятельством не исчерпывается. В 1986 г. произошла тяжелая авария на Чернобыльской АЭС, показавшая реальность катастрофических последствий, к которым может привести «мирный атом». Общество осознало практическую значимость проблем длительного радиационного воздействия в сравнительно невысоких дозах на население больших территорий, в том числе и на расположенные там войска. Это событие послужило поводом к выходу на первый план задач изучения, выяснения влияния на здоровье людей и возможности предотвращения вредных эффектов при длительном воздействии на человека полей излучения малых интенсивностей.
Все сказанное прямо указывает, с одной стороны, на сохраняющийся высокий уровень химической и радиационной опасности для вооруженных сил и населения, с другой — на значительные потенциальные возможности медицины по снижению этой опасности. Поэтому усилия международных организаций, направленные на разоружение, ни в одном государстве не привели к сокращению работ в области противохимической и противорадиационной защиты. Более того, обеспечение обширной программы дальнейшего совершенствования защиты населения и личного состава войск от химического и лучевого воздействия считается одним из приоритетных научных направлений как у нас в стране, так и за рубежом. Так, в США все виды американских вооруженных сил имеют программы совершенствования средств медицинской защиты, учитывающие их специфику. Сохранена система подготовки кадров по этим вопросам. Кадры военных специалистов, научный персонал, научные центры, лабораторная и полигонная базы рассматриваются как националь
ный ресурс, необходимый для обеспечения защиты вооруженных сил и населения в случае радиационной и химической угрозы.
Очевидно, что совершенствование медицинского обеспечения радиационной и химической безопасности личного состава Российских Вооруженных Сил возможно только на пути проведения глубоких научных исследований, основа которых — фундаментальная наука. Такой фундаментальной научной базой медицинской защиты личного состава являются современная токсикология и радиобиология.
Но мало иметь эффективные средства защиты и отлаженную систему мер обеспечения безопасности. Надо также уметь грамотно выполнять функции, возложенные на медиков. Понятно, что решение повседневных задач, связанных с медицинским обеспечением радиационной и химической безопасности, не мыслимо силами узкого круга специалистов-токсикологов и радиологов. Эти задачи решаются силами медицинской службы в целом, специалистами войсковой, профилактической и клинической медицины, организаторами военного здравоохранения. Этим обусловлена необходимость глубокой подготовки по вопросам военной токсикологии и радиобиологии всех будущих военных врачей, какой бы специальности в дальнейшем ни посвятили они свою жизнь.
Доктор медицинских наук, профессор С. А. Куценко, доктор медицинских наук, профессор Н. В. Бутомо
ГЛ ЦЕПЬ, ЗАДАЧ!
Часть I ТОКСИКОЛОГИЯ
Глава 1. ПРЕДМЕТ, ЦЕЛЬ, ЗАДАЧИ И СТРУКТУРА ТОКСИКОЛОГИИ
1.1. Предмет токсикологии
Общепринятого определения предмета токсикологии в настоящее время не существует. Самым простым является, непосредственно вытекающее из названия науки: toxicon — яд, logos — наука. Токсикология — наука о ядах и интоксикациях (отравлениях).
«Энциклопедический словарь медицинских терминов» (1982) дает развернутое определение: «Токсикология — область медицины, изучающая физические, химические свойства ядов (вредных и отравляющих веществ), механизмы их действия на организм человека и разрабатывающая методы диагностики, лечения и профилактики отравлений».
Близкими по сути являются и другие определения:
«Токсикология — наука, изучающая закономерности развития и течения патологического процесса (отравления), вызванного воздействием на организм человека или животного ядовитых веществ» (Голиков С. Н., 1972).
«Токсикология — это область медицины, изучающая законы взаимодействия живого организма и яда» (Лужников Е. А., 1994).
Однако определить токсикологию как науку о яде можно лишь при условии четкого определения самого понятия «яд», но сделать это, несмотря на многочисленные попытки, не удается.
Еще в начале XIX в. основоположник научной токсикологии Матео Жозе Бонавентура Орфила (1814) писал: «Яд — вещество, которое в малом количестве, будучи приведенным в соприкосновение с живым организмом, разрушает здоровье или уничтожает жизнь». Так же определял «яд», спустя практически сто лет, и один из пионеров отечественной токсикологии профессор Российской военно-медицинской академии Д. П. Косоротов (1907): «Ядами называются вещества, которые, будучи введены в организм в малых количествах, в силу своих химических свойств, могут причинить расстройство здоровья или самую смерть».
В этих определениях подчеркивается одна важная, по мнению авторов, характеристика ядов: малое количество, необходимое для провока-
ции отравления. Однако, что считать малым количеством? Ответ на этот вопрос носит весьма субъективный характер. В настоящее время науке известны вещества, вызывающие смерть экспериментального животного при введении в дозах, равных нескольким нанограммам (ботулотоксин). Вместе с тем самым распространенным «ядом» современности является этиловый спирт и его суррогаты, вызывающие отравление при поступлении в организм в количестве десятков и сотен грамм.
Вот почему существуют определения, в которых «малое количество» как свойство «ядов» упускают вовсе:
«Ядом называется всякое химическое вещество, способное причинить смерть или серьезный вред здоровью своим действием на ткани или соки тела» (Пеликан Е.,1878).
«Можно определить яд как меру (единство количества и качества) действия химического вещества, в результате которого при определенных условиях возникает отравление» (Саватеев Н. В., 1978).
Из этих определений вытекает, что при тех или иных условиях любое вещество может стать ядом. Один из основоположников отечественной промышленной токсикологии, выдающийся ученый и педагог Н. В. Лазарев пишет (1936): «Яды — суть вещества, вызывающие повреждение организма немеханическим путем».
В настоящее время человечеству известно около 10 млн химических соединений. Из них более 40 тыс. широко используются в быту, медицине, на производстве и в сельском хозяйстве. Этот перечень продолжает из года в год увеличиваться (по некоторым данным примерно на 1000 наименований ежегодно). Большая часть изученных соединений при определенных обстоятельствах может причинить «серьезный вред здоровью».
Подобное обстоятельство ставит под сомнение саму возможность выделить из всей совокупности химических веществ окружающего мира, естественных и синтезированных человеком, некую группу, обозначаемую как «яд». В наиболее категоричной форме эта мысль выражена еще в XIX в. известным французским судебным медиком Тардье: «Ядов в научном смысле слова нет».
Накопленные человечеством знания привели к пониманию того, что практически любое химическое вещество, в зависимости от действующего количества, может быть либо безразличным, либо полезным, либо вредным для организма (т. е. выступать в качестве яда).
Впервые на это указал еще в XV в. известный врач и химик Теофраст Бомбаст фон Гогенгейм (Парацельс): «Все есть яд. Ничто не лишено ядовитости. И только доза отличает яд от лекарства».
Хотя ядов в научном смысле слова нет, практически всем веществам окружающего нас мира присуща токсичность, т. е. способность, действуя на организм в определенных дозах и концентрациях, нарушать дееспособность, вызывать заболевания или даже смерть (или, в более общей форме — действуя на биологические системы, вызывать их повреждение или гибель). Вещества существенно различаются по токсичности. Чем в меньшем количестве они оказывают на биологические системы повреждающее дей-
ствие, тем они токсичнее (ядовитее). Изучение и оценка токсичности различных веществ составляет предмет науки токсикологии.
Действие веществ, приводящее к нарушению функций биологических систем, называется токсическим.
Химические вещества могут оказывать токсическое действие при взаимодействии с любым видом животных и растительных организмов. При этом токсическое действие может быть зарегистрировано и изучено на любом уровне организации живой материи: клеточном, тканевом, органном, организменном, популяционном, биоценологическом. Однако всегда в основе токсического действия веществ лежит их взаимодействие с биологическим объектом на молекулярном уровне.
Формирование и развитие реакций биосистемы на действие токсиканта, приводящих к ее повреждению (нарушению функций, жизнеспособности) или гибели, называется токсическим процессом.
Нередко полагают, что единственной формой токсического процесса является интоксикация. Именно поэтому и токсикологию определяют (см. выше), как «...науку, изучающую закономерности развития й течения ... отравления».
Однако в настоящее время все очевиднее становится, что пагубные последствия действия веществ на биосистемы вообще, и организм человека в частности, более многообразны.
Все увеличивающееся разнообразие условий, в которых многочисленные химические вещества воздействуют на человека, обусловливает развитие множественности форм, в которых проявляются токсические процессы. Даже на уровне отдельного организма это не только острые, подострые, хронические интоксикации (болезни химической этиологии), но и химический канцерогенез, нарушения репродуктивных функций, явление эмбриотоксичности, тератогенез, снижение иммунитета, аллер-гизация организма, многообразные астенические состояния и т. д.
Еще более расширяются представления о токсическом процессе и множественности форм его проявления при изучении последствий действия химических веществ на иных уровнях организации живого: клеточном, органном, популяционном.
Закономерности развития токсического процесса, его качественные и количественные характеристики, зависимость от строения вещества, действующей дозы, условий взаимодействия с биологическими системами — также составляют предмет изучения науки токсикологии.
Таким образом, предметом изучения науки токсикологии являются токсичность химических веществ и токсический процесс, развивающийся в биосистемах. А науку токсикологию можно определить как учение о токсичности и токсическом процессе — феноменах, регистрируемых при взаимодействии химических веществ с биологическими объектами.
Хотя дать научное определение понятию «яд» не представляется возможным, вполне обоснованным можно считать следующее утверждение: ядом становится любое химическое вещество, если при взаимодействии с организмом оно вызвало заболевание (интоксикацию) или гибель.
1 Э
Часть I. ТОКСИКОЛОГИЯ
В токсикологии используют и другие термины, характеризующие химические вещества как потенциальную или реализовавшуюся причину повреждения биологических систем.
Токсикант — более широкое, чем яд, понятие, употребляющееся для обозначения веществ, вызвавших не только интоксикацию, но провоцирующих и другие формы токсического процесса, и не только организма, но и биологических систем иного уровня организации (клетки, популяции).
Отравляющее вещество — химический агент, предназначенный для применения в качестве оружия в ходе ведения боевых действий.
Токсин — как правило, высокотоксичное вещество бактериального, животного, растительного происхождения.
Ксенобиотик — чужеродное (не участвующее в пластическом или энергетическом обмене организма со средой) вещество, попавшее во внутренние среды организма.
1.2L Цель и задачи токсикологии
Объектом воздействия химических веществ могут быть самые разные организмы — растения, животные, человек, и сложные биологические системы — популяции, биоценозы. Поэтому выделяют разделы токсикологии, в рамках которых изучают токсичность веществ для данных биологических объектов и свойственные этим объектам особенности течения токсического процесса, — ветеринарную токсикологию, фито-токсикологию, экологическую токсикологию и т. д.
Если объектом исследования является токсичность химических веществ для человека и человеческих популяций, говорят о медицинской токсикологии.
Цель медицинской токсикологии как области человеческой деятельности — непрерывное совершенствование системы мероприятий, средств и методов, обеспечивающих сохранение жизни, здоровья и профессиональной работоспособности отдельного человека, коллективов и населения в целом в условиях повседневного контакта с химическими веществами и при чрезвычайных ситуациях.
Эта цель достигается путем решения фундаментальных и прикладных токсикологических задач:
1. Установление количественных характеристик токсичности, причинно-следственных связей между действием химического вещества на организм и развитием той или иной формы токсического процесса. Раздел токсикологии, в рамках которого совершенствуется методология и накапливаются данные о токсичности веществ, называется «токсикометрия». Результаты токсикометрических исследований в медицинской практике используют для разработки системы нормативных и правовых актов, обеспечивающих химическую безопасность населения; оценки риска действия ксенобиотиков в условиях производства, экологических и бытовых контактов с токсикантами; сравнительной оценки эффективности
Глава 1. ПРЕДМЕТ, ЦЕЛЬ, ЗАДАЧИ И СТРУКТУРА ТОКСИКОЛОГИИ
средств и методов обеспечения химической безопасности населения и т. д.
2. Изучение проявлений интоксикаций и других форм токсического процесса, механизмов, лежащих в основе токсического действия, закономерностей формирования патологических состояний. Эта задача решается с помощью методических приемов, разрабатываемых и совершенствуемых в рамках раздела токсикологии — «токсикодинамика». Данные о токсикодинамике различных химических веществ лежат в основе разработки средств профилактики и терапии интоксикаций, методов предупреждения развития иных форм токсического процесса; совершенствования диагностики интоксикаций и оценки функционального состояния лиц, подвергшихся воздействию сверхнормативных доз токсикантов; совершенствования методологии оценки токсичности ксенобиотиков и биотестирования исследуемых проб.
3. Выяснение механизмов проникновения токсикантов в организм, закономерностей их распределения, метаболизма и выведения. Совершенствование методологии исследований, анализа получаемых результатов, накопление соответствующей информации осуществляются в рамках раздела токсикологии — «токсикокинетика». Знания токсикокинетики ксенобиотиков необходимы для разработки надежной системы профилактики токсических воздействий; диагностики интоксикаций, выявления профессиональной патологии, проведения судебно-медицинской экспертизы; они широко используются в процессе создания новых противоядий и схем их оптимального использования; совершенствования методов форсированной детоксикации организма и т. д.
4. Установление факторов, влияющих на токсичность вещества (особенности биологического объекта, особенности свойств токсиканта, особенности их взаимодействия, условия окружающей среды). Знание факторов, влияющих на токсичность, позволяет объективизировать наши представления о химической опасности, уточнить нормативные акты применительно к конкретным условиям действия веществ, разработать систему мер, обеспечивающих сохранение жизни, здоровья, работоспособности людей, контактирующих с химическими вредностями.
Все упомянутые задачи решаются в ходе экспериментальных исследований на животных, в процессе лечения людей и эпидемиологических исследований среди профессиональных групп и населения, подвергшихся действию токсикантов.
1.3. Структура токсикологии
Медицинская токсикологическая наука и практика представлена несколькими основными направлениями.
Профилактическая токсикология — изучает токсичность новых химических веществ; устанавливает критерии их вредности, обосновывает и разрабатывает ПДК токсикантов, нормативные и правовые акты, обеспечивающие сохранение жизни, здоровья, профессиональной работоспо-
Часть I. ТОКСИКОЛОГИЯ
собности населения в условиях химических воздействий, и осуществляет контроль за их соблюдением.
Клиническая токсикология — область практической медицины, связанная с оказанием помощи при острых токсических поражениях, выявлением и лечением патологии, обусловленной действием профессиональных вредностей. В рамках клинической токсикологии совершенствуются методы диагностики и лечения интоксикаций, изучаются особенности течения профессиональных болезней, вызванных действием химических веществ на организм.
Экспериментальная токсикология — изучает закономерности взаимодействия веществ и биологических систем (зависимости: «доза токсиканта — эффект», «строение токсиканта — эффект», «условия взаимодействия — эффект»), рассматривает феномен токсичности в эволюционном аспекте; совершенствует методологию решения практических задач, стоящих перед профилактической и клинической токсикологией; разрабатывает новые средства диагностики, профилактики и лечения различных форм токсического процесса.
С учетом условий (преимущественно особенностей профессиональной деятельности), в которых наиболее вероятно воздействие того или иного токсиканта на организм человека, а следовательно, и основного перечня наиболее актуальных для данных условий веществ в медицинской токсикологии иногда выделяют:
• промышленную токсикологию,
• сельскохозяйственную токсикологию,
• коммунальную токсикологию,
• токсикологию окружающей среды,
• токсикологию специальных видов деятельности и, в частности, военную токсикологию.
Глава 2. ОСНОВНЫЕ ПОНЯТИЯ ТОКСИКОЛОГИИ
2.1. Токсикант (яд)
В качестве ядов (токсикантов) могут выступать практически любые соединения различного строения, если, действуя на биологические системы немеханическим путем, они вызывают их повреждение или гибель.
В настоящее время науке известны миллионы химических веществ, многие из которых широко используются человеком в быту, медицине, на производстве, в сельском хозяйстве и т. д. Поскольку, как следует из определения, по сути любое из них при тех или иных условиях может вызвать развитие токсического процесса, единая, всеобъемлющая классификация токсикантов возможна только на основе особенностей химического строения. По этому принципу построены существующие справочные пособия по токсикологии («Вредные вещества в промышленности»; «Вредные химические вещества» и т. д.). Возможны и другие подходы к классификации веществ. С научных позиций они менее корректны, однако отчасти раскрывают сущность химической опасности на современном этапе.
Классификации веществ
1. По происхождению
1.1. Токсиканты естественного происхождения
1.1.1. Биологического происхождения ^
1.1.1.1. Бактериальные токсины
1.1.1.2. Растительные яды
1.1.1.3. Яды животного происхождения
1.1.2. Небиологического происхождения
1.1.2.1. Неорганические соединения
1.2.2.1. Органические соединения
1.2. Синтетические токсиканты (огромное количество веществ с раз-
личным строением)
2. По способу использования человеком
2.1. Ингредиенты химического синтеза и специальных видов производств
2.2. Пестициды
i лава с. v_/vnucji iuil. i in i vin i jr\svir\jj iui vw
2.3. Лекарства и пищевые добавки
2.4. Косметика
2.5. Топлива и масла
2.6. Растворители, красители, клеи
2.7. Побочные продукты химического синтеза, примеси и отходы 3. По условиям воздействия
3.1. Профессиональные (производственные) токсиканты
3.2. Бытовые токсиканты
3.3. Вредные привычки и пристрастия (табак, алкоголь, наркотические средства, лекарства и т. д.)
3.4. Загрязнители окружающей среды (воздуха, воды, почвы, продовольствия)
3.5. Поражающие факторы при специальных условиях воздействия
3.5.1. Аварийно-катастрофального происхождения
3.5.2. Боевые отравляющие вещества и диверсионные агенты
Подавляющее большинство веществ, известных человеку в настоящее время, синтезировано в лабораторных условиях. Однако химические вещества естественного происхождения также имеют большое токсикологическое значения.
Бактериальные токсины
По большей части бактериальные токсины представляют собой высокомолекулярные соединения, как правило, белковой, полипептидной или липополисахаридной природы, обладающие антигенными свойствами. В настоящее время выделены и изучены более 150 токсинов.
Многие бактериальные токсины относятся к числу самых ядовитых из известных веществ. Это, прежде всего, ботулотоксин, холерные токсины, тетанотоксин, стафилококковые токсины, дифтерийные токсины и т. д. Ботулотоксин и стафилококковый токсины рассматривались как возможные боевые отравляющие вещества. Бактериальные токсины действуют на разные органы и системы млекопитающих и человека, однако преимущественно страдают нервная и сердечно-сосудистая системы, реже слизистые оболочки.
Бактерии могут продуцировать и токсические вещества относительно простого строения. Среди них: формальдегид, ацетальдегид, бутанол и т. д.
Микотоксины
Химическое строение и биологическая активность микотоксинов чрезвычайно разнообразны. Они не представляют собой некую единую в химическом отношении группу. С практической точки зрения наибольший интерес представляют вещества, продуцируемые микроскопическими грибами и могущие заражать пищевые продукты. К таковым относятся, в частности, некоторые эрготоксины, продуцируемые грибами группы Cla-viceps (спорынья, маточные рожки), афлатоксины (Bl, В2; Gl, G2) и близкие им соединения, выделяемые грибами группы Aspergillus, трихоте-ценовые микотоксины (более 40 наименований), продуцируемые несколькими родами грибов, преимущественно Fusarium, охратоксины (В, С), патулин и др.
Отравления зерном, зараженным спорыньей, в старые времена нередко носили характер эпидемий. Заболевания проявлялись как гангренозными изменениями конечностей, так и психодислептическими эффектами («Антонов огонь», «пляска святого Вита»). В настоящее время подобные эпидемии среди населения практически не отмечаются, однако возможно поражение рогатого скота. Одним из известнейших производных эрготина, продуцируемого спорыньей, является диэтиламид ли-зергиновой кислоты (ДЛК) — выраженный галлюциноген.
Наиболее активным продуцентом афлатоксинов являются грибки Aspergillus flavus (отсюда и название токсинов), нередко поражающие зерновые: пшеницу, кукурузу и т. д. Помимо высокой острой токсичности, афлатоксины в опытах на животных проявляют свойства канцерогенов.
Трихотеценовые токсины также обладают высокой токсичностью. Вещества проявляют бактерицидную, фунгицидную, инсектицидную активность. Отравление человека сопровождается поносом, рвотой, явлениями атаксии. Некоторое время рассматривалась возможность использования этих веществ в качестве химического оружия.
Многие высшие грибы также продуцируют токсические вещества различного строения с широким спектром физиологической активности. Наиболее опасными являются аманитин и фаллоидин, содержащиеся в бледной поганке и при случайном использовании в пищу гриба вызывающие поражение печени и почек. Другими известными токсикантами являются мускарин, гиромитрин, иботеновая кислота. Вещества, синтезирующиеся отдельными видами высших грибов, обладают выраженной галлюциногенной активностью, например псилоцин, псилоцибин, мускарин и др.
Токсины высших растений
Огромное количество веществ, токсичных для млекопитающих, человека и других живых существ, синтезируется растениями (фитотоксины). Являясь продуктами метаболизма растений, фитотоксины порой выполняют защитные функции, отпугивая потенциальных консументов. Однако по большей части их значение для жизнедеятельности растения остается неизвестным. Фитотоксины представляют собой вещества с различным строением и неодинаковой биологической активностью. Среди них: алкалоиды, органические кислоты, терпеноиды, липиды, гликозиды, сапонины, флавоноиды, кумарины, антрахиноны и др. Особенно многочислен класс алкалоидов (табл. 1).

Алкалоиды — азотсодержащие органические основания, как правило, с гетероциклической структурой. В настоящее время известно несколько тысяч алкалоидов, многие из которых обладают высокой токсичностью для млекопитающих и человека.
Гликозиды — соединения, представляющие собой продукты конденсации циклических форм моно- или олигосахаридов со спиртами (фенолами), тиолами, аминами и т. д. Неуглеводная часть молекулы называется агликоном, а химическая связь агликона с сахаром — гликозидной. Гли-козидная связь достаточно устойчива и не разрушается в водных растворах веществ. Наиболее известны сердечные (стероидные) гликозиды, в которых в качестве агликона выступают производные циклопентанпер-гидрофенантрена. Эти соединения, продуцируемые растениями самых разнообразных видов, обладают высокой токсичностью, обусловленной отчасти избирательным действием на сердечную мышцу. Известны гликозиды и более простого строения (амигдалин — содержит в качестве агликона CN~).
Сапонины — наиболее часто встречаются в виде стероидов спироста-нового ряда и пентациклических терпеноидов. Сапонины обладают раздражающим действием на слизистые оболочки млекопитающих, а при попадании в кровь вызывают гемолиз эритроцитов.
Кумарины — кислородсодержащие гетероциклические соединения, часто определяются в растениях и обладают антикоагулянтным и фото-сенсибилизирующим действием. Известно несколько сот веществ, относящихся к классу кумаринов.
Многие вещества растительного происхождения широко используются в медицине, например: атропин, галантамин, физостигмин, строфантин, дигитоксин и многие другие. Ряд соединений вызывают вредные пристрастия и являются излюбленным зельем токсикоманов и наркоманов. Среди них: кофеин, никотин, кокаин, гармин, морфин, канабинои-ды и др. Нередко продукты жизнедеятельности растений являются аллергенами. Некоторые фитотоксины обладают канцерогенной активностью. Например: сафрол и близкие соединения, содержащиеся в черном перце; соланин, обнаруживаемый в проросшем картофеле; хиноны и фенолы, широко представленные в многочисленных растениях. Отдельные токсиканты содержатся в растениях в ничтожных количествах и могут оказывать токсический эффект только в форме специально приготовленных препаратов, другие вызывают интоксикацию при использовании в пищу растений, содержащих их.
Токсины животных (зоотоксины)
Любой живой организм синтезирует огромное количество биологически активных веществ, которые после выделения, очистки и введения другим организмам в определенных дозах могут вызывать тяжелые интоксикации (в том числе и при введении в организм, продуцирующий это соединение). Часть биологически активных веществ, вырабатываемых животными, — пассивные зоотоксины. Они оказывают действие при поедании животного-продуцента. Другие — активные токсины. Они вводятся в организм жертвы с помощью специального аппарата (жала, зубов, игл и т. д.).
Некоторые животные самых разных семейств, родов и видов продуцируют настолько токсичные вещества, что это позволяет выделить их в особую группу — ядовитых (опасных) животных. Часть из них являются вторично-ядовитыми, поскольку не продуцируют, но аккумулируют яды, поступающие из окружающей среды (например, моллюски, накапливают в тканях сакситоксин, синтезируемый одноклеточными организмами, которыми эти моллюски питаются). Химическое строение зоотоксинов чрезвычайно разнообразно. Это — энзимы и другие протеины, олиго- и полипептиды, липиды, биогенные амины, гликозиды, терпены и др.
Очень часто активный зоотоксин представляет собой сложную смесь большого числа биологически активных веществ. Так, в состав яда скорпионов входят: фосфолипаза А, фосфолипаза В, ацетилхолинэстераза, фос-фатаза, гиалуронидаза, рибонуклеаза и др. В состав яда змей входят вещества, имеющие сложное белковое строение. Ежегодно от укусов ядовитых животных в мире погибает несколько тысяч человек.
Высокотоксичные соединения относительно простого строения обнаружены в тканях некоторых насекомых, моллюсков, рыб и земноводных. Отдельные представители этой группы веществ рассматривались как возможные боевые отравляющие вещества или диверсионные агенты (сак-ситоксин, тетродотоксин, батрахотоксин, буфотенин и др.). Сакситоксин и тетродотоксин, являясь избирательными блокаторами натриевых каналов возбудимых мембран, широко используются в лабораторной практике. Буфотенин — известный галлюциноген. Кантаридин — вещество, продуцируемое жуком-нарывником, способно вызывать гибель клеток, с которыми приходит в контакт, и потому его действие зависит от способа аппликации.
Неорганические соединения естественного происхождения
Среди многочисленных неорганических соединений естественного происхождения, вероятно, наибольшее токсикологическое значение имеют металлы и их соединения, а также газообразные вещества — поллютанты атмосферного воздуха и воздуха производственных помещений.
В естественных условиях металлы встречаются в форме руд и минералов. Они определяются в воздухе, почве и воде. Выплавка металлов из руд и использование в самых разнообразных отраслях человеческой деятельности привели к существенному увеличению их содержания в окружающей среде. Наибольшее токсикологическое значение имеют ртуть, кадмий, хром, мышьяк, свинец, бериллий, цинк, медь, таллий и др. Ртуть нашла применение в электронной промышленности и производстве фунгицидов. Кадмий воздействует на человека при проведении сварочных работ и в ходе других производств. В настоящее время кадмий рассматривается как один из опаснейших экотоксикантов (вещества, загрязняющие окружающую среду). Широчайшее использование свинца в хозяйственной деятельности также приводит к постепенному накоплению металла в окружающей среде. Большую опасность представляют некоторые органические соединения металлов (ртути, свинца, олова, мышьяка).
В группу газообразных токсикантов входят вещества, находящиеся в газообразном виде при нормальной температуре и атмосферном давлении, а также пары летучих жидкостей. Среди веществ, представляющих наибольшую опасность: монооксид и диоксид углерода (СО, С02), сероводород (H2S), оксиды азота (NxOy), озон (03), оксиды серы (SxOy) и др. Обмен многих поллютантов в атмосфере происходит естественным путем. Так, в процессе вулканической активности в атмосферу выбрасываются оксиды серы, галогены, сероводород. В ходе лесных пожаров выделяется огромное количество СО, оксидов азота, сажи. Основным источником газообразных веществ в атмосфере являются растения. Источниками газообразных загрязнителей антропогенного происхождения являются:
• продукты сгорания топлива;
• отходы эксплуатации транспортных средств;
• промышленные производства;
• добывающая и горнорудная промышленность.
Результатом горения топлива является образование большого количество оксидов углерода, азота, серы. Эксплуатация транспортных средств также приводит к выбросу в атмосферу свинца, СО, N0, углеводородов. Производства — основной источник кислот, растворителей, хлора, аммиака, а также металлов. Некоторые виды добывающей промышленности сопряжены с выходом в атмосферу высокотоксичных веществ (например, при экстракции золота из руды в большом количестве используется синильная кислота).
Газообразные вещества в бытовых условиях образуются при приготовлении пищи, эксплуатации бытовой техники.
Органические соединения естественного происхождения
Основными природными источниками органических соединений являются залежи угля, нефти, вулканическая деятельность. Помимо предельных и непредельных алифатических углеводородов, большое токсикологическое значение среди представителей группы имеют полициклические ароматические углеводороды (ПАУ). Эти вещества также выделяются при неполном сгорании органических материалов и обнаруживаются в дыме при горении древесины, угля, нефти, табака, а также в каменноугольной смоле и жареной пище.
Поскольку некоторые из ПАУ являются канцерогенами, они рассматриваются как опасные экотоксиканты.
2.2. Токсический процесс
Токсичность проявляется и может быть изучена только в процессе взаимодействия химического вещества и биологической системы (клетки, изолированного органа, организма, популяции).
Формирование и развитие реакций биосистемы на действие токсиканта, приводящих к ее повреждению (т. е. нарушению ее функций, жизнеспособности) или гибели, называется токсическим процессом.
Механизмы формирования и развития токсического процесса, его качественные и количественные характеристики, прежде всего, определяются строением вещества и его действующей дозой (рис. 1).
 | |||
 | |||
Однако формы, в которых токсический процесс проявляется, несомненно, зависят также от вида биологического объекта, его свойств.
Внешние, регистрируемые признаки называются проявлениями токсического процесса. В ряде упомянутых выше определений токсикологии просматривается представление, согласно которому единственной формой проявления токсического процесса является интоксикация (отравление). Интоксикация действительно основная и наиболее изученная, однако далеко не единственная форма. Глубокое понимание множественности форм проявлений токсического процесса современным врачом совершенно необходимо для:
• правильной организации изучения токсичности новых химических веществ и интерпретации получаемых результатов;
• выявления пагубных последствий действия токсикантов на человека и окружающую природу;
• планирования и проведения мероприятий по санации выявленных очагов химической опасности для отдельного человека, коллективов, населения в целом.
Проявления токсического процесса прежде всего определяются уровнем организации биологического объекта, на котором токсичность вещества (или последствия его токсического действия) изучается:
• клеточным;
• органным;
• организменным;
• популяционным.
Если токсический эффект изучают на уровне клетки (как правило, в опытах in vitro), то судят о цитотоксичности вещества. Цитотоксичность выявляется при непосредственном действии соединения на структурные элементы клетки. На практике к изучению цитотоксичности прибегают при использовании культур клеток для оценки свойств новых веществ в опытах in vitro и исследования механизмов их токсического действия; для выявления токсикантов в объектах окружающей среды (биотестирование) и т. д.
Токсический процесс на клеточном уровне проявляется:
• обратимыми структурно-функциональными изменениями клетки (изменение формы, сродства к красителям, количества орга-нелл и т. д.);
• преждевременной гибелью клетки (некроз, апоптоз);
• мутациями (генотоксичность).
Если в процессе изучения токсических свойств веществ исследуют их повреждающее действие на отдельные органы и системы, выносится суждение об органной токсичности соединений. В результате таких исследований регистрируют проявления гепатотоксичности, гематотоксичности, нефротоксичности и т. д., т. е. способность вещества, действуя на организм, вызывать поражение того или иного органа (системы). Органоток-сичность оценивают и исследуют, прежде всего, в процессе изучения свойств (биологической активности, вредного действия) новых химических веществ; в процессе диагностики заболеваний, вызванных химическими веществами.
Токсический процесс со стороны органа или системы проявляется:
• функциональными реакциями (миоз, спазм гортани, одышка, кратковременное падение артериального давления, учащение сердечного ритма, нейтрофильный лейкоцитоз и т. д.);
• заболеваниями органа (как установлено, различные вещества, при соответствующих условиях, способны инициировать самые разные виды патологических процессов);
• неопластическими процессами.
Токсическое действие веществ, регистрируемое на популяционном и биогеоценологическом уровне, может быть обозначено как экотоксиче-ское. Экотоксическое действие, как правило, исследуют врачи-профи-лактики либо в порядке текущего планового надзора, либо в процессе заданных исследований.
Экотоксичность на уровне популяции проявляется:
• ростом заболеваемости, смертности, числа врожденных дефектов развития, уменьшением рождаемости;
• нарушением демографических характеристик популяции (соотношение возрастов, полов и т. д.);
• падением средней продолжительности жизни членов популяции, их культурной деградацией.
Особый интерес для врача представляют формы токсического процесса, выявляемые на уровне целостного организма. Они также множественны и могут быть классифицированы следующим образом:
• Интоксикации — болезни химической этиологии;
• Транзиторные токсические реакции — быстро проходящие, не угрожающие здоровью состояния, сопровождающиеся временным нарушением дееспособности (например, раздражение слизистых оболочек);
ЗО
• Аллобиотические состояния — наступающее при воздействии химического фактора изменение чувствительности организма к инфекционным, химическим, лучевым, другим физическим воздействиям и психогенным нагрузкам (иммуносупрессия, аллер-гизация, толерантность к веществу, астения и т. д.);
• Специальные токсические процессы — беспороговые, имеющие продолжительный скрытый период процессы, развивающиеся у части экспонированной популяции при действии химических веществ, как правило, в сочетании с дополнительными факторами (например, канцерогенез).
Интоксикация (отравление)
Из всех форм проявления токсического процесса наиболее изученной и значимой для врача является интоксикация. Механизмы формирования и особенности течения интоксикаций зависят от строения ядов, их доз, условий взаимодействия с организмом и т. д. Однако можно выделить некоторые общие характеристики этой формы токсического процесса.
1. В зависимости от продолжительности взаимодействия химического
вещества и организма интоксикации могут быть острыми, подострыми и
хроническими.
Острой называется интоксикация, развивающаяся в результате однократного или повторного действия веществ в течение ограниченного периода времени (как правило, до нескольких суток).
Подострой называется интоксикация, развивающаяся в результате непрерывного или прерываемого во времени (интермиттирующего) действия токсиканта продолжительностью до 90 сут.
Хронической называется интоксикация, развивающаяся в результате продолжительного (иногда годы) действия токсиканта.
Не следует путать понятие острой, подострой, хронической интоксикации с острым, подострым, хроническим течением заболевания, развившегося в результате контакта с веществом. Острая интоксикация некоторыми веществами (иприты, люизит, диоксины, галогенированные бензофураны, паракват и др.) может сопровождаться развитием длительно текущего (хронического) патологического процесса.
2. Периоды интоксикации.
Как правило, в течение любой интоксикации можно выделить четыре основных периода: период контакта с веществом, скрытый период, период разгара заболевания, период выздоровления. Иногда особо выделяют период осложнений. Выраженность и продолжительность каждого из периодов зависят от вида и свойств вещества, вызвавшего интоксикацию, его дозы и условий взаимодействия с организмом.
3. В зависимости от локализации патологического процесса проявле-
ния интоксикации могут быть местными и общими.
Местными называются проявления, при которых патологический процесс развивается непосредственно на месте аппликации яда. Возможно местное поражение глаз, участков кожи, дыхательных путей и легких, различных областей желудочно-кишечного тракта. Местное действие может проявляться альтерацией тканей (формирование воспалительно-некротических изменений — действие кислот и щелочей на кожные покровы и слизистые оболочки; ипритов, люизита на глаза, кожу, слизистые оболочки желудочно-кишечного тракта, легкие и т. д.) и функциональными реакциями (сужение зрачка при действии фосфорорганических соединений на орган зрения).
Общими называются проявления, при которых в патологический процесс вовлекаются многие органы и системы организма, в том числе удаленные от места аппликации токсиканта. Причинами общей интоксикации, как правило, являются: резорбция токсиканта во внутренние среды, резорбция продуктов распада пораженных покровных тканей, рефлекторные механизмы.
Если какой-либо орган или система имеет низкий порог чувствительности к токсиканту, в сравнении с другими органами, то при определенных дозовых воздействиях возможно избирательное поражение именно этого органа или системы. Вещества, к которым порог чувствительности того или иного органа или системы значительно ниже, чем других органов, иногда обозначают как избирательно действующие. В этой связи используют такие термины, как нейротоксиканты (например, норборнан), нефротоксиканты (соли ртути), гепатотоксиканты (четыреххлористый углерод), гематотоксиканты (мышьяковистый водород), пульмонотокси-канты (фосген) и т. д. Такое действие развивается крайне редко, как правило, при отравлениях чрезвычайно токсичными веществами (например, ботулотоксином, тетродотоксином, аманитином и т. д.). Чаще общее действие ксенобиотика сопровождается развитием патологических процессов со стороны нескольких органов и систем (например, хроническое отравление мышьяком сопровождается поражением нервной системы, кожи, легких, системы крови).
В большинстве случаев отравления носят смешанный характер и сопровождаются признаками как местного, так и общего плана.
4. В зависимости от интенсивности воздействия токсиканта (характеристика, определяющаяся дозо-временными особенностями действия) интоксикация может быть тяжелой, средней степени тяжести и легкой.
Тяжелая интоксикация — состояние, угрожающее жизни. Крайняя форма тяжелой интоксикации — смертельное отравление.
Интоксикация средней степени тяжести — болезнь, при которой возможно длительное течение, развитие осложнений, необратимые повреждения органов и систем, приводящие к инвалидизации или обезображиванию пострадавшего.
Легкая интоксикация заканчивается полным выздоровлением в течение нескольких суток.
Транзиторные токсические реакции
Транзиторные токсические реакции наиболее часто развиваются вследствие раздражающего и седативно-гипнотического действия токсикантов.
Явления раздражения слизистой оболочки дыхательных путей, глаз, кожи отмечаются при остром воздействии многих веществ — альдегидов, кетонов, галогенов и т. д. Не являясь заболеванием, это состояние тем не менее обращает на себя внимание, поскольку субъективно тяжело воспринимается пострадавшим, нарушает профессиональную работоспособность.
При действии наркотических средств, многих лекарств, органических растворителей, некоторых пищевых продуктов (спирт) в малых дозах проявляется их седативно-гипнотическое действие (опьянение).
Транзиторные токсические реакции могут стать следствием только острого действия химических веществ. Увеличение действующей дозы токсиканта приводит к превращению реакции в болезнь (контакт с раздражающими веществами может привести к токсическому отеку легких, сенсибилизации покровных тканей и развитию реактивной дисфункции дыхательных путей, а простое бытовое опьянение перерастает в кому). Токсические реакции могут привести пострадавшего к гибели, не успев стать болезнью (рефлекторная смерть от остановки сердечной деятельности и дыхания при ингаляции аммиака).
Аллобиоз
К числу аллобиотических состояний можно отнести:
• иммуносупрессию и, как следствие, повышение чувствительности к инфекции;
• аллергизацию организма и повышение чувствительности к различным веществам;
• фотосенсибилизацию покровных тканей;
• изменение чувствительности к лекарствам и наркотикам при их длительном приеме (привыкание, зависимость, толерантность);
• постинтоксикационные астении;
• «доклинические» формы патологии и др. Аллобиотические состояния могут развиваться в результате острых,
подострых и хронических воздействий, быть этапом на пути развития интоксикации (субклинические формы патологии различных органов и систем), последствием перенесенного отравления (остаточные явления) и, наконец, самостоятельной формой токсического процесса.
Специальные токсические процессы
Специальные токсические процессы могут сформироваться как результат острого, подострого, но чаще — хронического воздействия веществ. К числу специальных форм токсического процесса следует отнести, прежде всего, химический канцерогенез, тератогенез, нарушение репродуктивных функций и т. д.
К канцерогенам в настоящее время причисляют любое вещество, которое ускоряет развитие опухолей или увеличивает частоту появления новообразований в популяции: Скрытый период от момента действия канцерогена до появления опухоли порой составляет десятки лет. По современным представлениям, следует выделять генетические и эпигенетические механизмы химического канцерогенеза. Вещества, действующие на геном клетки, называются «генотоксическими агентами»; вещества, провоцирующие опухолевый рост через иные механизмы, — «эпигенетическими агентами». К числу эпигенетических эффектов следует отнести повреждение механизмов генной экспрессии, иммуносупрессию, нарушение гормонального баланса и др. В материалах, опубликованных Международной ассоциацией исследований рака (МАИР), содержится указание на более чем 60 вероятных и 150 возможных веществ, факторов и производств, контакт с которыми сопряжен с реальным риском развития новообразований.
Тератогенным называется действие химического вещества на организм матери, отца или плода, сопровождающееся существенным увеличением вероятности появления структурно-функциональных нарушений у потомства. Вещества, обладающие тератогенной активностью, называются тератогенами. Существует представление, согласно которому практически любое химическое вещество, введенное в организм матери в тот или иной период беременности в достаточно большой дозе, может вызывать тератогенез. Поэтому тератогенами в узком смысле слова следует называть лишь токсиканты, вызывающие эффект в концентрациях, не оказывающих заметного действия на организм родителей. Последствия тератогенного действия вещества порой выявляются лишь при достижении ребенком определенного возраста (периода половой зрелости, полного умственного развития и т. д.), т. е. через много лет после контакта родителей с веществом.
В соответствии с иным классификационным признаком токсические процессы, выявляемые на уровне целостного организма, можно отнести к одной из следующих групп:
А. Процессы, формирующиеся по пороговому принципу. Характеризуются следующими особенностями:
• причинно-следственная связь между фактом действия вещества и развитием процесса носит безусловный характер: при действии веществ в дозах ниже определенных уровней токсический процесс не развивается; при достижении определенной дозы процесс развивается непременно;
• зависимость «доза — эффект» прослеживается на уровне каждого отдельного организма, при этом чем больше доза, тем выражен-нее проявления токсического процесса.
К этой группе относятся: интоксикации, транзиторные токсические реакции, некоторые аллобиотические состояния.
Б. Процессы, развивающиеся по беспороговому принципу. Характеризуются следующими особенностями:
• причинно-следственные связи между фактом действия вещества и развитием процесса носят вероятностный характер: вероятность формирования эффекта сохраняется при действии на организм даже одной молекулы токсиканта, вместе с тем у отдельных экспонированных организмов процесс может не развиться несмотря на воздействие в дозах, близких к смертельным;
• дозовая зависимость выраженности повреждающего действия, как правило, прослеживается на уровне популяции: чем больше доза, тем у большей части особей испытуемой (исследуемой) группы регистрируется эффект.
К таким токсическим процессам относятся: некоторые аллобиотические состояния, специальные токсические процессы (канцерогенез, тератогенез, отчасти нарушение репродуктивных функций и т. д.).
' >а щи. > ч; '< 'г -in-
'>ИН'
' 4 />
' i it 1 '( I ,
Глава 3. ТОКСИКОМЕТРИЯ
Токсичность — свойство химических веществ, которое можно измерить.
Измерение токсичности означает определение'количество вещества, действуя в котором оно вызывает различные формы токсического процесса. Чем в меньшем количестве вещество инициирует токсический процесс, тем оно токсичнее.
Раздел токсикологии, в рамках которого оценивается токсичность, называется «токсикометрия». Выделяют теоретическую и практическую токсикометрию. Теоретическая токсикометрия — область токсикологии разрабатывающая и совершенствующая методы количественной оценки токсичности химических веществ. Практическая токсикометрия — это повседневная деятельность токсикологов по определению количественных характеристик токсичности различных веществ.
Определение количественных характеристик токсичности вещества осуществляется в экспериментах на лабораторных животных, а затем уточняется (применительно к человеку) в условиях клиники и/или в ходе популяционных исследований (эпидемиологические методы исследования).
Впервые количественно оценивать токсичность веществ в опытах на экспериментальных животных предложил J. W. Trevan в 1927 г.
В процессе токсикометрических исследований определяют токсические дозы, токсические концентрации, токсодозы, действуя в которых вещества вызывают различные неблагоприятные эффекты (нарушают работоспособность, вызывают заболевание или смерть и т. д.).
Количество вещества, попавшее во внутренние среды организмам вызвавшее токсический эффект, называется токсической дозой (D). Токсическая доза выражается в единицах массы токсиканта на единицу массы организма (мг/кг).
Количество вещества, находящееся в единице объема (массы) некоего объекта окружающей среды (воды, воздуха, почвы), при контакте с которым развивается токсический эффект, называется токсической концентрацией (С). Токсическая концентрация выражается в единицах массы токсиканта на единицу объема среды (воздуха, воды) — (мг/л; г/м3) или единицу массы среды (почвы, продовольствия) — (мг/кг).
Для характеристики токсичности веществ, действующих в виде пара, газа или аэрозоля часто используют величину, обозначаемую как токсо-доза (W). Эта величина учитывает не только содержание токсиканта в
воздухе (токсическую концентрацию), но и время пребывания человека в зараженной атмосфере. Расчет величин токсодозы предложен немецким химиком Габером в начале XX в. для оценки токсичности боевых отравляющих веществ:
W = ct,
где W — токсодоза;
С — концентрация вещества в окружающем воздухе; t — время действия вещества.
При расчете токсодозы допускается, что одинаковый эффект наблюдается при кратковременном действии токсиканта в высокой концентрации и продолжительной аппликации малых концентраций вещества. Единица измерения токсодозы — мг • мин/м3. Так, токсодоза фосгена по Габеру — 450 мг • мин/м3; т. е. одинаковый эффект следует ожидать при ингаляции в течение 1 мин вещества в концентрации 450 мг/м3 и 10 мин — 45 мг/м3.
В военной токсикологии, как правило, оценивают три уровня эффектов, развивающихся при действия токсиканта на организм:
• смертельный: характеризуется величиной летальной дозы (концентрации) — LD (LC);
• непереносимый: характеризуется величиной дозы (концентрации), вызывающей существенное нарушение дееспособности (транзиторную токсическую реакцию) — ID (1С);
• пороговый: характеризуется дозой (концентрацией), вызывающей начальные проявления действия токсиканта — Lim D (Lim С).
В промышленной, сельскохозяйственной, коммунальной токсикологии при оценке токсичности веществ иногда измеряют дозы и концентрации, в которых исследуемый агент вызывает самые разные эффекты (кардио-токсический, гепатотоксический, нефротоксический, иммунотоксический и т. д.). Доза (концентрация) вещества, вызывающая любое, оцениваемое исследователем неблагоприятное действие, обозначается как эффективная доза (ED).
Поскольку живым организмам свойственна внутривидовая изменчивость (в том числе проявляющаяся и неодинаковой чувствительностью к токсиканту), для характеристики смертельной, непереносимой, пороговой дозы (концентрации) используют специальные методы постановки эксперимента и оценки полученных результатов. В основе методов определения токсичности лежит нахождение зависимости «доза — эффект».
Наиболее распространенный способ определения зависимости «доза — эффект» состоит в формировании в группе подопытных животных нескольких подгрупп. Животным, входящим в подгруппу, токсикант вводят в одинаковой дозе, а в каждой последующей подгруппе доза увеличивается. Формирование подгрупп должно осуществляться методом случайных выборок. С увеличением дозы будет увеличиваться часть животных в каждой из подгрупп, у которых развился оцениваемый эффект. Получаемую при этом зависимость можно представить в виде кумулятивной кривой частот распределения, где количество животных с положительной реакцией на токсикант (часть общего количества животных в подгруппе) является функцией дозы (рис. 2).
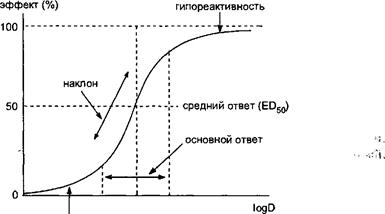
гиперреактивность
Рис. 2. Типичная кривая «доза — эффект» для группы животных, симметричная относительно средней точки (50% ответ). Основные значения ответа группы на токсикант сосредоточены вокруг среднего значения
В большинстве случаев график представляет собой S-образную кривую log-нормального распределения, симметричную относительно средней точки. Можно выделить ряд важных характеристик этой- кривой, которые целесообразно учитывать при интерпретации получаемых результатов.
1. Центральная точка кривой (значение 50% ответа) или среднеэф-фективная доза (ED50) — удобный способ характеристики токсичности вещества. Если оцениваемый эффект — летальность животных в группе, эта точка обозначается как среднесмертельная доза. Среднесмертельная доза является наиболее точной количественной характеристикой токсичности любого вещества, поскольку значение 95% доверительного интервала здесь минимально, а оцениваемый эффект — несомненен (гибель).
2. Небольшая часть популяции в левой части кривой «доза — эффект» реагирует на малые дозы токсиканта. Это группа гиперчувствительных или гиперреактивных особей. Другая часть популяции в правой части кривой реагирует лишь на очень большие дозы токсиканта. Это гипочув-ствительные, гипореактивные или резистентные особи.
3. Наклон кривой «доза — эффект», особенно вблизи среднего значения, характеризует разброс доз, вызывающих эффект. Эта величина указывает, как велико будет изменение реакции популяции на действие токсиканта с изменением действующей дозы. Крутой наклон указывает на то, что большая часть популяции будет реагировать на токсикант примерно одинаково в узком диапазоне доз, в то время как пологий наклон свидетельствует о существенных различиях в чувствительности особей к токсиканту.
3S
ЗЭ
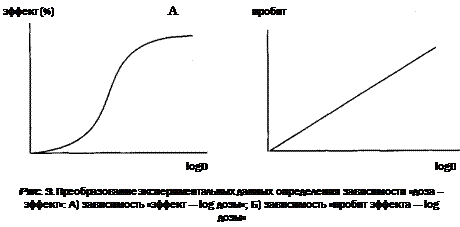
Для удобства анализа кривая «доза — эффект» часто преобразуется в линейную зависимость путем ее построения в координатах «log-пробит»: доза токсиканта представляется в логарифмах, выраженность ответной реакции — в пробитах (единицах вероятности развития эффекта). Соотношение частоты развития эффекта (в %) и вероятности его развития (в пробитах) определяется по специальным таблицам (рис. 3).
Большую сложность представляет количественная оценка способности веществ вызывать заболевания у человека при длительном действии в малых дозах, а также специальные формы токсического процесса (тератогенез, канцерогенез и т. д.). Исследования подобного рода требуют продолжительного эксперимента, проводимого по специально разработанным программам. В современной токсикометрии до конца не преодолены две основные трудности. Первая — перенос результатов, полученных в опытах на животных, на человека. Вторая — распространение результатов, полученных при относительно высоких уровнях воздействий, к малым, порой чрезвычайно малым, дозам и концентрациям ксенобиотиков, встречающимся в повседневной жизни. Для преодоления этих трудностей все данные, полученные экспериментально, по возможности, верифицируются в условиях клинических наблюдений за отравленными, а также в ходе по'пуляционных исследований состояния здоровья людей, контактировавших с вредными веществами.
Это преобразование позволяет исследователю легко, на основе анализа графика (Б), оценить результаты эксперимента: рассчитать токсические дозы и концентрации, вызывающие оцениваемый эффект у той или иной части популяции — LD(LC)so, LD(LC)i6, 84 и т. д., доверительный интервал искомых величин токсичности, крутизну наклона кривой и т. д.
Поскольку чувствительность животных различных видов к токсикантам не одинакова, а порой отличается очень значительно, опыты по оценке токсичности выполняют минимум на трех видах животных, один из которых — крупные (собаки, кошки).
Токсичность неодинакова при различных способах введения веществ (табл. 2). Поэтому в процессе исследования вещество вводят различными путями.
Таблица 2
Влияние способа введения на токсичность зарина и атропина для лабораторных животных
| Токсикант | Животное | Способ введения | Смертельная доза (мг/кг) |
| Зарин | Крысы | Внутримышечно | 0,17 |
| Через рот | 0,6 | ||
| Внутривенно | 0,05 | ||
| Атропин | Мыши | Через рот | |
| Внутривенно |
•4Q
плазма
интерстициальная жидкость
клеточная жидкость
% от массы тела
4%
13%
41%
Глава 4. ТОКСИКОКИНЕТИКА
 |
Токсикокинетика — раздел токсикологам, в рамках которого изучаются закономерности резорбции ксенобиотиков в организм, их распределения, биотрансформации и элиминации (рис. 4).
АППЛИКАЦИЯ
1 СРЕДА
------ РЕЗОРБЦИЯ-------------------------------------------------------------------------------------
I
РАСПРЕДЕЛЕНИЕ »► СВЯЗЫВАНИЕ *■ ДЕЙСТВИЕ

| ОРГАНИЗМ
---------- ЭКСКРЕЦИЯ
Рис. 4. Этапы взаимодействия организма с ксенобиотиком
Возможности современной науки по изучению токсикокинетики различных веществ возрастают по мере расширения знаний об организме и совершенствования методов химико-аналитического определения ксенобиотиков в биосредах. Токсикокинетические характеристики каждого вещества изучаются экспериментально на лабораторных животных и уточняются в условиях клиники.
Ц>А. Общие понятия токсикокинетики
С позиций токсикокинетики организм представляет собой сложную систему, состоящую из большого числа компартментов (отделов: кровь, ткани, внеклеточная жидкость, внутриклеточное содержимое и т. д.) с различными свойствами, отделенных друг от друга биологическими барьерами (рис. 5).
В ходе поступления, распределения, выведения вещества осуществляются процессы его растворения, диффузии, конвекции в жидких средах, осмоса, фильтрации через биологические барьеры.
Растворение — накопление вещества в жидкой фазе (растворителе) в молекулярной или ионизированной форме. Проникнуть во внутренние среды организма могут лишь растворившиеся (в поте, жировой смазке кожи, желудочном или кишечном соке и т. д.) вещества.
Конвекция — механическое «перемешивание» среды, приводящее к уравниванию концентрации ксенобиотика, растворенного в ней. Вещества, проникшие в кровоток, распределяются в организме, прежде всего, путем конвекции. Так как скорость кровотока в капиллярах существенно ниже, чем в крупных сосудах (в капиллярах — 0,03—0,05 см/с; в аорте — 20 см/с), перемешивание токсиканта в крови в основном осуществляется в сердце, аорте и крупных сосудах.
Диффузия — перемещение массы вещества в среде в соответствии с градиентом концентрации, осуществляемое вследствие хаотического движения молекул. Физиологически значимые диффузионные процессы осуществляются на небольшие расстояния — от нескольких микрон до миллиметра. Дело в том, что время диффузии возрастает пропорционально квадрату пути, проходимому молекулой (для диффузии на расстояние 1 мкм потребуется время 10-2 с, для 1 мм — 100 с, для 10 мм — 10 000 с, т. е. три часа). Поэтому за счет диффузии в организме осуществляется, главным образом, преодоление веществами различного рода барьеров и их распределение внутри клеток.
Фильтрация — движение растворенного вещества вместе с растворителем через пористые мембраны под действием гидростатического давления.
Осмос — процесс перемещения растворителя через мембрану, не проницаемую для растворенного вещества, в сторону более высокой концентрации последнего под влиянием силы осмотического давления. Осмотическое давление раствора пропорционально количеству частиц растворенного вещества.
Токсикокинетические характеристики вещества обусловлены как его свойствами, так и особенностями структурно-функциональной организации клеток, органов, тканей и организма в целом.
К числу важнейших свойств вещества, определяющих его токсикоки-нетику, относятся:
♦ Агрегатное состояние. Как известно, вещество может находиться в твердом, жидком и газообразном состоянии. Биодоступность ксенобиотика, т. е. его способность поступать во внутренние среды организма, а также пути проникновения во многом определяются агрегатным состоянием. Так, пары синильной кислоты поступают в организм через легкие, жидкая синильная кислота может попасть в организм через кожу (в очень ограниченном количестве) и через желудочно-кишечный тракт, через желудочно-кишечный тракт поступают также соли синильной кислоты и их растворы.
♦ Коэффициент распределения в системе «масло/вода». Определяется отношением растворимости вещества в неполярных растворителях (в том числе липидах) к растворимости в воде. Этот показатель влияет на способность соединений преимущественно накапливаться в соответствующей среде (жирорастворимые накапливаются в липидах; водорастворимые — в водной фазе плазмы крови, межклеточной и внутриклеточной жидкостях), а также преодолевать биологические барьеры.
♦ Размер молекулы. Чем больше молекула, тем меньше скорость ее диффузии, тем в большей степени затруднены процессы фильтрации и т. д. Поэтому размеры, прежде всего, влияют на проницаемость ксенобиотиков через биологические барьеры. Так, молекула СО (оксид углерода, угарный газ) практически мгновенно проникает в организм через легкце и быстро распределяется в крови и тканях, а молекуле ботулотоксина (MB более 150 ООО) для этого требуются часы.
♦ Наличие заряда в молекуле. Влияет на прохождение веществ через барьеры и их растворимость в различных биосредах. Заряженные молекулы (ионы) плохо проникают через ионные каналы, не проникают через липидные мембраны, не растворяются в липидной фазе клеток и тканей. Даже ионы одного и того же элемента, имеющие различный заряд, по-разному преодолевают биологические барьеры: ионы Fe+2 — всасываются в желудочно-кишечном тракте, a Fe+3 — нет.
♦ Величина константы диссоциации солей, слабых кислот и оснований. Определяет относительную часть молекул токсиканта, диссоциировавших на ионы в условиях внутренней среды.
♦ Химические свойства. Влияют на сродство токсикантов к структурным элементам клеток различных тканей и органов.
Важнейшими характеристиками организма, влияющими на токсико-кинетику ксенобиотиков, являются свойства его компартментов и разделяющих их биологических барьеров.
Основными свойствами компартментов являются:
♦ Соотношение воды и жира. Биологические структуры, ткани, органы могут содержать большое количество липидов (биологические мембраны, жировая ткань, мозг) либо преимущественно состоять из воды (мышечная ткань, соединительная ткань и т. д.). Чем больше жира в структуре, тем в большем количестве в ней накапливаются жирорастворимые вещества. Так, жирорастворимый хлорорганический пестицид дихлордифенилтрихлорметилметан (ДДТ) будет накапливаться в жировой клетчатке и сальнике. Хорошо растворимые в липидах молекулы фосфорорганических соединений легко проникают в мозг.
♦ Наличие молекул, активно связывающих токсикант. Например, клетки тканей с высоким содержанием цистеина (кожа и ее придатки) активно накапливают вещества, образующие прочные связи с сульфгидри-льными группами (мышьяк, таллий и т. д.). Белки костной ткани активно связывают двухвалентные металлы (стронций, свинец).
К числу биологических барьеров (с позиций токсикокинетики) относятся структуры самого разного строения. Это клеточные и внутриклеточные мембраны, гистогематические барьеры (например: гематоэнце-фалический, плацентарный и т. д.), покровные ткани (кожа, слизистые оболочки). Все барьеры — гидрофобные образования богатые липидами, поэтому их легко преодолевают вещества с высоким значением коэффициента распределения в системе «масло/вода» (хорошо растворимые в липидах). Многие барьеры содержат «поры» — заполненные водой «каналы» в биологическом барьере (структура и размеры пор в различных барьерах совершенно различны).
Основные свойства барьеров:
♦ Толщина и суммарная площадь. Чем тоньше барьер и чем больше площадь его поверхности, тем большее количество вещества может через него пройти в единицу времени. Как видно из данных, приведенных в табл. 3, среди барьеров, образованных покровными тканями, наибольшую поверхность имеют альвеолярно-капиллярный барьер легких и слизистая оболочка тонкого кишечника. Однако наибольшую суммарную площадь поверхности, во много раз превосходящую площадь покровных тканей и гистогематических барьеров, имеет гипотетический интегральный барьер, образуемый мембранами всех клеток организма, отделяющий их от внеклеточной жидкости. Поэтому все, что всасывается в организм через покровные ткани, быстро попадает в клетки тех или иных органов.
♦ Наличие и размеры пор. Через поры диффундируют и фильтруются водорастворимые соединения. Диаметр пор и их суммарная площадь в различных биологических барьерах не одинаковы (табл. 4).
♦ Наличие механизмов активного или облегченного транспорта химических веществ. Не растворимые в липидах соединения диффундируют и фильтруются через биопоры либо преодолевают барьер благодаря механизму активного транспорта. Активный транспорт веществ через биологические мембраны проходит с большей скоростью, чем диффузия. Он
осуществляется специальными транспортными белками и следует закономерностям ферментативных реакций. Активный транспорт обеспечивает ток малых молекул и ионов против градиента их концентраций. Для обеспечения процессов нужна энергия, запасенная в форме макроэргиче-ских соединений (например, АТФ) (табл. 5).
Таблица 3
Площадь «всасывающих» поверхностей тела человека, м2
| Орган | Площадь |
| Кожа | 1,2-2 |
| Полость рта | 0,02 |
| Желудок | 0,1-0,2 |
| Тонкий кишечник | |
| Толстый кишечник | 0,5-1,0 |
| Прямая кишка | 0,04-0,07 |
| Полость носа | 0,01 |
| Легкие |
Таблица 4
| Тип барьера |
| Примеры |
Характеристики различных биологических барьеров
| Липидная мембрана (поры отсутствуют) |
| Слизистые оболочки полости рта, эпителий почечных канальцев, эпителий кожи, гематоэнцефалический барьер Эпителий тонкой и толстой кишок |
Проницаемость для веществ
| Липидная мембрана с порами малого диаметра (0,3-0,8 нм) |
Хорошо растворимые в жирах, неионизированные молекулы
| Слизистые оболочки глаз, носоглотки, мочевого пузыря |
| Липидная мембрана с порами средних размеров (0,8-4 нм) Липидная мембрана с порами большого диаметра (более 4 нм) Пористая мембрана |
Хорошо растворимые в жирах и низкомолекулярные водорастворимые молекулы (до 200 Д)
| Печеночные капилляры, желчные капилляры, альвеолярно-капиллярный барьер, капилляры кожи, мышц Гломерулярный аппарат почек |
Липофипьные и в меньшей степени гидрофильные молекулы
Липофипьные и гидрофильные молекулы с молекулярной массой до 4000 Д
Гидрофильные молекулы с молекулярной массой до 50 000 Д
Таблица 5
Признаки специфического транспорта
1. Связывание ксенобиотика с наружной поверхностью мембраны и молекулой-носителем
2. Транслокация связавшегося вещества через мембрану специальным носителем
3. Высвобождение вещества из связи с носителем внутри клетки
4. Субстратная специфичность взаимодействия вещества с носителем
5. Кинетика процесса, описываемая гиперболой (наличие максимальной скорости процесса — Vmax и константы процесса — Кт)
6. Наличие веществ, избирательно блокирующих процесс
7. Более высокая скорость процесса в сравнении с процессом диффузии__________
Транспорт через биологические мембраны токсикантов, имеющих очень большую массу (белковых токсинов), может осуществляться с помощью цитозов (пиноцитоза, рецептор-связанного эндоцитоза и т. д.). Цитозы — процессы, неразрывно связанные с клеточным метаболизмом (табл. 6).
Таблица 6
Транспорт веществ путем цитозов
1. Эндоцитозы: захват вещества клеткой
1.1. Фагоцитоз: захват корпускулярных частиц
1.2. Пиноцитоз: захват капель жидкости и растворенных в ней молекул
1.3. Рецептор-обусловленный эндоцитоз: связывание макромолекул на специфических рецепторах клеточной мембраны с последующим образованием шеро-ховатых везикул__________________________
2. Экзоцитозы: выделение веществ из клетки
2.1. Гранулокринная секреция: выделение везикул, содержащих клеточное вещество
2.2. Отпочковывание: выделение части цитоплазмы содержащихся в ней веществ путем краевого отделения части клетки
3. Трансцитоз (цитопемзис): транспорт веществ через объем клетки_____________
4. Синцитозы
4.1. Слияние клеток
4.2. Слияние клеток липидными везикулами, содержащими вещества_____________
5.Интрацитоз: образование везикул и их слияние внутри клетки_________________
1.2. Резорбция
Резорбция — это процесс проникновения вещества из внешней среды в кровяное или лимфатическое русло организма.
Основными структурами, участвующими в резорбции токсикантов, являются легкие (ингаляционное воздействие), кожа (трансдермальное воздействие), желудочно-кишечный тракт (энтеральное воздействие, пе-роральная интоксикация).
Часть I. ТОКСИКОЛОГИЯ
Ингаляционное поступление ^
Легкие являются основным путем поступления в организм газов (паров) и аэрозолей.
Благодаря большой площади поверхности и тесному контакту воздуха с капиллярным руслом, процесс резорбции здесь проходит с высокой эффективностью.
Скорость перехода газа (пара) из вдыхаемого воздуха в кровь тем выше, чем больше градиент концентрации в системе воздух — кровь. Содержание газа в оттекающей от легких крови пропорционально его парциальному давлению во вдыхаемом воздухе. Усиление легочной вентиляции увеличивает диффузию газа (пара) в направлении концентрационного градиента или градиента парциального давления (из организма — в организм, в зависимости от указанных выше условий). Скорость резорбции газообразного (парообразного) токсиканта увеличивается с увеличением скорости кровотока в легочной ткани.
Захват газов кровью зависит от их растворимости в крови. При прочих равных условиях состояние равновесия в системе альвеолярный воздух — кровь устанавливается тем быстрее, чем менее растворим токсикант в крови.
Легочная резорбция аэрозолей. Аэрозоли представляют собой фазовые смеси, состоящие из воздуха и мелких частиц жидкости (туман) или твердого вещества (дымы). Закономерности резорбции аэрозолей в дыхательных путях отличаются от закономерностей резорбции газов (паров).
Резорбция в дыхательной системе аэрозоля является функцией количества вещества, адсорбировавшегося на поверхности легких и дыхательных путей, и зависит от концентрации аэрозоля, размера его частиц, частоты и глубины дыхания.
Адсорбция крупных частиц (около 5 мкм) происходит преимущественно в верхних дыхательных путях, мелких частиц (около 1 мкм) — в глубоких отделах дыхательных путей и альвеолах.
В силу тесного контакта между альвеолярным воздухом и капиллярным руслом, порозности альвеолярно-капиллярного барьера в дыхательных путях могут всасываться даже макромолекулы (ботулотоксин и др.). Частицы аэрозоля, адсорбировавшиеся на поверхности дыхательных путей, могут захватываться макрофагами и с ними поступать в кровоток.
Некоторые вещества, действуя в форме газов и аэрозолей, обладая высокой реакционной способностью, взаимодействуют непосредственно с легочной тканью, вызывая местное действие (хлор, фосген и т. д.). Такие вещества резорбции практически не подвергаются; закономерности, характеризующие процесс, на них не распространяются.
Поступление через кожу
Морфология, биохимия кожи препятствуют резорбции большинства токсикантов. Для водорастворимых веществ кожа представляет непреодолимый барьер. Некоторой проницаемостью кожные покровы обладают для веществ, хорошо растворимых в липидах (например, для зомана, фосфо-рилтиохолинов, иприта, люизита, тетраэтилсвинца и т. д.). Возможны два способа прохождения токсиканта через кожу: трансэпидермальный (через клетки эпидермиса) и трансфолликулярный (через волосяные фолликулы).
Помимо способности растворяться в липидах, на скорость резорбции веществ через кожу влияют: агрегатное состояние, дисперсность (размер частиц аэрозолей), площадь и область кожных покровов, на которую нанесен токсикант, интенсивность кровотока в кожных покровах.
Механические повреждения, мацерация кожи, раздражение, сопровождающиеся усилением кровотока, усиливают процесс резорбции токсикантов. Некоторые органические растворители, разрущающие липид-ный слой кожи, могут усиливать кожную резорбцию.
Поступление через желудочно-кишечный тракт
Энтеральная резорбция предполагает хотя бы минимальную растворимость токсиканта в содержимом ЖКТ. Слизистая оболочка желудочно-кишечного тракта в силу особенностей строения приспособлена для быстрой резорбции веществ. Поскольку сосудистая сеть желудочно-кишечного тракта развита хорошо, резорбция здесь не лимитирована фактором кровоснабжения. Закономерности резорбции аналогичны во всех отделах желудочно-кишечного тракта.
Имеющиеся особенности всасывания в различных отделах ЖКТ определяются:
♦ Различиями рН содержимого отделов. Содержимое желудка имеет кислую реакцию. Слабые кислоты (например, производные барбитуровой кислоты и др.), в основном, здесь находятся в недиссоциированном состоянии и потому относительно легко всасываются. Слабые основания (алкалоиды), напротив, в желудочном соке находятся в форме ионов и потому — не всасываются. В кишечнике рН — щелочная, и поэтому здесь преобладают ионизированная форма кислот и неионизированная форма слабых оснований.
♦ Неодинаковой площадью всасывающей поверхности (см. табл. 1). Количество и качество пищи, принятой вместе (до, после) с токсикантом, могут существенно повлиять на скорость его резорбции.
щавач. ivjrvuHrwcxyincmrvM
 Характер распределения токсикантов в организме определяется общими закономерностями (см. выше). Дополнительными факторами, влияющими на процесс, являются интенсивность кровоснабжения органов (рис. 6), а также суммарная площадь их капиллярного русла (табл. 7).
Характер распределения токсикантов в организме определяется общими закономерностями (см. выше). Дополнительными факторами, влияющими на процесс, являются интенсивность кровоснабжения органов (рис. 6), а также суммарная площадь их капиллярного русла (табл. 7).
Таблица 7
Площадь капиллярного русла различных органов собаки, см2/г ткани
| Мозг | Почки | Печень | Легкие | Мышцы |
Так, например, захвату ксенобиотиков печенью способствуют хорошее кровоснабжение органа, высокая степень порозности эндотелия капиллярного русла. Клеточные мембраны гепатоцитов также содержат большое количество пор, что облегчает поступление веществ в клетки. Помимо указанного, накоплению ксенобиотиков в органе способствуют механизмы их активного захвата из плазмы крови (активный транспорт кислот, щелочей, пиноцитоз макромолекул).
Напротив, проникновение из крови в ЦНС многих (прежде всего водорастворимых) ксенобиотиков существенно затруднено наличием так называемого гематоэнцефалического барьера (ГЭБ).
Гематоэнцефалический барьер формируется при участии ряда анатомических структур головного мозга.
Во-первых, эндотелий капиллярного русла головного мозга отличается от эндотелия других органов чрезвычайно тесным контактом клеток друг с другом. Эффективный радиус пор капилляров мозга значительно меньше, чем в других тканях, и составляет, например, у кролика 0,7—0,9 нм. Крупные молекулы не в состоянии проникать через эндотелиальный барьер. Водорастворимые и заряженные молекулы могут проходить непосредственно через биомембраны и цитоплазму эндотелиальных клеток только в том случае, если имеют малые размеры (CN~). В норме эндоте-лиальные клетки мозга лишены способности к пиноцитозу. Лишь при некоторых патологических состояниях (гипоксия мозга) в эндотелии сосудов образуются пиноцитарные вакуоли, при этом возрастает проницаемость гематоэнцефалического барьера, увеличивается уязвимость мозга для действия токсикантов.
Во-вторых, капилляры мозга плотно окутаны отростками астроцитар-ной глии. Астроцитарная оболочка препятствует проникновению гидрофильных ксенобиотиков из крови в ткань мозга и их взаимодействию с другими клеточными элементами. В некоторых областях мозга, таких как срединное возвышение гипоталамуса, медиальная преоптическая область, область IV желудочка, астроцитарная оболочка капилляров развита сравнительно слабо. В этих регионах возможно проникновение водорастворимых и даже заряженных молекул токсикантов в ЦНС, но также в ограниченном количестве.
Наконец, последней структурой, вносящей вклад в формирование ГЭБ, является базальная мембрана, залегающая между эндотелиальными клетками капилляров и отростками астроцитов. Эта мембрана имеет упорядоченную фибриллярную макропротеидную структуру, обеспечивающую избирательное проникновение в мозг ряда важных для обеспечения его жизнедеятельности молекул (кислорода, глюкозы и др.).
5 1
Аналогичный ГЭБ барьер окружает периферический отдел нервной системы (гематоневральный барьер). Однако, так же как и в ЦНС, здесь имеются анатомические образования с повышенной проницаемостью для токсикантов. К числу таких относятся спинальные корешки дорсальных (чувствительных) ганглиев и вегетативные (автономные) ганглии.
Плацентарный барьер проницаем для многих веществ, в том числе высокомолекулярных соединений. Это обстоятельство может иметь неблагоприятные последствия для плода, особенно при попадании токсикантов в организм матери в первые 12 нед беременности (период органогенеза).
Важным элементом распределения некоторых ксенобиотиков в организме является их депонирование. Депонирование — это накопление и длительное сохранение химического вещества в относительно высокой концентрации в одном или нескольких органах (или тканях). Порой депонирование не сопровождается повреждением биологически значимых молекул-мишеней (токсический процесс не формируется).
В основе депонирования лежат два явления:
• высокое физико-химическое сродство ксенобиотика к неким компонентам биосистемы (химическое взаимодействие с элементами биосистемы или избирательное накопление липофиль-ных веществ в жировой ткани);
• кумуляция благодаря избирательному, активному захвату токсиканта клетками органа (ткани).
Ряд токсикантов депонируются в тканях настолько прочно, что выведение их из организма практически невозможно. Например, период полуэлиминации кадмия из организма человека составляет более 20 лет.
Явление депонирования веществ связано с явлением кумуляции, но не тождественно ему. Под материальной кумуляцией понимают процесс постепенного накопления токсиканта при длительном поступлении в организм преимущественно в области функционально-значимых структур-мишеней, действие на которые приводит к развитию токсического процесса. Явление кумуляции лежит в основе хронических интоксикаций. В ряде случаев выявляют так называемую функциональную кумуляцию — накопление неблагоприятных эффектов токсиканта при его продолжительном введении.
ЧА» Элиминация
Элиминацией называется вся совокупность процессов, приводящих к снижению содержания токсиканта в организме. Она включает процессы экскреции (выведения) ксенобиотика из организма и его биотрансформацию.
4.4.1. Экскреция
Основными органами экскреции являются легкие (для летучих соединений), почки, печень, в меньшей степени слизистая оболочка желудочно-кишечного тракта, кожа и ее придатки.
Легочная экскреция
Газы и пары летучих веществ выделяются через легкие в соответствии с градиентом их парциального давления между кровью и альвеолярным воздухом. Закономерности экскреции газообразных (парообразных) веществ полностью идентичны закономерностям их поступления через легкие (см. выше).
Почечная экскреция
Почки — важнейший орган выделения. Через почки выводятся продукты обмена веществ, многие ксенобиотики и продукты их метаболизма. Масса почек чуть менее 0,3% массы тела, однако через орган протекает около 30% минутного объема крови. Благодаря хорошему кровоснабжению, находящиеся в крови вещества, подлежащие выведению, быстро переходят в орган, а затем и выделяются с мочой. В основе процесса лежат три механизма (рис. 7):
| ЭКСКРЕЦИЯ |
| ФИЛЬТРАЦИЯ |
• 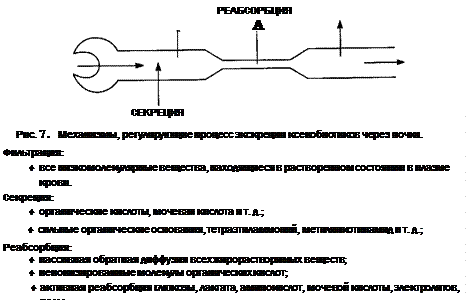
фильтрация через гломерулярно-капиллярный барьер;
• секреция эпителием почечных канальцев;
• реабсорбция клетками эпителия.
Через почки протекает около 700 мл плазмы крови в минуту, из которых 20% (125—130 мл/мин) отфильтровывается через гломерулярно-ка-пиллярный барьер. Собирающаяся в почечных клубочках первичная моча по сути представляет собой сыворотку крови. Более 99% отфильтрованной жидкости реабсорбируется в почечных канальцах. При этом концентрация растворенных в моче веществ возрастает в 100 раз. Хорошо растворимые в липидах соединения по этой причине практически полностью диффундируют из первичной мочи через эпителий почечных канальцев обратно в кровь (реабсорбция). Выведения таких веществ из организма практически не происходит.
Способность к выведению через почки у слабых кислот и оснований во многом определяется рН первичной мочи: выведение слабых оснований усиливается при подкислении мочи (преобладает ионизированная форма оснований — затруднена реабсорбция их в канальцах); выведение слабых кислот усиливается при подщелачивании мочи (преобладает ионизированная форма кислот).
Многие токсиканты выводятся через почки с помощью механизма активной секреции. Функции секретирующей структуры выполняет эпителий почечных канальцев. Существуют независимые механизмы активного транспорта для веществ со щелочными и кислотными свойствами.
Печеночная экскреция
Печеночная экскреция — отчасти следствие простой диффузии веществ в желчь, отчасти — активного транспорта ксенобиотиков, осуществляемого гепатоцитами. Благодаря активному транспорту отношение концентраций веществ в желчи и плазме крови значительно выше 1. Высокая концентрация химических веществ в желчи обеспечивает осмос воды из сосудистого русла в желчные ходы. Наиболее активно печенью выводятся вещества с молекулярной массой более 600 дальтон, имеющие в структуре полярную анионную или катионную группу.
Ряд ксенобиотиков, выделяющихся с желчью (липофильные вещества либо гидрофильные соединения, превращающиеся в липофильные под влиянием кишечной флоры), способны к обратному всасыванию слизистой оболочкой кишечника и по системе портальной вены повторно на^ капливаются в печени. Это явление называется гепато-энтеральной циркуляцией.
Метаболизм ксенобиотиков (биотрансформация)
Многие ксенобиотики в организме подвергаются метаболическим превращениям (биотрансформации).
Основной биологический смысл биотрансформации — превращение исходного токсиканта в форму, удобную для скорейшей экскреции. Биотрансформация — ферментативный процесс.
Выделяют 2 фазы метаболических превращений чужеродных соединений (рис. 8):
I — фаза окислительной, восстановительной либо гидролитической
трансформации молекулы;
| I ФАЗА |
II — фаза синтетических превращений.
| КОНЪЮГАТ |
| КСЕНОБИОТИК |
II ФАЗА
| ГЛЮКУРОНИЗАЦИЯ СУЛЬФАТАЦИЯ МЕТИЛИРОВАНИЕ СВЯЗЫВАНИЕ С ГЛУТАТИОНОМ |
ПРОМЕЖУТОЧНЫЙ ПРОДУКТ
ОКИСЛЕНИЕ
ВОССТАНОВЛЕНИЕ
ГИДРОЛИЗ
Рис. 8. Фазы метаболизма чужеродных соединении
В I фазе происходят следующие реакции биотрансформации:
• окисление — гидроксилирование, декарбоксилирование, образование оксидов, десульфурирование, дегалогенизирование молекул, окисление спиртов и альдегидов;
• восстановление — восстановление альдегидов, азовосстановле-ние, нитровосстановление;
• гидролиз — расщепление эфиров, амидных связей. Основные энзимы, активирующие процессы биотрансформации I фазы: цитохром Р-450 зависимые оксидазы смешанной функции (Р-450), флавинсодержащие монооксигеназы смешанной функции (ФМО), гид-ропероксидазы, алкоголь- и альдегиддегидрогеназы, флавопротеинредук-тазы, эпоксидгидролаза.
Нередко в результате метаболизма вещества на первом этапе образуются промежуточные продукты, обладающие высокой биологической активностью (табл. 8).
Большинство энзимов I фазы локализованы в гладком эндоплазма-тическом ретикулуме клетки (микросомальные энзимы); часть — в растворимой фазе цитозоля (алкоголь-, альдегиддегидрогеназа, эстеразы). Некоторые гидролазы содержатся в плазме крови (карбоксилэстераза, арилэстераза).
В II фазе происходят следующие реакции биотрансформации:
• конъюгация промежуточных продуктов с глюкуроновой кислотой,
• конъюгация с серной кислотой,
• конъюгация с глутатионом,
• метилирование,
• ацилирование,
• образование меркаптосоединений.
Таблица 9
Характеристика основных реакций конъюгации ксенобиотиков

 Основные энзимы, активирующие процесс биотрансформации II фазы: УДФ-глюкуронозилтрансфераза, сульфотрансфераза, ацетил- КоА-амин-N-ацетилтрансфераза, глутатион-Б-трансфераза, цистеинконъюгирующие лиазы.
Основные энзимы, активирующие процесс биотрансформации II фазы: УДФ-глюкуронозилтрансфераза, сульфотрансфераза, ацетил- КоА-амин-N-ацетилтрансфераза, глутатион-Б-трансфераза, цистеинконъюгирующие лиазы.
Общая характеристика реакций конъюгации ксенобиотиков представлена в табл. 9.
| Присоединяемый агент |
| Реакция |
Функциональная группа ксенобиотика
| ■ОН; -COOH; NH2; -NR2; -SH; -СН -ОН; -SH; COOH; =NH -OH; -NH2; -SH -OH; -NH2 -OH; -NH2 -CN- |
| УДФ-глюкуроновая кислота УДФ-глюкоза ФАФС S-аденозилметионин Ацетил КоА Сульфон-сульфид |
А. Реакции, протекающие при участии активированных форм присоединяемых агентов
Конъюгация с глюкуроновой кислотой
Конъюгация с глюкозой Сульфатация Метилирование Ацетилирование Детоксикация цианида
Б. Реакции, протекающие при участии активированных форм ксенобиотиков
Конъюгация с глутатионом
| Глутатион |
| Конъюгация с аминокислотами |
Ареноксиды; эпоксиды; галогенированные алкильные и арильные углеводороды
-СООН
Глицин; глутамин; орнитин; таурин; цистеин
Большинство энзимов II фазы локализованы в растворимой фазе ци-тозоля.
Основным органом, метаболизирующим ксенобиотики, является печень. В меньшей степени активно идут превращения ксенобиотиков в легких, почках, кишечнике, коже, селезенке и других тканях. Некоторые вещества метаболизируют в крови. Как правило, в метаболических превращениях ксенобиотика принимают участие несколько органов (рис. 9).
ДРУГИЕ ОРГАНЫ дальнейший метаболизм
ЭФФЕКТ
продукт фазы I
| продукт фазы II |
| ЖЕЛЧЬ |
ПЕЧЕНЬ Фаза I Фаза II
| ПОЧКИ дальнейший метаболизм ЭКСКРЕЦИЯ |
реабсорбция
КИШЕЧНИК
метаболизм в стенке кишечника бактериальный метаболизм
ЭКСКРЕЦИЯ
Рос. 9. Локализация этапов метаболических превращений ксенобиотиков в организме
5В
ШЫШк
5"7
 |
На интенсивность биотрансформации ксенобиотиков могут влиять различные факторы.
Естественные факторы:
• вид организма, пол, возраст, состояние питания. Экзогенные факторы:
♦ Повреждение структур, метаболизирующих ксенобиотики. На метаболизме ксенобиотиков сказываются: гепатоэктомия, адреналэктомия, кастрация.
♦ Химические вещества, способные вызывать индукцию (усиление) метаболизма, конкурентное и неконкурентное ингибирование метаболизма.
К числу индукторов биотрансформации чужеродных веществ относятся: барбитураты, полициклические углеводороды, андрогенные стероиды, анаболические стероиды, глюкокортикоиды, спиронолактон и др.
К числу ингибиторов биотрансформации относятся: метирапон, пи-перонилбутаксид, 7,8-бензофлавон, SKF-525, Lilly 18947 и др.
Биологическими последствиями биотрансформации ксенобиотиков могут стать:
• ослабление или полная потеря биологической активности токсикантов (ФОБ, синильная кислота);
• изменение биологической активности: исходное вещество и продукты его метаболизма в достаточной степени токсичны, но действуют на различные биомишени (метанол, дихлорэтан и т. д.);
• усиление токсичности или появление новых свойств (иприт, фторэтанол, бенз(а)пирен и др.).
Процесс увеличения активности токсиканта в ходе его метаболизма называется биоактивацией.
Биоактивация, как правило, осуществляется в ходе I фазы метаболизма (образование промежуточных продуктов метаболизма, часто обладающих высокой реакционной способностью).
В ходе II фазы метаболизма биологическая активность продукта превращения обычно существенно снижается.
Неопределенные последствия метаболизма многих ксенобиотиков заставляют с большой осторожностью относиться к модификации процесса с помощью доступных в настоящее время средств и методов.
4.5» Количественные характеристики токсикокинетики
Количественная токсикокинетика — раздел токсикологии, разрабатывающий математические модели, описывающие поступление, распределение, элиминацию ксенобиотиков.
Основой создания токсикокинетических моделей являются получаемые экспериментально графики зависимости концентрации веществ в крови и тканях от времени после различных способов введения токсиканта (рис. 10).
концентрация в плазме (мкг/мл)
экстраполяция кривой: < С(о) — условная начальная концентрация
угрл наклона касательной dC/dt;-
'скорость элиминации! !
| I 1 1 < 1 1 ■ 1 1 ППК — площадь под кривой | |||||
| г П | ПК = ППК | 1 + ППК2 | + ППК 3 +... | ||
| ; ППК 1 | ППК 2 | ППКЗ |
среди прочего, количеством всосавшегося токсиканта. Если соотнести величину ППК токсиканта для внутривенного введения (ППК;У) с величиной ППК_ при ином (любом) способе аппликации, то значение коэффициента QR = ППК(_/ППК)у и определит величину квоты резорбции для исследуемого способа введения токсиканта. Чем ближе значение QR к 1, тем лучше всасывается вещество исследуемым способом.
При анализе данных необходимо учитывать, что в таком прочтении величина биодоступности не в полной мере отражает последствия действия токсиканта на организм. Дело в том, что ППК при разных способах воздействия может быть одинаковой, но различная скорость поступления и одновременно протекающая элиминация соединения могут привести к совершенно разным эффектам действия одного и того же вещества. Пример такой ситуации приведен на рис. 11.
| О |
концентрация в плазме (мкг/мл)
| - | N1 | смертельная | ||||
| концентрация | ||||||
| N3 | ||||||
| пороговая | ||||||
| концентрация | ||||||
| 1 , L......... __... 1, _........ |_....... ,, I.................. I............. __......... __ |
0 1 2 3 4 5 время (ч)
Рис. 11. Кривые динамики концентрации вещества А в плазме крови экспериментального животного
Вещество введено в дозе D различными способами: N1 — внутривенное введение N2 — введение через желудочно-кишечный тракт
N3 — введение через желудочно-кишечный тракт в форме, адсорбированной на ионно-обменной смоле
Как видно из данных, приведенных на рис. 11, несмотря на прекрасную всасываемость вещества в ЖКТ смертельный эффект может развиться лишь при его внутривенном введении в дозе D.
Объем распределения. Абсолютным объемом распределения вещества (VD) называется сумма мнимых объемов внутренней среды организма, в которых вещество распределилось таким образом, что его концентрация в них равна концентрации в плазме крови (С).
ВО _________
Vd рассчитывается как отношение введенного количества токсиканта (D) к величине его концентрации в плазме крови:
VD = D/C.
Относительный объем распределения (Vr) целесообразно рассчитывать с учетом массы организма (М):
Vr = VD/M — выражается в процентах от массы тела.
Для веществ, распределяющихся только в плазме крови, Vr равен объему плазмы крови, распределяющихся во внеклеточной жидкости —-суммарному объему плазмы крови и внеклеточной жидкости и т. д. Для веществ, активно связывающихся тканями организма, относительный объем распределения может быть более 100%.
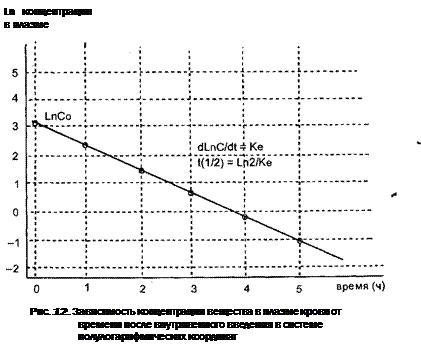 |
Периодом полуэлиминации называется время, в течение которого элиминирует половина введенного количества токсиканта. Период полуэлиминации зависит от строения вещества и функционального состояния органов, метаболизирующих и экскретирующих ксенобиотики. В подавляющем большинстве случаев элиминация осуществляется в соответствии с кинетическим уравнением 1-го порядка, т. е. зависимость «концентрация — время» носит экспоненциальный характер (см. рис. 10). Представление зависимости в координатах «1п концентрации — время» позволяет преобразовать ее в прямую (рис. 12).
Величина угла наклона кривой (lnC/t) называется константой скорости элиминации (Ке), зная которую, легко рассчитать период полуэлиминации (ti/г). Зная период полуэлиминации, просто оценить время пребывания вещества в организме: при в/в введении вещества — это время приблизительно составляет 5t1/2. Через этот промежуток времени в организме остается не более 3% от введенного количества токсиканта.
Клиренс (С1 — мл/мин) — часть абсолютного объема распределения (условно: плазмы крови), полностью освобождающегося от ксенобиотика в единицу времени. Величина клиренса может быть рассчитана по формуле:
CI = D/ППК,
где D — доза введенного вещества (мг); ППК— площадь под кривой (мг'мин/мл).
'-.if ■;ц<>:
Глава 5. ТОКСИКОДИНАМИКА
Токсикодинамика — раздел токсикологии, в рамках которого изучается и рассматривается механизм токсического действия, закономерности развития и проявления различных форм токсического процесса.
5.1. Механизм токсического действия
Взаимодействие на молекулярном уровне токсиканта с организмом, приводящее к развитию токсического процесса, называется механизмом токсического действия.
В основе механизма действия могут лежать физико-химические и химические реакции взаимодействия токсиканта с биологическим субстратом.
Токсический процесс, инициируемый физико-химическими эффектами, как правило, обусловлен растворением токсиканта в определенных компартментах клетки, ткани, организма. При этом существенно изменяются их физико-химические свойства. Так, неполярные молекулы ряда ксенобиотиков: предельных углеводородов, спиртов, эфиров, галогени-рованных углеводородов, низкомолекулярных циклических углеводородов — накапливаются в липидных бислоях возбудимых биологических мембран. При этом изменяются удельный объем, вязкость, проницаемость мембран для ионов и тем самым модифицируются их физиологические свойства. Кислоты, щелочи, растворяясь в водной фазе клетки, ткани, изменяют рН среды. При интенсивном воздействии это может привести к денатурации макромолекул, их разрушению.
Особенность данного типа эффектов — отсутствие специфичности в действии токсиканта. Токсичность определяется физико-химическими свойствами вещества (величиной коэффициента распределения в системе масло — вода, константы диэлектрической проницаемости, константы диссоциации и т. д.).
Чаще в основе токсичности лежат химические реакции токсиканта с определенными субстратами — компонентами живой системы.
В токсикологии (как и фармакологии) любой структурный элемент живой (биологической) системы, с которым вступает в химическое взаимодействие токсикант (лекарство), обозначают термином «рецептор». В таком прочтении это понятие ввел в химиобиологию в начале XX в. Пауль Эрлих (1913).
Спектр энергетических характеристик рецептор-лигандного взаимодействия необыкновенно широк: от образования слабых, легко разрушающихся связей до формирования необратимых комплексов (см. ниже). Характер взаимодействия и структура сформировавшегося комплекса зависят не только от строения токсиканта, конформации рецептора, но и от свойств среды: рН, ионной силы и т. д. В соответствии с законом действующих масс количество образовавшихся комплексов вещество-рецептор определяется энергией взаимодействия (сродством) и содержанием обоих компонентов реакции (вещества и рецептора к нему) в биологической системе.
Рецепторы могут быть «немыми» и активными. «Немой» рецептор — это структурный компонент биологической системы, взаимодействие которого с веществом не приводит к формированию ответной реакции (например, связывание мышьяка белками, входящими в состав волос, ногтей, или растворение ДДТ в липидах вакуолей жировых клеток сальника и подкожной клетчатки). Активный рецептор — структурный компонент биологической системы, взаимодействие которого с токсикантом инициирует токсический процесс (например, активный центр цитохромоксида-зы, взаимодействие которого с синильной кислотой приводит к острому отравлению).
Как известно, в биологии термин «рецептор» используется еще и для обозначения структур, способных избирательно взаимодействовать с эндогенными молекулами-биорегуляторами (нейромедиаторами, гормонами, субстратами и т. д.) и принимающих непосредственное участие в восприятии и передаче регуляторных сигналов.
Для того чтобы избежать терминологических трудностей, для обозначения структурных элементов организма, взаимодействуя с которыми токсикант инициирует токсический процесс, вместо термина «рецептор» в настоящее время часто используют термин «структура-мишень».
Мишенями (рецепторами) для токсического воздействия могут быть:
• структурные элементы межклеточного пространства;
• структурные элементы клеток организма;
• структурные элементы систем регуляции клеточной активности. Любая клетка, ткань, орган содержит огромное количество потенциальных рецепторов (структур-мишеней) различных типов («запускающих» различные биологические реакции), с которыми могут вступить во взаимодействие химические вещества. Поэтому связывание токсиканта на рецепторе какого-то одного типа является избирательным лишь в определенном диапазоне его концентраций во внутренней среде. Увеличение концентрации токсиканта в биосистеме приводит не только к увеличению числа связанных рецепторов одного типа, но и к расширению спектра типов рецепторов, с которыми он вступает во взаимодействие, а следовательно, к изменению его биологической активности. Это одно из фундаментальных положений токсикологии, доказанное многочисленными наблюдениями.
Принимаются постулаты:
• токсическое действие вещества выражено тем сильнее, чем большее количество активных рецепторов (структур-мишеней) вступило во взаимодействие с токсикантом;
• токсичность вещества тем выше, чем меньшее его количество связывается с «немыми» рецепторами, чем эффективнее оно действует на активные рецепторы (структуры-мишени), чем большее значение имеет рецептор и повреждаемая биологическая система для поддержания гомеостаза целостного организма.
Наиболее часто токсический процесс развивается в результате воздействия химических веществ на белки (повреждение структурных белков, нарушение активности энзимов), нуклеиновые кислоты, липиды биомембран, селективные рецепторы эндогенных биорегуляторов.
В результате такого воздействия клетки либо повреждаются (цитоток-сическое действие), либо нарушаются механизмы регуляции их функций.
5.1.1. Химизм реакции токсикант — рецептор
Взаимодействие токсиканта со структурами-мишенями подчиняется тем же закономерностям, что и любая химическая реакция, протекающая ex vivo, и, следовательно, во многом зависит от свойств вещества. Большинство высокотоксичных соединений — инертные в химическом отношении молекулы. Химически активные соединения при контакте с покровными тканями немедленно вступают с ними во взаимодействие и, вызывая лишь местные повреждения, не проникают во внутренние среды организма.
Сила межмолекулярного взаимодействия между токсикантом, проникшим во внутренние среды организма, и биологической молекулой-мишенью действует, как правило, локально; образующаяся связь способна к диссоциации. Высвободившаяся из связи с токсикантом биомишень часто восстанавливает исходные свойства. В подобных случаях достаточно элиминировать несвязавшуюся часть токсиканта из организма для того, чтобы сдвинуть химическое равновесие в сторону разрушения комплекса «токсикант — мишень» и тем самым устранить действие яда. Например, обратимо взаимодействуют со структурами-мишенями летучие неполярные растворители (гексан, толуол и др.), ингаляция которых сопровождается нарушением сознания, развитием наркотического эффекта.
Некоторые токсиканты образуют с молекулами-мишенями прочные комплексы, разрушить которые возможно только с помощью других средств, образующих с ядом еще более прочную связь. В частности, для восстановления активности ацетилхолинэстеразы, ингибированной фос-форорганическими соединениями (ФОС), применяют вещества из груп-
пы оксимов, вступающие во взаимодействие с токсикантами и вызывающие тем самым дефосфорилирование активного центра энзима.
Иногда в процессе метаболизма ксенобиотика в клетках образуются весьма активные в химическом отношении промежуточные продукты. При действии на биомолекулы они образуют с ними чрезвычайно прочные связи, разрушить которые практически невозможно: биомишень повреждается необратимо. Таким образом, например, иприт взаимодействует с пуриновыми основаниями нуклеиновых кислот.

Механизмы репарации
Взаимодействие с молекулами-мишенями
I
Нарушение клеточного метаболизма
--- *• I
Повреждение клетки
МАНИФЕСТАЦИЯ активации свободнорадикальных процессов
Генерация ' диффундирующих реактивных продуктов взаимодействия молекул и радикалов
♦ мутагенез; канцерогенез
♦ фотосенсибилизация; фотоаплергия
♦ гемолиз эритроцитов
♦ некроз клеток
♦ фиброз пораженных органов
Рис. 16. Активация свободнорадикальных процессов в клетках и их последствия
Характер повреждающего действия активных радикалов во многом определяется их стабильностью и расстоянием, на которое они могут мигрировать от места своего образования. Наиболее реакционноспособ-ные радикалы (винилгалогены, дигидропиридины) разрушают только образующие их энзимы. Метаболиты, обладающие меньшей реакционной способностью, способны выходить даже за пределы органов, в которых они образуются, и повреждать другие органы и ткани (метаболиты гексана вызывают периферическую нейропатию; метаболиты пирроли-зидиновых алкалоидов мигрируют из печени в легкие, где повреждают сосуды и т. д.).
5.2.3* Повреждение мембранных структур
Помимо непосредственного действия на липидный бислой (см. выше) возможны и иные механизмы повреждения токсикантами биомембран. К числу важнейших относятся:
• активация перекисного окисления липидов;
• активация фосфолипаз.
Активация перекисного окисления липидов. Благодаря высокому содержанию ненасыщенных связей в углеводородной цепи жирных кислот, фосфолипиды клеточных мембран наиболее предрасположены к реакции окисления, инициируемой свободными радикалами, образующимися в клетке (см. выше). Этому способствует то обстоятельство, что молекулярный кислород в 7—8 раз лучше растворяется в липидной фазе, чем в воде и гидрофильных сайтах клетки. Атака активных форм кислорода на ненасыщенные связи жирных кислот приводит к образованию пероксидных радикалов («перекисное окисление липидов») и разрушению биологических мембран. Процесс перекисного окисления сопровождается также образованием из липидов высокореакционноспособных и легко диффундирующих карбонильных радикалов, которые могут обусловливать неблагоприятные процессы, развивающиеся в клетках далеко за пределами места своего образования — не только клетки, но и органа. Хорошо кро-воснабжающиеся и насыщенные кислородом ткани (легкие, сердце, головной мозг) являются более чувствительными к повреждающему действию прооксидантов.
Активация фосфолипаз. Важным механизмом повреждения биологических мембран является гидролиз фосфолипидов, наступающий вследствие активации фосфолипаз (особенно фосфолипазы А2). Активация энзима происходит в результате прямого или опосредованного (гипоксия, нарушение гомеостаза внутриклеточного кальция и т. д.) действия многих токсикантов на клетки организма (рис. 17).
В результате действия фосфолипазы А2 на липиды биологических мембран высвобождается арахидоновая кислота. Последняя является, в свою очередь, субстратом энзима циклооксигеназы. Превращение арахи-доновой кислоты под влиянием энзима приводит к образованию эйкоза-ноидов (простагландинов, тромбоксанов, простациклинов) — веществ, активирующих воспалительные процессы в тканях. Под влиянием другого энзима 5-липоксигеназы арахидоновая кислота превращается в лей-котриены и эйкозатетраеноевые кислоты — химиоатрактанты нейтрофи-лов, вещества, регулирующие сосудистую проницаемость.
| экзогенные фосфолипазы (змеиные яды) |
Еще одним продуктом энзиматического расщепления липидов мембран является фактор агрегации тромбоцитов (ФАТ) — клон биологически активных веществ (более 150 аналогов) близкого строения. ФАТ — чрезвычайно токсичные вещества (LD50 для кролика — 0,005 мг/кг; для собаки _ 0,07 мг/кг), вызывающие при внутривенном введении шокоподоб-ное состояние (острый, некупируемый коллапс, бронхоспазм и др.).
| эндогенный кальций | ТОКСИКАНТЫ | |

| ФОСФОЛИПИДЫ (гидролиз) |
 А—У
А—У
| инозитол трифосфат |
| фактор агрегации тромбоцитов |
| фосфатидиловая кислота |
| диацил-глицерол |
| ♦ простагландины ♦ простациклины ♦ тромбоксаны |
| COOH |
| COR, COR,0 I -I СО—Р—О I R3 фактор агрегации тромбоцитов |

|
| НО ОН простагландин |
ПП1ИПИПК1 -—
леикотриены
Рис. 17. Образование биологически активных веществ при участии фосфолипаз, активируемых в ходе токсического процесса
Поскольку система внутриклеточных мембран также является мишенью для действия многочисленных токсикантов, среди них можно выделить группу митохондриальных ядов, повреждающих различные звенья процессов биоэнергетики, — веществ, действующих на шероховатый (нарушение процессов синтеза белка) и гладкий эндоплазматический рети-кулум (индукция или угнетение метаболизма ксенобиотиков), лизосома-льные мембраны (провоцируют аутолиз клеток) и др.
5.2*4. Нарушение гомеостаза внутриклеточного кальция
Нарушение гомеостаза внутриклеточного кальция, сопровождающееся существенным повышением его концентрации в цитоплазме клетки, лежит, как полагают, в основе механизма клеточной гибели при различных патологических состояниях, в том числе при острых отравлениях. Цито-токсическое действие самых разных токсикантов (цианидов, четыреххло-ристого углерода, свинца, органических соединений олова и ртути, алки-лирующих агентов, диоксина и т. д.), как полагают, хотя бы отчасти связано с повышением уровня кальция внутри клеток.
| 2+ |
В норме низкая концентрация кальция в цитоплазме поддерживается энергозависимыми механизмами его активного удаления из клетки и компартментализации в клеточных органеллах (рис. 18).
Са
| АТФ |
| АДФ |
1,3 мМ и
| 2+ |
| 2+ |
| Са2+ 100 нМ |
| Са |
КЛЕТКА
Са
| митохондрии |
Н+ Na+
АТФ
| АТФ |
эндоплазматический ретикулум
| 2+ |
АДФ
Са
ядро
Рис. 18. Схема регуляции ионов кальция в цитоплазме
Нарушение механизмов поддержания гомеостаза внутриклеточного кальция, как это видно из представленной схемы обмена иона, может стать следствием:
• повреждения биологических мембран и усиления их проницаемости для ионов;
• нарушения биоэнергетики клетки, приводящего к истощению запасов макроэрогов;
• изменения функционального состояния белковых комплексов (в том числе путем действия на соответствующие рецепторы), образующих каналы для Са2+.
Все эти механизмы могут приводить к усилению инфлюкса кальция из внеклеточной жидкости и его высвобождению из депо в цитоплазму клетки. Примеры веществ, повреждающих механизмы поддержания гомеостаза кальция внутри клеток, представлены в табл. 11.
Таблица 11
Некоторые вещества, нарушающие внутриклеточный гомеостаз кальция
| 1. Высвобождение кальция из митохондрий: - динитрофенол » динитрокрезол • кадмий | 3. Усиление поступления кальция через плазматическую мембрану: * четыреххлористый углерод ♦ 2,3,7,8-тетрахлордибензо-п-диоксин |
| 2. Высвобождение кальция из эндоплазматического ретикулума: ♦ четыреххлористый углерод ♦ бромбензол ♦ перекиси ♦ альдегиды | 4. Угнетение эффлюкса кальция из клетки: ♦ цистамин ♦ хиноны ♦ паракват t, ♦ ванадий |
Цитотоксический эффект, опосредованный стойким повышением содержания свободного кальция в цитоплазме, в настоящее время связывают с развивающимся при этом повреждением целостности цитоскелета и неконтролируемой активацией катаболических энзимов (фосфолипаз, протеаз, эндонуклеаз).
Повреждение цитоскелета. Цитоплазма клетки помимо цитозоля и клеточных органелл, как правило, содержит еще и нитевидные белковые структуры, которые в массе формируют клеточный скелет. Это образование выполняет не только стабилизирующую и структурирующую, но и другие функции, среди которых обеспечение клеточного деления, внутриклеточный транспорт, секреция, обмен рецепторных белков, регуляция клеточной подвижности и формы.
При действии разнообразных веществ на изолированные клетки (культура ткани) выявляется отчетливое изменение формы их поверхности: появляются выпячивания цитоплазмы (пузырьками — blebs). Такое «пу-зырение» (или вскипание — blebbing) клеточной мембраны — один из ранних признаков разрушения сети цитоскелета, предшествующий разрушению клетки.
Кальций вовлечен в процесс поддержания структуры цитоскелета через ряд Са2+-связывающих протеинов и Са2+-зависимых энзимов, обеспечивающих ассоциацию белков цитоскелета с белками плазматической мембраны. Во-первых, стойкое увеличение концентрации кальция в ци-тозоле разрушает комплекс актина микрофиламентов с а-актинином, белком, связывающим микрофиламенты цитоскелета с белками плазматической мембраны. Во-вторых, Са2+ активирует протеазы (см. ниже), которые могут расщеплять актин-связывающие белки, разрушая тем самым места прикрепления филаментов цитоскелета к клеточной мембране. Отщепление цитоскелета от мембраны приводит к ослаблению фик-
7В
Часть I. ТОКСИКОЛОГИЯ
 |
сации последней и ее «вскипанию», что и наблюдается при действии различных токсикантов на клетки.
Активация фосфолипаз. Эти энзимы широко представлены в различных клетках. Особое значение имеют фосфолипазы А2, основная функция которых состоит в удалении из мембран поврежденных фосфолипи-дов путем отщепления жирных кислот, подвергшихся пероксидации. Фосфолипазы А2 являются Са2+- и кальмодулин-зависимыми энзимами и, следовательно, чувствительными к повышению кальция в цитоплазме. При интоксикациях стимуляция фосфолипаз избыточным кальцием приводит к усилению разрушения фосфолипидов мембран и повреждению клеток.
Активация протеаз. К числу протеаз с оптимумом активности в области нейтральных значений рН относятся АТФ-зависимые и Са2+-зависи-мые (кальпаины) протеазы. Кальпаины присутствуют практически во всех кдетках млекопитающих. Они локализуются вне лизосом, в мембранных структурах в форме неактивного комплекса с ингибиторными протеинами (кальпастатины). Основные функции кальпаинов — репарация цитоскелета и клеточных мембран, разрушение рецепторных протеинов и их обновление, активация некоторых энзимов, участие в процессах митоза. Неуправляемая активация кальпаинов кальцием приводит к повреждению микрофиламентов цитоскелета и гибели клеток.
Активация эндонуклеаз. При завершении клеткой жизненного цикла активируется процесс «программированной» физиологической клеточной гибели — апоптоз. На ранних этапах в апоптотической клетке проявляются морфологические изменения: «вскипание» клеточной и ядерной мембран, уплотнение органелл, конденсация хроматина. Биохимическим коррелятом процесса является активация эндонуклеаз, энзимов, расщепляющих хроматин на фрагменты — олигонуклеосомы. Установлено, что кальций участвует в активации эндонуклеаз, а повышение его содержания в цитоплазме значительно активирует процесс фрагментации ДНК. Активация эндонуклеаз может быть причиной гибели клеток печени, миокарда, почек и других органов при отравлениях многими химическими веществами.
5.2.5. Повреждение процессов синтеза белка и клеточного деления
В основе нарушения процессов синтеза белка, клеточного деления и передачи наследственной информации лежит повреждение токсикантами молекул ДНК, РНК и ферментов, участвующих в их синтезе и репарации (табл. 12).
Кроме представленных в табл. 12 существуют и другие способы токсического повреждения процессов. Так, в фазе приготовления к митозу возможно повреждение центриолей и угнетение синтеза митотического аппарата, образующего клеточное веретено. Веретено формируется SH-содержащими протеинами (тубулином), которые благодаря -S-S-связям
ВО
образуют нитевидные структуры. Естественно, токсиканты, взаимодействующие с SH-группами, способны повреждать митотическое веретено и тем самым нарушать клеточное деление. Примерами таких токсикантов являются мышьяк, ртуть и их соединения, колхицин, подофилоток-син и др.
Таблица 12
Возможные точки приложения повреждающего действия токсикантов на процессы синтеза белка и клеточного деления
1. Синтез ДНК. Репликация
♦ изменение структуры (конформации) ДНК
♦ нарушение процесса полимеризации ДНК
♦ нарушение синтезе нуклеотидов
♦ нарушение процесса репарации ДНК
. нарушение механизмов регуляции синтеза ДНК
2. Синтез РНК. Транскрипция " .
♦ резрушение РНК
♦ нарушение полимеризации РНК » нарушение процессии РНК
♦ нарушение синтеза нуклеотидов
» нарушение механизмов регуляции синтеза РНК
3. Синтез белка. Трансляция
. нарушение организации и процессии рибосом и полисом
♦ нарушение полимеризации аминокислот
♦ нарушение образования аминоацетил-tPHK
♦ нарушение формирования конформации белка и его третичной и четвертичной структур
♦ нарушение механизмов регуляции трансляции
4. Синтеза клеточных компонентов для митоза (фаза G2). В частности, синтезируются мономеры и полимер тубулина и т. д. Процесс занимает около 19% времени цикла делящейся клетки.
5. Митоза (фаза М): разделение генетического материала между вновь образующимися дочерними клетками; клеточное деление. Процесс занимает 2% времени.
Некоторые химические вещества способны вызывать мутации лишь тех клеток, которые находятся в определенной фазе цикла, это так называемые цикло-специфичные вещества. Другие действуют на генетический аппарат не зависимо от того, в каком периоде клеточного цикла находится клетка (цикло-неспецифичные). Такая особенность определяется механизмом токсического действии веществ (см. выше). К числу цикло-неспецифичных принадлежат мутагены, способные вызывать химическое повреждение ДНК (алкилирующие агенты и химические модификаторы нуклеотидов). Все остальные мутагены являются цикло-специфичными.
Основными видами мутаций, вызываемых химическими веществами, являются:
1) точечная мутация, связанная с модификацией одного нуклеоти-да в структуре ДНК (замещение нуклеотида, выпадение нуклео-тида из цепи, включение дополнительного нуклеотида в цепь);
2) хромосомные аберрации, т. е. изменение структуры хромосом (разрывы молекул ДНК, транслокации фрагментов ДНК) или числа хромосом в клетке.
Далеко не всякая модификация молекулы ДНК (мутация) является опасной для организма.
Клетки обладают способностью корректировать и устранять повреждения ДНК. Вследствие этого лишь небольшое число мутаций, инициированных токсикантом, сохраняется в процессе репликации молекулы. Однако если мутация не распознана, извращенная информация транскрибируется в РНК, а затем экспрессируется в форме неполноценного протеина. Последствия этого для клетки могут быть либо несущественны, либо критичны, в зависимости от функций, выполняемых протеином.
Неблагоприятные эффекты мутагенеза определяются также и тем, в клетках какого типа он реализуется: половых или соматических, стволовых и делящихся или созревающих и зрелых. Результатом грубых мутаций половых клеток и делящихся клеток развивающегося плода являются: стерильность особи, врожденная патология у потомства, тератогенез, гибель плода. Мутации стволовых и делящихся соматических клеток сопровождаются структурно-функциональными нарушениями тканей с непрерывной физиологической регенерацией (система крови, иммунная система, эпителиальные ткани) и канцерогенезом. Повреждение токсикантом ДНК зрелой соматической клетки не приводит к пагубным последствиям для организма.
S2
Последствия повреждения ДНК зависят от дозы токсиканта. Высокие дозы вызывают цитостатический эффект (гибель пула делящихся клеток), дистрофические изменения в клетке, более низкие — канцерогенное, тератогенное действие.
Существует представление, согласно которому проникновение в организм даже единственной молекулы генотоксиканта (в отличие от токсикантов с иным механизмом токсического действия) может привести к пагубным последствиям. Дело в том, что химическое повреждение единичной молекулы ДНК в единичной клетке макроорганизма, при стечении обстоятельств, может стать причиной образования целого клона клеток с измененным геномом. Вероятность такого события бесконечно мала, но теоретически возможна. Такой характер действия веществ на биосистемы называется беспороговым.
5.3. Развитие токсического процесса
Повреждение биологических систем в наиболее общей форме реализуется нарушением основных функций живого:
• раздражимости;
• энергетического обмена;
• пластического обмена;
• системы физиологической регенерации и размножения;
• информационного обмена;
• интегративной регуляции.
Нарушение энергетического обмена, как правило, приводит к быстрому формированию нарушений наиболее энергоемких органов (ЦНС, сердечная мышца, почки). Нарушение пластического обмена сопровождается медленным развитием длительно текущих патологических процессов в наиболее чувствительных органах и системах. Нарушение системы физиологической регенерации тканей проявляется поражением прежде всего системы крови, эпителия слизистой оболочки ЖКТ, органов дыхания, кожи и ее придатков. Нарушение информационного обмена приводит к нарушению механизмов нервной и гуморальной регуляции процессов, происходящих в организме. Вещества, нарушающие неявную регуляцию, как правило, вызывают быстро развивающиеся эффекты.
Клиническая картина интоксикации зависит прежде всего от того, какие органы и ткани будут вовлечены в патологический процесс.
Проявления токсического процесса, инициируемого токсикантами различных групп, рассматриваются ниже.
Глава 6. АНТИДОТЫ. ОБЩИЕ ПРИНЦИПЫ ОКАЗАНИЯ НЕОТЛОЖНОЙ ПОМОЩИ ОТРАВЛЕННЫМ
Специфичность препаратов в отношении действующих токсикантов убывает в ряду: этиотропное — патогенетическое — симптоматическое средство. В такой же последовательности убывает эффективность применяемых средств. Этиотропные препараты, введенные в срок и в нужной дозе, порой практически полностью устраняют проявления интоксикации. Симптоматические средства устраняют лишь отдельные проявления отравления, облегчают его течение (табл. 14).
 | |||
 | |||
В токсикологии, как и в других областях практической медицины, для оказания помощи используют этиотропные, патогенетические и симптоматические средства (табл. 13). Поводом для введения этиотропных препаратов является знание непосредственной причины отравления, особенностей токсикокинетики яда. Симптоматические и патогенетические вещества назначают ориентируясь на проявления интоксикации.
В токсикологии термину «этиотропное средство терапии» тождествен термин «антидот» (противоядие).
Антидотом (от Antidotum — даваемое против) называется лекарство, применяемое при лечении отравлений и способствующее обезвреживанию яда или предупреждению и устранению вызываемого им токсического эффекта (В. М. Карасик, 1961).
Обычно выделяют следующие механизмы антагонистических отношений между антидотом и токсикантом, лежащие в основе предупреждения или устранения токсического эффекта: е химический;
• биохимический;
• физиологический;
• основанный на модификации процессов метаболизма ксенобиотика.
6.1. Характеристика современных антидотов
В настоящее время антидоты разработаны лишь для ограниченной группы токсикантов. В соответствии с видом антагонизма к токсиканту они могут быть классифицированы на несколько групп (табл. 15).
Таблица 15
Противоядия, используемые в клинической практике
| Вид антагонизма | Противоядия | Токсикант |
| 1. Химический | ЭДТА, унитиол и др. Со-ЭДТА и др. Азотистокислый Na Амилнитрит Диэтиламинофенол Антитела и Fab-фрагменты | Тяжелые металлы Цианиды, сульфиды Гликозиды, ФОС, паракаат, токсины |
| 2. Биохимический | Кислород Реактиваторы ХЭ Обратим, ингибит. ХЭ Пиридоксин Метиленовый синий | СО ФОС ФОС Гидразин Метгемоглобинообразователи |
| 3. Физиологический | Атропин и др. Аминостигмин и др. Сибазон и др. Флюмазенил Налоксон | ФОС, карбаматы Холинолитики, ТАД, нейролептики ГАМК-литики Бензодиазепины Опиаты |
| 4. Модификация метаболизма | Тиосульфат Na Ацетилцистеин Этанол, 4-метилпиразол | Цианиды < ' Ацетаминофен Метанол, этиленгликоль |
Антидоты с химическим антагонизмом непосредственно связываются с токсикантами. При этом осуществляется:
• химическая нейтрализация свободно циркулирующего токсиканта;
• образование малотоксичного комплекса;
• высвобождение структуры-рецептора из связи с токсикантом;
• ускоренное выведение токсиканта из организма за счет его «вымывания» из депо.
К числу таких антидотов относятся глюконат кальция, используемый при отравлениях фторидами, хелатирующие агенты, применяемые при интоксикациях тяжелыми металлами, а также Со-ЭДТА и гидроксикоба-ламин — антидоты цианидов. К числу средств рассматриваемой группы относятся также моноклональные антитела, связывающие сердечные гликозиды (дигоксин), ФОС (зоман), токсины (ботулотоксин).
Хелатирующие агенты — комплексообразователи. К этим средствам относится большая группа веществ, мобилизующих и ускоряющих элиминацию из организма металлов путем образования с ними водорастворимых малотоксичных комплексов, легко выделяющихся через почки.
По химическому строению комплексообразователи классифицируются на следующие группы:
1. Производные полиаминполикарбоновых кислот (ЭДТА, пента-цин и т. д.).
2. Дитиолы (БАЛ, унитиол, 2,3-димеркаптосукцинат).
3. Монотиолы (d-пенициламин, N-ацетилпенициламин).
4. Разные (десфериоксамин, прусская синь и т. д.).
Антитела к токсикантам. Для большинства токсикантов эффективные и хорошо переносимые антидоты не найдены. В этой связи возникла идея создания универсального подхода к проблеме разработки антидотов, связывающих ксенобиотики, на основе получения антител к токсикантам. Теоретически такой подход может быть использован при интоксикациях любым токсикантом, на основе которого может быть синтезирован комплексный антиген. Однако на практике существуют значительные ограничения возможности использования антител (в том числе моноклональных) в целях лечения и профилактики интоксикаций. Это обусловлено:
• сложностью (порой непреодолимой) получения высокоаффинных иммунных сывороток с высоким титром антител к токсиканту;
• технической трудностью изоляции высокоочищенных IgG или их Fab-фрагментов (часть белковой молекулы иммуноглобулина, непосредственно участвующая во взаимодействии с антигеном);
• «моль на моль» — взаимодействием токсиканта и антитела (при умеренной токсичности ксенобиотика, в случае тяжелой интоксикации, потребуется большое количество антител для его нейтрализации); ,
• не всегда выгодным влиянием антител на токсикокинетику ксенобиотика;
• ограниченностью способов введения антител;
• иммуногенностью антител и способностью вызывать острые аллергические реакции.
В настоящее время в эксперименте показана возможность создания антидотов на рассматриваемом принципе в отношении некоторых фос-форорганических соединений (зоман, малатион, фосфакол), гликозидов (дигоксин), дипиридилов (паракват) и др. Однако в клинической практике препараты, разработанные на этом принципе, применяются в основ-
Глава 6. АНТИДОТЫ. ОБЩИЕ ПРИНЦИ11Ы ОКАЗАНИИ НЬШлижпии I ШМЦЩИ и I ГАШ ItnnWM
ном при отравлении токсинами белковой природы (бактериальные токсины, змеиные яды и т. д.).
Биохимические антагонисты вытесняют токсикант из его связи с биомолекулами-мишенями и восстанавливают нормальное течение биохимических процессов в организме.
Данный вид антагонизма лежит в основе антидотной активности кислорода при отравлении оксидом углерода, реактиваторов холинэстеразы и обратимых ингибиторов холинэстеразы при отравлениях ФОС, пири-доксальфосфата при отравлениях гидразином и его производными (см. соответствующие разделы).
Физиологические антидоты, как правило, нормализуют проведение нервных импульсов в синапсах, подвергшихся атаке токсикантов.
Механизм действия многих токсикантов связан со способностью нарушать проведение нервных импульсов в центральных и периферических синапсах. Это проявляется либо перевозбуждением, либо блокадой постсинаптических рецепторов, стойкой гиперполяризацией или деполяризацией постсинаптических мембран, усилением или подавлением восприятия иннервируемыми структурами регулирующего сигнала. Вещества, оказывающие на синапсы, функция которых нарушается токсикантом, противоположное токсиканту действие, можно отнести, к числу антидотов с физиологическим антагонизмом. Эти препараты не вступают с ядом в химическое взаимодействие и не вытесняют его из связи с ферментами. В основе антидотного эффекта лежит непосредственное действие на постсинаптические рецепторы или изменение скорости оборота нейромедиатора в синапсе.
Специфичность физиологических антидотов ниже, чем у веществ с химическим и биохимическим антагонизмом. При этом установлено, выраженность наблюдаемого антагонизма конкретной пары токсиканта и «противоядия» колеблется в широких пределах — от очень значительной до минимальной. Антагонизм никогда не бывает полным. Это обусловлено:
• гетерогенностью синаптических рецепторов, на которые воздействуют токсикант и противоядие;
• неодинаковыми сродством и внутренней активностью веществ в отношении различных субпопуляций рецепторов;
• различиями в доступности синапсов (центральных и периферических) для токсикантов и противоядий;
• особенностями токсико- и фармакокинетики веществ.
Чем в большей степени в пространстве и времени совпадает действие токсиканта и антидота на биосистемы, тем выраженнее антагонизм между ними.
В качестве физиологических антидотов в настоящее время используют:
• атропин и другие холинолитики — при отравлениях фосфорорга-ническими соединениями (хлорофос, дихлофос, фосфакол, зарин, зоман и др.) и карбаматами (прозерин, байгон, диоксакарб и др.);
• галантамин, пиридостигмин, аминостигмин (обратимые ингибиторы ХЭ) — при отравлениях атропином, скополамином, BZ, дитраном и другими веществами с холинолитической активностью (в том числе трициклическими антидепрессантами и некоторыми нейролептиками);
• бензодиазепины, барбитураты — при интоксикациях ГАМК-ли-тиками (бикукуллин, норборнан, бициклофосфаты, пикротокси-нин и др.);
• флюмазенил (антагонист ГАМК-бензодиазепиновых рецепторов) при интоксикациях бензодиазепинами (диазепам и др.);
• налоксон (конкурентный антагонист опиоидных ц-рецепторов) — антидот наркотических анальгетиков (морфин, фентанил, клони-тазен и др.).
Модификаторы метаболизма препятствуют превращению ксенобиотика в высокотоксичные метаболиты либо ускоряют биодетоксикацию вещества.
Используемые в практике оказания помощи отравленным препараты могут быть отнесены к одной из следующих групп: А. Ускоряющие детоксикацию:
• натрия тиосульфат — применяется при отравлениях цианидами;
• бензонал и другие индукторы микросомальных ферментов — могут быть рекомендованы в качестве средств профилактики поражения фосфорорганическими отравляющими веществами;
• ацетилцистеин и другие предшественники глутатиона — используются в качестве лечебных антидотов при отравлениях дихлорэтаном, некоторыми другими хлорированными углеводородами, ацетаминофеном.
Б. Ингибиторы метаболизма:
• этиловый спирт, 4-метилпиразол — антидоты метанола, этилен-гликоля.
6.2. Применение противоядий
Поскольку любой антидот это так же химическое вещество, как и токсикант, против которого его применяют, как правило, не обладающее полным антагонизмом с ядом, несвоевременное введение, неверная доза противоядия и некорректная схема могут самым пагубным образом сказаться на состоянии пострадавшего. Попытки корригировать рекомендуемые способы применения антидотов, ориентируясь на состояние пострадавшего у его постели, допустимы только для высококвалифицированного специалиста, имеющего большой опыт использования конкретного противоядия. Наиболее частая ошибка, связанная с применением антидотов, обусловлена попыткой усилить их эффективность повышением вводимой дозы. Такой подход возможен лишь при применении некоторых физиологических антагонистов, но и здесь имеются жесткие ограничения, лимити
руемые переносимостью препарата. В реальных условиях, как и для многих других этиотропных препаратов, схема применения антидотов предварительно отрабатывается в эксперименте и лишь затем рекомендуется практическому здравоохранению. Отработка правильной схемы применения препарата является важнейшим элементом разработки и выбора эффективного противоядия. Поскольку некоторые виды интоксикации встречаются нечасто, порой проходит продолжительное время перед тем, как в условиях клиники удается окончательно сформировать оптимальную стратегию использования средства.
Лекарственные формы и схемы применения основных противоядий представлены в табл. 16.
Таблица 16
| Антидоты |
Лекарственные формы и схемы применения некоторых противоядий
Лекарственная форма. Способ применения
| Амилнитрит |
Ампулы по 0,5 мл в ватно-марлевой обертке. Раздавить ампулу, заложить ее под шлем-маску противогаза и сделать 1-2 глубоких вдоха. При необходимости может быть применен повторно. Отравление цианидами
| Аминостигмин |
Ампулы ло 1 мл 0,1% раствора. Содержимое одной ампулы ввести подкожно, внутримышечно или внутривенно. Назначать повторно при рецидивах проявлений отравлений М-холинолитиками
| Антициан |
Ампулы по 1 мл 20% раствора, внутримышечно, повторное введение в дозе 1 мл возможно не ранее чем через 30 мин. Для внутривенного введения содержимое одной ампулы разводят в 10 мл 25-40% раствора глюкозы или 0,85% раствора NaCI и вводят со скоростью 3 мл/мин. Отравление цианидами
| Атропина сульфат |
Ампулы по 1,0 мл 0,1% раствора; внутривенно, внутримышечно. При интоксикациях ФОС первоначальная доза 2-8 мг, затем по 2 мг через каждые 15 мин до явлений переатропинизации. Отравление ФОС, карбаматами
| Дефероксамин (десферал) |
| Дигоксин- специфичные Fab-антитела Дипироксим |
Ампулы, содержащие 0,5 г сухого препарата. Вводят обычно внутримышечно в виде 10% раствора, для чего содержимое 1 ампулы (0,5 г) растворяют в 5 мл стерильной воды для инъекций. Внутривенно вводят только капельно из расчета не более 15 мг/кг в час при тяжелом отравлении железом. Для связывания железа, еще не всосавшегося из желудочно-кишечного тракта, дают внутрь 5-10 г препарата, растворенного в питьевой воде
Порошок во флаконах. Содержимое одного флакона связывает 0,6 мг дигоксина
| Дикобальтовая соль ЭДТА Димеркапрол (БАЛ) |
Ампулы по 1,0 мл 15% раствора, внутримышечно, внутривенно. Можно повторять введение каждые 3-4 ч либо обеспечить постоянную внутривенную инфузию 250-400 мг/ч. Отравление ФОС
Ампулы по 20 мл 1,5% раствора внутривенно, капельно медленно. Отравление цианидами
Ампулы по 3 мл 10% раствора. Вводить 3-5 мг/кг каждые 4 ч внутримышечно в течение 2 дней, затем 2-3 мг/кг каждые 6 ч в течение 7 дней. Отравления мышьяком, свинцом, ртутью
| Антидоты |
Окончание таблицы 16
Лекарственная форма. Способ применения
| Метиленовый синий |
Ампулы по 20 мл или флаконы по 50-100 мл 1% раствора в 25% растворе глюкозы («хромосмон»). Содержимое одной ампулы вводить внутривенно медленно. Отравление цианидами, метгемоглобинообразователями (анилин, нитриты, нитробензол и др.)
| Налоксон |
Ампулы по 1,0 мл 0,1% раствора. Начальная доза 1-2 мг внутривенно, внутримышечно, подкожно. Назначать повторно при рецидивах проявлений отравлений наркотическими анальгетиками
| Натрия нитрит |
| Натрия тиосульфат Пенициламин |
Ампулы по 10-20 мл 2% раствора, внутривенно, капельно. Отравление цианидами
Ампулы по 10-20 мл 30% раствора, внутривенно. Отравления цианидами, соединениями ртути, мышьяка, метгемоглобинообразователями
| Пиридоксин гидрохлорид Пралидоксим (2-ПАМ) Тетацин-кальций (CaNa2 ЭДТА) |
Капсулы по 125-250 мг, таблетки по 250 мг. Принимать внутрь перед едой по 250 мг 4 раза в сутки в течение 10 дней. Интоксикации свинцом, мышьяком
Ампулы по 3-5 мл 5% раствора, внутримышечно, внутривенно при интоксикациях гидразином
Ампулы по 50 мл 1% раствора, вводить внутривенно капельно из расчета 250-400 мг/ч. Отравление ФОС
Ампулы по 20 мл 10% раствора. Содержимое одной ампулы вводят внутривенно капельно в 5% растворе глюкозы или в изотоническом растворе NaCI. Повторное введение возможно не ранее чем через 3 ч. Вводят ежедневно в течение 3-4 дней с последующим перерывом 3-4 дня. Курс лечения — 1 месяц. Отравления ртутью, мышьяком, свинцом
| Унитиол |
Ампулы по 5 мл 5% раствора, внутримышечно по 1 мл на 10 кг массы тела каждые 4 ч первые 2 дня, каждые 6 ч последующие 7 дней. Отравления мышьяком, ртутью, люизитом
| Физостигмин |
Ампулы по 1 мл 0,1% раствора. Содержимое одной ампулы ввести подкожно, внутримышечно или внутривенно. Назначать повторно при рецидивах проявлений отравлений М-холинолитическими препаратами
| Флюмазенил |
Ампулы по 0,5 мг в 5 мл. Начальная доза 0,2 мг внутривенно. Дозу повторяют до восстановления сознания (максимальная суммарная доза — 3 мг). Отравления бензодиазепинами.
Не вводить пациентам с судорожным синдромом и при передозировке трициклических антидепрессантов!
| Этанол |
Начальная доза рассчитывается на достижение уровня этанола в крови не менее 100 мг/100 мл (42 г/70 кг) — в виде 30% раствора внутрь по 50-100 мл. Отравления метанолом, этиленгликолем
6.3. Разработка новых антидотов
Поводом для создания эффективного противоядия является либо случайное обнаружение факта антагонизма веществ, либо целенаправленное и глубокое изучение механизмов действия токсиканта, особенностей его токсикокинетики и установление на этой основе возможности химиче-
ской модификации токсичности. При этом к новым антидотам предъявляются следующие требования:
• высокая эффективность,
• удобство применения,
• возможность длительного хранения,
• дешевизна.
В некоторых случаях к разрабатываемым антидотам предъявляются особо жесткие требования. Так, антидоты боевых отравляющих веществ должны обладать не только высокой эффективностью, но и прекрасной переносимостью, поскольку препараты выдаются на руки бойцам и четкий контроль за правильностью их использования организовать весьма затруднительно. Один из путей решения поставленной задачи — создание антидотных рецептур. В состав таких рецептур включают препараты — антагонисты действия токсиканта на разные подтипы структур-мишеней, вещества с различными механизмами антагонизма, а иногда и средства коррекции неблагоприятных эффектов действия антагонистов. За счет этого удается значительно снизить дозы препаратов, входящих в рецептуру, повысить терапевтическую широту (переносимость) антидота. По такому принципу разрабатываются антидоты ФОВ.
При разработке рецептур сталкиваются с дополнительными трудностями. Входящие в рецептуру препараты должны быть химически совместимыми и иметь близкие токсикокинетические характеристики (период полуэлиминации и т. д.).
6.4. Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях
Общими мероприятиями неотложной помощи при острых отравлениях являются:
1. Прекращение поступления токсиканта в организм.
2. Удаление невсосавшегося токсиканта из желудочно-кишечного тракта.
3. Применение антидотов.
4. Восстановление и поддержание нарушенных жизненно важных функций.
5. Устранение отдельных синдромов интоксикации.
Прекращение поступления токсиканта в организм
Мероприятия проводят непосредственно в очаге поражения ОВТВ и продолжают за его пределами:
а) при действии ОВТВ в форме газа, пара или аэрозоля и угрозе инга-
ляционного поражения — надевание противогаза (фильтрующего
или изолирующего типа) и немедленная эвакуация из зоны хими-
ческого заражения;
б) при угрозе поражения ОВТВ с выраженным кожно-резорбтивным
действием — надевание средств защиты кожных покровов и эвакуа-
ция из зоны поражения; при попадании ОВТВ на кожу — обработка
открытых участков водой, жидкостью индивидуального противохи-
мического пакета (ИПП) или другими специальными растворами в
течение 5—10 мин с последующей полной санитарной обработкой;
в) при попадании ОВТВ в глаза — немедленное промывание глаз во-
дой или специальными растворами в течение 5—10 мин.
Удаление невсосавшегося токсиканта из желудочно-кишечного тракта
К числу мероприятий, проводимых на догоспитальных этапах оказания помощи, относятся:
а) вызывание рвоты путем надавливания на корень языка после при-
ема 3—5 стаканов воды. Процедура повторяется 2—3 раза (прово-
дится только у пострадавших с сохраненным сознанием; противо-
показана при отравлении веществами прижигающего действия —
концентрированными кислотами, щелочами);
б) зондовое промывание желудка — проводится 10—15 л воды комнат-
ной температуры (18-20° С) порциями по 300-500 мл с помощью
толстого зонда с грушей в верхней его части, присоединенной через
тройник (для продувания зонда при его засорении пищевыми мас-
сами). После введения зонда в желудок необходимо провести ак-
тивную аспирацию желудочного содержимого. После окончания
процедуры через зонд целесообразно ввести один из энтеросорбен-
тов (активированный уголь, карболен, энтеродез, полифепан, аэро-
сил и др.) или 150—200 г вазелинового масла;
в) сифонная клизма.
Применение антидотов
Антидоты назначают в соответствии с рекомендуемыми схемами после идентификации причины интоксикации.
Восстановление и поддержание нарушенных жизненно важных функций
Мероприятия проводятся после выноса пораженного за пределы зоны химического заражения.
а) При нарушениях дыхания:
• восстановление проходимости дыхательных путей — устранение западения языка; скопления слизи в дыхательных путях;
• при угнетении дыхательного центра — введение аналептиков (кордиамина, кофеина, этимизола, бемегрида);
* при нарастающей гипоксии — оксигенотерапия (см. гл. 9. «Отравляющие и высокотоксичные вещества пульмонотоксического действия»);
• профилактика токсического отека легких (см. гл. 9. «Отравляющие и высокотоксичные вещества пульмонотоксического действия»).
б) При острой сосудистой недостаточности:
внутривенно натрия гидрокарбонат — 250—300 мл 5% раствора.
Устранение отдельных синдромов интоксикации
Мероприятия проводятся после выноса пораженного за пределы зоны химического заражения.
а) Судорожный синдром — внутримышечное или внутривенное вве-
дение диазепама (седуксена) — 3-4 мл 0,5% раствора; внутривенно мед-
ленно натрия тиопентал или гексенал — до 20 мл 2,5% раствора; введение
(внутримышечно или внутривенно) литической смеси: 10 мл 25% раство-
ра магния сульфата, 2 мл 1% раствора димедрола, 1 мл 2,5% раствора ами-
назина.
б) Интоксикационный психоз — внутримышечно аминазин — 2 мл
2,5% раствора и магния сульфат — 10 мл 25% раствора; внутримышечно
тизерцин (левомепромазин) — 2-3 мл 2,5% раствора; внутривенно фен-
танил — 2 мл 0,005% раствора, дроперидол — 1-2 мл 0,25% раствора;
внутрь натрия оксибутират — 3,0—5,0 мл.
в) Гипертермический синдром — внутримышечно анальгин — 2 мл
50% раствора; внутримышечно реопирин — 5 мл; внутривенно или внут-
римышечно литическая смесь.
< А г I >
* N ii ■
mm ц*4* • * (•
Раздел II. ВОЕННАЯ ТОКСИКОЛОГИЯ
Глава 7. ОСНОВНЫЕ ПОНЯТИЯ ВОЕННОЙ ТОКСИКОЛОГИИ
7.1. Предмет, цели, задачи военной токсикологии
Предметом изучения военной токсикологии является токсичность веществ, способных при экстремальных ситуациях вызвать групповое или массовое поражение людей, а также токсические процессы, формирование которых у личного состава приводит к снижению боеспособности воинских коллективов.
К числу основных критериев, позволяющих выделить токсиканты, способные при экстремальных ситуациях вызвать массовые поражения людей, относятся:
• возможность их применения с военными целями;
• высокая токсичность при действии через органы дыхания, неповрежденную кожу и слизистую оболочку желудочно-кишечного тракта;
» физико-химические свойства, способствующие формированию зон химического заражения;
• большие запасы веществ на производственных объектах и базах хранения.
Вещества, удовлетворяющие этим критериям, могут быть обозначены как отравляющие и высокотоксичные вещества (ОВТВ). К числу ОВТВ прежде всего относятся:
» отравляющие вещества (ОВ) и токсины;
• сильнодействующие ядовитые вещества (СДЯВ), или, по другой терминологии, токсичные химические вещества (ТХВ), или аварийно-опасные химические вещества (АОХВ), — потенциальные агенты формирования очагов массовых санитарных потерь при техногенных авариях и катастрофах на промышленных объектах;
• пестициды и фитотоксиканты боевого применения; » диверсионные яды;
• высокотоксичные вещества (ВТВ), действующие при применении современных образцов вооружений (угарный газ, пороховые газы и т. д.).
Как и любые химические вещества, ОВТВ, действуя в различных дозо-временных условиях, способны вызывать самые разнообразные формы токсического процесса. Однако военных токсикологов интересуют прежде всего процессы, развивающиеся в результате острого воздействия токсикантов, приводящие к снижению боеспособности воинского коллектива, — это транзиторные токсические реакции и острые интоксикации.
Цель военной токсикологии — совершенствование системы медицинских мероприятий, средств и методов, обеспечивающих предупреждение или ослабление действия ОВТВ при чрезвычайных ситуациях, а также сохранение жизни, восстановление здоровья и профессиональной работоспособности пораженного личного состава.
Эта цель достигается путем решения следующих задач:
• изучение токсичности веществ, способных вызвать групповое или массовое поражение личного состава при экстремальных ситуациях, механизмов, патогенеза, проявлений токсического процесса, формирующегося при действии ОВТВ;
• совершенствование методов диагностики химического поражения и оценки функционального состояния лиц, подвергшихся воздействию сверхнормативных доз токсикантов;
• создание медикаментозных и иных средств профилактики и оказания помощи пораженным ОВТВ, схем их оптимального использования, а также средств и методов предупреждения и минимизации пагубных отдаленных последствий химического воздействия;
• разработка нормативных и правовых актов, направленных на обеспечение химической безопасности личного состава.
7.2. Отравляющие и высокотоксичные вещества (ОВТВ)
Боевые отравляющие вещества (БОВ)
Бурное развитие химической промышленности во второй половине XIX в. явилось материальной основой для реализации идеи применения химических веществ в качестве оружия. 22 апреля 1915 г. с применения газообразного хлора войсками Германии началась эпоха использования современных средств массового уничтожения. В ходе Первой мировой войны было применено около 130 тыс. тонн высокотоксичных соединений примерно 40 наименований.
В годы Второй мировой войны химическое оружие применяли в крайне ограниченных масштабах. Тем не менее работы по созданию новых образцов ОВ не прекращались. В фашистской Германии, а позже и других странах, были созданы чрезвычайно токсичные фосфорорганические отравляющие вещества (ФОБ). В качестве БОВ в различное время испы-тывались такие вещества, как хлор, фосген, дифосген, хлорпикрин, мышьяковистый водород, синильная кислота, хлорциан, органические производные свинца и мышьяка, карбонилы металлов, галогенированные кетоны, 2,2-дихлордиэтилсульфид (сернистый иприт), 2,2,2-трихлортри-этиламин (азотистый иприт), различные фосфорорганические соединения (ФОС), и многие другие.
Цель применения боевых отравляющих веществ (БОВ) заключается в уничтожении противника или выведении его из строя в результате нарушения дееспособности и причинения ущерба здоровью. БОВ обладают самыми разнообразными физическими, химическими и токсическими свойствами. Далеко не каждое высокотоксичное соединение может рассматриваться как потенциальное ОВ. К числу основных требований, предъявляемых к боевым ОВ, относятся:
• способность действовать на разные органы и системы организма;
• быстрота или, напротив, «коварство» действия (наличие продолжительного скрытого периода);
• отсутствие органолептических характеристик;
• большая продолжительность заражающего действия;
• трудность распознавания причины поражения с помощью различных методов анализа;
• удобство боевого применения;
• устойчивость при хранении;
• дешевизна производства и т. д.
ОВ классифицируются по разным принципам. Значение имеют физические, химические, токсикологические свойства, тактические и методологические соображения.
Для военной медицины особый интерес представляет классификация в соответствии с основным действием на организм и последствиями, к которым это действие приводит. Так, различают ОВ:
1. Смертельного действия:
• нервно-паралитические (зарин, VX);
• кожно-нарывные (иприт, люизит);
• удушающие (фосген, дифосген);
• общеядовитые (синильная кислота, хлорциан).
2. Несмертельного действия:
• психохимические (BZ);
• раздражающие (CN, DM, CS, CR).
По скорости развития поражающего действия в группе ОВ различают:
• быстродействующие (поражение характеризуется минимальным скрытым периодом — минуты): зарин, синильная кислота, CN, DM, CS, CR;
• медленнодействующие (поражение характеризуется длительным скрытым периодом — часы): VX, иприт, люизит, фосген.
В зависимости от продолжительности заражения территории и войск после воздействия, отравляющие вещества подразделяются на:
» нестойкие — поражающие концентрации в зоне химического заражения сохраняются несколько десятков минут после их боевого применения;
• стойкие — поражающие концентрации в зоне химического заражения сохраняются в течение нескольких часов и суток.
В странах, производивших ОВ, кроме того, было принято выделять следующие группы (3. Франке, 1973):
♦ Табельные ОВ — вещества, производимые в больших количествах, состоящие на вооружении армий, боевое применение которых определяется соответствующими уставами. В США, например, к числу табельных относили V-газы, зарин, ботулотоксин, иприт, адамсит, хлорацетофенон, BZ и другие, включая их всевозможные смеси.
♦ Резервные ОВ — хорошо изученные вещества, которые на данный момент не производятся непосредственно в качестве ОВ, но при необходимости могут быть быстро изготовлены промышленностью в достаточных количествах (синильная кислота, галогенцианы, мышьякорганиче-ские и свинецорганические соединения, фосген и др.).
♦ ОВ ограниченного значения — токсичные вещества, свойства которых в целом удовлетворяют требованиям, предъявляемым к ОВ, но которые либо использовались и используются для других целей (фосфорорганические инсектициды, мышьяковистый водород и др.), либо производятся в малом количестве, в связи с отсутствием достаточных производственных возможностей.
В 1993 г. была принята Парижская «Конвенция о запрещении применения, разработки и накопления химического оружия». В настоящее время конвенцию подписали более 150 государств. В соответствии с принятыми документами в ближайшие годы предполагается уничтожить запасы химического оружия на планете.
Пестициды
Пестициды — вещества, предназначенные для борьбы с вредителями с целью повышения урожайности и сохранения материальных ценностей, созданных человеком (фитотоксиканты — вещества, предназначенные для поражения различных видов растительности). Наиболее желательным свойством пестицидов является избирательность их действия в отношении организмов-мишеней (высокая токсичность для вредителя и
за___________
низкая — для человека). Однако селективность действия подавляющего большинства пестицидов не является абсолютной, поэтому многие вещества представляют опасность для человека. Групповое и массовое поражение людей возможно при авариях и катастрофах на объектах производства и хранения веществ, при их транспортировке, а также при использовании в военных целях.

Различные классы пестицидов представлены в табл. 17.
К числу наиболее вероятных ОВТВ из числа пестицидов относятся некоторые инсектициды, родентициды и отдельные гербициды из группы фитотоксикантов.
Фосфорорганические инсектициды (ФОН) представляют собой по большей части эфиры фосфорной и тиофосфорной кислот. В настоящее время это наиболее широко используемые пестициды. Они токсичнее хлор-органических инсектицидов, но менее стойки в окружающей среде и потому менее опасны с точки зрения экологии. Среди наиболее известных ФОИ: паратион, диазинон, хлорофос, карбофос, дисульфотион, малати-он. Все ФОС — нейротоксиканты, нарушающие проведение нервных импульсов в центральных и периферических холинергических синапсах и вызывающие отсроченную периферическую нейропатию.
Близким ФОС по механизму токсического действия на организм насекомых и млекопитающих является класс инсектицидов из группы кар-баматов (производные карбаминовой кислоты). К наиболее известным пестицидам этой группы относятся: карбарил (севин), пропоксур (бай-гон), альдикарб (темик). Среди карбаматов найдены и вещества, обладающие чрезвычайной токсичностью для лабораторных животных.
Чрезвычайно опасны для человека средства борьбы с грызунами — родентициды. Производные фторуксусной кислоты, соли таллия, используемые для этой цели, — высокотоксичные соединения.
Гербициды — это вещества, предназначенные для борьбы с растениями, в частности, сорными травами. Динитрофенол, динитро-орто-кре-зол, пентахлорфенол используются как контактные гербициды. Хлорфе-нолы применяют и как фунгициды для защиты древесины от поражения грибами. Печальную известность после войны США против Вьетнама получили производные феноксиуксусной кислоты (2,4-Д и 2,4,5-Т), входившие в состав так называемой «оранжевой смеси», использовавшейся американцами в качестве дефолиантов. Эти вещества практически не токсичны для человека, однако содержавшийся в качестве примеси 2,4,7,8-тетрахлордибензодиоксин (ТХДД) вызывал поражение людей. Это вещество обладает свойствами иммунотоксиканта, тератогена, мутагена и канцерогена. Другими известными гербицидами являются парак-ват, дикват, атразин и т. д.
Диверсионные яды
Диверсионные яды — это вещества, которые могут быть использованы для заражения продовольствия, воды, обмундирования, других предметов снабжения и т. д. Такие вещества могут применяться диверсионными группами, диверсионно-десантными и воздушно-десантными подразделениями (3. Франке, 1973), а также различного рода террористическими группировками. Эти вещества даже в малых количествах могут оказаться весьма эффективными. К диверсионным ядам предъявляют следующие требования:
• высокая токсичность при поступлении через рот;
• отсутствие запаха, цвета, вкуса;
• хорошая растворимость в воде;
• устойчивость к нагреванию и гидролизу;
• наличие достаточно продолжительного скрытого периода действия;
• трудность обнаружения в организме и в зараженном материале;
• отсутствие специфики в клинической картине поражения;
• отсутствие противоядий и т. д.
Этим требованиям удовлетворяют многие соединения, с которыми может столкнуться военная медицина. С диверсионными целями могут использоваться вещества растительного происхождения (некоторые алкалоиды, гликозиды), яды грибов (аманитин, афлатоксины, трихотеце-новые микотоксины), яды животных (тетродотоксин, сакситоксин), бактериальные токсины (тетанотоксин, ботулотоксин), другие органические (производные фторкарбоновых кислот) и неорганические (соли таллия, мышьяка, ртути, азотистой кислоты и т. д.) соединения. Не исключено использование с целью диверсии лекарств, пестицидов, промышленных агентов и т. д., в том числе и боевых отравляющих веществ.
Сильнодействующие
и ядовитые вещества (СДЯВ)
Любое вещество, используемое в качестве сырья, исходного компонента синтеза, являющееся конечным продуктом производства или его отходом, обладающее высокой токсичностью, способное формировать достаточно устойчивые зоны химического заражения и находящееся на промышленном объекте в количестве нескольких десятков — сотен тонн, может при авариях и катастрофах стать причиной поражения людей. Перечни таких веществ неодинаковы для различных регионов страны (и тем более мира), они постоянно меняются, по мере совершенствования технологий и разработки новых технологических процессов. Поэтому списки и перечни СДЯВ, принятые различными ведомствами, порой включают разные вещества, числом от нескольких десятков до нескольких сотен наименований. Свойства этих веществ (агрегатное состояние, растворимость в воде, устойчивость к гидролизу, летучесть и проч.) и биологическая активность различны. Исходя из основных критериев, определяющих опасность СДЯВ (токсичность, способность формировать зону заражения, объем производства), к числу веществ, заслуживающих наибольшего внимания, относятся: хлор, аммиак, оксиды серы и азота, нитрилы и изоцианаты, гидразин и его производные, некоторые металлор-ганические соединения и др.
ЮО
1 D1
Патофизиологическая классификация ОВТВ
Несмотря на разнообразие химических веществ, представляющих интерес для военной токсикологии, они могут быть объединены в группы в соответствии с особенностями механизмов, лежащих в основе острого повреждающего действия на организм, известной близостью течения и проявлений формирующегося токсического процесса (транзиторных токсических реакций и острых отравлений). В рамках учебника будут рассмотрены следующие группы отравляющих и высокотоксичных веществ:
1. Вещества, оказывающие преимущественно местное действие на слизистые оболочки глаз и дыхательных путей и вызывающие их раздражение, сопровождающееся временной утратой пораженным дееспособности («ОВТВ раздражающего действия»).
2. Вещества, оказывающие преимущественно местное действие на дыхательные пути и ткань легких и вызывающие развитие токсического отека легких («ОВТВ удушающего действия»)
3. Вещества, оказывающие преимущественно резорбтивное действие на организм, сопровождающееся выраженным нарушением функций органов и тканей с высокой метаболической активностью, в основе которого лежит острое повреждение энергетического обмена («ОВТВ общеядовитого действия»),
4. Вещества, характеризующиеся как местным, так и резорбтивным действием на организм, сопровождающимся структурно-функциональными изменениями со стороны клеток различных органов и тканей, в основе которых лежит нарушение пластического обмена, процессов синтеза белка и клеточного деления («ОВТВ цитотокси-ческого действия»).
5. Вещества, оказывающие преимущественно резорбтивное действие на организм, сопровождающееся нарушением высшей нервной деятельности, механизмов регуляции жизненно важных органов и систем, в основе которого лежит повреждение процессов генерации, проведения и передачи нервных импульсов («ОВТВ нейротоксиче-ского действия»).
Как и любая другая, предлагаемая классификация веществ носит условный характер, так как все процессы, протекающие в организме, неразрывно связаны между собой и повреждение одного из них непременно приводит к повреждению и других. Необходимость выделения веществ в группы продиктована главным образом дидактическими соображениями.
■У.З. Химическая обстановка
В результате случайного или преднамеренного попадания ОВТВ в окружающую среду складывается химическая обстановка. Химическая обстановка характеризуется масштабом, продолжительностью и опасностью химического заражения.
Химическое заражение — это наличие ОВТВ в окружающей среде (на местности, в воздухе, на вооружении и военной технике и т. д.) в количествах, достаточных для поражения незащищенного личного состава в течение определенного времени.
Масштаб заражения определяется размерами зоны химического заражения, т. е. площадью, в пределах которой существует вероятность сверхнормативного воздействия ОВТВ и поражения незащищенного личного состава. Размеры зоны химического заражения определяются не только концентрацией вещества в окружающей среде, но и нормативами его допустимого воздействия, установленными руководящими документами, которые на мирное время, аварийные ситуации и военное время, как правило, различны. Так, в мирное время критериями гигиенической оценки степени загрязнения воздуха являются предельно допустимые концентрации (ПДК) веществ для рабочей зоны, максимальные разовые и среднесуточные концентрации для населенных мест и т. д., научно обоснованные в ходе специальных исследований. Однако эти критерии не предназначены для аварийных ситуаций. Поэтому, в соответствии с «Временным положением о порядке взаимодействия органов исполнительной власти при аварийных выбросах и сбросах загрязняющих веществ и экстремально высоком загрязнении окружающей природной среды» (1969), под экстремально высокими уровнями загрязнения атмосферного воздуха понимается содержание одного или нескольких веществ, превышающее ПДК более чем в 50 раз При сохранении токсиканта в зоне заражения на срок менее 8 ч, в 30-49 раз — на срок 8-24 ч и в 20-29 раз — на срок I—2 сут. Для поверхностных и морских вод экстремально высоким загрязнением считается превышение ПДК для веществ высокотоксичных (I—2-го класса опасности) в 5 и более раз, а для веществ умеренно и малотоксичных (3—4-го класса опасности) в 50 и более раз.
В любом случае размеры зон химического заражения будут тем больше, чем большее количество вещества попало в окружающую среду, чем выше его токсичность.
Продолжительность заражения характеризует временные границы, в пределах которых будет сохраняться зона химического заражения. Этот показатель обусловлен стойкостью ОВТВ на местности, т. е. способностью вещества сохранять во времени поражающее действие на незащищенный личный состав. Стойкость ОВТВ колеблется в чрезвычайно широких границах (табл. 18).
Часть I. ТОКСИКОЛОГИЯ
Глава 7. ОСНОВНЫЕ ПОНЯТИЯ ВОЕННОЙ ТОКСИКОЛОГИИ
Таблица 18
Период полу раз рушения некоторых ксенобиотиков на открытой местности при температуре +15° С
| Название | Продолжительность |
| Тетрахлорпарадибензодиоксин | 9 лет |
| Бенз(а)пирен | 2 года |
| Карбофуран | 45 дней |
| VX | 21 день |
| Иприт | 7 дней |
| Зарин | 4 часа |
| Синильная кислота | минуты |
Как следует из данных, представленных в табл. 18, зоны возможного химического заражения можно разделить на зоны:
• нестойкого заражения (минуты — часы);
• стойкого заражения (сутки — недели);
• длительного экологического неблагополучия (месяцы — годы). Если в зоне химического заражения находится личный состав, формируется очаг химического поражения — совокупность людей, подвергшихся сверхнормативному воздействию ОВТВ. Возникновение очагов химического поражения ОВТВ, как правило, сопровождается формированием санитарных потерь, т. е. у пораженных развиваются интоксикации различной степени тяжести, в результате чего часть личного состава выходит из строя. Выход из строя личного состава оценивается с учетом поражения не ниже легкой степени тяжести на срок не менее суток.
Основными характеристиками очага химического поражения являются: количество пораженных (массовость поражения), наличие и структура потерь, время формирования потерь, характер токсического процесса у пораженных. Основные характеристики очага могут быть спрогнозированы методами математического моделирования экстремальных ситуаций.
Массовость поражения людей в зоне химического заражения определяется как абсолютной численностью пораженных, так и их удельным весом среди населения или личного состава частей и соединений. Так, массовые случаи поражения среди населения по интенсивности поражения условно разделяют следующим образом: низкая интенсивность — 20 пораженных на 1000 человек населения; средняя — 21-50 пораженных; высокая — 51-100; очень высокая — свыше 100.
Время формирования санитарных потерь среди личного состава, попавшего в зону химического заражения различными ОВТВ, существенно различается. Некоторые ОВТВ действуют практически немедленно (например, синильная кислота, зарин, оксид углерода). Действие других сопряжено с наличием скрытого периода интоксикации (например, фосген, иприт, фторэтанол). Наконец, существуют ОВТВ, поражение которыми развивается спустя несколько дней (иногда более недели) после воздействия (например, ботулотоксин, рицин, диоксин, тетраэтилсви-нец). Следовательно, по этому признаку можно выделить ОВТВ быстрого действия, замедленного действия и крайне замедленного действия. Наибольшую опасность будут представлять зоны химического заражения, образуемые быстродействующими веществами, так как в этих условия возможности медицинской защиты личного состава будут существенно ограничены во времени. Однако зоны заражения, образуемые веществами крайне замедленного действия, также представляют опасность, поскольку факт воздействия может долгое время оставаться незамеченным и в этих условиях мероприятия медицинской защиты не будут проводиться.
В зонах химического заражения некоторыми веществами (раздражающие ОВТВ, низкие концентрации отдельных нейротоксикантов, веществ общеядовитого действия и др.) возможно поражение личного состава без формирования санитарных потерь (временная утрата дееспособности — формирование транзиторных токсических реакций). Опасность подобных зон заражения минимальна, однако боеспособность воинских подразделений, находящихся в этих зонах, будет существенно снижена.
Наконец, относительно длительное пребывание личного состава в зонах химического заражения, характеризующихся пороговыми концентрациями токсикантов в окружающей среде, может вовсе не приводить к снижению боеспособности, но быть опасным в плане формирования отдаленных последствий действия ОВТВ, проявляющихся аллобиотически-ми состояниями и специальными формами токсического процесса.
7М. Медицинская противохимическая защита
Медицинская противохимическая защита — это комплекс специальных санитарно-гигиенических, профилактических и лечебных мероприятий, проводимых в целях предупреждения или ослабления действия ОВТВ, а также сохранения жизни, восстановления здоровья и профессиональной работоспособности пораженного личного состава.
Специальные санитарно-гигиенические мероприятия предусматривают участие медицинской службы в проведении химической разведки в районе расположения войск, экспертизу воды и продовольствия на зараженность ОВТВ, обучение личного состава правилам поведения на зараженной местности и использования индивидуальных средств защиты (ИСЗ), а также проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные профилактические медицинские мероприятия включают применение специальных медикаментозных средств, повышающих устойчивость личного состава к химическим веществам (профилактических антидотов и др.), и индивидуальных средств частичной санитарной обработки.
Специальные лечебные мероприятия включают применение антидотов (само- и взаимопомощи, лечебных), а также некоторых средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности пораженного, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим.
Средства, применяемые для осуществления специальных профилактических и специальных лечебных мероприятий, называются медицинскими средствами защиты.
Глава 8. ОТРАВЛЯЮЩИЕ
И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА
РАЗДРАЖАЮЩЕГО ДЕЙСТВИЯ
8.1. Общая характеристика
Раздражающим называется действие химических веществ на окончания чувствительных нервных волокон, разветвляющихся в покровных тканях, сопровождающееся рядом местных и общих рефлекторных реакций и субъективно воспринимаемое как неприятное чувство покалывания, жжения, рези, боли и т. д.
Раздражающее действие присуще большому количеству химических соединений и, в том числе, широко используемых в хозяйственной деятельности. Среди них: галогены (хлор, бром), альдегиды (акролеин), кето-ны (ацетон), пары кислот, ангидриды кислот и др. Выраженность раздражающего действия в каждом конкретном случае определяется строением токсиканта, его количеством в окружающем воздухе и местом аппликации. Большинство веществ, действуя в концентрациях, вызывающих раздражение слизистых оболочек (глаз, дыхательных путей), инициируют и иные формы токсического процесса.
Вещества, обладающие высокой избирательностью в действии на чувствительные нервные окончания, разветвляющиеся в покровных тканях, называются раздражающими. Поражение ими в реальных условиях, как правило, ограничивается проявлениями исключительно раздражающего действия. Такие вещества могут использоваться в качестве ОВ или средств самозащиты.
Для раздражающих ОВ среднеэффективная концентрация местного действия в тысячи раз меньше среднесмертельной. Поэтому их рассматривают как временно выводящие из строя живую силу противника.
На предмет возможности создания новых образцов раздражающих ОВ в разное время изучались следующие классы соединений:
1. Алифатические и ароматические галогенированные кетоны.
2. Производные нитрилов.
3. Ароматические мышьякорганические соединения.
4. Эфиры форбола и дитерпеновые эфиры.
5. Другие ароматические и гетероциклические соединения.
По способности сообщать галогенированной молекуле кетона свойства раздражающего агента атомы галогенов располагаются в последовательности: F < CI < Вг < I. Среди алифатических кетонов наиболее активны бромпропанон и бромбутанон (оба вещества — жидкости), среди галоген-производных ароматических кетонов — хлорацетофенон (по номенклатуре ОВ иностранных армий — CN).
Общая токсичность нитрилов снижается при введении в молекулу галогена. Раздражающее действие при этом, напротив, усиливается. Среди веществ этой группы наиболее известны бромбензилцианид (СА) и ор-тохлорбензальмалонодинитрил (CS).
Некоторые производные трехвалентного мышьяка обладают выраженным раздражающим действием. В этих соединениях за счет двух валентностей осуществляется связь мышьяка с органическим радикалом. Третья, как правило, занята галогеном или CN-группой. Влияние атомов галогенов на физиологическую активность мышьякорганических веществ противоположно тому, которое они оказывают на ОВ двух первых групп. Активность токсикантов изменяется в ряду производных КВг<С1. CN-группа в наибольшей степени усиливает биологический эффект. Наиболее известным представителем группы является фенарсазинхлорид (адамсит — DM). Но и другие ароматические мышьякорганические соединения обладают высокой раздражающей активностью. Среди них: ди-фенилцианарсин (DC), дифенилхлорарсин (DA) и др.

|
| адамсит (DM) хлорацетофенон (CN) |
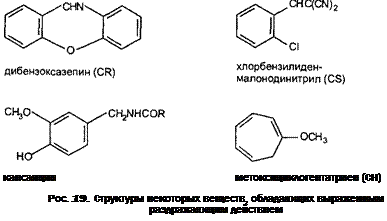 |
Высокой раздражающей активностью обладают соединения сложного строения, такие как дибензоксазепин (CR), экстракт красного перца — капсаицин, морфолид пеларгоновой кислоты, метоксициклогептатриен (СН) и др. (рис. 19).
Раздражающие ОВ используются правоохранительными органами как средства борьбы с нарушителями общественного порядка и для подавления террористов и криминальных элементов. В некоторых странах устройства, снаряженные раздражающими веществами, продаются для индивидуального пользования в целях самозащиты. Хотя полагают, что правильное применение раздражающих веществ обеспечивает формирование транзиторного токсического эффекта без серьезных последствий для пострадавшего, тем не менее результаты применения этого оружия порой трудно контролируемы, а формирующиеся эффекты малоопределенны. Непреодолимое желание скорее выбраться из зараженной атмосферы практически всегда провоцирует панику.
Широкое применение веществ может привести к появлению большого числа пострадавших, при этом не исключено поражение привлекаемого для оказания помощи медицинского персонала веществами, сохранившимися на одежде и кожных покровах пораженных.
Наиболее чувствительными к раздражению являются покровные ткани, в которых плотность нервных окончаний наивысшая, где они более доступны действию химических веществ. Это, прежде всего, конъюнктива глаз, слизистая оболочка дыхательных путей. Покровные ткани в этих областях имеют особенности строения, иннервации и поэтому неодинаково чувствительны к различным веществам. Некоторые соединения вызывают преимущественное раздражение органа зрения и потому называются слезоточивыми О В (лакриматоры), другие — носоглотки и органов дыхания (чихательные ОВ — стерниты).
Галогенированные кетоны и нитрилы проявляют свойства лакримато-ров, мышьякорганические соединения — стернитов, остальные в равной степени раздражают глаза и дыхательные пути (и даже кожу).
Ранее при разработке образцов химического оружия планировалось применение в военных целях не только «чистых» ОВ, но и их смесей. Например, рецептура CNS представляла собой смесь хлорацетофенона, хлороформа и хлорпикрина. Действие таких рецептур сопровождается развитием не только раздражающего, но и более тяжелых процессов, например отека легких (см. гл. 9. «Отравляющие и высокотоксичные вещества пульмонотоксического действия»).
Промышленные токсиканты, обладающие выраженным раздражающим действием, могут быть твердыми, жидкими и газообразными. Различие доз, вызывающих явление непереносимого раздражения слизистых оболочек и смертельное действие, у таких соединений может быть не столь большим, как у ОВ, поэтому в химических очагах, образуемых этими токсикантами при авариях и катастрофах, часто могут наблюдаться и угрожающие жизни формы патологии.

АТМОСФЕРНЫЙ ВОЗДУХ
р02 = 21,4 кПа (159 мм Hg)
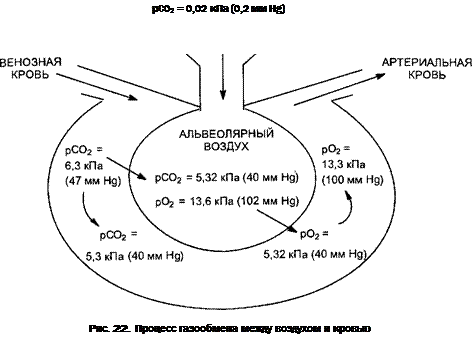 |
У части лиц, перенесших острое воздействие химических веществ, развивается прогрессирующий воспалительный процесс, который может закончиться стенозом трахеи, бронхоэктатической болезнью, облитерацией глубоких отделов дыхательных путей.
Поражение паренхимы легких
Паренхима легких образована огромным количеством альвеол. Альвеолы представляют собой тонкостенные микроскопические полости, заполненные воздухом, открывающиеся в альвеолярный мешочек, альвеолярный ход или в респираторную бронхиолу. Несколько сотен тесно примыкающих друг к другу альвеолярных ходов и мешочков образуют терминальную респираторную единицу (ацинус).
В альвеолах осуществляется газообмен между вдыхаемым воздухом и кровью. Барьер на пути диффундирующих газов образует мембрана, состоящая из слоя альвеолярного эпителия, промежуточного вещества и эндотелиальных клеток капилляров. Альвеолярный эпителий образуется клетками трех типов. Клетки первого типа представляют собой сильно уплощенные структуры, выстилающие полость альвеолы. Именно через эти клетки осуществляется диффузия газов. Клетки второго типа имеют кубовидную форму. Их поверхность покрыта микроворсинками, а цитоплазма богата ламеллярными телами. Эти клетки участвуют в обмене сур-фактанта — поверхностно-активного вещества сложной липопротеидной природы, содержащегося в тонкой пленке жидкости, выстилающей внутреннюю поверхность альвеол. Уменьшая силу поверхностного натяжения стенок альвеол, это вещество не позволяет им спадаться. Клетки третьего типа — это легочные макрофаги, фагоцитирующие чужеродные частицы, попавшие в альвеолы, и участвующие в формировании иммунологических реакций в легочной ткани. Макрофаги способны к миграции по дыхательным путям, лимфатическим и кровеносным сосудам.
Интерстициальное вещество обычно представлено несколькими эластическими и коллагеновыми волокнами, фибробластами, иногда клетками других типов.
При патологических процессах в паренхиме легких нарушается основная их функция — газообмен.
Суть газообмена состоит в диффузии кислорода из альвеолярного воздуха в кровь и диоксида углерода из крови в альвеолярный воздух. Движущей силой процесса является разница парциальных давлений газов в крови и альвеолярном воздухе (рис. 22).
Газообмен в легких затрудняется при повреждении любого элемента альвеолярно-капиллярного барьера — эпителия (пневматоцитов), эндотелия, интерстиция. Повреждение эпителия приводит к нарушению синтеза, выделения и депонирования сурфактанта, увеличению проницаемости альвеолярно-капиллярного барьера, усилению экссудации отечной жидкости в просвет альвеолы. Повреждение эндотелия усиливает проницаемость альвеолярно-капиллярного барьера, вызывает гемодинамиче-ские нарушения в легких, изменяет нормальное соотношение объема вентиляции и гемоперфузии легких и т. д. В результате нарушения газообмена развивается кислородное голодание, проявляющееся сначала при физической нагрузке, а затем и в покое. При патологии легких нарушение газообмена является основной причиной состояний, угрожающих жизни пострадавшего, а иногда и гибели.
Токсические пневмонии
В группу острых пневмоний химической этиологии входят различные, чаще комбинированные, поражения, морфологические особенности которых определяются особенностями токсического действия ксенобиотиков.
Некоторые ОВТВ, вызывающие химические пневмонии, представлены в табл. 22.
Таблица 22
ОВТВ, вызывающие острую химическую пневмонию
| Акролеин | Пары минеральных кислот |
| Аммиак | Иприты |
| Диоксид серы | Мышьякорганические соединения |
Токсиканты повреждают паренхиму легких, захватывая как альвеолярную стенку (острый, иногда геморрагический, экссудативный альвео-лит), так и легочный интерстиций (диффузная интерстициальная пневмония). В тяжелых случаях происходит некротизация легочной ткани и суперинфицирование с формированием абсцессов (акролеин), обструк-тивного поражения дыхательных путей (диоксид серы). Нередко острое воздействие приводит к развитию длительно и вяло текущих токсических процессов в легких.
Отсроченное развитие патологического процесса в легких может быть следствием не столько непосредственной альтерации легочной ткани токсикантом, сколько повреждения ее полиморфноядерными лейкоцитами и макрофагами, накапливающимися при воздействии ядовитых газов в паренхиме легких и дыхательных путях. Гибель этих клеток приводит к выходу в легочную ткань лизосомальных энзимов, простагландинов, кол-лагеназы, эластазы, плазмин-активирующих факторов и других биологически активных веществ, что стимулирует воспалительный процесс, фиброз, эмфизему, гранулематоз и т. д.
Отек легких
Характерной формой поражения пульмонотоксикантами является отек легких. Суть патологического состояния — выход плазмы крови в стенку альвеол, а затем в просвет альвеол и дыхательные пути. Отечная жидкость заполняет легкие — развивается состояние, обозначавшееся ранее как «утопление на суше».
Отек легких — проявление нарушения водного баланса в ткани легких (соотношения содержания жидкости внутри сосудов, в интерстициаль-ном пространстве и внутри альвеол). В норме приток крови к легким уравновешивается ее оттоком по венозным и лимфатическим сосудам (скорость лимфооттока — около 7 мл/ч).
Водный баланс жидкости в легких обеспечивается:
• регуляцией давления в малом круге кровообращения (в норме 7—9 мм рт. ст.; критическое давление — более 30 мм рт. ст.; скорость кровотока — 2,1 л/мин);
• барьерными функциями альвеолярно-капиллярной мембраны, отделяющей воздух, находящийся в альвеолах, от крови, протекающей по капиллярам.
Отек легких может возникать в результате нарушения как обоих регу-ляторных механизмов, так и каждого в отдельности.
В этой связи выделяют три типа отека легких:
• токсический отек легких, развивающийся в результате первичного поражения альвеолярно-капиллярной мембраны на фоне нормального, в начальном периоде, давления в малом круге кровообращения;
• гемодинамический отек легких, в основе которого лежит повышение давления крови в малом круге кровообращения вследствие токсического повреждения миокарда и нарушения его сократительной способности;
• отек легких смешанного типа, когда у пострадавших отмечается как нарушение свойств альвеолярно-капиллярного барьера, так и миокарда.
Основные токсиканты, вызывающие формирование отека легких разных типов, представлены в табл. 23.
Таблица 23
ОВТВ, вызывающие отек легких
| Вещества, вызывающие токсический отек легких | Вещества, вызывающие гемодинамический отек легких | Вещества, вызывающие отек смешанного типа |
| аммиак | арсин | люизит |
| дифосген | оксид углерода | сероводород, |
| диоксид серы | таллий | хлорпикрин и др. |
| диоксид азота | ФОС | |
| метилизоцианат и др. | цианиды и др. | |
| метилсульфат | ||
| пятифтористая сера | ||
| паракват | ||
| перфторизобутилен | ||
| трехфтористый хлор | ||
| фосген | ||
| хлор и др. |
Токсический отек легких
Собственно токсический отек легких связан с повреждением токсикантами клеток, участвующих в формировании альвеолярно-капиллярного барьера. Имеющие военное значение токсиканты, способные вызывать токсический отек легких, называют ОВТВ удушающего действия.
Механизм повреждения клеток легочной ткани удушающими ОВТВ не одинаков (см. ниже), но развивающиеся вслед за тем процессы достаточно близки (рис. 23).
12Б
1 27
ДЕЙСТВИЕ ТОКСИКАНТА
| ПЕРВИЧНЫЕ БИОХИМИЧЕСКИЕ ИЗМЕНЕНИЯ В ЛЕГОЧНОЙ ТКАНИ | |
| РАЗРАСТАНИЕ СОЕДИНИТЕЛЬНОЙ ТКАНИ |
НАРУШЕНИЕ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ И ГИБЕЛЬ КЛЕТОК:
| ГИПОКСИЯ ТКАНИ |
♦ эндотелиальных
♦ пневматоцитов 1-го и 2-го типов
♦ бронхиального эпителия
♦ клеток Клара
♦ фибробластов
| УСИЛЕНИЕ ПРОНИЦАЕМОСТИ АЛЬВЕОЛЯРНО-КАПИЛЛЯРНОГО БАРЬЕРА |
НАРУШЕНИЕ МЕТАБОЛИЗМА БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ:
| ОТЕК ЛЕГКИХ |
♦ угнетение разрушения катехоламинов, серотонина, гистамина, брадикинина и др.;
♦ активация синтеза простагландинов;
♦ нарушение синтеза сурфактанта
НАРУШЕНИЕ ГЕМОДИНАМИКИ
В МАЛОМ КРУГЕ КРОВООБРАЩЕНИЯ:
| НАРУШЕНИЕ ЛИМФАТИЧЕСКОГО ДРЕНАЖА ЛЕГОЧНОЙ ТКАНИ |
♦ увеличение объема циркулирующей крови;
♦ замедление скорости кровотока;
♦ увеличение притока крови к легким;
♦ нарастание сопротивления току крови;
♦ увеличение давления крови
Рис. 23. Схема патогенеза токсического отека легких
Повреждение клеток и их гибель приводят к усилению проницаемости барьера и нарушению метаболизма биологически активных веществ в легких. Проницаемость капиллярной и альвеолярной частей барьера изменяется не одновременно. Вначале усиливается проницаемость эндоте-лиального слоя, и сосудистая жидкость пропотевает в интерстиций, где временно накапливается. Эту фазу развития отека легких называют ин-терстициальной. Во время интерстициальной фазы компенсаторно примерно в 10 раз ускоряется лимфоотток. Однако эта приспособительная реакция оказывается недостаточной, и отечная жидкость постепенно проникает через слой деструктивно измененных альвеолярных клеток в полости альвеол, заполняя их. Эта фаза развития отека легких называется альвеолярной и характеризуется появлением отчетливых клинических признаков. «Выключение» части альвеол из процесса газообмена компенсируется растяжением неповрежденных альвеол (эмфизема), что приводит к механическому сдавливанию капилляров легких и лимфатических сосудов.
Повреждение клеток сопровождается накоплением в ткани легких биологически активных веществ, таких как норадреналин, ацетилхолин, серотонин, гистамин, ангиотензин I, простагландины Ei, Е2, F2, кини-ны, что приводит к дополнительному усилению проницаемости альвеолярно-капиллярного барьера, нарушению гемодинамики в легких. Скорость кровотока уменьшается, давление в малом круге кровообращения растет.
Отек продолжает прогрессировать, жидкость заполняет респираторные и терминальные бронхиолы, при этом вследствие турбулентного движения воздуха в дыхательных путях образуется пена, стабилизируемая смытым альвеолярным сурфактантом. Опыты на лабораторных животных показывают, что содержание сурфактанта в легочной ткани сразу после воздействия токсикантов снижается. Этим объясняется раннее развитие периферических ателектазов у пораженных.
Помимо указанных изменений, для развития отека легких большое значение имеют системные нарушения, включающиеся в патологический процесс и усиливающиеся по мере его развития. К числу важнейших относятся: нарушения газового состава крови (гипоксия, гиперкапния, а затем гипокарбия), изменение клеточного состава и реологических свойств (вязкости, свертывающей способности) крови, расстройства гемодинамики в большом круге кровообращения, нарушение функций почек и центральной нервной системы.
Характеристика гипоксии
Основная причина расстройств многих функций организма при отравлении пульмонотоксикантами — кислородное голодание. Так, на фоне развивающегося токсического отека легких содержание кислорода в артериальной крови снижается до 12 об.% и менее, при норме 18—20 об.%, в венозной — до 5—7 об.%, при норме 12—13 об.%. Напряжение СО2 в первые часы развития процесса нарастает (более 40 мм рт. ст.). В дальнейшем, по мере развития патологии, гиперкапния сменяется гипокарбией. Возникновение гипокарбии можно объяснить нарушением метаболических процессов в условиях гипоксии, снижением выработки СО2 и способностью диоксида углерода легко диффундировать через отечную жидкость. Содержание органических кислот в плазме крови при этом увеличивается до 24—30 ммоль/л (при норме 10—14 ммоль/л).
Уже на ранних этапах развития токсического отека легких повышается возбудимость блуждающего нерва. Это приводит к тому, что меньшее, по сравнению с обычным, растяжение альвеол при вдохе служит сигналом к прекращению вдоха и началу выдоха (рефлекс Геринга—Брейера). Дыхание при этом учащается, но уменьшается его глубина, что ведет к уменьшению альвеолярной вентиляции. Снижаются выделение двуокиси углерода из организма и поступление кислорода в кровь — возникает ги-поксемия.
Снижение парциального давления кислорода и некоторое повышение парциального давления СОг в крови приводят к дальнейшему нарастанию одышки (реакция с сосудистых рефлексогенных зон), но, несмотря на ее компенсаторный характер, гипоксемия не только не уменьшается, но напротив, усиливается. Причина явления состоит в том, что хотя в условиях рефлекторной одышки минутный объем дыхания и сохранен (9000 мл), альвеолярная вентиляция — снижена.
Так, в нормальных условиях при частоте дыхания 18 в минуту альвеолярная вентиляция составляет 6300 мл. Дыхательный объем (9000 мл : 18) — 500 мл. Объем мертвого пространства — 150 мл. Альвеолярная вентиляция: 350 мл • 18 = 6300 мл. При учащении дыхания до 45 и том же минутном объеме (9000) дыхательный объем уменьшается до 200 мл (9000 мл : 45). В альвеолы при каждом вдохе поступает только 50 мл воздуха (200 мл — 150 мл). Альвеолярная вентиляция за минуту составляет: 50 мл • 45 = 2250 мл, т. е. уменьшается примерно в 3 раза.
С развитием отека легких кислородная недостаточность нарастает. Этому способствует все усиливающееся нарушение газообмена (затруднение диффузии кислорода через увеличивающийся слой отечной жидкости), а в тяжелых случаях — расстройство гемодинамики (вплоть до коллапса). Развивающиеся метаболические нарушения (снижение парциального давления СОг, ацидоз, за счет накопления недоокисленных продуктов обмена) ухудшают процесс утилизации кислорода тканями.
Таким образом, развивающееся при поражении удушающими веществами кислородное голодание может быть охарактеризовано как гипоксия смешанного типа: гжоксическая (нарушение внешнего дыхания), цирку-ляторная (нарушение гемодинамики), тканевая (нарушение тканевого дыхания).
Гипоксия лежит в основе тяжелых нарушений энергетического обмена. При этом в наибольшей степени страдают органы и ткани с высоким уровнем энерготрат (нервная система, миокард, почки, легкие). Нарушения со стороны этих органов и систем лежат в основе клинической картины интоксикации ОВТВ удушающего действия.
Нарушение состава периферической крови
Значительные изменения при отеке легких наблюдаются в периферической крови. По мере нарастания отека и выхода сосудистой жидкости во внесосудистое пространство увеличивается содержание гемоглобина (на высоте отека оно достигает 200—230 г/л) и эритроцитов (до 7—9 • 1012/л), что может быть объяснено не только сгущением крови, но и выходом форменных элементов из депо (одна из компенсаторных реакций на гипоксию). Возрастает число лейкоцитов (9—11 ■ 109/л). Значительно ускорено время свертывания крови (30—60 с вместо 150 с в обычных условиях). Это приводит к тому, что у пораженных отмечается наклонность к тромбообразованию, а при тяжелых отравлениях наблюдается прижизненное свертывание крови.
Гипоксемия и сгущение крови усугубляют гемодинамические нарушения.
Нарушение деятельности сердечно-сосудистой системы
Сердечно-сосудистая система, наряду с дыхательной, претерпевает наиболее тяжелые изменения. Уже в раннем периоде развивается бради-кардия (возбуждение блуждающего нерва). По мере нарастания гипоксе-мии и гиперкапнии развивается тахикардия и повышается тонус периферических сосудов (реакция компенсации). Однако при дальнейшем нарастании гипоксии и ацидоза сократительная способность миокарда снижается, капилляры расширяются, в них депонируется кровь. Артериальное давление падает. Одновременно усиливается проницаемость сосудистой стенки, что приводит к отеку тканей.
Нарушение деятельности нервной системы
Роль нервной системы в развитии токсического отека легких весьма значительна.
Непосредственное действие токсических веществ на рецепторы дыхательных путей и паренхимы легких, на хеморецепторы малого круга кровообращения может быть причиной нервно-рефлекторного нарушения проницаемости альвеолярно-капиллярного барьера. Дуга такого рефлекса представлена волокнами блуждающего нерва (афферентный путь) и симпатическими волокнами (эфферентный путь), центральная часть проходит в стволе мозга ниже четверохолмий. В эксперименте показано, что повышенное наполнение малого круга кровообращения и нарушение водно-солевого обмена у животных, отравленных дифосгеном, являются следствием рефлекторного усиления продукции гипофизом вазопрессина.
Динамика развития отека легких несколько различается при поражении разными веществами удушающего действия. Вещества с выраженным раздражающим действием (хлор, хлорпикрин и т. д.) вызывают более стремительно развивающийся процесс, чем вещества, практически не вызывающие раздражения (фосген, дифосген и т. д.). Некоторые исследователи относят к веществам «быстрого действия» в основном те, которые повреждают преимущественно альвеолярный эпителий, «медленного действия» — поражающие эндотелий капилляров легких.
Обычно (при интоксикации фосгеном) отек легких достигает максимума через 16—20 ч после воздействия. На этом уровне он держится в течение суток — двух. На высоте отека наблюдается гибель пораженных. Если в этом периоде смерть не наступила, то с 3—4-х сут начинается обратное развитие процесса (резорбция жидкости лимфатической системой, усиление оттока с венозной кровью), и на 5—7-е сут альвеолы полностью освобождаются от жидкости. Смертность при этом грозном патологическом состоянии составляет, как правило, 5—10%, причем в первые 3 сут погибает около 80% от общего количества погибших.
Осложнениями отека легких являются бактериальная пневмония, формирование легочного инфильтрата, тромбоэмболия магистральных сосудов.
9.2. ОВТВ удушающего действия
9.2.1. Характеристика отдельных представителей ОВТВ удушающего действия
9.2.1.1. Фосген
| CI о—< xOCCI3 дифосген |
Фосген относится к группе галогенпроизводных угольной кислоты. Условием физиологической активности таких соединений является наличие связи галоген — карбонильная группа. Замещение одного из галогенов в молекуле соединения на водород или алкильный радикал приводит к резкому снижению пульмонотоксичности. Синтезированы хлор-, бром- и фторпроизводные угольной кислоты, токсичность которых близка. В большей степени требованиям, предъявлявшимся к ОВ, соответствовали хлорпроизводные. Помимо фосгена в качестве ОВ рассматривался трих-лорметиловый эфир угольной кислоты (дифосген). Вещества обладают практически одинаковой биологической активностью. Принято считать, что действие дифосгена обусловлено расщеплением его молекулы на две молекулы фосгена при контакте с тканями легких.
о—
фосген
Фосген получен в 1812 г. английским химиком Деви, наблюдавшим взаимодействие хлора с оксидом углерода на солнечном свету, отсюда и название вещества (фосген: от греч. — светорожденный). Применен впервые как ОВ в 1915 г. Германией. Общее количество ОВ, синтезированного за период 1915—1918 гг., оценивают в 150 ООО т. Около 80% погибших в ходе Первой мировой войны от ОВ приходится на долю отравленных фосгеном. В настоящее время запасы фосгена и дифосгена, хранящиеся на армейских складах, подлежат уничтожению. Однако фосген и его производные являются важным исходным продуктом синтеза пластмасс, синтетических волокон, красителей, пестицидов. Поэтому производство этого вещества во всех странах с развитой химической промышленностью неуклонно возрастает. Фосген является одним из токсичных продуктов термической деструкции хлорорганических соединений (фреоны, поливинилхлоридный пластик, тефлон, четыреххлористый углерод), что также необходимо учитывать при организации оказания помощи в очагах аварий и катастроф.
Физико-химические свойства
Дихлорангидрид угольной кислоты (фосген) — в обычных условиях бесцветный газ с запахом гнилых яблок или прелого сена, в малых концентрациях обладает приятным фруктовым запахом. Газообразный фосген в 2,48 раза тяжелее воздуха. При температуре 0° С вещество представляет собой жидкость с плотностью 1,432, кипящую при +8,2° С, замерзающую при — 118° С. В воде растворяется плохо: в одном объеме воды — два объема газообразного фосгена (примерно 0,8%). Хорошо растворяется в органических растворителях и некоторых других соединениях — в ледяной уксусной кислоте, хлористом мышьяке, хлороформе и т. д. При взаимодействии с водой фосген гидролизуется до соляной и угольной кислот.
При случайном (аварии, катастрофы) или преднамеренном выбросе в окружающую среду формирует зоны нестойкого заражения.
Пути поступления и токсичность
Фосген действует только ингаляционно, оказывает специфическое действие на органы дыхания, а в момент контакта — слабое раздражающее (порой незаметное) действие на глаза и слизистые оболочки. Во внутренние среды не проникает, разрушаясь при контакте с легочной тканью. Запах фосгена ощущается в концентрации 0,004 г/м3. Пребывание в атмосфере, содержащей до 0,01 г/м3, без последствий возможно не более часа. Концентрация 1 г/м3 уже при экспозиции 5 мин более чем в 50% случаев ведет к смерти. Смертельная токсодоза (LQ50) составляет 3,2 г ■ мин/м3.
Основные проявления интоксикации
В тяжелых случаях течение отравления условно может быть разделено на четыре периода: воздействия ОВ, скрытый, развития токсического отека легких, разрешения отека.
В период воздействия выраженность проявлений интоксикации зависит от концентрации фосгена. ОВ в небольшой концентрации в момент контакта явлений раздражения обычно не вызывает. С увеличением концентрации появляются неприятные ощущения в носоглотке и за грудиной, затруднение дыхания, слюнотечение, кашель. Эти явления исчезают при прекращении контакта с ОВ.
Скрытый период характеризуется субъективным ощущением благополучия. Продолжительность его в среднем составляет 4—6 ч, но определяется тяжестью интоксикации и зависит от общего состояния организма в момент отравления, поэтому возможны отклонения в обе стороны (1—24 ч).
Основные проявления интоксикации отмечаются в третьем периоде — токсического отека легких, когда отечная жидкость выходит в альвеолы. Усиливается одышка (до 50—60 дыхательных актов в минуту), носящая инспираторный характер. Появляется кашель, постепенно усиливающийся и сопровождающийся выделением изо рта и носа большого количества пенистой мокроты. При перкуссии определяются опущение нижних границ легких и неоднородный перкуторный звук. Выслушиваются влажные хрипы разных калибров. По мере нарастания отека жидкость заполняет не только альвеолы, но также бронхиолы и бронхи. Максимального развития отек достигает к концу первых суток.
При благоприятном течении интоксикации с 3-4-го дня наступает период разрешения отека. Однако на этом фоне возможно присоединение вторичной инфекции и развитие пневмонии, что и может явиться причиной смерти в более поздние сроки (8—15-е сут).
При вдыхании OB в малых концентрациях отек легких не развивается. Начальные проявления интоксикации включают головокружение, слабость, кашель, чувство сдавления в груди и диспноэ. Возможно развитие слезотечения, тошноты, головной боли. Эти явления исчезают в течение короткого времени после воздействия.
Механизм токсического действия
Попадая в дыхательную систему, вещество слабо задерживается в дыхательных путях вследствие низкой гидрофильное™. Поражение легких является следствием прямого повреждения веществом клеточных структур аэрогематического барьера. По механизму токсического действия фосген относится к алкилирующим агентам, способным связываться с SH-, NH2- и СОО- группами биологических молекул. Взаимодействуя с альвеолоцитами II типа, токсикант повреждает их, угнетая активность ферментов синтеза фосфолипидов и сурфактанта. Поскольку период полуобмена сурфактанта у человека достаточно продолжителен (12—24 ч), увеличение силы поверхностного натяжения в альвеолах и их «спадание» обнаруживаются только спустя несколько часов после ингаляции вещества. Проникая далее по градиенту концентраций в глубь альвеолярно-капиллярного барьера, фосген снижает жизнеспособность и метаболическую активность эндотелиальных клеток капилляров легких.
Важную роль в развитии патологии может играть действие вещества на окончания афферентных волокон блуждающего нерва, иннервирую-щего глубокие отделы дыхательной системы.
9.2.1.2. хлор
Хлор был первым веществом, примененным на войне в качестве ОВ. 22 апреля 1915 г. близ города Ипр германские части выпустили его из баллонов (около 70 т), направив поток газа, движимый ветром, на позиции французских войск. Эта химическая атака стала причиной поражения более чем 7000 человек. Позже вещество широко применялось на фронтах Первой мировой войны и потому клиническая картина поражения хорошо изучена.
В настоящее время хлор как ОВ не рассматривается. Тем не менее миллионы тонн вещества ежегодно получаются и используются для технических нужд — очистки воды (2-6%), отбеливания целлюлозы и тканей (до 15%), химического синтеза (около 65%) и т. д. Хлор является наиболее частой причиной несчастных случаев на производстве.
Физико-химические свойства. Токсичность
Хлор — газ желтовато-зеленого цвета с характерным удушливым запахом, примерно в 2,5 раза тяжелее воздуха. Распространяясь в зараженной атмосфере, он следует рельефу местности, затекая в ямы и укрытия. Хорошо адсорбируется активированным углем. Химически очень активен. При растворении в воде взаимодействует с ней, образуя хлористоводородную и хлорноватистую кислоты. Является сильным окислителем.
Нейтрализуется хлор водным раствором гипосульфита. Он сохраняется и транспортируется в сжиженном виде под повышенным давлением. В случае аварий на объектах производства, хранения, транспортировки и использования возможно массовое поражение людей.
Уже в минимальных концентрациях (0,01 г/м3) хлор раздражает дыхательные пути, действуя в более высоких концентрациях (более 0,1 г/м3), вызывает тяжелое поражение. Пребывание в атмосфере, содержащей хлор в концентрациях 1,5-2 г/м3, сопровождается быстрым (через 2-4 ч) развитием отека легких.
По данным А. А. Лихачева (1931), при регистрации гибели экспериментальных животных (собак) в течение трех суток LQ50 составляет около 70 г • мин/м3.
Основные проявления интоксикации
В редких случаях (при ингаляции чрезвычайно высоких концентраций) смерть может наступить уже при первых вдохах зараженного воздуха. Причина смерти — рефлекторная остановка дыхания и сердечной деятельности. Другой причиной быстрой гибели пострадавших (в течение 20-30 мин после вдыхания вещества) является ожег легких. В этих случаях окраска кожных покровов пострадавшего приобретает зеленоватый оттенок, наблюдается помутнение роговицы.
Чаще в случаях тяжелого отравления в момент воздействия пострадавшие ощущали резкое жжение в области глаз и верхних дыхательных путей, стеснение дыхания. Отравленный стремится облегчить дыхание, разрывая ворот одежды. Одновременно отмечается крайняя слабость, отравленные падают и лишаются возможности покинуть пораженную зону. Практически с начала воздействия появляется надрывный, мучительный кашель, позже присоединяется одышка, причем в дыхании участвуют добавочные дыхательные мышцы. Пораженный старается занять положение, облегчающее дыхание. Речь невозможна. Иногда наблюдается рвота.
Через некоторое время после выхода из зоны поражения может наступить некоторое облегчение состояния (скрытый период), однако чаще (в отличие от поражения фосгеном) полная ремиссия не наступает: сохраняется кашель, болезненные ощущения по ходу трахеи и в области диафрагмы.
Через некоторое время (от нескольких часов до суток) состряние вновь ухудшается, усиливаются кашель и одышка (до 40 дыхательных актов в минуту), лицо приобретает синюшную (синий тип гипоксии), а в крайне тяжелых случаях пепельную (серый тип гипоксии), окраску. Над легкими прослушиваются хрипы. Пострадавший постоянно отхаркивает пенистую желтоватую или красноватую жидкость (более 1 л за сутки). Наблюдаются сильнейшие головные боли, температура тела понижается. Пульс замедлен. Артериальное давление падает. Пострадавший теряет сознание и погибает при явлениях острой дыхательной недостаточности. Если отек легких не приводит к гибели, то через несколько часов (до 48) состояние начинает улучшаться, отечная жидкость рассасывается. Однако заболевание постепенно переходит в следующий период — осложнений, во время которого обычно развиваются явления бронхопневмонии.
Как правило, отравленные, не погибшие в первые 24 ч после воздействия, выживают. Явления бронхита и пневмонии могут наблюдаться в течение нескольких недель, а легочная эмфизема оказывается стойким последствием интоксикации. Часто в качестве осложнения регистрируются длительные нарушения сердечной деятельности.
Типичным проявлением поражения умеренными концентрациями хлора является увеличение сопротивления дыханию при сохранении диффузионной способности легочной ткани. Нормализация дыхательной функции у пострадавших возвращается к норме в течение нескольких месяцев.
В подавляющем большинстве случаев легких поражений хлором наблюдается полное восстановление здоровья.
Механизм токсического действия
Механизм повреждающего действия хлора на клетки дыхательной системы связывают с его высокой окислительной активностью, способностью при взаимодействии с водой образовывать соляную (резкое изменение рН среды и денатурация макромолекул) и хлорноватистую кислоты. Хлорноватистая кислота образует в цитозоле клеток хлорамины, имеющие достаточно высокую биологическую активность, может взаимодействовать с ненасыщенными связями жирных кислот фосфолипидов и образовывать пероксиды, блокировать сульфгидрильные группы олигопептидов и белков. Получены данные, что в реакциях хлорноватистой кислоты с биомолекулами образуется супероксидный радикал — инициатор процесса свободнорадикального окисления в клетках.
Данные о влиянии хлора на состояние биохимической системы лег- | ких весьма немногочисленны. Показано, что при ингаляции вещества в ' среднесмертельной токсодозе отмечается снижение в легких крыс содержания восстановленного глутатиона и аскорбиновой кислоты, а также активности глюкозо-6-фосфатдегидрогеназы, глутатионредуктазы, глута-тионпероксидазы и каталазы.
9.2.1.3. Оксиды азота
Оксиды азота (закись — N20; окись — N0; трехокись — N2O3; двуокись — N02; четырехокись — N2O4; пятиокись — N2O5) входят в состав так называемых взрывных и пороховых газов, образующихся при стрельбе, взрывах, запуске ракет, оснащенных двигателями, работающими на твердом ракетном топливе. При этом содержание оксидов азота в воздухе может возрастать до 20-40%, что приводит к интоксикации, характер которой определяется составом взрывных газов. Наибольшее значение, с точки зрения опасности воздействия на человека, имеют диоксид (NO2) и монооксид (N0) азота.
При ингаляции оксиды азота представляют опасность уже в концентрации 0,1 г/м3, а при концентрации 0,5-0,7 г/м3 возможно развитие отека легких. Порог раздражающего действия при 4-минутной экспозиции составляет 0,15 г/м3, при 15-минутной — 0,09 г/м3 (Тиунов Л. А. и соавт.).
Наиболее типичным для оксидов азота является удушающее действие, приводящее к развитию отека легких. В основе действия лежит способность веществ активировать свободнорадикальные процессы в клетках, формирующих альвеолярно-капиллярный барьер. Так, NO2, взаимодействуя в водной среде с кислородом, инициирует образование супероксидных и гидроксильных радикалов, перекиси водорода. Действуя на глутатион, аскорбиновую кислоту, токоферол и т. д., токсикант повреждает низкомолекулярные элементы антирадикальной защиты клеток. В результате активируется перекисное окисление липидов и повреждаются биологические мембраны клеток, формирующих альвеолярно-капиллярный барьер. Атаке подвергаются и другие макромолекулы — инициируются процессы, лежащие в основе цитотоксичности (см. раздел «Общая токсикология»).
Вдыхание диоксида азота в очень высоких концентрациях приводит к быстрому развитию нитритного шока, часто заканчивающегося гибелью пострадавших. В основе нитритного шока лежит массированное образование в крови метгемоглобина (см. гл. 10. «Отравляющие и высокотоксичные вещества общеядовитого действия») и химический ожег легких. При ингаляции монооксида азота происходит образование нитрозилгемоглобина с последующим превращением его также в метгемоглобин. Количество образовавшегося метгемоглобина при ингаляции оксидов азота в концентрациях до 0,15 г/м3 невелико и не играет существенной роли в проявлении токсических эффектов. При более высоких концентрациях роль метгемог-лобинообразования в механизме развития патологии возрастает.
Наконец, в случае преобладания в газовой смеси монооксида азота развивается так называемая обратимая форма интоксикации. Поражение сопровождается одышкой, рвотой, падением артериального давления за счет сосудорасширяющего действия NO. Эти явления быстро проходят после удаления пораженного из зараженной атмосферы.
Таким образом, интоксикация оксидами азота в зависимости от условий (концентрация и соотношение веществ во вдыхаемом воздухе) может развиваться либо по удушающему (токсический отек легких), либо по шокоподобному (метгемоглобинообразование, ожог легких), либо по обратимому (падение АД) типу.
9.2.1.4. Паракват
Паракват — 1,1-диметил,4,4-дипиридил хлорид, является контактным неселективным гербицидом.
НзС-^N^3J) СНз 2СГ
В 1955 г. его стали широко использовать в сельском хозяйстве. Основными поставщиками пестицида являются Китай, Тайвань, Италия, Япония, Великобритания и США. Применение ядохимиката разрешено более чем в 130 странах.
Физико-химические свойства. Токсичность
Паракват — кристаллическое вещество белого цвета, без запаха. Хорошо растворяется в воде и спиртах; температура кипения 300° С (при этом препарат разлагается). Применяется паракват в виде крупнодисперсного аэрозоля (300—600 мкм). После оседания аэрозольных частиц на почву агент быстро разрушается с образованием малотоксичных продуктов. Поэтому даже при интенсивном использовании ядохимиката не отмечено его накопления в окружающей среде.
Токсичность параквата для млекопитающих достаточно высока (табл. 24). Смертельная доза для человека составляет приблизительно 3—5 г.
Таблица 24
Токсичность (LD50) параквата для грызунов, мг/кг
| Путь введения | Крысы | Мыши | ||
| самцы | самки | самцы | самки | |
| Перорально | ||||
| Подкожно | ||||
| Внутрибрюшинно | - |
Токсикокинетика
Наиболее частой причиной отравления людей является поступление параквата через рот. После приема вещество всасывается в тонком кишечнике (не более 20% от введенного количества) и распределяется в организме. Легкие активно захватывают паракват через механизм аккумуляции биогенных аминов, метаболизм которых в основном проходит в легочной ткани.
Основные проявления интоксикации
Действуя в дозах выше среднелетальных, вещество поражает все жизненно важные органы (печень, почки, легкие). Развиваются ожог слизистой оболочки желудочно-кишечного тракта, диарея, повреждение паренхиматозных органов и острый токсический альвеолит. Характерна отсроченная гибель отравленных, через несколько дней или недель, от нарастающего фиброза легких.
Поражение легких при интоксикации паракватом протекает в две фазы. В первую — деструктивную (1-е — 3-й сут) — наблюдается гибель и десквамация альвеолоцитов 1-го и 2-го типов, что становится причиной острого альвеолита, токсического отека легких. Во второй фазе — проли-феративной — происходит замещение альвеолоцитов кубовидными клетками, постепенное разрастание фиброзной ткани.
В механизме токсического действия параквата ведущую роль играет образование в результате его метаболизма клетками, накапливающими вещество, активного промежуточного продукта, инициирующего свобод-норадикальный процесс. Повреждение мембран вследствие активации перекисного окисления липидов сопровождается гибелью клеток, формирующих альвеолярно-капиллярный барьер. Наиболее чувствительны к параквату альвеолоциты 1-го типа. Возможно, что в основе повреждения альвеолоцитов лежит не только активация ПОЛ, но и другие механизмы.
Важную роль в процессе разрастания соединительной ткани в легких играют альвеолярные макрофаги и нейтрофилы крови. Эти клетки, активированные паракватом, продуцируют специфические гликопротеины, усиливающие пролиферацию фибробластов и их фиксацию на базальной мембране альвеол.
Предотвратить накопление параквата в легких после его приема на практике не удается. Субстраты — конкуренты яда (цистамин, путресцин и т. д.) могут оказать эффект лишь в ранние сроки от начала интоксикации (первые 8—12 ч).
При отравлениях паракватом абсолютно противопоказана оксигеноте-рапия. Данное мероприятие достоверно ускоряет гибель отравленных. Только в случаях угрожающей жизни гипоксемии (р02 в артериальной крови менее 40 мм рт. ст.) возможна ингаляция кислорода.
9.2.2. Диагностика поражения
ОВТВ удушающего действия
Первым шагом на пути выявления лиц, подвергшихся острому воздействию токсикантов, является констатация самого факта воздействия. В тех случаях, когда этот факт очевиден (в лицо солдату выброшена струя токсического агента), процедура носит формальный характер (регистрация случая). Однако значительно чаще это не простая задача.
Поскольку транзиторные токсические реакции быстро исчезают, а стойкие признаки острого ингаляционного поражения формируются постепенно, диагностика развивающейся патологии в ранние сроки представляет известную сложность. Рентгенографические изменения в легких в первые часы после воздействия ОВТВ отсутствуют; содержание газов в крови — в пределах нормы. Существуют косвенные признаки, позволяющие предположить возможность поражения пульмонотоксикантами. К их числу относятся: ожег кожи лица, слюнотечение, затруднение дыхания, кашель и т. д. Лиц, доставленных из зоны пожара (особенно при возгорании синтетических материалов) или взрыва в закрытом помещении, всегда следует рассматривать как потенциально отравленных. Особое внимание следует уделять пострадавшим, находящимся в бессознательном состоянии, поскольку вероятность получения тяжелого отравления у них выше.
9.2.3. Медицинская защита
Медицинская защита от поражения веществами удушающего действия предполагает проведение целого комплекса мероприятий, в который входят:

Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Оказание помощи
За всеми лицами, доставляемыми из зон заражения ОВТВ удушающего действия, устанавливается тщательное наблюдение. Периодически проводятся клинико-диагностические исследования (частота дыхания и пульса, анализ крови, рентгенография легких, газовый состав крови и т. д.). Показания к принятию решений по оказанию помощи пораженным представлены в табл. 25.
Таблица 25
Показания к принятию решений по оказанию помощи пораженным ОВТВ удушающего действия
Показания к госпитализации:
« поражение в замкнутом пространстве
« сохранение признаков поражения (кашель, одышка и т. д.) долее 4 ч « нарушение сознания « ожог кожи лица
■ загрудинные боли
Показания к оказанию неотложной помощи: » угнетение сознания
| Показания к интубации: ■ ларингоспазм • тяжелый отек гортани « острая дыхательная недостаточность, угрожающая жизни |
• гипоксия "
> снижение объеме форсированного выдоха
4. Снижение объема крови, циркулирующей в малом круге кровообращения (вынужденное положение тела; форсированный диурез; жгуты на конечности).
5. Стимуляция сердечной деятельности.
6. Борьба с осложнениями (антикоагулянты; антибиотики).
Общая продолжительность лечения пострадавших — около 15—20
дней, осложненных форм — 45—55 дней.
Поскольку при экстремальных ситуациях пострадавшие часто имеют сопутствующие поражения (ожоги, шок) и нередко нуждаются в переливании большого количества жидкостей, оказание им помощи весьма затруднено.
Медицинские средства защиты

Антидоты ОВТВ удушающего действия отсутствуют. В качестве медицинских средств защиты (на догоспитальном этапе) используют препараты, предназначенные для профилактики или устранения (минимизации) развивающихся эффектов, угрожающих жизни, здоровью пострадавших, снижающих их дееспособность (табл. 26).
часть i. юксикология
Глава 9. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЬСIЬАI iyj IbMUHU I ЦКСИЧЬСКЦГО ДЕЙСТВИЯ
Кислородотерапия й
Традиционно одним из важных элементов оказания помощи пораженным удушающими ядами является раннее применение кислорода. Уже достаточно давно было отмечено, что использование 02 (в том числе под положительным давлением) благоприятно сказывается на течении токсического отека легких (Савицкий Н. Н., 1938; Голиков С. Н., 1972 и др.). Считалось, что кислородная терапия должна быть ранней. Проводить ее необходимо до исчезновения признаков гипоксии.
В последние годы наметилась тенденция к пересмотру некоторых положений, касающихся применения кислорода при поражении удушающими веществами. Основанием для этого служат данные о повреждающем действии высоких концентраций 02 на легочную ткань (преимущественно за счет активизации свободнорадикальных процессов в клетках эндотелия легочных капилляров), способности кислорода провоцировать бронхоспазм, спазм сосудов малого круга кровообращения, а также данные, свидетельствующие об усилении токсичности некоторых удушающих ядов на фоне ингаляции кислорода. Отчетливое потенцирующее действие кислорода отмечено при экспериментальных поражениях хлором и паракватом, в меньшей степени при ингаляции оксидов азота. В этой связи важен выбор оптимального режима ингаляции кислорода, позволяющего обеспечить эффективный газообмен при минимальной концентрации кислорода во вдыхаемой газовой смеси.
С учетом сказанного, после действия сильных прижигающих агентов (типа хлора) оказание помощи следует начинать не с ингаляции кислорода, а с ликвидации ларинго-, бронхоспазма и болевого синдрома, что нередко бывает достаточным для устранения гипоксии. Критериями необходимости оксигенотерапии являются клинические признаки дыхательной недостаточности — цианоз, тахипноэ, брадикардия, снижение АД, уменьшение парциального давления 02 в артериальной крови ниже 65 мм рт. ст. По мнению Мартина и Кохеля (1988), при поражениях удушающими ядами не следует использовать газовые смеси, содержащие более 50-55% 02.
В очаге поражения и при транспортировке на этапах медицинской эвакуации ингаляции кислорода осуществляют с помощью кислородных ингаляторов КИ-4М и И-2. Оба прибора рассчитаны на кратковременное применение. Поскольку газообмен при отеке легких затруднен из-за наличия в воздухоносных путях отечной вспенившейся жидкости, наряду с оксигенотерапией используют вещества, повышающие поверхностное натяжение отечной жидкости и уменьшающие ее объем. К таким веществам, получившим название противовспенивающих, относятся этиловый спирт, 10% водный раствор коллоидного силикона, 10% спиртовой раствор антифомсилана и др. Эти средства применяют ингаляционно.
Кортикостероидные препараты
Назначение глюкокортикостероидов при поражениях ОВТВ удушающего действия преследует три основные цели:
• снижение выраженности обструкции дыхательных путей;
• уменьшение проницаемости альвеолярно-капиллярной мембраны;
• устранение нарушений гемодинамики.
В экспериментальных исследованиях с ингаляцией удушающих веществ (фосгена, оксидов азота) показано, что раннее использование кор-тикостероидов приводит к заметному снижению летальности, уменьшению частоты и степени выраженности токсического отека легких. Авторы работ рассматривают глюкокортикостероиды как главное средство лечения этих поражений, подчеркивается необходимость их возможно более раннего использования, рекомендуются высокие и очень высокие дозы препаратов.
Вместе с тем хорошо известны и опасности, связанные с использованием кортикостероидов, главная из которых состоит в повышении вероятности развития серьезных инфекционных осложнений. Некоторые авторы считают эту опасность столь существенной, что рекомендуют воздержаться от этих препаратов при некоторых формах поражения, в частности, при комбинации респираторных поражений с ожогами.
Преодоление противоречия лежит в возможности ингаляционного (преимущественно местного) применения препаратов. Так, по мнению Диллера (1984), условием успешной терапии поражения удушающими веществами является возможно более раннее (в скрытом периоде) ингаляционное применение дексазона-21-изоникотината, причем только за первые сутки рекомендуется совершить до 250 ингаляций.
Оправдан ингаляционный способ введения такого аэрозольного препарата, как дексаметазон, со скоростью 150 ингаляций в течение первых 6 ч после поражения. При крайне тяжелой интоксикации или запоздалом лечении (развившемся отеке) переходят на парентеральное введение преднизолона.
Продолжается поиск альтернативных средств снижения альвеолярно-капиллярной проницаемости и предупреждения отека легких.^ В качестве таковых испытываются нестероидные противовоспалительные препараты, влияющие на метаболизм эйкозаноидов, простациклинов (диклофенак), антиоксиданты (большие дозы аскорбиновой кислоты, производные антрохинона, диметилсульфоксид, восстановленный глу-татион, унитиол, витамины Е и А), ингибиторы протеаз (контрикал), ингибиторы NO-синтазы (L-нитроаргинин), блокаторы кальциевых каналов (верапамил) и т. д.
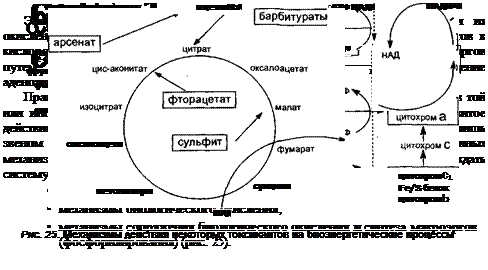 | |||
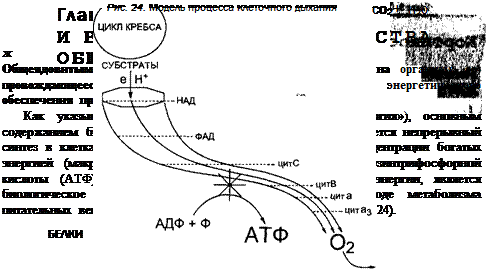 | |||
часть i. iuitwvmujiui ия
Глава 10. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ОБЩЕЯДОВИТОГО ДЕЙСТВИЯ
 |  | ||
 |  |  | 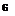 |  | |||||
нями организма. Процесс насыщения гемоглобина 02 и рассыщения ок-сигемоглобина описывается S-образной кривой (см. рис. 26). Такая форма зависимости между р02 и % НЮ есть следствие явления взаимодействия четырех субъединиц гемоглобина в молекулярном комплексе (гем-гем взаимодействие). Физиологический смысл явления — обеспечение максимально возможного выделения кислорода в ткани при незначительном различии парциального давления газа в крови и тканях (при р02 в крови около 40 мм рт. ст. и р02 в тканях около 20 мм рт. ст. гемоглобин высвобождает около 50% связанного кислорода).
В норме на сродство кислорода к гемоглобину влияют многочисленные факторы. Среди основных: рН, рС02 (эффект Бора), биорегуляторы процесса диссоциации оксигемоглобина (2,3-дифосфоглицерат и др.). При повышении рН, рС02 и содержания 2,3-дифосфоглицерата в эритроцитах сродство гемоглобина к кислороду снижается — отдача кислорода тканям возрастает.
Из сказанного ясно, что вещества, взаимодействующие с гемоглобином и нарушающие его свойства, будут существенно изменять кислород-транспортные свойства крови, вызывая развитие гипоксии гемического типа.
Кислородное голодание плохо переносится человеком и другими млекопитающими и в тяжелых случаях может привести к серьезным нарушениям со стороны различных органов и систем. Особенно чувствительными к гипоксии являются клетки органов с интенсивным энергообменом — сердечной мышцы, почек и головного мозга (табл. 27).
Таблица 27
Потребление кислорода различными органами крысы (по Field et al., 1939)
| Орган | Скорость потребления кислорода, мл/г ткани а минуту |
| Скелетная мускулатура | 0,875 |
| Кожа | 0,416 |
| Кости | 0,153 |
| Кровь | 0,025 |
| Печень | 2,010 |
| Почки | 4,120 |
| Мозг | 1,840 |
| Легкие | 1,250 |
| Сердце | 1,930 |
Функциональная состоятельность мозга целиком зависит от непрерывного снабжения его кислородом. Так, при полной аноксии «местных» запасов кислорода (7-10 мл) хватает лишь на 10 с. Мозг, составляя по массе 2-3% от массы тела, потребляет около 20% всего потребляемого
______ Глава 10. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ОБЩЕЯДОВИТОГО ДЕЙСТВИЯ
организмом кислорода. Нормальная скорость кровотока составляет 50—60 мл/мин/100 г ткани, а скорость поглощения 02 — 3,5 мл/мин/100 г ткани. Собственно нервные клетки составляют 5% от общей массы мозга, но потребляют 25% 02, потребляемого мозгом (нейрон — 350—450 мкл Ог/мин; глиальные клетки — 60 мкл Ог/мин). До 90% вырабатываемой и потребляемой энергии расходуется на поддержание электрохимического градиента возбудимых мембран и метаболизм биологически активных веществ, участвующих в передаче нервных импульсов. Неудивительно, что сознание, как функциональный феномен, утрачивается уже в течение несколько секунд полной аноксии мозга. Необратимые изменения нейронов наступают позже, спустя 4—5 мин после полного прекращения снабжения мозга кислородом. Другие органы и ткани, расходующие энергию в основном на обеспечение пластического обмена (процессы синтеза и разрушения структурных элементов живого), способны переживать (хотя и с нарушениями функций) нехватку кислорода в течение нескольких часов.
Токсиканты, избирательно нарушающие кислородтранспортные функции крови, обладают высокой токсичностью.
10.1.1.1. ОВТВ, образующие карбоксигемоглобин
Карбоксигемоглобин образуется при действии на организм монооксида углерода (СО), так называемого угарного газа, а также при отравлении некоторыми карбонилами металлов, которые, попав в организм, разрушаются с образованием СО. В недалеком прошлом тетракарбонил никеля [Ni(CO)4] и пентакарбонил железа [Fe(CO)s] изучались на предмет возможности создания на их основе боевых отравляющих веществ.
10*1.1.1.1. Карбонилы металлов
Соединения металлов с СО называются карбонилами металлов. Их применяют в некоторых областях химической промышленности. Из множества соединений особый интерес представляют пентакарбонил железа и тетракарбонил никеля — вещества, легко разлагающиеся с образованием СО. Оба токсиканта представляют собой бесцветные летучие жидкости (максимальная концентрация в воздухе — более 300 г/м3), пары которых примерно в 6 раз тяжелее воздуха (могут образовывать нестойкие зоны заражения). Плохо растворяются в воде; хорошо — в липидах.
Действуют как ингаляционно, так и через неповрежденную кожу (в крови разрушаются с образованием СО).
В зонах заражения возможны два варианта поражения — собственно веществами и продуктами их разложения. Собственно вещества обладают свойствами пульмонотоксикантов (см. выше). Тяжелое поражение сопровождается развитием (в течение 10—15 ч) токсического отека легких. Токсичным продуктом разложения веществ является оксид углерода, особенности действия которого представлены ниже.
10.1.1.1.2. Оксид углерода (СО)
Оксид углерода является продуктом неполного сгорания углерода. Он образуется в качестве примеси везде, где происходит горение углеродсодер-жащего топлива (топка печей, эксплуатация двигателей внутреннего сгорания и т. д.). Массовые поражение угарным газом возможны в очагах пожаров и при накоплении вещества в плохо вентилируемых пространствах — помещениях, туннелях, шахтах и т. д., где действует источник его образования.
Физико-химические свойства
СО — бесцветный газ, не имеющий запаха, с низкой плотностью по воздуху (0,97). Кипит при -191,5° С и замерзает при —205, Г С. В воде и плазме крови растворяется мало (около 2% по объему), лучше в спирте. Смесь СО с воздухом способна взрываться. Плохо сорбируется активированным углем и другими пористыми материалами. Оксид углерода как соединение с двухвалентным атомом углерода является восстановителем и может вступать в реакции окисления. На воздухе горит синим пламенем с образованием диоксида углерода. При нормальной температуре превращение СО в С02 идет при участии катализаторов, например гопкалита [смеси двуокиси марганца (60%) и окиси меди (40%)]. Поскольку газ легче воздуха, зоны нестойкого химического заражения на открытом пространстве могут формироваться лишь в очагах обширных пожаров.
Токсичность
Чувствительность людей к оксиду углерода колеблется в довольно широких пределах. Она зависит от многих факторов: от длительности экспозиции, степени физической нагрузки в момент действия яда, от температуры внешней среды и состояния организма. Отравление наступает быстрее и протекает тяжелее при анемиях, авитаминозах, у истощенных людей. Пребывание в атмосфере, содержащей 0,01 об. % СО (0,2 мг/л), при физической нагрузке допустимо не долее 1 ч. После этого появляются признаки отравления. Отчетливая клиническая картина острого поражения развивается при содержании СО в воздухе более 0,1 об. %.
Токсикокинетика
Единственный способ поступления газа в организм — ингаляционный. Оксид углерода, при вдыхании зараженного им воздуха, легко преодолевает легочно-капиллярную мембрану альвеол и проникает в кровь. Скорость насыщения крови оксидом углерода увеличивается при повышении его парциального давления во вдыхаемом воздухе, усилении внешнего дыхания и интенсификации легочного кровообращения (увеличиваются при физических нагрузках). По мере увеличения концентрации яда в крови скорость резорбции замедляется. При достижении равновесия в содержании СО в альвеолярном воздухе и в крови дальнейшее поступление его в организм прекращается.
Выделение оксида углерода из организма при обычных условиях происходит в неизмененном состоянии также через легкие. Период полувыведения составляет 2—4 ч.
Основные проявления интоксикации
Раздражающим действием оксид углерода не обладает. Контакт с веществом проходит незамеченным. Тяжесть клинической картины отравления угарным газом определяется содержанием СО во вдыхаемом воздухе, длительностью воздействия, потребностью организма в кислороде, интенсивностью физической активности пострадавшего. По степени тяжести интоксикации принято делить на легкие, средние и тяжелые.
Легкая степень отравления формируется при действии относительно невысоких концентраций яда. Она развивается медленно (порой в течение нескольких часов) и характеризуется сильной головной болью, головокружением, шумом в ушах, потемнением в глазах, понижением слуха, ощущением «пульсации височных артерий», тошнотой, иногда рвотой. Нарушается психическая деятельность: пораженные теряют ориентировку во времени и пространстве, могут совершать немотивированные поступки. Отмечается повышение сухожильных рефлексов. У отравленного развиваются тахикардия, аритмия, повышается артериальное давление. Возникает одышка — признак компенсаторной реакции организма на развивающуюся гипоксию. Однако в результате одышки увеличивается количество выдыхаемого диоксида углерода (С02), развивается газовый алкалоз. Кроме того, учащение дыхания при нахождении человека в отравленной зоне является дополнительным фактором, ускоряющим поступление оксида углерода в организм.
Легко пораженный СО утрачивает боеспособность. Однако при прекращении поступления яда в организм все перечисленные симптомы отравления в течение нескольких часов проходят без каких-либо последствий.
При продолжительном поступлении оксида углерода в организм или при действии его в более высоких концентрациях развивается отравление средней степени тяжести, характеризующееся более выраженными проявлениями интоксикации, большей скоростью их развития. Нарушается координация движений. Сознание затемняется, развиваются сонливость и безразличие к окружающей обстановке, появляется выраженная мышечная слабость. Слизистые оболочки и кожа приобретают розовую окраску. Могут развиваться фибриллярные подергиваний мышц лица. Возможно повышение температуры тела до 38—40° С. Одышка усиливается, пульс учащается. Артериальное давление после кратковременного подъема, связанного с возбуждением симпатико-адреналовой системы и выбросом катехоламинов из надпочечников, снижается. Этот эффект объясняют прямым действием СО и рефлекторной реакцией (с хеморе-цепторов каротидного синуса) на центры регуляции сосудистого тонуса.
Прогрессирующая гипоксия активирует процессы анаэробного гликолиза, о чем свидетельствует активация ряда ферментов (альдолазы, дегид-рогеназы-3-фосфоглицеринового альдегида, лактатдегидрогеназы). В результате в организме накапливаются молочная и пировиноградная кислоты.
15Q
Это способствует развитию метаболического ацидоза, который приходит на смену газовому алкалозу.
При отравлении средней степени тяжести в большинстве случаев через несколько часов (до суток) после прекращения действия яда состояние пострадавших существенно улучшается, однако довольно долго сохраняются тошнота, головная боль, сонливость, склонность к головокружению, шаткая походка.
Тяжелое отравление характеризуется быстрой потерей сознания, появлением признаков гипертонуса мышц туловища, конечностей, шеи и лица (ригидность затылочных мышц, тризм жевательной мускулатуры). На высоте токсического процесса могут развиться судороги клонико-то-нического характера. Кожные покровы и слизистые оболочки приобретают ярко-розовый цвет (признак высокого содержания карбоксигемогло-бина в крови). Если в этот период пострадавший не погибает, судороги прекращаются, но развивается кома: утрачиваются рефлексы, мышцы расслабляются. Дыхание становится поверхностным, неправильным. Зрачки расширены, на свет не реагируют. Пульс частый, слабого наполнения, артериальное давление резко снижено. При регистрации биоэлектрической активности сердца на электрокардиограмме определяются экстрасистолия, нарушение внутрисердечной проводимости, признаки диффузных и очаговых мышечных изменений, острой коронарной недостаточности. Изменения в мышце сердца, регистрируемые на ЭКГ, отчасти обусловлены изменением электролитного состава крови: увеличивается содержание кальция и магния, уменьшается содержание натрия и калия. В связи с сужением периферических сосудов происходит переполнение кровью внутренних органов и полых вен. Развиваются застойные явления, затрудняющие работу сердца.
В крови, вследствие рефлекторного сокращения селезенки, увеличивается до 6—7* 1012/л количество эритроцитов, развиваются лейкоцитоз со сдвигом формулы крови влево, относительная лимфопения и эозино-пения. Растет содержание мочевины в крови. В таком состоянии отравленный может пребывать несколько часов, и при нарастающем угнетении дыхания с прогрессирующим падением сердечной деятельности наступает смертельный исход. При благоприятном течении отравления и своевременном оказании медицинской помощи симптомы интоксикации исчезают, и через 3—5 дней состояние пострадавшего нормализуется. Изменения ЭКГ при тяжелых отравлениях порой выявляются в течение нескольких недель и даже месяцев.
В случае высокого содержания во вдыхаемом воздухе оксида углерода (до нескольких процентов) на фоне пониженного парциального давления 02 (до 17—14%) при выполнении физической нагрузки, сопровождающейся усиленным газообменом (ситуация, возникающая при пожарах, взрывах боеприпасов в замкнутых пространствах и т. д.), развивается молниеносная форма отравления (Другов Ю. В., 1959). Пораженные быстро теряют сознание. Возможны кратковременные судороги, за которыми наступает смерть или развивается тяжелая кома. Прогноз неблагоприятный, если коматозное состояние продолжается более двух суток.
Выделяют также синкопальную форму интоксикации. По данным Б. И. Предтеченского, эта разновидность поражения составляет до 10-20% всех случаев отравления и развивается у лиц с нарушенными механизмами регуляции гемодинамики. При этом варианте течения отравления наблюдается резкое снижение артериального давления, сознание быстро утрачивается, кожные покровы и слизистые оболочки становятся бледными («белая асфиксия»). Развившееся коллаптоидное состояние может продолжаться несколько часов. Возможен смертельный исход от паралича дыхательного центра.
Осложнения острой интоксикации
При отравлениях тяжелой степени могут наблюдаться осложнения, которые снижают дееспособность или полностью лишают человека работоспособности в течение длительного времени. Чаще эти осложнения развиваются не сразу после отравления, а по прошествии нескольких дней или даже недель. К таким осложнениям относятся деструктивные процессы в ткани мозга, приводящие к формированию стойких нарушений функций центральной нервной системы (ослабление памяти, неспособность к умственному напряжению, изменения психической деятельности). Нарушения со стороны периферической нервной системы характеризуются невритами, радикулитами, парестезии. Иногда развиваются параличи и парезы конечностей. Возможны расстройства зрения, слуха, обоняния и вкуса. Тяжелое отравление часто осложняется пневмонией и отеком легких, вследствие нарушения легочного кровообращения и сердечной недостаточности, а также рабдомиолизом с последующей острой почечной недостаточностью.
Механизм токсического действия
Оксид углерода in vitro активно взаимодействует с многочисленными гем-содержащими протеидами (гемоглобин, миоглобин, цитохромы и т. д.) при условии, что железо, входящее в структуру порфиринового кольца их простетической группы, находится в двухвалентном состоянии. Связь двухвалентного железа с СО — обратима. С трехвалентным железом вещество не взаимодействует.
Оксид углерода, проникший в кровь, вступает во взаимодействие с гемоглобином (Но) эритроцитов, образуя карбоксигемоглобин (НЬСО), не способный к транспорту кислорода. Развивается гемтеский тип гипоксии. Оксид углерода способен взаимодействовать как с восстановленной (Но), так и с окисленной (НЬО) формой гемоглобина, поскольку в обеих формах железо двухвалентно.
НЬО + СО ===== НЬСО + о К-1
К* = К+1/К_, — Константа Дугласа; К*= 300
Степень сродства токсиканта к гемоглобину может быть охарактеризована константой равновесия реакции взаимодействия (константа Дугласа). Установлено, что у человека, хотя скорость присоединения СО к гемоглобину в 10 раз ниже скорости присоединения кислорода, скорость диссоциации карбоксигемоглобина приблизительно в 3600 раз меньше соответствующей скорости для оксигемоглобина. Поэтому относительное сродство НЬ к СО примерно в 300 раз выше, чем к кислороду. Величина константы Дугласа у животных разных видов различна (у лошади — 240, канарейки — 100, кролика — 40). В состоянии равновесия СО, в концентрации 1 объемная часть на 1000 объемных частей воздуха, превращает 50% гемоглобина крови человека в карбоксигемоглобин. Как правило, в реальных условиях концентрация 0,1 % СО во вдыхаемом воздухе обусловливает образование около 10% карбоксигемоглобина в крови.
Количество карбоксигемоглобина, образовавшегося в крови в начале воздействия яда, может быть рассчитано по формуле Лилиенталя (1946):
% НЬСО = (pCO't«MOfl)«0,05,
где рСО — парциальное давление СО во вдыхаемом воздухе в мм рт. ст.; t — время экспозиции в минутах; МОД — минутный объем дыхания в литрах.
Поскольку карбоксигемоглобин не в состоянии переносить кислород а
от легких к тканям, существует тесная корреляция между его уровнем в
крови и выраженностью клинической картины отравления. Экспозиция
0,5% СО в течение часа при умеренной физической активности сопро- |
вождается образованием 20% карбоксигемоглобина, при этом пострадав-
ший начинает испытывать неприятные ощущения, предъявляет жалобы |
на головную боль. Интоксикация средней степени тяжести развивается I
при содержании крабоксигемоглобина 30—50%, тяжелая — около 60% и |
выше. Смертельные исходы при отравлении СО в эксперименте на жи- ?
вотных наблюдаются при уровне НЬСО в крови — 60—70%. Вместе с тем ]
механическое удаление 70% гемоглобина или ингаляция воздуха с пони- ^
женным парциальным давлением 02 (и снижение тем самым содержания }
НЬО до уровня 30%) к смерти экспериментальных животных не приво-
дят. Это наблюдение косвенно указывает на наличие дополнительных |
механизмов токсического действия СО. По существующим представле-
ниям они состоят в следующем. i
Во-первых, оксид углерода не только выключает из транспорта 02 |
часть гемоглобина, но также нарушает явление гем-гем взаимодействия,
затрудняя тем самым процесс диссоциации НЬО в крови отравленного и
передачу транспортируемого кислорода тканям (Л. А. Тиунов, В. В. Кус-
тов, 1969). Эффект еще более усиливается по мере развития интоксика-
ции и понижения парциального давления С02 в крови и тканях (эффект i
Бора). I
Во-вторых, СО взаимодействует не только с гемоглобином, но также с целым рядом различных цитохромов (цитохромом «а», цитохромом «С», цитохромом Р-450 и т. д.), угнетая тем самым биоэнергетические процессы в тканях (развивается гистотоксический тип гипоксии — см. ниже).
Поскольку валентность железа тканевых цитохромов переменна, они становятся уязвимыми для действия токсиканта при переходе в состояние Fe+2. Это состояние наиболее вероятно в условиях снижения парциального давления кислорода в тканях (при гипоксии). Так, установлено, что экспериментальные животные, находящиеся под воздействием газовой смеси 3 атм. кислорода и I атм. оксида углерода, не погибают, хотя при этих условиях практически весь НЬ превращается в НЬСО. Тем не менее тканевые цитохромы резистентны к действию СО (железо находится преимущественно в трехвалентной форме), а растворенного в плазме крови кислорода оказывается достаточно, чтобы удовлетворить потребность в нем тканей. При изменении соотношения газовой смеси — 3 атм. кислорода и 2 атм. оксида углерода — животные погибают, несмотря на то что количество растворенного в плазме крови кислорода остается таким же, как в первом опыте. Развитие интоксикации в этом случае можно объяснить угнетением системы цитохромов — нарушением тканевого дыхания.
Наконец, СО активно взаимодействует с миоглобином (сродство в 14—50 раз выше, чем к кислороду), пероксидазой, медь-содержащими ферментами (тирозиназа) тканей. Миоглобин (мышечный пигмент — аналог гемоглобина, состоящий из одной молекулы глобина, связанной с гемом) в организме выполняет функцию депо кислорода, а также значительно ускоряет диффузию кислорода в мышечной ткани. Взаимодействие оксида углерода с миоглобином приводит к образованию карбокси-миоглобина. Нарушается обеспечение работающих мышц кислородом. Этим отчасти объясняют развитие у отравленных выраженной мышечной слабости.
Определение карбоксигемоглобина в крови
Для уточнения диагноза отравления оксидом углерода производится определение НЬСО в крови различными физико-химическими и химическими методами.
Существуют довольно простые экспресс-методы определения содержания НЬСО в крови: проба с разведением, проба с кипячением, проба со щелочью, проба с медным купоросом, проба с формалином. Принцип методов основан на большей устойчивости НЬСО (сохраняет розовую окраску в растворе), в сравнении с НЬО, к денатурирующим воздействиям. Их чувствительность находится в пределах 25—40% НЬСО.
Количественное определение содержания НЬСО в крови производят спектрометрическими, фотометрическими, колориметрическими и газоаналитическими методами. Наиболее чувствительны фотометрический и спектрофотометрический методы, позволяющие определять НЬСО в крови начиная с 0,5—1%.
При необходимости направления проб в лабораторию для определения наличия НЬСО необходимо исключить контакт содержимого пробирок с воздухом, например, путем наслаивания вазелинового масла.
Мероприятия медицинской защиты |
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты 1 (средства защиты органов дыхания; при применении карбонилов i металлов — средства защиты органов дыхания и кожи) в зоне хи- : мического заражения.
Специальные профилактические медицинские мероприятия:
• применение антидота перед входом в зону пожара;
• проведение санитарной обработки пораженных карбонилами металлов на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных; ,i
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, > дееспособности, в ходе оказания первой (само- и взаимопо- ' мощь), доврачебной и первой врачебной (элементы) помощи по- J страдавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты i
Сразу после удаления пораженного из зараженной атмосферы начина- 'i ется процесс спонтанного выведения СО из организма, постепенно вое- 1 станавливаются свойства гемоглобина и тканевых ферментов. Специфическими противоядиями при отравлении СО являются вещества, ускоряю- | щие этот процесс: кислород (Н. Н. Савицкий и др.) и ацизол (Л. А. Тиунов ; и др.).
Кислород. В связи с тем что СО обратимо связывается с гемоглобином ] и при этом конкурирует за участок связывания (двухвалентное железо , гема) с кислородом, увеличение парциального давления последнего во ' вдыхаемой смеси (вдыхание чистого кислорода) способствует ускорению диссоциации образовавшегося карбоксигемоглобина и усиленному выве- : дению яда из организма отравленного (скорость элиминации возрастает в 3-4 раза). При ингаляции 02 под повышенным давлением (0,5-2 атмосферы избыточной), кроме того, увеличивается количество кислорода, | транспортируемого плазмой крови в форме раствора, снижается чувстви- тельность тканевых цитохромов к ингибиторному действию СО, что также способствует устранению явлений кислородного голодания, нормализации энергетического обмена.
Ингаляцию кислорода (или кислородо-воздушных смесей) с помощью имеющихся на снабжении технических средств (кислородные ингаляторы) следует начинать как можно раньше. В первые минуты рекомендуют вдыхать 100% кислород, затем в течение 1-3 ч — 80-90% кислородо-воздуш-ную смесь, затем — 40-50% смесь кислорода с воздухом. Продолжительность мероприятия определяется степенью тяжести пострадавшего.
Бессознательное состояние, признаки ишемии миокарда, уровень карбоксигемоглобина в крови выше 60%, дыхательная недостаточность — показания к проведению гипербарической оксигенации (при наличии технических средств).
Ацизол — бис-(1-виниламидазол)-цинкдиацетат — комплексное соединение цинка, которое при действии на гемоглобин уменьшает его сродство к оксиду углерода (константа Хила процесса взаимодействия уменьшается с 2,3 до 1,8). Препарат рекомендуют применять внутримышечно в форме 6% раствора на 0,5% растворе новокаина в объеме 1,0 мл на человека в возможно более ранние сроки после воздействия СО. В случае тяжелого отравления допускается повторное введение ацизола в той же дозе не ранее чем через 1 ч после первой инъекции.
Симптоматические средства. При легких и средней степени тяжести поражениях позитивный эффект на состояние пострадавших оказывает назначение, наряду с ингаляцией кислорода, средств, возбуждающих дыхание и сердечную деятельность: кордиамин — 1 мл (п/к), кофеин 10% — 1-2 мл (п/к), вдыхание паров нашатырного спирта. Применение таких средств у тяжелопораженных без одновременно проводимой кислородотера-пии — противопоказано.
При поражении карбонилами металлов, кроме указанного выше, при угрозе развития токсического отека легких необходимо использование средств и методов, применяемых при отравлениях ОВТВ удушающего действия (см. гл. 9. «Отравляющие и высокотоксичные вещества пульмонотоксического действия»).
10.1.1.2. ОВТВ, образующие метгемоглобин
Как уже указывалось, железо, входящее в структуру гемоглобина, — двухвалентно, не зависимо от того, связан пигмент крови с кислородом (НЬО) или нет (НЬ). Более того, только находясь в двухвалентном состоянии (Fe+2), железо обладает необходимым для осуществления транспортных функций сродством к кислороду.
В нормальных условиях спонтанно и под влиянием различных патогенных факторов, в том числе химической природы, двухвалентное железо гемоглобина окисляется, переходя в трехвалентную форму. Образуется так называемый метгемоглобин (MetHb). Метгемоглобин не участвует в переносе кислорода от легких к тканям, поэтому значительное повышение его содержания в крови представляет опасность. Эволюционно сформировались механизмы обратного превращения метгемоглобина в гемоглобин. Благодаря этим механизмам у здорового человека уровень метгемоглобина в крови не превышает 0,5-2%. Существуют два основных механизма защиты железа гемоглобина от окисления.
Первый связан с «обезвреживанием» проникающих в эритроциты ксенобиотиков-окислителей до момента их действия на гемоглобин. Так, в присутствии энзима глутатионпероксидазы (ГПО) восстановленный глутатион взаимодействует с молекулами-окислителями, попавшими в клетки крови, предотвращая их метгемоглобинообразующее действие.
Несостоятельность этого механизма (снижение активности глутатионпе-роксидазы, содержания восстановленного глутатиона в эритроцитах) может привести к умеренной метгемоглобинемии и появлению в крови телец Гейнца (продукты денатурации гемоглобина).
Второй механизм обеспечивает восстановление уже образовавшегося в крови метгемоглобина при участии двух ферментативных систем: НАДН-зависимой и НАДФН-зависимой метгемоглобинредуктаз. В одной из них донорами электронов (восстанавливающих агентов) являются продукты анаэробного этапа метаболизма глюкозы (НАДН), в другой — гексозомонофосфатного превращения (НАДФН) (рис. 27).
Гексозомонофосфатный шунт
НАДФН-MetHbRed
НАДФН + HbFe(+3)-OH ------------- >■ HbFe(+2) + НАДФ + НЦО
кофактор
(5% общей восстановительной активности)
бой необратимый дериват Hb. Он никогда не встречается в нормальной крови и также не способен обратимо присоединять кислород, хотя и содержит двухвалентное железо.
Наиболее токсичные метгемоглобинообразователи относятся к одной
из следующих групп:
| NH, |
1. Соли азотистой кислоты (нитрит натрия)
2. Алифатические нитриты (амилнитрит, изопропилнитрит, бутил-нитрит)
3. Ароматические амины (анилин, аминофенол)
4. Ароматические нитраты (динитробензол, хлорнитробензол)
5. Производные гидроксиламина (фенилгидроксиламин)
6. Производные гидразина (фенилгидразин)
N0,
,N(CH3)2
Путь Эмбдена-Мейергофа
НАДН-MetHbRed
НАДН + HbFe(+3)-OH »► HbFe(+2) + НАД + Н20
(67% общей восстановительной активности)
Рис. 27. Механизмы восстановления метгемоглобина
В количественном отношении более значимым является механизм, связанный с гликолизом. Однако в процессе гексозомонофосфатного превращения под влиянием гексозо-6-фосфатдегидрогеназы (Г-6Ф-ДГ) образуется восстановленный никотинамидадениндинуклеотид фосфат (НАДФН), который не только участвует в превращении метгемоглобина в гемоглобин в присутствии НАДФН-метгемоглобинредуктазы, но и в восстановлении окисленного глутатиона при участии НАДФН-зависимой глутатионредуктазы. Поэтому значение этого механизма «защиты» гемоглобина также велико. По этой причине лица с врожденной недостаточностью Г-6Ф-ДГ весьма чувствительны даже к относительно невысоким дозам целого ряда токсикантов.
Основной причиной массивного образования метгемоглобина в крови до уровня, порой угрожающего жизни человека, является действие на организм химических веществ, так называемых метгемоглобинообразователей (оксидов азота, органических и неорганических нитро- и аминосоединений, фенолов, хлоратов, сульфонов и т. д.). Наряду с MetHb при интоксикациях подобными веществами в крови нередко появляется и другой продукт повреждения гемоглобина — сульфгемоглобин. В отличие от MetHb, который легко восстанавливается в организме за счет редуктазных ферментных систем обратно до гемоглобина, сульфгемоглобин представляет со
| анилин |

 |
Результатом понижения уровня гемоглобина является нарушение кислородтранспортных функций крови. Кислородная емкость крови понижается (в зависимости от тяжести отравления) на 15—80%. Формируется гемический тип гипоксии со всеми сопутствующими ей проявлениями (см. выше).
В периоде выраженной анемии в патологический процесс вовлекаются почки. В тяжелых случаях на 4—6-й день отравления развивается оли-гурия, а затем и анурия. Появляются признаки уремии: запах мочи изо рта, рвота, расстройства сознания, судороги. В ряде случаев в клинической картине отравления появляются признаки печеночной недостаточности: увеличение размеров печени, ее болезненность и т. д. При патоло-гоанатомическом исследовании лиц, погибших в этом периоде, отмечается характерная картина изменения почек. Они увеличены в размерах, мягкие, цвета спелой сливы. На разрезе выявляются кровоизлияния и инфильтраты, рисунок почки сглажен, ткань ее буро-красного цвета. Полости боуменовых капсул растянуты и заполнены мелкозернистым содержимым. Просветы извитых и прямых канальцев выполнены бурой массой, дающей положительную реакцию на железо. Налицо признаки механического повреждения органа гемоглобином и продуктами его разрушения, содержащимися в огромных количествах в плазме крови отравленных.
При средней степени тяжести признаки отравления исчезают через 2—4 нед, при благоприятном течении тяжелой интоксикации полное восстановление трудоспособности наблюдается через 2—3 мес. Прогноз в значительной мере определяется функцией почек. Летальность составляет более 20%. Последствия перенесенной интоксикации могут проявиться длительным нарушением функций печени и почек. К числу отдаленных последствий относятся полиневриты, сопровождающиеся нарушением чувствительности.
Механизм токсического действия
Кривая токсичности арсина характеризуется большой крутизной, это означает, что различия доз, вызывающих пороговое действие и смертельное поражение, малы. Так, в опытах на животных показано, что ингаляционное воздействие токсикантом в течение 28 дней в концентрации 5 объемных частей газа на миллион частей воздуха (ppm — pars per million) переносится практически бессимптомно. Вместе с тем ингаляция в течение 4 сут вещества в концентрации 10 ppm приводит к 100% гибели животных. Такая закономерность соответствует представлениям о механизме токсического действия вещества. Во всех случаях воздействия арси-ном, сопровождавшихся гемолизом, отмечали существенное истощение содержания глутатиона в эритроцитах. Экспериментально установлено, что гемолитический эффект, по всей видимости, и обусловлен снижением содержания этого трипептида в клетках крови. Глутатион, как известно, необходим для поддержания целостности мембраны эритроцитов. Если скорость его синтеза превышает скорость истощения, наступающего под влиянием арсина, гемолиз не развивается. Напротив, если истощение превалирует над синтезом, развивается острая гемолитическая реакция. Наконец, в тех случаях, когда воздействие АбНз не сопровождается полным истощением запасов восстановленного глутатиона, гемолитический эффект носит дозо-зависимый характер.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения.
Специальные лечебные мероприятия:
» своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности пораженного, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Специфические противоядия токсиканта отсутствуют. Использование хелатирующих агентов, успешно применяемых для оказания помощи отравленным соединениями мышьяка иного строения, при отравлении арсином оказывается малоэффективным. Имеются данные о способности 2,3-димеркаптосукцината in vitro полностью предупреждать гемолитическое действие мышьяковистого водорода. Однако in vivo этот комплексон оказывается также практически неэффективным. В этой связи с целью медицинской защиты, направленной на спасение жизни и минимизацию ущерба, наносимого токсикантом здоровью пораженного, применяют симптоматические средства борьбы с развивающимися анемией, кислородным голоданием и поражением почек: обильное питье, кровопускание (300—400 мл), внутривенное введение 40% раствора глюкозы, физиологического раствора, других кровезаменяющих жидкостей, ингаляцию кислорода (см. выше). Важным мероприятием медицинской защиты является скорейшее выявление пораженных, до развития у них выраженного гемолиза, и скорейшая эвакуация их в лечебные учреждения.
.*1 ■
10.2. ОВТВ, нарушающие тканевые процессы биоэнергетики
10.2.1. Ингибиторы ферментов цикла Кребса
В результате гликолиза в клетках накапливается пировиноградная кислота, превращение которой при участии ферментов пируватоксидазного комплекса приводит к образованию уксусной кислоты. Последняя, в активированной форме ацетил-КоА, вступает в превращения, называемые циклом трикарбоновых кислот (цикл Кребса). Эти превращения, проходящие исключительно в митохондриях клеток, приводят к синтезу изо-цитрата, сс-кетоглютарата, сукцината, малата — непосредственных субстратов следующего этапа энергетического обмена — их биологического окисления. Угнетение ферментов цикла Кребса и истощение образующихся субстратов сопровождается острым нарушением энергообеспечения клеток.
Ингибиторы цикла трикарбоновых кислот — это, прежде всего, F- и С1-уксусная кислоты и вещества, метаболизирующие в организме с образованием этих соединений. Будучи аналогами ацетата, рассматриваемые вещества в форме F- и С1-ацетил-КоА вступают в метаболические превращения в цикле Кребса. На одном из этапов биотрансформации образуется субстрат, блокирующий всю цепь взаимозависимых реакций цикла. Чувствительность энзимов цикла трикарбоновых кислот к F-ацетату очень высока, к С1-ацетату ниже. С этим связана высокая токсичность F-уксусной кислоты и ее производных для человека (летальная доза — около 0,1 мг/кг), токсичность С1-уксусной кислоты в 10—15 раз меньше.
Для военной токсикологии особый интерес представляют фторорга-нические соединения.
10.2.1.1. Фторорганические соединения
Синтез фторорганических соединений явился в середине XX в. необходимым элементом крупномасштабного производства пластмасс, хладагентов, пестицидов, красителей, смазочных материалов и т. д. Высокая токсичность некоторых представителей этого класса соединений стала поводом для их пристального изучения, в том числе и с военными целями.
Фторорганические соединения значительно различаются по токсичности. Поданным Б. Сондерса (1957), решающим фактором, определяющим их биологическую активность, является способность метаболизиро-вать в организме с образованием фторуксусной кислоты. Именно это соединение ответственно за инициацию токсического процесса при поступлении в организм токсичных аналогов. Согласно данным автора, в ряду производных фторкарбоновых кислот [F(CH2)nC00R] ядовиты лишь соединения с нечетным числом метиленовых групп в молекуле. Чередованне токсичности в пределах гомологического ряда объяснимо с позиций теории р-окисления жирных кислот в организме, согласно которой последние ступенчато расщепляются, последовательно отделяя от исходной структуры молекулы уксусной кислоты. Если число метиленовых групп в молекуле исходного агента (п) — четное, то в результате такого расщепления последним метаболитом окажется относительно малотоксичная 3-фторпропионовая кислота (LD50 для мышей при внутрибрю-шинном способе введения — 60 мг/кг), если п — нечетное — фторуксус-ная.
Помимо фторкарбоновых кислот высокой токсичностью обладают некоторые производные эфиров фторкарбоновых кислот — F(CH2)nCOOR и фторированных спиртов — F(CH2)nCOH. Эти вещества также метабо-лизируют (гидролизуются, окисляются) с образованием фторуксусной кислоты. Метиловый эфир фторуксусной кислоты и 2-фторэтанол в середине XX в. рассматривались как возможные ОВ (3. Франке, 1973), однако в качестве таковых не производились.
Понятно, что наиболее токсичным представителем группы является сама фторуксусная кислота.
10.2.1.2. Фторуксусная кислота
Фторуксусная кислота, по мнению специалистов, почти идеально соответствует требованиям, предъявляемым к диверсионным ядам. Она сильно ядовита, устойчива в водных растворах, органолептически не обнаруживается, затруднено ее химико-аналитическое определение, действие проявляется после скрытого периода.
Вещество впервые синтезировано Свартсом в 1900 г. Позже кислота была выделена из листьев южноафриканских растений Dichapetalum су-mosum, D. veneatum и др. Несколько листьев этих растений достаточно для приготовления снадобья, способного умертвить лошадь.
Физико-химические свойства. Токсичность
Фторуксусная кислота — кристаллическое вещество, хорошо растворимое в воде. Стойкое при кипячении. Токсичность ее неодинакова для разных видов живых существ. Летальная доза для мышей составляет около 0,6 мг/кг, для овец — 0,7 мг/кг, для лошадей — 1,0 мг/кг, собак — 0,1 мг/кг. Средняя смертельная доза для человека определяется, как 2—5 мг на килограмм массы тела.
Токсикокинетика
Вещество хорошо всасывается в желудочно-кишечном тракте и быстро распределяется в организме. Проницаемость через гематоэнцефаличе-ский барьер умеренная. Вещество медленно метаболизирует в организме. Метаболиты выделяются с мочой и через легкие.
часть I. ЮКСИКОЛОГИЯ
F
Глава 10. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ОБЩЕЯДОВИТОГО ДЕЙСТВИЯ
Проявления интоксикации
У грызунов интоксикация протекает очень бурно. Уже через несколько минут после введения смертельной дозы развиваются судороги и через минуту — полторы после их начала у отдельных особей регистрируют смерть. Если смертельный исход не наступает, нормализацию состояния отмечают уже через 20 мин после прекращения судорог.
У человека, в зависимости от принятой дозы, действие на организм проявляется спустя 0,5—6 ч. Такое отсроченное начало отравления можно связать с прохождением во времени этапов метаболизма ксенобиотика в цикле Кребса и постепенным истощением субстратов биологического окисления, которые в норме присутствуют в клетке в некотором избытке. Появляются тошнота, боли в животе, оглушенность, спутанность сознания, чувство страха, выраженная одышка. Затем пострадавший теряет сознание, появляются приступы клонико-тонических судорог. Смерть наступает от остановки дыхания и нарушения сердечной деятельности, сопровождающейся фибрилляцией желудочков. Если на высоте интоксикации пострадавший не погибает, формируется затяжная кома, в которой пострадавший может оставаться до 6 сут.
Механизм токсического действия
Еще в 1947 г. Бартлет и Баррон, а позже Лиебиг и Питере показали способность фторуксусной кислоты блокировать в организме окисление ацетата. В настоящее время полагают, что в основе механизма токсического действия вещества лежит его способность в форме FAuKoA проникать в митохондрии и вступать в метаболические превращения в цикле Кребса. Установлено, что продукт превращения фторацетата — фтор-цитрат ковалентно связывается с ферментом транслоказой внутренней мембраны митохондрий, участвующим в процессе переноса цитрата через митохондриальную мембрану, и нарушает этот процесс. Кофактором транслоказы является глутатион, который также связывается с фторцит-ратом. Известно, что синтез АцКоА и его утилизация идет только при условии трансмембранного тока из митохондрий цитрата, поэтому блокада транслоказы угнетает превращение ацетата в цикле Кребса. Кроме того, блок цикла трикарбоновых кислот развивается на этапе превращения цитрата в цис-аконитат в результате конкурентного обратимого ин-гибирования образующимся фторцитратом фермента аконитатгидратазы. Поскольку in vivo вводимый в избытке цитрат существенно не облегчает течение интоксикации, этот механизм нарушения митохондриальных процессов не считают основным. В результате такого комплексного действия фторуксусной кислоты повреждаются митохондриальные процессы, лежащие в основе образования субстратов аэробной фазы дыхания, — нарушается синтез макроэргов.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• применение средств защиты органов дыхания в очагах поражения летучими соединениями (фторэтанолом, эфирами фторуксусной кислоты и т. д.).
Специальные лечебные мероприятия:
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Оказание неотложной помощи пострадавшим осуществляется в соответствии с общими принципами (см. 6.4. «Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях»).
В эксперименте на лабораторных животных показано, что при раннем введении ацетата натрия (2—3 г/кг) наблюдается снижение тяжести интоксикации, вызванной фторуксусной кислотой. При одновременном введении этанола (5% раствор на 5% глюкозе: из расчета — 1 мл 96" спирта на 1 кг массы) защитная эффективность препарата увеличивается более чем в два раза. Показано также, что известными антидотными свойствами обладают вещества, содержащие SH-группы, в частности ацетилци-стеин. Данные об использовании препаратов в условиях клиники отсутствуют.
10.21.2!. Ингибиторы цепи дыхательных ферментов
Процесс биологического окисления состоит в отщеплении с помощью соответствующих энзимов (дегидрогеназ) от изоцитрата, а-кетоглюта-рата, сукцината, малата, синтезируемых в цикле трикарбоновых кислот, атомов водорода (Н) и переносе их в форме протонов (Н+) и электронов (е-) по цепи дыхательных ферментов на кислород. Дыхательная цепь — это последовательность связанных друг с другом окислительно-восстановительных пар молекул-переносчиков протонов, электрохимический потенциал которых постепенно понижается (см. рис. 25). При таком «постепенном» окислении организму удается обеспечить очень высокий КПД утилизации химической энергии, запасенной в окисляющихся субстратах (в форме АТФ утилизируется около 42% энергии; около 58% часть i. iuk^mkujiui ни
рассеивается в форме тепла). Естественно, процесс должен идти непрерывно; «выход из строя» любого из звеньев мгновенно приводит к восстановлению всей цепи дыхательных ферментов «выше» выведенного из строя звена. При этом транспорт е- и Н+ по цепи переносчиков прекращается — нарушается процесс синтеза макроэргов.
Токсичность различных веществ рассматриваемой группы определяется их сродством к дыхательным ферментам, особенностями токсикоки-нетики. Наиболее токсичный агент из известных веществ общеядовитого действия — синильная кислота. Это вещество обладает и максимальным быстродействием. Аналогично синильной кислоте действуют на организм многочисленные ее производные, а также сульфиды (сероводород — H2S) и азиды (азид натрия — NaN3).
10.2.2.1. Синильная кислота и ее соединения
Синильная кислота (цианистоводородная кислота) впервые синтезирована шведским ученым Карлом Шееле в 1782 г. Ядовитые свойства кислоты были известны давно. Еще в период наполеоновских войн ею предлагали наполнять артиллерийские снаряды. В качестве отравляющего вещества синильная кислота впервые применена 1 июля 1916 г. на р. Сомме французскими войсками против немецких войск. Выраженный боевой эффект получить не удалось, так как относительная плотность паров HCN по воздуху меньше 1. Попытки утяжелить пары синильной кислоты путем добавления треххлористого мышьяка, хлорного олова и хлороформа также не привели к созданию боевых концентраций ядовитых паров в атмосфере.
Сама кислота и ее соли получили широкое применение в сельском хозяйстве (в качестве средств борьбы с вредителями плодовых деревьев), в промышленности (для извлечения золота и серебра из руд), в химическом синтезе нитрильного каучука, синтетических волокон, пластмасс и т. д.
В качестве ОВ применение маловероятно. Возможно использование производных синильной кислоты в качестве диверсионных агентов.
В настоящее время известны различные группы химических соединений, содержащих группу CN в молекуле. Среди них: нитрилы — R-CN (синильная кислота — HCN, дициан — CN-CN, цианистый калий — KCN, хлорциан — C1-CN, пропионитрил — C3H7-CN и т. д.); изонитри-лы — R-NC+ (фенилизонитрилхлорид); цианаты — R-0-CN (фенилциа-нат); изоцианаты — R-N=C=0 (метилизоцианат, фенилизоцианат); тио-цианаты — R-S-CN (роданистый калий); изотиоцианаты — R-N=C=S (метилизотиоцианат). Наименее токсичными (LD50 более 500 мг/кг) являются представители цианатов и тиоцианатов. Изоцианаты и изотиоцианаты обладают раздражающим и удушающим действием (см. гл. 8. «Отравляющие и высокотоксичные вещества раздражающего действия» и гл. 9. «Отравляющие и высокотоксичные вещества пульмонотоксического действия»). Общеядовитое действие (за счет отщепления в организме от исходного вещества иона CN-) проявляют нитрилы и в меньшей сте-
______ Глава 10. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ОБЩЕЯДОВИТОГО ДЕЙСТВИЯ
пени изонитрилы. Высокой токсичностью отличается, помимо самой синильной кислоты и ее солей, хлорциан, бромциан, а также пропионитрил, лишь в 3-4 раза уступающий по токсичности цианистому калию.
Синильная кислота встречается в растениях в форме гетерогликозидов. Около 2000 видов растений содержат CN-содержащие гликозиды. Например, в виде амигдалина HCN содержится в семенах горького миндаля (2,5-3,5%), в косточках персиков (2-3%), абрикосов и слив (1-1,8%), вишни (0,8%) и др.
Физико-химические свойства. Токсичность
Синильная кислота — бесцветная прозрачная жидкость с запахом горького миндаля (при малых концентрациях). Характерный запах ощущается при концентрации в воздухе 0,009 мг/л. Синильная кислота кипит при +25,7° С, замерзает при -13,4° С. Относительная плотность ее паров по воздуху равна 0,93. Пары синильной кислоты плохо поглощаются активированным углем, но хорошо сорбируются другими пористыми материалами.
При взаимодействии со щелочами HCN образует соли (цианистый калий, цианистый натрий и т. д.), которые по токсичности мало уступают самой синильной кислоте. В водных растворах кислота и ее соли диссоциируют с образованием иона CN-. Синильная кислота является слабой кислотой и может быть вытеснена из своих солей другими, даже самыми слабыми, кислотами (например, угольной). Поэтому соли синильной кислоты необходимо хранить в герметически закрытой посуде.
Отравление синильной кислотой возможно при ингаляции ее паров. LQ50 составляет 2 г • мин/м3. Смертельное отравление солями синильной кислоты возможно при проникновении их в организм с зараженной водой или пищей. При отравлении через рот смертельными дозами для человека являются: HCN - 1 мг/кг; KCN - 2,5 мг/кг; NaCN - 1,8 мг/кг.
Синильная кислота относится к некумулятивным ядам. Это подтверждается тем, что в концентрации менее 0,04 г/м3 HCN не вызывает симптомов интоксикации при длительном (более 6 ч) пребывании человека в зараженной атмосфере.
Токсикокинетика
Основным путем проникновения паров синильной кислоты в организм является ингаляционный. Не исключается возможность проникновения яда через кожу при создании высоких концентраций ее паров в атмосфере. При приеме внутрь кислоты и ее солей всасывание начинается уже в ротовой полости и завершается в желудке. Попав в кровь, вещество быстро диссоциирует и ион CN- распределяется в организме. Благодаря малым размерам он легко преодолевает различные гистогематические барьеры.
Некоторая часть синильной кислоты выделяется из организма в неизмененном виде с выдыхаемым воздухом (поэтому от отравленного пахнет горьким миндалем). Большая часть яда подвергается метаболическим превращениям: частично окисляется через циановую кислоту (HCNO) до
С02 и аммиака, но в основном вступает в реакцию конъюгации с эндогенными содержащими серу веществами с образованием малотоксичных роданистых соединений (CNS-), выделяющихся через почки и со слюной. Как полагают, донорами серы в клетках могут являться тиосульфит-ные ионы (S203_), цистеин, тиосульфаны (RSnSH). Превращение идет при участии тканевых ферментов (главным образом печени и почек) тио-сульфат-тиотрансферазы (роданеза) и р-меркаптопируват-цианидсуль-фотрансферазы. Максимум выделения роданистых соединений из организма отравленного отмечается на вторые сутки.
Основные проявления интоксикации
В результате тканевой гипоксии, развивающейся под влиянием синильной кислоты, в первую очередь нарушаются функции центральной нервной системы. У животных цианиды даже в малых дозах приводят к нарушению условнорефлекторной деятельности. Действуя в больших до- ; зах, вещества вызывают вначале возбуждение центральной нервной сис- i темы, а затем ее угнетение.
При действии сверхвысоких доз токсиканта развивается молниеносная
форма отравления. Пострадавший через несколько секунд после воздей-
ствия теряет сознание. Развиваются судороги. Кровяное давление после i
кратковременного подъема падает. Через несколько минут останавлива-
ются дыхание и сердечная деятельность. ;
При замедленном течении в развитии интоксикации можно выделить
несколько периодов. |
Период начальных явлений характеризуется легким раздражением ели- j
зистых оболочек верхних дыхательных путей и конъюнктивы глаз, непри-
ятным жгуче-горьким вкусом и жжением во рту. Ощущается запах горь- '
кого миндаля. Наблюдаются слюнотечение, тошнота, иногда рвота, голо- j
вокружение, головная боль, боль в области сердца, тахикардия (иногда '
брадикардия), учащение дыхания. Нарушается координация движений, >!
ощущается слабость, возникает чувство страха. Перечисленные признаки 1
появляются почти сразу после воздействия яда. Скрытого периода прак- ;
тически нет. |
Диспноэтический период характеризуется развитием мучительной 1 одышки. Наблюдается резко выраженное увеличение частоты и глубины дыхания. Развивающуюся одышку, видимо, следует рассматривать как компенсаторную реакцию организма на гипоксию. Первоначальное воз- буждение дыхания по мере развития интоксикации сменяется его угнете-' | нием. Дыхание становится неправильным — с коротким вдохом и длительным выдохом. Нарастают боль и чувство стеснения в груди. Причинами ,; этих нарушений являются тканевая гипоксия и истощение энергетиче- ' ских ресурсов в центрах продолговатого мозга. Сознание угнетено. Наблюдаются выраженная брадикардия, расширение зрачков, экзофтальм, рвота. Кожные покровы и слизистые оболочки приобретают розовую окраску. В легких случаях отравление синильной кислотой этими симптомами и ограничивается. Через несколько часов все проявления интоксикации исчезают.
Диспноэтический период сменяется периодом развития судорог. Судороги носят клонико-тонический характер с преобладанием тонического компонента. Сознание утрачивается. Дыхание редкое, но признаков цианоза нет. Кожные покровы и слизистые оболочки розовые. Первоначально наблюдавшиеся замедление сердечного ритма, повышение артериального давления и увеличение минутного объема сердца сменяются падением артериального давления, учащением пульса, его аритмичностью. Развивается острая сердечно-сосудистая недостаточность. Возможна остановка сердца. Корнеальный, зрачковый и другие рефлексы снижены. Тонус мышц значительно повышен.
Вслед за коротким судорожным периодом, если не наступает смерть, развивается паралитический период. Он характеризуется полной потерей чувствительности, исчезновением рефлексов, расслаблением мышц, непроизвольной дефекацией и мочеиспусканием. Дыхание становится редким, поверхностным. Кровяное давление падает. Пульс частый, слабого наполнения, аритмичный. Развивается кома, в которой пострадавший, если не наступает смерть от остановки дыхания и сердечной деятельности, может находиться несколько часов, а иногда и суток. Температура тела у пораженных в паралитическом периоде понижена.
Угнетение тканевого дыхания приводит к изменению клеточного, газового и биохимического составов крови. Содержание в крови эритроцитов увеличивается вследствие рефлекторного сокращения селезенки и выхода клеток из депо. Парциальное давление кислорода в венозной крови возрастает. Цвет венозной крови становится ярко-алым за счет избыточного содержания оксигемоглобина (НЬО). Артерио-венозная разница по кислороду резко уменьшается. Содержание СО2 в крови снижается вследствие меньшего образования и усиленного выделения при гипервентиляции легких. Такая динамика газового состава первоначально приводит к газовому алкалозу, который затем сменяется метаболическим ацидозом. В крови накапливаются недоокисленные продукты обмена: увеличивается содержание молочной кислоты, нарастает содержание ацетоновых тел (ацетон, ацетоуксусная и р-оксимасляная кислоты), повышается содержание сахара (гипергликемия).
Продолжительность течения всего отравления, как и отдельных периодов интоксикации, колеблется в значительных пределах (от нескольких минут до многих часов). Это зависит от количества яда, попавшего в организм, предшествующего состояния организма и других причин.
Последствия интоксикации
Выраженность, характер осложнений и последствий отравления во многом зависят от продолжительности гипоксического состояния, в котором пребывает отравленный. Особенно частыми являются нарушения функций нервной системы. После перенесения острого отравления в течение нескольких недель наблюдаются головные боли, повышенная утомляемость, нарушение координации движений. Речь затруднена. Иногда развиваются параличи и парезы отдельных групп мышц. Возможны нарушения психики.
Наблюдаются стойкие изменения функций сердечно-сосудистой системы вследствие ишемии миокарда.
Нарушения дыхательной системы проявляются функциональной лабильностью дыхательного центра и быстрой его истощаемостью при повышенных нагрузках.
Механизм токсического действия
Цианиды угнетают окислительно-восстановительные процессы в тканях, нарушая последний этап передачи протонов и электронов цепью дыхательных ферментов от окисляемых субстратов на кислород.
Как известно, на этом этапе переносчиками протонов и электронов является цепь цитохромов (цитохромы Ь, Сь С, а и а3). Последовательная передача электронов от одного цитохрома к другому приводит к окислению и восстановлению находящегося в них железа (Fe3+<-> Fe2+). Конечным звеном цепи цитохромов является цитохромоксидаза. Установлено, что энзим включает 4 единицы гема «а» и 2 единицы — «аз». Именно с цитохромоксидазы электроны передаются кислороду, доставляемому к тканям кровью. Установлено, что циан-ионы (CN~), растворенные в крови, достигают тканей, где вступают во взаимодействие с трехвалентной формой железа цитохрома а3 цитохромоксидазы (с Fe2+ цианиды не взаимодействуют). Соединившись с цианидом, цитохромоксидаза утрачивает способность переносить электроны на молекулярный кислород.
Вследствие выхода из строя конечного звена окисления блокируется вся дыхательная цепь и развивается тканевая гипоксия. Кислород с артериальной кровью доставляется к тканям в достаточном количестве, но ими не усваивается и переходит в неизмененном виде в венозное русло. Одновременно нарушаются процессы образования макроэргов (АТФ и др.). Активируется гликолиз, т. е. обмен с аэробного перестраивается на анаэробный.
Помимо непосредственного действия цианидов на ткани, существенную роль в формировании острых симптомов поражения имеет рефлекторный механизм.
Организм располагает специализированными структурами, чувствительность которых к развивающемуся дефициту макроэргов на много превосходит все другие структуры. Наиболее изученным из этих образований является каротидный клубочек (glomus caroticum). Каротидный клубочек расположен в месте бифуркации общей сонной артерии на внутреннюю и наружную. Через него за минуту протекает около 20 мл крови на 1 г ткани (через головной мозг — 0,6 мл). Он состоит из двух типов клеток (по Гессу): I тип — богатые митохондриями гломусные клетки, и II тип — капсулярные клетки. Окончания нерва Геринга, связывающего структуру с ЦНС, пронизывают тела клеток II типа и приходят в соприкосновение с клетками I типа. М. Л. Беленький показал, что рефлексы с гломуса возникают при изменениях р02, рН, других показателей обмена, которые отмечаются уже при минимальных нарушениях условий, необходимых для осуществления процесса окислительного фосфорилирования. Сильнейшим возбуждающим агентом этой структуры является цианистый калий. Был сделан вывод, что основная физиологическая роль каротидного клубочка — сигнализировать ЦНС о надвигающемся нарушении энергетического обмена. Есть предположение, что пусковым звеном формирующихся в гломусе рефлекторных реакций является понижение в клетках I типа уровня АТФ. Понижение уровня АТФ провоцирует выброс гломусными клетками химических веществ, которые и возбуждают окончания нерва Геринга. Хорошо известна чувствительность гломуса к ряду нейроактивных соединений, например, Н-холиномиметикам, ка-техоламинам (Аничков С. В.). Однако известно также и то, что ни одно из них не изменяет чувствительности структуры к цианиду. Действие адекватных раздражителей на гломус сопровождается возбуждением ЦНС, повышением АД, брадикардией, учащением и углублением дыхания, выбросом катехоламинов из надпочечников и, как следствие этого, гипергликемией и т. д. То есть всеми теми реакциями, которые отмечаются на ранних стадиях интоксикации веществами общеядовитого действия. Каким бы образом ни нарушали токсиканты механизмы энергообеспечения, реакция организма во многом однотипна. Проявления интоксикации — сначала это эффекты, формирующиеся как следствие возбуждения и перевозбуждения специализированных регулирующих систем (например, гломуса), а затем — нарушение биоэнергетики непосредственно в тканях, и, прежде всего, быстро реагирующих на дефицит макроэргов (мозг).
Особенности действия галогенпроизводных синильной кислоты
Замещение атома водорода в синильной кислоте галоидами ведет к образованию галоидцианов.
Хлорциан (CICN) как отравляющее вещество впервые был применен в период Первой мировой войны в октябре 1916 г. французскими войсками. Хлорциан — бесцветная прозрачная жидкость, кипит при 12,6° С и замерзает при -6,5° С. Обладает раздражающим запахом (запах хлора). Плотность пара по воздуху 2,1.
Бромциан (BrCN) впервые применен в годы Первой мировой войны (1916) австро-венгерскими войсками в виде смеси: 25% бромциана, 25% бромацетона и 50% бензола. Бромциан — бесцветное или желтое кристаллическое вещество, очень летучее, с резким запахом. Температура кипения 61,3° С, плавления 52° С. Плотность паров по воздуху — 7.
Оба соединения (особенно C1CN) по токсичности близки к синильной кислоте.
Хлорциан и бромциан, действуя подобно HCN, обладают и раздражающим действием. Они вызывают слезотечение, раздражение слизистых оболочек носа, носоглотки, гортани и трахеи. В больших концентрациях могут вызывать токсический отек легких.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников.
Специальные лечебные мероприятия:
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Известные в настоящее время антидоты цианидов либо обладают химическим антагонизмом к токсикантам, либо ускоряют их метаболизм.
Химически связывать ион CN- способны вещества, содержащие альдегидную группу в молекуле (глюкоза), а также препараты кобальта (гид-роксикобаламин, Со-ЭДТА и т. д.). Метгемоглобинообразователи, окисляющие железо гемоглобина до трехвалентного состояния (см. выше), также являются антагонистами цианидов в действии на организм, поскольку циан-ион связывается образующимся при метгемоглобинемии трехвалентным железом пигмента крови. Усиление элиминации цианидов достигается путем назначения веществ, ускоряющих их превращение в роданистые соединения (натрия тиосульфат).
Глюкоза. Антидотный эффект препарата связывают со способностью веществ, содержащих альдегидную группу в молекуле, образовывать с синильной кислотой стойкие малотоксичные соединения — циангидрины:
CN
Н—С—О + HCN >■ Н—С—ОН
I I
R R
Вещество вводят внутривенно в количестве 20-25 мл 25-40% раствора.
Помимо способности связывать токсикант, глюкоза оказывает благоприятное действие на дыхание, функцию сердца и увеличивает диурез.
Препараты, содержащие кобальт. Известно, что кобальт образует прочные связи с циан-ионом. Это дало основание испытать соли металла (хлорид кобальта) в качестве антидота при отравлении цианидами (Ме-рис, 1900). Был получен положительный эффект. Однако неорганические соединения кобальта обладают высокой токсичностью, следовательно малой терапевтической широтой, что делает сомнительной целесообразность их применения в клинической практике. Ситуация изменилась после того, как в опытах на животных была показана эффективность гид-роксикобаламина (витамина В^) для лечения отравлений цианистым калием. Препарат весьма эффективен, мало токсичен, но дорог, что потребовало поиска других соединений. Среди испытанных средств были: ацетат, глюконат-, глутамат-, гистидинат кобальта и кобальтовая соль этилендиаминтетраацетата (ЭДТА). Наименее токсичным и эффективным оказался последний препарат (Paulet, 1952), который и используется в некоторых странах в клинической практике (рис. 31).
СН,СОО^_ /СН2СОО-^
ch^^cJ2coo>Co _____ ^ а^^соо^Со-™
сн^сн.соо +2™ - <^<0*00>o-CN
xCH2COO-^ ^СНгСОО-"^
Рис. 31. Взаимодействие Со-ЭДТА с циан-ионом
В нашей стране препараты кобальта в качестве антидотов не применяются.
Метгемоглобинообразователи. Как и прочие метгемоглобинообразователи, антидоты цианидов окисляют двухвалентное железо гемоглобина до трехвалентного состояния.
Как известно, попав в организм, с железом гемоглобина, находящимся в двухвалентном состоянии, цианиды не взаимодействуют, и, проникнув в ткани, связываются с трехвалентным железом цитохромоксидазы, которая утрачивает при этом свою физиологическую активность. Если отравленному быстро ввести в необходимом количестве метгемоглобино-образователь, то образующийся метгемоглобин (железо трехвалентно) будет вступать в химическое взаимодействие с ядами, связывая их и препятствуя поступлению в ткани. Более того, концентрация свободных токсикантов в плазме крови понизится, и возникнут условия для разрушения обратимой связи циан-иона с цитохромоксидазой (рис. 32).
Образованный комплекс циан-метгемоглобин — соединение непрочное. Через 1-1,5 ч этот комплекс начинает постепенно распадаться. Однако поскольку процесс диссоциации CNMtHb растянут во времени, медленно высвобождающийся циан-ион успевает элиминироваться. Тем не менее при тяжелых интоксикациях возможен рецидив интоксикации.
К числу метгемоглобинообразователей — антидотов цианидов, относят: азотистокислый натрий, амилнитрит, 4-метиламинофенол, 4-этила-минофенол (антициан), метиленовый синий. Следует помнить, что метгемоглобин не способен связываться с кислородом, поэтому необходимо применять строго определенные дозы препаратов, изменяющие не более 25-30% гемоглобина крови.
 |
Наиболее доступным метгемоглобинообразователей является нитрит натрия (NaNC>2). Водные растворы препарата готовятся ex tempore, так как при хранении они нестойки. При оказании помощи отравленным нитрит натрия вводят внутривенно (медленно) в виде 1-2% раствора в объеме 10-20 мл.
Амилнитрит предназначен для оказания первой медицинской помощи. Ампулу с амилнитритом, которая находится в ватно-марлевой обертке, следует раздавить и заложить под маску противогаза. При необходимости его можно применять повторно. В настоящее время антидотные свойства препарата склонны объяснять не столько его способностью к метгемоглобинообразованию (которая выражена слабо), сколько усилением мозгового кровотока, развивающимся в результате сосудорасширяющего действия вещества (см. выше «Нитриты. Органические производные»).
Антициан (диэтиламинофенол) является еще одним веществом, которое можно использовать в качестве антидота. При отравлении синильной кислотой первое введение антициана в виде 20% раствора производится в объеме 1,0 мл внутримышечно или 0,75 мл внутривенно. При внутривенном введении препарат разводят в 10 мл 25-40% раствора глюкозы или 0,85% раствора NaCl. Скорость введения 3 мл в минуту. При необходимости через 30 мин антидот может быть введен повторно в дозе 1,0 мл, но только внутримышечно. Еще через 30 мин можно провести третье введение в той же дозе, если к тому есть показания.
Частичным метгемоглобинообразующим действием обладает метиленовый синий (см. выше). Основное же действие этого препарата заключается в его способности активировать тканевое дыхание. Препарат вводят внутривенно в виде 1% раствора в 25% растворе глюкозы (хромосмон) по 50 мл.
Натрия тиосульфат (Н^^О^). Как уже указывалось, одним из путей превращений цианидов в организме является образование роданистых соединений при взаимодействии с эндогенными содержащими серу веществами. Образующиеся роданиды, выделяющиеся из организма с мочой, примерно в 300 раз менее токсичны, чем цианиды.
Истинный механизм образования роданистых соединений до конца не установлен (рис. 33), но показано, что при введении натрия тиосульфата скорость процесса возрастает в 15—30 раз, что и является обоснованием целесообразности использования вещества в качестве дополнительного антидота (помимо препаратов, рассмотренных выше) при отравлениях цианидами. Препарат вводят внутривенно в виде 30% раствора по 50 мл. Натрия тиосульфат потенцирует действие других антидотов. Оказание неотложной помощи целесообразно начинать с метгемоглобинообразователей, а затем переходить на введение других препаратов.
1) cn"+s2o3"_ ---- *■ serosa,--
роданеза тиосульфат
2) CN~+ HSC^COCOOH ^ SCN-+ СН3СОСООН
меркаптопируват сульфотрансфераза
3) CN~+ [RSy—SH] —^-*- SCN~+ [RS^—SH]
[RSy—SH] — тиосульфан
Рис. 33. Предполагаемые механизмы образования роданистых соединений в организме отравленных цианидами
В процессе оказания помощи отравленным предусматривается применение и других средств патогенетической и симптоматической терапии. Положительный эффект оказывает гипербарическая оксигенация.
10.2.3. Разобщители тканевого дыхания
Известны вещества, способные разобщать процессы биологического окисления и фосфорилирования. Такими свойствами обладают, как правило, липофильные соединения, содержащие фенольную группировку в молекуле и являющиеся слабыми органическими кислотами. Наиболее известными и широко используемыми в хозяйственной деятельности являются 2,4-динитрофенол (ДНФ), динитро-о-крезол (ДНОК), пента-хлорфенол (рис. 34). При авариях на промышленных объектах и других чрезвычайных ситуациях эти вещества могут стать причиной массового поражения людей.
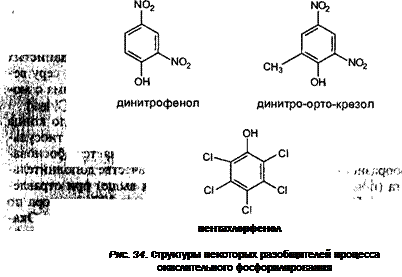
In vitro «разобщители» стимулируют скорость потребления кислорода митохондриями и индуцируют активность АТФазы. In vivo в результате их действия значительно активируются процесс биологического окисления и потребление кислорода тканями, однако содержание АТФ и других макроэргов в клетках при этом снижается. Развиваются типичные для отравления веществами общеядовитого действия признаки интоксикации (см. выше). Образующаяся в ходе окисления субстратов энергия рассеивается в форме тепла, температура тела отравленного резко повышается, что является характерным признаком острого отравления «разобщителями».
10.2.3.1. Динитро-орто-крезол Физико-химические свойства. Токсичность
Динитро-орто-крезол — кристаллическое вещество, относительно легко диспергирующееся в воздухе. Температура плавления 85° С. Растворяется в органических растворителях, например, бензоле, спирте, хуже — в воде. При заражении территории динитро-орто-крезолом возможно его испарение. Вещество применяется для борьбы с вредителями сельского хозяйства (входит в состав инсектицидов динозал, дитрол, крезонит и т. д.).
Описаны случаи смертельного поражения людей, находившихся в атмосфере, зараженной аэрозолем ДНОК в концентрации около 3 г/м3. При пероральном приеме 3—5 мг/кг массы тела развиваются признаки острого отравления.
Токси коки нети ка
Вещество способно проникать в организм ингаляционно (в виде пара и аэрозоля), через желудочно-кишечный тракт с зараженной водой и продовольствием и через неповрежденную кожу. Попав в кровь, распределяется в организме, достаточно легко преодолевая гистогематические барьеры, в том числе и гематоэнцефалический. В печени метаболизирует с образованием нетоксичного амино-орто-крезола.
Основные проявления интоксикации
При контакте вызывает легкое раздражение кожи, слизистой оболочки желудочно-кишечного тракта, глаз или дыхательных путей (в зависимости от пути поступления в организм). Выделяют легкую, средней степени тяжести и тяжелую формы отравления. При легкой интоксикации примерно через час после воздействия развиваются признаки общего недомогания: головная боль, вялость, понижение работоспособности, головокружение, тошнота. Характерными проявлениями интоксикации являются выраженная потливость и повышение температуры тела до 38° С. Эти нарушения сохраняются в течение суток. При интоксикации средней степени тяжести к описанным явлениям присоединяются одышка, чувство стеснения в груди, учащение пульса. Появляются чувство тревоги, беспокойство, бессонница. Температура тела повышается до 39° С. При тяжелом отравлении клиническая картина развивается довольно быстро. Пострадавший испытывает чувство жажды. Отмечаются выраженная одышка, нарушение сердечного ритма, повышение артериального давления. Появляется цианоз кожных покровов. Температура тела повышается до 40—42° С («тепловой взрыв»). Сознание утрачено, зрачки расширены, развивается судорожный синдром. Смерть может наступить от остановки дыхания или сердечной деятельности.
Механизм токсического действия
Как указывалось, окислительное фосфорилирование — это процесс, при котором энергия, выделяющаяся при постепенном окислении субстратов, запасается в форме макроэргических соединений (главным образом — АТФ). В настоящее время имеется несколько гипотез о механизме поддержания процесса образования АТФ в митохондриях за счет окислительно-восстановительных реакций. Одна из них, химико-осмотическая, предложена Нобелевским лауреатом П. Митчелом. Согласно этой гипотезе, движущей силой процесса фосфорилирования АДФ до АТФ является перманентный протонный градиент (Н+) по обе стороны мембраны митохондрии, поддерживаемый движением электронов и ионов водорода по цепи дыхательных ферментов. «Откачка» протонов из митохондрий за пределы мембраны обеспечивает течение реакции фосфорилирования, иными словами, энергетически обеспечивает сдвиг вправо следующего равновесного процесса:
АДФ + Н3Р04 <-> АТФ + Н+ + ОН-.
 |
In vitro без притока энергии эта реакция практически полностью смещена в сторону образования АДФ (АТФ в растворе немедленно подвергается гидролизу).
По существующим представлениям, «разобщители», будучи липофи-льными соединениями, накапливаются в митохондриальной мембране и за счет относительно легко диссоциирующей группы -ОН облегчают трансмембранный перенос протонов в соответствии с градиентом их концентрации. Вследствие такого повреждения мембраны и увеличения ее проницаемости для протонов, Н+ устремляются во внутренние среды митохондрий, градиент протонов исчезает, синтез макроэргов прекращается. При этом вся энергия, запасенная в субстратах, при их биологическом окислении рассеивается в форме тепла.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Оказание помощи пострадавшим направлено на удаление вещества с кожных покровов, из желудочно-кишечного тракта, борьбу с гипертермией, обезвоживанием, нарушением водно-электролитного баланса, профилактику дыхательной и сердечно-сосудистой недостаточности. Помощь оказывается в соответствии с общими принципами (см. 6.4. «Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях»). Специфические противоядия отсутствуют.
Глава 11. ОТРАВЛЯЮЩИЕ
И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА
ЦИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ
3. Галогенированные полициклические ароматические углеводороды:
• галогенированные диоксины;
• галогенированные бензофураны;
• галогенированные бифенилы и др.
4. Сложные гетероциклические соединения:
• афлатоксины;
• трихотеценовые микотоксины;
• аманитин и др.
5. Белковые токсины:
• рицин и др.
Для военной токсикологии особый интерес представляют вещества, способные при экстремальных ситуациях вызывать массовые санитарные потери. К числу таковых из группы цитотоксикантов относятся прежде всего боевые отравляющие вещества кожно-нарывного действия (иприт, азотистый иприт, люизит), некоторые промышленные агенты (соединения мышьяка, ртути и т. д.), фитотоксиканты и пестициды, и их токсичные примеси (диоксин и диоксиноподобные соединения), а также некоторые другие соединения.
Общим в действии ОВТВ этой группы на организм являются:
• медленное, постепенное развития острой интоксикаций (продолжительный скрытый период, постепенное развитие токсического процесса);
• изменения со стороны всех органов и тканей (как на месте аппликации, так и после резорбции), с которыми токсикант или продукты его метаболизма в силу особенностей токсикокинетики способны непосредственно взаимодействовать;
• основные формы нарушений со стороны органов и систем, вовлеченных в токсический процесс: воспалительно-некротические изменения, угнетение процессов клеточного деления, глубокие функциональные расстройства внутренних органов.
Вместе с тем поражения различными токсикантами имеют и свою специфику, обусловленную особенностями основного механизма их токсического действия. Основные ОВТВ рассматриваемого класса в соответствии с особенностями механизма действия можно отнести к одной из следующих групп:
1. Ингибиторы синтеза белка и клеточного деления.
1.1. Образующие аддукты нуклеиновых кислот:
« сернистый иприт, азотистый иприт.
1.2. Не образующие аддукты нуклеиновых кислот:
■ рицин.
2. Тиоловые яды:
■ мышьяк, люизит.
3. Токсичные модификаторы пластического обмена:
■ галогенированные диоксины, бифенилы.
11.1. Ингибиторы синтеза белка и клеточного деления
Процессы синтеза белка и клеточного деления необыкновенно сложны. Механизмы, посредством которых токсиканты способны воздействовать на них — многообразны (см. 5.2. «Общие механизмы цитотоксичности»). При этом условно вещества, нарушающие процессы, можно подразделить на две группы. Представители первой группы взаимодействуют с нуклеиновыми кислотами ядра клетки (образуют аддукты), повреждая ее генетический код и нарушая механизмы репликации. Поражение такими веществами сопровождается повреждением преимущественно делящихся клеток, нарушением пролиферации клеточных элементов. Соединения другой группы действуют на этапах транскрипции и трансляции генетической информации. Поэтому основным видом нарушения является угнетение синтеза белка. Наиболее чувствительными к этим ядам являются органы с высокой интенсивностью пластического обмена.
11.1.1. Ингибиторы синтеза белка
и клеточного деления, образующие '
аддукты ДНК и РНК
К числу веществ рассматриваемой группы относятся яды, образующие при интоксикациях прочные ковалентные связи с азотистыми основаниями нуклеиновых кислот. Среди ОВТВ — это прежде всего сернистый и азотистый иприты и их аналоги. При изучении нуклеиновых кислот, выделяемых из поврежденных этими токсикантами клеток, в пробах выявляются комплексы остатка молекулы токсиканта и пуриновых (пирими-диновых) оснований. Такие комплексы получили название аддуктов. При взаимодействии с нуклеиновыми кислотами ипритов (сернистого, азотистого) и их аналогов образуются аддукты, содержащие алкильные радикалы (фрагменты молекулы яда, представляющие собой алкильную группу). По этой причине вещества называют также алкилирующими агентами. Помимо нуклеиновых кислот алкилирующие агенты способны взаимодействовать с белками, пептидами и молекулами иного строения. В этой связи механизм их токсического действия сложен и не ограничивается повреждением только генетического аппарата клеток.
11.1.1.1. Иприты
Один из первых представителей галогенированных тиоэфиров, 2,2-дих-лордиэтилсульфид, был впервые синтезирован в 1822 г. Депре. В чистом виде соединение было выделено и изучено в 1886 г. Виктором Мейером в Геттингене. Им же дано и первое описание некоторых сторон пагубного действия этого вещества на человека и животных, выявившегося в про-
цессе работы с соединением. Опыты проводились при непосредственном участии практиканта русского химика Н. Д. Зелинского, который получил сильное поражение токсикантом, что послужило поводом для более детального изучения его токсических свойств.
В ходе Первой мировой войны, в июле 1917 г. возле города Ипр английские войска были обстреляны немецкими минами, содержащими 2,2-дихлордиэтилсульфид. ОВ, названное «ипритом», заражало местность, быстро проникало через одежду, вызывало поражение кожи. Так в историю войны вошел еще один тип отравляющих веществ, получивших название ОВ «кожно-нарывного действия». Позже ОВ использовали итальянцы в ходе итало-абиссинской войны (1936 г.). Во время Второй мировой войны (1943) его применяла в Китае японская армия. В 80-е гг. XX в. вещество вновь использовалось в качестве ОВ в ходе Ирако-Иран-ского военного конфликта. Из изученных галогенированных тиоэфиров иприт является самым токсичным агентом.
В 1934—35 гг. Уорд исследовал хлорированные этиламины и среди третичных производных этого ряда обнаружил новый вид веществ, вызывающих воспалительные процессы в коже. В результате исследований были получены данные, указывающие на возможность создания на основе органических соединений азота новой группы ОВ. Во время Второй мировой войны в Германии третичные хлорэтиламины синтезировали в производственном масштабе и сохраняли в автоцистернах, предполагая использовать для заражения местности. Обнаруженные в 1945 г. в Германии запасы 2,2,2-трихлортриэтиламина составляли около 2000 тонн. Из-за сходства молекулярной структуры трихлортриэтиламина с ипритом (рис. 35) и аналогичного физиологического действия вещество получило название «азотистый иприт».
у CHjCHjCI у CH2Cri,CI
S N— СНгСНгС!
^CHCHjCI CH2CH2CI
2,2-дихлордиэтилсульфид 2,2,2-трихлортризтиламин
(иприт) (азотистый иприт)
Рис. 35. Структуры сернистого и азотистого ипритов
Позже были изучены и аналоги азотистого иприта: метил-дихлорэти-ламин, этил-дихлорэтиламин и т. д. Эти соединения обладали токсичностью близкой токсичности исходного вещества. В качестве ОВ в ходе боевых действий трихлорэтиламин и его аналоги не использовались.
В соответствии с Конвенцией о запрещении химического оружия (1993) запасы сернистого и азотистого иприта странами, имеющими вещества на снабжении армий, должны быть уничтожены. Однако опасность поражения людей этими соединениями или их аналогами сохраняется. Так, на основе хлорэтиламинов созданы высокоэффективные цитостати-ки — лекарственные препараты, применяемые для лечения опухолей (цик-лофосфамид, мехлорэтамин, хлорамбуцил, мелфалан) и других форм патологии. В настоящее время эти вещества производятся в большом количестве и достаточно широко применяются в клинической практике. Многочисленные серо-, азот- и кислородсодержащие органические соединения с близким механизмом токсического действия широко используют в промышленности (этиленимин, этиленоксид и т. д.). Широкое применение алкилирующих агентов в хозяйственной деятельности, их доступность делают возможным применение веществ с террористическими целями.
Поскольку свойства, биологическая активность сернистого и азотистого ипритов и их аналогов во многом совпадают, токсикологическую характеристику веществ целесообразно представить на примере табельного ОВ — сернистого иприта, с указанием особенностей свойств наиболее токсичного представителя галогеналкиламинов — азотистого иприта.
Физико-химические свойства. Токсичность
Основные свойства сернистого и азотистого ипритов представлены в табл. 32 и 33.

Таблица 32

Сернистый иприт — тяжелая маслянистая жидкость. В чистом виде бесцветная, почти без запаха. В неочищенном виде — темного цвета (в качестве примесей содержит 17—18% сульфидов). При низких концентрациях обладает запахом, напоминающим запах горчицы или чеснока (отсюда еще одно название ОВ — «горчичный газ»). В воде плохо растворим. Хорошо растворяется в органических растворителях. Растворяется в других ОВ и сам растворяет их. Легко впитывается в пористые материалы, резину, не теряя при этом токсичности.
Азотистый иприт — маслянистая, слегка темная или бесцветная жидкость, легко растворяемая в органических растворителях, но практически не растворяющаяся в воде.
Давление насыщенного пара ипритов — незначительное; возрастает с увеличением температуры. Поэтому в обычных условиях иприты испаряются медленно, создавая при заражении местности стойкий очаг. Основное боевое состояние сернистого иприта — пары и капли.
Связь алкильных радикалов с атомами хлора в молекулах токсикантов может быть разрушена путем гидролиза. Конечными продуктам» гидролиза являются нетоксичные соединения, поэтому реакция может быть использована для дегазации зараженных объектов. Гидролизу подвергается только растворившееся количество сернистого и азотистого ипритов. Поскольку растворимость токсикантов крайне низка, находящиеся в воде ОВ долго сохраняют свою токсичность. Полный гидролиз возможен лишь в условиях очень большого избытка воды (1 г сернистого иприта на 2000 г воды). Процесс гидролиза можно ускорить нагреванием зараженной воды и добавлением разбавленных щелочей.
В организме вещества также подвергаются дегалогенированию. При этом возможно образование промежуточных продуктов (сульфоний-ка-тиона и иммоний-катиона), с действием которых на молекулы-мишени связывают механизм токсического действия ипритов.
Сернистый иприт подвергается окислению, при этом последовательно образуются токсичные 2,2-дихлордиэтилсульфоксид (1) и 2,2-дихлор-диэтилсульфон (2):
/СН£Н£ О /CHjCHjCI
О—S
^СНгСНгС! сН;>СН2С1
(1) (2)
Только глубокое окисление приводит к потере токсических свойств и полному разрушению молекулы иприта с образованием серной кислоты, хлористого водорода, диоксида углерода и воды.
При хлорировании ипритов в водной и безводной среде их молекулы разрушаются, что сопровождается потерей токсических свойств.
Токсикокинетика
Иприты способны проникать в организм, вызывая при этом поражение, любым путем: ингаляционно (в форме паров и аэрозоля), через неповрежденную кожу, раневую и ожоговую поверхности (в капельно-жид-
гоо
кой форме) и через рот с зараженной водой и продовольствием. Контакт с веществами не сопровождается неприятными ощущениями (немой контакт).
После поступления в кровь вещества быстро распределяются в организме, легко преодолевая гистогематические барьеры, проникают в клетки. Метаболизм веществ проходит с большой скоростью. Так, в экспериментах на кроликах показано, что 90% сернистого иприта, меченного по сере (35S), исчезает из крови в течение 20 мин, а уже через 10 мин радиоактивность обнаруживается в моче. Наибольшая радиоактивность определяется в органах, выполняющих экскреторную функцию (почки, легкие, печень). В моче животных после внутривенного введения иприта (35S) обнаруживаются продукты его превращения (гидролиза и окисления молекулы). Метаболизм веществ осуществляется при участии тканевых микросомальных ферментов. Поскольку в процессе метаболизма ипри-тов образуются токсичные промежуточные продукты (сульфоний, иммо-ний катионы и др.), индукция микросомальных ферментов, вызываемая в эксперименте путем назначения специальных средств (производные барбитуровой кислоты и др.), сопровождается усилением их токсичности.
Основные проявления интоксикации
Поражение ипритом складывается из местного и резорбтивного действия яда. Токсический процесс развивается медленно, после скрытого периода, продолжительность которого — от часа до нескольких суток. Местное действие приводит к развитию симптомов воспаления покровных тканей (гиперемия, отек, боль и нарушение функции). Резорбтивное действие характеризуется угнетением кроветворения, центральной нервной системы, нарушением кровообращения, пищеварения, всех видов обмена веществ, терморегуляции и т. д. Подавляется иммунная система организма, и поэтому отмечается наклонность к присоединению вторичной инфекции. У иприта выражено кумулятивное действие. Более того, в экспериментах на животных и в ходе наблюдений за отравленными людьми установлено, что контакт с этим ядом вызывает сенсибилизацию к нему. Наиболее опасным является ингаляционное поражение парами или аэрозолем иприта. Именно при данном способе воздействия весьма вероятны тяжелые и крайне тяжелые формы поражения со смертельным исходом. Также высока токсичность вещества при поступлении его в организм с зараженной водой или пищей. Хотя вещество прекрасно всасывается через кожные покровы и вызывает их глубокое повреждение, вероятность летальных исходов при данном способе воздействия наименьшая.
Поражение органов дыхания
Поражение органов дыхания происходит при ингаляции паров иприта. Непосредственно в момент воздействия на слизистую оболочку дыхательных путей ОВ не оказывает раздражающего действия. Лишь при очень высоких концентрациях в момент контакта у пострадавшего может появиться позыв к чиханию. По прошествии скрытого периода, который продолжается от 2 до 6 ч — при тяжелых поражениях и поражениях средней тяжести и более 12 ч — при легких формах отравления, появляются признаки воспаления дыхательных путей. Вначале они развиваются в верхних, а затем и в более глубоких отделах. Начало поражения характеризуется появлением насморка (токсический ринит), затруднением при глотании (фарингит), саднением за грудиной, осиплостью голоса, а иногда и потерей его (афония), т. е. признаками ларингита. В легких случаях поражение этим ограничивается и острый ринофаринголарингит через 10-12 дней проходит.
Поражение средней степени тяжести характеризуется проявлениями трахеобронхита: мучительным кашлем, вначале сухим, а затем с выделением гнойной мокроты, болями за грудиной. Обычно такое состояние сопровождается ощущением недомогания и повышением температуры тела до 39° С. Выздоровление наступает через 30-40 дней.
При тяжелом поражении симптомы воспалительного процесса в дыхательных путях отчетливо выражены уже на вторые сутки. При кашле отходит обильная слизисто-гнойная мокрота, в которой могут быть обнаружены пленчатые образования. Это так называемые псевдомембраны, состоящие из некротизированной слизистой оболочки, фибрина и форменных элементов крови. Через некоторое время, как правило, присоединяется вторичная инфекция. Температура тела резко повышается. Иногда уже на вторые сутки заболевания может наступить смерть пораженного. Причина гибели (помимо общетоксического действия иприта) — развивающаяся бронхопневмония, перерастающая в гангрену легких. При вскрытии умерших людей выявляются гиперемия, изъязвление и некроз слизистой оболочки на всем протяжении дыхательных путей: в носовой полости, гортани, трахее, крупных бронхах. Слизистая оболочка грязно-серого цвета, пропитана фибрином и лейкоцитами, рыхло связана с подслизистой. В просвете мелких бронхов — гной, в легких — очаги бронхопневмонии, чередующиеся с эмфизематозными участками и участками ателектаза. При гибели в поздние сроки можно увидеть участки гнойного лизиса легочной ткани (абсцесс легких).
Даже' при благоприятном исходе поражение дыхательной системы ипритом не заканчивается полным выздоровлением. У перенесших отравление наблюдаются хронические воспалительные процессы в дыхательных путях (преимущественно гипертрофического типа), рецидивирующие бронхопневмонии, бронхоэктатическая болезнь, эмфизема легких. Появляется предрасположенность к туберкулезу. Будучи, как и другие алки-лирующие агенты, канцерогеном, иприт существенно увеличивает вероятность заболевания раком легких у лиц, перенесших отравление.
Поражение глаз
Поражение глаз наблюдается при воздействии как парообразным, так и капельно-жидким ипритом. Глаза чрезвычайно чувствительны к токсиканту. Минимально действующая концентрация яда — 0,005 г/м3. При действии вещества в более высоких концентрациях развивается конъюнктивит. После скрытого периода (4-5 ч) проявляются явления раздражения: ощущение песка в глазах, чувство жжения и рези, светобоязнь, слезотечение, гиперемия и отек слизистой оболочки век. Патологический процесс полностью разрешается через 6—15 дней.
При воздействии вещества в более высокой концентрации или при длительной экспозиции в патологический процесс вовлекается роговая оболочка: все указанные выше симптомы выражены более интенсивно, отек усиливается, распространяется на кожу век, конъюнктива гипереми-рована и окружает роговицу в виде отечного валика. Развивается помутнение роговицы, носящее поверхностный характер. Происходит воспаление мейбомиевых желез, края век склеиваются, образуются корочки. Формируются условия для развития вторичной инфекции. Наивысшего развития процесс достигает на 3—4-е сут: появляются признаки гнойного кератоконъюнктивита. В дальнейшем острые явления постепенно стихают. Поражения парообразным ипритом обычно достигают средней тяжести и локализуются в переднем отделе глаза. Прогноз, как правило, благоприятный, однако выздоровление может затянуться на 2—3 мес.
Картина тяжелого поражения наблюдается при попадании жидкого иприта в глаз. Процесс протекает первоначально по типу серозного, а затем гнойно-некротического и гнойно-геморрагического воспаления. Скрытый период действия яда не превышает 3 ч. Процесс развивается относительно быстро, а выраженность уже описанных ранее изменений существенно выше. Помутнение роговицы захватывает глубокие ее слои, воспаление приобретает характер паренхиматозного кератита. Края плотно сомкнутых век склеиваются. Обильно отделяемый секрет застаивается в конъюнктивальном мешке. С 3—4-х сут присоединяется вторичная инфекция. Развивается язвенный блефарит. В случаях тяжелых поражений с присоединением вторичной инфекции возможно глубокое изъязвление роговицы, вплоть до ее прободения. В воспалительный процесс тогда вовлекаются все среды глаза, развивается панофтальмит, в результате которого наступает гибель глаза. Разрушение ипритом окружающих глаз кожных покровов и других мягких тканей с последующим их рубцеванием также может привести к инвалидизации.
Повторное поражение глаз ипритом приводит к стойкой сенсибилизации. После перенесенного поражения глаз даже через несколько лет не может считаться полностью излеченным. Его сопротивляемость к разным патологическим агентам снижена, что способствует возникновению различных патологических состояний и рецидивирующих конъюнктивитов.
Поражение кожи
Поражение кожи развивается при воздействии ипритом как в парообразном, так и капельно-жидком состоянии. Интенсивность поражения зависит от многих условий, наибольшее значение имеют агрегатное состояние токсиканта, продолжительность воздействия, температура и влажность воздуха, область поверхности кожи, подвергшейся заражению и т. д.
Основная масса яда всасывается через протоки потовых и сальных желез, волосяных фолликулов, но клеточные и соединительно-тканные элементы кожи также проходимы для иприта. Наиболее чувствительны места с нежной кожей и большим содержанием потовых протоков (область гениталий, подмышек, внутренняя поверхность бедер). Выраженные поражения кожи возникают и в местах плотного прилегания одежды (пояс, воротник).
Симптомы поражения кожи появляются после скрытого периода, продолжительность которого от 5 до 15 ч — в случае действия парообразного иприта и 4—6 ч — при попадании жидкого иприта. При воздействии паров ОВ развивающееся поражение носит распространенный характер, но менее выражено, чем поражение жидким ядом, площадь которого ограничена местом растекания капли по поверхности кожи.
В течении поражений кожи выделяют сменяющие друг друга стадии (они же степени тяжести поражения):
I — эритематозная (появление разлитой эритемы, не исчезаю-
щей при надавливании);
II — буллезная (появление мелких пузырей, сливающихся затем
в один);
III — язвенно-некротическая (появление изъязвлений на месте
пузыря).
Четко все три стадии бывают выражены лишь в случае воздействия иприта в капельно-жидком состоянии. При поражении парообразным веществом может наблюдаться развитие только эритемы, которая через неделю пропадает, а на ее месте длительное время сохраняется выраженная пигментация.
Эритема развивается на отечных тканях, сопровождается болезненностью, ощущением жара и зуда. Появляющиеся вслед за нею мелкие пузыри вначале располагаются по краям эритемы («жемчужное ожерелье»), а затем сливаются в крупные пузыри. При буллезном поражении выделяют поверхностную и глубокую формы. При поверхностной форме процесс локализуется только в эпидермисе, сопровождается его отторжением и обнажением язвенной поверхности, представляющей собой верхние слои дермы. При глубокой форме поражения в патологический процесс вовлекаются как эпидермис, так и слой дермы.
В III стадии формируются чрезвычайно болезненные язвенно-некротические изменения кожи. Поражение характеризуется вялостью репара-тивных процессов. Развивается состояние парабиоза тканей. Ипритные язвы обычно осложняются присоединением вторичной инфекции. Заживление язв происходит крайне медленно, иногда до 2 мес. На месте язвы обычно остается рубец, окруженный пигментированной кожей.
У отравленных долгое время сохраняется повышенная чувствительность к иприту: при повторных кожных поражениях местная реакция на участке непосредственного нанесения яда значительно усиливается, а на участках бывших ранее поражений вновь формируются патологические изменения (явление реинфламмации).
Поражение желудочно-кишечного тракта
Поражение желудочно-кишечного тракта наблюдается при попадании иприта внутрь с зараженной водой или пищей, при заглатывании зараженного ипритом содержимого ротовой полости — как сопутствующее при тяжелых формах интоксикации, возникающих при любом способе поступления ОВ в организм (ингаляционно, через кожу и т. д.). Не исключено, что поражение стенки кишечника обусловлено выведением из организма токсичных промежуточных продуктов метаболизма вещества.
Токсические дозы иприта для человека и экспериментальных животных при пищевых формах отравления — 0,5-10 мг/кг. Попадание иприта в организм через желудочно-кишечный тракт (в действующих дозах) вызывает, как правило, тяжелую форму отравления, поскольку всасывание ОВ здесь происходит чрезвычайно интенсивно. Быстро развиваются, помимо местных, явления общерезорбтивного действия яда. Изолированное поражение пищеварительного тракта практически никогда не встречается. Как правило, при этом страдают органы дыхания за счет ингаляции воздуха, проходящего через зараженную ротовую полость, и кожа вокруг рта.
Скрытый период действия яда составляет 1—3 ч. К концу периода появляются саливация, тошнота, рвота, боль в животе. Пораженный становится вялым, аппетит отсутствует, отмечается расстройство стула. При поступлении внутрь иприта в малых дозах поражение дальше желудка не распространяется. При этом явления отравления ограничиваются описанными выше признаками. Выздоровление наступает в течение недели.
При приеме внутрь больших доз вещества развивается тяжелое поражение всех отделов пищеварительного тракта. К указанным выше симптомам присоединяются признаки, обусловленные некротическим изменением слизистой оболочки рта, глотки, кишечника. Отмечаются болезненность по всему животу, частые поносы жидкими дегтеобразными массами, что указывает на геморрагический характер развивающегося патологического процесса.
К числу последствий тяжелого пищевого отравления ипритом относятся рубцовые изменения стенки пищевода и желудка, стенозирование пищевода.
Резорбтивное действие
При всасывании иприта во внутренние среды организма развиваются симптомы общей интоксикации, свидетельствующие об универсальном характере повреждающего действия яда. Ведущими являются изменения со стороны системы крови, нервной системы, сердечно-сосудистой системы и обмена веществ.
Изменения в крови при отравлении ипритом обусловлены, с одной стороны, непосредственным действием на клетки костного мозга и зрелые форменные элементы, с другой — общим развитием патологического процесса в организме отравленного. При отравлениях легкой и средней степени тяжести изменения в крови бывают непостоянны и выражены
2Q6
слабо. В случае тяжелых отравлений изменения постоянны и носят закономерный характер. Динамика нарушений со стороны системы крови напоминает картину, наблюдаемую при поражении человека и экспериментальных животных ионизирующим излучением, поэтому иприты (как сернистый, так и азотистый) иногда называют «радиомиметиками» (т. е. воспроизводящими эффекты действия радиации).
При отравлении большими дозами иприта изменения крови появляются уже в первые часы интоксикации (2-4 ч). Со стороны красной крови — некоторое увеличение числа эритроцитов, вследствие развивающегося сгущения крови (гемолиз не развивается), со стороны белой крови — гиперлейкоцитоз с нейтрофильным сдвигом влево до палочкоядерных или юных форм. К концу первых суток существенно увеличивается количество сегментоядерных нейтрофилов в крови. Количество эозинофилов и базофилов в это время снижается (вплоть до полного исчезновения). Одновременно уменьшается количество моноцитов и лимфоцитов (мо-ноцито- и лимфопения). Начиная со вторых суток сгущение крови прекращается, количество эритроцитов в крови уменьшается. Анемизация в дальнейшем чрезвычайно медленно прогрессирует. Лейкопения со вторых суток быстро нарастает и в крайне тяжелых случаях (на 4-5-е сут после отравления) переходит в алейкию. Одновременно развивается тром-боцитопения. В ядрах палочкоядерных и сегментоядерных нейтрофилов, циркулирующих в крови, наблюдаются признаки дегенеративных изменений: пикноз ядра, хроматинолиз, гиперсегментоз, вакуолизация, фрагментация. Наличие выраженной лейкопении при отравлении является плохим прогностическим признаком и при крайне тяжелом отравлении сохраняется до наступления смерти. Если смертельный исход не наступил, отмечается довольно быстрое увеличение числа лейкоцитов в крови. Как в клинике, так и в эксперименте показано, что при отравлении ип-ритами (а особенно азотистым ипритом) резко нарушаются процессы размножения и созревания клеток костного мозга. Размножение клеток приостанавливается на стадии промиелоцитов. Отношение количества промиелоцитов, миелоцитов и юных форм к количеству палочко- и сегментоядерных лейкоцитов (индекс созревания гранулоцитов — в норме 0,8-0,9) достигает 38. Количество миелоидных элементов в пробах костного мозга резко уменьшается, значительно увеличивается количество ретикуло-эндотелиальных клеток (аплазия костного мозга). Развивается атрофия лимфоидной ткани. В селезенке и лимфатических узлах — резко выраженный склероз. Важнейшим результатом поражения системы крови является мощное иммуносупрессивное действие ипритов, подавляющее как клеточный, так и гуморальный компонент иммунной системы организма.
При выздоровлении сначала наступает регенерация элементов костного мозга, а затем лимфоидной ткани. Относительно быстро нормализуется количество лейкоцитов в периферической крови, реактивность ге-мопоэза восстанавливается полностью.
При затяжном течении несмертельного поражения ипритом изменение гемограммы в целом соответствует описанным выше, но имеет свои
особенности. Так, в поздние сроки болезни довольно отчетливо проявляются признаки анемии, нарушения со стороны белой крови непостоянны и во многом определяются особенностями течения патологии других органов и систем.
Нарушения со стороны нервной системы обусловлены непосредственным действием на ее структурные элементы самого иприта и токсичных продуктов его метаболизма, биологически активных веществ, поступающих в кровь при деструкции клеточных элементов поврежденных ипритом тканей, а также патологической импульсацией из очагов альтерации покровных тканей. Выраженность нарушений определяется степенью тяжести интоксикации. К числу ранних проявлений относятся общая вялость пораженных, головная боль, головокружение, сонливость, апатия. Степень угнетения ЦНС пропорциональна дозе попавшего в организм иприта. Поражения средней степени тяжести и длительно текущая тяжелая интоксикация проходят на фоне выраженного угнетения возбудимости и лабильности нервной ткани. У лиц, перенесших острое отравление, регрессия астении проходит медленно, пораженные надолго лишаются возможности заниматься полноценным умственным и физическим трудом (Ю. В. Другое). Н. Н. Савицкий и др. наблюдали у пораженных развитие парезов, параличей, невритов, стойкое нарушение памяти, затруднение мышления, расстройство сна и т. д.
При попадании в организм очень больших количеств сернистого иприта (летальные поражения) и при отравлении (в эксперименте на животных) азотистым ипритом выявляется психомоторное возбуждение, судорожное действие ядов. Первоначально наблюдается сокращение отдельных групп мышц, начиная с жевательной мускулатуры, мышц головы и шеи. Затем в процесс вовлекаются мышцы туловища и конечностей. Приступы носят характер эпилептических припадков, но с преобладанием клонических компонентов. Азотистый иприт обладает значительно более выраженным возбуждающим действием на ЦНС, чем сернистый. Одновременно с поражением центральной нервной системы выявляются признаки действия вещества на вегетативную нервную систему и прежде всего на парасимпатический ее отдел. Эффекты развиваются в две стадии. Сначала наблюдаются признаки возбуждения холинергических структур (саливация, слезотечение, брадикардия и др.), затем проявляется достаточно стойкое холинолитическое действие ядов. Азотистый иприт, кроме того, обладает слабым симпатолитическим и антигистаминным действием.
В основе действия ипритов на нервную ткань лежат сложные механизмы, обусловленные отчасти их цитотоксическим действием на нейроны (характерны вакуолизация и лизис нервных клеток, пикноз ядер — признаки токсической энцефалопатии), отчасти синаптической активностью. Так, в эксперименте показано мускарино- и никотиноподобное действие ядов. У веществ выявляется антихолинэстеразная активность и способность к прямому взаимодействию с холинорецепторами (сначала их возбуждение, а затем блокада).
Расстройства сердечно-сосудистой системы проявляются рано наступающим снижением артериального давления, вследствие расширения периферических сосудов. При тяжелых интоксикациях (в эксперименте) кровяное давление начинает литически падать до низких цифр; острая гибель животных происходит на фоне развившегося коллапса. По данным А. И. Черкеса, в основе эффекта лежит парализующее влияние иприта на сосуды (паралич прекапилляров). Действие ипритов на сердце обусловлено влиянием веществ на систему блуждающего нерва. Первоначальное холиномиметическое действие сменяется холинолитическим (брадикардия, аритмия, сменяющаяся тахикардией).
Одной из характерных особенностей действия иприта является глубокое нарушение обмена веществ, в результате которого у лиц, перенесших интоксикацию, развивается истощение, описываемое как постипритная кахексия. Нарушаются все виды обмена, но главным образом страдает белковый обмен: синтетические процессы замедляются, увеличивается выделение продуктов распада белка, в моче повышается содержание азота, креатинина, фосфатов. Нарушения обмена веществ плохо поддаются лечению и могут служить причиной гибели пораженных.
Канцерогенез
В настоящее время в экспериментах на животных продемонстрировано мутагенное, канцерогенное и тератогенное действие ипритов. Эти данные согласуются с результатами наблюдений над людьми, имевшими контакт с веществом. Так, по данным ВОЗ (1972), у рабочих, занятых на промышленных предприятиях, где они постоянно подвергаются воздействию иприта (как сернистого, так и азотистого), в 10 раз чаще развиваются опухоли легкого, чем у людей других профессий. Анализ историй болезни 1267 британских бывших военнослужащих (пенсионеров), подвергшихся в Первой мировой войне отравлению ипритом, показал, что через 15 лет после воздействия среди них случаи смерти от рака легких были в два раза чаще, чем у неотравленных людей того же возраста.
Механизм токсического действия
Как указывалось выше, действуя в высоких дозах, иприты (сернистый и азотистый) при резорбции нарушают механизмы проведения нервных импульсов в синапсах (главным образом холинергических) центральной нервной системы и на периферии. Этим отчасти объясняются эффекты со стороны сердечно-сосудистой системы (коллапс, брадикардия) или мозга (угнетение высшей нервной деятельности, судороги и т. д.). В последнее время появилась информация о способности ипритов вызывать индукцию и повышать активность NO-синтетазы. Поскольку установлено, что оксид азота является активным регулятором тонуса стенки сосудов и функционального состояния нервных клеток, влиянием на обмен N0 также можно отчасти объяснить развивающиеся сосудистые реакции и нарушения со стороны нервной системы.
Тем не менее основным является цитотоксическое действие ипритов, лежащее в основе большинства патологических процессов, развиваю-
щихся как на месте аппликации ядов, так и после их поступления во внутренние среды организма. Механизмы цитотоксичности ОВ сложны, многообразны и до конца не выяснены.
Установлено, что на клеточном уровне иприты и активные промежуточные продукты их метаболизма взаимодействуют с нуклеофильными группами молекул клеточных мембран и внутриклеточных структур, вызывая их алкилирование. Основными функционально значимыми мишенями для действия токсикантов являются белки и нуклеиновые кислоты. Взаимодействием с белками можно объяснить ингибиторную активность ипритов в отношении ряда ферментов: гексокиназы, холинацетилазы, ацетилхолинэстеразы, супероксиддисмутазы и т. д. Однако особое значение придают их повреждающему действию на дезоксирибонуклеиновые кислоты (ДНК), формирующие генетический код клетки. В этой связи иприты относят к группе генотоксикантов (веществ, повреждающих генетический код).
В основе повреждающего действия ипритов на ДНК лежит образование ковалентных связей с пуриновыми основаниями нуклеотидов (аде-нином, гуанином).
Рис. 36. Взаимодействие аденозина с ипритом
Поскольку иприт обладает двумя функциональными группами, за счет которых осуществляется атака на нуклеофильные группы оснований (рис. 36), возможно «сшивание» комплементарных нитей двойной спирали ДНК (Папирмейстер и соавт. 1993). Уже эта реакция повреждает генетический код клеток, нарушает процессы редупликации и транскрипции, лежащие в основе синтеза белка и клеточного деления. Показано, что иприт блокирует клеточный цикл митоза обратимо в фазе G2M (синтез компонентов клеточных структур, участвующих в процессе деления клеток, например тубулина) и необратимо в фазе GjS (этап утилизации пурино-вых и пиримидиновых оснований и синтеза ДНК). Тем не менее алкилирование ДНК является лишь пусковым механизмом процессов, приводящих к еще более глубокому повреждению клеток и их гибели. Как установлено, поврежденные участки ДНК подвергаются депуринизации (отщеплению алкилированных пуриновых оснований от молекулы), а затем депуринизированные участки под влиянием эндонуклеаз «вырезаются» из структуры нитей нуклеиновых кислот. Появление в ядре фрагментов ДНК активирует ферменты репарации этих макромолекул и, в частности,
Глава 11. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ЦИТ0Т0КСИЧЕСК0Г0 ДЕЙСТВИЯ
поли(аденозиндифосфорибозо)полимеразу (ПАФРП). Этот энзим участвует в синтезе новых фрагментов ДНК и встраивании их на место поврежденных участков. Поскольку при действии ипритов на клетки повреждаются смежные участки комплементарных нитей ДНК, в процессе репарации возможны грубые ошибки. Иными словами, генетический код клетки полностью не восстанавливается. Как известно, субстратом ПАФРП является никотинамидадениндинуклеотид (НАД), активно потребляемый в ходе репаративных процессов. Истощение этого субстрата (in vitro наблюдается уже через 2 ч после воздействия иприта на культуру клеток) сопровождается нарушением энергообеспечения клетки, снижается уровень АТФ. Это в свою очередь приводит к нарушению внутриклеточного обмена кальция. По данным Гросса и Смитта (1993), концентрация Са2+ в клетках, обработанных ипритом, резко увеличивается, что является пусковым механизмом каскада патологических реакций, приводящих поврежденную клетку к гибели (см. 5.2. «Общие механизмы цитотоксичности»). В эксперименте показано, что добавление к культуре лимфоцитов ингибиторов поли(аденозиндифосфорибозо)полимеразы (никотинами-да, 3-аминобензамида) повышает резистентность клеток к иприту.
Представленные сведения объясняют, почему наибольшей чувствительностью к ипритам обладают органы и ткани, клетки которых активно размножаются (клетки эпидермиса, эпителия желудочно-кишечного тракта, костного мозга и т. д.). Именно здесь нуклеиновый обмен идет с наивысшей интенсивностью, а повреждение генетического аппарата быстро приводит к пагубным последствиям: приостанавливается процесс пополнения пула зрелых, функционально полноценных клеток, выполняющих барьерные, трофические, транспортные и иные функции.
Механизм цитотоксического действия ипритов тесно связан с метаболизмом ксенобиотика в клетках. Полагают, что в реакцию алкилирования биологических субстратов (в том числе и ДНК) вступает не сам иприт, а активные промежуточные продукты его метаболизма. Образование активных метаболитов, как указывалось, проходит при участии микросома-льных монооксигеназ. Во второй фазе биопревращения иприта реактивные метаболиты вступают в реакцию конъюгации с глутатионом и деток-сицируются. Такой характер превращения токсиканта создает условия для инициации свободнорадикальных процессов в клетке, во-первых, за счет активации перекисных процессов и, во-вторых, за счет подавления механизмов антирадикальной защиты. Значительное снижение уровня глутатиона в клетках после воздействия иприта и активация в них пере-кисного окисления липидов показаны в эксперименте (Уитфидд, 1987). Активация свободнорадикальных процессов — важный механизм повреждения клеток ксенобиотиками (см. 5.2. «Общие механизмы цитотоксичности»).
Результатом цитотоксического действия ипритов является инициация ряда патохимических процессов, играющих существенную роль в патогенезе интоксикации. Так, установлено, что под влиянием этих ядов нарушается обмен «медиаторов» воспалительной реакции — цитокинов (эндогенных регуляторов клеточного роста и активности), о чем свидетель-
"tat* i a i.
ствует изменение их уровня в крови и пораженных тканях. Имеются данные о снижении под влиянием иприта продукции интерлейкина-1а .(IL-la) и увеличении продукции IL-6, IL-8. Продукция интерлейкина-1 р и фактора некроза опухоли (TNF-a) не изменяется. Дисбаланс в продукции цитокинов может существенно влиять на процесс развития воспалительной реакции, вызванной ипритами. Этим, вероятно, можно объяснить вялость течения патологических изменений, скудость клеточных реакций, слабость репаративных механизмов.
Таким образом, имеющиеся в настоящее время данные свидетельствуют о чрезвычайно сложном механизме действия ипритов на организм, выяснение которого очень важно для понимания явления цитотоксично-сти в целом.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты кожи; средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск, проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение частичной санитарной обработки (использование ИПП) в зоне химического заражения;
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• оказание первой, доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты и порядок их использования
После проведения санитарной обработки целесообразно применение средств, направленных на дальнейшее обезвреживание ОВ, не всосавшегося во внутренние среды организма, на поверхности кожи, слизистой оболочке глаз, в просвете желудочно-кишечного тракта, и препаратов, облегчающих состояние пораженных.
Для дегазации иприта на коже человека рекомендуется применение 2-5% водных растворов хлораминов (монохлорамин Б и дихлорамин Б) или 5-15% спиртовых растворов этих веществ. Особенностью хлораминов
Глава 11. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ЦИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ
является их способность «догонять» иприт, всосавшийся в толщу кожи, и дегазировать его. Также для дегазации иприта на коже могут применяться растворы соды, аммиака, едкого натра, калия марганцовокислого, перекиси водорода. В случае сильного зуда, сопровождающего ипритную эритему, можно смазывать пораженные участки кожи 5% раствором ментола.
Для обработки слизистых оболочек глаз применяют 1—2% растворы двууглекислой соды или борной кислоты, 0,25—0,5% водные растворы монохлорамина, 0,02% раствор калия марганцевокислого. При резкой отечности век и явлениях конъюнктивита делают примочки из 2% раствора кальция хлорида или содового раствора. При светобоязни в конъ-юнктивальный мешок вводят 1—2 капли 0,5% раствора пилокарпина; при сильных болях — 0,25-0,5% раствор дикаина или 2% раствор новокаина с адреналином.
Для обработки верхних дыхательных путей делают промывание носа и полоскание рта и глотки 0,5% раствором хлорамина, 2% раствором соды или 0,1-0,05% раствором калия марганцевокислого. При кашле назначают противокашлевые средства типа кодеина, дионина.
В случае попадания иприта в желудок необходимо вызвать рвоту и промыть желудок. Хорошие результаты дает промывание желудка 0,05% раствором калия марганцевокислого. Целесообразно ввести в желудок активированный уголь (25 г угля на 100 мл воды).
Для уменьшения явлений общерезорбтивного действия ядов рекомендуют внутривенное введение 30% раствора натрия гипосульфита в количестве 10—15 мл. При явлениях возбуждения центральной нервной системы рекомендуют седативные средства из группы производных барбитуровой кислоты или бензодиазепина в обычных дозах.
Изучается возможность использования в качестве средств защиты ингибиторов NO-синтетазы (метиловый эфир L-нитроаргинина) (Соейер и соавт., 1996), антиоксидантов (токоферол, аскорбиновая кислота, глута-тион и т. д.),-ингибиторов поли-АДф-рибозилирования (никотинамида, бензамида и др.) (Иорик и сотр., 1991). Однако эффективность испытанных препаратов этих групп оказалась невысокой.
11.1.2. Ингибиторы синтеза белка, не образующие аддукты ДНК и РНК
В настоящее время с целью создания эффективных противоопухолевых препаратов активно изучается группа полипептидных токсинов высших растений, действие которых обусловлено, как принято считать, ингиби-рованием синтеза белка в клетках млекопитающих. К ним относятся аб-рин, модецин, кротин, рицин и другие вещества, сходные по молекулярной массе, структуре и характеру биологического действия.
Одним из наиболее изученных и токсичных представителей группы является рицин, рассматривавшийся ранее на предмет возможности использования в качестве боевого отравляющего вещества (В. В. Мясников, 1989; Курочкин и соавт., 1994).
часть i. i uftwpmuJiui hi>i
Глава 11. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ЦИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ
Рицин
Рицин в большом количестве (до 3%) содержится в бобах клещевины обыкновенной (Ricinus communis L), откуда его и извлекают методом экстракции.
Физико-химические свойства. Токсичность
Рицин относится к классу лектинов — растительных гликопротеидов, in vitro агглютинирующих клетки млекопитающих в результате избирательного связывания с углеводными компонентами поверхности клеточной мембраны. Белок этот состоит из двух полипептидных цепей, соединенных дисульфидной связью. А-цепь состоит из 265 аминокислот и 6 углеводных фрагментов. Молекулярная масса А-цепи — 32 ООО дальтон. В-цепь рицина состоит из 260 аминокислот, фрагментов глюкозамина и маннозы. Молекулярная масса В-цепи равна 34 ООО дальтон.
Очищенный рицин представляет собой белый, не имеющий запаха, легко диспергируемый в воздухе и растворимый в воде порошок. Вещество малоустойчиво в водных растворах и при хранении постепенно теряет токсичность. При низких температурах водные растворы сохраняются достаточно долго.
Рицин токсичен для большинства видов теплокровных животных. Расчетная смертельная доза вещества для человека при приеме через рот составляет около 0,3 мг/кг. При ингаляции мелкодисперсного аэрозоля его токсичность значительно выше. Через неповрежденную кожу рицин не оказывает токсического действия.
Токсикокинетика
Вещество легко проникает в организм через легкие, значительно хуже — через желудочно-кишечный тракт. Взаимодействуя с клетками, формирующими альвеолярно-капиллярный барьер и слизистую оболочку ЖКТ, рицин повреждает их. Попав в кровь, вещество распределяется в организме. Через гематоэнцефалический барьер проникает плохо. Значительная его часть быстро фиксируется на поверхности эритроцитов, клеток эндотелия различных органов и тканей. Время пребывания несвязанной формы токсина в крови не превышает нескольких минут. Токсикант разрушается при участии протеолитических ферментов.
Основные проявления интоксикации
Сведения о токсическом действии рицина скудны. Они получены главным образом при изучении случаев отравления людей клещевиной, а также в экспериментах на лабораторных животных. Признаки поражения проявляется, как правило, через сутки — трое после попадания вещества в организм. Даже значительное увеличение дозы токсиканта не приводит к существенному сокращению продолжительности скрытого периода. Проявления интоксикации складываются из картины местного и резорб-тивного действия, в основе которого лежат цитотоксический и цитостатический эффекты, нарушение процессов метаболизма в клетках, с которыми вещество вступает в контакт.
При заглатывании семян клещевины животными или людьми через Ю—12 ч или позднее появляются признаки сильного раздражения желудочно-кишечного тракта: тошнота, рвота, сильные боли в животе, приступы кишечной колики, профузный понос (часто с кровью). Позже развиваются лихорадка, головная боль, цианоз кожных покровов, появляется чувство жажды, артериальное давление падает, пульс частый слабого наполнения, выступает холодный пот. В крайне тяжелых случаях на высоте интоксикации (на вторые — третьи сутки) наблюдаются судорожный синдром, признаки поражения печени (желтуха) и почек (альбуминурия, гематурия, уменьшение количества отделяемой мочи вплоть до анурии). При смертельных интоксикациях летальный исход наступает, как правило, на 2-7-е сут. Для несмертельного отравления клещевиной характерно затяжное течение, проявляющееся гипертермией, гиподинамией, заторможенностью, прогрессирующей слабостью, анорексией, поносом, истощением.
Описан случай имплантации частиц бобов клещевины под кожу голени с целью умышленного членовредительства. Через 12—24 ч у отравленного наблюдались сильный озноб, повышение температуры тела до 39-4Г С, сильная головная боль и общая слабость. Через 7 сут на месте введения образовалась глубокая, болезненная язва, не заживавшая более 2 лет.
Пыль, образующаяся при переработке клещевины и других растений, содержащих токсичные лектины, может вызывать конъюнктивит, острый ринит, фарингит, хроническое воспаление бронхов. У пострадавших наблюдаются слезотечение, головная боль, кашель, одышка со свистящим дыханием и т. д. При попадании порошкообразного рицина в глаза развивается воспалительный процесс, переходящий в тяжелый панофталь-мит.
Характерно аллергизирующее действие рицина. Человек, однажды подвергшийся действию пыли, содержащей вещество, становится чувствительным к ничтожным количествам токсиканта.
В эксперименте установлена высокая ингаляционная токсичность рицина. При поражении аэрозолем в высокой концентрации у животных развиваются тяжелое острое воспаление слизистой оболочки дыхательных путей с перибронхиальным отеком ткани, переходящее в гнойный трахеобронхит, крайне тяжелая очаговая пневмония, завершающаяся некрозом легочной ткани.
Резорбтивное действие рицина при его системном введении экспериментальным животным проявляется выраженным нарушением проницаемости сосудов, изменениями со стороны системы крови, деструктивными процессами в печени, почках, миокарде. У отравленных животных обнаруживаются умеренный отек легких и кровоизлияния в легочную ткань, гидроторакс, экссудативный плеврит, отек мозга, асцит, выраженный геморрагический гастроэнтероколит, кровоизлияния во внутренние органы. В основе нарушения сосудистой проницаемости лежат повреждение эндотелиальных клеток, а также деструктивные изменения стенок сосудов.
У крыс, отравленных рицином, уже в первые часы после воздействия наблюдаются морфологические признаки активации ретикуло-эндотели-альных элементов печени в виде их гипертрофии и гиперплазии, затем отмечаются некротические изменения синусных клеток, а затем жировое перерождение и некроз гепатоцитов. Участки некроза располагаются как в центральных, так и в периферических отделах печеночных долек. В почках в выделительных канальцах первого и второго порядка выражена дистрофия эпителия. В сердечной мышце выявляются признаки острого очагового миокардита.
В крови отравленных лабораторных животных (на 3-й — 20-е сут) отмечаются умеренный гемолиз, стойкий нейтрофильный лейкоцитоз, лимфоцитоз, моноцитоз. Изменяются реологические свойства крови. Повышается уровень фибриногена в крови, активируется система превращения фибриногена в фибрин. Складываются условия для диссеми-нированного внутрисосудистого свертывания крови.
Механизм токсического действия
Всю совокупность токсических процессов, развивающихся при поражении рицином, можно объяснить повреждением клеток различных органов и тканей. В токсическом действии рицина на клетки можно выделить три периода: фиксации токсина на мембране клеток, проникновения в клетку, повреждения клетки.
Фиксация рицина на мембране клеток осуществляется путем взаимодействия В-цепи молекулы с рецепторами, активно связывающими лектины. Центры связывания имеются в клетках различных типов, однако количество таких центров на поверхности мембран различных клеток неодинаково. Этим объясняется и неодинаковая чувствительность различных клеточных популяций к токсиканту. Так, в опытах in vitro установлено, что у лимфоцитов и некоторых других соматических клеток количество участков связывания рицина достигает 106—108 на клетку, у эритроцитов — значительно меньше. Связывание токсина клетками in vitro существенно блокируется лактозой.
Проникновение токсина, фиксировавшегося на поверхности мембраны, в клетку осуществляется путем эндоцитоза. Вещества, усиливающие проницаемость биологических мембран (нигерицин), in vitro в несколько раз увеличивают цитотоксическое действие рицина. Внутри клетки молекула токсина разрушается с высвобождением А-цепи, которая и оказывает повреждающее действие.
Основной «точкой приложения» А-цепи рицина являются рибосомы, а именно их 60-S (большие) субъединицы. Как известно, процесс трансляции — синтез полипептидных цепей на матрице информационной РНК согласно генетическому коду — осуществляется преимущественно на рибосомах сложным комплексом макромолекул. Этот комплекс, помимо рибосомальных макромолекул, включает: информационные РНК, транспортные РНК, аминоацил-тРНК-синтетазы, а также белковые факторы инициации (начала) синтеза, элонгации (удлинения) полипептидной цепи, терминации (окончания) процесса. Рицин связывается с рибосомами в той их области, где последние взаимодействуют с факторами элонгации (ФЭ-1 и ФЭ-2). В результате удлинение формируемых на рибосомах полипептидных цепей прекращается — нарушается синтез белка в клетке и она погибает. Синергистами токсического действия рицина являются ингибиторы синтеза белка с иными механизмами повреждающего действия, в частности, актиномицин Д, который нарушает процесс транскрипции (ДНК-зависимый синтез информационной РНК в клетках), задерживая продвижение РНК-полимеразы вдоль цепи ДНК.
По некоторым данным, рицин выводит из строя эндогенные ингибиторы протеолиза в клетках, активирует протеолитические процессы, инициируя разрушение клеточных белков, что также приводит к гибели клеток.
Рицин, как и другие лектины, действуя в малых дозах, является сильным митогеном, активирующим клеточное деление и, в частности, пролиферацию популяции Т-лимфоцитов в организме. Не исключено, что повреждение клеток органов и тканей, наблюдаемое при отравлении, может быть также следствием атаки на них активированных Т-киллеров, других фагоцитирующих элементов иммунной системы.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск, проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• оказание первой, доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Помощь пораженным оказывается по общим правилам с использованием этиотропных и патогенетических средств терапии состояний, развивающихся после воздействия яда (см. 6.4. «Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях»). Для ослабления местного действия рицина на догоспитальном этапе пораженным необходимо тщательно промыть глаза, обработать слизистые оболочки носоглотки и полости рта водой, раствором соды или физиологическим раствором. При пероральном отравлении с целью оказания помощи показано промывание желудка. При болях в глазах, по ходу желудочно-кишечного тракта показано назначение местных анестетиков. Поскольку токсический процесс развивается медленно, имеется резерв времени для эвакуации пораженных в специализированные лечебные учреждения.
Специальные табельные средства медицинской защиты отсутствуют. Существует теоретическая возможность разработки таких средств. Поскольку рицин является полным антигеном, возможно создание специфических антитоксических сывороток. Использование таких препаратов с профилактической целью могло бы оказывать защитное действие. Однако их лечебное применение будет затруднено, так как рицин быстро элиминируется из крови отравленных.
11.2. Тиоловые яды
К тиоловым ядам относятся вещества, в основе механизма токсического действия которых лежит способность связываться с сульфгидрильными группами, входящими в структуру большого количества биологических молекул, среди которых: структурные белки, энзимы, нуклеиновые кислоты, регуляторы биологической активности и т. д. В частности, к числу ферментов, содержащих сульфгидрильные группы, относятся: гидролазы (амилаза, липаза, холинэстераза, уреаза и др.), оксидоредуктазы (алко-гольдегидрогеназа, аминоксидазы, дегидрогеназы яблочной, янтарной, олеиновой кислот и др.), фосфатазы (аденозинтрифосфатаза, миокиназа, креатинфосфокиназа, гексокиназа и др.), ферменты антирадикальной защиты клетки (глутатионпероксидаза, глутатионредуктаза, глутатион-S-трансфераза, каталаза). Рибосомы клеток млекопитающего содержат около 120 сульфгидрильных групп, причем примерно половина из них имеет функциональное значение для осуществления белкового синтеза. Гормоны полипептидной структуры, такие как инсулин и глюкагон, также содержат сульфгидрильные группы в молекулах и т. д.
Образование комплекса токсиканта с SH-группами биомолекул сопровождается их повреждением, нарушением функции, что и инициирует развитие токсического процесса.
К числу тиоловых ядов прежде всего относятся металлы: мышьяк, ртуть, цинк, хром, никель, кадмий, и их многочисленные соединения. Сродство различных тиоловых ядов к разным соединениям, содержащим SH-группы, неодинаково. Неодинакова и токсикокинетика ядов. Этим объясняются различия токсичности веществ и особенности формирующегося токсического процесса. Среди веществ рассматриваемой группы для военной медицины наибольший интерес представляют соединения мышьяка.
11.2.1. Соединения мышьяка
Мышьяксодержащие вещества широко используются в медицине, а также в качестве пестицидов (инсектицидов и гербицидов), осушителей в производстве изделий из хлопка, консервантов древесины, пищевых добавок в рацион некоторых животных и т. д. Хотя случаи массовых интоксикаций соединениями мышьяка в настоящее время редки, сохраняется потенциальная возможность таких инцидентов. Так, в Японии (1972 г.) более 12 тыс детей получили отравление консервированным молоком, зараженным мышьяком. Случай привел к гибели 130 человек. Широкое применение мы-шьяксодержащих веществ в хозяйственной деятельности, их доступность делают возможным их применение с террористическими целями.
На основе мышьяка в начале XX в. были созданы высокотоксичные боевые отравляющие вещества, запасы которых в настоящее время подлежат уничтожению.
Общая характеристика
Мышьяк (As) — переходный элемент V группы периодической системы, металлоид, атомный номер 33, атомная масса 74,9. В природе встречается в виде минералов: ауропигмент (as2o3), реальгар (as4s4), арсенопирит (FeAsS), примесей к рудам различных металлов. Способен взаимодействовать с углеродом, водородом, кислородом, хлором, серой и образовывать многочисленные соединения.
По особенностям строения и биологической активности соединения мышьяка подразделяют на 3 основные группы:
а) неорганические соединения;
б) органические соединения;
в) арсин (АвНз).
К настоящему времени синтезировано более 6000 неорганических и органических соединений мышьяка. В группе неорганических соединений выделяют соединения трехвалентного (As+3 — арсениты — триоксид мышьяка, арсенит натрия, трихлорид мышьяка и т. д.) и пятивалентного (As+5 — арсенаты) мышьяка (пятиокись мышьяка, мышьяковая кислота и т. д.).
Среди органических соединений также различают вещества, в которых мышьяк может находиться в трех- и пятивалентном состоянии. Кроме того, выделяют алкильные и арильные органические производные этого элемента (рис. 37). К числу наиболее опасных органических соединений трехвалентного мышьяка относятся хлорсодержащие алкильные производные — метилдихлорарсин, этилдихлорарсин, дихлорвинилхло-Рарсин, трихлорвиниларсин и р-хлорвинилдихлорарсин — известное боевое отравляющее вещество кожно-нарывного действия (люизит). Арильные производные трехвалентного мышьяка, представляющие интерес для военной медицины, это прежде всего вещества, раздражающие носоглотку, например адамсит (фенарсазинхлорид) — боевое отравляющее вещество (см. гл. 8. «Отравляющие и высокотоксичные вещества раздражающего действия»).
21 S
21 Э
| а |
| аснсн—as |
Представителями группы органических производных пятивалентного мышьяка являются, в частности, метиларсоновая кислота, диметиларси-новая кислота (какодиловая кислота). Последнее вещество входило в состав «голубой жидкости», применявшейся американскими войсками в период Вьетнамской войны (70-е гг. XX в.) в качестве фитотоксиканта.
.а
| Н3С— As' |
| •а |
| -а |
CHCHCI
CI—As'
| метилдихлорарсин |
^CHCHCI
дихлорвинилхлорарсин
О
| НО—As' ^СН3 диметиларсиновая (какодиловая) кислота |
i| ОН H3C—As'
^ОН
метиларсоновая кислота
Рис. 37. Некоторые представители мышьякорганических соединений
Некоторые соединения мышьяка обладают высокой биологической активностью при местном и резорбтивном действии на организм. При резорбции наиболее токсичными являются арсин (АбНз — см. гл. 10. «Отравляющие и высокотоксичные вещества общеядовитого действия»), хлорсодержа-щие органические соединения трехвалентного мышьяка (люизит, этиддих-лорарсин и др.), а также неорганические соединения трехвалентного мышьяка (арсенит натрия, триоксид мышьяка). Менее токсичны неорганические соединения пятивалентного мышьяка (арсенат натрия, пятиокись мышьяка). Органические соединения пятивалентного мышьяка (какодиловая кислота, метиларсоновая ксилота и др.) по большей части относятся к числу малотоксичных соединений.
При местном действии наивысшей активностью обладает люизит (вызывает воспалительные изменения покровных тканей) и ароматические производные трехвалентного мышьяка (адамсит — раздражающее действие на слизистые оболочки глаз и дыхательных путей).
Токсические процессы, развивающиеся в результате острого действия неорганических соединений мышьяка и металлорганических соединений, имеют существенные особенности.
11.2.1.1. Неорганические соединения мышьяка
Арсенит натрия (NaAsOrf
Хотя достаточно высокой токсичностью обладают все соединения мышьяка, в качестве диверсионных агентов наибольшую опасность представляют триоксид мышьяка (as2o3), мышьяковистая кислота (HAs02) и ее соли, в частности арсенит натрия. Токсичность неорганических соединений существенно зависит от их способности растворяться в воде. Так, водорастворимый арсенит натрия примерно в 10 раз более токсичен, чем хуже растворимый в воде оксид металла.
Арсенит натрия (NaAs02) — белый порошок, умеренно растворимый в воде. Достаточно стоек при хранении. Для людей смертельное количество вещества при приеме через рот составляет 30—120 мг. Смертельной дозой для человека может оказаться 200 мг триоксида As (as2o3).
Токсикокинетика
Около 90% попавшего в желудочно-кишечный тракт вещества абсорбируется. В виде аэрозоля возможно проникновение арсенита натрия через легкие.
После поступления в кровь вещество довольно быстро перераспределяется в органы и ткани (в крови неотравленных людей содержание мышьяка находится в пределах 0,002-0,007 мг/л). Наивысшие концентрации металла в тканях отмечаются через час после внутривенного введения арсенита натрия экспериментальным животным. Наибольшее его количество определяется в печени, почках, коже (в последующем в ее придатках — ногтях, волосах), легких и селезенке. Металл проникает через гематоэнцефалический барьер, однако концентрация его в головном мозге ниже, чем в других органах.
В большинстве органов содержание металла быстро падает (за 48 ч — в 10—60 раз). Исключение составляет кожа, где и через двое суток определяется большое, количество мышьяка (до 30% от максимального уровня). Высокое сродство металла к коже и ее придаткам объясняют большим содержанием сульфгидрильных белков (в частности кератина), с которыми As образует прочный комплекс.
Выделение As осуществляется главным образом с мочой. Скорость экскреции достаточно высока — в первые сутки выделяется до 30—50% введенного количества, более 80% — в течение 2,5 сут. Перед экскрецией As подвергается реакции метилирования. Большая его часть выводится из организма в форме монометиларсоновой и диметиларсиновой кислот.
У лабораторных животных (обезьяны) через 1—2 дня после введения соединений трехвалентного мышьяка в крови обнаруживали менее 1 % от введенной дозы. В этот период уровень металла в цельной крови в 2—7 раз выше, чем в плазме.
В норме мышьяк определяется в моче в количестве 0,01—0,15 мг/л.
Основные проявления острой интоксикации
Острое пероральное отравление мышьяком сопровождается поражением желудочно-кишечного тракта, нервной системы, сердечно-сосудистой системы, системы крови, почек, печени.
При приеме через рот очень больших доз токсиканта развивается так называемая «паралитическая форма» отравления. Уже через несколько минут после воздействия яда появляются тошнота, рвота, боли в животе, профузный понос. Затем присоединяются болезненные тонические судороги, кожа приобретает цианотичный оттенок. Через несколько часов возможен смертельный исход на фоне полной утраты сознания, расслабления мускулатуры тела, глубокого коллапса.
Чаще острое отравление характеризуется признаками тяжелого гастроэнтерита с постепенным развитием клинической картины. Первые симптомы появляются через полчаса — час после приема яда. Если мышьяк содержится в большом количестве пищи, начало заболевания может быть еще более отсрочено. Картина развивающегося отравления напоминает холеру. Основные симптомы поражения: чесночный или металлический привкус во рту, сухость и жжение слизистой оболочки губ и полости рта, сильная жажда, тошнота, дисфагия, боли в животе, рвота. Если в течение нескольких часов рвота не прекращается, в рвотных массах появляются следы крови. По прошествии нескольких часов (как правило, около суток) присоединяется сильный понос, гематемезис. Развиваются признаки обезвоживания организма, гиповолемия, падение артериального давления, нарушение электролитного баланса. Сознание спутано, состояние напоминает делирий. На ЭКГ регистрируются тахикардия, удлинение интервала QT, изменение зубца Т, желудочковая фибрилляция.
Количество отделяемой мочи снижается, в моче определяется белок, а через 2—3 сут и кровь. В крови выявляются лейкопения, нормо- и микро-цитарная анемия, тромбоцитопения и т. д. Возможно развитие гемолиза.
Проявления острой несмертельной интоксикации неорганическими соединениями мышьяка представлены в табл. 34. Спустя несколько недель после воздействия мышька иногда развивается отсроченная нейропатия.
 |
Таблица 34
11.2.1.2. Галогенированные алифатические арсины
Важнейшими представителями ОВТВ из группы органических производных мышьяка являются галогенированные алифатические арсины, такие как метил-, этилдихлорарсины, дихлорвинилхлорарсин и др. По своим токсическим свойствам эти вещества достаточно близки. Типичным представителем группы является боевое отравляющее вещество, относимое к группе «кожно-нарывных», р-хлорвинилдихлорарсин (люизит).
Люизит
Люизит синтезирован в 1917 г. американским химиком Льюисом и независимо от него немецким химиком Виландом.
Физико-химические свойства. Токсичность
Свежеперегнанный люизит — бесцветная, умеренно летучая жидкость; при хранении через некоторое время приобретает темную окраску с фиолетовым оттенком. Запах люизита напоминает запах растертых листьев герани. Температура кипения: 196,4° С, температура замерзания: —44,7° С. Относительная плотность паров люизита по воздуху равна 7,2. Люизит хорошо растворяется в органических растворителях, в жирах, смазках, впитывается в резину, лакокрасочные покрытия, пористые материалы. Вещество примерно в 2 раза тяжелее воды, в которой оно растворяется плохо (не более 0,05%). Растворившийся в воде люизит довольно быстро гидролизуется с образованием хлорвиниларсеноксида, уступающего по токсичности исходному агенту. Слабые щелочи ускоряют гидролиз. Люизит легко окисляется всеми окислителями (йодом, перекисью водорода, хлораминами и т. д.) с образованием малотоксичной хлорвинилмы-шьяковой кислоты.
Попавший в окружающую среду люизит формирует зоны стойкого химического заражения. В зависимости от погодных условий вещество сохраняется на местности от суток (дождливая, теплая погода) до месяца (холодное время года).
Люизит в парообразном состоянии уже в концентрации 0,002 г/м3 вызывает раздражение глаз. LQ50 вещества при ингаляции составляет примерно 1,2—1,5 г-мин/м3 при действии через кожу — около 100 г-мин/м3. Повреждающая глаз токсодоза паров люизита составляет менее 0,3 г • мин/м3, кожи — более 1,5 г • мин/м3. При попадании люизита в желудочно-кишечный тракт смертельная доза для человека составляет 2—10 мг/кг.
Токсикокинетика
Благодаря высокой растворимости в липидах люизит сравнительно быстро всасывается через кожу и слизистые оболочки дыхательных путей и желудочно-кишечного тракта в кровь и ею разносится по органам и тканям организма. Вещество легко преодолевает гисто-тематические барьеры и проникает внутрь клеток через клеточные мембраны.
Спонтанно и при участии ферментативных систем вещество подвергается гидролизу, окислению, дегалогенированию, деалкилированию. В результате образуются многочисленные мышьяксодержащие метаболиты, выделяющиеся из организма со скоростью выделения неорганических соединений металла (см. выше).
Основные проявления интоксикации
Клиническая картина поражения люизитом складывается из местного и резорбтивного действия яда. Местное действие характеризуется воспалительно-некротическими изменениями и явлением раздражения тканей на месте аппликации. Резорбтивное действие проявляется нарушением пластического и энергетического обмена в органах и тканях, структурными изменениями и гибелью клеток, с которыми взаимодействует токсикант (сосудистая система, нервная система, паренхиматозные органы).
Поражение органов дыхания
Люизит в парообразном состоянии и в форме аэрозоля уже в низких концентрациях оказывает выраженное раздражающее действие на слизистую оболочку верхних дыхательных путей. Пораженные ощущают першенье и царапанье в горле, появляются чихание, насморк, кашель, слюнотечение, осиплость голоса. Объективно обнаруживаются гиперемия слизистых оболочек зева, гортани и носа и их отечность. При прекращении контакта с ОВ все эти проявления интоксикации через сутки — двое исчезают.
В более тяжелых случаях через час — полтора после воздействия развиваются прогрессирующие воспалительно-некротические изменения слизистой оболочки трахеи и бронхов. Пораженные ощущают затруднение при дыхании, появляется кашель, отделяется гнойная мокрота с прожилками крови и обрывками некротизированной слизистой оболочки дыхательных путей. При аускультации выслушиваются сухие и влажные хрипы. Такая картина острой интоксикации сохраняется в течение нескольких недель. При действии в концентрациях, близких к смертельным, люизит вызывает развитие токсического отека легких с характерной симптоматикой (см. 9.2. «ОВТВ удушающего действия»). При этом воспалительно-некротические изменения дыхательных путей носят выраженный характер. Выздоровление при благоприятном течении наступает только через полтора — два месяца.
Поражение глаз
При действии паров люизита в момент контакта появляются чувство жжения, боль в области глаз, слезотечение.
Легкая степень поражения органа зрения характеризуется симптомами катарального конъюнктивита (покраснением конъюнктивы, обильным слезотечением, светобоязнью). После прекращения действия токсиканта симптомы раздражения довольно быстро проходят.
При увеличении времени контакта или повышении концентрации паров ОВ наблюдается поражение средней степени тяжести: симптомы раздражения конъюнктивы более выражены, появляется отек конъюнктивы и век, развивается стойкий блефароспазм. В конъюнктиве появляются мелкоточечные кровоизлияния, постепенно катаральный конъюнктивит переходит в гнойный. Процесс может затянуться на несколько недель.
Действуя в более высоких концентрациях, яд вызывает развитие поражения тяжелой формы, при которой в процесс вовлекаются не только веки, конъюнктива, но и роговая оболочка глаза. В этих случаях, помимо симптомов описанных выше, через 5—8 ч появляются признаки помутнения роговицы. Через 10—14 дней кератит проходит, а через 20—30 дней наступает выздоровление.
При попадании в глаза люизита в капельно-жидком виде быстро развиваются выраженный отек всех тканей глаза, резкая гиперемия конъюнктивы, появляются кровоизлияния. Затем формируются очаги некроза роговицы. Процессу некротизации, кроме роговицы, подвергаются слизистая оболочка, подслизистая, клетчатка и мышцы глаза (панофталь-мит). Такое поражение заканчивается потерей глаза.
Поражение кожи
Действуя в капельно-жидком состоянии люизит быстро проникает в толщу кожи (в течение 3—5 мин). Скрытый период практически отсутствует. Сразу развивается явление раздражения: ощущаются боль, жжение на месте воздействия. Затем проявляются воспалительные изменения кожи, выраженность которых определяет степень тяжести поражения. Легкое поражение характеризуется появлением болезненной эритемы. Поражение средней степени тяжести приводит к образованию в течение нескольких часов поверхностного пузыря. Последний быстро вскрывается. Эрозивная поверхность эпителизируется в течение 1—2 нед. Тяжелое поражение — это глубокая, длительно незаживающая язва.
При поражении кожи парами люизита наблюдается скрытый период продолжительностью 4—6 ч, за которым следует период формирования разлитой эритемы, прежде всего на открытых участках кожи. Действуя в высоких концентрациях, вещество может вызвать развитие поверхностных пузырей. Заживление наступает в среднем через 8-15 дней. При защите органов дыхания смертельное поражение парообразным люизитом практически не возможно.
Сравнительная характеристика поражения кожи люизитом и ипритом представлена в табл. 35.
При вскрытии погибших животных выявляются дегенеративные изменения паренхиматозных органов (жировая дистрофия, некроз паренхимы, перерождение эпителия). Отчетливо выражены дистрофические изменения нервных клеток различных отделов ЦНС (вегетативных ганглиев и т. д.) в виде вакуолизации, сморщивания, пикноза ядер, кариорек-сиса.
Таким образом, для резорбтивного действия люизита характерными являются сосудистые расстройства, а также дегенеративные изменения со стороны клеток нервной системы и паренхиматозных органов.
11.2.1.3. Галогенированные ароматические арсины
Высокотоксичным представителем группы ароматических арсинов является фенилдихлорарсин. Это соединение также рассматривали как возможное ОВ кожно-нарывного действия. Поскольку в структуру токсиканта входит арильный радикал, вещество, помимо свойств, присущих всем галогенированным органическим производным трехвалентного мышьяка (люизиту), обладает сильно выраженным раздражающим действием. Основные свойства вещества представлены в табл. 36.
Таблица 36
| 222,91 7,7 1,65 (при 25° С) 252-255° С Высокая HCI и фениларсиноксид Стабилен Отсутствует 0,0009 г/м3 2,6 Г'мин/м3 0,016 г-мин/м3 1,8 г-мин/м3 |
Основные свойства фенилдихлорарсина
| ' it |
Молекулярный вес Плотность пара (по воздуху) Плотность жидкости Температура кипения Скоростьтидролиза Продукты гидролиза Стабильность при хранении Запах
Средняя концентрация органолептического определения (раздражение носоглотки)
Среднесмертельная доза (ингаляционно)
Средненепереносимая доза (рвотное действие)
| Действие на кожу и глаза (на глаза — немедленное; на кожу — отсрочено на 30 мин — 1 ч). Резорбтивное действие (см. люизит) |
Средненепереносимая доза (кожно-нарыаное действие)
Клинические эффекты
Механизм токсического действия соединений мышьяка
В 1925 г. Фегтлиным было высказано предположение, что токсическое действие соединений трехвалентного мышьяка, сопровождающееся значительным нарушением функций и гибелью клеток различных органов и тканей, обусловлено их взаимодействием с сульфгидрильными группами биологических молекул. Предпосылкой к этому послужили данные о способности арсенитов взаимодействовать с сероводородом с образованием сульфидов мышьяка:
As203 + 3H2S ----------- *■ As2S3 + 3H20
R— As—О + H2S *- R— As—S + H20.
По мнению автора, основным объектом токсического воздействия в клетках является глутатион, сульфгидрильные группы которого в процессе реакции блокируются:
SG
R—As—О + 2GSH ** R—As^ + Н20.
^SG
Было установлено, что предварительное введение глутатиона защищает лабораторных животных от арсеноксида и арсенита натрия, вводимых в смертельных дозах.
Теоретически отравление мышьяком может сопровождаться нарушением активности всех SH-содержащих молекул (см. выше). Однако в начале 40-х гг. XX в. Томпсоном и соавторами было показано, что реакции соединений мышьяка, и в частности люизита, с тиоловыми группами протекают двояко. При взаимодействии арсенитов с монотиолами образуются малопрочные, легко гидролизуемые соединения. При взаимодействии же токсикантов с молекулами, в которых две тиоловые группы расположены рядом (в положении 1,2 либо — 1,3), образуются прочные, не поддающиеся гидролизу циклические соединения:
.CI HS—CHR /S—CHR
| s—СН |
CICH—CHAs^ + | *• CICH—CHAsC' | + 2HCI.
CI HS—СН
R R
Была высказана гипотеза (Питере, Томпсон, Стокен), согласно которой токсическое действие различных соединений мышьяка обусловлено главным образом их реакцией с молекулами со смежным расположением SH-групп, в результате чего образуются прочные циклические структуры.
В частности, токсиканты активно связываются с липоевой кислотой (рис. 38), являющейся коэнзимом пируватоксидазного ферментного комплекса, регулирующего превращение пировиноградной кислоты (конечного продукта гликолиза) в активную форму уксусной кислоты (ацетил КоА), утилизируемую циклом Кребса. В результате в крови и тканях накапливается пирс-виноградная кислота (ацидоз), блокируется цикл трикарбоновых кислот — нарушаются процессы энергетического обмена в клетках различных органов (в этой связи люизит можно рассматривать и как вещество общеядовитого действия).
СН2СН2СН(СН2)4СООН
SH SH h
Рис. 38. Липоввая кислота
Взаимодействием мышьяксодержащих веществ с сульфгидрильными группами можно объяснить и их гипотензивное действие. Так, полагают, что рецепторные структуры для оксида азота, активного регулятора сосудистого тонуса, включают в качестве функционально-значимых элементов SH-группы. В основе расслабляющего действия N0 на сосуды лежит его способность образовывать с SH-группами нестабильные нитрозотио-лы (период полусуществования комплекса в организме — около 3—5 с):
2 RSH + 2 N0 »■ 2 RSNO + Н2
2RSN0 >■ RS—SR + 2N0.
Падение артериального давления, наблюдаемое при отравлении соединениями мышьяка, может быть объяснено образованием относительно стойких связей As с SH-группами сосудистых рецепторов оксида азота.
Широкое представительство в организме лигандов с высоким сродством к мышьяку и их большая роль в поддержании гомеостаза лежат в основе способности токсикантов действовать практически на все органы и системы, инициируя различные формы токсических процессов. Этим, в частности, можно объяснить развитие не только тяжелых воспалительно-некротических изменений в покровных тканях при непосредственном действии на них токсикантов, но и целого ряда функциональных нарушений со стороны ЦНС, печени, миокарда и т. д., наблюдаемых при отравлении соединениями мышьяка.
Способностью взаимодействовать с сульфгидрильными группами молекул и молекулярных комплексов, регулирующих процессы, лежащие в основе клеточного деления, можно объяснить и канцерогенное действие соединений мышьяка (по данным МАИР — мышьяк канцероген для человека).
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств зашиты (средства зашиты кожи; средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск, проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение частичной санитарной обработки (использование ИПП) в зоне химического заражения;
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности пораженного, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Средства, применяемые при отравлениях мышьяксодержащими веществами, представлены препаратами трех групп:
1. Препараты для обезвреживания мышьяка, не всосавшегося во внутренние среды организма, на поверхности кожи, слизистой оболочке глаз, в просвете желудочно-кишечного тракта.
2. Лечебные антидоты.
3. Средства симптоматической и патогенетической помощи пострадавшим.
Средства для обезвреживания мышьяка на покровных тканях. При попадании капельно-жидкого ОВ на кожу или одежду в первые 5—10 мин производят частичную санитарную обработку с помощью содержимого индивидуального противохимического пакета. Помимо содержимого ИПП, для обезвреживания мышьяка на поверхности кожи могут быть использованы вещества, которые окисляют, хлорируют или приводят к гидролизу его соединения. Дегазирующие свойства окислителей основаны на превращении трехвалентного мышьяка, входящего в состав люизита, в пятивалентный и снижении в связи с этим токсичности образующихся соединений. В качестве окислителей могут быть использованы растворы 5% монохлорамина, 5% калия марганцовокислого в 5% уксусной кислоте, 5-10% йода, 40% гидропирита (перекис мочевины).
Для ослабления поражений кожи люизитом в виде мази применяют комплексообразователи из группы дитиолов: 3,5% или 5% мазь 2,3-ди-меркаптопропанола под названием «дикаптол» или 30% мазь унитиола.
При поражении глаз люизитом необходимо промыть глаз водой либо 0,25% раствором хлорамина и ввести в конъюнктивальный мешок на 1-2 мин 30% мазь унитиола (затем глаз опять промыть).
При поражении слизистых оболочек дыхательных путей следует провести обмывание слизистой оболочки растворами 0,05% кмпо4, 0,25-1% хлорамина.
При попадании соединений мышьяка с зараженной водой или пищей обильно промывают желудок и пищевод раствором калия марганцовокислого (0,05% раствор). После этого следует назначить внутрь 5 мл 5% раствора унитиола.
Специфические противоядия соединений мышьяка
Как уже указывалось, Фегтлин и Розенталь еще в начале XX в. установили защитную роль глутатиона против токсического действия арсенок-сида и арсенита натрия. Позже было показано, что защитными свойствами обладают и другие соединения, содержащие одну сульфгидрильную группу (монотиолы): цистин, цистеин, ацетилцистеин, тиоэтиленгли-коль, натрия тиогликонат, тиомалоновая кислота и т. д. Однако одновременно отмечалась малая активность монотиолов при лечении мышьяковых (особенно люизитных) отравлений.
Работами Стокена и Томпсона было показано, что можно существенно повысить эффективность антидотной терапии используя дитиольные соединения — вещества, образующие прочные циклические комплексы с мышьяком. Из препаратов такого типа весьма эффективным оказался 2,3-ди-меркаптопропанол, синтезированный в Великобритании в 1941-1942 гг. и вошедший в медицинскую практику под названием «Британский антилюизит» (БАЛ). Под влиянием БАЛ скорость выведения мышьяка из организма отравленных с мочой увеличивается в 5-10 раз, особенно в первый день после воздействия токсиканта. По данным разработчиков, терапевтический эффект БАЛ при отравлении люизитом и другими соединениями мышьяка обусловлен его способностью реагировать не только со свободными токсикантами, циркулирующими в крови (химический антагонизм), но и с мышьяком, который уже успел связаться с сульфгид-рильными группами в тканях. Вследствие этого БАЛ не только предотвращает токсическое действие яда на биомолекулы, но и восстанавливает их физиологическую активность (биохимический антагонизм):
SH CL S
фермент + ^As—R фермент' /As—R + 2 HCI
| ySH S—СН2 фермент. + R — As^f„ 1 ои о—им |
NSH СК NSX
S HS—СН2
| SH , НО-СН2 |
фермент ' ^ As—R + I
о/ HS—СН
ь I
HO-CH2
2,3-Димеркаптопропанол — бесцветная маслянистая жидкость с запахом меркаптана. В воде растворяется плохо (менее 6%), хорошо — в органических растворителях. Для практических целей БАЛ рекомендуют применять внутримышечно в виде 5-10% раствора в масле из расчета 2-3 мг/кг.
Глава 11. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА ЦИТОТОКСИЧЕСКОГО ДЕЙСТВИЯ
Отдельные свойства 2,3-димеркаптопропанола понижают его ценность как средства медицинской защиты. К таковым относятся: высокая токсичность (смертельная доза для крыс — около 200 мг/кг; непереносимая доза для человека, вызывающая тошноту, рвоту, головокружение и т. д., — около 5 мг/кг) и плохая растворимость в воде (и, следовательно, невозможность внутривенного способа введения). Это дало повод для поиска новых средств.
В настоящее время в литературе имеется описание большого количества тиоловых соединений, испытанных в качестве антидотов мышьяка. Среди них дитиоэтиленгликоль, 2,3-димеркаптопропилэтиловый эфир, 2,3-димеркаптопропил-глюкозид, 2,3-димеркаптопропиламин, димер-каптосукцинат и т. д. Лишь некоторые из них нашли применение в клинической практике (рис. 39).
| NaOOCCH —CHCOONa I I SH SH димеркаптосукцинат |
ch2-sh ch,-sh
I I
сн—sh сн—sh
I l
CH2-OH CH2-S03Na
димеркаптопропанол унитиол
сн, NH2 II
носс—ссоон l
SH
d-пенициламин
Рис. 39. Структуры некоторых комплексообразователей из групп ди- и монотиолов
В нашей стране профессором А. И. Черкесом с соавторами был разработан антидот 2,3-димеркаптопропансульфонат натрия (унитиол), тоже относящийся к группе дитиолов, лишенный недостатков БАЛ. Это вещество хорошо растворимо в воде. Широта терапевтического действия — 1:20. Унитиол, так же как БАЛ, взаимодействует в крови и тканях отравленного и со свободным люизитом, и с ядом, уже связавшимся с молекулами-мишенями. Комплекс «люизит-унитиол», называемый тиоарсени-том, малотоксичен, хорошо растворим в воде и легко выводится из организма с мочой. Под влиянием унитиола у отравленных нормализуется состояние сердечно-сосудистой системы и системы крови: восстанавливается уровень кровяного давления, коллапс и сгущение крови, как правило, не развиваются. Отмечается нормализация биохимических показателей. Лечебная эффективность антидота в известной мере определяется сроками начала лечения. Наилучшие результаты наблюдались при введении вещества в течение первых 0,5—1 ч после отравления мышьяком. Однако введение унитиола и через 4—6 ч после отравления обеспечивает выживание экспериментальных животных, отравленных абсолютно смертельными дозами яда.

ИННЕРВИРУЕМАЯ |
КЛЕТКА сигнал
Рис. 45. Схема функционирования холинергического синапса:
XP — холинорецептор; АХЭ — ацетилхолинэстераза; 1-3 — способы воздействия токсикантов на синапс: 1 — ботулотоксин; 2 — ингибиторы АХЭ; 3 — холинергические и антихолинергические средства
Установлено, что нейромедиатор и в ЦНС и в ПНС взаимодействует с двумя видами рецепторов — мускариновыми и никотиновыми, отличающимися способностью отвечать на воздействие ряда агонистов (М-хо-линорецепторы избирательно возбуждаются мускарином; Н-холиноре-цепторы — никотином), механизмом рецепции сигнала и его передачи на эффекторную клетку (нейрон, миоцит, железистую клетку). Н-холиноре-цепторы непосредственно связаны с ионными каналами постсинаптиче-ской мембраны для Na+, К+, Са2+. М-холинорецепторы также влияют на проницаемость ионных каналов для Na+ и К+. Однако это влияние опосредовано изменением активности сопряженных с рецептором ферментов, регулирующих содержание в иннервируемой клетке вторичных мес-сенджеров восприятия сигнала (цАМФ, цГМФ, фосфоинозитола и т. д.). Действие ацетилхолина на рецепторы приводит к усилению проницаемости постсинаптических мембран для ионов натрия, что сопровождается
деполяризацией мембраны и ее возбуждением. Различается скорость генерации постсинаптического сигнала: в Н-холинергических синапсах изменение конформации ионных каналов развивается практически мгновенно, а в М-холинергических — постепенно.
Прерывание нервного импульса осуществляется путем гидролиза аце-тилхолина ферментом ацетилхолинэстеразой.
В ЦНС плотность М-холинергических синапсов между нейронами существенно выше, чем Н-холинергических. Наивысшая — в хвостатом, прилежащем, чечевичном ядрах, гиппокампе, гипоталамусе, коре головного мозга, мозжечке млекопитающих и человека.
На периферии М-холинергические синапсы связывают окончания постганглионарных нервных волокон парасимпатической системы с ин-нервируемыми ими гладкомышечными волокнами (кишечника, бронхов, миокарда) и клетками экзокринных желез (слюнных, желудочно-кишечного тракта, бронхиальных, потовых).
Периферические Н-холинергические синапсы выявляются главным образом в области окончаний нервных волокон мотонейронов, иннерви-рующих поперечно-полосатую мускулатуру, волокон, иннервирующих ганглионарные нейроны парасимпатического и симпатического отделов вегетативной нервной системы, а также в каротидном клубочке, хромаф-финных клетках мозгового вещества надпочечников.
Перевозбуждение центральных холинергических механизмов может приводить к развитию судорожного синдрома. Наибольшей активностью в этом плане обладают ингибиторы АХЭ, способные проникать через ге-матоэнцефалический барьер (ФОС, карбаматы). Перевозбуждение периферических холинореактивных структур этими токсикантами сопровождается существенным, порой не совместимым с жизнью, нарушением функций дыхательной и сердечно-сосудистой систем.
12.1.1*1.1.1. Ингибиторы холинэстеразы
Фосфорорганические соединения
Фосфорорганические соединения нашли применение как инсектициды (хлорофос, карбофос, фосдрин, лептофос и др.), лекарственные препараты (фосфакол, армии и т. д.). Наиболее токсичные представители группы приняты на вооружение армий целого ряда стран в качестве боевых отравляющих веществ (зарин, зоман, табун, VX). Поражение ФОС людей возможно при авариях на объектах по их производству, при применении в качестве ОВ или диверсионных агентов.
Впервые ФОС были синтезированы Тенаром в 1846 г. В нашей стране основоположником химии ФОС был А. Е. Арбузов, предложивший в 1905 г. новый метод их синтеза. На токсические свойства этих соединений внимание было обращено только в 1932 г., когда Ланге и Крюгер впервые описали симптомы отравления диметил- и диэтилфторфосфа-том, синтезированными в процессе поиска новых инсектицидов. Бесспорная практическая значимость таких средств явилась причиной масштабных исследований, направленных на всестороннее изучение нового класса биологически активных веществ. Так, за короткий промежуток времени только в Германии, в лаборатории Шрадера, с целью изыскания все новых средств борьбы с вредными насекомыми было синтезировано и изучено более 2000 ФОС, среди которых многие обладали высокой токсичностью и для млекопитающих. Это послужило поводом для создания на их основе новых образцов химического оружия. К началу Второй мировой войны химиками Германии были синтезированы такие высокотоксичные отравляющие вещества, как табун, зарин, несколько позже — зоман. Одновременно были определены перспективы изыскания еще более токсичных для человека соединений, что на практике было реализовано Таммелином (1955), синтезировавшим метилфторфосфорилхолин, явившийся прообразом новой группы ФОВ, обозначаемых как V-газы (VX). В 70-80-х гг. XX столетия была разработана технология применения ФОВ в так называемых бинарных боеприпасах. При этом два относительно мало ядовитых химических соединения хранятся, транспортируются и размещаются в боеприпасах раздельно. Компоненты смешиваются лишь после выстрела и образуют на пути к цели в ходе химической реакции высокоядовитое ОВ. Чрезвычайно высокая токсичность и особенности физико-химических свойств, позволяющие быстро создавать обширные очаги химического заражения, до недавнего времени делали ФОВ (зарин, зоман, V-газы) наиболее опасными из всех известных ОВ. В соответствии с международными договоренностями, запасы ФОВ в большинстве стран мира подлежат уничтожению.
В настоящее время исследования в области создания все новых биологически активных веществ на основе ФОС продолжаются. Сейчас это, как и в начале 30-х гг. XX в., в основном поиск инсектицидов, которых на сегодняшний день известны сотни наименований.
Физико-химические свойства. Токсичность
| ?1 -Р—О I R2 (3) |
| OR, i X—Р—О I R2 (2) |
ФОС — производные кислот пятивалентного фосфора. Все токсичные соединения фосфорной (1), алкилфосфоновой (2) и диалкилфосфиновой (3) кислот имеют структуру:
OR, I
X—Р—О
I
OR2 (D
Фосфор с помощью двойной связи соединен с атомом кислорода или серы; двумя связями — с алкил-, алкокси-, арил-, моно- или диалкила-миногруппами и т. д. (Rb R2); пятая (X) — насыщена группой, относительно легко отщепляющейся от атома фосфора (F~, CN-, -OR, -SR и т. д.). За счет высвобождающейся при этом валентности, ФОС и взаимодействует с активными центрами ряда энзимов.
Структурные формулы некоторых ФОС представлены на рис. 46.
25Q

 |  | ||
S54
 |
V-газы
Агрегатное состояние
Молекулярный вес Плотность пара (по воздуху) Плотность жидкости Температура замерзания Температура кипения Концентрация пара (мг/м3) Скорость и температура разрушения
Скорость гидролиза
Продукты гидролиза
Растворимость в липидах Стабильность при хранении
Действие на металлы
Среднесмертельная токсодоза (ингаляционно)
Средненепереносимая токсодоза (ингаляционно)
Кожная токсичность
Средненепереносимая доза (через кожу)
Защита
Стойкость
Таблица 46
VX
Янтарного цвета жидкость, напоминающая машинное масло
267,4 9,2
1,008 (при 25° С)
Ниже -51° С
300° С
5 (при 20° С)
Период полураспада — 36 ч при 150° С; 1,6 ч-при 200° С; 36 с — при 295° С
Период полураспада при 25° С, рН 2-3 — 100 дней; рН 13— 16 мин, рН 14 — 1,3 мин
Диэтилметилфосфонат; 2-диизопропил-аминоэтилмеркаптан; при рН 7—10 продукты гидролиза токсичны
Очень высокая
Относительно стабильно при комнатной температуре
Практически отсутствует
30 мг'мин/м3
50 мг-мин/м3
Чрезвычайно токсичен при попадании на кожу и слизистые оболочки глаз. Кожу не повреждает, абсорбция быстрая. Необходима немедленная деконтаминация кожи
0,006 г/человека
Противогаз, защитная одежда
Зависит от способа применения и погодных условий. Обширные проливы жидкого ОВ персистируют на местности при обычных погодных условиях
Токсикокинетика
Отравление происходит при вдыхании паров и аэрозолей, всасывании ядов в жидком и аэрозольном состоянии через кожу, слизистую оболочку глаз, с зараженной водой или пищей — через слизистую оболочку желудочно-кишечного тракта. Высокотоксичные ФОС не обладают раздражающим действием на месте аппликации (слизистые оболочки верхних дыхательных путей и желудочно-кишечного тракта, конъюнктива глаз, кожа) и проникают в организм практически незаметно. Наивысшая скорость проникновения ядов в организм при их ингаляции, наименьшая — при действии через кожу. Но и при нанесении на кожу действующей дозы ФОС, резорбция осуществляется в течение нескольких минут (скорость зависит от строения токсиканта).
Попав в кровь, ФОС неспецифически связываются с мембранами клеток эндотелия сосудов, эритроцитов, белками плазмы крови. За счет этого некоторая часть токсикантов выключается из токсикодинамическо-го процесса. Специфично взаимодействуют вещества с активным центром карбоксилэстеразы-гидролазы, присутствующей в плазме крови человека. Это взаимодействие играет существенную роль в элиминации ФОС. Предварительное угнетение активности карбоксилэстеразы три-о-кре-зилфосфатом (ТОКФ) существенно повышает токсичность зарина и зо-мана.
Распределение веществ в организме и скорость элиминации определяются наличием или отсутствием в молекуле ФОС заряженных группировок, способностью связываться со структурными элементами крови и тканей, интенсивностью метаболических превращений. Незаряженные молекулы, к числу которых относятся практически все высокотоксичные ФОС, в том числе все ОВ, легко проникают через гематоэнцефалический барьер и оказывают токсическое действие как в центральной нервной системе, так и на периферии. Заряженные соединения, содержащие, например, аммониевые, сульфониевые группировки, обладают практически только периферическим действием.
Важными механизмами элиминации фосфорорганических соединений из организма являются реакции их метаболизма. При этом некоторые, по большей части, мало токсичные вещества способны к относительно продолжительному персистированию (карбофос — сутки и более). Наиболее токсичные представители, как правило, быстро гидролизуются, окисляются (см. выше) при участии гидролаз (фосфорилфосфатаз, флюо-рогидролаз, карбоксилэстераз, арилэстераз и т. д.) крови и тканей, микросомальных цитохром-Р-450-зависимых оксидаз смешанной функции, а затем связываются энзимом глутатион-Б-трансферазой с глутатионом. Уже спустя час после внутрибрюшинного введения экспериментальным животным в крови ФОВ определяются в следовых количествах либо не определяются вовсе. Период полуэлиминации зарина и зомана составляет около 5 мин, VX несколько больше. Осуществлять метаболизм ФОС способны практически все органы и ткани в соответствии с содержанием
и активностью в них энзимов, принимающих участие в превращениях ксенобиотиков.
Из организма выделяются только нетоксичные метаболиты веществ и потому выдыхаемый воздух, моча, кал не опасны для окружающих.
Основные проявления интоксикации
Симптомы интоксикации ФОС при ингаляционном поражении развиваются значительно быстрее, чем при поступлении через рот или кожу.
При ингаляции ФОВ смерть может наступить в течение 1—10 мин после воздействия. В случае поступления ОВТВ с зараженной пищей симптомы интоксикации развиваются в течение 0,5 ч. Резорбция с поверхности кожи действующей дозы высокотоксичных веществ происходит в течение 1—10 мин, однако скрытый период может продолжаться в течение 0,5—2 ч.
ФОС оказывают местное и резорбтивное действие. Подавляющее большинство развивающихся эффектов является следствием перевозбуждения мускарин- и никотинчувствительных холинергических синапсов центральной нервной системы и периферии.
Местное действие проявляется функциональными изменениями органов на месте аппликации: возникновением миоза и гиперемии конъюнктивы при контакте яда со слизистой оболочкой глаза; гиперемией слизистой оболочки носа и ринореей — при проникновении ФОС ингаляционным путем; тошнотой, рвотой, спастическими болями в области живота — при попадании ядов внутрь; фибрилляцией подлежащих мышечных групп, пилоэрекцией и выделением капелек пота на зараженном участке кожи. Однако все явления непродолжительны и в конечном итоге не определяют тяжести интоксикации.
Резорбтивное действие ФОС всегда сопровождается нарушениями со стороны ЦНС, жизненно важных органов и систем: дыхательной, сердечно-сосудистой, а также желудочно-кишечного тракта и др. Продолжительность этих нарушений и степень их выраженности зависят от количества яда, попавшего в организм, и в известной степени, — от путей проникновения. Интоксикации могут быть легкими, средней степени тяжести и тяжелыми.
При отравлении легкой степени обычно наблюдаются возбуждение, бессонница, головные боли, галлюцинации, чувство страха, апатия, депрессия, легкий тремор. Зрачки сужены (при поражении незащищенного человека ФОС в парообразной или аэрозольной форме). При этом нарушается зрение, особенно в темноте. Появляются головная боль, затруднение при дыхании, тошнота и другие диспептические явления. Военно-профессиональная работоспособность отравленного временно утрачивается. Пострадавший нуждается в оказании медицинской помощи. Сроки врачебного наблюдения за пораженным — от нескольких часов до 5—7 сут.
При отравлении средней степени тяжести возникают приступы удушья, напоминающие тяжелые приступы бронхиальной астмы. Поэтому такие формы отравления определяются как бронхоспастические. Приступы, как правило, возобновляются через каждые 10—15 мин, но и в промежутках между ними дыхание остается затрудненным. Отмечается усиленная секреция бронхиальных, слюнных и потовых желез. Отчетливо выражено повышение артериального давления. Отравление нередко сопровождается рвотой, поносом и схваткообразными болями в области живота. Наблюдаются фибриллярные подергивания мышц, в особенности жевательных. Чаще сознание сохранено, но чувство страха, возбуждение, эмоциональная лабильность нарушают критическое восприятие окружающей обстановки. Зрачки резко сужены. Симптомы интоксикации отмечаются в течение 2—3 сут и более. К последствиям отравления средней степени тяжести можно отнести сохраняющуюся в течение 2—3 нед эмоциональную неустойчивость, вегетативную лабильность, мышечную слабость, нарушения функций желудочно-кишечного тракта и другие признаки астено-вегетативного синдрома.
При тяжелых поражениях развивается судорожный синдром, который протекает на фоне полной утраты сознания. Если отравление не заканчивается летальным исходом от остановки дыхания в первые 10—30 мин, развивается кома. Кожа бледная, влажная, с резко выраженным акроциа-нозом. Наблюдается непрекращающаяся фибрилляция всех групп мышц, тремор. Дыхание дезорганизовано из-за периодически возникающих приступов удушья. Также отмечаются гипотензия и брадикардия. Зрачки сужены (однако миоз может сменяться мидриазом), реакция зрачков на свет отсутствует. Периодически возникают повторные приступы клони-ко-тонических судорог. Изо рта и носа выделяется пенистая жидкость. Наблюдаются непроизвольные мочеиспускание и дефекация, а в особо тяжелых случаях — развивается полная арефлексия. Смерть может наступить в течение ближайших часов или первых суток после начала отравления от остановки дыхания, реже — сердечной деятельности. При благоприятном исходе на протяжении длительного времени (1,5—2 мес и более) у таких пораженных сохраняются общая слабость, астенизация, повышенная раздражительность, нарушение сна, устрашающие сновидения, головокружение, головная боль и другие невротические расстройства, составляющие астенический симптомокомплекс. Нередко, особенно при поражении зоманом или длительно персистирующими в организме отравленного ФОС, в периоде выздоровления у пострадавших развиваются признаки нейропатий (нарушения кожной чувствительности, мышечная слабость, как правило, дистальных групп мышц). Кроме того, могут возникать пневмония, острая сердечно-сосудистая недостаточность (причина поздней гибели), нарушение функции желудочно-кишечного тракта (тошнота, расстройство стула, боли в эпигастральной области), печени и почек.
Патогенез интоксикации
Пусковым механизмом практически всех симптомов, развивающихся пРи интоксикации ФОС, является перевозбуждение никотиновых и мус-кариновых холинергических синапсов, локализованных в центральной нервной системе и на периферии (табл. 47). При тяжелых поражениях в
патологический процесс, по мере развития интоксикации, вовлекаются и нехолинергические механизмы. К числу таковых относятся: нарушение функционального состояния глутаматергической, катехоламинергических, ГАМК-ергической нейромедиаторных систем мозга, увеличение содержания в крови биологически активных веществ (гормонов, продуктов пе-рекисного окисления липидов, лейкотриенов, простагландинов, фактора агрегации тромбоцитов и т. д.), прогрессирующая гипоксия, изменение кислотно-основного состояния и электролитного баланса и т. д.
Таблица 47
| Развивающиеся эффекты |
Признаки острого поражения ФОС и механизмы их развития
Анатомическое образование
| Зрачок Цилиарное тело |
МЕСТНОЕ ДЕЙСТВИЕ Воздействие на мускаринчувствительные синепсы
Миоз, иногда максимальный (размер с «булавочную головку»), анизокория
| Слизистая оболочка носа Дыхательные пути (слизистая оболочка, гладкомышечные волокна) Кожа Желудочно-кишечный тракт (слизистая оболочка, гладкомышечные волокна) |
Боль в области глаз, нарушение дальнего зрения (спазм аккомодации)
Гиперемия, ринорея
Затруднение дыхания, кашель, бронхоспазм, усиление секреции бронхиальных желез
Локальное усиление потоотделения, пилоэрекция
Тошнота, рвота
| Дыхательные пути Желудочно-кишечный тракт Потовые железы Слюнные железы Сердце Зрачок Цилиарное тело Мочевой пузырь |
РЕЗОРБТИВНОЕ ДЕЙСТВИЕ 1. Воздействие на периферические мускаринчувствительные синапсы
Нарушение дыхания с затрудненным выдохом (как следствие бронхоспазма и повышенной секреции бронхиельных желез), диспноэ, боли в груди, кашель, отек легких
Анорексия, тошнота, рвота, схваткообразные боли в животе, боли в эпигастрии, понос, тенезмы, непроизвольная дефекация
Усиленное потоотделение
Слюнотечение
Брадикардия
Миоз, анизокория
Нарушение зрения, боли в области глаз Непроизвольное мочеиспускание
| Слабость, фасцикулляции, непроизвольные сокращения отдельных групп мышц, паралич мускулатуры (включая дыхательную) |
2. Воздействие на периферические никотинчувствительные синапсы
Произвольная мускулатура
| Окончание таблицы 47 | |
| Анатомическое образование | Развивающиеся эффекты |
| Симпатические ганглии | Бледность кожных покровов, транзиторный подъем ертериального давления, сменяющийся гипотензией |
| 3. Воздействие на центральные холинергические синепсы | |
| Остро развивающиеся эффекты | Общая слабость, гипотермия, потеря сознания, судороги, кома, угнетение дыхательного и сосудо-двигательного центров (диспноэ, цианоз, гипотензия, остановка дыхания) |
| Отсроченные эффекты | Головокружение, напряженность, беспокойство, возбуждение, эмоциональная лабильность, бессонница, кошмарные сновидения, головная боль, тремор, депрессия, заторможенность, затруднение концентрации внимания, спутанность сознания, нарушение речи, атаксия |
| 4. Нехолинергические мехенизмы | |
| Остро развивающиеся эффекты | Прогрессирующая кома, тканевая гипоксия, ацидоз, отек мозга |
| Отсроченные эффекты | Нарушение функций печени и почек, пневмония, невропатии, энцефалопатия |
Особое значение в патогенезе интоксикации придают гипоксии, носящей смешанный характер. В результате бронхоспазма, бронхореи, угнетения дыхательного центра и слабости дыхательной мускулатуры развивается расстройство легочной вентиляции, что приводит к недостаточному насыщению артериальной крови кислородом и формированию гипокси-ческой гипоксии. Если бронхоспазм появляется рано (в результате местного действия ФОС), то уже через несколько минут после начала отравления происходит снижение степени насыщения артериальной крови кислородом. При возникновении судорог снижение прогрессирует. Вследствие гипотонии и брадикардии, замедления скорости кровотока и ухудшения микроциркуляции появляются застойные явления и также нарушается снабжение тканей кислородом — возникает и циркуляторная гипоксия. Наконец, по мере углубления нарушений биоэнергетических процессов, накопления в тканях недоокисленных продуктов, развития ацидоза, ткани утрачивают способность утилизировать кислород, доставляемый кровью — развивается тканевая гипоксия. Кислородная недостаточность занимает важное место в патогенезе отравления ФОС, во многом определяя и степень тяжести, и исход интоксикации.
В основе отдаленных последствий острых отравлений может лежать иммунотоксическое действие ФОС. Так, иммуносупрессия может стать причиной развивающихся пневмоний, а инициация аутоиммунного процесса и угнетение активности нейрэстеразы (фермента, необходимого Для обеспечения обменных процессов в нервных волокнах) — нейро- и энцефалопатии.
26Q
Механизм токсического действия
Как указывалось, практически все эффекты, выявляемые на начальных этапах развития интоксикации ФОС, могут быть объяснены явлением гиперактивации холинергических механизмов передачи нервного импульса в ЦНС и на периферии. В основе феномена, как установлено, лежит способность токсикантов угнетать активность ацетилхолинэстера-зы, а также некоторые другие механизмы действия на холинергические структуры, в частности, непосредственное взаимодействие с холинорецепторами, сопровождающееся прямым холиномиметическим эффектом и повышением чувствительности холинорецепторов к ацетилхолину и негидролизуемым холиномиметикам (холиносенсибилизирующее действие).
Антихолинэстеразное действие. ФОС являются ингибиторами ацетил-холинэстеразы (АХЭ), практически необратимо взаимодействующими с ее активным центром. В результате их действия угнетается процесс разрушения ацетилхолина в синапсах. Так, при отравлении ФОС существенно возрастает содержание ацетилхолина в мозге (более чем в три раза; нормальное содержание — 2,4 мкг/г ткани). Медиатор накапливается в синаптиче-ской щели и вызывает стойкое перевозбуждение постсинаптических холинергических рецепторов (непрямое холиномиметическое действие. ФОС). Перевозбуждение холинорецепторов избытком ацетилхолина приводит к стойкой деполяризации постсинаптических мембран иннервируемых клеток. Это, в свою очередь, первоначально сопровождается гиперактивацией центральных и периферических М- и Н-холинореактивных механизмов передачи нервных импульсов, а затем, в случае крайне тяжелого отравления, — блоком проведения нервного импульса, преимущественно в Н-хо-линергических синапсах. Таким образом, отравление ФОС, по сути — отравление эндогенным ацетилхолином, накапливающимся в крови и тканях вследствие прекращения его разрушения ферментом ацетилхолинэсте-разой.
С антихолинэстеразной теорией согласуются факты, свидетельствующие о существовании параллелизма между токсичностью ФОС и их способностью угнетать активность фермента in vitro, степенью угнетения холинэстеразы различных органов и выраженностью развивающихся эффектов. Легкое поражение ФОС, как правило, развивается при угнетении АХЭ более чем на 40%, средней степени тяжести — более 70%, тяжелой — около 90%.
Способность ФОС взаимодействовать с активным центром энзима объясняют структурным сходством молекул ядов с молекулой ацетилхолина. Некоторые ФОС (зарин, диизопропилфторфосфат и др.) имитируют сложноэфирную часть молекулы медиатора, поскольку группировка (Р=0) поляризована так же, как и карбонильная (С=0) группа ацетилхолина. Другие ФОС (например, фосфорилхолины) могут имитировать как эфирную, так и катионную часть ацетилхолина. При этом катионная головка, взаимодействуя с анионным участком активного центра фермента, обеспечивает ориентацию на нем токсиканта, а фосфорсодержащая часть молекулы яда взаимодействует с эстеразным центром. И в первом и во втором случае взаимодействие ФОС с активным центром ацетилхолин-эстеразы приводит к образованию прочной ковалентной связи атома фосфора с гидроксильным радикалом серина, входящего в структуру эс-теразного участка активного центра холинэстеразы, вызывая его фосфо-рилирование.
Таким образом, можно представить, что взаимодействие фермента с ФОС проходит по тому же механизму, что и с ацетилхолином. Взаимодействие ацетилхолина, зарина и VX с активным центром холинэстеразы показано на рис. 47.
+ .снз *■ |
сн3-с—О—CH2CH2-N—сн3 сн3-с
"I чсн3 1|
о о
/Т
он
| СН3-Р-0-С(СНз)2 о |
F
I
CHj-P—0-С(СНз)2 и
о
СН,-Р—S—CHЈH2-N(C3H7)2 СН3-Р—О—CzHs
О' ОС2Н5 |l
о
Рис. 47. Схемы взаимодействия ацетилхолина, зарина и фосфорилтиохолина с активным центром ацетилхолинэстеразы
Чем выше структурное сходство ФОС с ацетилхолином, тем, как правило, выше его антихолинэстеразная активность и токсичность.
Принципиальное различие во взаимодействии ацетилхолина и ФОС с АХЭ состоит в том, что реакция декарбоксилирования активного центра после гидролиза ацетилхолина проходит практически мгновенно и энзим снова восстанавливает способность взаимодействовать с субстратом, а дефосфорилирование — протекает медленно. Причем с течением времени изначально обратимая связь ФОС — АХЭ, которая может разрушаться спонтанно («спонтанная реактивация») или с помощью некоторых веществ, вводимых отравленному (реактиваторы АХЭ), становится необратимой, неспособной к разрушению. Таким образом, взаимодействие
2вг
часть i. i и кии кили i ни
Глава 12. ОТРАВЛЯЮЩИЕ И ВЫСОКОТОКСИЧНЫЕ ВЕЩЕСТВА НЕИРОТОКСИЧЕСКОГО ДЕЙСТВИЯ
ФОС и АХЭ проходит в две фазы и может быть представлено следующим образом:
ФОС + АХЭ ^ ■ w ФОС АХЭ *• ФОС:АХЭ
Процесс превращения образовавшейся в'первой фазе обратимо фос-форилированной холинэстеразы в необратимо связанную форму называется «старением» фосфорилхолинэстеразы. Скорость как «спонтанной реактивации» АХЭ (и самопроизвольное восстановление ее активности), так и «старения» зависит от структуры ФОС, а именно от строения алки-льных радикалов при атоме фосфора. Чем «тяжелее» радикалы, тем ниже скорость «спонтанной реактивации» и выше скорость «старения». Поэтому АХЭ, ингибированная VX (R -ОС2Н5), стареет чрезвычайно медленно, зарином (R -ОСН(СНз)2) — в течение нескольких часов, зоманом (R -ОСНСНзС(СНз)з) — в считанные минуты. В основе «старения» лежит процесс отщепления от атома фосфора, связанного с активным центром энзима, алкильных радикалов. При этом одновременно изменяется конформация белковой части энзима (с этим, вероятно, связано то обстоятельство, что фосфорилированные одним и тем же веществом холинэстеразы, выделенные из тканей разных млекопитающих, «стареют» с разной скоростью).
В настоящее время обнаружены соединения (гидроксиламин, гидро-ксамовые кислоты, оксимы), способные, взаимодействуя с остатком ФОС, связанного с АХЭ, отрывать его от молекулы энзима (если не произошло его «старение») и тем самым восстанавливать ферментативную активность. Такие вещества, получившие название реактиваторов холинэстеразы, при своевременном введении отравленному существенно ослабляют выраженность токсического процесса, что подтверждает справедливость антихолинэстеразной теории действия ФОС.
Даже ингибированная VX ацетилхолинэстераза, «стареющая» с минимальной скоростью, а «спонтанно реактивирующаяся» относительно быстро, дефосфорилируется в течение нескольких суток. Вот почему ФОС называют необратимыми ингибиторами холинэстеразы. In vitro способность ФОС угнетать АХЭ уменьшается при увеличении концентрации в инкубационной среде естественного субстрата энзима — ацетилхолина. По этой причине ФОС называют также конкурентными ингибиторами АХЭ. За активный центр энзима ФОС конкурируют не только с ацетил-холином, но и с ингибиторами энзима из других классов соединений, в частности с карбаматами. Последние вызывают обратимое карбамидиро-вание активного центра АХЭ и потому называются обратимыми ингибиторами АХЭ. Установленная в опытах in vitro и in vivo способность обратимых ингибиторов холинэстеразы (прозерина, галантамина и т. д.) защищать холинэстеразу от угнетения ФОС, предупреждать действие этих ядов на органы и системы и тем самым препятствовать развитию интоксикации используется на практике при разработке профилактических антидотов ФОС (см. ниже).
Холинэстеразная активность выявляется не только в синаптических структурах, но и в крови млекопитающих и человека. Причем в мембране эритроцитов содержится ацетилхолинэстераза, по сути идентичная энзиму нервной ткани, а в плазме крови — бутирилхолинэстераза, отличающаяся от АХЭ более высоким сродством к эфирам холина и жирных кислот с большей молекулярной массой, чем ацетат (например, бутирилхолину — эфиру холина и масляной кислоты). ФОС при поступлении в организм угнетают оба типа холинэстераз крови. Степень инактивации энзимов пропорциональна степени угнетения активности синаптической ацетил-холинэстеразы. Это явление используется для диагностики интоксикации ФОС, а также для верификации степени тяжести поражения. При отсутствии иных причин, снижение активности холинэстеразы крови более чем на 50% свидетельствует об интоксикации антихолинэстеразными ядами. При необходимости контролировать состояние синаптического энзима, для исследования можно изучать активность АХЭ в эритроцитах, выделенных методом центрифугирования.
Способность ФОС угнетать холинэстеразу используют также для индикации ФОС в воде, продовольствии и т. д. (биохимический метод индикации).
Действие на холинорецепторы. Из возможных неантихолинэстеразных механизмов наиболее важным является действие ФОС на холинорецепторы. Поскольку и холинорецепторы, и холинэстераза адаптированы к одному и тому же нейромедиатору, ингибиторы холинэстеразы могут проявить активность и по отношению к холинорецепторам.
По-видимому, блокада проведения нервно-мышечного сигнала, развивающаяся при смертельной интоксикации ФОС, связана не только со стойким деполяризующим действием избыточного количества ацетилхолина, но и с прямым действием ФОС на нервно-мышечные синапсы (по типу действия деполяризующих миорелаксантов). Так, в эксперименте на изолированном нервно-мышечном препарате млекопитающего, при внесении в инкубационную среду достаточной дозы ФОС, наблюдается полное прекращение передачи нервного импульса с нервного волокна на мышцу. Однако через некоторое время на фоне практически «тотального» угнетения активности холинэстеразы отмечается восстановление нервно-мышечной проводимости в синапсах. Повторно блок можно вызвать вновь добавив ФОС в инкубационную среду.
Сенсибилизирующее действие на холинорецептор зарина, ДФФ и других ФОС проявляется, в частности, существенным повышением чувствительности отравленных экспериментальных животных к холиноми-метикам, негидролизуемым ацетилхолинэстеразой (никотину, ареколину и т. д.). Установлено, что сенсибилизация к М-холиномиметикам (ареколину) сохраняется значительно дольше, чем к Н-холиномиметикам (никотину). Причины различия, вероятно, обусловлены особенностями проведения нервных импульсов в М- и Н-холинергических синапсах (см. выше).
Восстановление нормального проведения нервного импульса у лиц, перенесших интоксикацию ФОС, осуществляется за счет медленно протекающих процессов дефосфорилирования АХЭ («спонтанная реактивация»), синтеза АХЭ в перикарионе нервных клеток de novo и транспорта ее в нервные окончания, снижения содержания ацетилхолина в синапти-ческой щели, десенситизации холинорецепторов (понижение чувствительности к ацетилхолину).
Нехолинергические механизмы токсического действия. Помимо действия на холинореактивные структуры, ФОС в высоких дозах обладают прямым повреждающим действием на клетки различных органов и тканей (нервной системы, печени, почек, системы крови и т. д.), в основе которого лежат общие механизмы цитотоксичности: нарушение энергетического обмена клетки; нарушение гомеостаза внутриклеточного кальция; активация свободнорадикальных процессов в клетке; повреждение клеточных мембран. Чем менее токсично ФОС, тем значимее роль указанных механизмов в развитии проявлений тяжелого поражения данным токсикантом. Существуют ФОС, полностью лишенные антихолинэсте-разной активности, токсичность которых обусловлена исключительно их цитотоксическим действием (три-о-крезилфосфат). Клиническая картина отравления такими веществами полностью отличается от описанной выше.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты кожи; средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение частичной санитарной обработки (использование ИПП) в зоне химического заражения;
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
• применение профилактических антидотов перед входом в зону химического заражения и контактом с пораженными, поступающими из очага.
Специальные лечебные мероприятия:
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим; • подготовка и проведение эвакуации.
Медицинские средства защиты
К числу средств медицинской защиты относятся:
1. Средства, предотвращающие поступление веществ в организм
через кожу — индивидуальные противохимические пакеты
(ИПП — см. гл. 25. «Специальная обработка в подразделениях
и частях медицинской службы»).
2. Медикаментозные средства медицинской защиты.
Медикаментозные средства представлены препаратами, назначаемы-
ми с целью профилактики поражения, само- и взаимопомощи, раннего
(догоспитального) лечения. Сюда относятся этиотропные, патогенетиче-
ские и симптоматические средства.
Этиотропные средства защиты (антидоты).
Разработка этиотропных средств защиты — специфических противоядий (антидотов) ФОВ, долго считавшихся основным видом химического оружия, началась сразу после Второй мировой войны и продолжается до настоящего времени. Основные направления исследований в области разработки медицинских средств защиты представлены в табл. 48.
Таблица 48
Основные направления разработки средств медицинской защиты от фосфорорганических отравляющих веществ (по С. Н. Голикову и соавт., 1972)
| Направление | Препараты |
| Защита холинорецепторов | Холинолитические (антихолинергические) средства |
| Реактивация холинэстеразы | Оксимы |
| Защита холинэстеразы от необратимого угнетения ФОС | Обратимые ингибиторы холинэстеразы |
| Нейтрализация ФОС | Оксимы; специфические антитела |
| Ускорение метаболизма ФОС | Индукторы микросомальных ферментов |
| Возмещение холинэстеразы | Препараты очищенной холинэстеразы |
| Подавление синтеза и высвобождения ацетилхолина | Производные дифенилгликолятов, гемихолиний |
Холинолитики как антидоты ФОС. Как известно, вещества различного строения имеют неодинаковую способность проникать через гемато-энцефалический барьер. Поэтому все холинолитики подразделяются на центральные (проникающие через ГЭБ: амизил, тропацин и др.) и периферические (непроникающие через ГЭБ). Неодинаково и сродство веществ с различным строением к рецепторам разных типов. По этому показателю антихолинергические препараты разделяют на М-холинолитики (атропин, скополамин, метацин и др.) и Н-холинолитики (пентамин, бензогексоний, мекамиламин и др.).
Холинолитики (антихолинергические средства) являются физиологическими антагонистами ФОС в действии на холинергические синапсы. Они связываются с постсинаптическими рецепторами, защищая их от гиперактивации ацетилхолином, накапливающимся в избытке в синапти-ческой щели.
Как указывалось ранее, ингибирование ацетилхолинэстеразы, развивающееся при отравлении ФОС, приводит к накоплению нейромедиатора в холинергических синапсах всех типов: центральных и периферических, мускарин- и никотинчувствительных. Поэтому при интоксикации ФОС с целью защиты изучалась антидотная активность холинолитиков разных Типов (С. В. Аничков, С. Н. Голиков, М. Я. Михельсон, Н. В. Са-ватеев и др.). В результате многолетних исследований удалось установить ряд закономерностей:
1. Ни один из представителей различных групп холинолитиков не является полным антагонистом ФОС, так как, блокируя лишь определенный тип рецепторов, устраняет эффекты, инициируемые возбуждением только рецепторов этого типа.
2. Чувствительность отравленных к холинолитикам резко снижается и для получения антидотного эффекта препараты следует вводить в дозах, во много раз превосходящих фармакопейные. t
3. Продолжительность действия холинолитиков в организме (блокада М- и Н-холинорецепторов) не велика, а на фоне тяжелой интоксикации ФОС еще более сокращается и, как правило, в среднем составляет не более 1—3 ч. Это указывает на необходимость повторного назначения холинолитиков при отравлениях.
4. Наибольший защитный эффект удается получить при раннем использовании комплекса холинолитиков, связывающихся как с центральными, так и периферическими М- и Н-холинорецепторами. Однако в то время как симптоматика, обусловленная возбуждением М-холинорецеп-торов, сохраняется длительное время (дни), нарушения, связанные с активацией Н-холинорецепторов, отмечаются сравнительно непродолжительное время (часы). Поэтому по мере развития токсического процесса эффективность Н-холинолитиков быстро снижается и потребность в их назначении исчезает.
5. При раннем назначении отравленным препаратов отдельных групп наибольшая антидотная активность выявляется у центральных холинолитиков (амизил, скополамин, циклодол и т. д.). Однако активность этих средств на периферии выражена менее отчетливо. Поскольку всегда существует необходимость повторного введения препаратов, в том числе и для устранения периферических эффектов, возникает опасность их побочного действия на центральную нервную систему. Поэтому при создании профилактических противоядий предпочтение отдают центральным холинолитикам, а лечебных — препаратам периферического действия.
Выявленные закономерности позволили разработать тактику использования холинолитиков при поражениях ФОС. В состав профилактических средств и средств само- и взаимопомощи, назначаемых при появлении первых признаках интоксикации, они входят в качестве важнейших компонентов соответствующих рецептур (см. ниже), а для целей лечения пораженных используются в виде самостоятельных препаратов.
В течение длительного времени препаратом выбора для лечения отравленных ФОС является атропин. Этот препарат был предложен уже через несколько недель после окончания Второй мировой войны и захвата арсеналов химического оружия немецкой армии. Будучи М-холиноли-тиком преимущественно периферического действия, атропин устраняет такие проявления интоксикации, как бронхоспазм, бронхорея, брадикардия, тошнота, рвота, боли в животе, понос, гиперсаливация и т. д. Однако атропин не защищает никотиновые рецепторы от токсического действия ФОС и, следовательно, не устраняет явления, связанные с перевозбуждением нейронов симпатических ганглиев (нарушения гемодинамики и т. д.), нервно-мышечных синапсов (фасцикулляции, паралич мускулатуры). Атропин обладает слабой противосудорожной активностью.
Доза и схема назначения атропина отравленным определяются по клиническим показаниям.
Для устранения проявлений местного действия ФОС на орган зрения (спазма аккомодации) несколько капель 0,1% раствора препарата вносят в конъюнктивальный мешок.
При легкой интоксикации вещество вводят внутримышечно в дозе 2 мг. При необходимости (сохранение или рецидив симптоматики) инъекции повторяют каждые 30 мин до появления признаков легкой переат-ропинизации (сухость и покраснение кожных покровов, прекращение саливации, расширение зрачка, учащение пульса).
При отравлении средней степени тяжести внутримышечно вводят 4 мг атропина, а затем каждые 10 мин по 2 мг вещества до полного прекращения симптоматики и появления признаков легкой атропинизации (см. выше). Иногда пострадавшие нуждаются в ведении вещества в течение 2 сут.
Тяжело пораженному ФОС желательно внутривенно (или внутримышечно) ввести 4—6 мг атропина, а затем через каждые 5-10 мин повторять инъекцию в дозе 2 мг. По существующим данным, в течение первых суток может потребоваться до 100 мг и более атропина.
Необходимость введения атропина в больших дозах делает чрезвычайно опасным случайное (ошибочное) его назначение неотравленным людям (неправильный диагноз, паника и т. д.). В таких случаях развиваются признаки отравления антидотом: покраснение кожных покровов, сухость во рту, жажда, мидриаз, ухудшение зрения вблизи (паралич аккомодации), тахикардия, головокружение, нарушение ориентации, галлюцинации. Плохая переносимость препарата здоровым человеком делает невозможным его использование как средства индивидуальной защиты, выдаваемого бойцу на руки.
Еще одна опасность связана с введением атропина тяжелопоражен-ным в поздние сроки на фоне выраженной гипоксии. В этом случае возрастающая чувствительность миокарда к симпатомиметическим влияни
ям может стать причиной смертельной фибрилляции желудочков сердца при блокаде атропином окончаний блуждающего нерва. Для предупреждения этого осложнения введению препарата должны предшествовать мероприятия по устранению гипоксии.
Антидотными свойствами помимо атропина обладают и многие другие холинолитики, особенно, как указывалось, с выраженным действием на центральную нервную систему. Перечень холинолитических средств, рекомендуемых для лечения отравлений ФОС, представлен в табл. 49.
тивации. Фармакологические препараты, способные ускорять этот процесс, называются реактиваторами холинэстеразы и являются биохимическими антагонистами ФОС. Первым веществом, для которого была показана реактивирующая способность, был гидроксиламин (Виллсон, 1951), затем последовали производные гидроксамовой кислоты и, наконец, в качестве средств оказания помощи пораженным, были предложены оксимы, менее токсичные и более активные вещества, содержащие в молекуле оксимную группировку (-HC=N-OH). К числу наиболее известных реактиваторов холинэстеразы относятся пралидоксим (2-ПАМ), дипи-роксим (ТМБ-4), токсогонин (LuH-б) (рис. 48).
СН—NOH СН—NOH СН—NOH СН—NOH
 |
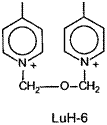
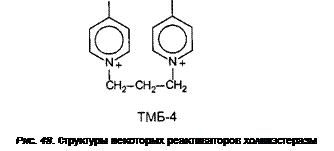

Помимо классических холинолитиков, выраженным центральным и периферическим антихолинергическим действием обладают препараты и других фармакологических групп: некоторые нейролептики, антидепрессанты, главным образом производные тиоксантена (хлорпротиксен и др.) и фенотиазина (аминазин, фторацизин и др.). Фторацизин является компонентом профилактических антидотов ФОВ (П-6, П-10М).
Некоторые миорелаксанты (Н-холинолитики), например мекамила-мин, потенцируют профилактическую эффективность рецептур, включающих М-холинолитики и обратимые ингибиторы холинэстеразы.
Реактиваторы холинэстеразы. Восстановление каталитической активности холинэстеразы, угнетенной ФОС, определяется как процесс реак-
СН3
2-ПАМ
Биохимический механизм процесса реактивации холинэстеразы (Е) схематично представлен на рис. 49.
О
l/Ri
R—СН—N—ОН +
.R-i Е
R—СН—N—О— + I
U К2 ОН
Рис. 49. Дефосфорилирование холинэстеразы с помощью оксима
В результате нуклеофильной атаки оксимной группы на фосфорили-рованный энзим разрывается ковалентная связь между атомом фосфора ФОС с кислородом серина активного центра холинэстеразы и образуются новое соединение — фосфорилированный оксим и свободный энзим.
Реактивация ингибированных холинэстераз как in vitro, так и in vivo характеризуется двумя показателями: скоростью, т. е. количеством восстановленного энзима в единицу времени, и уровнем реактивации — максимальным количеством дефосфорилированного фермента, которое можно получить обрабатывая фосфорилированную холинэстеразу реак-тиватором. Эти характеристики зависят от структуры ФОС, строения ре-активатора и времени, прошедшего с момента взаимодействия ФОС с активным центром холинэстеразы. Например, скорость реактивации холинэстеразы эритроцитов человека, ингибированной зарином, под влиянием 2-ПАМ в 10 раз выше, чем холинэстеразы, угнетенной ДФФ. Феномен может быть следствием влияния стерических (пространственно-структурных) факторов. Так, при реактивации холинэстеразы, ингибированной веществами с сильно разветвленными алкильными радикалами (ДФФ), затрудняется образование связи между атомом фосфора и кислородом оксимной группы, без чего невозможна реактивация.
Из известных реактиваторов наивысшей активностью обладают биспи-ридиниевые соединения (содержат два пиридиновых кольца в молекуле): ТМБ-4, токсогонин и др. Слабой реактивирующей и антидотной активностью, несмотря на способность проникать через ГЭБ, обладают реактива-торы, не содержащие в молекуле пиридиновых радикалов с четвертичным азотом: диацетиламиноксим (ДАМ-оксим), изонитрозин и др.
Как указывалось ранее, холинэстеразы, ингибированные ФОС, с течением времени приобретают устойчивость к воздействию реактиваторов. Это явление получило название «старения» фосфорилхолинэстераз. Поэтому на реактивационный эффект при действии оксимов можно рассчитывать только при условии их применения в первую (обратимую) фазу торможения, продолжительность которой, в зависимости от строения действующих ФОС, будет значительно различаться (минуты — часы). Наиболее устойчивой к реактиваторам является быстро «стареющая» хо-линэстераза, ингибированная зоманом.
Помимо дефосфорилирования холинэстеразы и восстановления ее активности, реактиваторы способны деблокировать (десенсибилизировать) холинорецепторы и восстанавливать их функцию, разрушать ФОС при непосредственном взаимодействии.
Деблокирующее действие реактиваторов достаточно подробно изучено на мионевральных синапсах. Так, показано, что с помощью 2-ПАМ, ТМБ-4 удается устранять блок проведения на нервно-мышечном препарате диафрагмы крысы, вызванный зоманом или метилфторфосфорилхо-лином. Этот факт нельзя объяснить реактивацией холинэстеразы, так как яды образуют с ферментом практически нереактивируемый комплекс.
Десенсибилизирующее действие оксимов проявляется способностью снижать возникающую при действии ФОС повышенную чувствительность Н-холинорецепторов (центральной нервной системы, вегетативных ганглиев) к холиномиметикам, не гидролизуемым холинэстеразой. Полагают, что и деблокирующее и десенсибилизирующее действие оксимов на Н-холинорецепторы осуществляется за счет расщепления комплекса ФОС — холинорецептор.
Некоторые оксимы (2-ПАМ, ТМБ-4) обладают Н-холинолитической активностью (курареподобным действием), что также играет роль в их способности устранять нервно-мышечный блок.
Один из механизмов защитного действия реактиваторов связан с прямой нейтрализацией (разрушением) яда, циркулирующего в крови. Суть явления состоит в том, что оксимы образуют связь с атомом фосфора, замещая при этом подвижную группу в молекуле ФОС. При этом образуется комплекс яда с оксимом, который, распадаясь, дает уже неактивное соединение. Однако в некоторых случаях скорость распада продукта взаимодействия ФОС — оксим мала. При этом в организме накапливается вещество, обладающее порой высокой токсичностью. Поэтому в практике оказания помощи отравленным следует избегать введения неоправданно большого количества оксимов.
В последнее время появились сообщения о способности реактиваторов холинэстеразы восстанавливать активность карбоксилэстеразы крови и тканей, что важно, поскольку при отравлении ФОС этот фермент играет существенную роль в детоксикации ядов.
Под влиянием реактиваторов холинэстеразы ускоряется восстановление сознания у пораженных, ослабляется выраженность бронхоспазма, спазма кишечника, ослабляются или прекращаются фибриллярные мышечные подергивания, предупреждается развитие мышечной слабости, нормализуется функция нервно-мышечных синапсов и восстанавливается деятельность дыхательной мускулатуры, что в свою очередь приводит к ослаблению гипоксии.
Изложенные представления о механизмах антидотного действия оксимов определяют тактику их применения.
Необходимостью раннего введения обусловлено включение реактива-тора холинэстеразы в состав антидота само- и взаимопомощи АЛ-85 (см. ниже). В качестве лечебных антидотов реактиваторы применяют при отравлениях средней степени тяжести и тяжелых поражениях ФОС.
В опытах на животных показано, что минимальной действующей концентрацией пралидоксима (2-ПАМ) в крови является 4 мг/мл. Внутривенное введение препарата со скоростью 500 мг/ч обеспечивает поддержание концентрации в плазме крови 15 мг/мл. Для достижения действующей концентрации препаратов в крови и тканях человека и поддержания ее на этом уровне в течение необходимого времени (около 1,5 ч) рекомендуют повторно, с интервалом 20 мин вводить внутривенно (или внутримышечно) 500-2000 мг пралидоксима (2-ПАМ) или 150-250 мг дипироксима (ТМБ-4). При необходимости инъекции можно повторить спустя 4-6 ч после первого введения. Возможно внутривенное капельное введение препаратов в указанных дозах со скоростью: 2-ПАМ — 100 мг/мин, ТМБ-4 — 25 мг/мин. Более высокие дозы оксимов или более частое и длительное их применение не только не оправдано, но может привести к осложнениям, обусловленным способностью образовывать с ФОС стойкие токсичные комплексы, миорелаксирующим действием оксимов.
При лечении острых отравлений ФОС реактиваторы холинэстеразы применяются в сочетании с холинолитическими веществами. В эксперименте установлено, что при применении атропина или других холинолитиков (например амизила, пентафена) вместе с оксимами наблюдается
эффект потенцирования. Это выражалось в увеличении антидотной мощности противоядий и в ускорении восстановления нарушенных функций.
На снабжении армии США принят реактиватор холинэстеразы пра-лидоксим (2-ПАМ). При чрезвычайных ситуациях на руки бойцу выдают 3 автоинъектора с пралидоксимом, каждый содержит 600 мг оксима. Препараты рекомендуют вводить при появлении первых признаков поражения. Отечественной наукой разработан эффективный, отличающийся высокой реактивационной способностью биспиридиноксим — карбо-ксим.
Обратимые ингибиторы холинэстеразы. В 1946 г. Костер показал, что предварительное введение физостигмина (алкалоид растительного происхождения) существенно повышает резистентность экспериментальных животных к ДФФ, а Келле в том же году связал этот эффект со способностью алкалоида защищать активный центр АХЭ от действия яда. Этим было положено начало изучения еще одной группы биохимических антагонистов ФОС — обратимых ингибиторов холинэстеразы. Эти вещества, как правило, являются производными карбаминовой кислоты (NH2COOH) и потому нередко называются карбаматами (рис. 50).
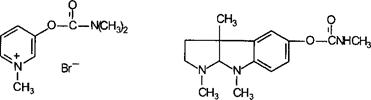
пиридостигмин физостигмин
Рис. 50. Структуры некоторых обратимых ингибиторов холинэстеразы
В настоящее время установлено, что профилактическое введение обратимых ингибиторов, как проникающих (физостигмин, галантамин, аминостигмин), так и непроникающих (пиридостигмин) через ГЭБ, обеспечивает защиту экспериментальных животных от высокотоксичных ФОС. Наибольшей активностью обладают проникающие через ГЭБ третичные карбаматы (физостигмин, галантамин, аминостигмин и др.).
Структурно эти вещества напоминают естественный субстрат энзима — ацетилхолин, однако как катионная, так и кислотная часть молекулы ингибитора имеют большую массу, чем соответствующие фрагменты молекулы субстрата. За счет этого осуществляется относительно прочная фиксация веществ на активном центре фермента (карбамилирование активного центра), что и лежит в основе его ингибирования. Поскольку комплекс фермент — ингибитор достаточно быстро спонтанно разрушается (как правило, в течение 6 ч), карбаматы называют конкурентными, обратимыми ингибиторами холинэстеразы. Обратимость в действии кар-баматов на фермент отличает их от ФОС.
Профилактический эффект при воздействии ФОВ наблюдается при введении обратимых ингибиторов в дозах, вызывающих угнетение холинэстеразы на 40% и более. В этих условиях ФОС, попавшее в организм, в значительно меньшей степени угнетает активность холинэстеразы, поскольку активные центры энзима в момент воздействия яда защищены карбаматом и накапливающимся в синаптической щели ацетилхолином. В дальнейшем ФОС быстро разрушается в организме, а карбамат покидает активный центр холинэстеразы, активность которой восстанавливается. При этом подъем уровня ацетилхолина в тканях защищенного не столь выражен и значительно менее продолжителен. Так, на фоне тяжелой интоксикации зоманом повышенное содержание ацетилхолина в мозге крыс отмечается в течение 5-6 ч. При профилактическом введении физостигмина нормализация уровня ацетилхолина происходит в течение 30 мин.
Человек бессимптомно переносит карбамилирование 20-30% ацетил-холинэстеразы. Поэтому для предотвращения развития неблагоприятных эффектов, связанных с угнетением холинэстеразы обратимым ингибитором, и защиты холинорецепторов в состав профилактических антидотов дополнительно вводят холинолитики.
В США препаратом выбора является четвертичный карбамат, не проникающий через ГЭБ — пиридостигмин. Препарат выпускается в таблетках по 30 мг вещества в каждой. Продолжительность защитного действия — 6—8 ч. •
В состав отечественных профилактических антидотов входит аминостигмин, вещество проникающее через ГЭБ и, следовательно, защищающее не только периферические, но и центральные холинергические синапсы.
Индукторы микросомальных ферментов. Поскольку ФОВ метаболизи-руют в организме при участии микросомальных ферментов с образованием нетоксичных продуктов, в 60-е годы прошлого века была высказана идея о возможности использовать для целей профилактики вещества, активирующие эту группу энзимов — индукторы микросомальных ферментов (Рыболовлев Р. С, Линючев М. Н. и др.). Препаратом выбора долгое время считался бензонал (производное барбитуровой кислоты), не обладающий снотворным действием и потому не снижающий военно-профессиональную работоспособность. Вещество рекомендовали к приему в течение 3 сут, после чего примерно на неделю резистентность организма к действию ФОВ (по данным на экспериментальных животных) возрастала в 1,5 и более раз. В настоящее время к этой группе средств профилактики отношение достаточно настороженное, поскольку при чрезвычайных ситуациях причиной поражения человека чаще могут стать не ФОС, а другие вещества, некоторые из которых усиливают свою токсичность в организме в процессе метаболизма.
Другие этиотропные средства. Препараты с иными механизмами антагонизма с ФОС (см. табл. 48) при их изучении показали слабую эффективность или плохую переносимость и потому не нашли применения в военно-медицинской практике. Наиболее продуктивно изучалась возможность создания средств иммунной профилактики поражения ФОВ на основе получения антител к ним. Теоретически такой подход может быть использован применительно к любому токсиканту, на основе которого может быть синтезирован комплексный антиген (токсикант или его фрагмент, связанный с высокомолекулярной иммуногенной группой). В настоящее время в эксперименте показана возможность создания антидотов на рассматриваемом принципе в отношении некоторых фосфорорганических соединений (зомана, малатиона, фосфакола и др.). Однако на практике существуют значительные ограничения возможности использования антител (в том числе моноклональных) в целях лечения и профилактики интоксикаций (см. гл. 6. «Антидоты. Общие принципы оказания неотложной помощи отравленным»).
Симптоматические и патогенетические средства, применяемые с целью медицинской защиты при поражении ФОС. Необходимость применения средств симптоматической и патогенетической терапии для целей медицинской защиты от ФОС определяется прежде всего тем обстоятельством, что среди противоядий не существует «абсолютного» антагониста этих ядов в действии на биологические системы. Кроме того, средства медицинской защиты и лечебные антидоты оказываются эффективными лишь при своевременном (раннем) введении. Появление симптоматики свидетельствует о развитии патологического процесса, и в этих условиях устранение пускового звена (нормализация состояния холинореактивных структур) совсем не означает устранение проявлений, которые могут, быть следствием вторичных патохимических и патофизиологических процессов. Наиболее ранимой в этом плане является функция ЦНС. Спасти жизнь пострадавшему оказывается проще, чем сохранить его профессиональную работоспособность, так как перевозбуждение холинерги-ческих механизмов быстро перерастает в полимедиаторную патологию за счет тесного структурно-функционального взаимодействия различных нейромедиаторных систем мозга. Поэтому при поражении ФОС в высоких дозах клиническая картина интоксикации может развиться несмотря на своевременное применение этиотропных средств защиты. Во всех этих случаях необходимо использовать значительно больший арсенал средств и методов терапии, с помощью которых только и удается оказать помощь пострадавшему: спасти жизнь, сохранить здоровье. Группы препаратов, используемые для указанных целей, представлены в табл. 50.
Из препаратов, представленных в табл. 50, в качестве средств медицинской защиты могут быть рекомендованы противосудорожные средства из группы производных бензОдиазепина, в частности диазепам (10 мг препарата, желательно ввести внутривенно). Как указывалось ранее, при отравлении ФОС возбуждение холинергических структур в центральной нервной системе является лишь пусковым моментом в механизме развития судорог. В последующем этот процесс в значительной степени теряет свою специфичность. Поэтому при продолжающихся судорогах, которые не удалось купировать введением холинолитиков, следует использовать фармакологические средства, повышающие тонус тормозных нейромедиаторных систем мозга, в частности ГМАК-ергической. Бензодиазепинам как средствам медицинской защиты предпочтение отдают в силу их высокой противосудорожной активности, большой терапевтической широты, удобства применения при массовом потоке пораженных (препараты могут быть изготовлены в форме шприцев-тюбиков). Необходимо иметь в виду, что устранение судорожного синдрома не защищает жизнь пострадавшего. В эксперименте показано, что на фоне диазепама ФОС в смертельной дозе вызывает гибель животных при полном отсутствии судорог.
Таблица 50
Основные направления патогенетической и симптоматической терапии
| Основные направления Нормализация гомеостаза внутриклеточного кальция Нормализация электролитного обмена Устранение гипоксии Угнетение перекисного окисления липидов Защита клеток мозга от повреждения возбуждающими аминокислотами Устранение психических нарушений Устранение судорожного синдрома Стимуляция дыхания Поддержание сердечно-сосудистой деятельности |
отравлений ФОС
Группы препаратов
Блокаторы кальциевых каналов (верапамил, нифедипин и др.)
Электролиты (препараты калия)
Кислородотерапия
Антигипоксанты (олифен, цитохром «С») Препараты янтарной кислоты
Антиоксиданты (токоферол, аскорбат)
Антагонисты глутаматных рецепторов (кеталар и др.)
Нейролептики
Антидепрессанты
Психостимуляторы
Противосудорожные (производные бензодиазепина; производные барбитуровой кислоты; антагонисты ВАК и т. д.)
Этим изо л
Сердечные гликозиды Вазотоники
Профилактические антидоты представляют собой таблетированные средства, которые военнослужащие принимают по указанию командира (начальника) до возможного контакта с токсикантом (перед входом в зону, зараженную ФОС, при необходимости контакта с военнослужащими, выходящими из зоны химического заражения и т, д.). Профилактические антидоты представляют собой сбалансированный комплекс обратимых ингибиторов холинэстеразы и холинолитиков. Иногда в состав антидота включают реактиватор холинэстеразы или противосудорожное средство. В качестве средств профилактики в разные годы на снабжение армии принимали препараты: П-3 (галантамин, атропин и другие холинолитики, изонитрозин), П-6, П-10М. Препараты отличаются антидот-ной мощностью, продолжительностью защитного действия, способностью потенцировать действие антидотов само- и взаимопомощи.
Антидоты само- и взаимопомощи представляют собой средства, изготовленные в форме шприца-тюбика объемом 1,0 мл, которые военнослужащие вводят себе самостоятельно при появлении первых признаков отравления. Это рецептуры, состоящие из холинолитиков с различным сродством к М- и Н-холинорецепторам центральной нервной системы и периферии и, в некоторых случаях, реактиваторов ХЭ. В различное время на снабжение армии принимались такие средства, как сафолен, афин, бу-даксим, АЛ-85 (пеликсим) и др. Препараты различаются по антидотной мощности и переносимости военнослужащими.
Карбаматы
Производные карбаминовой кислоты — карбаматы (рис. 51, 52) давно известны человечеству. Первый представитель этого класса химических соединений, физостигмин (эзерин, калабарин), был выделен в 1864 г. Джобстом и Хессом из растения, произрастающего на западе Африки, Physostigma venenosum (калабарские бобы) и идентифицирован как алкалоид — производное карбаминовой кислоты в 1926 г. Стедманом и Баргером. В настоящее время известны сотни химических веществ этого класса как растительного, так и, главным образом, синтетического происхождения.
60-80 мг/кг; бендиакарб — 60 мг/кг). В настоящее время известны и чрезвычайно токсичные для млекопитающих синтетические производные карбаминовой кислоты (Т-1123; бис-(диметилкарбамоксибензил)-алкан диметил галид: LD50 — 0,005 мг/кг), которые рассматривались как возможные образцы химического оружия (Бадави, Хассан, 1995; Байгар, 1998).

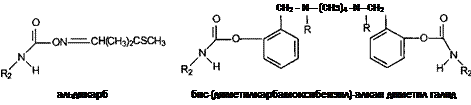
бендиакарб
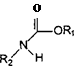 | |||
 | |||
Рис 51. Структурная формула карбаматов
Аварии при производстве карбаматов, их хранении и транспортировке опасны в плане формирования очагов поражения людей. Не исключено использование средств для совершения террористических актов.
Токсичность. Физико-химические свойства
Токсичность соединений определяется строением радикала (R) при кислородном атоме карбамильной группы кислоты (рис. 52), Большинство высокотоксичных карбаматов содержат в молекуле заряженный атом азота. R.2 у современных синтетических карбаматов представлен метиль-ной группой.
Некоторые представители группы обладают достаточно высокой токсичностью (LD50 физостигмина для мышей при подкожном введении — 0,75 мг/кг; альдикарба — 1 мг/кг), но в силу избирательности действия они широко используются в качестве лекарственных препаратов (физостигмин, галантамин, пиридостигмин, неостигмин и т. д.), а также средств борьбы с грызунами (альдикарб). Многие синтетические аналоги, обладающие меньшей токсичностью для млекопитающих, но высокотоксичные для насекомых, применяются как инсектициды (LD50 для мышей: изопрокарб — 400-485 мг/кг; пропоксур — 90-124 мг/кг; диоксакарб —
Производные карбаминовой кислоты — твердые кристаллические соединения, способные образовывать в воздухе мелкодисперсную пыль. Они хорошо растворяются в воде, хуже в липидах. В химическом отношении инертны. Не летучи. Устойчивы к гидролизу. Образуют зоны стойкого химического заражения. Прибывающие из зоны заражения пораженные могут представлять опасность для окружающих.
Токсикокинетика
Вещества способны проникать в организм через желудочно-кишечный тракт с зараженной водой и пищей. Высокотоксичные соединения могут вызывать интоксикацию действуя в форме аэрозоля через слизистую оболочку глаз и органы дыхания. При ингаляционном поступлении токсичность веществ в 10-50 раз выше, чем при приеме через рот. Через неповрежденную кожу карбаматы в организм проникают плохо.
Незаряженные молекулы легко проникают через гематоэнцефаличе-ский барьер и оказывают непосредственное действие на холинергические синапсы мозга. Соединения, содержащие в молекуле четвертичный атом азота (заряженные), действуют преимущественно на ПНС (вегетативный и двигательный отделы). Элиминация токсикантов в основном осуществляется путем энзиматического гидролиза эфирной связи, а также выведением через почки неизмененной молекулы вещества. Действующие концентрации карбаматов в крови могут быть определены, как правило, в течение не более 3—5 ч.
Основные проявления интоксикации
Проявления токсического процесса при остром отравлении карбама-тами, закономерности и механизмы его развития чрезвычайно напоминают поражение ФОС. Основная особенность действия токсикантов (в сравнении с ФОС) — меньшая продолжительность развивающихся нарушений. Так, при внесении физостигмина в конъюнктивальный мешок глаза спазм аккомодации регистрируется в течение не более 2 ч.
При приеме веществ через рот наблюдаются усиление перистальтики кишечника, схваткообразные боли в области живота, тошнота, рвота, понос. При ингаляционном поражении первые симптомы — чувство стеснения в груди, затруднение дыхания, обусловленное бронхоспазмом и гиперсекрецией бронхиальных желез. При резорбции высоких доз токсикантов симптоматика усиливается. Проникающие через ГЭБ вещества, вызывают психоэмоциональные нарушения — сначала возбуждают, а затем угнетают дыхательный и сосудо-двигательный центры — подъем артериального давления сменяется его падением, возможна остановка дыхания. Эффекты обусловлены не только способностью веществ активировать холинергические механизмы мозга, но и действовать на рефлексогенную зону синокаротидного клубочка. Как и при отравлении ФОС, наблюдаются фасцикулляции мышечных групп. Проявлением тяжелого поражения карбаматами является судорожный синдром. Если в течение нескольких часов не развивается летальный исход, состояние пострадавшего относительно быстро улучшается.
Механизм токсического действия
Карбаматы являются конкурентными, обратимыми ингибиторами холинэстеразы (см. 12.1.1.1.1.1. «Ингибиторы холинэстеразы»). Отравление ими приводит к накоплению в холинергических синапсах ацетилхолина, который и вызывает перевозбуждение М- и Н-холинореактивных структур в ЦНС и на периферии. Помимо антихолинэстеразного, эти вещества обладают прямым холиномиметическим действием на холинорецето-ры синапсов. Так, внутриартериальное введение физостигмина экспериментальному животному вызывает сокращение денервированных (путем перерезки нервных стволов) мышечных групп, т. е. возбуждает Н-холи-норецепторы поперечно-полосатой мускулатуры в условиях отсутствия выброса ацетилхолина из пресинаптических нервных окончаний.
Процесс восстановления нормального проведения нервного импульса в холинергических синапсах осуществляется в основном за счет быстрого, в течение нескольких часов, декарбамилирования АХЭ (спонтанной реактивации) и удаления вещества из синапсов.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение частичной санитарной обработки (использование ИПП) в зоне химического заражения;
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Средства медицинской защиты
В качестве медицинских средств защиты при поражении карбаматами могут быть использованы средства защиты от ФОВ (см. выше). При этом необходимо учитывать, что холинолитики и рецептуры на их основе оказываются более эффективными при отравлении карбаматами (оказывают положительный эффект в меньших дозах, чем это требуется для оказания помощи пораженным ФОС); реактиваторы холинэстеразы — менее эффективными (увеличение доз вводимых препаратов с целью повышения эффективности ни при каких условиях не допустимо). Противопоказано для целей профилактики применять препараты П-6, П-10М, содержащие в рецептуре высокоактивные обратимые ингибиторы холинэстеразы.
2ВО
2В1
 |
12.1.1.1.2. Конвульсанты, действующие на ГАМК-реактивные синапсы
ГАМК — нейромедиатор в тормозных межнейрональных синапсах ЦНС животных и человека (рис. 53).
H2N СН2СН2 / СН2 С—О I
ОН
Рос. 53. Структура у-аминомасляной кислоты (ГАМК)
Действуя на соответствующие рецепторы, ГАМК формирует ингиби-торный постсинаптический потенциал (ИПСП). Установлено, что в основе эффекта лежит усиление нейромедиатором проницаемости возбудимых мембран для ионов хлора, которые под влиянием концентрационного градиента устремляются из внеклеточной среды в клетку и вызывают тем самым гиперполяризацию мембраны.
ГАМК обнаружена во всех структурах ЦНС. Концентрация аминокислоты в разных областях мозга колеблется в пределах от 2 до 10 мкМ/г ткани. Наивысшее ее содержание — в черной субстанции. Высокая плотность ГАМК-ергических синапсов выявлена в коре головного мозга, клиновидном ядре, ядре Дейтерса, ядрах передних рогов спинного мозга, в обонятельных бугорках, коре мозжечка, гиппокампе, продолговатом мозге (нейронах ретикулярной формации), латеральных коленчатых телах, гипоталамусе. Нейроны этих образований высокочувствительны к ГАМК.
В нервных окончаниях ГАМК обнаруживается главным образом в цитоплазме в несвязанной форме (60—80%); относительно небольшое количество вещества заключено в пресинаптических везикулах.
В нервной ткани ГАМК образуется путем декарбоксилирования глу-тамата под влиянием энзима глутаматдекарбоксилазы (ДГК) (рис. 54). Источником веществ-предшественников глутамата является цикл Кребса. ДГК — цитоплазматический энзим, широко представленный в структурах мозга, содержащих ГАМК в высокой концентрации. Катаболизм нейромедиатора осуществляется митохондриальным энзимом ГАМК-транс-аминазой (ГАМК-Т), превращающей вещество в сукцинатсемиальдегид (ССАД). Этот метаболит в свою очередь окисляется другим митохондриальным энзимом, дегидрогеназой сукцинатсемиальдегида, до янтарной кислоты; последняя утилизируется циклом Кребса. Поскольку и ДГК и ГАМК-Т являются пиридоксальфосфат-зависимыми энзимами, вещества, нарушающие обмен этого кофактора, вызывают при интоксикациях тяжелые нарушения функций ЦНС, вплоть до развития судорожного синдрома.
ЦТК — цикл трикарбоновых кислот; ГК — глутаминовая кислота; ДГК — декарбоксилаза глутаминовой кислоты; ГАМК-Т— ГАМК-трансаминаза; ССАД — сукцинатсемиальдегид
Большая часть выделившейся в синаптическую щель ГАМК удаляется путем высокоаффинного, Ыа+-зависимого активного захвата как нервными окончаниями, так и клетками глии. До 50% ГАМК мозга определяется в глиальных элементах. Пул ГАМК, содержащейся в глиальных клетках, также имеет функциональное значение: выход нейромедиатора из глии в межклеточное пространство инициируется повышением в межнейрональной жидкости ионов калия (что наблюдается при гиперактивации нейронов).
Конвульсанты, действующие на ГАМК-ергический синапс, либо блокируют синтез ГАМК (производные гидразина и др.) и ее высвобождение (тетанотоксин) в синаптическую щель, либо являются физиологическими антагонистами нейромедиатора, взаимодействующими с ГАМК-ре-цепторами (ГАМК-литики).
Структура и физиология ГАМК-рецепторов окончательно не изучены. Не существует и их единой классификации. Наиболее распространено разделение рецепторов на ГАМКА и ГАМКБ типы. Рецепторы первого типа чувствительны к ГАМК-литику бикукуллину, второго типа — не чувствительны к этому веществу, но избирательно возбуждаются бакло-феном. ГАМКА-рецепторы непосредственно сопряжены с хлор-ионными каналами возбудимых мембран. ГАМКБ-рецепторы сопряжены с калиевыми и кальциевыми каналами мембран через систему G-протеинов. Наиболее изучены ГАМКА-рецепторы, действию на которые и приписывают основные тормозные эффекты нейромедиатора. С ГАМКА-рецепто-рами способно взаимодействовать большое количество химических веществ, как облегчающих, так и блокирующих поступление ионов хлора через возбудимую мембрану (рис. 55). Эти вещества являются соответственно агонистами (мусцимол, диазепам, гексобарбитал и т. д.) или антагонистами ГАМК (бикукуллин, флюмазенил, пикротоксин и т. д.).
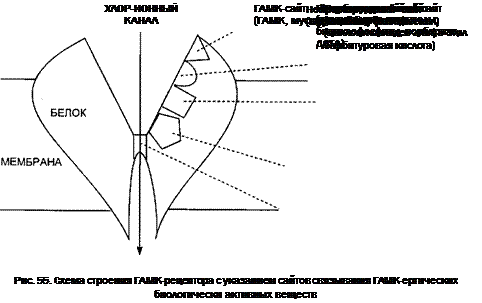
Ингибиторы синтеза ГАМК
К числу веществ, угнетающих синтез ГАМК, принадлежат прежде всего ингибиторы декарбоксилазы глутаминовой кислоты (ДГК), в частности антагонисты пиридоксальфосфата (коэнзим ДГК). По большей части это производные гидразина. Структуры некоторых из них представлены на рис. 56.
СН,
| N—NH2 |
| СН3 несимметричный диметилгидразин |
| H2N— С-------- NH—NH2 |
| H2N- |
| -С-О |
H2N— NH2 гидразин
| семикарбазид |
-NH— NH2
| / |
| N />—С------------ NH—NH2 ^ // I" О |
 тиосемикарбазид
тиосемикарбазид
NH2—NH— С------------ NH— NH2
I' S
тиокарбо гидразид
изоникотиновой кислоты
Рис. 56. Структуры некоторых веществ-антагонистов пиридоксальфосфата Е84
Наиболее токсичным веществом,' из представленных на рис. 56, является тиокарбогидразид, наименее токсичным — гидразид изоникотиновой кислоты (изониазид).
Для военной токсикологии особый интерес представляют гидразин и его алкильные производные (диметилгидразин), являющиеся компонентами ракетных топлив. Вещества могут вызывать формирование зон стойкого химического заражения и очаги химического поражения людей при аварийных ситуациях на объектах по производству и хранению токсикантов, при их транспортировке.
Гидразин
Гидразин применяется в производстве лекарств, пластмасс, резин, инсектицидов, взрывчатых веществ, в качестве консерванта и как компонент ракетного топлива.
Физико-химические свойства. Токсичность
Гидразин — бесцветная маслянистая жидкость с запахом аммиака. Летуч. Плотность пара в 1,1 раза выше плотности воздуха. Вещество хорошо растворяется в воде. Водные растворы обладают свойствами оснований. Разлагается при нагревании. Гидразин и его производные (монометил-гидразин и диметилгидразин) — легковоспламеняющиеся вещества; горят с образованием высокотоксичных летучих нитросоединений.
Летальная доза гидразина для грызунов при введении в желудок составляет около 60 мг/кг, диметилгидразина — 33 мг/кг. При ингаляции паров в течение 4 ч смертельной является концентрация гидразина 0,32 г/м3, диметилгидразина — 0,11 г/м3 (в 200-500 раз менее токсичны, чем зарин).
Токсикокинетика
В организм гидразин и его алкильные производные в виде пара и аэрозоля проникают ингаляционно и через кожу, в виде жидкости — через кожные покровы и при приеме внутрь. Проникновению веществ через кожу способствует повреждающее действие токсикантов на покровные ткани. С кровью распределяются в органах и тканях, легко проникают через ГЭБ. Элиминация гидразина из организма частично'осуществляется за счет выделения с мочой в неизмененном виде, частично за счет метаболизма. Основной путь метаболических превращений — конъюгация с эндогенным уридином, фосфатом, ацетатом при участии соответствующих трансфераз (реакции конъюгации) и биологическое окисление, активируемое микросомальными цитохром-Р-450-зависимыми оксидазами смешанной функции, до азота, диимида и диазена. Пораженные, подвергшиеся санитарной обработке, не представляют опасности для окружающих.
Основные проявления интоксикации
Пары гидразина вызывают сильное раздражение слизистых оболочек глаз, дыхательных путей. При тяжелых поражениях возможно развитие токсического отека легких, токсической пневмонии. Жидкий гидразин
(в эпицентре аварии) при попадании на кожу или глаза вызывает химический ожог ткани и сопутствующие этому общие реакции организма. Местное действие на покровные ткани диметилгидразина выражено значительно слабее.
При резорбции гидразина к проявлениям местного действия токсикантов присоединяются признаки поражения ЦНС, крови, печени и почек. Симптоматика отравления развивается спустя 30—90 мин от начала воздействия.
При легкой интоксикации (наиболее вероятная форма поражения в зоне химического заражения) появляются беспокойство, возбуждение, чувство страха, бессонница. Нарушение работоспособности в течение суток и более.
При поступлении в организм в дозах, близких к смертельным, вещества вызывают тошноту, рвоту, нарушение сознания, клонико-тониче-ские судороги, приступы которых чередуются с периодами ремиссии. У пострадавших развивается коматозное состояние на фоне нарушений функций сердечно-сосудистой системы (брадикардия, коллапс). По выходе из комы наблюдается психоз с бредом, слуховыми и зрительными галлюцинациями. Состояние психоза может продолжаться в течение нескольких дней.
Характерным проявлением интоксикации являются метгемоглобине-мия, гемолиз (метгемоглобинообразование более характерно для арильных производных гидразина, например фенилгидразина). Максимум снижения содержания эритроцитов в крови отмечается к 10-м сут.
Достаточно часто встречающимся проявлением острой интоксикации гидразином является отсроченное во времени поражение печени и почек в форме острого токсического гепатита и токсической нефропатии. В эксперименте у животных, отравленных гидразином в высоких дозах, отмечаются жировое перерождение печени, некроз эпителия проксимального отдела извитых канальцев почек. Изменения со стороны внутренних органов развиваются через 48 и более часов после поступления яда в организм.
Механизм токсического действия
Основными механизмами, лежащими в основе токсического действия гидразина и его производных на ЦНС, являются:
1) снижение содержания пиридоксальфосфата в тканях мозга;
2) инактивация ферментов, кофактором которых является пири-доксальфосфат, и в частности, энзимов, участвующих в метаболизме ГАМК;
3) снижение содержания ГАМК и, как следствие этого, подавление тормозных процессов в ЦНС;
4) снижение активности моноаминоксидазы (МАО) и повышение содержания биогенных аминов (норадреналина, дофамина, се-ротонина) в ЦНС.
При отравлении гидразином и его производными запасы пиридоксальфосфата в тканях резко снижаются. В основе эффекта лежит способность токсиканта вступать в химическую связь с альдегидными группами пиридоксаля:
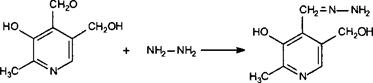
В результате этой реакции, во-первых, снижается содержание пиридоксаля, во-вторых, образуется пиридоксальгидразон — вещество, являющееся конкурентным обратимым ингибитором фермента пиридоксаль-киназы (как in vitro, так и in vivo). Функция пиридоксалькиназы — активация реакции фосфорилирования пиридоксаля, в ходе которой образуется пиридоксальфосфат — кофактор многих энзимов, участвующих в метаболизме веществ. Угнетение пиридоксалькиназы пиридоксальгид-разоном быстро приводит к истощению запасов пиридоксальфосфата и, следовательно, к снижению активности ферментов, кофактором которых он является.
При отравлении гидразинами из строя выходит около 20 энзимов, среди них трансаминазы, декарбоксилазы аминокислот, аминоксидазы и др. Особенно сильно снижается активность декарбоксилазы глутамино-вой кислоты (ДГК) — основного энзима синтеза ГАМК в мозге. Как указывалось ранее, ДГК — пиридоксальфосфат-зависимый энзим. Судорожный синдром при введении гидразина развивается на фоне снижения активности энзима до уровня 40% от нормы. В результате нарушается синтез ГАМК. Гамма-аминомасляная кислота не проникает через гема-тоэнцефалический барьер. Ее синтез осуществляется непосредственно в ГАМК-ергических нейронах. Глиальные элементы также не синтезируют нейромедиатор.
Одновременно подавляется активность и ГАМК-Т (также пиридокса-льфосфат-зависимого энзима) и, следовательно, блокируются не только процессы синтеза, но и распада ГАМК. Блок синтеза нейромедиатора в нейронах с одновременным замедлением его распада приводит к перераспределению ГАМК: в нервных клетках (где осуществляется синтез нейромедиатора) содержание вещества снижается, в глиальных — несколько возрастает. По этой причине не всегда удается проследить четкую корреляцию между тяжестью интоксикации и степенью снижения ГАМК в ткани мозга. Тем не менее при тяжелых отравлениях экспериментальных животных, сопровождающихся развитием судорог, уровень ГАМК составляет 50-70% от нормы.
Таким образом, от момента начала действия гидразина до развития эффектов, являющихся непосредственной причиной судорожного синдрома, разыгрывается целая цепь патохимических процессов. С этим свя-
2ВВ
 зано наличие скрытого периода, наблюдающегося даже при крайне тяже- " лых формах отравления гидразином.
зано наличие скрытого периода, наблюдающегося даже при крайне тяже- " лых формах отравления гидразином.
Гидразин и его производные являются необратимыми ингибиторами моноаминоксидазы (МАО) — фермента, участвующего в разрушении нейромедиаторных веществ мозга: дофамина, норадреналина, серотони-на. На основе гидразина созданы лекарственные препараты — ингибиторы МАО (фенелзин и др.). При отравлении веществом через 5—6 ч после начала интоксикации количество катехол- и индоламинов в ЦНС существенно увеличивается, что может явиться дополнительной причиной явлений, наблюдающихся как при легких интоксикациях (состояние возбуждения, бессонница), так и по выходе пострадавшего из коматозного состояния (зрительные, слуховые галлюцинации, бред и т. д.).
Гемолитическое действие гидразина и его производных, по-видимому, связано с их метгемоглобинообразующей активностью. Образование метгемоглобина приводит к снижению содержания в эритроцитах глута-тиона, необходимого для стабилизации биологических мембран. Поэтому эритроциты, содержащие метгемоглобин, менее устойчивы и легко разрушаются в селезенке.
Механизмы поражения печени и почек окончательно не установлены. Возможно, в основе цитотоксического действия гидразина и его производных лежит все то же нарушение активности пиридоксальзависимых ферментов. Кроме того, в эксперименте установлены снижение митохон-дриальной активности в тканях печени и почек, активация свободнорадикальных процессов и перекисного окисления липидов, повреждение системы антирадикальной защиты, и в частности, глутатиона.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты кожи и органов дыхания) в зоне химического^ заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим; • подготовка и проведение эвакуации.
Средства медицинской защиты
При попадании гидразина на поверхность кожи, в глаза первая помощь оказывается в соответствии с общими принципами оказания помощи отравленным. В отношении легкоотравленных осуществляются мероприятия, проводимые при оказании помощи пораженным и другими веществами раздражающего действия (см. гл. 8. «Отравляющие и высокотоксичные вещества раздражающего действия»). При тяжелых поражениях кожи и глаз мероприятия аналогичны, проводимым при отравлении ипритом (см. гл. 11. «Отравляющие и высокотоксичные вещества цитотоксического действия»). При ингаляционном поражении мероприятия должны быть направлены на профилактику, а в случае необходимости — на раннее лечение токсического отека легких (см. 9.2. «ОВТВ удушающего действия»)..
В процессе целенаправленного поиска антидотов резорбтивного действия гидразина испытаны вещества, обладающие химическим, биохимическим и физиологическим антагонизмом к токсиканту.
В качестве химических антагонистов изучены вещества, содержащие в молекуле альдегидную группу. Как указывалось, гидразин взаимодействуя с альдегидами образует гидразоны. По большей части это вещества менее токсичные, чем исходный яд. В частности, показано, что in vitro токсикант активно связывается а-кетоглутаровой кислотой. Это же вещество в эксперименте оказывает положительное действие при профилактическом введении лабораторным животным. Применение а-кетоглутаровой кислоты с лечебной целью не дает желательного результата, так как вещество не способно вытеснять гидразин из связи с пиридоксалем. Препарат не используется в практике медицинской защиты, так как не отвечает требованиям, предъявляемым к профилактическим антидотам.
Биохимическим антагонистом гидразина является пиридоксин. Введение вещества отравленным сопровождается увеличением его содержания в тканях, вытеснением пиридоксальгидразонов из связи с активным центром пиридоксалькиназы и восстановлением ее активности. В итоге происходит нормализация процесса синтеза пиридоксальфосфата. За счет этого восстанавливается активность пиридоксальфосфат-зависимых энзимов. Людям, отравленным гидразинами, пиридоксин (витамин Вб) с лечебной целью вводят в форме 5% раствора в дозе 25 мг/кг (1/4 дозы в/в, 3/4 — в/м); при необходимости инъекцию повторяют через каждые 2 ч.
Поиск антидотов, обладающих физиологическим антагонизмом по отношению к гидразину, проводили среди веществ, повышающих тонус ГАМК-ергической медиаторной системы мозга и нейролептиков (блокируют а-адренорецепторы, дофаминергические и серотонинергические рецепторы мозга).
Эффективными оказались препараты из группы производных бензо-диазепина. Эти вещества потенцируют действия ГАМК в ГАМК-ергиче-
28Э
ских синапсах центральной нервной системы. Диазепам (седуксен) в дозе 5—10 мг/кг в 100% случаев предотвращает острую гибель экспериментальных животных, отравленных гидразином в смертельной дозе.
Производные барбитуровой кислоты (фенобарбитал) и оксазолидин-дионы (триметадион) также подавляют судороги, вызываемые производными гидразина, как у человека, так и у лабораторных животных.
Дибензодиазепины (клозапин) снижают выраженность психотических реакций, развивающихся при легкой и средней степени тяжести отравления гидразином. Вещества малотоксичны, обладают слабым седа-тивным и гипотензивным действием. Клозапин назначают в дозе 25—100 мг (таблетки).
Из указанных препаратов достаточной эффективностью, переносимостью и удобством применения в полевых условиях отличаются диазепам и клозапин, которые и могут быть рекомендованы как средства медицинской защиты: клозапин — при возбуждении, чувстве страха; диазепам — при появлении судорог.
12.1*1.1.2.2. Пресинаптические блокаторы высвобождения ГАМК
Тетанотоксин
Тетанотоксин — физиологически активное вещество (ФАВ), исследовавшееся за рубежом в военных целях (3. Франке, 1973; В. К. Курочкин и соавт., 1994). Является экзотоксином микроорганизма, вызывающего инфекционное заболевание «столбняк».
Боевое применение тетанотоксина маловероятно. Это вещество может рассматриваться лишь в качестве возможного диверсионного агента.
Физико-химические свойства. Токсичность
Тетанотоксин продуцируется анаэробными спорообразующими бак-„ териями Clostridium tetani. Это белок, состоящий из двух субъединиц с молекулярной массой 100 000 и 50 000 дальтон. Растворим в воде. Неустойчив при нагревании. Летальная доза для грызунов при подкожном введении — около 2 • 10~6 мг/кг массы животного. Для людей смертельная одноразовая доза токсина составляет менее 0,2—0,3 мг.
Пораженные не представляют опасности для окружающих.
Токсикокинетика
В желудочно-кишечном тракте быстро разрушается и потому при поступлении per os не действует. Через неповрежденную кожу в организм не проникает. При внутримышечном введении лабораторным животным быстро попадает в кровь, где также достаточно быстро разрушается при участии протеаз до неактивных пептидов, а затем и аминокислот. Время нахождения в крови токсина не установлено. Будучи белком, вещество не проникает через ГЭБ. Полагают, что в двигательные ядра ЦНС поступает с помощью механизма ретроградного аксонального тока по волокнам нервных стволов, с окончаниями которых специфично связывается. Имеются доказательства способности токсина к транссинаптической миграции, т. е. переходу от одного нейрона к другому, диффундируя через синаптическую щель.
Основные проявления интоксикации
После воздействия скрытый период может продолжаться от нескольких часов до 3 и более суток. Вслед за общими проявлениями недомогания (головная и мышечная боль, лихорадка, повышение потливости, слабость, сонливость) развиваются возбуждение, чувство страха, тризм жевательной мускулатуры, а затем приступы клонико-тонических судорог. Захватываются мышцы спины, конечностей, возникает опистотонус. Приступы судорог провоцируются внешним звуковым и тактильным раздражением. Выраженность судорожных приступов столь велика, что порой приводит к разрывам мышц, компрессионному перелому позвоночника. Сознание, как правило, сохранено. Поэтому субъективно интоксикация переносится крайне тяжело. Стойкое сокращение дыхательных мышц, диафрагмы и мышц гортани может привести пострадавшего к смерти от асфиксии.
Механизм токсического действия
Механизм действия вещества изучен недостаточно. Установлено, что тетанотоксин блокирует выброс тормозных нейромедиаторов ГАМК и глицина нервными окончаниями соответствующих нейронов ЦНС. В ряде исследований показано наличие в окончаниях волокон нервных клеток специфических сайтов связывания токсина. Эти структуры представляют собой ганглиозиды или углеводные комплексы, близкие по строению ганглиозидам. Сиаловая кислота, как полагают, — важнейший компонент этих сайтов. Тетанотоксин не связывается с ненейрональны-ми клеточными мембранами и в этом одна из причин его высокой токсичности. Как установлено, структурно рецептор тетанотоксина напоминает рецептор белкового гормона тириотропина. In vitro токсин способен связываться с препаратом мембран, приготовленных из ткани щитовидной железы, при этом тиреотропин блокирует это связывание. Вместе с тем in vivo гормон потенцирует связывание токсина мембранами нервных клеток, усиливая его токсичность. Связавшийся с пресинапти-ческими структурами токсин проникает внутрь нервного окончания путем пиноцитоза и, разрушаясь здесь, выделяет полипептид, угнетающий механизм спонтанного и вызываемого нервными импульсами экзоцитоза нейромедиаторов (ГАМК, глицина). Поскольку последние перестают оказывать тормозное воздействие на нейроны мозга, развивается возбуждение ЦНС и судорожный приступ.
Мероприятия медицинской защиты
Специальные профилактические медицинские мероприятия: • организация профилактических прививок.
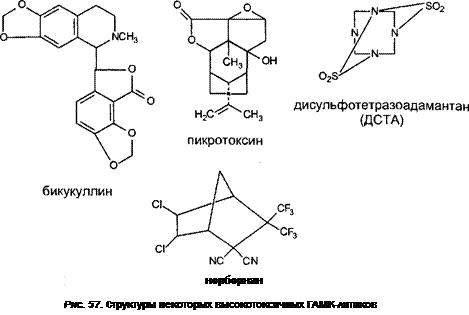 |
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Средства медицинской защиты
С целью профилактики поражения тетанотоксином возможна плановая иммунизация военнослужащих столбнячным анатоксином.
Поскольку интоксикация развивается постепенно, в случае возникновения поражения важнейшая задача медицинской службы состоит в скорейшем выявлении пострадавших.
На догоспитальном этапе при выявлении пораженных перед их эвакуацией, с целью профилактики судорожного синдрома, необходимо ввести нейроплегическую смесь: 2,5% раствор аминазина — 2,0; 2% раствор пантопона — 1,0; 2% раствор димедрола — 2,0; 0,05% раствор ско-поламина — 0,5. Через 30 мин внутримышечно — 5-10 мл 10% раствора гексенала. Бензодиазепины малоэффективны при поражении тетанотоксином.
Специфическим противоядием токсина является противостолбнячная сыворотка, содержащая антитела к веществу, а также противостолбнячный гамма-глобулин. Так как введение этих препаратов на догоспитальном этапе не возможно, они не используются в качестве средств медицинской защиты.
В специализированных центрах пострадавших переводят на искусственную вентиляцию легких после предварительной тотальной миорелак-сации и внутримышечно вводят сыворотку по 100 000—150 000 ME.
12.1.1.1.2.3. Антагонисты ГАМК
Антагонисты у-аминомасляной кислоты (ГАМК-литики), взаимодействуя с различными сайтами связывания на ГАМКд-рецепторах, либо экранируют их, либо изменяют чувствительность к нейромедиатору. Это приводит к деполяризации возбудимых мембран и повышению чувствительности многочисленных популяций нервных клеток к возбуждающим воздействиям. Развивается активация, а затем и гиперактивация структур мозга, сопровождающаяся глубоким нарушением функций ЦНС, а в случаях тяжелого поражения судорогами и смертью.
К числу ГАМК-литиков относятся вещества самого разного строения. Здесь и алкалоиды растительного происхождения (бикукуллин), и безазотистые растительные вещества (пикротоксин), а также многочисленные синтетические соединения: дисульфотетразоадамантан (ДСТА), норборнан, силатраны, бициклофосфаты и т. д. (рис. 57).
В практике здравоохранения и хозяйственной деятельности эти вещества не используются. В силу высокой токсичности и избирательности действия их применяют в лабораторных исследованиях при изучении физиологии и биохимии ЦНС. С военными целями изучались бицикличе-ские фосфорорганические соединения и их аналоги (В. К. Курочкин и соавт., 1994; Байгар, 1998).
Бициклические фосфорорганические соединения (БЦФ) и их аналоги
 |
В 1973 г. Bellet и Casida описали группу бициклических фосфорорга-нических соединений, не обладающих антихолинэстеразной активностью, но вызывающих приступ судорог и гибель экспериментальных животных при введении в малых дозах. Структуры БЦФ представлены на рис. 58. Биологически активные вещества такого строения относятся к бициклофосфатам, бициклофосфоротионатам и бициклофосфитам.
гэа
газ
Токсичность БЦФ существенно зависит от строения радикала (R) и может быть очень высокой для отдельных соединений. Так, LD50 трет-бу-тилбициклофосфата для грызунов составляет около 0,05 мг/кг массы (близка токсичности зарина).
Близкие по структуре соединения — бицикло-орто-карбоксилаты (БЦК) (рис. 59) также способны инициировать токсический процесс.

бицикло-орто-карбоксилаты Рис. 59. Структура молекулы триоксибициклокарбоксилатов
Токсичность БЦК зависит от строения радикалов R и R.2 и для некоторых представителей при внутрибрюшинном способе введения LD50 составляет около 1 мг/кг массы экспериментального животного (4-трет-бу-тил-1 (3,4-дихлорфенил)-бицикло-орто-бензоат).
Все БЦФ и БЦК — твердые вещества, плохо растворимые в воде. Не проникают в организм через неповрежденную кожу. Могут оказывать токсическое действие при подкожном, внутримышечном, внутривенном, а некоторые представители, и при ингаляционном способе введения (в форме аэрозоля). Хорошо всасываются в желудочно-кишечном тракте.
Основные проявления интоксикации
Признаки отравления БЦФ и БЦК изучались на лабораторных животных. Поскольку проявления интоксикации различными ГАМК-ли-тиками достаточно близки, для характеристики поражения можно использовать также результаты немногочисленных клинических наблюдений людей, отравленных аналогами рассматриваемых веществ, в частности пикротоксином и др.
БЦФ не обладают выраженным местным действием. Эффекты развиваются после резорбции веществ в кровь и поступления их в ЦНС. Скрытый период редко превышает 30 мин. На центральную нервную систему ГАМК-литики действуют возбуждающим образом. Первым признаком отравления является повышение рефлекторной деятельности. Усиливается дыхание, возникает тошнота, возможна рвота. Появляются беспокойство, чувство страха, возбуждение, иногда с галлюцинациями. Отмечается напряженность различных групп мьппц, дрожание конечностей. Температура тела повышается. Такое состояние может продолжаться в течение нескольких часов и более и сопряжено с полной утратой дееспособности.
Если доза вещества близка смертельной, спустя несколько минут от начала интоксикации формируется состояние повышенной судорожной готовности — внешние раздражители (прикосновение, звук и т. д.) провоцируют ризус. Пострадавший падает на бок. Развиваются тонические судороги, опистотонус. На фоне судорог дыхание останавливается. Лицо становится цианотичным. Зрачки расширены (реже сужены). Возможны непроизвольные мочеиспускание и дефекация. В таком положении пострадавший находится 1—2 мин, затем приступ прекращается, мускулатура расслабляется. Восстанавливается дыхание. В межсудорожном периоде выявляются некоторый подъем артериального давления, брадикардия. Через непродолжительное время приступ повторяется. При первых судорожных припадках сознание сохранено, затем, после нескольких судорожных приступов, наблюдается переход в ступорозное состояние и потеря сознания. Через 5—10 припадков наступает смерть от асфиксии, нарушения сердечной деятельности, резкого падения артериального давления.
Среди ГАМК-литиков особенностью токсического действия обладает 2,2-ди(трифторметил)-3,3-дициано-5,6-дихлорнорборнан (норборнан) — один из самых токсичных синтетических конвульсантов.
Норборнан — кристаллическое вещество, практически нерастворимое в воде, оказывает эффект при всех способах введения. Видовая чувствительность к нему выражена слабо. Среднелетальная доза — 0,07—0,2 мг/кг. Вещество синтезировано в начале 80-х гг. XX в. Мидлтоном (США).
Интоксикация веществом характеризуется растянутой во времени клинической картиной. Так, при подкожном введении экспериментальным животным смертельной дозы норборнана скрытый период составляет около 1,5 ч, судорожный — до 4 ч, продолжительность жизни отравленных смертельными дозами животных — более 6 ч (для сравнения, аналогичные токсикодинамические характеристики пикротоксина составляют, соответственно: 0,5 ч; 0,5 ч и 1 ч). При несмертельных интоксикациях повышенная судорожная готовность у экспериментальных животных сохраняется несколько суток.
Механизм токсического действия
Поскольку ГАМК-реактивные структуры выявлены только в ЦНС, все эффекты, наблюдаемые при отравлении ГАМК-литиками, имеют центральное происхождение. Считается, что БЦФ и БЦК — неконкурентные антагонисты ГАМК. Они не взаимодействуют с сайтом связывания ГАМК на ГАМКА-рецепторе, а непосредственно действуют на хлорионо-форный канал (на эту же структуру действуют некоторые другие ГАМК-литики: пикротоксин, ДСТА, норборнан). В результате такого действия конформация ионофорного протеина изменяется — стабилизируется его «запертое» состояние. В итоге активация ГАМК-рецептора гамма-амино-масляной кислотой в физиологических концентрациях оказываемая недостаточной для «открытия» канала и усиления трансмембранного тока ионов хлора. Неспособность ионов хлора проникать через возбудимые мембраны нейронов ЦНС приводит к снижению их потенциала покоя (деполяризации) и, следовательно, существенному понижению порога
гэ4
гэ5
чувствительности к возбуждающим воздействиям. Существуют два методических приема, позволяющих количественно оценить способность различных ГАМК-литиков действовать на хлорионофорные каналы. Первый — основан на способности исследуемого вещества связываться с хлорионофорным протеином (изучается методами радиолигандных исследований). Второй метод предполагает определение in vitro способности вещества угнетать захват радиоактивного хлора суспензией, приготовленной из нейрональных мембран, выделенных методом ультрацентрифугирования. В многочисленных опытах показано, что токсичность БЦФ и БЦК для экспериментальных животных прямо пропорциональна их активности, по обоим показателям.
Установлено, что различия в продолжительности судорожного периода в клинике отравления ГАМК-литиками также могут быть объяснены особенностями их взаимодействия с хлорионофорным белком. Так, в отличие от БЦФ и БЦК, образующих с протеином хотя и прочную, но обратимую связь, норборнан практически необратимо связывается ионо-фором.
Полагают, что способность ГАМК-литиков изменять конформацию хлорионофорного канала зависит от степени активации других сайтов связывания на ГАМК-рецепторе. Так, in vitro при добавлении в инкубационную среду гамма-аминомасляной кислоты (активация ГАМК-сайта) переход рецептора в неактивное состояние под влиянием ГАМК-литиков ускоряется, а при добавлении бензодиазепинов (активация бензодиазе-пинового сайта) — замедляется. Это открывает возможность создания медицинских средств защиты от токсикантов.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск, экспертиза воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим; • подготовка и проведение эвакуации.
Медицинские средства защиты
Поскольку ГАМК-литики не являлись и не являются табельными ОВ современных армий, а масштабы их использования в хозяйственной деятельности крайне ограничены, разработка средств медицинской защиты от высокотоксичных веществ данной группы систематически не проводилась. Имеются отдельные сообщения о возможности разработки таких средств и целесообразности их использования в случае необходимости.
Основу медицинской защиты могут составить медикаментозные средства. Основные направления исследований в этой области представлены в табл. 51.
Таблица 51
Основные направления разработки средств медицинской защиты от поражающего действия ГАМК-литиков (А. И. Головко и соавт., 1996)
| Направление | Препараты |
| Активация ГАМКд-рецепторов | Барбитураты |
| Бензодиазепины и др. | |
| Противосудорожные средства, действующие | Антагонисты возбуждающих аминокислот |
| на иные нейромедиаторные системы | (МК-801, кетамин и др.) |
| Подавление разрушения и обратного | Ингибиторы ГАМК-трансаминазы |
| захвата ГАМК | (аминооксиуксусная кислота, вигабатрин и др.) |
| Ускорение метаболизма токсикантов | Индукторы микросомальных ферментов |
Ускорение метаболизма. Установлено, что профилактическое назначение индукторов микросомальных энзимов экспериментальным животным (бензонал, фенобарбитал — 1 раз в сутки, трехкратно в дозе 40 мг/кг, внутрибрюшинно; перфтордекалин — 2 г/кг) в 1,5—1,8 раз снижает чувствительность к БЦФ на трое и более суток. Практическому использованию данного направления защиты препятствует существующая у индукторов, наряду со способностью понижать токсичность БЦФ, способность одновременно на относительно длительный срок повышать чувствительность организма к веществам, активируемым в процессе метаболизма. Поражение такими веществами не исключается в современных военных конфликтах.
Подавление разрушения ГАМК. Аминооксиуксусная кислота (АОУК), вигабатрин, у-винил-ГАМК и другие ингибиторы ГАМК-трансаминазы повышают уровень ГАМК в тканях головного мозга за счет угнетения процесса ее разрушения. При этом, возможно, блокируется также процесс обратного захвата ГАМК нервными окончаниями ГАМК-ергиче-ских нейронов и осуществляется накопление нейромедиатора в клетках глии. Повышение уровня ГАМК в ткани мозга приводит к усилению тормозных процессов в ЦНС и тем самым к снижению токсичности ГАМК-
литиков. Так, при профилактическом введении АОУК (50 мг/кг внутри-брюшинно за 2 ч до введения токсиканта) в 1,2—1,5 раза понижает чувствительность экспериментальных животных к смертельным дозам пикро-токсина. Этот факт указывает на теоретическую возможность разработки профилактических антидотов на основе ингибиторов ГАМК-Т. Средства, допущенные к клиническому применению, среди ингибиторов ГАМК-Т в настоящее время отсутствуют.
Бензодиазепины. В качестве специфических противоядий ГАМК-литиков, обладающих физиологическим антагонизмом, возможно использование бензодиазепинов. Вещества этой группы, в зависимости от вводимой дозы, обладают седативным, противосудорожным и центральным миорелаксирующим действием и потому широко используются в медицинской практике. В настоящее время синтезированы и испытаны тысячи соединений. К клиническому использованию допущено несколько десятков веществ. В качестве противосудорожных средств предпочтение отдают клоназепаму, нитразепаму, лоразепаму, диазепаму. Бензодиазепины хорошо всасываются в желудочно-кишечном тракте, некоторые обладают удовлетворительной биодоступностью при внутримышечном введении (диазепам, феназепам и т. д.). Диазепам (рис. 60), лоразепам выпускают в форме таблеток и раствора для инъекций (5 мг/мл и 2,4 мг/мл соответственно).
О
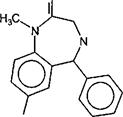
CI
Рис. 60. Диазепам
Вещества легко проникают через ГЭБ. Взаимодействуя с ГАМКА-ре-цепторами, они усиливают эффекты ГАМК в ЦНС (включая спинной мозг, гиппокамп, черную субстанцию, кору мозга и мозжечка), повышая эффективность ГАМК-ергического синаптического торможения. Бензодиазепины взаимодействуют с собственным сайтом ГАМК-рецептора и не действуют на сайт связывания ГАМК и хлорионофорный протеин. Их фармакологический эффект обусловлен повышением частоты открытий хлорионного канала возбудимых мембран нейронов, а также увеличением сродства (аффинности) ГАМК-рецептора к ГАМК.
Как следует из приведенного ранее материала, основными механизмами антидотного действия бензодиазепинов при отравлении ГАМК-ли-тиками являются: повышение эффективности обусловленного ГАМК торможения нейронов ЦНС, за счет модификации функционального состояния ГАМК-рецепторов, не связанных с ГАМК-литиками; уменьшение сродства ГАМК-рецепторов к ГАМК-литикам; понижение активности ГАМК-литиков в отношении рецепторов, защищенных бензодиа-зепином. При интоксикации ГАМК-литиками бензодиазепины оказываются эффективными при лечебном, но особенно при профилактическом способе применения. Так, в эксперименте, при введении за 30 мин до ДСТА феназепам (2 мг/кг) защищал от 2 и более среднесмертельных доз токсиканта. Показана их антидотная активность при отравлениях лабораторных животных бикукуллином, пикротоксином, БЦФ.
К числу недостатков бензодиазепинов как антидотов относится их слабая эффективность при отравлениях ГАМК-литиком длительного действия норборнаном, а также выраженное и продолжительное седатив-ное, а в действующих дозах и снотворное действие. Время действия бензодиазепинов зависит от скорости их метаболизма микросомальными энзимами печени и последующей конъюгации метаболитов и составляет после однократного введения от 10 до 100 и более часов.
Барбитураты. Барбитураты — физиологические антагонисты ГАМК-литиков. Они обладают антидотными свойствами при отравлениях бикукуллином, пикротоксином, БЦФ. Мединал, барбамил и фенобарбитал проявляли антидотную активность при профилактическом (за 15 мин) и лечебном (при появлении первых признаков интоксикации) применении в условиях пероральной интоксикации лабораторных животных (крыс, кошек) БЦФ (трет-бутилбициклофосфатом) (С. И. Локтионов и соавт.). Антидотная активность различных барбитуратов не в полной мере коррелирует с выраженностью их седативного и снотворного действия. Наибольшей активностью отличается фенобарбитал.
Механизм антидотного действия объясняют: потенцированием действия ГАМК на ГАМК-ергические рецепторы различных отделов ЦНС, обусловленным способностью барбитуратов увеличивать продолжительность периода открытия хлорионных каналов; способностью непосредственно активировать хлорионные каналы, взаимодействуя в относительно высоких дозах с хлорионофорным протеином; препятствовать действию на возбудимые мембраны возбуждающих аминокислот (глутамата и др.); блокировать Са2+-ионные каналы, препятствуя тем самым проникновению кальция из межклеточной среды внутрь нейрона, что необходимо для развития процесса возбуждения (Mg2+-noflo6Hoe действие) и т. д.
К числу недостатков барбитуратов, препятствующих их использованию в качестве средств медицинской защиты, можно отнести: недостаточную терапевтическую широту (противосудорожное действие отчетливо проявляется при введении веществ в дозах, вызывающих сон, угнетение дыхательного центра); необходимость введения веществ в относительно больших объемах (5 и более мл).
Другие противосудорожные средства. Препараты других фармакологических групп оказались недостаточно эффективными при цтравлении ГАМК-литиками. Способностью потенцировать антидотное действие бензодиазепинов и барбитуратов обладают антагонисты возбуждающих аминокислот (кетамин), некоторые блокаторы кальциевых каналов (ни-федипин и др.).
12.1.1.2. Отравляющие и высокотоксичные вещества паралитического действия
12.1.1*2.1. Пресинаптические блокаторы высвобождения ацетилхолина
Ботулотоксин
Ботулотоксин — белок, продуцируемый микроорганизмами Clostridium botulinum. Эти бактерии способны размножаться в белковой среде в анаэробных условиях, и продуцируемый ими экзотоксин порой является причиной массовых отравлений, при использовании в пищу испорченных консервов, копченостей, грибов и т. д. (ботулизм). Впервые случай ботулизма был зарегистрирован в 1735 г. Первое описание вспышки массового отравления, обусловленного потреблением контаминированной кровяной колбасы, было сделано в Германии в 1793 г. Название — ботулизм, происходит от латинского слова botulus — колбаса (термин впервые использован для обозначения заболевания в XIX в.). В конце XIX в. Ван Эрменген связал развитие ботулизма с действием водорастворимого токсина, вырабатываемого анаэробной бактерией, названной тогда Bacillus botulinus.
Очищенный препарат экзотоксина Clostridium botulinum — ботулотоксин изучался военными специалистами США в качестве возможного отравляющего вещества (шифр — XR).
Физико-химические свойства. Токсичность
В настоящее время известны более 7 серологических типов токсина: А, В, С, D, Е, F и т. д., близких по структуре и токсической активности. Ботулотоксин представляет собой протеины с молекулярной массой 150 ООО дальтон, состоящие из двух субъединиц (MB 100 ООО и 50 ООО), соединенных дисульфидными связями. Токсин выделен в кристаллической форме. В водных растворах частично гидролизуется; устойчив к кипячению в течение часа.
Вещество проникает в организм через желудочно-кишечный тракт с зараженной водой и пищей, а при применении его в виде аэрозоля — через органы дыхания и раневые поверхности. Смертельная доза токсина для человека при алиментарном способе воздействия составляет около 50 нг/кг массы. При применении в форме аэрозоля среднесмертельная токсодоза (LQ50) — 2' Ю-5—5 • Ю-5 г -мин/м3. Наибольшей токсичностью ботулотоксин обладает при попадании в организм через раневые поверхности (LD50 менее 1 нг/кг).
Токсикокинетика
В пищеварительном тракте ботулотоксин не разрушается протеолити-ческими ферментами и всасывается через слизистые оболочки желудка и кишечника. При ингаляции аэрозоля вещество проникает в дыхательные пути и адсорбируется на поверхности слизистой оболочки бронхов, бронхиол и альвеолоцитов, где также происходит его всасывание. Часть адсорбированного токсина мерцательным эпителием дыхательных путей выносится в ротовую полость, откуда он поступает в желудочно-кишечный тракт. Поскольку молекулярная масса токсина велика, скорость резорбции мала. Механизмы проникновения этого белкового токсина через неповрежденные слизистые оболочки не выяснены.
Циркулирующий в крови токсин постепенно разрушается протеазами плазмы. Точное время нахождения молекулы токсина в крови не известно.
При исследовании радиоизотопным методом распределения токсиканта в организме установлено, что он избирательно захватывается нервными терминалиями холинергических волокон; часть введенного токсина путем ретроградного аксонального тока транспортируется в тела нервных клеток. Об этом свидетельствует, в частности, высокое содержание 125J в телах мотонейронов спинного мозга экспериментальных животных после введения им яда, меченного этим изотопом.
Проявления интоксикации
Скрытый период интоксикации составляет от нескольких часов до суток и более (чаще до 36 ч). Продолжительность периода зависит от пути поступления токсина в организм и подействовавшей дозы. Наименее продолжителен скрытый период при попадании вещества на раневые поверхности. В клинической картине поражения выделяют общетоксический, гастроинтестинальный и паралитический синдромы. Первые симптомы — это вегетативные реакции (тошнота, рвота, слюнотечение) и признаки общего недомогания (головная боль, головокружение). Через 1—2 сут постепенно развивается неврологическая симптоматика. Усиливается слабость, появляется сухость во рту и сухость кожных покровов. Нарушается зрение (затруднена аккомодация, расширяются зрачки, выявляется их слабая реакция на свет). Основным проявлением интоксикации является постепенно развивающийся паралич поперечно-полосатой мускулатуры. Процесс начинается с глазодвигательной группы мышц (диплопия, нистагм). Ранним признаком отравления является птоз век. Позже присоединяется паралич мышц глотки, пищевода (нарушение глотания), гортани (осиплость голоса, афония), мягкого неба (речь с носовым оттенком, при попытке глотания жидкость выливается через нос). Затем присоединяется парез (а позже и паралич) мимической мускулатуры, жевательных мышц, мышц шеи, верхних конечностей и т. д. Мышечная слабость нарастает в нисходящем направлении и порой первоначально более выражена в проксимальных мышечных группах конечностей (важный диагностический признак). Токсический процесс постепенно нарастает. Иногда лишь на 10-е сут и в более поздние сроки может наступить смерть от паралича дыхательной мускулатуры и асфиксии (при тяжелых поражениях на 3—5-й день заболевания). Расстройств чувствительности при поражении ботулотоксином не бывает. Сознание у пострадавшего полностью сохранено весь период интоксикации. Нередко присоединяются острые пневмонии, токсический миокардит, сепсис (при
раневом процессе). Летальность при отравлении ботулотоксином составляет от 15 до 30%, а при несвоевременном оказании помощи может достигать 90%. По данным литературы (И. В. Маркова и соавт., 1999), кардинальными признаками ботулизма являются:
• отсутствие лихорадки;
• полностью сохраненное сознание;
• нормальная или замедленная частота пульса;
• отсутствие нарушений чувствительности;
• симметричность неврологических нарушений.
Механизм токсического действия
Ботулотоксин оказывает повреждающее действие на различные структурно-анатомические образования периферической нервной системы: нервно-мышечный синапс, нервные окончания преганглионарных нейронов и парасимпатических постганглионарных нейронов. Токсины избирательно блокируют высвобождение ацетилхолина в этих структурах. Наиболее уязвимыми являются нервно-мышечные синапсы.
В опытах in vitro и in vivo, выполненных за рубежом (Пирс и соавт., 1997), установлено, что действие ботулотоксина приводит к угнетению как спонтанного, так и вызванного возбуждением нервного волокна выброса нейромедиатора в нервных окончаниях. Чувствительность постсинаптических рецепторов к ацетилхолину не изменяется. Блокада передачи сигнала не сопровождается изменением характеристик процессов синтеза и хранения ацетилхолина. При исследованиях in vitro установлено, что после добавления в инкубационную среду токсина в концентрации Ю-8 М спонтанная и вызванная активность концевой пластинки мотонейрона снижается на 90% в течение 60-90 мин. По расчетам, для блокады одного синапса достаточно 10 молекул яда. В экспериментах также установлено, что чем выше нервная активность, тем быстрее развивается блок проведения импульса в синапсах.
Полагают, что в основе эффекта лежит нарушение токсином механизма взаимодействия синаптических везикул, в которых депонирован аце-тилхолин, с аксолеммой, — необходимый этап процесса Са2+-зависимого экзоцитоза медиатора в синаптическую щель. Электрофизиологические исследования показывают, что в отличие от нормальной реакции нервно-мышечного синапса на повышение содержания кальция в инкубационной среде (дозо-зависимый выброс нейромедиатора) увеличение концентрации экстрацеллюлярного кальция с 2 до 16 мМ не приводит к усилению выброса ацетилхолина нервным окончанием, обработанным ботулотоксином. Только совместное введение в инкубат Са2+ (4 мМ и выше) и некоторых ионофоров (4-аминопиридин, гуанидин и др.) временно усиливает выброс ацетилхолина из нервных окончаний.
Действие вещества продолжительно, до нескольких недель, и потому характер взаимодействия токсина с пресинаптическими структурами-мишенями можно рассматривать как необратимое. Полагают, что восстановЛение нормальной иннервации мышц происходит в результате формирования новых синаптических контактов.
Морфологические изменения в пораженных синапсах не выявляются методами световой и электронной микроскопии.
Молекулярный механизм действия токсина окончательно не выяснен. Доказанными являются следующие представления.
Как указывалось ранее, периоду клинических проявлений предшествует скрытый период, во время которого происходит взаимодействие токсиканта с нервными окончаниями. Выделяют четыре периода действия токсина на синапс:
• связывание его с плазматической мембраной холинергических нервных окончаний;
• интернализация токсина путем эндоцитоза внутрь нервного окончания;
• высвобождение действующей части белковой молекулы токсина и проникновение ее в цитозоль пресинаптического окончания при участии рН-зависимой транслоказы;
• проявление действующей частью токсина свойств металл-зависимых эндопротеаз и разрушение специфических белков, участвующих в процессе выделения ацетилхолина из нервного окончания.
За процесс связывания с рецептором (акцептором) нервного окончания ответственна прежде всего тяжелая субъединица сложной молекулы токсина. Аффинность окончаний различных холинергических нейронов к молекулам ботулотоксина неодинакова. Наивысшим сродством обладают окончания мотонейронов, иннервирующих произвольную мускулатуру. У различных серологических типов, ботулотоксина сродство к акцепторам неодинаково.
Интернализация связавшегося с рецепторами токсина осуществляется путем эндоцитоза. В результате токсин оказывается внутри нервного окончания заключенным в мембранные везикулы, называемые эндосомами.
После проникновения внутрь нервного волокна высокомолекулярная субъединица токсина образует пору в мембране эндосомы, которая действует как канал, через который легкая цепь проникает в цитозоль пресинаптического окончания.
Теперь, свободно передвигаясь в нервном окончании, легкая цепь токсина оказывает воздействие на субстратные белки.
Биохимические исследования показали, что нейротоксины обладают цинк-зависимой эндопептидазной активностью и энзиматически расщепляют ряд белков нервных окончаний, важных для нормального высвобождения нейротрансмиттеров. Ботулотоксины А и Е расщепляют белок SNAP-25, ботулотоксин С — НРС-1 (синтаксин), токсины D и F расщепляют изоформу VAMP-1 (синаптобревин-1), токсин В — VAMP-2 (синаптобревин-2) и т. д. Протеолитическое расщепление этих специфических белков в нервных окончаниях приводит к угнетению нормального высвобождения ацетилхолина и в конечном счете к появлению основных признаков ботулизма.
Мероприятия медицинской защиты /
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Специфическими противоядиями ботулотоксина являются противо-ботулинические сыворотки (А, В, Е). При подозрении на поражение токсином возможно профилактическое внутримышечное введение сывороток по 1000-2000 ME каждого типа с последующим наблюдением за пострадавшим в течение 10-12 дней. Решение о назначений сывороток достаточно сложно и требует участия квалифицированного специалиста, поскольку, с одной стороны, эти лекарственные средства не всегда оказываются эффективными (иные серологические типы токсина, быстрое необратимое взаимодействие яда с нервными окончаниями), а с другой — достаточно высока вероятность осложнений, связанных с их применением (анафилаксия, сывороточная болезнь).
В эксперименте in vitro нервную передачу в синапсах, нарушенную бо-тулотоксином, временно нормализует 4-аминопиридин. Полагают, что действие вещества обусловлено его способностью облегчать транспорт ионов кальция через мембрану нервных окончаний и преодолевать тем самым блок Са2+-зависимого экзоцитоза ацетилхолина. При введении летальной дозы токсина экспериментальному животному последующее назначение 4-аминопиридина отчасти восстанавливает двигательную активность животного на 1-2 ч. К сожалению, из-за высокой токсичности и кратковременности эффекта 4-аминопиридин не может рассматриваться как эффективное противоядие. Табельные средства медицинской защиты отсутствуют.
При появлении признаков угнетения дыхания необходимо предусмотреть возможность перевода пострадавшего на искусственную вентиляцию легких.
12.1.1.2.2. Блокаторы Na+-ионных каналов возбудимых мембран
Сакситоксин. Тетродотоксин
В строгом смысле слова вещества этой группы не относятся к «чистым» нейротоксикантам, поскольку, блокируя ионные каналы, действуют на возбудимые мембраны всех типов клеток организма: нервных, мышечных, железистых. Порой не возможно решить, поражение какой из структур является ведущим в патогенезе острой интоксикации. Тем не менее внешние признаки тяжелого поражения очень напоминают действие миорелаксантов, традиционно относимых к группе нейротоксикан-тов. И поэтому, хотя механизм действия веществ иной, представляется целесообразным рассмотреть их свойства в данном разделе. Достаточно хорошо изученными представителями группы являются сакситоксин и тетродотоксин, признаки поражения которыми, по сути, одинаковы. Боевое применение токсинов маловероятно, однако эти вещества рассматривались в качестве возможных диверсионных средств (В. В. Мясников, 1989; Франке, 1973). В 60-70-х гг. XX в. свойства токсинов активно изучались военным ведомством США.
Физико-химические свойства. Токсичность
Сакситоксин. В 1957 г. Шантцем с соавт. были изучены свойства так называемого «паралитического яда моллюсков» — одного из наиболее токсичных веществ небелковой природы. По названию морского моллюска, из ткани которого токсикант выделили (Saxidomus), вещество получило название сакситоксин. Позже было установлено, что в организме животных сакситоксин не синтезируется, а поступает туда с одноклеточными (жгутиковые) вида Gonyaulax catenella, которыми моллюски питаются. Количество вырабатываемого простейшими вещества колеблется в очень широких пределах и зависит от географического региона, времени года и других условий.
В случае массового размножения Gonyaulax целый ряд моллюсков поглощают их в большом количестве и концентрируют в своих тканях токсин, который для них практически безвреден. Становясь при этом ядовитыми, моллюски, съедобные для человека в обычных условиях, при использовании в пищу, вызывают случаи массового отравления людей.
Сине-зеленые водоросли пресноводных водоемов также синтезируют сакситоксин. Наблюдались случаи отравления скота водой, зараженной этими водорослями.
Сакситоксин (МВ-372) - аморфный, хорошо растворимый в воде спирте, метаноле, ацетоне порошок. Вещество устойчиво в водных растворах. Химическое строение представлено на рис. 61. Молекулы сакси-токсина, выделенные из разных источников, не полностью идентичны
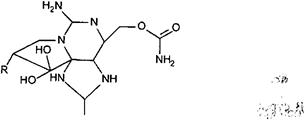
NH2
Рис. 61. Структура молекулы сакситоксина
Расчетная смертельная доза сакситоксина для человека составляет по разным данным 0,004—0,01 мг/кг. Токсичность для мышей при внутри-брюшинном способе введения — около 0,009 мг/кг (с регистрацией гибели в течение 30 мин). При назначении вещества через рот смертельная доза — 0,25 мг/кг.
Тетродотоксин обнаружен в тканях целого ряда живых существ, среди которых рыбы (более 70 видов, в том числе семейства Tetrodontidae — четы-рехзубообразные), лягушки (3 вида), моллюски (1 вид). В Японии, где представитель четырехзубообразных, рыба Фугу, является деликатесом, десятки людей ежегодно отравляются в результате неумелого приготовления блюда.
Вещество выделено в чистом виде, структура его изучена (рис. 62). Это — бесцветный порошок, хорошо растворимый в воде. Раствор стабилен при комнатной температуре. Молекулярная масса — 319,3.
о
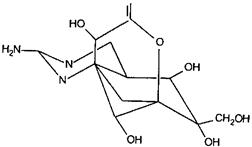
Рис. 62. Структура молекулы тетродотоксина
бе в1еле^ия otn^m ^ 6елыхттмыи«* "Ри внугрибрюшинном спосо-
v ccSJ ' МГ/КГ МаССЬЬ Доза в °'005 ^Асг (подкожно) вызывает
Jcf ™ Р ^ наРУшение дыхания, а дозы более 0,006 мг/кг в течение часа приводят к гибели в результате прекращения дыхания и асфиксии
Токсикокинетика
Через неповрежденную кожу вещества не проникают. Опасность представляет попадание токсинов на раневые поверхности, а также (прежде всего) потребление воды и пищи, зараженной ядами. Вещества быстро абсорбируются в кишечнике и столь же быстро выводятся из организма с мочой. Детально токсикокинетика токсинов не изучена. Дискуссионным остается вопрос о способности веществ проникать через гематоэнцефалический барьер.
Основные проявления интоксикации
Независимо от способа поступления в организм симптомы отравления практически одинаковы.
Спустя 10—45 мин появляются тошнота, рвота, боли в животе, понос. Ранними признаками поражения являются парестезии в области рта, губ, языка, десен, распространяющиеся на область шеи, покалывание, ощущение жжения кожи конечностей. Позже развиваются бледность кожных покровов, беспокойство, общая слабость, онемение конечностей, возникает ощущение невесомости тела. Зрачок сначала сужен, затем расширяется. В тяжелых случаях взгляд фиксирован, зрачковый и корнеальный рефлексы отсутствуют, появляются признаки бульбарных нарушений: затруднение глотания, речи (иногда — афония), нарастают брадикардия и гипотензия, отмечаются гиперсаливация, профузная потливость, понижение температуры тела. Дыхание учащается, становится поверхностным, развивается цианоз губ и конечностей.
Двигательные расстройства проявляются все отчетливее: появляются подергивания отдельных групп мышц, тремор, координация движений нарушается. Начавшись в области конечностей, постепенно развивающийся паралич распространяется на другие мышечные группы, охватывая все большие группы мышц. Сознание, как правило, сохраняется весь период интоксикации. Смерть наступает от паралича дыхательной мускулатуры и асфиксии в течение 6—24 ч от начала интоксикации. Если больной выживает, в течение последующих суток наступает практически полная нормализация состояния, в большинстве случаев, без отдаленных последствий.
Помимо типичной паралитической формы выделяют также гаст-ро-интестинальный и аллергический варианты течения отравления. Первый вариант проявляется признаками общего недомогания, чувством жажды, саливацией, болями в животе, тошнотой, рвотой, поносом.
Аллергическая форма отравления развивается у отдельных лиц с повышенной чувствительностью к токсинам. Характерно появление экзантем (эритематозная форма). Иногда на коже и слизистых оболочках образуются пузыри.
Механизм токсического действия
Тетродотоксин, как и сакситоксин, оказывает избирательное действие на возбудимые мембраны нервов и мышц. Как известно, градиент концентрации ионов между внутренней и внешней средой клетки формирует потенциал покоя возбудимой мембраны, равный примерно 90 мВ (табл. 52).
Таблица 52
Распределение ионов внутри и вне возбудимых клеток, мМ/л
_______________________ (по Katz, 1971)
| Ионы | Мышечная клетка | Нервная клетка | ||
| снаружи | внутри | снаружи | внутри | |
| Na+ | 9,2 | |||
| К+ | 2,5 | |||
| ci- | 3-4 | 40-100 |
Градиенты концентраций калия и хлора примерно уравновешивают друг друга. Поэтому проницаемость мембраны для этих ионов хотя и ограничена, но относительно высока. Проницаемость натриевых каналов в покое ничтожно мала. Более того, Na+ постоянно «выкачивается» за пределы нейрона с помощью энергозависимых механизмов против высокого электрохимического градиента. Таким образом, потенциал покоя представляет собой не что иное, как готовый к использованию источник накопленной энергии, необходимой для генерации сигнала (потенциала действия). Если возбудимая мембрана деполяризуется примерно на 15 мВ, электровозбудимые натриевые каналы открываются, проницаемость их для ионов резко возрастает, Na+устремляется в клетку, разница потенциалов по обе стороны мембраны падает, деполяризация мембраны еще более усиливается, формируется потенциал действия и возбуждение передается по нервному (или мышечному) волокну. Затем в течение около 0,8 мс потенциал на мембране возвращается к исходному уровню, главным образом за счет выхода ионов калия из клетки. Усиление проницаемости для К+ необходимо для полной реполяризации мембраны и восстановления исходного потенциала покоя. При этом восстанавливается и исходная проницаемость мембраны для натрия.
Тетродотоксин и сакситоксин полностью блокируют проникновение ионов Na+ по ионным каналам возбудимых мембран внутрь клеток. При этом становится невозможным формирование потенциала действия возбудимых мембран — нарушается проведение нервных импульсов по нейронам, сокращение миоцитов. В эксперименте показано, что вещества действуют только при экстрацеллюлярной аппликации. В соответствии с расчетами одна молекула токсинов полностью блокирует один ионный канал. Полагают, что взаимодействие токсикантов с белковыми молекулами, формирующими ионный канал, осуществляется за счет группы гуанидина, содержащейся в структуре как сакси-, так и тетродотоксина. Взаимодействие токсинов с белками ионных каналов обратимо. In vitro яды могут быть удалены с поверхности возбудимой мембраны простым отмыванием биопрепарата.
Исчерпывающих данных о причинах развивающихся эффектов нет. Так, до конца не определено, возбудимые мембраны каких структур, нервных клеток (ЦНС, периферии) или миоцитов, являются более чувствительными к действию токсинов. Так, по мнению одних исследователей,' остановка дыхания является следствием действия токсинов на нейроны
дыхательного центра, другие полагают, что основным является нарушение проведения нервного импульса по дыхательным нервам или возбудимости дыхательных мышц. Вероятно, более справедливо последнее предположение, поскольку электровозбудимость диафрагмы блокируется меньшими дозами токсикантов, чем проведение нервного импульса по диафрагмаль-ному нерву. Кроме того, в опытах на анестезированных кошках показано, что при введении вещества в смертельной дозе проведение нервных импульсов по диафрагмальному нерву не прекращается даже тогда, когда элект-ромиограмма диафрагмальной мышцы уже безмолвствует.
Развивающееся снижение артериального давления также связывают как с блокадой проведения нервных импульсов по симпатическим нервным волокнам, так и с параличом гладкомышечных клеток сосудистой стенки. Сердечная мышца вовлекается в процесс при введении токсиканта лабораторным животным в дозе 0,007 мг/кг.
Нарушение чувствительности (парестезии с последующим онемением) — следствие поражения возбудимых мембран чувствительных нейронов.
Многие центральные эффекты, такие как атаксия, головокружение, нарушение речи и т. д., могут быть связаны с действием вещества непосредственно на нейроны ЦНС.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
, . • применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации. Медицинские средства защиты
В порядке оказания доврачебной и первой врачебной помощи у пострадавшего необходимо вызвать рвоту, провести зондовое промывание желудка. Специфических средств профилактики и терапии интоксикации нет. Поскольку при тяжелых формах поражения единственным надежным способом сохранения жизни является перевод пострадавшего на искусственную вентиляцию легких, необходимо принять меры к скорейшей эвакуации пострадавших в лечебные учреждения. В случае сохранения жизни прогноз благоприятный: выздоровление бывает быстрым и полным.
ЗОВ
3Q9
12.1.2. Отравляющие и высокотоксичные вещества психодислептического действия
Психодислептическим называется токсическое действие химических веществ, сопровождающееся нарушением процессов восприятия, эмоций, памяти, обучения, мышления и формированием состояния, характеризующегося неадекватными поведенческими реакциями личности на внешние раздражители.
Научное изучение психоактивных веществ (влияющих на психические процессы) началось лишь во второй половине XX в., хотя действие некоторых из них знакомо человечеству уже тысячелетия. В настоящее время известны сотни соединений с подобными свойствами, причем многие — широко используются в клинической практике, а некоторые — испытывались на предмет применения с военными целями как боевые отравляющие вещества.
Способность вызывать психодислептический эффект у разных психоактивных веществ выражена неодинаково. Так, в рекомендованных врачом дозах большинство психотропных лекарственных препаратов (нейролептики, антидепрессанты, психостимуляторы, наркотические анальгетики и т. д.) угнетают или активируют (в зависимости от свойств) процессы, лежащие в основе высшей нервной деятельности, сохраняя в целом адекватное отношение личности к окружающей действительности. Только в относительно больших дозах они в той или иной степени могут извращать процессы восприятия, эмоций, памяти и т. д.
Однако известны вещества, для которых психодислептический эффект является основным в профиле их биологической активности. Количество такого вещества, делающее человека полностью недееспособным, в сотни — тысячи раз меньше того, в котором это же вещество угнетает сознание или вызывает соматические расстройства. Такие вещества иногда называют психодислептиками, психотомиметиками, психогениками, психоделиками, подчеркивая их особую способность извращать функции высшей нервной деятельности.
В табл. 53 представлена классификация наиболее изученных соединений.
Строение некоторых веществ, относящихся к этой группе, представлено на рис. 63.
Признаки тяжелого поражения психодислептиками достаточно однотипны. Напротив, картина легкого и средней степени тяжести отравления характеризуется значительной полиморфностью и даже при воздействии одного и того же соединения развивающиеся эффекты существенно зависят от индивидуальных личностных особенностей человека и ситуации, на фоне которой произошло поражение. Тем не менее наблюдения показывают, что можно выделить несколько типичных вариантов течения интоксикации. Так, при отравлениях некоторыми веществами доминирует изменение эмоционального статуса (эйфория и т. д.); другие вещества преимущественно вызывают нарушения процессов восприятия (иллюзии, галлюцинации и т. д.) с умеренным извращением ассоциативных процессов;
третьи — формируют глубокое извращение психической активности, затрагивающее все ее стороны (делирий). Эти особенности обусловлены прежде всего различными механизмами действия веществ на центральную нервную систему. В этой связи есть основания выделить группы токсикантов в соответствии с особенностями формируемых ими токсических процессов:
1. Эйфориогены: Д-тетрагидроканнабинол, суфентанил, клонитазен и др.
2. Галлюциногены (иллюзиогены): ДЛК, псилоцин, псилоцибин, буфотенин, мескалин и др.
3. Делириогены: BZ, скополамин, дитран, фенциклидин и др.
Таблица 53
Химическая классификация психодислептиков
| Группа соединений | Представители |
| Производные триптамина | диметилтриптамин буфотенин псилоцин псилоцибин диэтипамид лизергиновой кислоты (ДЛК) гармин |
| Производные фенилалкиламинов | мескалин 2,5-диметокси-4-метиламфетамин 2,5-диметокси-4-этиламфетамин триметоксифенизопропиламин |
| Пиперидилгликоляты | атропин скополамин хинуклединилбензилаты |
| Производные фенилпиперидина и бензимидазола | фентанил суфентанил этонитазен |
| Разные | фенциклидин (сернил) Д-тет раги дрокан набинол |
Поскольку препараты первой группы вызывают отчетливое психодис-лептическое действие лишь в дозах, близких к тем, в которых отмечается угнетение сознание, нарушение двигательной активности, а иногда и угнетение дыхательного и сосудо-двигательного центров, для военной медицины интерес представляют психодислептики только второй и третьей групп. Некоторые из них ранее предполагали использовать на поле боя в качестве отравляющих веществ, временно выводящих из строя личный состав противника (психотомиметические ОВ). С этой целью в различное время изучали такие вещества, как М,К-диметилтриптамин, буфотенин, мескалин, диэтиламид лизергиновой кислоты (ДЛК), фенил-циклогек-сил-пиперидин (фенциклидин), 3-хинуклидинил-бензилат (BZ) и т. д. Эти вещества также можно рассматривать как потенциальные диверсионные яды.
| с,н, |
| ?п5 |
| I / |
| N |
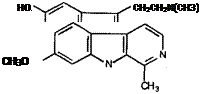 |  | ||
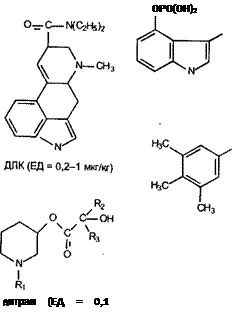
 |


хинуклединилбензилат (ECt = 100 мг'мин/м3)
С2Н5
клонитазен
Рис. 63. Структуры некоторых химических веществ, обладающих психодислептической активностью
Галлюциногены
Галлюциногенами называют вещества, в клинической картине отравления которыми преобладают нарушения восприятия в форме иллюзий и галлюцинаций, при этом пострадавшие, как правило, не утрачивают контакт с окружающими. К числу галлюциногенов относятся некоторые производные триптамина и фенилэтиламина (см. выше), нарушающие проведение нервного импульса преимущественно в серотонинергических и катехола-минергических синапсах мозга. Характерной особенностью интоксикации галлюциногенами является отсутствие амнезии на пережитые события.
Большинство галлюциногенов — вещества животного и растительного происхождения, используемые человеком с древних времен для самоотравления с ритуальными целями. Некоторые токсиканты и сегодня ис- f пользуются наркоманами. 3—4 ежедневных приема веществ приводит к развитию толерантности, которая, однако, быстро проходит. Перекрест-312 ная толерантность отмечается между мескалином, псилоцибином, ДЛК, некоторыми другими психодислептиками. Наиболее опасным из галлюциногенов считается синтетическое вещество — метилен диоксиамфета-мин (МДА). Острые отравления МДА иногда заканчиваются смертью.
Представителем группы, глубоко исследовавшимся военными ведомствами, является диэтиламид лизергиновой кислоты.
12.1.2.1.1. Диэтиламид лизергиновой кислоты (ДЛК)
Психодислептические свойства ДЛК стали известны человечеству 16 апреля 1943 г. Именно в этот день Гофман, работавший в лаборатории Штоля в Базеле, случайно принял ничтожное количество вещества внутрь. В результате развилась интоксикация, сопровождавшаяся нарушением психики. С этого момента началось экспериментальное изучение галлюциногенов. Долгое время ДЛК рассматривали как потенциальное ОВ и потому свойства его подверглись глубокому исследованию. В настоящее время целесообразность применения вещества на поле боя отрицается, но не исключено использование его в качестве диверсионного агента.
Физико-химические свойства. Токсичность
ДЛК — белый кристаллический порошок без запаха. Плавится при температуре 83° С с разложением. Не летуч. Плохо растворим в воде, растворяется в органических растворителях. Некоторые соли ДЛК (тартарат) хорошо растворимы в воде.
Летальная доза для мышей — 50 мг/кг, для крыс — 15 мг/кг. При приеме вещества внутрь человеком в дозе 0,005 мг/кг развиваются выраженные психозы. В качестве пороговой дозы называют 0,0002—0,0003 мг/кг. Выводящая из строя токсодоза при ингаляционном воздействии аэрозоля составляет 0,01—0,1 г* мин/м3.
Токсикокинетика
Вещество способно быстро проникать в организм через желудочно- кишечный тракт, а также через слизистые оболочки дыхательных путей при ингаляции в форме аэрозоля. Максимальная концентрация в крови и тканях отмечается через 10—20 мин после приема. В ткани мозга в этот момент содержится менее 1% от введенного количества. Через 3 ч 80% вещества определяется в стенках и содержимом кишечника, 3% — в печени. С мочой в неизмененном виде выделяется около 1 % от введенного количества вещества. Метаболизм ДЛК включает реакции окисления молекулы (6-гидроксилиро-вание) и ее конъюгации с метальным радикалом (N-метилирование).
Основные проявления интоксикации
В экспериментальных исследованиях, выполненных на животных различных видов (мыши, крысы, кролики, собаки, обезьяны), установлено, что ДЛК вызывает изменения спонтанного поведения и нарушения условнорефлекторной деятельности.
Характер действия ДЛК. на поведение иллюстрируется протоколом опыта на павиане гамадриле, у которого был выработан прочный двигательный пищевой рефлекс на два типа звонков (сильный и слабый), двигательный оборонительный рефлекс на метроном и ориентировочная реакция на комплексный раздражитель (тон+свет).
11 ч 00 мин. Обезьяна подвижна. При включении положительных сигналов быстро подходит к стержню, сильно толквет его и бежит к кормушке. Получает пищевое подкрепление. Дифференцировка полная. При включении метронома подбегает к рычагу и нажимает на него, тем самым выключая ток, поданный на решетку, расположенную на полу камеры. При включении первого компонента ориентировочного сигнала (тон) бежит к окну, где включается свет, и рассматривает выставленные там предметы. 11 ч 25 мин. Внутримышечно введен ДЛК в дозе 0,04 мг/кг. 11 ч 35 мин. Включен слабый звонок. Реакции нет, облизывается. При движении качается. На звуковой сигнал (звонок) не реагирует. Включен ориентировочный сигнал. Оглянулась и пошла не к ориентировочному окну, а к противоположной стенке.
11 ч 40 мин. Включен метроном. Реакции нет. Сделала неудачную попытку побежать. Сидит в необычной позе.
11ч 50 мин. При включении сигнала испуганно убегает. Резкая настороженность.
12ч 00 мин. Подошла к рычагу. Взяла его двумя лапами, но не нажала, чтобы выключить ток. Включены последовательно сильный и слабый звонок. Реакции нет. Движения стали более координированными. При включении ориентировочного сигнала вздрогнула. Движения резкие.
14 ч 30 мин. Состояние близко к исходному. Несколько угнетена. Большую часть времени сидит на одном месте. Восстановилась условная реакция на сильный и слабый звонки. Дифференцировка полная. Реагирует правильно на ориентировочный сигнал.
Клиническая картина отравления ДЛК у человека складывается из нарушений восприятия, психики, соматических и вегетативных нарушений.
Нарушения восприятия проявляются искажением формы и цвета наблюдаемых объектов, затруднением фокусирования зрения на объекте, обострением слухового восприятия и, реже, парестезиями и синестезиями, зрительными, тактильными, вкусовыми галлюцинациями, расстройством ощущения «схемы тела».
Психические нарушения — это изменение настроения (эйфория, сменяющаяся депрессией, беспокойство), напряжение, сонливость; нарушение чувства времени («время остановилось»), затрудненность в выражении мыслей, деперсонализация (утрата представлений о собственном «Я»), возникновение ощущений, похожих на сновидения, спутанность сознания.
Соматические нарушения сопровождаются головокружением, слабостью, тремором рук, атаксией, дизартрией, спастическими состояниями, угнетением дыхания и т. д.
Вегетативные расстройства — тошнота, мидриаз, тахикардия, сменяющаяся брадикардией, гипергликемия, пиломоторные реакции, гипотония.
Первые признаки отравления появляются через 40-60 мин после приема токсиканта (при внутривенном введении вещества — через 5—10 мин). Симптомы достигают максимума через 1,5—3 ч.
Отравление, как правило, развивается в определенной последовательности: вначале появляются соматические и вегетативные симптомы, затем нарушается перцепция, изменяется настроение, нарушается психика.
Перед началом психоза отравленный чувствует легкую тошноту, зрачки расширяются. Появляются беспокойство, расстройство зрения, ослабление внимания, беспричинный смех, затруднения речи. Зрительные восприятия искажаются — предметы и вещи деформируются, увеличиваются или уменьшаются в размерах и принимают неестественную окраску (иллюзии). Отравленный теряет ощущение времени. Реакции значительно замедляются.
Зрительные галлюцинации проявляются в виде фантастических ярко окрашенных и пестрых образов, калейдоскопически сменяющих друг друга. Галлюцинации более выражены при закрытых глазах. Настроение при этом у испытуемых, по их словам, «необыкновенно хорошее». Однако иногда (как правило, у людей, не знавших о назначении им галлюциногена) появляются чувство страха, враждебное и недоверчивое отношение к окружающим. Пораженные повышенно чувствительны к прикосновению и иногда реагируют на него импульсивно и злобно. На протяжении всего периода легкой интоксикации сохраняется способность к правильным суждениям и умозаключениям. Контакт с пораженным затруднен, но возможен. Тяжелые интоксикации сопровождаются нарушениями мышления вплоть до помрачения сознания.
Общая продолжительность интоксикации составляет 6-12, реже до 24 ч. По выходе из этого состояния пострадавший помнит пережитое. Возможны спонтанные рецидивы, а также затяжные психозы в результате воздействия галлюциногена в обычной дозе (как правило, у лиц со скрытой формой психических заболеваний).
Механизм токсического действия
ДЛК действует на центральный и периферический отделы нервной системы. К числу центральных эффектов ДЛК относятся все сенсорные и психические нарушения, часть соматических и вегетативных реакций, таких как гипертермия, гипергликемия, тахикардия и т. д. Периферическое действие ДЛК проявляется тремором, мидриазом, сокращением мускулатуры матки, гипотонией, пилоэрекцией, брадикардией и т. д.
В основе токсических эффектов, развивающихся при действии ДЛК на нервную систему, лежит способность токсиканта вмешиваться в проведение нервных импульсов в серотонинергических и катехоламинерги-ческих синапсах.
Серотонинергическая медиаторная система мозга представлена 10—20 тысячами клеток (менее 0,1% нейронов), тела которых компактно залегают в ядрах шва — образованиях вентральной покрышки среднего мозга, расположенных в основном под сильвиевым водопроводом. Эти нейроны ин-нервируют все отделы ЦНС, особенно плотно образования зрительного анализатора, лимбической системы, гипоталамуса (в норме содержание серотонина в различных структурах мозга составляет 5—30 нг/мг белка).
Первоначально полагали, что основным видом действия токсиканта является способность блокировать постсинаптические рецепторы в синапсах, образуемых окончаниями аксонов серотонинергических нейронов в иннервируемых ими отделах мозга. Было показано, что особенно выражено антисеротонинергическое действие на 5-НТ2-подтип рецепторов (преимущественная локализация — кора головного мозга). Однако только этим объяснить развивающийся эффект не удается, поскольку в настоящее время существует большое количество центральных серотонинолитиков, обладающих преимущественно антагонистическим действием в отношении 5-НТ2-подтипа рецепторов серотонина, лишенных психодислептической активности. В какой-то мере снимают противоречие данные, полученные в эксперименте. Так, установлено, что ДЛК не только выступает в качестве антагониста серотонина, но и способен угнетать спонтанную активность самих серотонинергических нейронов. Более того, установлено, что при определенных концентрациях в тканях мозга ДЛК может выступать и как аго-нист серотонина, особенно в отношении 5-HTia (преимущественная локализация — ядра шва) и 5-HTic-peuerrropoB. Высказано предположение, что вещество прежде всего возбуждает ауторецепторы, образуемые окончаниями нейронов на своих собственных телах. Функция такой иннервации — подавлять активность нервных клеток по механизму отрицательной обратной связи. За счет этого, в отличие от эффектов классических серотонино-литиков, при отравлении ДЛК уровень нейромедиатора в ЦНС не только не понижается, но, напротив, существенно возрастает (в основном связанной формы). Установлено, что ДЛК в эффективных дозах не действует на ферменты, обеспечивающие синтез (5-гидрокситриптофандекарбоксилаза) и разрушение (моноаминоксидаза) серотонина, а также на систему его транспорта в мозге. Предполагается, что повышение содержания серотонина в мозге является следствием замедления скорости его «оборота», которое наступает при подавлении активности нервных клеток. В пользу такого предположения свидетельствуют и данные, указывающие на снижение секреции с мочой 5-гидроксиндолилуксусной кислоты, которая рассматривается как основной метаболит серотонина. Выявлено совпадение во времени указанных биохимических изменений с развитием нарушений поведения.
Так или иначе, происходит смещение баланса процессов торможения и возбуждения как внутри самой серотонинергической системы, так и в других тесно взаимодействующих с ней нейромедиаторных системах мозга (катехоламинергической, холинергической, ГАМК-ергической), что в определенной степени коррелирует с симптомами интоксикации.
Нейрофармакологические, биохимические и электрофизиологические исследования показывают, что ДЛК избирательно воздействует на нейро-нальные катехоламинергические системы ретикулярной формации и других образований мозга. Отдельные симптомы отравления, такие, как моторная гиперактивность, тахикардия, гипертензия, мидриаз, гипертермия и другие, указывают на преобладание у отравленных симпатотонии.
Дофаминергическая медиаторная система мозга представлена четырьмя основными отделами: стрионигральным, мезолимбическим, фронтальным, тубероинфундибулярным. Тела нейронов этих отделов залегают в области черной субстанции и межножкового ядра среднего мозга и иннервируют соответственно: стриатум, мезолимбические структуры, фронтальные отделы коры мозга и некоторые ядра гипоталамуса.
ДЛК активирует ДА-ергические нейроны всех отделов системы (дофа-миномиметическое действие). При этом активируется процесс синтеза нейромедиатора, ускоряется его оборот в стриатуме, гипоталамусе, лимби-ческих ядрах. Ускорение оборота приводит к снижению уровня дофамина в соответствующих структурах мозга. Активируются и другие катехоламинергические системы. В последнее время получены убедительные данные, свидетельствующие о снижении у животных под влиянием ДЛК уровня норадреналина, главным образом в среднем мозге и гипоталамусе. По-видимому, ДЛК повышает активность и норадренергических структур мозга (как показано, возбуждая а-адренорецепторы), вследствие чего увеличивается высвобождение норадреналина и развивается дефицит его функциональных запасов. О значении нарушений со стороны катехоламинергиче-ских образований в патогенезе интоксикации ДЛК говорит и то, что назначение отравленным животным аминазина (дофамин- и адренолити-ка) облегчает течение интоксикации, резерпин (истощает запасы катехола-минов и серотонина в ЦНС), напротив, усиливает действие ДЛК.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих здоровью и дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Табельные средства защиты отсутствуют. Частичными специфическими антагонистами ДЛК (физиологические антагонисты) являются нейролептики. Как известно, в основе антипсихотического действия препаратов этой группы лежит способность блокировать рецепторы дофамина (преимущественно D2- и О^рецепторы, в меньшей степени Di-рецепто-ры), а также сц-рецепторы норадреналина и 5-НТ2-рецепторы. К числу нейролептиков относятся производные фенотиазина (аминазин, тиори-дазин, трифлюоперазин и т. д.), тиоксантена (тиотикрен), бутирофенона (гало пер идол), бензамида (метоклопрамид, диметпрамид) и т. д. Эти средства могут быть использованы при оказании помощи пострадавшим с целью ликвидации приступа паники, нормализации психического статуса, восстановления психической работоспособности. Наиболее эффективны: аминазин (50—75 мг внутримышечно), трифлюоперазин (2—6 мг внутримышечно), галоперидол (5—15 мг внутримышечно). Поскольку нейролептики блокируют не только DA- и аррецепторы, возбуждаемые ДЛК, но и НТг-рецепторы, которые также блокируются токсикантом, антагонизм между лечебными средствами и ядом не полный. Отсюда ограничения эффективности препаратов. Попытка усилить антидотный эффект путем значительного увеличения дозы вводимых нейролептиков
недопустима, так как при этом проявляется их центральное холинолити-ческое действие и психоз может усилиться (см. ниже).
При развитии психомоторного возбуждения, реакции беспокойства, страха возможно назначение симптоматических средств, в частности бен-зодиазепинов (диазепам 2—10 мг через рот или внутримышечно).
Поскольку вещество отчасти в неизмененном состоянии выводится в просвет кишечника, откуда затем может повторно всасываться (энтераль-ная циркуляция), целесообразно назначить пострадавшим активированный уголь, солевое слабительное.
Эвакуация необходима лишь при развитии затяжных психозов.
12.1.2.2. Делириогены
Делирий способны вызывать все вещества, обладающие центральной хо-линолитической активностью. Издавна известны случаи отравлений беленой, дурманом, красавкой — растениями, содержащими алкалоиды атропин и скополамин. Дозы соответствующих лекарственных препаратов, вызывающих психодислептический эффект, указаны в табл. 54.
Таблица 54
«Психотомиметические» дозы некоторых холинолитиков
| Вещество | Доза, мг/кг |
| Атропин | 0,08-0,12 |
| Скополамин | 0,04-0,06 |
| Пентафен | 3,0-4,0 |
| Амизил | 0,1-1,0 |
| Дитран | 0,04-0,12 |
Наряду с «классическими» холинолитиками, сходную клиническую картину поражения могут вызывать лекарственные препараты из группы нейролептиков (производные фенотиазина) и некоторые трицикличе-ские антидепрессанты (фторацизин и др.), которые в высоких дозах также блокируют центральные М-холинорецепторы, т. е. проявляют свойства холинолитиков.
Основными проявлениями делирия являются:
• беспокойство;
• нарушение оценки своего состояния;
• спутанность сознания;
• галлюцинации;
• бред;
• нарушение контакта с окружающими;
• нарушение координации движений;
• гиперрефлексия;
• гипертермия;
• психомоторное возбуждение;
• амнезия.
Можно выделить несколько степеней тяжести острого отравления (табл. 55).
Таблица 55
Степени тяжести и фазы течения интоксикаций атропиноподобными препаратами (по С. С. Крылову и соавт., 1999)
| Степени тяжести | Основные проявления | Фазы течения |
| Субпсихотиче екая Легкая | Снижение работоспособности, ухудшение самочувствия Оглушенность, маниакально-и галлюцинозоподобные комплексы | Не прослеживаются Астения с резидуальными состояниями |
| Средняя | «Субделирий» | ■ Оглушенность « «Субделирий» • Критический сон « Астения |
| Тяжелая | Делирий, делириозноаментивные состояния | « Оглушенность • Делирий ■ Критический сон « Астения (возможна энцефалопатия) |
| Сверхтяжелая | Делирий, сопор, кома | « Оглушенность « Делирий » Кома (при недостаточности лечения) • Астения (возможна энцефалопатия) |
Наиболее токсичным представителем группы является вещество BZ — производное хинуклединилбензилата, находившееся на снабжении армий некоторых государств в качестве ОВ несмертельного действия.
12.1.2.2.1. Вещество BZ
Физико-химические свойства. Токсичность
Это твердое кристаллическое, термостабильное вещество без цвета и запаха, устойчивое в водном растворе. Планируемый способ применения — аэрозоль (дым). Среднеэффективная токсодоза (ECt50) для человека составляет около 0,1 г-мин/м3; среднесмертельная токсодоза — ПО г - мин/м3. Возможно использование с диверсионными целями.
Токсикокинетика
В организм вещество проникает через легкие при ингаляции аэрозоля, либо через желудочно-кишечный тракт с зараженной водой и продовольствием. Через неповрежденную кожу в организм не проникает. При распределении в организме BZ легко преодолевает гематоэнцефаличе-ский барьер. Так, исследования, проведенные с использованием вешест
 |
ва, меченного радиоактивным изотопом, показали, что BZ быстро поступает в мозг и уже через 2,5 мин после внутривенного введения животным достигает максимальной концентрации в большинстве его структур. По уровню аккумуляции BZ структуры мозга располагаются в следующем порядке: полосатое тело > кора больших полушарий > гиппокамп > гипоталамус > мозжечок.
Проникший в мозг хинуклединилбензилат практически необратимо (по некоторым данным ковалентно) связывается с холинорецепторами, на много суток выводя их из строя. По-видимому, стабильность комплекса «вещество — рецептор» и определяет длительность психоза, развивающегося у пораженных.
Не связавшаяся часть токсиканта довольно быстро разрушается, в основном за счет гидролиза эфирной связи пиперидинового кольца с гликолиевой группой. В неизмененном виде с мочой выделяется менее 1% от введенного количества вещества.
Основные проявления интоксикации
В эксперименте на животных (крысы, собаки) при интоксикации BZ после непродолжительного латентного периода наблюдаются расстройства спонтанного поведения. Вначале извращаются движения животных (становятся замедленными, неуверенными). Затем нарастает оглушенность, снижаются или полностью исчезают реакции на внешние раздражители. На высоте интоксикации животные чаще лежат или бесцельно передвигаются по помещению, не способны преодолеть препятствия, встречающиеся на пути. Нарушения спонтанного поведения сохраняются на протяжении 6-8 ч. В последующем наблюдается слабость. Нарушение «выработанных» поведенческих навыков и срывы условнорефлектор-ной деятельности также характерны для интоксикации. Одновременно регистрируются и вегетативные нарушения. Они проявляются тахикардией, сухостью слизистых оболочек носа, мидриазом. Электрофизиологическими методами определяется медленно-волновая, высокоамплитудная биоэлектрическая активность головного мозга.
Картина отравлений BZ у людей развивается через 15-20 мин (до нескольких часов) после воздействия. Она сходна с клинической картиной отравления другими холинолитиками. Симптоматика включает вегетативные, соматические и психические расстройства.
При действии BZ в малых дозах превалирует вегетативная симптоматика. Одновременно наблюдаются легкая заторможенность, безразличное отношение к окружающему, замедление мышления. Особенно чувствительными к действию психотомиметика являются такие функции мозга, как запоминание и активное внимание, нарушение которых приводит к полной утрате психической работоспособности. Критическое отношение к своему состоянию при этом не страдает.
Вдыхание аэрозоля BZ в достаточно высоких концентрациях приводит к развитию интоксикации, которая, по данным ВОЗ, характеризуется следующей динамикой (табл. 56).
Характерным проявлением тяжелой интоксикации является психомоторное возбуждение. При этом состоянии пораженные мечутся, не реагируют на препятствия, проявляют агрессивность и сопротивление при попытках ограничения их активности.
Приведенную динамику отравлений BZ следует рассматривать только как схему, поскольку характер симптоматики определяется совокупностью ряда факторов, включающих, помимо дозы ОВ, индивидуальные особенности пораженного.
Помимо центральных эффектов, при отравлении BZ отмечаются периферические эффекты (соматические и вегетативные реакции). Важнейшими среди них являются нарушения сердечной деятельности (тахикардия) и гипертермия. В условиях повышенной температуры окружающего воздуха при тяжелой интоксикации BZ возможен смертельный исход.
Механизм токсического действия
Основа механизма токсического действия BZ — блокада мускарино-чувствительных холинергических структур в головном мозге и нарушение вследствие этого медиаторной функции ацетилхолина в синапсах ЦНС. BZ — мощный центральный холинолитик, прочно связывающийся с М-холинорецепторами мозга (константа связывания с мембранами си-наптосом, выделенных из ткани головного мозга крыс, кошек и обезьян, имеет величину порядка 2 • Ю-8 моль). Характер распределения BZ в ЦНС соответствует плотности М-холинорецепторов в структурах мозга: полосатое тело > кора больших полушарий > гиппокамп > гипоталамус > мозжечек. Известно, что ацетилхолину принадлежит важная роль в обеспечении равновесия процессов возбуждения и торможения в ЦНС, а холинергические механизмы лежат в основе многих форм поведения, включая обучение и память. В связи с этим понятно, почему блокада холинорецепторов центральной нервной системы приводит к нарушению психической деятельности человека.
Влияние психотомиметика на холинергическую передачу не ограничивается блокадой постсинаптических холинорецепторов. BZ действует и на пресинаптические рецепторы, активность которых контролирует выброс ацетилхолина нервными окончаниями и интенсивность его оборота (по механизму обратной связи: возбуждение рецепторов ацетилхолином угнетает его выброс и снижает скорость оборота). Кроме того, токсикант вызывает усиленное высвобождение ацетилхолина в синаптическую щель и избыточное его разрушение ацетилхолинэстеразой, а также угнетает активность холинацетилазы, тормозя синтез ацетилхолина. В итоге запасы ацетилхолина в центральной нервной системе существенно истощаются (в норме содержание АХ в ткани мозга: 10—30 нМ/г ткани; скорость оборота: 2-20 нМ/г мин).
Снижение содержания ацетилхолина имеет функциональное значение. Об этом свидетельствует наличие корреляции между изменениями уровня ацетилхолина в мозге и поведением животных, возникающими под влиянием BZ. Наряду с центральными, блокируются и периферические холинореактивные системы. Этим можно объяснить развитие вегетативных нарушений, наблюдаемых при отравлении BZ.
Поскольку в ЦНС существует тесное взаимодействие нейронов, передающих нервный импульс с помощью различных нейромедиаторов, помимо нарушений холинергических механизмов мозга при отравлении BZ, как и другими холинолитиками, отмечаются нарушения в системе норадренергической, дофаминергической, серотонинергической медиации.
Многие симптомы, характерные для отравления BZ (например, периодические вспышки психомоторного возбуждения), могут быть объяснены гиперактивностью адренергических медиаторных систем мозга. Нельзя исключить, что в больших дозах гликолаты могут тормозить синтез и обратный захват катехоламинов в синапсах мозга.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
» проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
» применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Специфическими противоядиями (функциональными антагонистами) при отравлении холинолитиками вообще, и BZ в частности, являются непрямые холиномиметики — обратимые ингибиторы холинэстеразы, способные проникать через гематоэнцефалический барьер, например: галантамин, эзерин, аминостигмин и т. д. (Г. И. Милыдтейн, Г. А. Софронов и др.). Механизмы антагонистических отношений между холинолитиками и ингибиторами холинэстеразы рассмотрены выше (см. 12.1.1.1.1.1. «Ингибиторы холинэстеразы»).
Недостатком обратимых ингибиторов как антидотов BZ является непродолжительность их действия. Вещества угнетают активность энзима всего на несколько часов, в то время как токсикант связывается с рецепторами синапсов очень прочно и надолго (до нескольких суток). В этой связи однократного введения антидотов бывает недостаточно — развиваются ремиссии интоксикации. При повторном введении обратимые ингибиторы становятся менее эффективными. Это дало повод рекомендовать для устранения психозов необратимые ингибиторы ХЭ (ДФФ, фосфорилтиохолины). Однако высокая токсичность и малая терапевтическая широта веществ препятствуют их применению в клинической практике.
Исходная доза и продолжительность введения обратимых ингибиторов ХЭ определяются степенью тяжести интоксикации. Препараты целесообразно назначать как можно раньше, желательно при появлении первых признаков интоксикации. Однако при этом важно установить, что нарушения психики обусловлены именно действием холинолитиков, а не психодислептиков с иным механизмом действия (например, ДЛК) или нейротоксикантов смертельного действия в малых дозах (ФОС, карбаматы, ГАМК-литики). Поскольку сделать это быстро практически невозможно, перед введением антидота следует понаблюдать за пострадавшим и убедиться, что в основе процесса лежит антихолинергическое действие (ориентируясь в основном на характер вегетативных нарушений и особенности нарушения психики).
При легкой степени поражения BZ для восстановления нормальной психической деятельности препараты вводят внутримышечно: аминостигмин — 2 мл 0,1% раствора; галантамин — 2 мл 0,5% раствора; эзерин — 2 мл 0,05%. Если лечебный эффект недостаточно полный, препараты следует вводить повторно через 30—60 мин до исчезновения симптомов отравления.
При средних и тяжелых формах отравления показано раннее многократное введение обратимых ингибиторов холинэстеразы дробными дозами. Так, аминостигмин в первые третьи сутки следует вводить 3—5 раз; галантамин вначале следует вводить внутримышечно или внутривенно в 1 % растворе по 2—3 мл. В последующем через каждые 30—40 мин по 1—2 мл 0,5% раствора до получения позитивного эффекта.
Поскольку помимо холинергических механизмов в действии BZ на мозг присутствуют и другие механизмы (в частности активация катехо-ламинергических механизмов), при тяжелых отравлениях устранить патологические эффекты с помощью только холиномиметиков не представляется возможным. Чрезвычайно сложным, но вместе с тем и ответственным мероприятием при интоксикации является борьба с психомоторным возбуждением. Из медикаментозных средств для этой цели прежде всего рекомендуют нейролептики, лишенные холинолитической активности, например трифтазин (0,2% — 1,0 мл).
Кроме нейролептиков для борьбы с психомоторным возбуждением могут быть использованы симптоматические средства: бензодиазепины (диазепам) и наркотические анальгетики (промедол: 2 мл 2% раствора внутримышечно).
Для устранения нарушений, обусловленных периферическим холино-литическим действием ОВ (тахикардия, сухость кожи, нарушение функции кишечника, задержка мочевыделения и др.), и усиления действия антидотов показано применение ингибиторов ХЭ, не проникающих через ГЭБ, например прозерина (в виде 0,05% раствора по 3—5 мл внутримышечно).
При выраженной тахикардии (порой угрожающей жизни) показаны препараты с р-адреноблокирующим действием, например анаприлин (пропранолол), который следует вводить внутримышечно в дозе 2 мл 0,25% раствора. Блокируя р-рецепторы синусного узла и обладая мембра-ностабилизирующим действием, эти препараты устраняют активирующее влияние на сердце симпатической иннервации и адреналина и нормализуют сердечный ритм.
После купирования (по возможности) проявлений острого психоза пораженные должны быть эвакуированы в специализированные медицинские учреждения и оставаться под наблюдением психиатра не менее недели. Длительность наблюдения определяют индивидуально в зависимости от тяжести перенесенной интоксикации.
12.1.2.2.2. Фенциклидин (сернил)
Это вещество впервые синтезировано в 50-е гг. XX в. как средство ДЛЯ наркоза (один из аналогов кетамина). В процессе испытаний была выявлена его высокая психодислептическая активность. В медицине в настоящее время не используется. В ветеринарии применяют как анестезирующее средство. Вещество изучалось военными ведомствами на предмет создания на его основе ОВ. Возможно использование в качестве диверсионного агента.
Физико-химические свойства. Токсичность
Бесцветное кристаллическое вещество, хорошо растворимое в воде. Эффективная доза — 0,02—1 мг/кг.
Токсикокинетика
Вещество всасывается в желудочно-кишечном тракте и быстро распределяется в органы, хорошо снабжаемые кровью. Обладая высокой ли-пофильностью, легко проникает в мозг. Затем происходит перераспределение токсиканта и накопление его в тканях с низкой интенсивностью гемоперфузии. Вещество метаболизируется в печени. Конечным продуктом метаболизма является пиперидин (вещество с запахом рыбы), выделяющийся, в том числе, и через легкие. Период полуэлиминации составляет около 11 ч. Частично выводится в неизмененном виде (до 9%) печенью и почками.
Основные проявления интоксикации
При приеме вещества в количестве 5 мг развивается состояние, напоминающее опьянение, появляются галлюцинации, нарушается чувство времени. Проявления интоксикации фенциклидином в зависимости от действующей дозы представлены в табл. 57.
Таблица 57
Проявления интоксикации фенциклидином в зависимости от дозы
| Доза, мг | Проявления интоксикации |
| 5-10 | Атаксия, нистагм, деперсонализация, нарушение чувства времени, ухудшение настроения, галлюцинации, перестезии, тошнота, рвота. Начало: 1-2 ч; продолжительность: 4-8 ч |
| 10-20 | Ступор, гиперрефлексия, гипертензия, стереотипии, нистагм, миоз. Начало: 0,5-1 ч; продолжительность: 8-24 ч |
| 50-100 | Нистагм, гипотензия, брадикардия, затруднение дыхания, судорожные приступы, кома. Продолжительность: до 4 сут, амнезия. |
| более 100 | Гипертермический криз, угнетение дыхания, смерть в течение 3-10 сут от остановки дыхания |
Характерными нарушениями, возникающими при легком отравлении сернилом, являются апатия, эмоциональное безразличие, утрата побуждения к действию, инициативы. Пораженный испытывает сонливость, появляются чувство нереальности окружающего и ощущение глубокого изменения собственной личности.
При более высоких дозах появляются кататонические расстройства (восковая ригидность мышц), расстройства мышления (нелогичность суждений, конфабуляции).
Психозы, развивающиеся при отравлении сернилом, характеризуются грубым расстройством «схемы тела», развитием делириозного состояния: зрительными и слуховыми галлюцинациями, бредом, агрессивным поведением, буйством.
Механизм токсического действия
В основе токсического действия фенциклидина лежит способность блокировать проведение нервных импульсов в глутаматергических синапсах центральной нервной системы. Глутамат — возбуждающий медиатор ЦНС. Выявлено несколько подтипов рецепторов к этому нейротран-смиттеру. Основными являются: каинатный (избирательный агонист — каиновая кислота), АМПА-рецептор (агонист — сх-амино-З-гидрокси-5-метил-4-изоксазол пропионовая кислота), НМДА-рецептор (агонист — N-MeTR/i-D-acnapraT). Фенциклидин — блокатор НМДА-рецепторов глу-тамата. Наибольшая плотность этих рецепторов в мозге выявляется в ядрах таламуса. Как известно, таламус — «релейная» структура, в которую стекается вся сенсорная информация, получаемая мозгом. Здесь она обрабатывается и передается в кору головного мозга. Фенциклидин, нарушая передачу нервных импульсов в глутаматергических синапсах таламуса, выступает в качестве разобщителя между структурами, передающими в ЦНС информацию, поступающую от проприоцепторов и органов чувств, и воспринимающими ее (кора мозга). За счет этого реализуется не только аналгезирующее действие вещества (аналог кетамина), но одновременно и его психодислептическое действие.
При действии больших доз токсиканта отмечаются нарушения со стороны и других нейромедиаторных систем (холинергической, дофаминер-гической, адренергической).
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности пораженного, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
В настоящее время медицина не располагает веществами, способными избирательно возбуждать НМДА-рецепторы и устранять эффекты токсиканта. С целью оказания неотложной помощи при интоксикациях, сопровождающихся психомоторным возбуждением, буйством, судорогами, целесообразно назначение диазепама (5—10 мг, внутривенно или внутримышечно). В эксперименте введение диазепама в дозе 0,2—0,3 мг/кг внутривенно за 5 мин до фенциклидина существенно снижает риск развития психоза. Назначение нейролептиков при отравлении фенцик-лидином противопоказано. В эксперименте на лабораторных животных аминазин усиливает проявления интоксикации веществом. Для оказания квалифицированной помощи необходимо эвакуировать пострадавшего в специализированное лечебное учреждение.
12.2. Вещества, вызывающие органические повреждения нервной системы
В основе токсического действия веществ рассматриваемой группы лежат нарушения пластического обмена в нервной системе, сопровождающиеся ее структурно-морфологическими изменениями. Механизмы действия токсикантов, благодаря которым они вызывают нарушения, многообразны и малоизученны. Проявления токсического процесса часто зависят не столько от механизма действия веществ, сколько от анатомического образования, на которое они подействовали, т. е. особенностей их токсикокинетики. Характерной особенностью поражения является медленное, постепенное развитие, часто прогрессирующее и после прекращения действия токсиканта. Следствием острой интоксикации чаще является длительно текущий, хронический патологический процесс, инвалидизация пораженных, а не их гибель в острой фазе интоксикации. Перечисленные особенности сближают вещества рассматриваемой группы с ОВТВ цитотоксического действия. Их отличительная особенность — чрезвычайно высокое сродство к нервной системе.
К числу веществ, вызывающих органические повреждения структур центрального и периферического отделов нервной системы, имеющих военно-медицинское значение, относятся некоторые металлы и метал-лорганические соединения (таллий, тетраэтилсвинец и др.).
12.2.1. Таллий
Физико-химические свойства. Токсичность
Таллий принадлежит к группе алюминия. Атомное число — 81, атомный вес — 204,4. Это кристаллический, бело-голубой металл. В своих соединениях встречается в одно- и трехвалентной форме. На воздухе окисляется, покрываясь пленкой коричневато-черного оксида. Таллий высокоактивный элемент, растворимый в кислотах. Известно, по крайней мере, 18 природных соединений таллия, среди которых оксид таллия (Т120з), ацетат таллия (CH3COOTI), карбонат таллия (ТЛ2СО3), хлорид таллия (Т1С1), йодид таллия (T1J), сульфат таллия (TI2SO4). Растворенные в воде соли образуют безвкусные, бесцветные, лишенные запаха растворы. Наиболее распространенное соединение — сульфат таллия.
Таллий — сильный токсикант, поражающий центральную и периферическую нервную систему, желудочно-кишечный тракт, почки, кожу и ее придатки. Он опасен при остром, подостром и хроническом воздействии. Производные одновалентного таллия более токсичны, чем трехвалентного. LD50 сульфата таллия для мышей составляет 35 мг/кг, хлорида таллия — 24 мг/кг. Не смертельные, но вызывающие тяжелые нарушения со стороны нервной системы дозы в десятки раз меньше. Токсичность металла для человека значительно выше, чем для грызунов.
Источники. Производство. Использование
Металл был открыт в 1861 г. Вильямом Крукесом. Его высокая токсичность была обнаружена уже в 1863 г.
Таллий добывают из металлсодержащих руд, а также в качестве побочного продукта при получении кадмия, свинца, цинка.
В развитых странах основные области потребления таллия — это производство электроники, фотоэлектрических элементов, ламп, сцин-тилляционных счетчиков. Таллий также применяют для изготовления оптических линз, красителей, как катализатор в химическом синтезе, в производстве искусственных ювелирных изделий.
В 1920 г. в Германии соли таллия начали применять в качестве пестицидов (инсектицидов и средств для борьбы с грызунами). Действующий агент содержал 2% сульфата таллия. Стойкость вещества в окружающей среде и кумуляция в организме млекопитающих сделали его идеальным родентицидом. Именно в качестве пестицида таллий стал причиной отравлений человека. В 1965 г. использование таллия в качестве пестицида в США было запрещено, однако в других странах мира он продолжает использоваться с этой целью.
В военной токсикологии таллий рассматривается как возможный диверсионный агент (3. Франке). Поражение наиболее вероятно при приеме воды й/или пищи, зараженной металлом.
Токсикокинетика
Острые отравления таллием, как правило, являются следствием случайного или преднамеренного приема больших доз солей металла per os. Возможны также ингаляционные поражения металлической пылью или парами металла, а также отравления при попадании его на кожу.
Всасывание вещества осуществляется всеми возможными путями: через кожу, слизистые оболочки желудочно-кишечного тракта и дыхательных путей — быстро (в течение 1 ч) и практически полностью (в опытах на грызунах — до 100% нанесенного вещества). Соединения таллия в руках неопытного человека представляют большую опасность как для него самого, так и для окружающих.
После проникновения в кровь элемент быстро распространяется в организме. Наибольшее количество концентрируется в почках. Высокое содержание определяется также в слюнных железах, сердечной мышце, печени. Концентрация в жировой ткани и мозге относительно невелика.
Основные пути выделения — через почки и желудочно-кишечный тракт. Слюнными железами таллия выделяется в 15 раз больше, чем почками. Однако выделившееся со слюной вещество опять поступает в кишечник, где вновь всасывается. Период полувыведения из организма человека — около 30 сут. Даже в тех случаях, когда в моче и фекалиях обнаруживается достаточно высокое содержание металла, концентрация его в плазме крови относительно невысока.
Основные проявления интоксикации
Основные проявления интоксикации таллием представлены в табл. 58.
Таблица 58
Основные проявления интоксикации таллием
| Острое отравление | Тошнота, рвота, боли в животе, желудочно-кишечные кровотечения, тремор, атаксия, нейропатия черепномозговых нервов (птоз, офтальмоплегия, неврит лицевого нерва и др.), психоз, судороги, кома, параличи, мышечная атрофия |
| Подострое отравление | Утомляемость, эмоциональные нарушения, атаксия, дистальная парастезия, дистальная мышечная слабость, восходящая нейропатия, полиневрит, психозы, дерматит (эритема, изменение ногтей, шелушение кожи), запоры |
При однократном приеме даже высоких доз токсиканта клиническая картина отравления развивается после продолжительного скрытого периода (до 12—14 ч и более). При пероральной интоксикации первыми симптомами являются тошнота, рвота, общая слабость, бессонница, усиленное слюноотделение. Затем, в течение последующих 2—14 дней появляются боли в животе, запоры, ощущение тяжести в желудке. Другие клинические проявления интоксикации таллием развиваются также медленно, в течение нескольких недель. Одним из ранних признаков отравления таллием является симптом Види: черное веретенообразное утолще-
ние длиной 1 мм в прикорневой части растущего волоса. Поражения кожи проявляются эритемой, ангидрозом, симптомами себореи, потерей волосяного покрова, шелушением кожных покровов, нарушением нормального роста ногтей.
Неврологические симптомы характеризуются невритами, преимущественно нижних конечностей. Появляются характерные сенсорные нарушения в виде парестезии, онемения конечностей, болезненности по ходу нервных стволов. Чем тяжелее интоксикация, тем быстрее формируются и в большей степени выражены проявления. Через 1—3 нед развиваются атаксия, тремор конечностей, болезненность по ходу нервов усиливается. Мышечные рефлексы сохраняются обычно достаточно долго. В процесс вовлекаются краниальные нервы (нистагм, скотома, офтальмоплегия). Поражение блуждающего нерва сопровождается тахикардией, умеренной гипертензией, парезом кишечника. Психические расстройства проявляются депрессией и психозом. Выздоровление происходит медленно и растягивается на месяцы.
При тяжелых смертельных интоксикациях после скрытого периода появляются рвота, кровавый понос, беспокойство, чувство тревоги, делирий, галлюцинации, судороги, кома. Смерть развивается в течение нескольких суток в результате угнетения сердечной деятельности, шока, нарушения функций почек. При вскрытии обнаруживаются: воспаление слизистой оболочки кишечника, жировая дегенерация печени и почек, отек и кровоизлияния в миокарде и мозге.
Механизм токсического действия
В основе токсического действия таллия лежит его способность повреждать клеточные структуры, в которых он накапливается (цитоток-сичность). Механизм повреждающего действия изучен недостаточно. Как и другие металлы, вещество может вступать во взаимодействие с многочисленными эндогенными лигандами, нарушая свойства биомолекул. Некоторое значение имеет образование химических связей с низкомолекулярными веществами, например цистеином. За счет этого взаимодействия таллий накапливается в клетках кожи, ее придатках и вызывает их поражение. Однако можно предположить, что основными молекулами-мишенями являются структурные белки, каталитические центры ферментов, транспортные системы биомембран.
Действие таллия на белки может приводить к перераспределению зарядов внутри макромолекул и в результате изменению их третичной структуры и биологической активности. Таллий взаимодействует с митохондриями, эндоплазматическим ретикулумом, лизосомами, вызывая их повреждение. Первой взаимодействует с металлом внешняя поверхность клеточной мембраны, поэтому прежде всего именно здесь образуются прочные связи металла с лигандами. Нарушаются механизмы трансмембранного движения ионов и других биологически активных веществ.
Токсическое действие таллия на нервные клетки и миоциты, как полагают, во многом обусловлено его конкуренцией с ионом калия. Токсикант накапливается преимущественно внутриклеточно, замещает К+ в биосредах. Показано, что таллий является конкурентом калия за трансмембранный перенос ионов (блокатор «Na-K-АТФ-азного насоса»). Как известно, калий участвует в формировании потенциала покоя возбудимых мембран и ответственен за восстановление потенциала биомембраны после ее деполяризации, лежащей в основе формирования потенциала действия (см. выше). Замещение калия таллием в возбудимых клетках приводит к тому, что процесс реполяризации клеточных мембран после формирования потенциала действия (и приведение системы в «исходное» состояние) замедляется. Клетки становятся более чувствительными к возбуждающему сигналу.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• проведение экспертизы воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим.
Средства медицинской защиты
При пероральном отравлении рекомендуют промыть желудок 1% раствором йодистого натрия или 3% раствором натрия тиосульфата.
В настоящее время специальные средства медицинской защиты отсутствуют. Они могут быть разработаны на основе препаратов, ускоряющих выведение таллия из организма. В опытах на животных известной активностью обладали комплексообразователи диэтилдитиокарбамат (ди-тиокарб: 30 мг/кг в сутки, через рот) и дифенилтиокарбазон (дитизон: 20 мг/кг в сутки, через рот). Однако, по данным некоторых авторов, введение этих препаратов при тяжелой острой интоксикации приводит к перераспределению таллия в организме с усилением комы. По-видимому, дитиокарб образует с токсикантом липофильный комплекс, облегчающий поступление металла в ЦНС.
Хотя калий и таллий — конкуренты за механизм активного транспорта через клеточные мембраны и калий в высоких дозах вытесняет таллий из связи с внутриклеточными рецепторами, назначение только препаратов калия в ряде случаев приводит к усилению симптомов интоксикации в результате нежелательного перераспределения металла внутри организма. Поэтому в некоторых исследованиях рекомендуют применение хлористого калия в сочетании с активированным углем. При использовании этого комплекса средств схема оказания помощи следующая: КС1 —
ЗЗО
20 миллиэквивалента 4 раза в сутки; активированный уголь — 20-30 г 4 раза в сутки. Оба препарата — per os (терапия продолжается в течение нескольких недель, а иногда и месяцев).
Имеются указания на эффективность использования при острой интоксикации таллием прусского голубого (ферроцианоферрат калия). Препарат назначают per os в дозе 250 мг/кг в сутки в 50 мл 15% маннитола в два приема (до 10 г два раза в день). Прусский голубой не всасывается в желудочно-кишечном тракте. Ион калия, образующийся при диссоциации вещества в кишечнике, всасывается во внутренние среды организма и вытесняет таллий, который, выделяясь в просвет кишечника, связывается с ионом ферроцианоферрата и выводится из организма.
Есть сообщения об эффективности бензодиазепинов при судорогах и возбуждении, вызванных таллием. Однако эти препараты, хотя и облегчают оказание помощи пораженным, не сказываются на общем течении токсического процесса.
12.2.2. Тетраэтилсвинец (ТЭС)
С 1923 г. ТЭС применяют в качестве антидетонатора. В чистом виде вещество не используется, а идет на приготовление этиловой жидкости, которую добавляют к различным сортам бензина с целью улучшения их эксплуатационных свойств. За последние десятилетия производство вещества непрерывно возрастает. Большая часть расходуемого во всем мире горючего этилирована тетраэтилсвинцом.
ТЭС обладает высокой токсичностью и поэтому до начала Второй мировой войны рассматривался как возможное ОВ. По программе англоамериканских военно-химических исследований токсикология свинец-органических соединений была изучена систематически. В настоящее время военное применение ТЭС отрицают. Однако вещество следует рассматривать как чрезвычайно опасный промышленный агент, могущий при авариях и катастрофах стать причиной формирования зон химического заражения и очагов поражения людей.
Физико-химические свойства. Токсичность
Тетраэтилсвинец (ТЭС) — РЬ(С2Н5)4 — металлорганическое соединение, в котором атом свинца ковалентно связан с четырьмя этильными радикалами. Это маслянистая жидкость, практически не растворимая в воде, но хорошо растворяющаяся в жирах и органических растворителях, легко проникает через одежду, обувь, сорбируется штукатуркой, бетоном, древесиной. Не замерзает при температурах до -130° С. ТЭС летуч, и при 20° С насыщенный его парами воздух содержит свыше 5 г/м3 вещества. Пары в 11,2 раза тяжелее воздуха. В малых концентрациях имеет ароматический, сладковатый запах; в высоких — резкий, неприятный. Образует зоны стойкого химического заражения. Дегазация ТЭС, в результате которой он превращается в неорганические соединения, возможна при обработке поверхностей растворами хлористого водорода в дихлорэтане. Лабораторную посуду рекомендуют дегазировать бромной водой или растворами хлорной извести. Среднесмертельная концентрация для крыс при внутрибрюшинном способе введения составляет около 10 мг/кг массы. Несмертельные поражения, сопровождающиеся тяжелыми и стойкими нарушениями функций нервной системы, развиваются при действии вещества в значительно меньших дозах. Люди более чувствительны к действию токсиканта, чем экспериментальные животные. Отравления людей наблюдались при ингаляции паров ТЭС в концентрации около 0,0015 г/м3.
Токсикокинетика
В виде пара вещество может проникать в организм ингаляционно и через неповрежденную кожу; в жидком виде — через кожу; через рот — с продовольствием, контаминированным токсикантом. В течение 3—4 сут ТЭС в неизмененном виде обнаруживается в крови и тканях. Легко проникает через гематоэнцефалический барьер в мозг. Постепенно в результате метаболизма в печени и других органах ТЭС превращается в три-этилсвинец, с образованием которого и связывают развитие патологии. Триэтилсвинец длительно (до 20 сут) определяется в крови, постепенно локализуясь в печени и ЦНС. Наибольшее количество вещества депонируется в таламусе, гипоталамусе, стриатуме, фронтальных отделах коры больших полушарий мозга — структурах, плотно иннервируемых дофа-минергическими нервными окончаниями. В дальнейшем вещество разрушается до неорганического свинца, который частично откладывается в тканях, а частично выводится с мочой и калом.
Основные проявления интоксикации
Вещество не оказывает местного действия ни на кожные покровы, ни на слизистые оболочки глаз, органов дыхания или желудочно-кишечного тракта. Симптомы резорбтивного действия вещества появляются после скрытого периода, продолжающегося от 10 ч до 10 сут (чаще до 2 сут). В основе острого токсического процесса лежат нарушения функций ЦНС, главным проявлением которых является острый интоксикационный психоз.
Различают молниеносную (развивается при действии чрезвычайно высоких доз ТЭС) и затяжную формы острого отравления. Весь период развития тяжелой интоксикации разделяют на скрытый период, начальный период, период разгара заболевания, период выздоровления (Е. В. Ермаков, 1963).
В начальном периоде пострадавшие предъявляют жалобы на слабость, быструю утомляемость, головную боль, потерю аппетита, усиленное слюнотечение, расстройства сна (бессонница, кошмарные сновидения). Позже присоединяются артралгии, миалгии, боли в области груди и живота. Характерны вегетативные нарушения, такие как повышенная саливация, потливость и т. д. Ранними объективными признаками отравления являются гипотония (АД до 80/40 мм рт. ст.), брадикардия (до 40 уд/мин) и гипотермия (до 35° С). В ряде случаев эти нарушения могут длительно сохраняться (недели) и быть единственными признаками поражения. При более тяжелых вариантах течения у отравленных обнаруживаются признаки органического поражения центральной нервной системы: атаксия, тремор, амимия, оглушенность или эйфория, нарушение памяти, тактильные иллюзии (ощущение инородного тела во рту). При легких отравлениях процесс более не прогрессирует, но период выздоровления продолжается 2—4 нед.
Период разгара характеризуется клинической картиной острых нервно-психических нарушений. Формируется делириозный симптомо-комплекс: устрашающие зрительные (реже тактильные, обонятельные, слуховые) галлюцинации, бред преследования, физического воздействия, психомоторное возбуждение, нарушение ориентации в окружающей обстановке. Температура тела резко повышается (до 40° С). Усиливаются признаки органического поражения мозга: отмечается атаксия, дизартрия, нарушение координации движений, птоз, парез лицевого нерва, патологические рефлексы, появляются приступы беспорядочных сокращений различных групп мышц или мышц всего тела. При крайне тяжелых отравлениях ТЭС психомоторное возбуждение может смениться депрессией, адинамией, гипотонией (пульс становится учащенным, нитевидным). Нарушается дыхание, развивается цианоз, иногда формируется отек легких (признак острой сердечной недостаточности). На этом фоне пострадавшие нередко погибают. Со стороны других внутренних органов особых изменений обычно не наблюдается (кроме незначительного увеличения печени).
Если не наступил летальный исход, болезнь переходит в период выздоровления, который продолжается в течение двух и более месяцев. У больных нарушена память, отмечаются утомляемость, вялость, заторможенность (признаки кататонии), кошмарные сновидения, галлюцинации. Хотя возможны и благоприятные исходы, часто случаи отравления заканчиваются стойкими нарушениями психики.
Механизм токсического действия
ТЭС обладает прямым цитотоксическим действием на нервные клетки, вызывая их повреждение вплоть до некробиоза и некроза. В большей степени повреждаются структуры мозга, в которых вещество преимущественно накапливается (см. выше). Гибель нервных клеток лежит в основе органического синдрома поражения мозга. Механизм цитотоксично-сти ТЭС до конца не выяснен. Полагают, что в основе процесса лежит нарушение пластического обмена в клетках, обусловленное ковалентным связыванием свинца с биомолекулами, в состав которых входят амино-, карбокси-, имидазол-, фосфатные и SH-группы. Результатом такого взаимодействия является денатурация молекул, нарушение их свойств и функций. Свинец, высвободившийся в нервных клетках, в результате метаболических превращений, из связи с алкильными радикалами, конкурирует здесь с двухвалентными металлами, такими как Са2+ и Zn2+. В итоге угнетается активность большого числа ион-зависимых энзимов (аденилатциклазы, Na-K-АТФазы и т. д.), нарушается синтез белка в клетках, повреждаются процессы, проходящие в митохондриях (угнетение окисления жирных кислот, декарбоксилирования пировиноградной кислоты, снижаются запасы макроэргов) и т. д.
Существенно страдает обмен дофамина в ЦНС, свидетельством чего является увеличение потребления тирозина тканями мозга; усиливается выброс дофамина окончаниями дофаминергических нейронов в стриа-туме, гипоталамусе, лобных отделах коры мозга; нарушается обратный захват нейромедиатора соответствующими нейронами клеток. Одновременно повышается тонус холинергических структур: уровень ацетилхолина в ткани мозга возрастает, активность холинэстеразы снижается. Повреждение дофаминергических и холинергических систем мозга обусловлено тесным структурно-функциональным взаимодействием этих двух нейромедиаторных систем ЦНС.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
• использование индивидуальных технических средств защиты (средства защиты кожи; средства защиты органов дыхания) в зоне химического заражения;
• участие медицинской службы в проведении химической разведки в районе расположения войск, экспертиза воды и продовольствия на зараженность ОВТВ;
• запрет на использование воды и продовольствия из непроверенных источников;
• обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
• проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
• своевременное выявление пораженных;
• применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само- и взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим;
• подготовка и проведение эвакуации.
Медицинские средства защиты
Для целей медицинской защиты необходимо использовать средства, препятствующие всасыванию вещества во внутренние среды организма, и симптоматические средства, облегчающие течение токсического процесса. Специфические противоядия ТЭС не разработаны.
Для частичной санитарной обработки открытых участков кожи, зараженной ТЭС, в зависимости от условий можно использовать: ИПП, бензин и керосин с последующим обмыванием кожи теплой водой с мылом, 10—15% раствор дихлорамина или монохлорамина в 70° спирте. Для про-
мывания глаз рекомендуют 0,25—0,5% водный раствор монохлорамина. С целью предотвращения всасывания яда в желудочно-кишечном тракте вызывают рвоту, назначают активированный уголь, проводят зондовое промывание желудка.
Медикаментозные средства. Хотя в моче отравленных в течение длительного времени в малых количествах определяется свинец, назначение комплексообразователей (унитиол, пентацин и т. д.) неэффективно. Тем более неэффективно назначение этих средств на догоспитальном этапе, поскольку действующим фактором, инициирующим развитие токсического процесса, являются органические соединения свинца (тетраэтил-свинец, триэтилсвинец), не связывающиеся комплексонами.
При появлении признаков психомоторного возбуждения (на догоспитальном этапе) назначают седативные средства: барбитураты, бензодиа-зепины, нейролептики, 25% раствор сернокислой магнезии (по 3—5 мл внутривенно). Облегчая течение интоксикации, эти средства тем не менее не устраняют проявлений токсического процесса, обусловленных органическим повреждением нервной ткани. Применение наркотических анальгетиков противопоказано!
Часть II РАДИОБИОЛОГИЯ
... ,. м>.:.:'- :ш V.
Раздел III. ОБЩАП РАДИОБИОЛОГИЯ
| Вся биота на Земле, включая человека, постоянно находится в сфере воздействия естественного и техногенного радиационного фона. Постоянно возрастающее число людей подвергается облучению в процессе профессиональной деятельности, при применении радиоактивных источников в промышленном производстве и научных исследованиях. В онкологической практике все шире используется способность радиации убивать живые клетки, причем наряду со злокачественно перерожденными клетками неизбежно повреждаются и здоровые. Реально имели место радиационные аварии, при которых персонал аварийных установок получал высокие, порой смертельные дозы облучения, а обширные территории подвергались загрязнению радиоактивными продуктами в опасных для здоровья человека количествах. Еще более опасны по сравнению с техногенными воздействиями и авариями последствия применения ядерного оружия. Энергия ионизирующих излучений превосходит значения энергий химических и физико-химических связей между атомами и молекулами. Поэтому воздействие ионизирующей радиации не может не сказаться на процессах, происходящих в облучаемых структурах. Значимость радиационного фактора для всего живого и неживого и, прежде всего, для здоровья человека определяет необходимость четких представлений о всех сторонах и последствиях воздействия ионизирующих излучений. Предмет радиобиологии составляют многообразные проявления действия излучений на всех уровнях организации живого — от молекулярного до орга-низменного, а часто и популяционного, механизмы возникновения этих проявлений, влияние на развитие конкретных биологических эффектов условий воздействия радиации (вида излучения, его дозы, мощности дозы, ее распределения в пространстве, продолжительности облучения), модифицирующие воздействия на эффекты облучения факторов нерадиационной природы. В исследованиях радиобиологических процессов удается проводить тщательный количественный анализ полученных материалов. Существующая в дополнение к этому возможность воздействовать излучением как на все органы и ткани, так и на точно ограниченный участок определяет высокую надежность и информативность сведений, получаемых с помощью радиобиологических методик. |
Глава 13. ПРЕДМЕТ, ЦЕЛЬ И ЗАДАЧИ РАДИОБИОЛОГИИ
На грани со смежными науками сформировались радиационная биохимия, радиационная иммунология, радиационная гематология, радиационная генетика, радиационная цитология и др. Значение радиобиологической составляющей в этих направлениях не исчерпывается потребностями решения частных задач определения влияния излучений на соответствующие системы или процессы. Эффекты, наблюдающиеся после воздействия излучений, позволяют понять механизмы функционирования этих систем и сущность этих процессов/Многие достижения последних десятилетий в биохимии, молекулярной биологии, иммунологии, генетике, геронтологии, вообще в медицине стали возможны лишь благодаря тесным связям этих наук с радиобиологией. Это — и открытие механизмов ферментативной репарации ДНК, и выяснение и конкретизация наиболее ранних этапов развития кроветворных клеток, и раскрытие сложных межклеточных кооперативных взаимодействий в иммунном ответе, и изучение процессов физиологической регенерации, и исследования многих других фундаментальных научных явлений.
Целью радиобиологических исследований являются познание закономерностей биологического действия ионизирующих излучений и обоснование таких важных прикладных аспектов, как:
• прогнозирование последствий радиационных воздействий;
• нормирование радиационных воздействий при работе с источниками ионизирующих излучений;
• разработка режимов поведения и защитных мероприятий при вынужденном пребывании в зонах воздействия ионизирующих излучений;
• разработка средств и методов профилактики радиационных поражений, диагностики и прогнозирования тяжести поражений, обоснование проведения при них неотложных мероприятий первой помощи и последующего лечения;
• разработка наиболее рациональных режимов терапевтического облучения и др.
Фундаментальные положения радиобиологии являются результатом анализа тщательно проведенных на четкой количественной основе экспериментальных исследований и клинических наблюдений.
В альянсе радиобиологии с другими дисциплинами оформились отдельные самостоятельные направления, такие, как радиационная гигиена и радиационная экология, радиобиология опухолей, космическая радиобиология и др. Одно из таких направлений — военная радиобиология. Таким образом, сегодня радиобиологию справедливо относят к числу фундаментальных наук, и изучение ее полезно не только для ориентировки в проблемах медицинской противорадиационной защиты.
Глава 14. ВИДЫ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ И ИХ СВОЙСТВА
Ионизирующие излучения (ИИ) получили свое название по свойству, отличающему их от большинства остальных излучений — способности вызывать ионизацию атомов и молекул в облучаемом веществе. Все ИИ подразделяются на электромагнитные и корпускулярные.
14.1. Электромагнитные ионизирующие излучения
В зависимости от источника электромагнитные ИИ подразделяются на тормозное, характеристическое и у-излучение. Тормозное излучение возникает при замедлении в электрическом поле (например, окружающем атомные ядра) ускоренных заряженных частиц. Характеристическое излучение обусловлено энергетическими перестройками внутренних электронных оболочек возбужденных атомов, а у-излучение является продуктом ядерных превращений радиоактивных элементов (радиоизотопов).
Совокупность тормозного и характеристического излучений называют рентгеновским излучением (в англоязычной литературе чаще употребляют термин «Х-излучение»). В земных условиях оно всегда имеет искусственное происхождение, в то время как у-излучение может иметь как искусственное, так и естественное происхождение.
Наиболее важные свойства электромагнитных ИИ стали известны человечеству уже через 50 сут после их обнаружения В. К. Рентгеном. 28 декабря 1895 г. он вручил председателю вюрцбургского физико-медицинского общества тезисы, содержащие характеристику Х-излучения, актуальную и в наши дни. Эта характеристика справедлива и для других электромагнитных ИИ; основные ее положения приведены в табл. 59.
Таблица 60
 |  | ||
Несмотря на значительные различия свойств рентгеновского излучения и видимого света, немецкому физику Максу Лауэ в 1912 г. удалось выяснить, что они тождественны по своей природе, различаясь лишь длиною волн. Самые длинные из волн рентгеновского излучения на порядок короче, чем волны видимого света, что объясняет их разное поведение на зеркальных поверхностях, в линзах и на дифракционных решетках. С этим же связано и наличие у рентгеновских и у-лучей ионизирующих свойств.
Действительно, энергия фотона (Е) прямо пропорциональна частоте электромагнитных колебаний (v) и обратно пропорциональна длине их волны (X):
Е = hv = hc/X,
где h — постоянная Планка, с — скорость света.
В электрон-вольтах эту энергию можно рассчитать по формуле:
Е = 12 400/Х,
где величина X выражена в нм.
Поскольку минимальная энергия ионизации атома в веществе равна 34 эВ, легко определить, какие из электромагнитных излучений обладают ионизирующими свойствами: это те из них, длина волны которых меньше 365 нм. Несмотря на то, что энергия некоторых квантов ультрафиолетового излучения достаточна для ионизации вещества, термин «ионизирующие» закрепился лишь за первыми двумя из представленных в табл. 60 излучений.
Как будет показано далее, ионизация веществ лежит в основе биологической активности ИИ. Этот же феномен используется для их выявления и количественной оценки (дозиметрии).
Взаимодействие электромагнитного ИИ с атомами вещества может протекать в формах фотоэффекта, комптон-эффекта и образования элек-трон-позитронных пар.
Фотоэффект — поглощение одной из внешних электронных оболочек атома всей энергии фотона с превращением ее в кинетическую энергию «выбитого» из атома электрона. Этот эффект преобладает при энергии фотонов до 0,05 МэВ.
Комптон-эффект — передача электрону лищь части энергии фотона; остальная энергия передается вторичному («рассеянному») фотону, который взаимодействует с атомами по механизму фотоэффекта или комптон-эффекта. При энергиях квантов от 0,1 до 2,0 МэВ (например, в случае проникающей радиации ядерного взрыва) на долю комптон-эффекта приходится до 99—100% поглощенной веществом энергии у-излучения.
Образование электрон-позитронных пар при прохождении у-кванта в непосредственной близости от ядра атома — это основной вид взаимодействия фотонов с веществом при их энергии более 50 МэВ, его удается наблюдать лищь в лабораторных условиях.
Образующиеся при поглощении квантов электромагнитного излучения ускоренные заряженные частицы (фотоэлектроны, комптоновские электроны) являются вторичным, но первостепенным по значимости фактором ионизации и возбуждения атомов в облучаемом веществе. Поэтому рентгеновы и у-лучи называют косвенно ионизирующими излучениями.
Энергия фотонов определяет не только их ионизирующую, но и проникающую способность. Высокоэнергетические («жесткие» — по определению В. К. Рентгена) электромагнитные излучения легко проникают вглубь тела человека и животных, вызывая ионизацию во всех клетках организма. Напротив, «мягкие» рентгеновы лучи, которые получают при напряжении на аноде рентгеновской трубки величиной в несколько кВ, задерживаются в основном кожей, не оказывая существенного прямого действия на глубоко лежащие ткани.
При прохождении электромагнитных ИИ через вещество интенсивность их потока уменьшается в соответствии с уравнением:
где I — интенсивность прошедшего сквозь экран потока излучения; 10 — интенсивность пвдающего потока излучения; е — основание натурального логарифма;
ц — коэффициент ослабления, величина которого зависит от энергетического
спектра ИИ и свойств вещества; х — толщина экрана.
Практически удобным показателем экранирующей способности материалов является толщина их слоя, при которой излучение ослабляется вдвое (слой половинного ослабления). Эта величина связана с коэффициентом ослабления ИИ зависимостью:
d0,5 = 0,693/ц.
Коэффициент ослабления электромагнитных ИИ растет с увеличением порядкового номера в таблице Менделеева, а значит, и атомной массы входящих в вещество элементов. Поэтому наиболее эффективно экранируют от электромагнитных ИИ вещества, содержащие тяжелые металлы («защита экранированием»). Свинец и барий вводят в состав материалов, используемых при сооружении помещений для лучевой диагностики и терапии. «Защита экранированием» дополняется «защитой расстоянием», основанной на зависимости интенсивности потока ИИ от расстояния до его источника, и «защитой временем» — минимизацией времени воздействия ИИ на персонал.
14.2. Корпускулярные ионизирующие излучения
К корпускулярным ИИ относят нейтроны и ускоренные заряженные частицы.
Нейтронное излучение возникает при бомбардировке атомного ядра ускоренной заряженной частицей или фотоном высокой энергии. Помимо лабораторных условий, такой путь реализуется при взрывах атомных боеприпасов, где источником этих частиц служат цепные реакции деления ядер 235U или 239Ри. Другой путь образования нейтронов -- синтез ядер легких элементов — дейтерия (jD2), трития ОТ3) и лития (3U6), происходящий при взрывах термоядерных (водородных) боеприпасов.
Нейтроны могут быть классифицированы по их энергии (табл. 61).
Таблица 61
Классификация нейтронов в зависимости от энергии
| Название | Энергия частицы |
| Тепловые | <0,1 эВ |
| Медленные | 0,1-500,0 эВ |
| Промежуточные | 0,5-100,0 кэВ |
| Быстрые | 0,1-10,0 МэВ |
| Очень больших энергий | 10-1000 МэВ |
| Сверхбыстрые (релятивистские) | >1000 МэВ |
Большинство нейтронов, образующихся при взрывах атомных боеприпасов, относится к быстрым нейтронам, а при взрывах водородных боеприпасов — к нейтронам очень больших энергий.
Так как нейтроны не имеют заряда, они не оказывают непосредственного влияния на электронную оболочку атомов, взаимодействуя только с ядрами. Сталкиваясь с ядрами, нейтроны либо отталкиваются от них (рассеяние), либо поглощаются ими (участие в ядерных перестройках). Ниже раскрывается содержание процессов взаимодействия нейтронов с атомами вещества.
Упругое рассеяние. При столкновении с ядрами углерода, азота, кислорода, фосфора нейтроны теряют 10—15% , а при столкновении с ядрами водорода — до 2/3 своей энергии. Потерянная нейтронами энергия передается «ядрам отдачи» — положительно заряженным частицам, имеющим высокую ионизирующую способность. Упругое рассеяние — основной путь потери энергии нейтронами, возникающими при атомных и водородных взрывах.
Неупругое рассеяние. В этом случае часть энергии расходуется нейтронами на возбуждение (разновидность колебательного движения) ядер-мишеней. В исходное состояние ядра возвращаются испуская фотоны у-излучения.
Ядерные перестройки. При поглощении ядрами нейтронов происходит выброс протонов, а-частиц, у-квантов, возникают искусственные радиоактивные изотопы (это явление называется наведенной активностью).
Образующиеся при взаимодействии нейтронов с веществом ускоренные заряженные частицы — ядра отдачи — вносят основной вклад в ионизацию и возбуждение атомов вещества. Поэтому нейтроны, так же как рентгеновы и у-лучи, называют косвенно ионизирующим излучением.
Проникающая способность нейтронов несколько меньше, чем у у-из-лучения, но существенно больше, чем у ускоренных заряженных частиц. При ядерных и водородных взрывах нейтронный поток распространяется на сотни метров, легко проникая сквозь стальную броню и железобетон. Энергия нейтронов наиболее эффективно передается ядрам легких атомов. Поэтому вещества, богатые атомами водорода, бериллия, углерода, находят применение в экранировании от нейтронного излучения. Тяже-
лые металлы, плохо задерживающие нейтроны, могут применяться для ослабления вторичного у-излучения, возникающего в легких материалах в результате неупругого рассеяния нейтронов и ядерных перестроек.
Ускоренные заряженные частицы — это перемещающиеся в пространстве источники электрического поля (поток электронов — р-частиц, протонов, ядер атома гелия — а-частиц). Естественными источниками ускоренных заряженных частиц являются некоторые из природных радиоизотопов. К искусственным источникам относятся искусственные радиоизотопы и ускорители заряженных частиц.
При прохождении через вещество заряженные частицы могут взаимодействовать с его атомами. Ниже раскрываются формы этого взаимодействия.
Упругое рассеяние — изменение траектории заряженной частицы в результате отталкивания от атомных ядер без потери энергии. Чем меньше масса частицы, тем больше ее отклонение от прямого направления. Поэтому траектории р-частиц в веществе изломаны, а протонов и а-частиц — практически прямые.
Неупругое торможение. Электрон при прохождении вблизи атомного ядра теряет скорость и энергию. При этом может испускаться фотон тормозного излучения, летящий в том же направлении, что и электрон.
Ионизация и возбуждение атомов в результате взаимодействия частицы с их электронными оболочками — основной путь потери энергии ускоренных заряженных частиц в веществе. Под действием их электрического поля происходит возмущение электронных оболочек атомов с переходом последних в возбужденное или ионизированное состояние. Способность ускоренных заряженных частиц непосредственно взаимодействовать с электронными оболочками атомов позволила определить их как первично ионизирующие излучения.
Проникающая способность ускоренных заряженных частиц, как правило, невелика. Она прямо пропорциональна энергии, массе и квадрату скорости частицы. Напротив, связь проникающей способности с абсолютной величиной заряда частиц является отрицательной. Пробег р-частиц в воздухе составляет десятки сантиметров, а а-частиц — миллиметры. Одежда надежно защищает человека от воздействия этих излучений извне. Однако поступление их источников внутрь организма является опасным, поскольку пробег а- или р-частиц в тканях превышает размеры клеток, что создает условия для воздействия излучения на чувствительные к нему субклеточные структуры.
W.3. Плотноионизирующие
и редкоионизирующие излучения
Первичные изменения атомов и молекул сводятся к ионизации или возбуждению и качественно не зависят от вида действующего на них ИИ. Однако при одном и том же количестве энергии, поглощенной единицею массы вещества, микропространственное распределение этой энергии в облученном объеме различно. Это различие определяется линейной передачей энергии (ЛПЭ) — количеством энергии, передаваемой частицей веществу в среднем на единицу длины пройденного в нем пути:
ЛПЭ = ДЕ/Дх,
где Е — энергия частицы (эВ); х — путь частицы (мкм).
ЛПЭ зависит от вида ИИ и плотности вещества. Значения этого показателя, приводимые в справочных таблицах, обычно соответствуют величине ЛПЭ конкретного ИИ в воде. ЛПЭ электромагнитных ИИ и нейтронов определяется величиной ЛПЭ первичных ионизирующих факторов (электронов и ядер отдачи, соответственно).
Зная величину ЛПЭ, можно определить среднее число ионов, образующихся на единицу длины пути частицы ИИ. Для этого надо разделить величину ЛПЭ на величину энергии, необходимой для образования одной пары ионов (как отмечалось, эта величина составляет 34 эВ). Количество пар ионов, образующихся в среднем на 1 мкм пути частицы ИИ в веществе, называется линейной плотностью ионизации (ЛПИ).
В зависимости от величины ЛПЭ все ионизирующие излучения делят на редко- и плотноионизирующие (табл. 62).
Таблица 62
Редкоионизирующие и плотноионизирующие излучения
| Критерий | Ионизирующие излучения | |
| редкоионизирующие | плотноионизирующие | |
| Величина ЛПЭ, КэВ/мкм | Менее 10 | Более 10 |
| Название ИИ | Все электромагнитные ИИ; | Протоны, другие ядра отдачи; |
| Р-излучение | а-частицы; | |
| нейтроны |
Редкоионизирующие излучения отличаются сравнительно высокой проникающей способностью, и в силу этого их энергия распределяется в объеме облучаемых тел более равномерно, чем в случае воздействия плот-ноионизирующих ИИ. Для микроскопических тел (по размерам сопоставимых с клетками) эта разница несущественна и различия в эффекте равных по энергии количеств излучения определяются исключительно величиной ЛПЭ. С величиной ЛПЭ прямо связана и относительная биологическая эффективность (ОБЭ) излучения в отношении микроскопических биообъектов.
При воздействии на вещество нейтронов образуются ядра отдачи, величина ЛПЭ которых велика. Поэтому и нейтроны относят к плотноиони-зирующим ИИ. Вместе с тем нейтроны обладают и большой проникающей способностью; образующиеся при их действии плотноионизирующие частицы возникают на разной глубине в толще облучаемого объекта.
WA. Количественная оценка ионизирующих излучений. Основы дозиметрии
Выявление ИИ и количественная оценка уровня радиационных воздействий называется дозиметрией. Для количественной характеристики уровня лучевого воздействия введено понятие дозы излучения. Применяются три основных вида дозы — экспозиционная, поглощенная и эквивалентная.
Экспозиционная доза (X) — мера количества ИИ, физическим смыслом которой является суммарный заряд ионов одного знака, образующихся при облучении воздуха в его единичной массе:
X = Д07дт,
где ДО — суммарный заряд всех ионов одного знака, возникающих в воздухе при полном торможении всех вторичных электронов, образовавшихся в малом объеме пространства, Дт — масса воздуха в этом объеме.
В системе СИ единицей экспозиционной дозы является кулон, деленный на килограмм (Кл/кг). Более часто, однако, применяется внесистемная единица экспозиционной дозы — рентген (Р), соответствующая образованию 2,1 • 109 пар ионов в 1 см3 сухого воздуха при нормальных условиях. 1Кл/кг = 3876 Р; 1Р = 2,58 • Ю-4 Кл/кг.
Изменения, вызываемые излучением в воздухе и в других средах, количественно различны. Это связано с разным количеством энергии, передаваемой излучением одинаковым по массе количествам разных веществ. Учесть этот фактор можно выражая количество ИИ в единицах поглощенной дозы (D). Физический смысл поглощенной дозы — количество энергии, передаваемой излучением единичной массе вещества:
D = ДЕ/Дт,
где ДЕ — энергия излучения, поглощенная малой массой вещества Дт.
В системе СИ поглощенную дозу выражают в греях (Гр). 1 Гр = 1 Дж/кг. Часто пользуются внесистемной единицей поглощенной дозы — рад (аббревиатура eradiation absorbed dose»). Рад равен сантигрею (1 рад = Ю-2 Гр).
Непосредственно измерить биологически значимые величины поглощенных доз не всегда возможно из-за незначительности соответствующей им энергии. Так, при общем облучении человека массой 76 кг в смертельной дозе 4 Гр его телу сообщается энергия 305 Дж. Ее достаточно лишь для нагревания тела на 0,001 С. Поэтому непосредственно измеряется, как правило, экспозиционная доза ИИ, а поглощенная доза рассчитывается с учетом свойств облучаемой среды. В воздухе 1 рентген соответствует 0,89 рад, а в тканях организма в среднем 0,95 рад.
Эквивалентная доза. Различные ИИ вызывают в биосистемах количественно различные эффекты даже при одинаковой поглощенной дозе. Это связано, главным образом, с такими характеристиками ИИ, как ЛПЭ и коэффициент ослабления ц. Для малоразмерных биологических объектов (например, для макромолекул, клеточных органелл и клеток) большему значению ЛПЭ воздействующего на них излучения соответствует большее число актов ионизации и возбуждения, возникающих в пределах конкретного биообъекта. Соответственно, большим оказывается и повреждающий эффект плотноионизирующих излучений в отношении клеток и субклеточных структур. Данное различие выражается величиной ОБЭ. Для рентгеновского и у-излучения ее принимают равной 1, а для каждого из остальных ИИ значение ОБЭ рассчитывают как отношение равноэффективных поглощенных доз рентгеновского и рассматриваемого ИИ. Значения ОБЭ для некоторых видов ИИ представлены в табл. 63.
Таблица 63
Относительная биологическая эффективность ионизирующих излучений для клеток
| Ионизирующее излучение | Величина ОБЭ |
| Рентгеновское, у- и р-излучение | |
| Нейтроны медленные | |
| Нейтроны быстрые и очень больших энергий | |
| а-излучение |
Эквивалентная доза (Н) позволяет учесть различия биологической активности ИИ:
Н = D-ОБЭ,
где D — поглощенная доза ИИ в данной точке биообъекта.
В системе СИ единицей эквивалентной дозы служит зиверт (Зв), а внесистемной единицей является бэр (аббревиатура «биологический эквивалент рада»). 1 Зв = 100 бэр.
Приборы, предназначенные для измерения дозы облучения объекта внешним источником, называются измерителями дозы (дозиметрами).
Мощность дозы излучения (уровень радиации). Этот показатель характеризует интенсивность лучевого воздействия. Мощность дозы понимают как дозу (экспозиционную, поглощенную или эквивалентную), регистрируемую за единицу времени. В системе СИ мощность экспозиционной дозы выражают в Кл/(кг • с), т. е. А/кг. Весьма часто пользуются внесистемной единицей мощности дозы — Р/ч и ее производными (мР/ч, мкР/ч). Единицами мощности поглощенной дозы служат Гр/с, рад/с и их производные. При длительных воздействиях недифференцированных потоков ИИ используют внесистемные единицы мощности эквивалентной дозы — Зв/год и бэр/год.
В зависимости от величины мощности дозы различают кратковременное, пролонгированное и хроническое облучение. Кратковременным облучение считается при мощности дозы свыше 0,02 Гр/мин. Непрерывное радиационное воздействие в течение нескольких месяцев или лет называют
хроническим, а пролонгированное облучение занимает промежуточное положение между первыми двумя. В случае облучения организма человека, если не менее 80% всей дозы регистрируются не более чем за 4 сут, облучение называется однократным.
В зависимости от распределения дозы во времени различают непрерывное и фракционированное облучение. Если доза ИИ разделена на части (фракции), чередующиеся с интервалами времени, в течение которых облучения не происходит, облучение называют фракционированным. Если эти интервалы меньше суток, то по результатам действия на человека фракционированное облучение приближается к непрерывному.
Значение мощности дозы излучения состоит в том, что при равной дозе облучения радиобиологические эффекты выражены тем сильнее, чем больше мощность дозы излучения. Основные дозиметрические величины и единицы их измерения представлены в табл. 64.
Таблица 64
Основные дозиметрические величины и единицы их измерения
| Дозиметрическая величина | Единица, ее наименование, обозначение | Соотношение единиц | |
| внесистемная | СИ | ||
| Экспозиционная доза | Рентген | Кулон на килограмм | 1 Кл/кг .= 3876 Р |
| (Р) | (Кл/кг) | ||
| Мощность | Рентген в час | Ампер на килограмм | 1 А/кг= 1,4«107Р/ч |
| экспозиционной дозы | (Р/ч) | (А/кг) | |
| Поглощенная доза | Рад (рад) | Грей (Гр) | 1 Гр = 100 рад |
| Мощность | Рад в час | Грей в секунду | 1 Гр/с = 3,6«105 рад/ч |
| поглощенной дозы | (рад/ч) | (Гр/с) | |
| Эквивалентная доза | Бэр (бэр) | Зиверт (Зв) | 1 Зв = 100 бэр |
| Мощность | Бэр в год (бэр/год); | Зиверт в секунду | 1 Зв/с = 3.15-109 бэр/год |
| эквивалентной дозы | зиверт в год (Зв/год) | (Зв/с) |
Приборы, предназначенные для измерения мощности дозы облучения объекта из внешнего источника, называются измерителями мощности дозы (рентгенметрами).
Основные источники ионизирующих излучений
По происхождению источники ИИ подразделяются на естественные и искусственные. В промышленно развитых странах от естественных источников население получает около 2/3 суммарной дозы облучения. Медицинские процедуры (лучевая диагностика и лучевая терапия) обусловливают около трети этой дозы, а вклад в нее атомной энергетики, других мирных форм применения источников ИИ и испытаний ядерного оружия пренебрежимо мал (рис. 64).
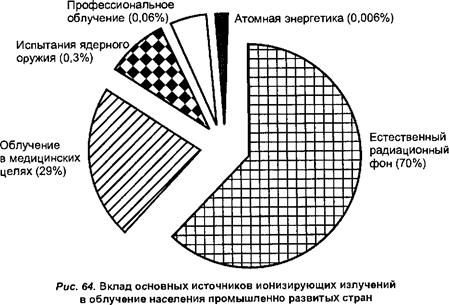
Совокупность потоков ИИ, происходящих из естественных источников, называется природным радиационным фоном Земли. Согласно современным представлениям, последний играет важную роль в качестве движущей силы изменчивости биологических видов, а также одного из факторов поддержания неспецифической резистентности организма.
Извне на организм воздействует в основном у-излучение, источником которого преимущественно являются радиоактивные вещества, присутствующие в земной коре. В каменных зданиях интенсивность внешнего у-облучения в несколько раз ниже, чем на открытой местности, что объясняется экранирующими свойствами конструкционных материалов. Используя специальные приемы экранирования, удается практически полностью устранить внешнее у-облучение организма. По мере увеличения высоты над поверхностью моря роль земных источников внешнего облучения уменьшается. При этом возрастает космическая составляющая природного радиационного фона.
Большинство естественных источников ИИ таковы, что избежать их излучения невозможно: это радиоактивные вещества, входящие в состав организма. Их вклад в суммарную дозу от естественных источников составляет около 2/3.
Искусственные (техногенные) источники ИИ включают в себя рентгеновские трубки, ускорители заряженных частиц, а также устройства, содержащие радионуклиды. Последняя группа подразделяется на открытые (имеющие непосредственный контакт с атмосферой) и закрытые (заключенные в герметичную оболочку) источники ИИ. Как правило, закрытые источники ИИ используют с целью внешнего лучевого воздействия на объекты. Они являются конструктивными элементами у-терапевтических установок, дефектоскопов, атомных реакторов, а также некоторых дозиметрических и радиометрических приборов.
Источниками слабого рентгеновского излучения могут служить радиолампы и электронно-лучевые трубки, широко представленные в производственной и бытовой технике. Однако в штатных условиях эксплуатации интенсивность лучевого воздействия на человека со стороны этих устройств не выходит за основные дозовые пределы, регламентируемые нормами радиационной безопасности.
Основной вклад в дозу, получаемую человеком от искусственных источников ИИ, в настоящее время вносят лечебные и диагностические процедуры. Лучевая нагрузка при некоторых из них указана в табл. 65. В экономически развитых странах дозы облучения населения с медицинскими целями втрое выше, чем в мире в среднем.
Таблица 65
Ориентировочные значения поглощенной дозы излучения при некоторых медицинских процедурах
| Медицинская процедура | Доза излучения, сГр |
| Рентгенография грудной клетки | |
| Флюорография грудной клетки | |
| Рентгеноскопия грудной клетки | 5-10 |
| Рентгеноскопия брюшной полости | 10-20 |
| Лечение злокачественных опухолей | 2000-10 000 |
Источники ИИ, наиболее актуальные в военное время. В случае применения ядерного оружия или крупномасштабных аварий на объектах ядер--ной энергетики ожидается многократное возрастание интенсивности лучевых воздействий на организм. Основными радиационными факторами ядерного взрыва являются проникающая радиация и радиоактивное заражение местности (РЗМ).
Глава 15. РАДИОНУКЛИДЫ КАК ИСТОЧНИК РАДИАЦИОННОЙ ОПАСНОСТИ
15.1. Радиоактивность.
Параметры радиоактивного распада
Свойство самопроизвольного испускания некоторыми элементами ИИ называется радиоактивностью. Радиоактивные свойства впервые обнаружены А. Беккерелем у урана в 1896 г. После того как в 1934 г. Ирен и Фредерик Жолио-Кюри открыли искусственную радиоактивность, были не только получены радиоактивные изотопы всех без исключения элементов, но и заполнены свободные до того времени клетки в периодической системе Менделеева. В 40-х гг. XX в. удалось получить элементы с атомными номерами, превышающими 92 («трансурановые элементы»). Радиоактивность присуща также и нейтронам: за 11 мин один из двух свободных нейтронов превращается в протон, испуская при этом электрон.
Установлено, что источником ИИ, испускаемых радиоизотопами, служат внутриядерные перестройки, сопровождающиеся распадом атомного ядра и образованием нового химического элемента. Химические элементы, имеющие атомные ядра, подверженные самопроизвольному радиоактивному распаду, получили название радионуклидов.
Радиоактивный распад вызывает непрерывное уменьшение числа атомов радиоактивного элемента. Интервал времени, в течение которого распадается половина атомов радионуклида, называется периодом полураспада. Зная эту величину, можно рассчитать число нераспавшихся атомов радионуклида в любой момент времени t:
N=N0 '2-"т,
где N — число атомов в момент t; No — начальное число атомов; Т — лериод полураспада.
Период полураспада является одной из основных характеристик радиоактивного вещества, поскольку его величина строго постоянна и не зависит от условий внешней среды. Если период полураспада измеряется секундами — часами, говорят о короткоживущих радионуклидах, если го-
 |
дами — о долгоживущих радионуклидах. Период полураспада основного природного изотопа урана — 238U — составляет 4,5 млрд лет. Медицинское значение скорости радиоактивного распада состоит в том, что при равном количестве радиоактивных веществ, поступивших в организм или загрязнивших кожные покровы, более длительное облучение (а следовательно, и более высокую дозу облучения) обусловит то из них, которое содержит радионуклид с большим периодом полураспада.
По характеру испускаемых ИИ радионуклиды делят на а- и ^-излучатели. Наряду с этими корпускулами, некоторые радионуклиды излучают также у-кванты. Характер излучения весьма важен для обнаружения радионуклидов во внешней среде и в организме. у-Лучи легко проникают наружу из толщи тел, содержащих радиоактивные вещества. Поэтому наличие у-составляющей ИИ радионуклидов способствует их выявлению и измерению их количества.
15.2. Количество радиоактивных веществ. Радиометрия
Выражать количество радиоактивных веществ в традиционных единицах (массы, веса или объема) неудобно из-за незначительности этих величин для биологически значимых количеств радионуклидов, а также из-за того, что последние, как правило, находятся в смеси с нерадиоактивными веществами и друг с другом. Поэтому критерием оценки количества радиоактивных веществ служит их радиоактивность (активность), т. е. способность к испусканию ИИ. В системе СИ за единицу радиоактивности принят 1 распад в секунду (беккерель, Бк), а традиционной единицей служит кюри (Ки). Активность, отнесенная к единице объема или единице массы зараженного радионуклидами вещества, называется удельной активностью. Активность, отнесенная к единице площади зараженной радионуклидами поверхности, называется плотностью поверхностного радиоактивного заражения. Единицы радиоактивности и производные от них представлены в табл. 66.
Выявление радиоактивных веществ и количественная оценка их содержания в различных объектах и на поверхностях называется радиометрией. В связи с тем что радиоактивные вещества определяются по испускаемым ими ИИ, для радиометрических исследований могут применяться некоторые дозиметрические приборы, в частности измерители мощности дозы у-излучения.
Активность — главный параметр, определяющий дозу облучения тканей, а следовательно, и повреждающий эффект радионуклидов при поступлении в организм и при наружном радиоактивном заражении тела. Вместе с тем, опасность радионуклидов зависит от агрегатного состояния и других физических свойств (адгезивности, липофильности) содержащих их радиоактивных веществ, а также от характера поступления, распределения и выведения радионуклидов из организма.
15.3. Источники радионуклидов. Радионуклиды в природе и народном хозяйстве
Природные радионуклиды
Ранее отмечалась роль радионуклидов как источника естественного радиационного фона. Его земная составляющая включает в себя внешнее и внутреннее облучение от радионуклидов, присутствующих в земной коре и атмосфере.
Внешнее облучение организма на уровне моря обусловлено, в основном, у-излучением радионуклидов уранового ряда, присутствующих в грунте и строительных материалах (рис. 65).
Помимо семейства 238U, в природе существуют еще два радиоактивных семейства — тория (232Th) и редкого изотопа урана — 235U. Разумеется, мощность дозы внешнего облучения зависит от концентраций радионуклидов в том или ином участке земной коры. В местах проживания основной массы населения они примерно одного порядка. Однако есть и такие места, где содержание природных изотопов урана значительно выше. В Бразилии, в 200 км к северу от Сан-Паулу, есть небольшая возвышенность, где уровень радиации в 800 раз превосходит средний и достигает 250 мЗв в год. Чуть меньшие значения (175 мЗв в год) регистрируются на пляжах морского курорта Гуарапаи, также расположенного в Бразилии. Известны и другие места с многократно повышенным уровнем радиации — в Индии, во Франции, Нигерии, на Мадагаскаре. По данным Научного комитета ООН по действию атомной радиации (НКДАР ООН), средняя доза внешнего облучения, которую человек получает от земных источников ИИ естественного происхождения, составляет примерно 350 мкЗв в год.

Внутреннее облучение организма обусловливают преимущественно радиоизотопы, происходящие из земной коры (37К, 238U и радионуклиды уранового ряда). Включение в состав организма (инкорпорация) радионуклидов происходит в основном за счет их поступления с пищей. Поэтому интенсивность внутреннего облучения зависит от состава почв и характера питания населения. Так, например, десятки тысяч людей на Крайнем Севере питаются в основном мясом северного оленя, в котором в высокой концентрации присутствуют изотопы уранового ряда — 210Ро и 206РЬ. Они попадают в организм оленей зимой, когда единственным источником корма животных служат лишайники, накапливающие оба радионуклида. Дозы внутреннего облучения от 210Ро и 206РЬ при этом в 35 раз превышают средний уровень. А в Западной Австралии, на почвах с повышенной концентрацией 238U, облучение, обусловленное этим радионуклидом, в 75 раз превосходит средний уровень у аборигенов, питающихся мясом и требухой овец и кенгуру.
Радионуклидом уранового ряда, проникающим в организм ингаляционным путем, является радон (222Rn). Этот инертный газ высвобождается из почвы и строительных материалов, накапливаясь в закрытых непроветриваемых помещениях. Воздействуя на бронхиальный эпителий а- и у-излучением, радон и радиоактивные продукты его распада оказывают канцерогенный эффект. Задолго до открытия радона вызываемое этим радионуклидом заболевание (позже идентифицированное как рак легких) наблюдал у работников плохо вентилируемых шахт Парацельс, в 1567 г. описавший его в трактате «Uber die Bergsuht und andere Bergkranke-iten».
Вклад в дозу внутреннего облучения радионуклидов «космического» происхождения, т. е. образующихся в земной атмосфере под влиянием космического излучения, существенно меньше. Содержание в тканях живого организма одного из них — 14С — отличается постоянством, но после смерти, вследствие радиоактивного распада, экспоненциально снижается. Это служит основой для радиоуглеродного метода определения возраста палеонтологических находок.
Техногенные источники радионуклидов
В процессе хозяйственной деятельности человека возникает необходимость концентрировать радионуклиды, находящиеся в природном сырье (этот процесс называется обогащением), и накапливать их большие количества в ограниченных объемах. Некоторая часть радиоактивных изотопов, используемых в народном хозяйстве и научных исследованиях, никогда не встречается в естественных условиях. В отличие от естественно-радиоактивных веществ, встречающихся в природных минералах, искусственно-радиоактивные вещества образуются в ходе ядерных реакций при целенаправленной бомбардировке природных изотопов нейтронами или тяжелыми ускоренными заряженными частицами.
К техногенным объектам, содержащим радиоактивные вещества, относятся атомные энергетические установки, атомные исследовательские реакторы, объекты радиохимического производства, а также боевые части ядерного оружия. Кроме того, радиоактивные вещества широко применяются в практике лучевой диагностики (радиография), лучевой терапии (внешнее, внутреннее облучение), при у-дефектоскопии промышленных изделий, при изготовлении постоянно светящихся (люминесцентных) красок. Радионуклиды служат весьма ценным средством научных исследований. Так, радиоизотопные методы применяются для изучения метаболизма у человека, животных и растений. В среднем, доза облучения организма человека от радиоактивных изотопов техногенного происхождения на порядок меньше, чем от природных.
Роль радионуклидов техногенного происхождения как источника облучения организма существенно возрастает при радиационных авариях и применении ядерного оружия.
Глава 16. РАДИОБИОЛОГИЧЕСКИЕ ЭФФЕКТЫ
Глава 16.
РАДИОБИОЛОГИЧЕСКИЕ ЭФФЕКТЫ
Радиобиологическими эффектами называются изменения, возникающие в биологических системах при действии на них ИИ. Сложность организма как биологической системы предопределяет многообразие радиобиологических эффектов. Критериями их классификации служат уровень формирования, сроки появления, локализация, характер связи с дозой облучения, значение для судьбы облученного организма, возможность передачи по наследству последующим поколениям и др.
16.1 Классификация радиобиологических эффектов
16.1.1. Уровень формирования
На молекулярном уровне облучение биосистем вызывает набор характерных изменений, обусловленных взаимодействием биомолекул с самим излучением либо продуктами радиолиза воды. К таким изменениям относят разрывы, сшивки, изменения последовательности мономеров в молекулах биополимеров, потерю ими фрагментов, окислительную модификацию, образование аномальных химических связей с другими молекулами. Доля поврежденных биомолекул положительно связана с их молекулярной массой. Например, после облучения в дозе 10 Гр в клетке оказываются поврежденными 0,015% молекул олигосахаридов, 0,36% — аминокислот, 1% — белков и 100% — нуклеиновых кислот. С уязвимостью ДНК и ее уникальной ролью генетической матрицы связана ведущая роль повреждений ДНК как основы радиобиологических эффектов, формирующихся на более высоких иерархических уровнях биосистемы. Во время митоза повреждения ДНК в клетке проявляются хромосомными аберрациями, основными видами которых являются фрагментация хромосом, формирование хромосомных мостов, дицентриков, кольцевых хромосом, внутри- и межхромосомных обменов и т. п. Однако многие клетки погибают после облучения еще до митоза, а следовательно, и до появления хромосомных аберраций.
На клеточном уровне воздействие ИИ вызывает интерфазную или репродуктивную гибель клеток, временный блок митозов и нелетальные мутации.
Действие ИИ на системном уровне характеризуется цитопеническим эффектом, в основе которого лежат, преимущественно, гибель клеток и радиационный блок митозов.
Радиобиологические эффекты, возникающие на уровне организма и популяции, классифицируются в соответствии с критериями, перечисленными ниже.
16.1.2» Сроки появления
По этому признаку радиобиологические эффекты, возникающие в организме и популяции, принято подразделять на ближайшие и отдаленные. Ближайшие эффекты проявляются в сроки до нескольких месяцев после облучения и связаны с развитием цитопенических состояний в различных тканевых системах организма. Примерами ближайших эффектов облучения могут быть острая лучевая реакция, острая лучевая болезнь, лучевая алопеция, лучевой дерматит.
Отдаленные эффекты возникают спустя годы после облучения, на фоне полной регрессии основных клинических проявлений острого поражения. Несмотря на причинную связь с облучением, отдаленные радиобиологические эффекты не являются специфическими для радиационного воздействия — эта патология вызывается и нелучевыми факторами. Примерами отдаленных последствий облучения являются опухоли, гемобластозы, гипопластические, дистрофические, склеротические процессы. Интегральным проявлением этих последствий служит сокращение продолжительности жизни организмов, перенесших острое лучевое поражение. В случае общего внешнего однократного облучения млекопитающих данный эффект составляет 2—6% средней видовой продолжительности жизни на каждый грей, хотя в области малых доз облучения (по разным данным, менее 4-15 сГр) он, по-видимому, не проявляется.
16.1.3. Локализация
Радиобиологические эффекты могут быть классифицированы в зависимости от органа или части тела, в которых они регистрируются. Весьма актуальна такая классификация в практике лечения онкологических заболеваний, когда пораженный опухолью участок тела облучается в высокой дозе при тщательном экранировании здоровых тканей. При локальном облучении органа или сегмента тела наиболее сильное поражающее действие ИИ проявляется именно в нем (такой эффект называют местным действием ИИ). Однако изменения возникают и в необлученных тканях. В последнем случае говорят о дистанционном действии ИИ. Его примером может служить уменьшение числа миелокариоцитов в костном мозге экранированной конечности после облучения животных. Данный
 |
эффект обусловлен миграцией форменных элементов в опустошенные участки кроветворной ткани, подвергшиеся облучению, подавлением ми-тотической активности «радиотоксинами», поступающими с кровью в экранированные ткани из облученных, физиологическим стрессом, сопровождающим облучение. Конечно, эти факторы влияют и на ткани в зоне облучения, однако в ней непосредственное действие ИИ преобладает над опосредованным.
Местное действие ИИ имеет решающее значение для возникновения не только ближайших, но и отдаленных радиобиологических эффектов. Поэтому для оценки риска канцерогенного эффекта, сопровождающего неравномерное облучение, каждому органу присвоен взвешивающий коэффициент, величина которого меньше 1. Умножением эквивалентной дозы облучения органа на соответствующий ему взвешивающий коэффициент получают эффективную дозу облучения органа. Суммируя эффективные дозы для органов, подвергшихся облучению, получают эффективную дозу неравномерного облучения организма. Последняя численно равна эквивалентной дозе равномерного облучения организма, при которой вероятность развития потенциально смертельной опухоли соответствует рассматриваемому варианту неравномерного облучения.
16.1.4. Характер связи с дозой облучения
По данному критерию радиобиологические эффекты четко разграничены на стохастические (вероятностные) и нестохастические (детерминированные).
Признаками стохастического эффекта являются (1) беспороговость и (2) альтернативный характер. Беспороговость стохастических эффектов означает, что сколь угодно малые дозы облучения способны влиять на частоту их возникновения. Альтернативный характер проявляется в том, что стохастические эффекты, подчиняясь закону «все или ничего», не могут быть охарактеризованы таким показателем, как «выраженность». Примером стохастического эффекта облучения на клеточном уровне может служить гибель клетки; на уровне целостного организма — возникновение злокачественной опухоли. С увеличением дозы облучения вероятность возникновения стохастического эффекта растет (рис. 66, слева), но его качество остается неизменным. При достаточно больших дозах часть облученных организмов погибает до развития у них соответствующих стохастических эффектов, что объясняет «плато» на графике, показанное пунктиром.
Признаками нестохастического эффекта являются (1) пороговый характер и (2) градиентная связь амплитуды с дозой облучения. Если доза облучения превышает пороговую величину (Дп), то нестохастический эффект возникает со 100% вероятностью, причем его амплитуда монотонно возрастает с увеличением дозы (рис. 66, справа).
Знание дозовых «порогов» нестохастических эффектов*(т. е. минимальных значений вызывающих их доз) весьма важно для диагностики и профилактики лучевых поражений. В табл. 67 представлены минимальные величины доз ИИ, вызывающих некоторые из нестохастических эффектов облучения организма человека.
 |
Таблица 67
16.1.5» Значение для судьбы облученного организма
Как правило, радиобиологические эффекты неблагоприятным образом сказываются на биологическом объекте. Исключением из этого правила является герметический эффект. Радиационный гормезис проявляется повышением жизнеспособности организмов под влиянием облучения в малых дозах. О возможности такого феномена свидетельствуют следующие факты.
♦ Всхожесть и энергия прорастания семян может быть повышена их предпосевным облучением.
♦ Выращивание животных в условиях изоляции от естественного радиационного фона сопряжено со снижением неспецифической резистентности относительно контрольного уровня.
♦ У населения территорий, имеющих высокий уровень природного радиационного фона (до 175 мЗв в год), не наблюдается более высокой онкологической заболеваемости, чем в контрольных популяциях. Поскольку повышение заболеваемости, сопряженное с повышенным облучением, вытекает из гипотезы о беспороговости канцерогенного действия ИИ, этот факт не может быть объяснен без допущения о стимулирующем действии малых доз ИИ на неспецифическую резистентность организма (т. е. о горметическом эффекте).
♦ Прием радоновых ванн, сопровождающийся облучением организма в малых дозах, обладает положительным влиянием на функциональное состояние и резистентность организма.
Реальность горметического эффекта признается не всеми специалистами.
Возможность передачи по наследству последующим поколениям. Изменения в генетическом аппарате клеток человеческого организма могут быть унаследованы потомством лишь при условии, что эти изменения возникают в половых клетках. Мутации соматических клеток в естественных условиях не наследуются (такая возможность создается лишь при клонировании организма). Поэтому практически важно разграничивать соматические (возникающие в соматических клетках) и генетические (индуцируемые при воздействии ИИ на половые клетки) радиобиологические эффекты. При общем облучении организма можно ожидать появления как соматических, так и генетических эффектов.
Следует подчеркнуть, что все генетические эффекты облучения проявляются в виде врожденных признаков. В то же время далеко не все врожденные признаки являются проявлением генетических эффектов облучения. Наблюдения за лицами, родители которых были облучены до зачатия во время атомных бомбардировок Японии, не выявили значимого возрастания частоты врожденных дефектов. В то же время риск таких дефектов чрезвычайно высок при равном по дозе лучевом воздействии на эмбрион или плод — особенно при облучении беременной женщины в сроки с 8-й по 15-ю нед беременности. В последнем случае врожденными являются изменения, обусловленные не генетическими, а соматическими эффектами облучения плода.
16.2. Начальные этапы биологической стадии в действии ионизирующих излучений
16.2.1. Первичные стадии в действии излучений
В действии ионизирующих излучений на биологический объект выделяют несколько стадий.
В стадии физических процессов образуются ионизированные и возбужденные атомы и молекулы, случайным образом распределенные в веществе, поскольку вероятность поглощения энергии тем или иным атомом, из которых построены биологические молекулы, практически одинакова.
На стадии физико-химических явлений поглощенная энергия мигрирует по макромолекулярным структурам и распределяется между отдельными биомолекулами, что сопровождается разрывами химических связей там, где эти связи менее прочны. Поэтому, хотя на физической стадии поглощение энергии различными молекулярными структурами было не избирательным, по окончании физико-химической стадии разрывы связей обнаруживаются преимущественно в определенных структурах. В белковых молекулах — это аминокислоты, содержащие спаренные ариль-ные радикалы (например, триптофан), а также тиоловые и дисульфидные группировки; в нуклеиновых кислотах — это азотистые (в первую очередь, пиримидиновые) основания. Разрывы химических связей приводят к образованию свободных радикалов, отличающихся очень высокой химической активностью.
Во время химической стадии образовавшиеся свободные радикалы вступают в химические реакции как между собой, так и с другими молекулами.
Названные эффекты могут быть следствием поглощения энергии излучения самими макромолекулами белков, нуклеопротеидов, структурами внутриклеточных мембран. В этом случае говорят о прямом действии излучения. Энергия излучения может также поглощаться молекулами воды, которые подвергаются радиолизу. Повреждение биомолекул химически высокоактивными продуктами радиолиза воды называют непрямым действием излучения.
Рассмотренные стадии в действии излучений получили наименование первичных. Они осуществляются в течение чрезвычайно короткого промежутка времени (в пределах 1 миллисекунды) и являются общими для действия излучений как на живую, так и на неживую материю.
Биологическая стадия, сущность которой составляют вторичные, так называемые радиобиологические эффекты, прослеживаемые на всех уровнях организации живого, занимает значительно большее время и продолжается иногда в течение всей жизни (табл. 68).
Таблица 68
Основные стадии в действии излучений на биологические системы
| Стадия | Процессы | Продолжительность стадии |
| Физическая | Поглощение энергии излучения. Образование ионизированных и возбужденных атомов и молекул | Ю-16-10-15 с |
| Физико-химическая | Перераспределение поглощенной энергии внутри молекул и между ними. Образование свободных радикалов | 10-14-10"11 с |
| Химическая | Реакции между свободными радикалами, между радикалами и неактивированными молекулами. Образование широкого спектра молекул с измененными структурой и функциональными свойствами | Ю-*-™-3 с ■1 |
| Биологическая | Последовательное развитие поражения на всех уровнях биологической организации — от субклеточного до организменного. Активация процессов биологического усиления и репарации повреждений | Секунды — годы |
:ГУЧК<
16.2.2. Молекулярные механизмы лучевого повреждения биосистем
Относительное количество молекул малого размера, повреждаемых в течение первичных стадий действия излучений, невелико. При дозе облучения .10 Гр (абсолютно летальная доза для млекопитающих) из числа молекул, находящихся в клетке, доля поврежденных составляет для углеводов 0,015%, для нуклеотидов — 0,023%,'для аминокислот — 0,36%. Такое незначительное число поломок молекул, из числа содержащихся в клетке, не может существенно сказаться на жизнедеятельности клетки. Если эти малые молекулы являются компонентами полимерных соединений, их относительная поражаемость оказывается еще меньшей. Однако, в расчете на одну макромолекулу, в полимерах с большой молекулярной массой число повреждений может быть достаточно большим. В растворах белков при облучении их в той же дозе возникает 1 повреждение на 100 молекул, а в молекулах ДНК — 220 на 1 молекулу. В каждой молекуле ДНК оказываются пораженными около 10 нуклеотидов.
Наиболее биологически значимыми в облученной клетке являются изменения ДНК. Это повреждения, лежащие в основе одиночных и двойных разрывов цепочек ДНК: химическая модификация пуриновых и пиримидиновых оснований, их отрыв от цепи ДНК, разрушение фосфоэфирных связей в макромолекуле, распад дезоксирибозы. Кроме того, наблюдаются повреждения ДНК-мембранного комплекса, разрушение связей ДНК-белок, повышающее уязвимость ДНК при атаке вторичными радикалами и ферментами, сшивки ДНК-ДНК и ДНК-белок, нарушения вторичной, третичной и четвертичной структур этого биополимера.
В липидной фракции в присутствии кислорода вследствие активации свободнорадикальных процессов накапливаются продукты перекисного окисления, в первую очередь перекиси и гидроперекиси ненасыщенных жирных кислот. В ряде случаев окислительные процессы в липидах могут принять цепной характер. Липиды являются структурными компонентами внутриклеточных мембран, и их повреждение приводит к существенному нарушению метаболических процессов в клетке, вносит значимый вклад в патогенез лучевого поражения. Некоторые продукты перекисного окисления липидов (гидроперекиси, перекиси, эпоксиды, альдегиды, ке-тоны) обладают выраженными радиомиметическими свойствами: под их влиянием в клетках возникают повреждения, во многом сходные с теми, которые вызываются самим облучением. Такие продукты получили наименование первичных радиотоксинов. Липидные радиотоксины, в частности, изменяют свойства внутриклеточных мембран, их проницаемость, способствуют высвобождению ферментов. Они нарушают регуляцию биохимических процессов, вызывают глубокие нарушения ультраструктуры клеток.
Активации процессов перекисного окисления липидов способствует снижение активности собственных антиокислительных систем клетки. Это обусловлено как радиационным разрушением естественных антиокислителей в клетке, которыми являются в первую очередь фосфолипи-ды, так и разрушением фосфолипидов в результате активации цепной окислительной реакции.
К первичным радиотоксинам относят также образующиеся в облученных клетках продукты окисления фенолов — хиноны и семихиноны.
Изменения обнаруживаются и в других молекулярных компонентах клетки. Наблюдаются повреждения азотистых оснований и разрывы цепей РНК, распад мукополисахаридов, в частности гиалуроновой кислоты, нарушения первичной (вследствие избирательного поражения отдельных аминокислот) и вторичной структур ферментов, изменения их функциональных свойств и химических характеристик и т. п.
16.3. Реакции клеток на облучение
Клетки представляют собой основные ячейки жизни, в которых формируются начальные эффекты лучевых воздействий, приводящие к поражениям, проявляющимся позднее на более высоких уровнях биологической организации — тканевом, органном, системном, организменном. Поэтому в радиобиологии особое внимание уделяют процессам, развивающимся после облучения именно в клетках.
В живой клетке постоянно осуществляется обмен веществ с внешней средой, между отдельными внутриклеточными структурами. Молекулярные повреждения, возникшие в клетках на начальных стадиях действия ионизирующих излучений, изменяют ход обменных процессор, осуществляющихся при участии поврежденных структур. Поскольку локализация и характер первичных повреждений в той или иной молекулярной структуре клетки носят в значительной степени вероятностный характер, весьма разнообразны и связанные с ними изменения метаболизма.
Нарушение метаболических процессов в свою очередь приводит к увеличению выраженности молекулярных повреждений в клетке. Этот феномен получил наименование биологического усиления первичного радиационного повреждения. Однако, наряду с этим, в клетке развиваются и репарационные процессы, следствием которых является полное или частичное восстановление структур и функций.
16.3.1, Биологическое усиление радиационного поражения
Наиболее значимы для судьбы облученной клетки изменения нуклеинового обмена, белкового обмена, окислительного фосфорилирования.
Практически сразу после облучения в делящихся клетках замедляется синтез ДНК. Активируются эндо- и экзонуклеазы, вследствие чего повышается ферментативный гидролиз молекул ядерной ДНК; увеличение проницаемости внутриклеточных мембран способствует поступлению ферментов во внутриядерное пространство, повышает доступность ядерной ДНК для ферментативной атаки. Распад ДНК приводит к повышению содержания в тканях полидезоксинуклеотидов. В крови и моче облученных нарастает количество нуклеотидов и продуктов их разрушения — азотистых оснований, нуклеозидов, мочевой кислоты и др.
Синтез РНК снижается в меньшей степени, чем ДНК. Отчасти нарушение синтеза РНК зависит от повреждения матричных структур ДНК.
Повреждение мембран лизосом и выход за их пределы протеаз способствуют в ранние сроки после облучения активации процессов протео-лиза. Эта активация проявляется повышением уровня свободных аминокислот и других аминосоединений в тканях и жидкостях организма, аминоацидурией, развитием отрицательного азотистого баланса. Повышается активность протеолитических ферментов в крови, тканях, моче. Нарушается активность ингибиторов протеаз. Активация протеолиза не всегда является выражением процессов, происходящих в сохранивших жизнеспособность клетках. Она может отражать завершение деструкции уже погибших клеток.
Биосинтез белка нарушается мало. Однако продолжающийся синтез белка в сочетании с глубоким снижением или даже прекращением синтеза ДНК может привести к серьезным нарушениям структуры и пространственной организации нуклеопротеидных комплексов. Распад комплекса
ДНК — гистон облегчает доступ мутагенов к освобожденным от связей с белком участкам ДНК.
Интенсивность потребления кислорода существенно не изменяется. Однако в первые часы после облучения иногда наблюдаются признаки тканевой гипоксии. В высокорадиочувствительных клетках уже после облучения в сравнительно невысоких дозах отмечается нарушение окислительного фосфорилирования, проявляющееся снижением коэффициента Р/О.
В клетках кроветворных тканей угнетение окислительного фосфорилирования выявляется уже через 2—4 ч после облучения, параллельно с глубоким распадом ДНК. По мнению ряда исследователей, нарушение синтеза АТФ является пусковым звеном в послелучевой деградации ДНК. Нарушение синтеза макроэргов может сказаться и на развитии восстановительных процессов, в частности на работе системы ферментов репарации ДНК. Таким образом, подавление окислительного фосфорилирования играет заметную роль в радиационном поражении генетических структур клетки.
Тканевое дыхание и окислительное фосфорилирование в клетках перенесшего облучение организма, как правило, довольно быстро восстанавливаются.
16.3.2. Репарация лучевых повреждений
Одновременно в ответ на возникшие первичные повреждения в облученной клетке активируются репарационные системы, деятельность которых направлена на устранение возникших повреждений. Наиболее важной из них является система ферментативной репарации повреждений ДНК. Повреждения биомолекул других типов чаще всего не являются фатальными для клетки: продукты их распада могут быть удалены из клетки, а функцию инактивированных соединений могут взять на себя сохранившиеся молекулы того же строения. Молекулы ДНК уникальны, и в случае повреждения их функция не может быть продублирована. При репликации нарушенных матриц будут воспроизводиться дефектные копии — будут синтезироваться аномальные продукты, например ферменты с измененными характеристиками. Поэтому возникшие в результате облучения повреждения ДНК, во избежание развития тяжелых для клетки последствий, должны быть репарированы таким образом, чтобы исходное строение этого чрезвычайно сложно устроенного биополимера было точно восстановлено. В клетке существуют различные системы, способные ре-парировать большинство нарушений структуры ДНК, связанных с повреждением одной из комплементарных цепей, и даже значительную часть повреждений, захватывающих обе нити. Однако избыточная активность ферментов, обеспечивающих такую репарацию, может иногда привести к утяжелению повреждения генома клетки. Так, репарация повреждений ДНК представляет собой весьма энергоемкий процесс, в ходе которого расходуется значительное количество АТФ. Кроме того, в про-
ЗББ
цессе репарации интенсивно потребляется АДФ, что снижает продукцию АТФ клетками. Возникающий в результате дефицит макроэргов может отрицательно сказаться на функциях особенно чувствительных к нему нервных клеток.
Существование в клетках механизмов и ферментных систем, обеспечивающих репарацию большинства начальных повреждений ДНК, эво-люционно обусловлено необходимостью поддержания стабильности генома в условиях постоянно возникающих повреждений ДНК в результате воздействия естественного радиационного фона, присутствия в среде химических мутагенов, случайно возникающих в процессе жизнедеятельности клеток нарушений и сбоев. Если бы не было таких механизмов, жизнь была бы невозможна.
16.3.3. Судьба облученной клетки
Судьба облученной клетки определяется соотношением эффективности процессов биологического усиления и репарации. Чем выше доза облучения, тем выше вероятность того, что в результате процессов биологического усиления появятся необратимые изменения, приводящие к гибели клетки, ее злокачественному перерождению, нарушению пролифератив-ной активности, ограничению дифференцировочных потенций, снижению функциональных возможностей и т. п. Чем ниже доза, чем меньше повреждений возникло в клетке, тем вероятнее восстановление от возникших повреждений, сохранение жизнеспособности и основных функций клетки.
Во всех делящихся клетках сразу после облучения временно прекращается митотическая активность («радиационный блок митозов»). Резкое снижение митотического индекса и, как следствие, прекращение увеличения количества клеток наблюдается как в культурах in vitro, так и при облучении многоклеточного организма. Длительность задержки деления тем больше, чем выше доза (обычно не дольше суток). Может наблюдаться задержка перехода из фазы Gi в S и из фазы G2 в М,
Подавление синтеза ДНК не может рассматриваться как причина торможения митотической активности: последняя снижается ранее, чем начинает обнаруживаться уменьшение включения в ДНК меченых предшественников. Блок митозов объясняют нарушением процессов, регулирующих клеточное деление. В частности, может иметь значение нарушение образования веретена, обеспечивающего расхождение хромосом в митозе.
Задержка деления в клетках активно пролиферирующих тканей (таких, например, как костный мозг) является существенной причиной их опустошения после облучения.
К функциональным нарушениям в клетках могут быть отнесены и такие проявления, как снижение фагоцитарной активности нейтрофилов после облучения, изменения активности некоторых ферментов в этих клетках. При дозах облучения, превышающих несколько десятков грей, важным послелучевым эффектом является нарушение функциональной активности нервных клеток, связанное с дефицитом макроэргов, в результате расходования их предшественников в процессе репарации разрывов ДНК.
Формы лучевой гибели клеток
Важнейшим радиобиологическим эффектом является гибель клеток. Различают две основные ее формы: репродуктивную, т. е. непосредственно связанную с процессом деления клетки, и интерфазную, которая может произойти в любой фазе клеточного цикла.
Репродуктивная форма гибели клеток
Как указывалось ранее, радиационное повреждение уникальных молекул ядерной ДНК имеет особо важное значение для развития лучевого процесса. Однако, если речь идет о ДНК в неделящихся клетках, повреждение «немых» участков ее цепей может и не сказаться существенно на функциях этих клеток.
Для пролиферирующих же клеток значение повреждения ДНК трудно переоценить. Необходимым подготовительным этапом к делению клетки является репликативный синтез ДНК. Двойная спираль ДНК разделяется на две самостоятельные нити, и на каждой из образовавшихся одиночных цепей, ставшими матрицами, достраивается парная к ней путем последовательного присоединения нуклеотидов, комплементарных матричным. В конце концов генетическая информация удваивается и клетка оказывается готовой к делению.
Если в результате облучения возникли повреждения ДНК, например двойные разрывы или сшивки, нормальная репликация делается невозможной. При формировании хромосом повреждения ДНК проявляются возникновением мостов, фрагментов и других типов хромосомных аберраций, многие из которых детальны, поскольку невозможно равномерное распределение генетического материала между дочерними клетками. Эта форма гибели клеток (в митозе) получила наименование репродуктивной гибели.
Количество повреждений ДНК, возникающих в результате облучения, достаточно велико. Так, например, при облучении в дозе 1 Гр в каждой клетке человека возникает около 1000 одиночных и 100—200 двойных разрывов. Каждое из этих событий могло бы иметь фатальные последствия, если бы не существовало упоминавшихся ранее систем, способных ликвидировать большинство возникших повреждений ДНК. Клетки, успевшие репарировать повреждения ДНК до вступления в фазу митоза, способны к нормальному делению. Вызываемое облучением торможение процессов подготовки к делению объективно может благоприятно сказаться на судьбе клетки, поскольку в результате увеличивается время, необходимое для репарации лучевого повреждения. Сейчас большинство исследователей считают, что непосредственной причиной репродуктивной гибели клеток являются нерепарированные повреждения ДНК, прежде всего двойные разрывы цепей и повреждения ДНК-мемб-
зев
ЗВЗ
ранного комплекса. Морфологически клетки, погибающие по репродуктивному типу, можно выявить в ана- или метафазе митоза, обнаружив в них хромосомные аберрации.
Интерфазная форма гибели клеток
По интерфазному типу могут погибать как неделящиеся клетки, так и делящиеся, но находящиеся вне фазы митоза. Чаще всего для возникновения интерфазной гибели требуется облучение в достаточно высокой дозе. Для некоторых типов клеток (миоциты, нейроциты) это десятки и даже сотни грей. В то же время такие клетки, как лимфоциты, тимоциты, ооциты, могут погибнуть уже после воздействия в дозах порядка десятых и даже сотых долей грея.
Механизмами интерфазной гибели клеток могут быть некроз и апоп-тоз. Исходным событием для некроза клеток, подвергшихся облучению, является чаще всего вызванное активацией перекисного окисления липидов повреждение внутриклеточных мембран. Повреждение мембран нарушает работу связанных с мембранами ферментов, подавляет процесс окислительного фосфорилирования. Повышение проницаемости мембран приводит к нарушению градиентов концентраций низкомолекулярных веществ в клетке, выходу лизосомальных протеаз и нуклеаз в цитоплазму и проникновению их в ядро. Угнетается клеточное дь!хание. В результате всех этих процессов развивается деградация нуклеопротеид-ных комплексов в ядре, происходит расплавление или (реже) пикноз ядра, цитолиз с выходом содержимого клетки за пределы клеточной мембраны.
В случае апоптоза происходит межнуклеосомная деградация хроматина, проявляющаяся позднее фрагментацией ядра. Распадается и цитоплазма, участки которой, окружающие осколки ядра, получили наименование «апоптотических телец». По существующим представлениям, процесс апоптоза запускается включением программы самоуничтожения клетки. Происходит активация участков генома, которые контролируют синтез ферментов, участвующих в деградации хроматина. Эту активацию могут вызывать стимулы, возникающие под влиянием разных факторов, в том числе и вызванных облучением повреждений мембранных структур ядерного хроматина. Таким образом, апоптоз — это генетически опосредуемая программированная форма клеточной гибели. Механизм апоптоза особенно характерен для интерфазной гибели лим-фоидных клеток, клеток кроветворной ткани.
Как при репродуктивной, так и при интерфазной формах гибели клетки наблюдается разрушение генетического материала. Однако в первом случае это разрушение происходит в результате прямого или непрямого действия радиации на уникальные структуры ядерной ДНК. В инициировании интерфазной гибели существенная роль принадлежит повреждениям иных структур — внутриклеточных мембран, ферментов, нарушению клеточного метаболизма, и лишь на конечных этапах поражается геном.
Нелетальные повреждения генома клетки
Важным для организма результатом некоторых типов лучевой модификации молекул ДНК является возникновение наследуемых повреждений генетического материала — мутаций, следствием которых может быть злокачественное перерождение соматических клеток. Причиной возникновения мутации могут стать и вызванная облучением дестабилизация ДНК, и процесс репарации ее повреждений. В обоих случаях облегчается внедрение онковирусов в геном клетки или происходит активация тех онковирусов, которые уже предсуществовали в геноме в репрессированном состоянии. Следствием мутации в зародышевых клетках могут стать дефекты развития у потомства облученных родителей.
16.3.4. Количественные характеристики лучевого поражения клеток
При определении зависимости между дозой облучения и количеством сохраняющих при ней жизнеспособность клеток оказывается, что некоторое их число погибает после воздействия уже в самой малой дозе. В то же время и при весьма больших дозах, порядка 10 Гр и более, некоторые клетки могут сохранить жизнеспособность. Кривая убывания числа выживших клеток в зависимости от дозы идет в большей своей части экспоненциально, что свидетельствует о случайности события радиационной гибели клетки. В соответствии с формальными представлениями, в клетке имеется «мишень», под которой понимается критическая микроструктура или совокупность каких-то микропроцессов, повреждение которых несовместимо с сохранением клеткой жизнеспособности. Совпадение микрообъема, в котором реализуется порция поглощенной в веществе энергии, с такой мишенью — событие, приводящее к инактивации клетки. Такое совпадение носит вероятностный характер. С повышением дозы эта вероятность возрастает. Уже при самой малой дозе воздействия, если единственный акт ионизации произошел в пределах мишени, клетка погибает. Но и при очень высокой дозе существует вероятность того, что ни одна из ионизации не затронула мишени. В этом случае клетка должна сохранить жизнеспособность.
Для удобства анализа зависимость выживания клеток от дозы облучения обычно изображают кривой, выполненной в полулогарифмическом масштабе (рис. 67). Кривая состоит из двух участков. Основной (конечный) участок кривой прямолинеен, что отражает экспоненциальный характер зависимости при облучении в относительно высоких дозах. Более пологий начальный участок («плечо») отражает процессы репарации, которые при невысоких дозах облучения обеспечивают известную резистентность клеток.
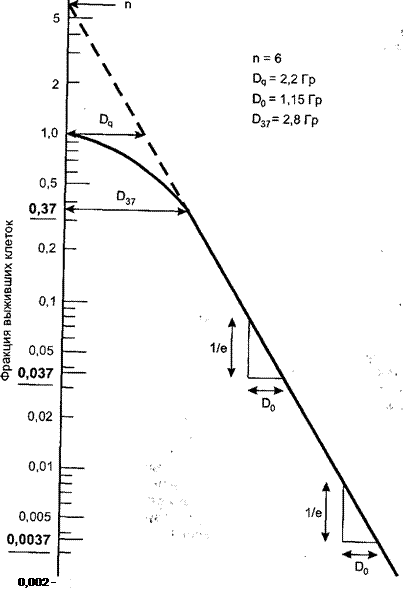
0,001 I--------------- 1___________ J____________ |___________ |____________
2 4 6 8 10
Доза излучения, Гр
Рис. 67. Кривая выживаемости клеток при действии редкоионизирующего излучения
(по С. П. Ярмоненко, 1988)
Основными параметрами радиочувствительности клеток являются величины Do и Dq.
Do характеризует угол наклона экспоненциального участка кривой и определяется как доза, при облучении в которой количество жизнеспособных клеток снижается в е (2,72) раз, т. е. до 37% от величины, принятой за начало отсчета.
Dq (доза плеча) характеризует способность к внутриклеточной репарации и определяется как доза, соответствующая точке пересечения продолжения прямолинейного участка кривой с горизонтальной линией, проведенной на уровне 100% выживаемости клеток.
Чем меньше значения Dq и Dq, тем выше радиочувствительность изучаемой популяции клеток.
Аналогичные зависимости доза—эффект характеризуют и многие другие радиобиологические эффекты, как, например, зависимость от дозы облучения доли клеток, в которых не возникли хромосомные повреждения, доли неповрежденных молекул при облучении растворов и т. п.
16.4. Действие излучений на ткани, органы и системы. Радиочувствительность тканей
Ткани организма весьма различаются по радиочувствительности. Если гибель лимфоцитов или костномозговых клеток удается зарегистрировать после облучения в дозах, равных десятым долям грея, то мышечные и нервные клетки выдерживают нередко дозы в десятки грей. Определенная закономерность в распределении тканей по радиочувствительности отмечена еще в самом начале изучения биологического действия излучений в 1906 г. французскими учеными Бергонье и Трибондо. Ими было сформулировано правило, согласно которому ткани тем более радиочувствительны, чем выше пролиферативная активность составляющих их клеток, и тем более радиорезистентны, чем выше степень их дифференцировки.
Высокую радиочувствительность активно пролиферирующих клеток связывают с особой ролью при облучении повреждений уникальных структур ядерной ДНК (см. выше). На тканевом уровне острое радиационное поражение проявляется нарушениями структуры и функции, зависящими прежде всего от клеточного опустошения ткани.
Хотя радиочувствительность тканей определяется главным образом радиочувствительностью составляющих эту ткань клеток, нельзя сбрасывать со счетов и опосредованные влияния радиации через поражение регулирующих систем — нервной, эндокринной. Кроме того, радиочувствительность органа зависит от его функционального состояния. Так, чувствительность обычно повышается при усилении функции органа (молочной железы в периоде лактации, щитовидной железы в состоянии гипертериоза и т. д.).
Во взрослом организме, в соответствии с правилом Бергонье и Трибон-до, непролиферирующие высокодифференцированные нервные клетки высокорадиорезистентны. Однако это относится лишь к морфологическим проявлениям повреждения. Функциональные же реакции нейронов обнаруживаются в ответ на облучение уже в ничтожных дозах. Так, ранние изменения электроэнцефалограммы появляются после облучения в дозе 0,5 мГр; облучение в дозе 1 мГр вызывает заметное удлинение времени рефлекса в ответ на электрораздражение. Спящие крысы просыпаются в результате облучения в дозе 0,01—0,02 Гр. Волны электрической активности в переживающих in vitro нервных клетках вызывает облучение в дозе 0,01 Гр. Все это говорит о высокой реактивности элементов нервной системы по отношению к радиационным воздействиям.
Можно заключить, что термин «радиочувствительность» в его обычном употреблении не очень удачен. Казалось бы, логичнее, как это предлагал в свое время видный патофизиолог и радиобиолог П. Д. Горизонтов, понимать под радиочувствительностью количественное выражение любых форм реакции биологического объекта на облучение, а не только повреждения. Если бы это предложение утвердилось, нервную ткань называли бы наиболее радиочувствительной. Однако в радиобиологии термин радиочувствительность применяется чаще всего как синоним радио-поражаемости.
16.4.1. Радиационное поражение системы крови
Система крови относится к числу систем клеточного обновления, функционирование которых обеспечивает поддержание постоянного числа функциональных клеток, обладающих короткой продолжительностью жизни. Схема функционирования такой системы приведена на рис. 68.
Послелучевые изменения, происходящие в системе клеточного обновления, будут рассмотрены на примере гранулоцитопоэза.
Одним из важных эффектов является приостановка клеточного деления (блок митозов), которая тем продолжительнее, чем выше доза облучения.
По выходе из блока часть клеток, в которых повреждения ядерной ДНК не были репарированы, подвергается репродуктивной гибели. Часть клеток погибает по интерфазному типу. С повышением дозы число погибающих клеток увеличивается. Наиболее радиочувствительны клетки стволового отдела (Do составляет около 1 Гр), и по критерию утраты способности к образованию колоний дочерних клеток число стволовых клеток резко снижается практически сразу после облучения. Высокой радиочувствительностью обладают и клетки пула пролиферации. Что же касается клеток пула созревания, то их радиочувствительность сравнительно невысока, большинство этих клеток сохраняют жизнеспособность, созревают и выходят в периферическую кровь. В результате количество клеток в костном мозге, а затем и в периферической крови довольно быстро убывает. Вначале снижается число наиболее молодых, наиболее радиочувствительных клеток. Затем процесс опустошения захватывает все более и более зрелые отделы, так как созревание и выход в кровь созревших клеток продолжаются, а восполнения их числа за счет поступления из пролиферативного пула нет. Наконец, и в периферической крови развивается гранулоцитопения (рис. 68).

Рис 68. Схема развития опустошения в системе клеточного обновления после облучения в высокой дозе (по В. Бонду и соавт., 1971)
На ход кривой содержания в крови гранулоцитов влияют и другие факторы. Так, в ближайшие часы после облучения обнаруживается ранний нейтрофильный лейкоцитоз перераспределительного характера — неспецифическая реакция, наблюдаемая при воздействии и других раздражителей. Важное значение имеет так называемый абортивный подъем
числа нейтрофилов, наблюдающийся у человека с середины 2-й нед после облучения и сменяющийся еще более глубоким снижением количества этих клеток. Абортивный подъем объясняют возобновлением (после выхода из митотического блока) пролиферации клеток, способных к ограниченному числу делений, что обеспечивает лишь временное увеличение числа зрелых нейтрофилов. Однако и оно оказывается полезным, сокращая период глубокой нейтропении.
В клетках периферической крови облученных обнаруживаются морфологические и цитохимические изменения, что свидетельствует о их неполной функциональной полноценности. Однако в основном клетки крови после облучения в дозах несколько грей (при острой лучевой болезни) выполняют свои функции удовлетворительно, и главной причиной клинических нарушений, связанных с поражением кроветворения, являются не качественные изменения в клетках, а уменьшение их количества.
Начало снижения содержания в крови отдельных видов функциональных клеток после облучения и срок, когда глубина этого снижения максимальна, зависят главным образом от времени, в течение которого клетки-предшественники находятся в составе пулов пролиферации, созревания, а также от продолжительности циркуляции в крови созревших клеток. Эти параметры различны как для разных клеточных линий, так и для разных видов животных. У человека прохождение предшественников гранулоцитов через пул пролиферации занимает 4-6 дней и примерно столько же времени — прохождение через пул созревания. Зрелые грану-лоциты циркулируют в крови в среднем всего 8-10 ч.
В соответствии с названными сроками нейтропения у человека начинает обнаруживаться примерно через 5 сут после облучения. Продолжительность пребывания в крови человека тромбоцитов оценивается в 6-8 дней и минимальный их уровень достигается через 2—2,5 нед.
Длительность жизни эритроцитов в крови составляет 100-120 дней. Поражение зрелых эритроцитов после облучения в дозах, составляющих несколько грей, невелико и поэтому даже в случае полного прекращения продукции новых эритроцитов их число в сутки может снизиться примерно на 1% и анемия развивается очень медленно (если не возникнет кровотечения).
Продолжительность блока митозов зависит от дозы облучения и составляет от нескольких часов до суток, редко более. После выхода из блока сохранившие жизнеспособность стволовые клетки возобновляют пролиферацию, создавая тем самым основу для восстановления морфологического состава костного мозга, а затем и крови. Это восстановление числа стволовых кроветворных клеток можно наблюдать уже тогда, когда в крови только еще начался процесс опустошения. Однако, чтобы процесс восстановления в стволовом отделе реализовался увеличением числа зрелых функциональных клеток, необходимо время как для восстановления достаточного числа самих стволовых клеток, так и для прохождения клеток через пулы деления и созревания.
Выраженность цитопении (т. е. глубина, время достижения и продолжительность снижения содержания в крови клеток) нарастает с увеличением дозы облучения.
Поражение кроветворения и связанные с ним клинические проявления, в первую очередь инфекционные осложнения и повышенная кровоточивость, получили наименование костномозгового синдрома, который лежит в основе одноименной формы ОЛБ, развивающейся после облучения в дозах 1—10 Гр.
16.4.2. Радиационное поражение органов желудочно-кишечного тракта
При общем облучении среди органов желудочно-кишечного тракта наиболее значимо поражение эпителия слизистой оболочки тонкой кишки, который является принципиально такой же системой клеточного обновления, как и костный мозг. Но если в костном мозге клетки разной степени созревания располагаются без видимого порядка, в слизистой оболочке кишки взаимное расположение клеток, относящихся к разным пулам, четко разграничено.
На дне крипт находятся стволовые клетки. По мере деления стволовых клеток и последующего их созревания клетки продвигаются по направлению к устью крипт и далее по стенке ворсинки к ее верхушке, откуда слу-щиваются в просвет кишки. Утрата клеток с ворсинок сбалансирована притоком вновь образованных клеток из крипт. Продвижение клетки от дна крипты до верхушки ворсинки занимает около 4 сут.
Как и в других системах клеточного обновления, в эпителии кишки после облучения наступает временный блок митозов, погибают прежде всего стволовые и другие делящиеся клетки. Созревающие и функциональные клетки, будучи радиорезистентны (Do составляет 15 Гр), после облучения продолжают продвижение к верхушкам ворсинок и слущива-ются. Эпителиальная выстилка кишки при отсутствии пополнения за счет клеточного деления быстро исчезает, ворсинки «оголяются» и уплощаются.
Стволовые энтероциты менее чувствительны к гамма- и рентгеновскому облучению, чем стволовые кроветворные клетки, вследствие более высокой активности в них систем внутриклеточной репарации повреждений ДНК: Dq для стволовых клеток составляет в костном мозге величину менее 1 Гр, а в эпителии тонкой кишки — порядка 4 Гр. Поэтому опасное для жизни повреждение эпителия кишки происходит при более высоких дозах (порядка 10 Гр), чем дозы, достаточные для глубокого повреждения костного мозга (4-5 Гр). В случаях, когда доза общего облучения достигает величины, при которой повреждение кишки становится несовместимым с сохранением жизни организма, патологический процесс развивается очень быстро и уже к концу 3-5-х сут происходит полная денудация слизистой оболочки. Несовместимая с жизнью панцитопения в крови развивается значительно позднее.
Если в ранние сроки не наступит смертельного исхода, сохранившиеся стволовые клетки эпителия кишки обеспечивают его быструю регенерацию, восстановление структуры и функции кишечной стенки.
Описанные изменения слизистой оболочки тонкой кишки, достигающие в случае общего облучения максимальной выраженности при дозах, превышающих 10 Гр, лежат в основе развития так называемого кишечного синдрома.
Другие отделы желудочно-кишечного тракта менее радиочувствительны, чем тонкая кишка, и их повреждение при общем облучении чаще всего не имеет самостоятельного значения.
Во всех отделах желудочно-кишечного тракта после общего облучения в дозах, не доходящих до уровня, при котором типичным является развитие кишечного синдрома, могут наблюдаться эрозии, изъязвления, местные некрозы вплоть до перфорации кишечной стенки. Чаще всего возникновение этих проявлений связано с развитием вторичной инфекции и геморрагии на почве костномозгового синдрома. В практическом отношении наиболее важны некротическая энтеропатия и орофарингеа-льный синдром.
При местном облучении области живота в достаточно высоких дозах возможно возникновение некрозов и изъязвлений участков желудочно-кишечного тракта, подвергшихся воздействию.
16.4.3. Лучевое поражение центральной нервной системы
Выраженные морфологические проявления поражения клеток центральной нервной системы наблюдаются, как правило, только после воздействия в дозах, приближающихся к 50 Гр и выше. Наиболее ранние изменения обнаруживаются в синапсах (слипание синаптических пузырьков в скоплениях, появляющихся в центральной части пресинаптических терминалов или в активной зоне). При световой микроскопии через 2 ч после облучения в таких дозах обнаруживается набухание клеток, пикноз ядер зернистых клеток мозжечка, реже — других нейронов, явления вас-кулита, менингита, хориоидального плексита с гранулоцитарной инфильтрацией. Максимум изменений приходится на 1-е сут после облучения. При более высоких дозах может наблюдаться ранний некроз ткани мозга.
При облучении в дозах 10-30 Гр в клетках центральной нервной системы обнаруживают угнетение окислительного фосфорилирования. Последнее связывают с дефицитом АТФ, расходуемого в процессе репарации вызванных облучением разрывов ДНК. Развиваются очаги так называемого реактивного состояния нервных клеток: набухание нейронов, повышение аргирофильности. При этом погибают, как правило, лишь отдельные нейроны. Распространенные очаговые изменения в вегетативных ганглиях могут явиться одной из причин дискоординации функций внутренних органов.
Отмеченные изменения в нервных клетках неспецифичны для лучевого поражения и наблюдаются при действии некоторых токсических факторов. В значительной мере изменения нервных структур вторичны, т. е. являются следствием изменений в других системах в ходе развития лучевого поражения (токсемия, инфекционный процесс).
Уже отмечалась способность нервных клеток отвечать функциональными реакциями на воздействие даже малых доз облучения. К этому следует добавить, что на функции нервной системы могут повлиять и обильная патологическая афферентная импульсация из поврежденных радиочувствительных тканей, и токсические влияния продуктов клеточного распада, эндотоксинов, проникающих во внутреннюю среду из кишки, и т. п.
В ходе лучевой болезни выявляются изменения биоэлектрической активности коры головного мозга, в эксперименте регистрируются расстройства условнорефлекторной деятельности, особенно резко выраженные в терминальном периоде.
Расстройства нервной системы могут проявляться и непосредственными клиническими симптомами, как, например, при остром пострадиационном ЦНС-синдроме, при первичной реакции на облучение, которые будут рассмотрены позднее, и нарушениями регуляции вегетативных функций, процессов восстановления поврежденных тканей.
После облучения в дозах порядка нескольких десятков Грей нарушения функций центральной нервной системы лежат в основе развития церебральных нарушений, определяющих клиническую картину поражения организма.
Таким образом, хотя радиочувствительность нейронов и невысока, нарушения функций нервной системы могут иметь существенное значение для развития лучевого поражения.
Раздел IV. ВОЕННАЯ РАДИОБИОЛОГИЯ
Задачами военной радиобиологии являются: обоснование мероприятий, направленных на обеспечение радиационной безопасности личного состава войск в условиях воздействия факторов радиационной природы мирного и военного времени; обоснование мероприятий медицинской противорадиационной защиты и лечебных вмешательств в условиях применения ядерного оружия, разрушения ядерных энергетических установок, радиационных аварий мирного времени; разработка средств медикаментозной профилактики острых радиационных поражений, средств повышения радиорезистентности человека, находящегося в условиях повышенной лучевой нагрузки, средств и методов оказания неотложных мероприятий в случае возникновения острых лучевых поражений, порядка применения этих средств в войсках.
Глава 17. ФАКТОРЫ, ВЫЗЫВАЮЩИЕ ПОРАЖЕНИЯ ЛИЧНОГО СОСТАВА ВОЙСК ПРИ ЯДЕРНЫХ ВЗРЫВАХ И РАДИАЦИОННЫХ АВАРИЯХ
В случае применения ядерного оружия или крупномасштабных аварий на объектах ядерной энергетики на личный состав войск могут действовать различные виды ИИ, неблагоприятные факторы нелучевой природы, а также их комбинации. При ядерных взрывах именно эти воздействия выводят из строя личный состав войск, поэтому наиболее важные из них называются поражающими факторами ядерного взрыва.
17.1. Поражающие факторы ядерного взрыва
К числу поражающих факторов ядерного взрыва относятся ударная волна, световое излучение, проникающая радиация, радиоактивное заражение местности (РЗМ) и электромагнитный импульс. Прямым поражающим действием на организм человека обладают первые четыре фактора; электромагнитный импульс вызывает повреждения электронных и электротехнических устройств. По продолжительности действия различают кратковременно действующие поражающие факторы ядерного взрыва (ударная волна, световое излучение и проникающая радиация) и длительно действующий фактор — РЗМ. По физической природе поражающие факторы ядерного взрыва могут быть радиационными либо нерадиационными.
17.1.1. Радиационные поражающие факторы ядерного взрыва
Радиационными факторами ядерного взрыва являются проникающая радиация и радиоактивное заражение местности (РЗМ).
Проникающая радиация ядерного взрыва представляет собой поток у-излучения и нейтронов, распространяющийся в воздухе во все стороны из центра взрыва на расстояние до 3 км. Источником проникающей радиации являются ядерные реакции деления и синтеза, протекающие в боеприпасах в момент взрыва, а также радиоактивный распад продуктов ядерного деления.
у-Кванты могут быть мгновенными, испускаемыми в ходе протекания ядерных реакций взрыва при взаимодействии нейтронов с конструкционными материалами боеприпаса, осколочными, образуемыми при радиоактивном распаде осколков деления, или захватными, возникающими при ядерных перестройках, вызываемых нейтронами в атомах воздуха и грунта.
Нейтроны проникающей радиации могут быть мгновенными, испускаемыми в ходе протекания ядерных реакций взрыва, и запаздывающими, образующимися в процессе распада продуктов ядерного деления в первые 2—3 с после взрыва.
Время действия проникающей радиации при атомных и водородных взрывах не превышает нескольких секунд и определяется временем подъема облака взрыва на такую высоту, при которой у-излучение практически полностью поглощается толщей воздуха. Поражающее действие проникающей радиации на человека определяется дозой облучения, а также (в случае частичного экранирования) фактором неравномерности распределения этой дозы по телу.
Радиоактивное заражение местности возникает в результате выпадения радиоактивных веществ из облака ядерного взрыва. Его значение как поражающего фактора определяется тем, что высокие дозы облучения личного состава войск и населения могут наблюдаться не только в районе, прилегающем к месту взрыва, но и за сотни километров от него. Кроме того, радиационное воздействие, обусловленное РЗМ, более продолжительно, чем действие проникающей радиации. Спад активности выпавших на местность продуктов ядерного взрыва происходит экспоненциально:
А, = Ао (t/t0)-12,
где Ао и А, — активность продуктов ядерного взрыва ко времени t0 и t после взрыва.
Наиболее существенное РЗМ происходит при наземных ядерных взрывах, когда площади заражения с опасными значениями мощности дозы излучения многократно больше размеров зон поражения ударной волной, световым излучением и проникающей радиацией. Масштабы РЗМ зависят также от мощности ядерного взрыва и метеоусловий (скорости ветра в слое атмосферы, ограниченном высотой подъема облака, наличия осадков). При воздушных ядерных взрывах РЗМ незначительно и не вызывает санитарных потерь личного состава.
Лучевое поражение людей, находящихся на РЗМ, обусловлено (в порядке убывания значимости) равномерным внешним у-облучением тела, внешним р-облучением открытых участков кожи, конъюнктив и слизистых оболочек, а также излучениями радионуклидов, которые могут проникать в организм ингаляционным либо пероральным путем.
Последствия пребывания личного состава на РЗМ с достаточной точностью могут прогнозироваться по величине дозы внешнего у-облучения тела. Такой расчет наиболее целесообразно производить заблаговременно, что позволяет избежать неоправданного переоблучения и минимизировать потери личного состава. Для удобства расчета доз облучения вся территория, подвергшаяся радиоактивному заражению, разделяется на участки, различающиеся величинами мощности дозы излучения на местности — зоны РЗМ. Воображаемые границы между ними представляют собой изолинии эллиптической формы, все точки каждой из которых характеризуются одинаковыми значениями мощности дозы. Характеристика зон РЗМ, данные для расчета их размеров, а также интенсивности радиационных воздействий на личный состав (дозы, мощности дозы у-излучения, плотности поверхностного радиоактивного заражения кожных покровов и обмундирования) содержатся в Справочнике по поражающему действию ядерного оружия. Эти данные необходимы для прогнозирования величины, структуры и динамики возникновения санитарных потерь среди личного состава, находившегося на РЗМ.
17.1.2. Нерадиационные поражающие факторы ядерного взрыва
Ударная волна является основным поражающим фактором ядерных взрывов средней и большой мощности. Она представляет собой область резко сжатого воздуха, распространяющегося во все стороны от центра взрыва. Поражения людей ударной волной возникают в результате действия избыточного давления во фронте ударной волны, скоростного напора воздуха и действия вторичных ранящих снарядов (предметов, отброшенных скоростным напором воздуха).
В результате действия ударной волны у незащищенных людей могут возникать разнообразные травмы. В Хиросиме их получили 40% пораженных, ее воздействием было обусловлено 20% смертельных исходов. Показателем, позволяющим достаточно точно предсказать действие ударной волны на личный состав, сооружения и военную технику, является величина избыточного давления во фронте ударной волны.
Световое излучение ядерного взрыва представляет собой поток видимого света, ультрафиолетового и инфракрасного излучения, исходящий из светящейся области взрыва. Поражающее действие этого фактора обусловлено нагревом подлежащих поверхностей и вторичными ожогами от воспламенившегося обмундирования. При формировании зон обширных пожаров могут возникать «огненные бури», при которых возможны термические ожоги не только кожи, но и верхних дыхательных путей, а также массовые отравления оксидом углерода.
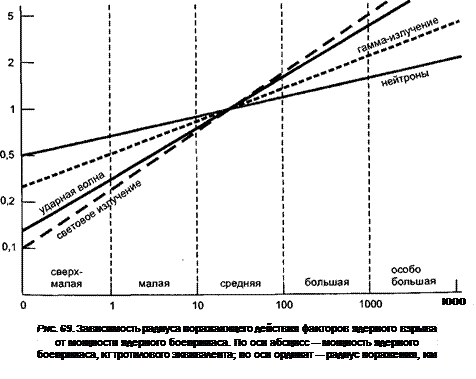
Радиус поражающего действия ударной волны, светового излучения и проникающей радиации представляет собой расстояние, на котором они могут выводить из строя открыто расположенный личный состав. Для проникающей радиации этот показатель возрастает с увеличением мощности ядерного боеприпаса медленнее, чем радиус поражающего действия ударной волны и светового излучения ядерного взрыва (рис. 69). При взрывах сверхмалой (до 1 кт) и малой (1-10 кт) мощности он больше у проникающей радиации, чем у других кратковременно действующих поражающих факторов ядерного взрыва. При взрывах средней (10-100 кт), большой (100-1000 кт) и особо большой (>1 Мт) мощности радиус поражающего действия ударной волны и светового излучения больше или равен таковому для проникающей радиации. У нейтронных боеприпасов, создающих повышенную интенсивность нейтронной компоненты проникающей радиации ядерного взрыва, радиус ее поражающего действия существенно превосходит таковые для ударной волны и светового излучения. Эти соотношения учитываются при прогнозировании структуры санитарных потерь от ядерного оружия. При взрывах малой и сверхмалой мощности (включая нейтронные) можно ожидать появления большого количества больных с изолированными лучевыми поражениями. Санитарные потери в зоне кратковременно действующих факторов более мощных ядерных взрывов будут характеризоваться преобладанием комбинированных радиационных поражений, при которых клиническая картина травм и ожогов будет отягощена облучением в различных дозах.
При авариях или разрушениях ядерных реакторов основным радиационным фактором, способным вызвать поражения личного состава войск и населения на прилегающих территориях, является РЗМ. Особенностями последнего являются более медленный, чем в случае ядерного взрыва, спад мощности дозы излучения на местности, более сложная конфигурация зараженных участков местности, а также более высокие адгезивность и контаминирующая способность выпадающих на местность радиоактивных веществ. Кроме того, внешнее р- и у-облучение в поражающих человека дозах может происходить в момент прохождения радиоактивного па-ро-аэрозольного облака аварийного радиационного выброса. Масштаб РЗМ определяется типом аварийного ядерного реактора, степенью его разрушения и метеоусловиями (скорость ветра, устойчивость приземного слоя атмосферы, наличие осадков).
При радиационной аварии риск поступления радионуклидов в организм выше, чем при ядерном взрыве, что обусловлено пребыванием некоторой их части в газообразном состоянии и способностью преодолевать противогазы и респираторы. В ранние сроки (несколько суток) после начала аварии наибольшую опасность представляет инкорпорация смеси радиоактивных изотопов йода. В более поздние сроки (спустя годы после аварии) на первый план выходит внутреннее облучение организма за счет поступивших в него долгоживущих радионуклидов 137Cs и 90Sr.
Потери личного состава, обусловленные пребыванием в зоне следа облака аварийного радиационного выброса, так же как и на следе облака ядерного взрыва, определяются дозой внешнего у-облучения. Для удобства ее расчета на местности, подвергшейся радиоактивному загрязнению, выделяют зоны РЗМ. Характеристика зон РЗМ, методика расчета их размеров и показателей уровня облучения находящегося в них личного состава (дозы, мощности дозы) содержатся в соответствующих справочниках.
17.21. Характеристика лучевых поражений
Лучевые поражения личного состава как при применении ядерного оружия, так и вследствие техногенных аварий на радиационно-опасных объектах могут стать результатом внешнего облучения и проникновения радионуклидов во внутренние среды организма. При этом выделяют:
1. Лучевые поражения от внешнего облучения:
• поражения в результате общего (тотального) облучения;
• местные лучевые поражения от внешнего облучения.
2. Поражения от наружного заражения покровных тканей радионук-
лидами.
3. Поражения от внутреннего радиоактивного заражения.
Формирующаяся при этом патология характеризуется многообразием клинических форм, закономерностью развития, четкой зависимостью между величиной лучевого воздействия и тяжестью заболевания. Медицинская защита личного состава и лечение пораженных предполагают использование специальных медикаментозных средств. Их разработка, совершенствование и практическое применение основываются на понимании сущности лучевых поражений.
Глава 18. ЛУЧЕВЫЕ ПОРАЖЕНИЯ В РЕЗУЛЬТАТЕ ВНЕШНЕГО ОБЛУЧЕНИЯ
Под внешним облучением понимают такое, при котором источник излучения располагается на расстоянии от облучаемого объекта. Результатом внешнего облучения человека являются общие и местные лучевые поражения. Особенности течения лучевых поражений от внешнего облучения определяются видом излучения, дозой, распределением поглощенной дозы в объеме тела и во времени.
18.1. Классификация лучевых поражений от внешнего облучения в зависимости от вида и условий воздействия
По виду воздействия различают лучевые поражения:
1) от у- или рентгеновского излучения;
2) от нейтронного излучения;
3) от р-излучения (при внешнем воздействии а-излучения поражение не может возникнуть вследствие очень низкой проникающей способности а-частиц).
Рентгеновы и у-лучи, а также нейтроны высоких энергий характеризуются высокой проникающей способностью и оказывают повреждающее воздействие на все ткани, лежащие на пути пучка. При общем облучении в соответствующей дозе в этом случае развивается острая лучевая болезнь. Острая лучевая болезнь может быть вызвана и воздействием высо-коэнергетичных электронов, генерируемых в специальных ускорителях.
Р-Излучение, исходящее от радиоактивных источников, находящихся вблизи человека, обладает невысокой проникающей способностью и может явиться причиной поражения только кожи и слизистых оболочек. Однако, добавляясь к воздействию у-излучения, эффект р-воздействия может существенно утяжелить общее поражение.
Тяжесть лучевого поражения зависит в первую очередь от дозы облучения. При общем внешнем у- или нейтронном облучении доза является
основным фактором, определяющим развитие той или иной патогенетической формы ОЛБ и степени ее тяжести (табл. 69).
Таблица 69
Патогенетическая классификация острой лучевой болезни от внешнего облучения
| Клиническая форма | Степень тяжести | Доза, Гр (+ 30%) |
| Костномозговая | 1 (легкая) | 1-2 |
| Костномозговая | 2 (средняя) | 2-4 |
| Костномозговая | 3 (тяжелая) | 4-6 |
| Костномозговая (переходная) | 4 (крайне тяжелая) | 6-10 |
| Кишечная | - | 10-20 |
| Токсемическая (сосудистая) | - | 20-50 |
| Церебральная | - | Более 50 |
Клинические проявления, наблюдающиеся иногда после облучения в дозах менее 1 Гр, называют лучевой реакцией.
По характеру распределения поглощенной дозы в объеме тела различают общее (тотальное) и местное (локальное) облучение. Общее облучение бывает равномерным и неравномерным. Неравномерность распределения дозы может создаться вследствие экранирования отдельных областей тела, а также в результате внутреннего поглощения при прохождении излучения через толщу тканей. В реальных условиях облучение всегда в той или иной степени неравномерно. Однако, если различия в дозах, поглощенных разными участками тела не превышают 10-15%, такое облучение называют равномерным.
Поражения при общем равномерном и умеренно неравномерных (Dmax / Dmin < 3-5) вариантах облучения укладываются в общее представление об острой лучевой болезни.
При локальном облучении в дозах, превышающих толерантность тканей, находящихся на пути пучка, возникают местные лучевые поражения. Такие поражения наиболее характерны для ситуаций, связанных с лучевой терапией злокачественных новообразований, но могут возникнуть и при радиационных авариях и инцидентах.
Если местное повреждение тканей происходит на фоне общего облучения в дозах (неравномерное облучение с высокой степенью неравномерности), приводящих к развитию острой лучевой болезни, поражение называют сочетанным.
Характеризуя временные условия, лучевые воздействия подразделяют на однократные и фракционированные. По общей продолжительности набора дозы выделяют кратковременное, пролонгированное и хроническое облучения.
В зависимости от длительности облучения развиваются острые, подо-стрые и хронические формы лучевого поражения. Развитие острого поражения (особенно это относится к острой лучевой болезни) характерно для варианта облучения, при котором продолжительность периода набора поражающей дозы не превышает одной — полутора недель. При более длительном (пролонгированном) облучении развиваются подострые формы поражения. Если же общая продолжительность облучения превышает несколько месяцев, развиваются хронические формы. При этом важна общая длительность облучения, и несущественно, было ли облучение непрерывным или разделенным на фракции.
18.2. Зависимость эффекта облучения от его продолжительности
Если облучение оказывается растянутым во времени, за счет снижения мощности дозы или разделения дозы на отдельные фракции, биологический его эффект, как правило, оказывается меньшим по сравнению с тем, каким бы он был, если бы та же доза была получена за меньший срок. Соответственно, в эксперименте, чтобы получить эффект одинаковый с эффектом кратковременного облучения суммарную дозу фракционированного или пролонгированного облучения необходимо увеличить. С увеличением промежутка времени между фракциями устойчивость к повторному облучению увеличивается.
Снижение поражающего действия облучения при разделении дозы на фракции обозначают как эффект фракционирования. Следует усвоить некоторые термины, связанные с этим эффектом. Часть поражения, которая восстановилась к моменту определения, так и называют восстановленная часть поражения. Ее определяют как разность между суммарной дозой двукратного облучения и равноэффективной ей дозой однократного. Часть поражения, оставшаяся «невосстановленной», получила наименование остаточной дозы или, удачнее, дозы остаточного поражения.
Эффективная доза фракционированного облучения определяется как сумма остаточного поражения и дозы последнего облучения. По смыслу, эффективная доза фракционированного облучения — это равная ей по эффективности доза однократного облучения. Величина остаточного поражения снижается со временем экспоненциально, однако, как было установлено, 10% исходного поражения не восстанавливается (необратимая компонента).
Наиболее выражены восстановительные процессы после облучения в дозах достаточно больших, но еще не приводящих к гибели. При дозах выше и ниже этого уровня темп восстановления замедляется. При малых дозах воздействия количество возникающих поломов недостаточно для индукции максимально возможного уровня восстановления. Облучение в высоких дозах повреждает сами механизмы восстановления. При практических расчетах снижения величины остаточного поражения со временем дозовые различия темпа восстановления часто не учитывают. У человека
3SB
период полувосстановления (снижения остаточного поражения вдвое) оценивается ориентировочно в 28 дней.
Важно отметить, что восстановление радиорезистентности может происходить на фоне прогрессирующего развития лучевого поражения, оцениваемого по клиническим проявлениям, картине крови и т. п. Механизмы восстановления устойчивости к повторному воздействию радиации неодинаковы в ранние и поздние сроки после предварительного облучения. Главными из них являются следующие.
В ранние сроки (первые 10-12 ч) — это репарация сублетальных молекулярных повреждений клетках, сохранивших жизнеспособность после первого облучения и, соответственно, повышение радиоусточиво-сти этих клеток. Позднее (около 1 сут и далее) — регенерация на клеточном уровне за счет размножения клеток, сохранивших жизнеспособность, в частности стволовых клеток костного мозга. Большое значение имеет также развитие адаптивных и компенсаторных реакций, приводящих к повышению устойчивости к повторному облучению.
Восстановление радиорезистентности можно наблюдать не только при фракционировании дозы в перерыве между фракциями, но и в процессе самого облучения, если оно растянуто во времени. Поэтому при длительном непрерывном облучении значение эффективной дозы также снижается.
При различном распределении дозы во времени происходит не только количественное изменение эффективной дозы, но изменяются и динамика патологического процесса, и характер поражения разных систем. Увеличение общего периода облучения приводит к более длительному течению лучевого поражения (при равноэффективных по смертности дозах), к развитию подострых и хронических форм лучевых поражений.
Если общая продолжительность внешнего облучения превышает 10 сут, может развиться костномозговая форма острой лучевой болезни с подо-стрым течением. Клинические проявления первичной реакции мало выражены или могут отсутствовать. Растягивается во времени период разгара, и максимум проявлений приходится на более поздний срок, чем при кратковременном облучении. Сильнее выражена гипорегенераторная анемия. Замедляются восстановительные процессы.
При растянутом во времени облучении не развиваются церебральная и кишечная формы лучевой болезни. Дело в том, что процессы послелучево-го восстановления в эпителии тонкой кишки и в центральной нервной системе идут с весьма высокой скоростью и при длительном облучении успевают ликвидировать основную часть возникающих повреждений. По мере увеличения продолжительности облучения все большее значение приобретают расстройства нервной регуляции различных функций организма, ас-тенизация, нервно-сосудистые дистонии.
В результате облучения, продолжающегося многие месяцы и годы, может развиться хроническая лучевая болезнь.
18.3. Зависимость эффекта облучения от распределения поглощенной дозы в объеме тела
Если при общем облучении различия в дозах, поглощенных различными областями тела, не превышают 10-15%, облучение называют равномерным; при более сильных различиях — неравномерным. Неравномерное облучение людей чаще всего имеет место в аварийных ситуациях разного рода, при несчастных случаях, а также при взрывах атомных бомб.
При облучении в дозах, вызывающих развитие костномозгового синдрома, если коэффициент неравномерности (Кн — отношение максимальной поглощенной дозы к минимальной) менее 3, сохраняются основные патогенетические особенности поражения, характерные для равномерного облучения. В то же время одинаковый по выраженности эффект возникает при заметно более высокой дозе неравномерного облучения по сравнению с равномерным. При одной и той же среднетканевой поглощенной дозе тяжесть поражения в случае неравномерного ее распределения оказывается существенно меньшей, чем при равномерном облучении.
Снижение повреждающего эффекта при неравномерном облучении зависит, прежде всего, от благоприятного влияния сохранившихся в менее облученных участках костного мозга стволовых кроветворных клеток, которые, мигрируя в участки костного мозга, подвергшиеся облучению в более высоких дозах, способствуют ускорению восстановительных процессов и в этих участках.
Расчеты, основанные на знании дозовой зависимости гибели стволовых кроветворных клеток у человека и распределения кроветворной ткани по организму, позволяют предложить оптимальный вариант размещения экранирующих приспособлений с тем, чтобы при заданной массе защитного материала эффект был максимален.
Так, чтобы сколько-нибудь существенно защитить водителя автомобиля от у-излучения на радиоактивно загрязненной местности, равномерно распределив экранирующий материал по кабине, потребовалось бы такое его количество, которое бы резко утяжелило машину. Сопоставимый защитный эффект можно получить при значительно меньшей массе экранирующего материала, лишь усилив им сиденье и спинку кресла и использовав фиксированный на сиденье пояс. В этих случаях эффект будет особенно выражен, поскольку в защищаемых областях сосредоточены значительное количество кроветворной ткани и существенная часть кишечника.
Если прогнозируется воздействие облучения в дозах, приводящих к развитию церебрального синдрома, особенно в случаях, когда голова может явиться преимущественно облучаемой частью тела, целесообразно экранирование головы. В случае преимущественно нейтронного воздействия, для такой защиты могут быть применены полимерные материалы,
заа
заэ
содержащие в своем составе много водорода. Предложены специальные подшлемники из таких материалов.
Если при неравномерном облучении дозы, поглощенные ограниченными участками тела, превышают порог толерантности тканей и возникает их местное повреждение, говорят о сочетанном лучевом воздействии и сочетанном лучевом поражении. Сочетанные лучевые поражения могут возникнуть у человека, оказавшегося на местности, загрязненной продуктами ядерного взрыва.
В патогенезе сочетанного радиационного поражения взаимодействуют механизмы, связанные с одновременным поражением критической системы в результате общего облучения и формированием местной лучевой травмы. Даже при сравнительно равномерном облучении, наряду с определяющим значением поражения критических систем, существенную роль играет весь комплекс воздействий ионизирующих излучений на другие органы и ткани. Ведущим фактором, определяющим течение сочетанного поражения, является, как правило, доза общего внешнего облучения, однако в части случаев на основные проявления и исход могут существенно влиять и местные процессы. Вследствие неравномерности облучения костного мозга восстановление кроветворения при сочетанном поражении начинается раньше, а продолжительность глубокой цито-пении сокращается. Однако состояние пораженных часто остается тяжелым вследствие продолжающегося поступления эндотоксинов из очагов локального поражения.
В боевой обстановке чаще всего могут возникать сочетанные радиационные поражения с преимущественным воздействием на голову и развитием при достижении достаточной дозы церебрального и орофарингеа-льного синдромов. На втором месте по вероятности возникновения стоят варианты с преимущественным облучением живота и развитием при соответствующей дозе модифицированного кишечного синдрома.
t
Глава 19. ЛУЧЕВЫЕ ПОРАЖЕНИЯ
В РЕЗУЛЬТАТЕ ОБЩЕГО
(ТОТАЛЬНОГО) ОБЛУЧЕНИЯ_
19.1. Острая лучевая болезнь
Наиболее важным для военного врача вариантом лучевого поражения является так называемая острая лучевая болезнь (ОЛБ). Патогенетическую основу ОЛБ составляет несовместимое с нормальной жизнедеятельностью поражение одной из систем, называемых «критическими»: кроветворной, эпителия тонкой кишки, центральной нервной системы.
Острая лучевая болезнь (ОЛБ) — симптомокомплекс, развивающийся в результате общего однократного равномерного или относительно равномерного внешнего рентгеновского, у- и (или) нейтронного облучения в дозе не менее 1 Гр. Каждое из перечисленных условий является необходимым для формирования ОЛБ. Так, если доза облучения меньше 1 Гр, лучевое поражение проявляется, преимущественно, гематологическими изменениями («острая лучевая реакция») без существенного ухудшения функционального состояния организма. Возможны лишь легкие транзиторные клинические проявления в виде тошноты и чувства слабости. Если большая часть дозы получена в результате пролонгированного облучения, заболевание приобретает подострое течение, а если необходимая доза накапливается несколько месяцев, формируется хроническая лучевая болезнь. При экранировании во время облучения значительных по объему частей тела (т. е. несоблюдении условия равномерности пространственного распределения дозы) клиническая картина также не соответствует ОЛБ, определяясь преимущественно местным лучевым поражением.
В клинической картине ОЛБ преобладают проявления поражения той тканевой системы, дисфункция которой лимитирует продолжительность жизни организма при данной дозе облучения. Такая тканевая система называется критической. В зависимости от дозы, в качестве критической тканевой системы при внешнем облучении могут выступать кроветворная, пищеварительная или центральная нервная система. В соответствии с этим выделяют четыре клинические формы ОЛБ (см. табл. 69), подробная характеристика которых будет дана ниже.
 |
19.1.1. Костномозговая форма J
острой лучевой болезни
В случае общего облучения в дозах 1 — 10 Гр судьба организма определяется поражением преимущественно кроветворной ткани. Костномозговую форму иногда называют типичной, поскольку при ней наиболее четко проявляется присущий ОЛБ периодизм. В течении ОЛБ выделяют:
1) период общей первичной реакции на облучение;
2) скрытый период (период мнимого благополучия);
3) период разгара;
4) период восстановления.
Период общей первичной реакции на облучение
Свободные радикалы, образовавшиеся в результате взаимодействия продуктов радиолиза воды между собой и с кислородом, повреждают | биомолекулы, вызывая образование их перекисных соединений и ве- "| ществ хиноидного ряда, именуемых радиотоксинами. В пролиферирую- ' щих тканях отмечаются задержка митозов, репродуктивная и интерфазная гибель клеток. Продукты их распада (в том числе такие биологически активные вещества, как гистамин, серотонин) совместно с радиотоксинами циркулируют в крови. Обусловленные этим повышение проницаемости сосудистой стенки, нарушение регуляции сосудистого тонуса, мощная афферентная импульсация и гиперстимуляция триггер-зоны рвотного центра составляют патогенетическую основу симптомокомп-лекса общей первичной реакции на облучение. Он включает в себя дис-пептический (тошнота, рвота, диарея) и астено-вегетативный (головная боль, слабость, гиподинамия, артериальная гипотензия) синдромы.
В периферической крови в это время прогрессирует дозозависимое снижение числа лимфоцитов, гибнущих интерфазно в течение нескольких часов после облучения. В течение первых суток отмечается перераспределительный нейтрофильный лейкоцитоз (этот показатель неспецифичен для лучевого воздействия и количественно не связан с дозой).
Выраженность и продолжительность общей первичной реакции на облучение тем больше, чем выше доза облучения. Время начала проявлений этого симптомокомплекса, напротив, отрицательно связано с дозой. Диагностика ОЛБ в первые 2—3 сут после облучения основывается на перечисленных проявлениях общей первичной реакции на облучение и осуществляется в соответствии с данными, представленными в табл. 70. Вспомогательное диагностическое значение в эти сроки может иметь возникновение распространенной лучевой эритемы после общего облучения в дозах более 6 Гр.
сформировавшейся еще в период первичной реакции на облучение глубокой лимфопении, данный показатель с достаточным приближением отражает содержание в крови нейтрофильных гранулоцитов. На 7—9-й день после облучения содержание лейкоцитов кратковременно стабилизируется (благодаря феномену абортивного подъема) на уровне, хорошо коррелирующем с дозой (табл. 71).
Вспомогательное диагностическое значение может иметь лучевая алопеция, наблюдаемая в конце скрытого периода при облучении в дозах, превышающих 3 Гр.
Таблица 71
Реконструкция дозы общего однократного равномерного внешнего у-облучения организма по содержанию лейкоцитов в периферической крови на 7-9-е сут после облучения
| Уровень лейкоцитов, х109/л | Доза, Гр |
| 3-4 | 1-2 |
| 2-3 | 2-4 |
| 1-2 | 4-6 |
| Менее 1 | Более 6 |
Продолжительность скрытого периода тем меньше, чем выше доза облучения. При легкой форме ОЛБ скрытый период может закончиться лишь через 30 и более суток после облучения, при средней — через 15—30 сут, при тяжелой — через 5—20 сут, а при крайне тяжелой — скрытый период может отсутствовать. Прогнозирование продолжительности скрытого периода важно для своевременной эвакуации больных в лечебные учреждения, располагающие условиями для лечения ОЛБ.
Период разгара
Его наступление при типичной форме ОЛБ обусловлено падением числа функциональных клеток крови ниже критического уровня. Грану-лоцитопения и тромбоцитопения являются ведущими причинами развития аутоинфекционных осложнений и геморрагического синдрома — потенциально смертельных клинических проявлений ОЛБ в период разгара.
Наряду с симптомами, прямо проистекающими из нарушения кроветворения, при костномозговой форме ОЛБ наблюдаются проявления и других дисфункций: токсемия, астения, преобладание катаболизма над анаболизмом, вегетативная дистония, аутоиммунные поражения. Эти нарушения, конечно, должны учитываться при оценке состояния больного и проведении комплексной терапии ОЛБ, хотя основу поражения составляет нарушение кроветворной функции.
Глубина и продолжительность цитопении и, соответственно, тяжесть клинических проявлений ОЛБ, зависят прежде всего от дозы облучения. Существенное значение имеют и различия в индивидуальной радиочувствительности организма. Продолжительность аутоинфекционных и геморрагических проявлений приблизительно соответствует времени, в течение которого в периферической крови регистрируются субкритические значения содержания лейкоцитов и тромбоцитов. На рис. 70 представлен случай, при котором клиническая картина аутоинфекционных осложнений наблюдается с 12-х по 20-е сут после облучения. Нарушения устойчивости к экзогенной инфекции наблюдаются значительно дольше, что обусловлено более медленной, в сравнении с клетками гранулоцитарного ряда, нормализацией содержания в крови лимфоцитов.

Рис. 70. Динамика содержания нейтрофильных гранулоцитов (1) и лимфоцитов (2) в периферической крови при ОЛБ (схема).
По оси абсцисс — время после облучения, сутки; по оси ординат - содержание клеток крови в процентах от исходного уровня. Пунктиром показан критический уровень для нейтрофильных гранулоцитов
Непосредственной причиной смерти при ОЛБ чаще всего служат тяжелые инфекционные процессы и кровоизлияния в жизненно важные органы.
Период восстановления
Если в периоде разгара не наступит смерть, регенераторные процессы в кроветворной системе обеспечивают через определенный срок увеличение числа зрелых клеток крови, а с ним и ликвидацию симптоматики периода разгара. Начинается период восстановления, в течение которого происходит полная или частичная нормализация функций критических систем организма.
Прогноз для жизни. Экспертиза бое- и трудоспособности
Прогноз для жизни при ОЛБ легкой степени — благоприятный. При ОЛБ средней степени — благоприятный при проведении надлежащего лечения. При ОЛБ тяжелой степени прогноз сомнительный: даже интенсивная комплексная терапия не всегда оказывается успешной. Без лечения среднесмертельная доза у- или рентгеновского излучения для человека составляет ориентировочно 3,5—4,0 Гр. Продолжительность жизни в случаях, заканчивающихся летально, составляет при типичной форме ОЛБ 3-5 нед.
Трудоспособность при ОЛБ легкой степени во все периоды сохраняется. В течение 2-го месяца болезни требуется ограничение тяжелого физического труда. При ОЛБ средней степени к началу 3-го месяца болезни возможно возвращение к легкому труду, а через год — к обычной деятельности. После перенесенной ОЛБ тяжелой степени работоспособность полностью не восстанавливается. Легкий труд возможен с 4-го месяца болезни.
19.1.2. Кишечная форма острой лучевой болезни
После общего облучения в дозах 10—20 Гр развивается кишечная форма ОЛБ, основу проявлений которой составляет кишечный синдром. Этот симптомокомплекс развивается в течение недели после облучения. Он связан с повреждением и гибелью клеток эпителия тонкой кишки. Основная роль в механизмах оголения подслизистого слоя отводится прямому радиационному поражению стволовых клеток эпителия. Имеет значение также нарушение трофики кишечной стенки, обусловленное снижением порога возбудимости нейронов интрамуральных парасимпатических ганглиев и развитием спазма гладкой мускулатуры кишки.
Наиболее важным следствием оголения подслизистого слоя тонкой кишки является прекращение резорбции из ее просвета воды и электролитов. Развивается дегидратация, которая сама по себе угрожает жизни больного. Из-за нарушения барьерной функции кишечной стенки во внутреннюю среду поступают токсичные вещества, в частности токсины кишечной палочки. Их количество также может оказаться несовместимым с жизнью. По этой же причине в кровь и лимфу проникает кишечная микрофлора. Ее размножению способствует развивающаяся одновременно гранулоцитопе-ния. При достаточной выраженности перечисленные процессы приводят к гибели, если не предпринимаются попытки лечения, в течение недели.
Поскольку исчезновение эпителиальной выстилки тонкой кишки происходит уже при у-облучении в дозе 10 Гр, дальнейшее увеличение дозы не может что-либо добавить к этому достаточному условию смертельного исхода, и сроки гибели не меняются с изменением дозы в диапазоне 10-20 Гр.
В течении кишечной формы ОЛБ часто можно выделить отдельные периоды, подобные тем, которые описывались при костномозговой форме. Начальный период отличается большей тяжестью проявлений и большей длительностью. Кроме того, нередко уже с первых дней отмечается диарея. Глубже снижается артериальное давление (иногда развивается коллаптоидное состояние). Весьма выражена и длительно сохраняется ранняя эритема кожи и слизистых оболочек. Температура тела повышается до фебрильных значений. Больные жалуются на боль в животе, мышцах, суставах, голове.
Продолжительность первичной реакции при кишечной форме ОЛБ составляет 2—3 сут. Затем может наступить кратковременное улучшение общего состояния (эквивалент скрытого периода костномозговой формы ОЛБ), однако проявления заболевания полностью не исчезают. Продолжительность скрытого периода не превышает 3 сут.
Наступление периода разгара кишечной формы ОЛБ знаменуется резким ухудшением самочувствия, развитием диареи, повышением температуры тела до 39—40° С, развитием проявлений орофарингеального синдрома, обезвоживания, интоксикации и эндогенной инфекции, которой способствует раннее наступление агранулоцитоза. Смертельному исходу обычно предшествует развитие сопора и комы.
При условии лечения пораженные с кишечной формой ОЛБ могут прожить до двух и даже двух с половиной недель. В этом случае есть время для развития панцитопенического синдрома, вторичной инфекции и кровоточивости, которые и служат причиной смерти.
19.1.3. Токсемическая форма острой лучевой болезни
Развивается после облучения в дозовом диапазоне 20—50 Гр. Для этой формы характерны тяжелые гемодинамические расстройства, связанные с парезом и повышением проницаемости сосудов, проявления интоксикации продуктами распада тканей, радиотоксинами и токсинами кишечной микрофлоры.
Токсемия обусловливает нарушения мозгового кровообращения и отек мозга, прогрессирующие признаки которого наблюдаются до смертельного исхода, наступающего в течение 4—7 сут. В связи со значимостью расстройств циркуляции в развитии токсемической формы ОЛБ ее называют еще сосудистой.
19.1.1. Церебральная форма острой лучевой болезни
В основе церебральной формы ОЛБ, развивающейся у человека после облучения головы или всего тела в дозах 50 Гр и выше, лежат дисфункция и гибель нервных клеток, обусловленные преимущественно их прямым радиационным поражением. При таком уровне доз повреждения ядерного хроматина столь многочисленны, что вызывают гиперактивацию систе-
ЗЭВ
мы ферментов репарации ДНК. ДНК-лигазная реакция сопровождается гидролизом АТФ, а реакция, катализируемая аденозиндифосфорибозил-трансферазой, способна вызвать быстрое и глубокое истощение внутриклеточного пула НАД+. Зависимые от этого кофермента реакции гликолиза и клеточного дыхания оказываются заторможенными, что приводит к нарушению ресинтеза АТФ. Продолжительный дефицит АТФ глубоко и необратимо влияет на клетки коры головного мозга, отличающиеся крайне высокой потребностью в энергии.
Проявления церебрального лучевого синдрома зависят от мощности дозы облучения: если она превышает 10—15 Гр/мин, то в течение нескольких минут после облучения могут развиться коллаптоидное состояние, резчайшая слабость, атаксия, судороги. Данный симптомокомплекс получил название синдрома ранней преходящей недееспособности (РПН). Наиболее вероятно его развитие при импульсном (особенно нейтронном) облучении, например, при действии проникающей радиации нейтронного боеприпаса. Через 10—45 мин основные проявления РПН проходят, сменяясь временным улучшением состояния. В менее выраженной форме РПН возможен и при кратковременном облучении в меньших дозах — от 20 до 50 Гр.
Если облучение происходит с небольшой мощностью дозы, то РПН не развивается, и после проявлений первичной реакции на облучение (тошнота, рвота и др.) может наступить временное улучшение состояния. Однако нарастают признаки отека мозга, психомоторное возбуждение, атаксия, дезориентация, гиперкинезы, судороги, расстройства дыхания и сосудистого тонуса. Эта симптоматика обусловлена не только дисфункцией, но и гибелью нервных клеток. Смерть наступает в течение не более чем 48 ч после облучения, ей предшествует кома.
19.2. Особенности поражений нейтронами
В основе отличий, присущих ОЛБ при воздействии нейтронами, лежат меньшая репарируемость нейтронных поражений на клеточном уровне и меньшая, в сравнении с рентгеновыми и у-лучами, проникающая способность (а стало быть, и меньшая равномерность распределения дозы по телу). Нетрудно заметить, что эти факторы действуют в противоположных направлениях. Поэтому при нейтронных воздействиях сильнее поражается кишечный эпителий, радиорезистентность которого в сравнении с кроветворной тканью в значительной мере связана с большей способностью к репарации сублетальных повреждений клеток. Кроветворная же система поражается меньше, чем при соответствующей поглощенной дозе электромагнитного ИИ: это связано с ускорением процесса восстановления кроветворной ткани за счет миграции клеток из менее облученных ее участков.
По этим же причинам серьезные повреждения тонкой кишки развиваются даже при несмертельных дозах нейтронного облучения организма. В отличие от случаев у-облучения, наличие кишечного синдрома не всегда является неблагоприятным прогностическим признаком; его лечение может привести в дальнейшем к выздоровлению.
К другим особенностям ОЛБ от воздействия нейтронов относятся:
• большая выраженность первичной реакции на облучение и РПН-синдрома;
• большая глубина лимфопении в период первичной реакции на облучение;
• признаки более тяжелого повреждения органов и тканей на стороне тела, обращенной к источнику излучения;
• более выраженная кровоточивость как следствие прямого повреждения нейтронами стенки сосудов.
Перечисленные особенности необходимо учитывать при действии на организм проникающей радиации ядерного взрыва, когда соотношение вклада нейтронов и у-лучей в дозу облучения зависит от мощности, типа ядерного боеприпаса и расстояния до центра взрыва.
19.3. Отдаленные последствия общего (тотального) облучения
У больных, перенесших острую лучевую болезнь, в течение длительного времени, иногда всю жизнь, могут сохраняться остаточные явления и развиваться отдаленные последствия.
Остаточные явления чаще всего проявляются гипоплазией и дистрофией тканей, наиболее сильно поврежденных при облучении. Они представляют собой последствия неполного восстановления повреждений, лежавших в основе острого поражения: лейкопения, анемия, нарушения иммунитета, стерильность и др. В отличие от них отдаленные последствия — это развитие новых патологических процессов, признаки которых в остром периоде отсутствовали, таких как катаракты, склеротические изменения, дистрофические процессы, новообразования, сокращение продолжительности жизни. У потомства облученных родителей в результате мутаций в герминативных клетках могут проявиться генетические последствия.
Среди форм отдаленной лучевой патологии будут рассмотрены:
• неопухолевые отдаленные последствия;
• канцерогенные эффекты;
• сокращение продолжительности жизни.
19.3.1. Неопухолевые отдаленные последствия облучения
Неопухолевые (нестохастические) отдаленные последствия относятся к числу детерминированных эффектов облучения, тяжесть которых зависит главным образом от степени дефицита числа клеток соответствующих тканей (гипопластические процессы). К числу наиболее важных компонентов комплекса причин, определяющих развитие отдаленных последствий облучения, относятся повреждения мелких кровеносных сосудов и расстройства микроциркуляции, ведущие к развитию тканевой гипоксии и вторичному поражению паренхиматозных органов. Имеют также существенное значение клеточный дефицит в тканях, в которых пролиферация недостаточна для восполнения числа погибших после облучения клеток (рыхлая соединительная ткань, гонады и др.), сохранение изменений, возникших во время облучения в клетках непролиферирующих и медленно пролиферирующих тканей.
В большинстве некритических тканей возникновение тяжелых отдаленных последствий после общего кратковременного облучения маловероятно. Дозы, которые при общем облучении не абсолютно детальны, как правило, не превышают порога толерантности для некритических тканей и не могут привести к существенному дефициту клеток в них (как исключение из этого общего правила могут быть названы хрусталик, семенники). В критических же тканях регенераторные процессы, если организм не погибает, обычно довольно быстро восстанавливают клеточный состав. Поэтому отдаленные последствия, развивающиеся по причине дефицита клеток, более характерны для локального облучения, когда и в относительно радиорезистентных тканях могут быть поглощены дозы, превышающие их толерантность. Развитие названных изменений во взаимодействии с естественными возрастными процессами определяет развитие функциональных расстройств. Отдаленные последствия лучевого поражения могут проявиться функциональными расстройствами регулирующих систем: нервной, эндокринной, сердечно-сосудистой (асте-но-невротический синдром, вегето-сосудистая дистония).
К отдаленным нестохастическим эффектам относят и некоторые гиперпластические процессы, развивающиеся как компенсаторная реакция на снижение функций определенного типа клеток. Такие реакции характерны для эндокринных органов. Например, очаговая гиперплазия ткани щитовидной железы при повреждении других ее участков в случае инкорпорации радиоактивного йода.
19.3.2. Канцерогенные эффекты облучения
Радиационный канцерогенез относится к числу стохастических эффектов. Основной причиной злокачественной трансформации облученной клетки являются нелетальные повреждения генетического материала. На первых порах исследования радиационного канцерогенеза господствовало представление о том, что прямой причиной злокачественной трансформации клетки является мутация, возникшая в результате поглощения порции энергии излучения соответствующим участком генома клетки. Хотя в отдельных случаях такой ход событий и может иметь место, более вероятны другие возможности.
Наиболее распространена гипотеза, в соответствии с которой под влиянием облучения повышается нестабильность ядерной ДНК. В процессе репарации ее нелетальных повреждений возникают условия, способствующие включению онковируса в геном соматической клетки или активации онковируса, уже находившегося в репрессированном состоянии в составе генома, с последующей раковой трансформацией.
Злокачественной трансформации клетки, сохранившей жизнеспособность после облучения, может способствовать ее контакт с большим количеством клеточного детрита. Вследствие повреждения мембранных структур может измениться чувствительность клеток к регулирующим воздействиям со стороны гормонов, ингибиторов и т. п.
Фактором, способствующим злокачественной трансформации клетки, бывают расстройства гормональной регуляции. Особенно велико значение этого фактора при внутреннем радиоактивном заражении, когда радионуклиды длительное время воздействуют на железу, нарушая выработку ею гормонов, влияющих на функции других органов. В результате создаются условия для возникновения гормон-зависимой опухоли (например, опухоли гипофиза у животных с вызванной введением ш1 гипоплазией щитовидной железы). Щитовидную железу рассматривают как критический орган в формировании отдаленной патологии при поступлении в организм продуктов ядерного деления.
Способствуют развитию опухоли и вызванные облучением нарушения иммунитета, в результате чего облегчается развитие опухоли не только из трансформированных облучением клеток, но и из клеток, мутации в которых возникли спонтанно или под влиянием других факторов.
Латентный период между радиационным воздействием и возникновением новообразования составляет в среднем 5—10 лет, но в некоторых случаях может достигать 35 лет (рак молочной железы).
Вероятность возникновения опухоли в результате радиационного воздействия оценивается как один дополнительный случай на 20 человек, облученных в дозе 1 Гр. Относительный риск возникновения злокачественного новообразования в течение всей жизни выше для облученных в детстве. Выход опухолей на единицу дозы зависит от ряда факторов, таких как качество излучения (ОБЭ нейтронов по риску возникновения злокачественного новообразования после облучения в малых дозах может превышать 10), мощность дозы и др.
19.3.3. Сокращение продолжительности жизни
Интегральным показателем состояния здоровья популяции может служить средняя продолжительность жизни (СПЖ) составляющих эту популяцию особей. Важным проявлением отдаленных последствий действия облучения как раз и является сокращение СПЖ.
У грызунов оно составляет от 1 до 5% на 1 Гр. При длительном воздействии малых доз у-излучения сокращение СПЖ у грызунов наблюдали, начиная с ежесуточной дозы 0,01 Гр, причем суммарная накопленная доза, после достижения которой начинало достоверно проявляться сокращение СПЖ, составляла не менее 2 Гр (для нейтронов значения суточной дозы и общей накопленной дозы, при которых СПЖ сокращалась, были на порядок меньше).
При анализе феномена сокращения СПЖ не удается выделить какой-нибудь типичный патологический процесс, непосредственно приводящий облученных животных к преждевременной гибели. В тех случаях, когда причину смертельного исхода у отдельных особей удавалось связать с каким-то конкретным патологическим процессом, это мог быть и сосудистый криз, и новообразование, и склеротические изменения, и лейкоз, и т. д.
Основной причиной сокращения СПЖ после облучения в сублетальных дозах в настоящее время называют повреждение капилляров и мелких артериол, нарушения микроциркуляции, приводящие к гипоксии и гибели паренхиматозных клеток, преимущественно, в органах иммунитета и железах внутренней секреции. Отчасти сокращение СПЖ может быть связано с более частым развитием у облученных злокачественных новообразований.
Сокращение продолжительности жизни у человека может составить, по разным оценкам, от 100 до 1000 сут на 1 Гр при однократном кратковременном облучении и порядка 8 сут при хроническом. В то же время, как уже отмечалось, при дозах ниже 2 Гр само наличие сокращения продолжительности жизни признается не всеми исследователями.
Продолжительность жизни врачей-рентгенологов в период 1932—1942 гг. составила в среднем 60,5 лет против 65,7 лет у врачей других специальностей, т. е. была на 5,2 года меньше. Расчеты показывают, что за 35 лет практики накопленная в то время рентгенологами доза могла составить 5 Гр.
Наиболее частыми причинами преждевременной гибели оказались новообразования, в том числе лейкозы, смертность от которых была в 3 раза выше, чем среди прочего взрослого населения, дегенеративные изменения, инфекционные процессы и др. После 1945 г., в результате внедрения мер противорадиационной защиты, различия в продолжительности жизни рентгенологов и врачей других специальностей исчезли.
Глава 20. МЕДИЦИНСКАЯ ЗАЩИТА ОТ ВНЕШНЕГО ОБЛУЧЕНИЯ
Данным термином обозначена система мероприятий медицинской службы, направленных на сохранение жизни, здоровья и профессиональной работоспособности личного состава войск в условиях сверхнормативного воздействия проникающей радиации ядерного взрыва, а также у- или нейтронного излучения из других внешних источников. Главным условием сохранения жизни, здоровья и профессиональной работоспособности личного состава в условиях радиационного воздействия является недопущение сверхнормативного облучения. Это достигается техническими и организационными мероприятиями, направленными на реализацию трех принципов физической защиты от ИИ: временем, расстоянием и экранированием. Медицинские средства играют в противолучевой защите личного состава вспомогательную роль: они необходимы при невозможности избежать сверхнормативного облучения.
Медицинские средства защиты применяют с профилактической или лечебной целью. Те из них, которые предназначены для профилактики последствий внешнего облучения, подразделяются на радиопротекторы, средства длительного поддержания повышенной радиорезистентности организма, средства профилактики первичной реакции на облучение и средства профилактики ранней преходящей недееспособности. Препараты, применяемые в ранние сроки (часы) после облучения с целью уменьшения его негативных последствий, называются средствами раннего (догоспитального) лечения лучевых поражений.
20.1. Радиопротекторы
К числу радиопротекторов относятся препараты или рецептуры, которые при профилактическом применении способны оказывать защитное действие, проявляющееся в сохранении жизни облученного организма или уменьшении тяжести лучевого поражения. Для радиопротекторов, в отличие от других радиозащитных средств, противолучевой эффект среди прочих проявлений фармакологической активности является основным. Радиопротекторы эффективны исключительно в условиях профилактического применения, действие их развивается в первые минуты или часы после введения, сохраняется в течение 2—6 ч и проявляется, как правило, лишь в условиях кратковременного (но не хронического или пролонгированного) облучения. О пригодности веществ к использованию в качестве радиопротекторов судят по показателям их защитной эффективности и переносимости.
20.1.1. Показатели защитной эффективности радиопротекторов
Степень повышения радиорезистентности организма при введении радиопротектора характеризуется величиной противолучевого эффекта. Простейшим ее показателем служит процент защиты — разность между выраженным в процентах количеством экспериментальных животных, выживших после облучения на фоне введения радиопротектора и без него. Более объективной характеристикой величины противолучевого эффекта является фактор изменения дозы (ФИД) или (при наличии у препарата защитного эффекта) — фактор уменьшения дозы (ФУД). Этот показатель рассчитывается как отношение средних эффективных доз ИИ на фоне применения радиопротектора и без него. Если в качестве критерия биологического эффекта используется 50% летальность, то ФИД представляет собой отношение дозы излучения, вызывающей гибель половины получивших препарат особей, к дозе того же излучения, смертельной для половины особей незащищенной группы:
^Ид _ cflso с препаратом (опыт) СДэд без препарата (контроль)
Так, СД50 при облучении крыс без фармакологической защиты составляет 6 Гр. Если же животным предварительно вводится радиопротектор (например, цистамин), то гибель половины особей наблюдается при дозе 9 Гр. В этом случае ФИД радиопротектора будет составлять 1,5 (9/6).
Действие радиопротекторов направлено прежде всего на защиту костного мозга и других кроветворных органов (с этим связано определение этой группы противолучевых средств как «миелопротекторов»). Поэтому, как правило, расчет показателей защитной эффективности осуществляют на основании данных моделирования в эксперименте костномозговой формы лучевого поражения. При введении существующих радиопротекторов человеку ожидаемая величина ФИД не превышает 1,5.
Защитную эффективность радиопротекторов характеризуют также такие показатели, как скорость развития противолучевого эффекта (интервал времени между введением радиопротектора и развитием повышенной радиорезистентности организма), длительность радиозащитного действия (продолжительность противолучевого эффекта) и переносимость.
Переносимость радиопротекторов характеризуется соотношением их токсических и рекомендуемых к практическому применению доз. Наиболее часто используется показатель «радиозащитная широта» — отношение средней смертельной дозы радиопротектора к его оптимальной радиозащитной дозе (последняя понимается как доза, обеспечивающая максимальный противолучевой эффект при отсутствии токсического). Переносимость радиопротектора существенно зависит от условий, сопутствующих его применению. Многие факторы военного труда (физическая нагрузка, лишение сна, повышенная и пониженная температура окружающей среды, психоэмоциональное напряжение, действие токсикантов, работа в защитном снаряжении) могут существенно снижать переносимость радиопротекторов, приближая их токсические дозы к радиозащитным. Поэтому среди многих тысяч веществ, проявляющих противолучевую активность, практическое значение в качестве радиопротекторов имеют лишь немногие, основные группы которых представлены в табл. 72.
Таблица 72
Группы радиопротекторов, имеющих наибольшее практическое значение
| Класс веществ | Важнейшие препараты | Ожидаемое значение ФИД | Длительность радиозащитного действия | Радиозащитная широта |
| Тиоалкиламины | Цистеамин Цистамин Гаммафос | 1,2-1,5 | 4-6 ч | 2-3 |
| Индолилалкиламины | Триптамин Серотонин Мексамин | 1,2-1,4 | 30-60 мин | 20-30 |
| Имидазолины | Индралин Нафтизин | 1,2-1,4 | 30-60 мин | 30-90 |
20.1.2. Механизмы радиозащитного действия
Согласно современным представлениям, механизмы радиозащитного действия радиопротекторов связаны с возможностью снижения косвенного (обусловленного избыточным накоплением в организме продуктов свободнорадикальных реакций: активных форм кислорода, оксидов азота, продуктов перекисного окисления липидов) поражающего действия ионизирующих излучений на критические структуры клетки — биологические мембраны и ДНК. Указанный эффект может быть достигнут:
• «фармакологическим» снижением содержания кислорода в клетке, что ослабляет выраженность «кислородного эффекта» и проявлений оксидативного стресса;
• прямым участием молекул радиопротектора в «конкуренции» с продуктами свободнорадикальных реакций за «мишени» (инактивация свободных радикалов, восстановление возбужденных и ионизированных биомолекул, стимуляция антиоксидантной системы организма и т. д.);
• торможением под влиянием радиопротектора митотической активности стволовых клеток костного мозга;
• сочетанием всех вышеперечисленных механизмов.
К препаратам, механизм радиозащитного действия которых связан преимущественно с кислородным эффектом, относятся биологически ак-
4Q4
4Q5
/пивные амины и их фармакологические агонисты (серотонин и другие ин-долилалкиламины, фенилалкиламины, мезатон, клонидин, препараты из группы производных имидазола и др.). Эти препараты вызывают гипоксию преимущественно паренхиматозных органов (и костного мозга), оказывая здесь сосудосуживающее действие. В результате напряжение кислорода вблизи внутриклеточных мишеней ИИ снижается, что сопровождается повышением радиорезистентности кроветворных клеток. Это уменьшает выраженность костномозгового синдрома, которая при дозах облучения до 10 Гр определяет исход лучевого поражения.
Активность серосодержащих радиопротекторов определяется главным образом наличием в их молекуле свободной или легко высвобождаемой SH-группы, в силу чего они способны выступать в роли «перехватчиков» свободных радикалов окислительного типа, образующихся при действии ИИ на воду и биомолекулы. Наряду с перехватом радикалов серосодержащие радиопротекторы способны непосредственно воздействовать на возбужденные молекулы биосубстрата и гасить их колебания еще до того, как их структура претерпит необратимые изменения. Обладая комплек-сообразующими свойствами, серосодержащие радиопротекторы могут также связывать ионы двухвалентных металлов (железа, меди), являющихся катализаторами перекисного окисления липидов.
Важным механизмом радиозащитного действия тиоалкиламинов является их способность снижать внутриклеточное напряжение кислорода в кроветворных клетках, стимулируя процессы его утилизации в митохондриях. При наличии значительных диффузионных барьеров между кровью и внутриклеточной средой такой метаболический эффект сопровождается увеличением трансмембранного градиента напряжения кислорода и, соответственно, снижением величины рОг во внутриклеточных компарт-ментах. То есть, в отличие от биогенных аминов, тиоалкиламины снижают оксигенацию внутриклеточных мишеней ИИ не за счет уменьшения доставки кислорода в ткани, а за счет его ускоренного расходования.
Наконец, важную роль в механизмах противолучевого действия серосодержащих радиопротекторов играет их способность временно ингиби-ровать митотическую активность клеток радиочувствительных тканей, в результате чего создаются благоприятные условия для пострадиационной репарации поврежденных в момент облучения молекул ДНК.
20.1.3. Краткая характеристика и порядок применения радиопротекторов, имеющих наибольшее практическое значение
Наиболее быстродействующими радиопротекторами являются препараты, обладающие сосудосуживающими свойствами. Одним из эффективных радиопротекторов указанной группы является индралин — производное имидазола, агонист а-адренореактивных структур организма. Индралин является радиопротектором экстренного действия. Препарат предназначен для применения в экстремальных ситуациях, сопровождающихся угрозой облучения в дозах более 1 Гр, для снижения тяжести острого лучевого поражения организма. Применялся участниками ликвидации аварии на Чернобыльской АЭС. Индралин принят на снабжение медико-санитарных частей Минздрава РФ. Препарат назначается внутрь в дозе 0,45 г (3 табл. по 0,15 г) за 10-15 мин до предполагаемого облучения. Продолжительность действия радиопротектора — около 1 ч. Противолучевой эффект индралина наиболее выражен в условиях импульсного воздействия ИИ (например, у-лучей и нейтронов ядерного взрыва).
Другим эффективным радиопротектором из группы имидазолинов является нафтизин. Препарат выпускается в виде 0,1% раствора для внутримышечных инъекций. Вводится в объеме 1 мл за 3—5 мин до предполагаемого облучения.
Из производных индола достаточно выраженным радиозащитным действием обладает мексамин (5-метокситриптамин). Радиозащитный эффект препарата развивается в течение нескольких минут, но его продолжительность невелика (40-50 мин). Мексамин принимают внутрь в дозе 50-100 мг (1-2 табл.) за 30-40 мин до предполагаемого облучения.
Радиопротекторы с сосудосуживающим механизмом действия в радиозащитных дозах редко вызывают неблагоприятные реакции организма. Однако при повышении температуры окружающей среды до 30° С и более их переносимость резко снижается. Это связано с суперпозицией двух эффектов — терморегуляторного перераспределения кровотока в ущерб тепловому «ядру» тела и сосудосуживающего действия препаратов, также проявляющегося преимущественно в тканях «ядра» тела.
Самую многочисленную группу радиопротекторов составляют серосодержащие соединения: меркаптоэтиламин, его дисульфид — цистамин, а также производные этих соединений — цистафос, гаммафос и др. Как правило, эти препараты предназначены для приема внутрь. Противолучевой эффект развивается через 30—40 мин, его продолжительность достигает 6 ч.
Цистамина дигидрохлорид (дигидрохлорид бис-(Р-аминоэтил)-дисуль-фид), белый кристаллический порошок, хорошо растворимый в воде. Препарат принимают в количестве 1,2 г (6 табл. по 0,2 г), запивая водой, но не разжевывая, за 30—60 мин до воздействия ИИ. В течение первых суток при новой угрозе облучения возможен повторный прием препарата в дозе 1,2 г через 4—6 ч после первого применения. Цистамин эффективен при угрозе кратковременного облучения в дозах, вызывающих костномозговую форму острой лучевой болезни. Побочное действие препарата проявляется нарушениями со стороны желудочно-кишечного тракта (диспептические явления в виде дискомфорта и жжения в области эпига-стрия, тошнота) и со стороны сердечно-сосудистой системы (снижение артериального давления). К противопоказаниям к применению относятся острые заболевания желудочно-кишечного тракта, острая недостаточность сердечно-сосудистой системы, нарушения функции печени.
Гаммафос (этиол, амифостин, WR-2721) представляет собой у-ами-нопропиламиноэтилтиофосфорную кислоту. Применяется при лучевой и химиотерапии онкологических больных для избирательного снижения поражения тканей, не вовлеченных в опухолевый рост. В экспериментах
на животных проявляет противолучевой эффект также в условиях, моделирующих воздействие радиационных факторов ядерного взрыва. Препарат вводят один раз в сутки внутривенно, медленно (в течение 15 мин), в дозе 340 мг/м2 поверхности тела, за 15 мин до каждого облучения. Противопоказаниями к применению гаммафоса являются артериальная гипотония, дегидратация, беременность, лактация, а также индивидуальная непереносимость. Следует отметить, что, несмотря на более выраженные чем у цистамина, противолучевые свойства, применению гаммафоса в качестве индивидуального медицинского средства защиты препятствует необходимость внутривенного введения: в полевых условиях предпочтение отдается препаратам, вводимым перорально либо внутримышечно.
Зная возможности современных радиопротекторов, необходимо учитывать и ограничения их применимости. Выше отмечалось, что противолучевое действие этих препаратов проявляется преимущественно в снижении пострадиационной смертности облученных организмов. Поэтому применение радиопротекторов при кратковременном облучении в дозах менее 1 Гр нецелесообразно, ввиду отсутствия практически значимого противолучевого эффекта в этих условиях. Малоэффективны они и при дозах облучения, соответствующих кишечной, токсемической и церебральной формам острой лучевой болезни. Так, например, противолучевое действие циста-мина не распространяется за пределы дозового интервала 1—10 Гр.
Сложной проблемой является и кумуляция токсического действия радиопротекторов при многократном их введении в организм. В течение суток радиопротекторы можно применять не более 2—3 раз, что не обеспечивает круглосуточную защиту, необходимую в условиях угрозы внезапного облучения (например, при наличии данных о вероятном применении ядерного оружия) либо в условиях пролонгированного облучения. С большой осторожностью радиопротекторы должны назначаться специалистам операторского профиля профессиональной деятельности (членам летных экипажей, водителям транспортных средств), а также при повышенной температуре воздуха (более 30° С).
20.2. Средства длительного поддержания повышенной радиорезистентности организма
Чернобыльская авария показала, что проблему защиты личного состава при пролонгированном облучении с низкой мощностью дозы невозможно решить с помощью радиопротекторов. В подобных условиях критерий радиозащитного действия — не столько снижение смертности от острой лучевой болезни (которая часто и не развивается), сколько профилактика отдаленных последствий облучения (рака, лейкоза, катаракты, сокращения продолжительности жизни). Радиопротекторы мало влияют на эти эффекты, поэтому их применение при пролонгированном облучении с низкой мощностью дозы нецелесообразно.
Для защиты личного состава, участвующего в ликвидации последствий ядерных взрывов или радиационных аварий, рекомендованы препараты из другой группы противолучевых средств — средства длительного поддержания повышенной радиорезистентности организма. Их существенным отличием от радиопротекторов является то, что радиозащитный эффект часто не является для препаратов этой группы основным, и большинство из них обладают противолучевой активностью в условиях как профилактического, так и лечебного применения. Эти препараты, как правило, не вызывают грубых изменений тканевого метаболизма и в силу этого могут применяться многократно, непрерывно и длительно.
С практической точки зрения средства длительного повышения радиорезистентности организма целесообразно разделить на две основные группы.
♦ Средства защиты от «поражающих» доз облучения, куда относятся препараты, обладающие достаточно выраженным противолучевым действием, т. е. способные предупреждать или ослаблять ближайшие последствия внешнего облучения в дозах, вызывающих ОЛБ. Если эти средства используются до облучения, т. е. профилактически, то в литературе их часто обозначают как «радиопротекторы длительного (или пролонгированного) действия».
♦ Средства защиты от «субклинических» доз облучения. В эту группу входят препараты, имеющие относительно низкую противолучевую активность, но способные снижать выраженность неблагоприятных (в том числе и отдаленных) последствий облучения в дозах, не вызывающих развития клинических проявлений лучевой патологии.
Механизм противолучевого действия средств защиты от «поражающих» доз облучения принципиально отличен от реализации эффекта радиопротекторов кратковременного действия, т. е. непосредственно не связан с первичными радиационно-химическими и биохимическими процессами в клетках. В настоящее время считается, что решающую роль в противолучевом действии этих средств играет их способность вызывать мобилизацию защитных систем организма и активизировать процессы пострадиационной репопуляции костного мозга и восстановления всей системы крови. Наряду с этим, в основе радиозащитного эффекта ряда средств защиты от «поражающих» доз облучения лежит их способность изменять гормональный фон организма. Так, спустя 1—2 сут после введения эстрогенов или их синтетических нестероидных аналогов развивается состояние гиперэстрогенизма, которое определяет длительное (до 2-3 нед) повышение общей неспецифической устойчивости организма к действию экстремальных факторов, в том числе ионизирующих излучений.
Наиболее эффективными средствами из этой группы являются гормональные препараты стероидной структуры и их аналоги и иммуномодуля-торы.
Из гормональных препаратов, обладающих противолучевыми свойствами, наиболее изучен диэтилстильбестрол (ДЭС). Повышение радиоре-
4оа
ЧД u I О II. rMMnWDflUIIVI ft Л
Глава 20. МЕДИЦИНСКАЯ ЗАЩИТА ОТ ВНЕШНЕГО ОБЛУЧЕНИЯ
зистентности организма (ФУД в пределах 1,15—1,2) происходит обычно спустя 2 сут после его введения и сохраняется в течение 1—2 нед. В механизмах радиозащитного действия ДЭС ведущую роль играет обратимое торможение пролиферативной активности клеток костного мозга, повышение уровня гранулоцитарно-макрофагального колониестимулирующе-го фактора и, как следствие, активация миелоидного и мегакариоцитар-ного ростков костного мозга. Кроме того, под влиянием эстрогенов происходит стимуляция системы мононуклеарных фагоцитов, что в свою очередь приводит к повышению резистентности облученного организма к токсемии и бактериемии. ДЭС в качестве радиопротектора пролонгированного действия назначается однократно внутрь в дозе 25 мг (1 табл.) за 2 сут до предполагаемого воздействия ионизирующего излучения. Следует помнить, что при приеме больших доз ДЭС увеличивается вероятность развития токсических поражений печени и почек, а также возможно появление признаков феминизации, связанных с эстрогенной активностью препарата.
Для исключения нежелательных побочных эффектов ДЭС среди ин-дольных аналогов синтетических нестероидных антиэстрогенов разработан и проходит клинические испытания новый радиопротектор длительного действия, получивший название индометафен. Индометафен обладает выраженным радиозащитным эффектом в условиях острого, фракционированного и пролонгированного у-облучения. Однократное пероральное применение индометафена способно повысить радиорезистентность организма на срок продолжительностью до двух недель, а противолучевое действие препарата проявляется уже через 3—6 ч после его приема.
Другим важным механизмом реализации противолучевых эффектов средств повышения радиорезистентности организма является их стимулирующее действие на факторы неспецифической защиты (в том числе противоинфекционной), гемопоэтическую и иммунную системы облученного организма. Этот механизм является основным для вакцин, полисахаридов, цитокинов, органных пептидов и других иммуномодуляторов. Кроме того, многие иммуномодуляторы вызывают обратимое ингибиро-вание синтеза ДНК в клетках, что способствует оптимизации процессов постлучевой репарации повреждений в этих уникальных биомолекулах, а также вызывают активацию детоксицирующих функций различных органов и систем организма.
Наибольшим противолучевым действием из экзогенных иммуномодуляторов отличаются вакцинные препараты из бактерий кишечно-тифозной группы, а также препараты полисахаридных, липополисахаридных и бел-ково-липополисахаридных компонентов этих микроорганизмов.
Вакцина протейная из антигенов сухая представляет собой очищенные антигенные комплексы, извлеченные из микробных клеток протея. Обладает способностью повышать устойчивость организма к воздействию ионизирующего излучения и ускорять восстановление кроветворной системы. Вакцина стимулирует фагоцитарную активность нейтрофилов, бактерицидные и защитные функции сыворотки крови. Протейную вакцину применяют профилактически (за 12—24 ч до облучения) или в качестве средства раннего (через 6—24 ч после радиационного воздействия) лечения радиационных поражений в дозе 0,2 мг в 1 мл 0,9% раствора натрия хлорида подкожно.
Среди корпускулярных микробных препаратов высокой радиозащитной эффективностью обладают также брюшнотифозная вакцина с секстаанатоксином, вакцина БЦЖ, тетравакцина, гретая вакцина из кишечной палочки, дизентерийный диантиген, противогриппозная, сибиреязвенная, тифопаратифозная вакцины и другие вакцины из живых или убитых микроорганизмов.
Другой группой экзогенных иммуномодуляторов являются экстракты, фракции и продукты жизнедеятельности различных микроорганизмов. Среди представителей этой группы высокой противолучевой активностью при профилактическом и раннем лечебном применении обладают биостим, бронховаксон, рибомунил, полисахариды маннан, леван, зимо-зан, пептидогликан, мурамилдипептид. Наиболее изученным препаратом этой группы является продигиозан.
Продигиозан — полисахарид, выделенный из «чудесной палочки» — Bacterium Prodigiosum. Активизирует факторы неспецифического (естественного) и специфического иммунитета, в частности образование эндогенного интерферона. После однократного введения создает повышенный фон радиорезистентности на срок от 4 до 7 сут. Препарат вводят внутримышечно — 1 мл 0,005% раствора за 1 сут до или в течение 0,5—6 ч после радиационного воздействия.
Имеются также данные о достаточно выраженном противолучевом действии эндогенных иммуномодуляторов — интерлейкинов, интерферо-нов, колониестимулирующих и туморонекротических факторов. К эндогенным иммуномодуляторам, обладающим высокой радиозащитной активностью, можно отнести и полисахарид полианионной структуры гепарин, продуцируемый тучными клетками. При его введении за 1 сут до облучения развивающееся состояние повышенной радиорезистентности организма сохраняется до 2—3 нед. Гепарин может также применяться в качестве средства ранней терапии радиационных поражений; наибольшая лечебная эффективность отмечается при его одно- или двукратном использовании через 1—2 сут после облучения.
Среди синтетических иммуномодуляторов в качестве потенциальных средств повышения радиорезистентности организма испытаны высокомолекулярные соединения (левамизол, дибазол, полиадениловая, поли-инозиновая кислоты, поливинилсульфат и др.) и ингибиторы синтеза простагландинов (интерлок, интрон, реаферон). Их радиозащитный эффект в большинстве случаев проявляется уже через 0,5—2 ч и сохраняется от нескольких часов до 1—2 сут.
В механизмах противолучевого действия средств защиты от «сублетальных» доз облучения важную роль играет их способность в течение достаточно длительного периода повышать так называемый «эндогенный фон радиорезистентности» (Гончаренко Е. Н., Кудряшов Ю. Б., 1980). Полагают, что препараты этой группы способны изменять соотношение «эн-
догенных радиопротекторов» (биогенные амины, небелковые тиолы и другие компоненты антиоксидантной системы, кортикостероиды) и «эндогенных радиосенсибилизаторов» (продукты перекисного окисления липидов и другие прооксиданты) в пользу «радиопротекторов». Многие средства биологической защиты (нуклеозиды, витаминно-аминокислот-ные комплексы, ноотропы) благоприятно влияют на процессы углеводного и энергетического обмена, биосинтез нуклеиновых кислот и белка в различных тканях, в том числе и радиочувствительных. Наконец, немаловажный вклад в реализацию противолучевого действия многих представителей этой группы (прежде всего, природных адаптогенов) вносит их иммунотропная активность, в частности, стимулирующее влияние на компоненты неспецифической резистентности организма — мононукле-арные и полиморфноядерные фагоциты, комплемент, интерферон, лизо-цим и др.
Средства защиты от «субклинических» доз облучения можно разделить на три основные группы: корректоры тканевого метаболизма, витамины и витаминно-аминокислотные комплексы, адаптогены растительного и животного происхождения.
Среди лекарственных препаратов — корректоров тканевого метаболизма, способностью длительно повышать радиорезистентность организма обладают производные пиримидина, аденозина и гипоксантина. Большинство из них относится к естественным метаболитам, необходимым для биосинтеза АТФ и нуклеиновых кислот, или способствуют увеличению их содержания и ускорению процессов репарации пострадиационных повреждений ДНК.
Одним из наиболее эффективных препаратов из этой группы является нуклеозид пурина рибоксин, применявшийся для повышения радиорезистентности у участников ликвидации последствий аварии на Чернобыльской АЭС. В экспериментальных и клинических исследованиях показано, что в условиях профилактического перорального или парентерального применения рибоксин не только существенно увеличивает выживаемость животных, подвергнутых кратковременному, пролонгированному или фракционированному облучению, но и снижает образование хромосомных аберраций. Это явилось основанием рекомендовать его в качестве стимулятора радиорезистентности при выполнении аварийно-спасательных и ремонтных работ в зонах с повышенным уровнем ионизирующих излучений. Препарат применяют в дозе 0,4 г (2 табл.) 2 раза в день в течение всего периода работ на местности с повышенным радиационным фоном. Курсовое применение препарата возможно в течение 1 мес.
Для предупреждения неблагоприятных последствий действия «субклинических» доз облучения можно также использовать витамины и витаминно-аминокислотные комплексы, например, амитетравит и тетрафолевит.
Амитетравит — это препарат, состоящий из аскорбиновой кислоты, рутина, тиамина, пиридоксина, а также аминокислот триптофана и гис-тидина. Прием амитетравита начинают за 5—7 сут до входа на радиоактивно зараженную местность по 3 табл. 2 раза в день после еды. Курс терапии составляет 2 нед. В перерывах между курсами амитетравита или при его отсутствии применяют тетрафолевит (по 1 табл. 3 раза в сутки после еды в течение 2 нед), который представляет собой поливитаминный препарат, в состав которого входят тиамин, рибофлавин, фолиевая кислота и никотинамид. Прием этих препаратов должен осуществляться в течение всего периода пребывания в условиях повышенного радиационного фона.
Повышение резистентности организма к Низкоинтенсивным радиационным нагрузкам может быть достигнуто также с помощью адаптогенов природного происхождения (фито- и зоопрекаратов), в основе фармакологического действия которых лежит их способность повышать неспецифическую резистентность организма. Адаптогены относятся к препаратам с относительно слабой противолучевойг активностью: при однократном облучении в поражающих дозах она невелика (ФИД не превышает 1,1). В то же время при длительных низкоинтенсивных радиационных воздействиях они позволяют улучшить самочувствие людей, повысить их работоспособность, а главное — повысить устойчивость организма к целому ряду экстремальных факторов: психоэмоциональному стрессу, физическим нагрузкам, гипо- и гипертермии, несбалансированным рационам питания, токсикантам и др.
Среди зоопрепаратов наибольшей радиозащитной активностью обладает прополис, среди адаптогенов растительного происхождения — экстракт элеутерококка и настойка женьшеня. В условиях повышенного радиационного фона прием препаратов проводится курсами в течение 14—21 сут с перерывами на 2—3 нед по 20—30 капель за 30 мин до еды ежедневно по 3 раза в сутки. Профилактическое применение адаптогенов проводится в дозах ниже лечебных: один раз в день (утром) по несколько капель настойки или экстракта.
20.3. Средства профилактики общей первичной реакции на облучение
Первичная реакция на облучение (ПРО) относится к числу наиболее ранних клинических проявлений радиационного поражения организма. В результате ее развития пострадавшие выходят из строя уже в ранние сроки после воздействия ИИ. Особенно опасны проявления ПРО в ситуациях, когда от состояния работоспособности людей зависит эффективность действий по завершению работ в зоне радиационного воздействия и скорейшему выходу из нее. В этих условиях профилактика ПРО способствует не только поддержанию боеспособности личного состава, но и косвенно — снижению доз облучения организма.
Для профилактики ПРО могут использоваться препараты, лекарственная форма которых (таблетки) позволяет применять их в порядке само- и взаимопомощи. Показано, что наибольшей эффективностью обладают препараты из группы нейролептиков, в частности этаперазин и метоклопрамид, а также комбинированные препараты на их основе (ди-меткарб).
41 а
-iai.it> н. гядииоиили! пп
Глава 20. МЕДИЦИНСКАЯ ЗАЩИТА ОТ ВНЕШНЕГО ОБЛУЧЕНИЯ
Этаперазин относится к нейролептикам из ряда фенотиазина. Механизм противорвотного действия связан с угнетением дофаминовых рецепторов триггер-зоны рвотного центра. Для профилактики рвоты этаперазин принимают внутрь по 1—2 табл. (4—8 мг) 1—2 раза в сутки, но не более 6 табл. в сутки. Профилактическое действие проявляется при дозах облучения до 6 Гр. Как и другие нейролептики, этаперазин понижает мышечный тонус и двигательную активность, а также может вызывать экстрапирамидные нарушения (лекарственный «паркинсонизм», ригидность) вследствие подавления дофаминергической системы в стриопаллидарной области мозга. Обладая дофамино-, адрено-, серотониноблокирующим действием, препарат препятствует передаче нервных импульсов из лобных долей мозга на его нижележащие структуры, что может проявляться снижением умственной и физической работоспособности. Однако при приеме в рекомендуемых дозах выраженность этих побочных эффектов существенно меньше, чем клинически сходных с ними проявлений ПРО.
Метоклопрамид (церукал, реглан) — противорвотный препарат из группы производных метоксибензамида. Является специфическим бло-катором Бг-дофаминовых рецепторов триггер-зоны рвотного центра. Обладает противорвотным действием, оказывает регулирующее влияние на двигательную активность желудочно-кишечного тракта. Быстро и полно всасывается в желудочно-кишечном тракте. Противорвотный эффект продолжается до 12 ч. Для профилактики рвоты препарат принимают по 1 табл. (10 мг) 3 раза в день. Из побочных эффектов возможны экстрапирамидные нарушения (лекарственный «паркинсонизм»), сонливость, усталость, сухость во рту.
Диметкарб — рецептура, содержащая, наряду с противорвотным компонентом, психоаналептик сиднокарб, действие которого направлено на профилактику пострадиационной астении. Диметкарб принимают по 1 табл. за 30—60 мин до предполагаемого облучения. Действие рецептуры проявляется через 20—30 мин после приема и сохраняется в течение 5—6 ч. При облучении в дозах 4—6 Гр рецептура предупреждает проявления ПРО у 40—50% пораженных и ослабляет выраженность ее проявлений у остальных. Повторный прием препарата возможен через 4—6 ч. Суточная доза не должна превышать 6 табл.
20.4. Средства профилактики ранней преходящей недееспособности
Ранняя преходящая недееспособность (РПН) — симптомокомплекс, развивающийся только при облучении организма в дозах, вызывающих церебральную форму лучевой болезни, исключающих выживание. Применение средстр, модифицирующих проявления РПН, не имеет целью изменить абсолютно неблагоприятный для индивидуума исход лучевого поражения. Профилактика РПН диктуется необходимостью сохранения контроля над системами вооружений и техники в условиях применения ядерного оружия и при радиационных авариях. При этом целью профилактических мероприятий является сохранение личным составом экипажей и боевых расчетов бое- и трудоспособности в течение нескольких часов, необходимых для выполнения боевой задачи, несмотря на облучение в потенциально смертельной дозе.
Радиопротекторы, защищающие организм от облучения в дозах, вызывающих ОЛБ в костномозговой форме, неэффективны в отношении церебрального лучевого синдрома и не предотвращают развитие его ранних проявлений — РПН. Симптоматические средства, нацеленные на подавление отдельных проявлений РПН (судорог, атаксии, гиперкинезов), не устраняют собственно недееспособности, поскольку ее непосредственной причиной служит несостоятельность энергетического обеспечения функций головного мозга.
Эффективными в отношении РПН оказались лишь средства патогенетического типа действия, разработка которых потребовала предварительного исследования механизмов этого синдрома. Установлено, что облучение в «церебральных» дозах вызывает множественные повреждения ДНК и, как следствие, гиперактивацию одного из ферментов ее репарации — аденозиндифосфорибозилтрансферазы (АДФРТ). АДФРТ катализирует реакцию полимеризации АДФ-рибозильных фрагментов НАД+. При этом внутриклеточная концентрация НАД+ снижается и уменьшается интенсивность НАД+-зависимых процессов гликолиза и клеточного дыхания. Истощение пула НАД+ происходит во всех облучаемых тканях, но в головном мозге, критически зависящем от метаболизма глюкозы и от окислительного ресинтеза АТФ, снижение активности НАД+-зависи-мых дегидрогеназ обусловливает катастрофические функциональные нарушения, клиническим эквивалентом которых как раз и является РПН-синдром.
В связи с этим были предложены два пути метаболической коррекции энергодефицитного состояния мозга при РПН. Первый путь предусматривает введение в организм ингибиторов АДФ-рибозилирования. К их числу относится ретроингибитор (конечный продукт) этого процесса — никотинамид, его структурные аналоги и их производные (бензамид, 3-аминобензамид, алкил- и ацил-аминобензамиды), а также производные пурина (аденин, кофеин, теофиллин и др.). В концентрациях 0,1—1,0 мМ эти вещества почти полностью подавляют активность АДФРТ изолированных клеток. Для достижения эффекта эти вещества должны применяться в дозах не менее 10 мг на кг массы тела. В частности, прием церебрального радиопротектора Биана рекомендован в дозе 500 мг (1 табл.), никотинамида — в дозе 500 мг (10 табл. по 0,05 мг).
С целью уменьшения интенсивности РПН рассматривается возможность использования веществ, активизирующих НАД+-независимые процессы клеточного дыхания в головном мозге. С этой целью могут быть, в частности, использованы препараты на основе янтарной кислоты.
Поскольку доза предстоящего облучения всегда неизвестна, а вызываемое ингибиторами поли-АДФ-рибозилирования нарушение пострадиационной репарации ДНК может неблагоприятно повлиять на процессы пострадиационного восстановления организма при костномозговой форме лучевого поражения, Биан, никотинамид и другие препараты этой группы должны назначаться с осторожностью и, как правило, в сочетании с радиопротекторами.
20.5. Средства раннего (догоспитального) лечения острой лучевой болезни
Раннее догоспитальное лечение ОЛБ проводится по двум направлениям: купирование проявлений первичной реакции на облучение (симптоматическая терапия) и активация процессов пострадиационной репарации и восстановления костномозгового кроветворения (ранняя патогенетическая терапия).
Купирование проявлений первичной реакции на облучение обеспечивается применением препаратов, направленных против рвоты, астении и диареи. Из средств противорвотной терапии в период ПРО могут применяться метоклопрамид, диметпрамид, латран, диксафен и некоторые нейролептики.
Фармакологические свойства метоклопрамида описаны выше. При уже развившейся рвоте препарат вводят внутримышечно или внутривенно медленно по 2 мл (10 мг). Высшая суточная доза — 40 мг.
Диметпрамид также относится к производным бензамида, механизм его противорвотного действия такой же, как у метоклопрамида. Для купирования рвоты препарат вводят внутримышечно по 1 мл 2% раствора. Высшая суточная доза — 100 мг.
Латран (зофран) — противорвотный препарат из группы селективных антагонистов 5-НТз серотониновых рецепторов нервной системы. Препарат не вызывает седативного эффекта, нарушений координации движений или снижения работоспособности. Для купирования развившейся рвоты латран применяют внутривенно в виде 0,2% раствора однократно в дозе 8—16 мг.
Рецептура диксафен (ампулы или шприц-тюбики по 1,0 мл) вводится внутримышечно при развитии пострадиационной рвоты, когда применение таблетированных форм противорвотных препаратов уже невозможно. При дозах облучения 4—6 Гр рецептура в 100% случаев снимает рвоту и адинамию, а при дозах до 10 Гр существенно ослабляет тяжесть проявлений первичной реакции. Действие диксафена проявляется через 10—15 мин после введения и сохраняется в течение 4-5 ч. В случае отсутствия эффекта допустимо повторное одно- или двукратное введение рецептуры, но не более 4 раз в сутки.
Помимо перечисленных средств для купирования лучевой рвоты могут применяться и другие нейролептики: аминазин, галоперидол, дропе-ридол и т. д.
Для купирования постлучевой диареи используют метацин, обладающий периферическим М-холинолитическим действием, превосходящим атропин и спазмолитин. Препарат вводится внутримышечно 0,5—2 мл 0,1% раствора. В крайне тяжелых случаях, сопровождающихся профуз-ным поносом и признаками обезвоживания организма, целесообразно внутривенное введение 10% раствора натрия хлорида, физиологического раствора, 5% раствора глюкозы.
Средства ранней патогенетической терапии назначаются в первые часы—сутки после облучения. Их действие направлено на активацию процессов постлучевой репарации в системе костномозгового кровообращения и стимуляцию пролиферативной активности стволовых кроветворных клеток, в результате чего происходит более быстрое восстановление костномозгового кровообращения и, как следствие, повышается выживаемость облученных организмов. К средствам ранней патогенетической терапии относятся дезинтоксикационные средства и методы, препараты с преимущественным действием на иммунную систему (иммуно-модуляторы), адаптогены и стимуляторы регенерации.
Наиболее эффективным патогенетически обоснованным подходом к ранней терапии ОЛБ является ранняя детоксикация. Процедура предусматривает иммобилизацию радиотоксинов, их разбавление и ускоренную элиминацию. С этой целью в условиях клиники рекомендуют применять плазмозамещающие препараты (гемодез, аминодез, глюконеодез, поливисолин, полиглюкин, изотонический раствор натрия хлорида и др.) и методы экстракорпоральной сорбционной детоксикации (гемосорбция, плазмаферез, лимфосорбция).
В качестве средств медицинской защиты в первые часы после облучения весьма перспективно использование средств детоксикации перо-рального применения — неселективных энтеросорбентов. Показано, что угольный сорбент ВУГС, полиметилсилокеан и другие энтеросорбенты существенно уменьшают выраженность пострадиационных нарушений функций кишечника, ускоряют выведение из организма токсических веществ гистиогенного и бактериального происхождения, повышая в итоге выживаемость облученных животных.
Активация процессов пострадиационной репарации и восстановления костномозгового кроветворения обеспечивается также ранним применением стимуляторов регенерации (дезоксинат, рибоксин), иммуномо-дуляторов (вакцина протейная из антигенов сухая, продигиозан, гепарин) и адаптогенов. Свойства иммуномодуляторов и адаптогенов описаны выше.
Дезоксинат (деринат) представляет собой натриевую соль ДНК, полученную из молок осетровых рыб. Препарат выпускается в виде 0,5% раствора в ампулах по 5 и 10 мл. В качестве средства ранней терапии ОЛБ дезоксинат применяется не позднее 24 ч после облучения: вводится однократно внутримышечно или подкожно в объеме 15 мл (75 мг активного вещества).
Глава 21.
МЕСТНЫЕ ЛУЧЕВЫЕ ПОРАЖЕНИЯ
Местные лучевые поражения, возникающие в результате локального или неравномерного внешнего радиационного воздействия, встречаются значительно чаще, чем острая лучевая болезнь от внешнего относительно равномерного облучения. Кроме того, около половины всех случаев острой лучевой болезни сопровождается тяжелыми местными лучевыми поражениями, что обусловлено крайне неравномерным распределением поглощенной дозы по телу человека.
21.1. Местные лучевые поражения кожи
Одной из наиболее распространенных форм местных радиационных поражений при внешнем облучении являются лучевые дерматиты. Они развиваются в результате неравномерного радиационного воздействия при взрывах ядерных боеприпасов и при авариях на атомных энергетических установках, а в повседневных условиях могут быть следствием рентгено-или у-терапии опухолей и неопухолевых заболеваний. Наиболее частой локализацией местных лучевых поражений кожи являются лицо, кисти рук (пальцы) и передняя поверхность бедер.
Для правильного понимания радиобиологических эффектов, проявляющихся при лучевых дерматитах, необходимо знать, что нормальная кожа состоит из эпидермиса, который представляет собой типичный пример системы клеточного самообновления, и собственно дермы. Кровь к эпидермису не подходит, его питание осуществляется за счет диффузии кислорода и питательных веществ из капилляров, расположенных в нижележащей дерме. Толщина кожи в среднем составляет 2 мм, эпидермиса — 0,1 мм, дермы — 1,9 мм.
Эпидермис состоит из пяти слоев клеток, каждый из которых представляет собой определенную стадию дифференцировки эпителиальных элементов. В порядке физиологической смены эпителиальных клеток в эпидермисе различают: базальный (или зародышевый) слой, слой шиповатых клеток, слой зернистых клеток, элеидиновый (или блестящий) слой, роговой слой. Полный цикл обновления клеток эпидермиса составляет, в зависимости от локализации, от 4-5 до 14-20 сут. Основная масса стволовых клеток кожи (и около 70% всех пролиферирующих клеток) расположена в базальном слое эпидермиса на глубине чуть менее 200 мкм от поверхности кожи. По мере размножения и созревания клетки эпидермиса поднимаются от базального слоя к поверхности кожи, формируя роговой слой. Роговой слой составляет примерно четвертую часть толщины эпидермиса. Его толщина в разных участках кожи колеблется от 10 до 20 мкм, а наибольшей толщины (до 200 мкм) он достигает в эпидермисе ладоней и подошв.
Различают ранние и поздние проявления лучевых дерматитов. Ранние лучевые дерматиты (лучевые ожоги кожи) проявляются в первые несколько суток после облучения в виде так называемой первичной эритемы, сменяющейся после латентного периода сухим, влажным (буллезным) или язвенно-некротическим дерматитом. Поздние проявления развиваются спустя несколько месяцев после облучения как следствие поражения сосудов кожи и соединительной ткани. Для них наиболее характерно нарушение трофики кожи, дермофиброз, язвенно-некротические процессы, симптомы атрофического или гипертрофического дерматита.
Ранние эффекты местных радиационных поражений связаны в основном с повреждением эпидермиса, поздние — с повреждением дермы и подлежащих слоев кожи. В эпидермисе наиболее чувствительными являются стволовые клетки, находящиеся в базальном слое: их Do составляет 1,35 Гр. По способности к пострадиационной репарации стволовые клетки кожи занимают промежуточное положение между полипотентными клетками кроветворной системы и клетками крипт кишечника (Dq = 2,0—2,5 Гр). Созревающие и функциональные клетки эпидермиса, фиб-робласты, мышечные и нервные клетки дермы более радиорезистентны и практически не повреждаются при облучении в дозах, вызывающих острое лучевое поражение кожи. Таким образом, критическими структурами кожи при облучении являются стволовые клетки базального слоя эпидермиса и эпителия вокруг придатков кожи.
В механизмах развития ранних лучевых поражений кожи большое значение имеет индуцированное облучением блокирование деления стволовых клеток базального слоя эпидермиса. Так, при облучении кожи в дозах 15—25 Гр деление стволовых клеток блокируется на срок до 10—15 сут. Как следствие этого процесса, прекращается поступление новых клеток из базального слоя в слой шиповатых клеток. Поскольку продвижение созревающих и функционирующих клеток и их физиологическая потеря с поверхности кожи продолжаются после облучения с прежней скоростью, то по мере того как число стволовых клеток падает, эпидермис отслаивается и оголяется дерма.
При облучении в высоких дозах имеет место и прямая (как митоти-ческая, так и интерфазная) гибель базальных клеток и клеток вышележащих слоев кожи. Вследствие этого при глубоких лучевых ожогах некротические и дегенеративные процессы охватывают все слои кожи, распространяясь постепенно на глубжележащие ткани, вплоть до костных.
В генезе поздних радиационных поражений кожи, развивающихся через месяцы-годы после облучения, помимо повреждения стволовых клеток базального слоя эпидермиса, существенную роль играет поражение эндотелия сосудов кожи. На пораженных участках наблюдается прогрессирующая облитерация капилляров, развитие атрофической аваскулярной неэластичной дермы, неспособной питать лежащий поверх нее эпидермис, что в свою очередь приводит к его атрофии, изъязвлению и некрозу.
Говоря о факторах, влияющих на степень тяжести местного лучевого поражения, следует отметить, что лучевой ожог протекает тем тяжелее, чем выше поглощенная доза и ее мощность, чем больше площадь и глубина облученных тканей. Характер поражений зависит и от их локализация (табл. 73).
Таблица 73
Сроки выявления основных клинических проявлений местных лучевых поражений кожи в зависимости от вида радиационного воздействия, площади поражения и величины локальной поглощенной дозы (по Селидовкину Г. Д., Барабановой А. В., 2001)
| Вид облучения | Локальная поглощенная доза, Гр | Латентный период, сут | Клиника разгара (сроки максимальных проявлений, сут) | Исход |
| Гамма-облучение | 10-15* 12-18* | 20-22 18-20 | Эритема, сухое шелушение (36-40) | Восстановление в 100% случаев |
| 15-20* 18-30" | 18-20 15-18 | Пузыри, влажная десквамация (30-36) | Восстановление с явлениями атрофии | |
| 20-30* 30-50** | 15-18 10-15 | Эрозии, язвы, некроз (24-30) | Восстановление редко и только при малой площади поражения | |
| Более 50*** | 5-10 | Ранний некроз (15-24) | Отсутствие восстановления | |
| Гамма-нейтронное облучение | 8-10* 8-12" | 18-22 15-20 | Эритема, сухая десквамация (4(М4) | Восстановление в 70-80% случаев |
| 10-15* 12-18" | 15-18 10-15 | Пузыри, «влажное» шелушение (32-40) | Восстановление с выраженными дефектами | |
| 15-25* 18-30" | 10-15 7-10 | Эрозии, язвы (26-32) | Восстановления нет | |
| Более 30"* | 5-7 | Ранний некроз (ранее 8) |
* Площадь поражения более 150 см2 (более «одной ладони»). •* Площадь поражения до 150 см2 (менее «одной ладони»). '* Размеры поражения на клинические проявления не влияют.
Определяющее влияние на глубину, а следовательно, и степень тяжести лучевого ожога оказывает и проникающая способность ионизирующего излучения. Так, а-частицы проникают в кожу на несколько десятков микрон и почти полностью поглощаются в роговом слое. (З-Из-лучение проникает в ткань гораздо глубже — до 2-4 мм, в результате чего значительная доля энергии р-частиц поглощается в базальном слое эпидермиса, сальными и потовыми железами, кровеносными сосудами и другими образованиями поверхностного слоя дермы. Наконец, у-, рентгеновское и нейтронное излучения, обладающие высокой проникающей способностью, поражают кожу на всю ее глубину.
В соответствии с современной классификацией лучевые ожоги кожи подразделяются на 4 степени тяжести. Ожог I степени характеризуется легкой воспалительной реакцией кожи. При ожоге II степени происходит частичная гибель эпидермиса, который отслаивается с образованием тонкостенных пузырей, содержащих прозрачный желтоватый экссудат. Эпи-телизация происходит за счет регенерации сохранивших жизнеспособность глубоких слоев эпидермиса. При ожоге IIIA степени погибает не только эпидермис, но, частично, и дерма. Эпителизация обеспечивается, главным образом, дериватами кожи (волосяные фолликулы, сальные и потовые железы), сохранившими жизнеспособность в глубоких слоях дермы. На месте заживших ожогов могут сформироваться глубокие рубцы, в том числе — келоидные. Ожог ШВ степени приводит к гибели всех слоев кожи, а нередко и подкожно-жировой клетчатки. Возможно самостоятельное заживление лишь небольших ожогов за счет рубцевания и краевой эпителизации. Наконец, ожог IV степени вызывает омертвение не только кожи, но и анатомических образований, расположенных глубже собственной фасции — мышц, сухожилий, костей, суставов. Самостоятельное заживление таких ожогов невозможно.
Ожоги I, II и IIIA степени являются поверхностными и обычно заживают самостоятельно при консервативном лечении. Ожоги ШВ и IV степени относятся к глубоким и требуют оперативного восстановления кожного покрова.
В клиническом течении местных лучевых поражений прослеживается определенная фазность, позволяющая выделить следующие стадии поражения:
• первичная эритема,
• скрытый период,
• период разгара,
• период разрешения процесса,
• период последствий ожога.
Острый лучевой дерматит I степени тяжести (эритематозный дерматит) развивается после у-облучения в дозах 8—12 Гр. Первичная эритема длится несколько часов, выражена слабо. Латентный период составляет 2—3 нед. Острый период проявляется развитием вторичной эритемы, имеющей темно-красный или розово-лиловый цвет, отеком кожи, чувством жара, зуда, болевыми ощущениями в пораженной области. Эритема проходит через 1—2 нед, шелушение и депигментация кожи сохраняются довольно продолжительное время.
Облучение в дозах 12—30 Гр вызывает лучевой ожог II степени тяжести (экссудативная или буллезная форма дерматита, влажный эпидер-мит). Первичная эритема сохраняется от нескольких часов до 2—3 сут, скрытый период составляет 10—15 сут. Период разгара начинается с появления вторичной эритемы, отека кожи и подкожной клетчатки, чувства жжения, зуда, боли, признаков общей интоксикации, лихорадки. В отеч-
ной коже появляются пузыри, после вскрытия которых образуются эрозии и поверхностные язвы, заживающие в течение 2-3 нед за счет сохранившихся клеток базального слоя. Продолжительность заболевания составляет 1-2 мес, обширные ожоги (более 20-40% площади кожи), как правило, несовместимы с жизнью.
При воздействии ионизирующих излучений в дозах 30-50 Гр развивается местное лучевое поражение III степени тяжести (язвенный дерматит). Первичная эритема возникает в ближайшие часы после облучения и продолжается от 3 до 6 сут, сопровождается отеком кожи и подкожной клетчатки, чувством напряжения и онемения в пораженной области, признаками общей интоксикации (слабость, анорексия, сухость во рту, тошнота, головная боль). Скрытый период короткий (1-2 нед) или вовсе отсутствует. Период разгара начинается с гиперемии, вначале яркой, затем багрово-синюшной. Развивается отек пораженных участков кожи, образуются пузыри, затем эрозии и язвы, глубоко проникающие в подкожную клетчатку и быстро осложняющиеся гнойными процессами. Отмечаются лихорадка, регионарный лимфаденит, выраженный болевой синдром. Заживление затягивается на несколько месяцев, характеризуется рецидивирующим течением (вторичными изъязвлениями), трофическими дегенеративными и склеротическими изменениями кожи.
Наконец, при облучении в дозах 50 Гр и выше возникают лучевые ожоги крайне тяжелой (IV) степени с явлениями некроза. Ярко выраженная первичная эритема без скрытого периода переходит в разгар заболевания, проявляющийся отеком кожи, кровоизлияниями и очагами некроза в пораженных участках, развитием выраженного болевого синдрома, быстрым присоединением вторичной инфекции, нарастанием общей интоксикации организма. При очень тяжелых у-поражениях кожи (50-100 Гр и выше) уже с конца 1-х сут развивается так называемая «парадоксальная ишемия»: кожа, подкожно-жировая клетчатка, мышцы образуют единый плотный конгломерат, обескровленная кожа становится белой. Через 3-4 сут кожа над очагом поражения становится черной — развивается сухой коагуляционный некроз.
Во всех случаях тяжелых и крайне тяжелых местных поражений отмечается сопутствующие симптомы ожоговой болезни (интоксикация, плазморея, потеря белков и электролитов, дегидратация, тромбоцитопе-ния и анемия, эндоперибронхит и другие инфекционные осложнения). Лихорадочно-токсический синдром часто осложняется почечно-пече-ночной недостаточностью и энцефалопатической комой, приводящими к гибели, и лишь своевременная радикальная операция может спасти пострадавшего. В более благоприятных ситуациях заживление ожога затягивается на длительный срок (более 6-8 мес), возникает деформация тканей, резкая атрофия, расстройства местного кровообращения, контрактуры суставов. Атрофические и склеротические изменения затрагивают не только кожу, но и подлежащие ткани, расстройства периферического крово- и лимфообращения часто приводят к индуративному отеку и образованию вторичных лучевых язв. Поздняя симптоматика включает также лучевой фиброз и (спустя 8-10 лет) образование различных опухолей.
21.2. Местные лучевые поражения слизистых оболочек
В условиях внешнего у- или у-нейтронного облучения высокой мощности дозы наряду с лучевыми реакциями кожи могут наблюдаться и радиационные поражения слизистых оболочек (мукозиты, лучевые эпителииты). Наибольшей радиочувствительностью среди слизистых оболочек отличаются неороговевающий эпителий мягкого неба и небных дужек. Его радиационное поражение получило специальное наименование — лучевой орофарингеальный синдром. Он проявляется в виде гиперемии, отека, очагового и сливного эпителиита, нарушений слюноотделения (ксеросто-мия), болей при глотании и прохождении пищи по пищеводу, а при облучении гортани — явлений ларингита.
Пороговой для развития лучевого орофарингеального синдрома считается доза 5-7 Гр. Спустя 4-8 ч после облучения можно обнаружить преходящую сосудистую реакцию слизистых оболочек ротоносоглотки, проявляющуюся в виде покраснения, отека, опалесценции, появления отпечатков зубов.
При облучении в дозах порядка 10 Гр и выше после латентного периода развиваются поражения слизистых оболочек ротоносоглотки различной степени тяжести.
При орофарингеальном синдроме I степени тяжести период разгара наступает спустя 2 нед после облучения. Он проявляется в виде застойной гиперемии с синевато-синюшным оттенком, отечности и мелких единичных эрозий на слизистой оболочке мягкого неба и небных дужек. Нормализация состояния слизистых оболочек наступает в течение 2 нед.
Основные проявления орофарингеального синдрома II степени тяжести возникают через 1-2 нед, когда появляются многочисленные, иногда с геморрагиями, эрозии слизистой оболочки щек, мягкого неба, подъязычной области, осложняющиеся, как правило, вторичной инфекцией и региональным лимфаденитом. Длительность процесса занимает около 3 нед, и завершается он полным восстановлением слизистых оболочек, хотя эрозии могут возникать и повторно с последующей полной репарацией.
При орофарингеальном синдроме III степени тяжести латентный период длится около 1 нед. В период разгара на всех участках слизистой оболочки полости рта возникают довольно крупные множественные язвы и эрозии, покрытые некротическим налетом. Эрозивно-язвенный процесс сопровождается весьма выраженным болевым синдромом, имеет рецидивирующий характер и, как правило, осложняется бактериально-грибковой и вирусной (чаще всего герпетической) инфекцией. Длительность его составляет более 1 мес, а после регенерации слизистых оболочек на местах бывших глубоких язв остаются рубцы.
При крайне тяжелой (IV) степени орофарингеального синдрома после некоторого ослабления первичной гиперемии на 4—6-е сут она вновь рецидивирует: слизистая оболочка становится синюшной, с белыми налетами, отекает. Вскоре развиваются обширные язвенно-некротические поражения, распространяющиеся на подслизистый слой и глубже, язвы инфицируются, возникают местные геморрагии, отмечается выраженный болевой синдром. Течение процесса весьма длительное (около 1,5 мес) и часто рецидивирующее. Полной репарации слизистых оболочек не Hacfy-пает: слизистая оболочка остается истонченной, сухой, с множественными легко ранимыми рубцами.
После облучения области ротоносоглотки в дозах более 15 Гр почти в половине случаев орофарингеальный синдром может явиться непосредственной причиной летального исхода.
21.3. Особенности местных лучевых поражений в результате наружного заражения кожных покровов р адионуклидами
При ядерных взрывах и авариях (разрушениях) на объектах атомной энергетики происходит радиоактивное загрязнение местности (см. выше). По мере выпадения радиоактивных частиц на местность нарастает дистанционное воздействие у-излучения на личный состав, находящийся на загрязненной территории. В этом случае источник излучения имеет как бы объемный характер и излучение воздействует на человека со всех сторон относительно равномерно. От воздействия же р-излучения, характеризующегося существенно меньшей проникающей способностью, в первую очередь будут страдать открытые участки тела. В случае скопления радиоактивной пыли у воротника, поясного ремня, в сапогах за счет р-частиц высокой энергии (до 2—5 МэВ) могут поражаться и кожные покровы под обмундированием. В связи с этим, одной из отличительных особенностей р-лучевых ожогов кожи является весьма пестрая топография поражений, обусловленная неравномерностью загрязнения поверхности тела радионуклидами.
По сравнению с у- и у-нейтронным излучением р-излучение вызывает более легкие, как правило, поверхностные, местные поражения. Даже если р-ожоги протекают в буллезной или некротической форме (лучевые ожоги II и III степени тяжести), а по распространенности превышают 80% поверхности тела, сами по себе они не могут вызвать летального исхода у пострадавшего. Наряду с низкой проникающей способностью р-излучений, еще одной важной причиной относительно благоприятного течения лучевых ожогов кожи от наружного заражения является то, что клинически они всегда проявляются разновременно: к тому времени, когда ожог возникает на частично экранированных или закрытых участках тела, на открытых поверхностях он уже проходит обратное развитие.
На участках кожи, где доза р-облучения составила 12—30 Гр, к концу 3-й нед возникает застойная гиперемия, сменяющаяся сухой десквамацией, нарушением пигментации. Заживление наступает спустя 1,5—2 мес.
Дозы р-облучения свыше 30 Гр вызывают развитие первичной эритемы, проходящей обычно через 2—3 дня. Вторичная эритема появляется, в зависимости от дозы воздействия, через 1—3 нед (чем выше доза, тем быстрее). На ее фоне вскоре развивается отек кожи, образуются мелкие, быстро разрушающиеся пузыри. Клинические проявления поражения сохраняются 2—3 мес, а нарушения пигментации и слущивание эпидермиса могут наблюдаться и более длительное время.
На участках кожи, на которых аппликация р-излучающих радионуклидов была наиболее продолжительной, а поглощенные кожей дозы р-облучения достигали 100—150 Гр, обычно обнаруживаются очаги язвенно-некротических изменений. Выраженные проявления патологического процесса в таких случаях развиваются на 7—14-й день от момента аппликации радиоактивных веществ, заживление затягивается на срок, превышающий 3 мес, а на месте язв остаются мелкие рубцы, напоминающие оспенные дефекты кожи.
Следует также отметить, что для ожогов, вызванных аппликацией р-излучающих радионуклидов, не характерно развитие поздних лучевых поражений кожи. Исключение составляют лишь случаи, когда лучевой ожог располагается на анатомически неблагоприятных областях (кожные складки или переходные участки от кожи к слизистым оболочкам) или осложняется инфекционным процессом.
У ликвидаторов последствий аварии на Чернобыльской АЭС, подвергшихся воздействию р-излучения в дозах на уровне базального слоя эпидермиса порядка 9—12 Гр (кожа лица) и 12—30 Гр (другие участки тела), наблюдались только эритема и сухая десквамация, не требующие специального лечения. р-Облучение в дозах 30—60 Гр вызывало образование мелких пузырей, слущивание эпидермиса, а при воздействии более высоких доз отмечалась влажная десквамация. Эти проявления требовали соответствующего лечения, особенно при локализации ожогов на лице и областях кожных складок.
В случае невозможности укрытия в фортификационных сооружениях, блиндажах, технике и т. п. для предотвращения наружного радиоактивного заражения необходимо использовать средства защиты кожи фильтрующего или изолирующего типа. Весьма эффективной мерой профилактики лучевых поражений, вызванных аппликацией радиоактивных веществ, является проведение частичной или полной санитарной обработки. В случае формирования местных радиационных поражений необходимо проведение комплекса лечебных мероприятий, включающих применение средств и методов, направленных на ограничение некротического процесса, ослабление воспалительной реакции, улучшение кровообращения и микроциркуляции в пораженных тканях, профилактику и лечение раневой инфекции, борьбу с болевым синдромом, дезинтоксикационную терапию, стимуляции процессов эпителизации, профилактику фибрози-Рования тканей.
Глава 22. ПОРАЖЕНИЯ В РЕЗУЛЬТАТЕ ВНУТРЕННЕГО РАДИОАКТИВНОГО ЗАРАЖЕНИЯ
22.1. Кинетика радионуклидов
в организме £
22.1.1. Поступление радионуклидов в организм
Во внутреннюю среду радиоактивные вещества (РВ) могут попасть ин-галяционно, через стенки желудочно-кишечного тракта, через травматические и ожоговые повреждения, через неповрежденную кожу. Всосавшиеся РВ через лимфу и кровь могут попасть в ткани и органы, фиксироваться в них, проникнуть внутрь клеток и связаться с внутриклеточными структурами.
Знание пути поступления радионуклида в организм весьма важно в практическом отношении. У ряда РВ характер всасывания, распределение по органам и тканям, выведение и биологическое действие существенно зависят от пути поступления.
Ингаляционное поступление радиоактивных веществ
При контакте, особенно профессиональном, с аэрозолями РВ, радиоактивными газами и парами ингаляционный путь заражения является основным.
Около 25% попавших в органы дыхания частиц радионуклидов в чистом виде, а также входящих в состав определенных химических соединений, выдыхается. Если оставшиеся после выдоха РВ принять за 100%, то 50% из них подвергаются ретроградному выносу со слизью в результате деятельности мерцательного эпителия в глотку с последующим заглатыванием (отчасти, отхаркиванием). Около 25% резорбируются в кровь через альвеолярные мембраны. Резорбции подвергаются по преимуществу растворимые частицы. Степень резорбции одного и того же радионуклида в значительной степени зависит от химической формулы соединения, в состав которого он входит. Приблизительно 25% частиц фагоцитируются макрофагами. Это нерастворимые частицы и коллоидные формы радионуклидов. Часть захвативших их фагоцитов возвращается в глотку и заглатывается или отхаркивается. Таким путем удаляется около 15% радионуклидов. Фагоциты, захватившие оставшиеся 10% радиоактивных веществ, перемещаются через альвеолярную мембрану.
Небольшая часть РВ задерживается в паренхиме легких, эпителиальных клетках с периодом полувыведения из них около 600 сут. Еще прочнее фиксация РВ в бронхолегочных лимфатических узлах, куда они попадают с фагоцитами. Наибольшее практическое значение этот вид отложения имеет при ингаляционном поступлении нерастворимых или слабо растворимых соединений плутония, тория и некоторых других элементов.
В случае ингаляции продуктов наземных или подземных ядерных взрывов, которые в основном прочно связаны с крупными частицами носителей, доля радионуклидов, удаляемых из органов дыхания и поступающих в желудочно-кишечный тракт, существенно выше. По некоторым данным, до 80—90% таких РВ при ингаляционном поступлении уже через несколько часов оказываются в желудке.
При оценке опасности ингаляционного поступления РВ учитывают лучевую нагрузку на легкие, эпителий бронхов, регионарные лимфатические узлы, на стенку желудочно-кишечного тракта, последствия резорбции, а в случае ингаляции у-излучающих радионуклидов некоторое значение может иметь и облучение других органов грудной полости.
Поступление радиоактивных веществ через желудочно-кишечный тракт
Желудочно-кишечный тракт — второй основной путь поступления РВ в организм. Поражающее действие связано в этом варианте заражения как с лучевой нагрузкой на стенку пищеварительного тракта, так и с всасыванием РВ в кровь и лимфу. Резорбция РВ зависит от химических свойств вещества (главным образом растворимости), физиологического состояния желудочно-кишечного тракта (рН среды, моторная функция), состава пищевого рациона. Резорбция радионуклидов снижается при увеличении содержания в пище стабильных изотопов этих же элементов и наоборот.
Всасывание хорошо растворимых радионуклидов происходит в основном в тонкой кишке. Значительно меньше РВ всасывается в желудке. Всасывание в толстой кишке практического значения не имеет. Наиболее интенсивно и полно резорбируются растворимые радионуклиды, находящиеся в ионной форме. Радионуклиды щелочных металлов и галоидов после попадания в желудочно-кишечный тракт практически полностью всасываются в кровь. Изотопы редкоземельных элементов, плутония, трансурановых элементов вследствие склонности их солей к гидролизу и образованию труднорастворимых и нерастворимых соединений резорбируются в кишке в пределах нескольких сотых-десятитысячных долей процента от поступившего количества. Величины коэффициентов резорбции РВ в желудочно-кишечном тракте можно найти в справочных таблицах.
Нерастворимые и мало растворимые у-излучатели облучают кишечник и другие органы брюшной полости, а р-излучатели — только слизистую оболочку кишки, в основном до выведения их с калом, в течение примерно 30 ч. Однако в криптах кишечника РВ могут задерживаться в течение длительного времени, формируя высокие локальные дозы.
Все сказанное относится и к радионуклидам, вторично попавшим в органы пищеварения после ингаляции.
Поступление радиоактивных веществ
через неповрежденную кожу, раневые и ожоговые поверхности
Большинство радиоактивных веществ практически не проникают через неповрежденную кожу. Исключение составляют окись трития, йод, нитрат и фторид уранила, а также полоний. Коэффициенты резорбции в этих случаях составляют сотые и тысячные доли единицы.
Проникновение РВ через кожные покровы зависит от плотности загрязнения, от площади загрязненного участка, от физико-химических свойств самого элемента или соединения, в состав которого он входит, растворимости в воде и липидах, рН среды, от физиологического состояния кожи. Всасывание радионуклидов повышается при повышении температуры среды вследствие расширения кровеносных и лимфатических сосудов, раскрытия сальных и потовых желез.
Всасывание с поверхности раны труднорастворимых РВ (это, в частности, относится и к продуктам наземного ядерного взрыва) происходит медленнее и в значительно меньшем количестве, но все же в сотни раз интенсивнее, чем через интактную кожу. С поверхности ожогов I—II степеней продукты ядерного взрыва всасываются всего в 2—10 раз быстрее, чем через здоровую кожу. Проявление общего действия резорбированных с раневых и ожоговых поверхностей продуктов ядерного взрыва маловероятно. Лишь в редких случаях возможно поступление через раны значительных количеств редкоземельных элементов.
Следует считаться с воздействием испускаемого радиоактивными веществами излучения на течение раневого процесса. При поступлении в рану большого количества плохо резорбирующихся радионуклидов под влиянием облучения в клетках тканей раневой поверхности развиваются дегенеративные и некротические процессы, снижается способность клеток к размножению. В ранах часто развиваются гнойные, иногда анаэробные процессы. Медленно отторгаются некротизированные ткани, замедляется регенерация.
Большое практическое значение имеет радиоактивное загрязнение ран в производственных и лабораторных условиях. Основную опасность в случае производственного заражения представляет резорбция высокотоксичных радионуклидов, таких как, например, полоний, которая у растворимых РВ может достигать десятков процентов от общего количества, поступившего в рану. Опасные количества РВ могут поступить не только через колотые или резаные раны, но и через небольшие царапины и ссадины. Всасывание через них щелочных, щелочноземельных элементов и галоидов в 100—200 раз превышает резорбцию через неповрежденную кожу.
Резорбция плохо растворимых соединений РВ происходит в основном по лимфатическим путям, в результате чего радионуклиды накапливаются в лимфатических узлах. Некоторая часть радионуклидов из лимфатических узлов поступает с фагоцитами в органы ретикулоэндотелиальной системы.
В месте нахождения радионуклида в плохо растворимой форме могут возникнуть опухоли (чаще остеогенные саркомы).
22.1.2. Судьба радионуклидов, проникших в кровь
В крови радионуклиды могут находиться в свободном состоянии или в составе различного рода химических соединений и комплексов. Многие радионуклиды связываются протеинами. Часть РВ, попавших в кровь, сразу выводится из организма, другие проникают в различные органы и депонируются в них. Многие радионуклиды обладают определенным сродством к некоторым тканям и органам, откладываются в них, обеспечивая преимущественное их облучение. Органы, в которых преимущественно накапливается тот или иной радионуклид, получили наименование «критических» при заражении этим радионуклидом. Знание характера распределения, особенностей обмена и депонирования РВ, возможного перераспределения со временем необходимо для предвидения преимущественного поражения того или другого органа, дозы облучения этого критического органа, предсказания клинических проявлений и исхода поражения.
Концентрация РВ в органе после однократного поступления постепенно снижается, что зависит от радиоактивного распада изотопа и его биологического выведения. Время, за которое из органа выводится половина содержавшегося в нем количества радионуклида, получило наименование периода биологического полувыведения (ТбИОЛ.)- Важное практическое значение имеет знание эффективного периода полувыведения (ТЭфф.) — показателя, учитывающего уменьшение содержания радионуклида в органе за счет совместного влияния радиоактивного распада (ТфИ3.) и биологического выведения.
Тэфф. — Тфиз .'Тбиол70"фИз. + Тбиоп.)-
Бывает, что после одноразового сравнительно массивного радиоактивного заражения поступление РВ в организм не прекращается полностью, а продолжается длительное время, но в меньших количествах. В этих случаях могут преобладать (в зависимости от уровня поступления) либо процессы депонирования в органе, либо процессы выведения из него.
22.1.3. Выведение радионуклидов из организма
Попавшие в организм РВ могут выводиться через почки, желудочно-кишечный тракт (в том числе с желчью), со слюной, молоком, потом, через
легкие. В большинстве случаев основные количества радиоактивных веществ экскретируются с калом и мочой.
С калом преимущественно выводятся РВ, поступившие алиментарным путем, а также при ингаляционном заражении и вторичном заглатывании частиц, вынесенных ретроградно в глотку. Некоторые растворимые радионуклиды могут выделяться с желчью и другими пищеварительными соками и также выводиться с калом. В желудочно-кишечном тракте процессы экскреции РВ постоянно сопровождаются процессами их реабсорбции.
При выведении радионуклидов преимущественно с мочой, высокая доза облучения может быть получена почками.
Выведение с выдыхаемым воздухом имеет существенное значение для трития, радона и торона, образующихся при распаде поступивших в организм радия и тория.
Динамика выведения РВ из организма описывается таким же образом, как и при характеристике скорости уменьшения концентрации радионуклидов в отдельных органах. По содержанию РВ в выделениях можно судить о количестве их в организме как на момент определения, так и на момент поступления.
Таким образом, в кинетике поступивших в организм радионуклидов можно выделить 4 этапа:
1) образование на месте поступления первичного депо (кожа, раны, слизистые оболочки желудочно-кишечного тракта, верхних дыхательных путей);
2) всасывание с мест поступления в кровь или лимфу;
3) инкорпорирование в критическом органе (образование вторичных депо);
4) выведение различными путями, в том числе и с явлениями рециркуляции.
Продолжительность перечисленных этапов существенно различается для различных радионуклидов, их соединений, путей поступления.
22.2. Биологическое действие радиоактивных веществ
22.2.1» Влияние на развитие поражения особенностей распределения инкорпорированных радионуклидов
Специфика биологического действия отдельных радионуклидов (отличительные черты поражения, основные патогенетические механизмы его развития, причины смерти) определяется в первую очередь поражением определенных (критических) органов, нарушение жизнедеятельности которых может проявиться относительно рано, когда общие реакции и изменения в других системах выражены значительно слабее или могут вовсе отсутствовать.
При внутреннем радиоактивном заражении концепция критического органа представляется сложнее, чем при общем внешнем облучении. В этом случае имеют значение, прежде всего, особенности распределения радионуклидов по органам и тканям (тропность радионуклидов), величины пороговых повреждающих доз для разных тканей, значение функционирования органа, по отношению к которому имеется повышенная тропность радионуклида, для жизнедеятельности организма.
По способности преимущественно накапливаться в тех или иных органах выделяют следующие основные группы радиоактивных элементов.
♦ Радионуклиды, избирательно откладывающиеся в костях («остео-тропные»). Это щелочноземельные элементы: радий, стронций, барий, кальций. Остеотропность проявляют некоторые соединения плутония. Поражения, развивающиеся при поступлении в организм остеотропных радионуклидов, характеризуются изменениями, прежде всего, в кроветворной и костной системах. В начальные сроки после массивных поступлений патологический процесс может напоминать острую лучевую болезнь от внешнего облучения. В более поздние сроки, в том числе и после инкорпорации сравнительно небольших активностей, обнаруживаются костные опухоли, лейкозы.
♦ Радионуклиды, избирательно накапливающиеся в органах, богатых элементами ретикулоэндотелиальной системы («гепатотропные»). Это изотопы редкоземельных элементов: лантана, церия, прометия, празеодима, а также актиний, торий, некоторые соединения плутония. При их поступлении наблюдаются поражения печени, проксимальных отделов кишки (эти элементы, выделяясь с желчью, реабсорбируются в кишечнике и поэтому могут неоднократно контактировать со слизистой оболочкой тонкой кишки). В более поздние сроки наблюдаются циррозы, опухоли печени. Могут проявиться также опухоли скелета, желез внутренней секреции и другой локализации.
♦ Радионуклиды, равномерно распределяющиеся по организму. Это изотопы щелочных металлов: цезия, калия, натрия, рубидия; изотопы водорода, углерода, азота, а также некоторых других элементов, в частности полония. При их поступлении поражения носят диффузный характер: атрофия лимфоидной ткани, в том числе селезенки, атрофия семенников, нарушения функции мышц (при поступлении радиоактивного цезия). В поздние сроки наблюдаются опухоли мягких тканей: молочных желез, кишечника, почек и т. п.
♦ В отдельную группу выделяют радиоактивные изотопы йода, избирательно накапливающиеся в щитовидной железе. При их поступлении в большом количестве вначале наблюдается стимуляция, а позже угнетение Функции щитовидной железы. В поздние сроки развиваются опухоли этого органа.
4ЭО
Плохо резорбирующиеся радионуклиды являются причиной возникновения местных процессов, локализующихся в зависимости от путей поступления РВ.
В зависимости от физико-химической формы соединения, в состав которого входит радионуклид, особенно от его растворимости, в роли критических могут выступать разные органы. Так, при ингаляционном поступлении нерастворимых соединений элементов из группы остео-тропных или равномерно распределяющихся по телу критическим органом оказываются легкие. В разные сроки после поступления радионуклида в организм распределение его по органам может быть различным, т. е. роль критических могут выполнять различные органы.
22.2.2. Влияние на развитие поражения активности инкорпорированных радионуклидов и продолжительности их пребывания в организме
Характер патологического процесса при внутреннем заражении РВ существенно зависит от количества поступившей активности и времени пребывания ее в организме. Темп накопления поглощенной дозы определяется как режимом поступления радионуклида (однократное, длительное), так и периодом эффективного полувыведения.
Основная доля суммарной дозы облучения от таких сравнительно ко-роткоживущих нуклидов, как 131I, 32Р, 198Аи, накапливается за сравнительно короткий срок, что определяет в случае попадания в организм поражающих количеств острый или подострый характер патологического процесса. При поступлении 226Ra, 239Pu и других радиоактивных элементов, характеризующихся очень длительными периодами полураспада и медленным выведением из организма, имеет место длительное облучение с постоянной мощностью дозы и, соответственно, хроническое течение.
Если инкорпорация радионуклидов произошла в количествах, обеспечивающих накопление в течение короткого срока (несколько дней) среднетканевой дозы, эквивалентной 1 Гр у-облучения и выше, развивается острое лучевое поражение. При этом в значительной степени утрачивается специфичность действия различных радионуклидов и поражение во многих чертах напоминает острую лучевую болезнь от внешнего облучения.
Более вероятны ситуации, в которых количество инкорпорированного РВ не может обеспечить накопление достаточно высокой дозы в течение короткого времени и следствием внутреннего радиоактивного заражения является развитие хронической лучевой болезни или злокачественного новообразования.
22.2.3. Последствия поступления
в организм отдельных радионуклидов
Патологические процессы, развивающиеся в результате инкорпорации различных радионуклидов, отличаются большим своеобразием, зависящим от ряда факторов, из которых главными являются вид испускаемого излучения, особенности кинетики в организме, скорости распада и выведения, органотропность. Ниже будут приведены примеры, характеризующие специфику действия отдельных радионуклидов, имеющих наибольшую биологическую значимость при загрязнении внешней среды продуктами ядерных взрывов и аварий ядерных энергетических установок — радиоактивных цезия, стронция, йода, плутония.
Цезий-137,134
137Cs — смешанный (3,у-излучатель с периодом полураспада около 30 лет. Максимальная энергия р-частиц составляет 0,51 МэВ; энергия у-квантов — 0,662 МэВ. Основное количество 137Cs поступает в организм человека с пищей, до 25% — через органы дыхания.
Большинство солей цезия хорошо растворимы, и поэтому всасывание их из легких и желудочно-кишечного тракта осуществляется быстро и практически полностью. Распределение в организме l37Cs сравнительно равномерное. До 50% этого радионуклида концентрируется в мышечной ткани, причем чем интенсивнее работает мышца, тем больше в ней откладывается радиоцезия. Наибольшее содержание 137Cs обнаруживается в миокарде. В более поздние сроки довольно большое количество ,37Cs содержится в печени и почках. В скелете задерживается не более 5% поступившего в организм изотопа.
Выведение цезия, независимо от пути его поступления, на 3/5 происходит с мочой и на 2/5 с калом. Выводимый через кишечник цезий в значительной мере подвергается реабсорбции. Эффективный период полувыведения 137Cs у человека составляет от 50 до 150, в среднем 110 сут.
При длительном поступлении 137Cs в организм происходит его накопление. Через плаценту радиоактивный цезий легко проникает в организм плода. У лактирующих животных около 10% 137Cs поступает в молоко.
Характер распределения радиоцезия в организме во многом определяет клиническую симптоматику при его поступлении. При достижении определенной дозы вначале обнаруживаются общие реакции со стороны системы крови, нервной системы. Позже присоединяются нарушения функций критических органов: мышц, печени. Они проявляются нарушениями некоторых ферментных систем в клетках этих органов, изменениями ЭКГ, электромиограммы.
При одновременном поступлении в организм цезия и калия, калий накапливается в 3 раза быстрее и может вытеснять цезий. В связи с этим при лечении поражений радиоактивным цезием рекомендуется и с успехом применяется метод изотопного разбавления. Повышение содержания калия в пище и интенсификация водного обмена способствуют выведению цезия из организма.
Изотопы цезия включаются в биологический круговорот и свободно мигрируют по биологическим цепочкам. Сейчас (как следствие ядерных испытаний и радиационных аварий) 137Cs повсеместно обнаруживают в организмах разных животных и у человека.
Содержание 137Cs в организме может быть измерено как прямыми (измерение мощности дозы у-излучения от тела), так и косвенными (измерение р- и у- излучений от выделений) методами. С помощью стационарных СИЧ с защитной камерой удается зарегистрировать присутствие в организме 1,0 нКи 137Cs (40 Бк). В пробах мочи определяются концентрации порядка 15 пКи/л (0,6 Бк/л).
Изотоп 134Cs имеет период полураспада около 2 лет, что и определяет его меньшую опасность по сравнению с 137Cs. Мощность дозы от 134Cs на зараженной территории снижается значительно быстрее. По проявлениям биологического действия оба изотопа существенно не различаются.
Стронций-90
90Sr — р-излучатель с периодом полураспада 28,6 лет. Энергия испускаемых при его распаде р-частиц составляет 0,54 МэВ. В результате распада 90Sr образуется 90Y, тоже р-излучатель с максимальной энергией р-частиц 2,18 МэВ. Период полураспада 90Y составляет 64,2 ч.
Выпадающие на поверхность Земли изотопы стронция мигрируют по биологическим цепочкам и, в конце концов, могут поступить в организм человека.
Степень и скорость всасывания радиостронция из желудочно-кишечного тракта зависит от того, в состав какого химического соединения он входит, от возраста человека и функционального состояния организма, от состава пищевого рациона. Так, у лиц молодого возраста стронций всасывается быстрее и полнее. Увеличение содержания в диете солей кальция снижает всасываемость соединений стронция. При потреблении молока всасываемость стронция повышается. В разных условиях всасываемость стронция из желудочно-кишечного тракта человека колеблется от 11 до 99%.
Всосавшийся стронций активно включается в минеральный обмен. Являясь аналогом кальция, радиоактивный стронций депонируется преимущественно в костях и в костном мозге, которые и оказываются критическими органами.
Выводится стронций с калом и мочой, а, как установлено в эксперименте, у лактирующих самок и с молоком. Эффективный период полувыведения составляет - 17,5 лет.
В ранние сроки после поступления 90Sr в большом количестве наблюдаются изменения в органах, через которые он поступает или выводится: слизистые оболочки рта, верхних дыхательных путей, кишечник. Позднее нарушаются функции печени. При ингаляционном поступлении малорастворимых соединений стронция изотоп может достаточно прочно фиксироваться в легких, которые в этих случаях вместе с дыхательными путями являются критическими органами. Однако в отдаленные сроки и после ингаляционного поступления критическими органами становятся кости и костный мозг, в которых депонируются до 90% всей активности.
В процессе реакции кроветворной ткани на радиостронций в течение длительного времени морфологический состав крови меняется мало. Лишь при поступлении больших количеств развивается и прогрессирует цитопения. Тяжелых случаев поражения с острым или подострым течением у человека не наблюдали. По аналогии с данными, полученными на животных, можно полагать, что такие случаи будут напоминать клиническую картину острой лучевой болезни после внешнего облучения в дозах, при которых преимущественно поражается костный мозг.
При длительном поступлении радиостронция и подостром течении лучевой болезни постепенно развивается анемия, наблюдаются угнетение спермато- и овогенеза, нарушения иммунитета, функции печени и почек, нейроэндокринной системы, сокращается продолжительность жизни.
В отдаленные сроки развиваются гипер- или гипопластические процессы в костном мозге, лейкозы, саркомы кости. Реже наблюдаются новообразования в гипофизе и других эндокринных органах, в яичниках, молочной железе.
Большой период полураспада 90Sr определяет длительное сохранение высоких уровней заражения территорий и объектов среды после загрязнения этим радионуклидом.
Среди продуктов ядерного деления присутствует и 89Sr, который также является р-излучателем; энергия р-частиц у него составляет 1,5 МэВ. Однако период полураспада 89Sr короче — 53 сут, поэтому степень радиоактивного загрязнения объектов в этом случае снижается гораздо быстрее.
Йод-131
1311 — р,у-излучатель с периодом полураспада 8,05 сут. Энергия р-частиц составляет 0,25-0,812 МэВ, энергия у-квантов — 0,08—0,722 МэВ. Соединения йода хорошо растворимы и при алиментарном поступлении практически полностью всасываются в кровь. Большая часть йода всасывается и при ингаляционном поступлении.
Около 30% поступившего в кровь йода откладывается в щитовидной железе и выводится из нее с биологическим периодом полувыведения 120 сут. Эффективный период полувыведения из щитовидной железы равен 7,5 сут. Остальные 70% всосавшегося йода равномерно распределяются по другим органам и тканям. Биологический период полувыведения этой фракции составляет 12 сут; эффективный — 4,8 сут. Примерно 10% от этой органически связанной формы йода выводится с калом. Основное же количество радиоактивного йода выводится с мочой. Незначительное количество — через легкие, а также с потом, слюной, молоком.
У взрослого человека при алиментарном поступлении 1 мкКи 1311 ожидаемая эквивалентная доза облучения щитовидной железы составляет 1,8 бэр (4,8 • Ю-7 Зв/Бк). При ингаляционном поступлении соотношение составляет 1,1 бэр/мкКи (2,9 • Ю-7 Зв/Бк). Доза облучения щитовидной железы детей и подростков при поступлении такого же количества 1311 больше из-за меньшей массы щитовидной железы. После однократного поступления 13Ч доза облучения щитовидной железы накапливается очень быстро: 50% дозы за 7,5 дней, а 90% — уже за 25.
Биологическую активность 1311 характеризуют следующие экспериментальные данные.
У крыс при однократном введении в желудок среднесмертельная доза 1311 за 120 сут наблюдения составила 88,8 Бк/г. При введении изотопа в дозе в 10 раз меньшей наблюдали развитие деструктивных процессов в щитовидной и паращитовидной железах, реактивные изменения в гипофизе. Развивалось расстройство функций половых желез, нарушался эстральный цикл, снижалась плодовитость вплоть до полной стерильности. При длительном введении животным радиоактивного йода развивались изменения в передней доле гипофиза, нарушались функции всех желез внутренней секреции. В поздней стадии хронического поражения развивался нефросклероз. В отдаленные сроки после введения радиоактивного йода у животных развивались опухоли щитовидной, паращитовидной и молочной желез.
Пороговой дозой для развития гипотиреоза у человека называют дозу 45 Гр. Эта доза соответствует результату однократного поступления в организм примерно 3 мКи радиоактивного йода. Наибольшая опасность при поступлении в организм 1311 связана с возможностью возникновения рака щитовидной железы. Коэффициент риска его развития после радиационного воздействия составляет 5 • 10~43в-1.
Плутоний-239
239Ри — трансурановый элемент, обладающий высокой радиотоксичностью. Это смешанный а- и у-излучатель. Энергия а-частиц составляет 5,5 МэВ, а у-квантов — 0,01—0,4 МэВ. Период полураспада 239Ри составляет 24 360 лет.
Среди продуктов, участвующих в формировании зон радиоактивного заражения после ядерных взрывов или аварий ядерных энергетических установок, присутствует часть нераспавшегося горючего или заряда, в частности плутоний. Обычно его количества малозначимы, однако в случаях механического разрушения ядерных боеприпасов заражение плутонием может быть достаточно существенно.
Плутоний легко гидратируется и склонен к комплексообразованию. Образующиеся в результате соединения в большинстве своем очень плохо растворимы.
Внешнее облучение 239Ри не опасно для человека. Поступление же этого изотопа внутрь организма, которое может произойти алиментарным, ингаляционным путем или через поврежденную и даже неповрежденную кожу, требует проведения немедленных и весьма активных лечебных мероприятий.
Абсорбция плутония из желудочно-кишечного тракта в кровь очень мала. Для наиболее хорошо растворимых соединений (нитрат плутония) она составляет 3 • Ю-5, а для сравнительно плохо растворимых (оксид плутония) — 1 • Ю-6. Иногда могут быть и более высокие значения резорбции. На абсорбцию существенно влияет состав пищевого рациона.
При ингаляционном поступлении значительное количество плутония надолго оседает в легких, позднее частично перемещается в бронхолегоч-ные лимфатические узлы, а затем и в кровь.
Всасывание плутония через кожу зависит от ее состояния. Наличие ссадин и царапин, воздействие растворителей, кислот резко повышают резорбцию плутония через кожу. Если кожа не повреждена, плутоний поступает в основном через волосяные фолликулы.
Поступивший в кровь плутоний откладывается в печени (45%), в скелете (45%), остальное его количество — в других органах и тканях, и выводится с экскретами в ранние сроки после поступления.
Доля плутония, отложившегося в гонадах, составляет примерно 3,5 ■ Ю-4 у мужчин и 1 • Ю-4 у женщин.
Биологический период полувыведения плутония из скелета составляет 100 лет, а из печени — 40 лет. Эффективный период полувыведения для 239Ри практически равен биологическому.
В экспериментах после энтерального введения больших количеств плутония в клинической картине преобладали проявления поражения функций кроветворения и кровообращения. Животные погибали в течение 2—3 нед от апластической анемии и кровоизлияний. При подостром поражении нарушения кроветворной функции сопровождались развитием регенераторных процессов в системе крови. Происходило рассасывание костного вещества. Животные погибали от цирроза печени, проявлявшегося асцитом, желтухой, истощением.
После введения малых доз 239Ри крысам развивалась хроническая форма поражения, проявлявшаяся возникновением гипо- и гиперпластических процессов в системе крови, развитием цирроза печени, неф-росклероза, злокачественными новообразованиями в различных органах, наиболее часто в костях.
При поступлении плутония через органы дыхания критическим органом оказываются легкие. Острые поражения плутонием при ингаляционных затравках характеризовались развитием фибринозной пневмонии с пневмосклерозом, от которой при введении высоких доз (порядка 8,1 ■ 104 Бк/кг) собаки погибали через 4 мес. Наблюдалось истощение животных, постепенно развивались умеренные лимфопения и лейкопения. Развитие пневмосклероза наблюдалось при введении в легкие и меньших количеств плутония, однако в этих случаях процесс протекал медленнее. Для поздних сроков характерно возникновение опухолей легких.
Время накопления дозы медленное — 50% дозы в скелете и печени реализуются в течение 27—100 лет. Прижизненное определение плутония в организме возможно с помощью СИЧ или по активности проб мочи.
22.2.4. Лучевые поражения в результате алиментарного и ингаляционного поступления продуктов ядерного деления
Представления о патогенезе и клинической картине поражений большими количествами продуктов ядерного деления (ПЯД) основываются на экспериментальных данных. В реальных условиях собственно ПЯД могут оказаться смешанными в разных соотношениях с продуктами наведенной радиоактивности и нераспавшейся частью урана или плутония.
Радиоактивность поступивших в организм молодых ПЯД быстро снижается в первое время за счет распада короткоживущих изотопов, и интенсивность облучения организма со временем падает. Во всех органах, кроме костей, 30-50% всей накопленной дозы формируется в течение 1 сут после поступления ПЯД в организм, в течение недели — практически вся доза.
При распаде ПЯД испускают р-, а во многих случаях и у-излучение. Характерна резкая неравномерность в распределении поглощенных доз (до 3 порядков) между различными органами и тканями, что зависит прежде всего от тропности отдельных радионуклидов к различным органам и низкой проникающей способности р-частиц. у-Излучение более равномерно поглощается различными участками тела. В экспериментах И. Я. Василенко после введения собакам ПЯД возрастом 36 ч соотношение поглощенных доз в щитовидной железе, кишечнике, печени и скелете составляло 1000:100:10:1 соответственно. Радионуклиды накапливались неравномерно и в пределах одного органа.
Вначале наиболее интенсивно облучаются органы дыхания и пищеварения, через которые ПЯД поступают в организм. Далее следуют органы преимущественного депонирования: щитовидная железа, печень, почки. В этих органах основная часть дозы формируется в ближайшие дни после заражения. В костях доза формируется гораздо медленнее по причине накопления в них таких долгоживущих радионуклидов, как стронций.
О количестве ПЯД, приводящих к развитию острых проявлений поражения, можно судить на основании следующих экспериментальных данных. При введении собакам через рот 111 МБк (3 мКи) на 1 кг массы ПЯД суточного возраста развивалась ОЛБ легкой степени, после 222 МБк/кг — болезнь средней степени тяжести, а большие дозы приводили к развитию тяжелого лучевого поражения. Дозы облучения кишечника при этом составили 10, 20 и более 20 Гр соответственно; дозы облучения щитовидной железы были примерно на порядок больше, а печени — на порядок меньше.
В клинической картине лучевой болезни при алиментарном поступлении больших количеств ПЯД доминируют проявления поражения кишечника, вызванные контактным р-облучением. Повреждения кишечника часто имеют очаговый характер, особенно при поступлении плохо растворимых радионуклидов, длительно задерживающихся в криптах и регионарных лимфатических узлах, в результате чего местно формируются высокие дозы. Нарушается баланс жидкостей и электролитов, развиваются интоксикация, бактериемия, страдают секреция и ферментообразова-ние в желудке, кишечнике. Клинически для тяжелой степени поражения характерны рвота, понос, тенезмы, слизь и кровь в кале, обезвоживание организма, общее угнетение животных, снижение количества поедаемого корма. Патологический процесс можно обозначить как острый геморрагический гастроэнтероколит. Состояние тонкой кишки при этом напоминает поражение при кишечной форме острой лучевой болезни от внешнего облучения. В связи с очаговым характером поражения, а также с большей длительностью облучения равноэффективные дозы для кишечника при внутреннем заражении ПЯД оказываются в 2-2,5 раза выше, чем при внешнем облучении.
Ингаляционное поступление ПЯД опаснее, чем алиментарное. Это связано в первую очередь с облучением легких за счет продуктов, задержавшихся в них и попавших в лимфатические узлы.
В результате высоких местных доз, формирующихся вокруг задержавшихся в легких радиоактивных частиц, развиваются очаги кровоизлияний, переходящие в фибринозно-геморрагическую пневмонию со слабо выраженной клеточной реакцией. Наблюдаются проявления радиационного ожога верхних дыхательных путей. Наряду с органами дыхания при ингаляционном поступлении ПЯД поражается и кишечник. В остром периоде болезнь можно определить как бронхопневмонию с гастроэнтеро-колитом.
Гематологические изменения при поступлении ПЯД внутрь организма зависят от их количества, изотопного состава (который меняется в зависимости от «возраста» осколков) и растворимости. Если поступление невелико, а продукты мало растворимы, обычно наблюдают умеренный лейкоцитоз, моноцитоз, сдвиг лейкоцитарной формулы влево, иногда лейкемоидную реакцию костного мозга. При поступлении больших количеств радионуклидов появляются признаки угнетения лейко- и эритропоэза. В числе причин изменений кроветворения кроме прямого облучения гемопоэтических органов могут быть названы и отраженные реакции. Так, начальный лейкоцитоз выражен сильнее, чем при общем облучении, что связано с р-поражениями слизистых оболочек дыхательных путей и пищеварительного тракта. Значимость гематологических изменений для прогноза тяжести лучевой болезни в случае внутреннего поступления ПЯД значительно меньше, чем при внешнем облучении.
Из органов депонирования ПЯД на первом месте стоит щитовидная железа, в которой концентрируется до 30% всех всосавшихся молодых продуктов деления.
До 15% всосавшихся ПЯД депонируются в печени ("Мо, 132Те, i3i-i35i; 140ва и др.). Выделяющиеся с желчью изотопы могут повторно всасываться в кишечнике и вновь служить причиной облучения печени.
Так же как и при ОЛБ от внешнего облучения, при внутреннем заражении ПЯД развиваются существенные расстройства иммунологической реактивности: повышается чувствительность к инфекции, развиваются
Глава 22. ПОРАЖЕНИЯ В РЕЗУЛЬТАТЕ ВНУТРЕННЕГО РАДИОАКТИВНОГО ЗАРАЖЕНИЯ
аутоиммунные реакции. Поражения кишечника, печени, щитовидной железы при внутреннем заражении ПЯД обусловливают нарушения углеводного, липидного и белкового обмена, активности ферментов, накопление токсичных метаболитов.
Причиной смерти при острых поражениях ПЯД чаще всего являются повреждения желудочно-кишечного тракта и органов дыхания, развивающиеся на фоне глубоких нарушений кроветворной функции и приводящие к обезвоживанию, потере электролитов, интоксикации, генерализации инфекции.
Для восстановительных процессов при внутреннем заражении ПЯД характерно все то, что отмечают и при общем внешнем облучении: репарация молекулярных повреждений, клеточная регенерация, восстановление функций на органном и организменном уровнях. К этому следует добавить процессы, направленные на удаление ПЯД из организма. Мешает течению восстановительных процессов после внутреннего заражения продолжающееся облучение инкорпорированными радионуклидами, а также изменения гормональной регуляции, связанные в первую очередь с повреждением щитовидной железы радиоактивным йодом.
Течение ОЛБ от внутреннего поступления ПЯД отличают слабая выраженность первичной реакции и гематологического синдрома, отсутствие четких границ между периодами течения, рано появляющиеся признаки поражения критических органов (кишечника, легких), замедление восстановительных процессов.
Длительное присутствие в организме радионуклидов, отличающихся низкими константами распада и выведения, таких как 90Sr, нередко обусловливает возникновение хронических форм заболевания, многообразных опухолевых и неопухолевых отдаленных последствий.
Уже после воздействия активностями порядка единиц мКи возможно развитие лучевых реакций в результате радиационного ожога слизистых оболочек. Реакции эти проявляются лейкоцитозом, переходящим в лейкопению, некоторыми нарушениями обмена веществ, иммунитета.
При поступлении молодых ПЯД в количествах, не приводящих к развитию острой лучевой болезни, наиболее значимым радионуклидом является радиоактивный йод. При поступлении в организм 1 мКи молодых ПЯД доза на щитовидную железу взрослых может достичь 0,4-1 Гр, а у детей в 2—10 раз больших величин. После распада радиоактивного йода на первое место по биологической значимости перемещаются радионуклиды цезия и стронция, а при поражении ПЯД возрастом 1 месяц — 1 год относительная доза в щитовидной железе оказывается значительно меньше, а в других органах, особенно в скелете, значительно больше.
Отдаленные последствия при внутреннем заражении ПЯД принципиально такие же, как и при внешнем облучении, однако существенно большая доля приходится на опухоли желез внутренней секреции, в возникновении которых ведущее значение принадлежит повреждению щитовидной железы, которую рассматривают как критический орган в формировании отдаленной патологии при поступлении в организм ПЯД.
22.3. Профилактика поражений радионуклидами. Медицинские средства защиты и раннего лечения
22.3.1. Специальные
санитарно-гигиенические
и профилактические медицинские
мероприятия
Для предупреждения поражений при нахождении на радиоактивно зараженной местности необходимо проведение ряда профилактических мероприятий.
♦ Для снижения ингаляционного поступления РВ могут быть применены респираторы, достаточно эффективные при загрязнении воздуха продуктами наземного ядерного взрыва. При нахождении на радиоактивно зараженной местности также необходимо использовать средства защиты кожи.
♦ При авариях ядерных энергетических установок укрытие в помещениях с закрытыми, а еще лучше законопаченными, окнами и дверями, выключенной вентиляцией во время прохождения факела выброса будет способствовать не только снижению дозы внешнего облучения, но и ограничению ингаляционного поступления РВ.
♦ Для предупреждения алиментарного поступления продуктов ядерного взрыва необходимо не допускать потребления воды и пищевых продуктов, уровень заражения которых превышает безопасный. Обязательными являются следующие рекомендации: приготовление пищи на открытой местности допускается при уровне радиации не более 1 Р/ч; при 1-5 Р/ч кухни следует развертывать в палатках. Если уровень радиации еще выше, приготовление пищи допускается лишь в дезактивированных закрытых помещениях, территория вокруг которых должна быть также дезактивирована или хотя бы увлажнена.
♦ Контроль уровня радиоактивного загрязнения воды и продовольствия. Наиболее точным способом выражения радиоактивной зараженности являются величины удельной активности (МБк/л, МБк/кг, Ки/л и т. п.). Эти единицы и применяются при анализах, проводимых в радиометрических лабораториях. Когда прямая оценка зараженности затруднительна, используется зависимость между степенью заражения и мощностью дозы у-излучения, исходящего от загрязненного объекта. В соответствующих единицах (мР/ч) и отградуированы современные полевые радиометрические приборы, и представлены в таблицах нормативные значения радиоактивной зараженности, не приводящие к развитию поражения или чреватые определенными последствиями.
"ItlU I fc> II. rHHriUDinUllUI Yin
Глава 22. ПОРАЖЕНИЯ В РЕЗУЛЬТАТЕ ВНУТРЕННЕГО РАДИОАКТИВНОГО ЗАРАЖЕНИЯ
При действиях на радиоактивно загрязненной местности очень часто высокие значения у-фона не позволят определить степень зараженности по мощности дозы. В этих случаях радиоактивная зараженность воды и пищевых продуктов может быть определена расчетным методом, по мощности дозы на местности. Применяемые при этом формулы учитывают зависимость между плотностью радиоактивного загрязнения местности продуктами ядерного взрыва и мощностью дозы на местности (ориентировочно мощность дозы 1 Р/ч соответствует плотности загрязнения местности 0,01 мКи/см2), растворимость в воде продуктов ядерных взрывов на карбонатных, силикатных и смешанных грунтах, глубину водоема, а для расчета загрязнения пищевых продуктов — отношение площади незащищенной поверхности продовольствия к его массе. Расчетный метод применяется всеми звеньями медицинской службы для получения предварительных данных о степени загрязнения воды и продовольствия, а в случаях, когда применение других методов невозможно, — также и для окончательной оценки. В сомнительных случаях пробы воды и продовольствия направляют для заключения в специальные лаборатории.
♦ Мероприятия, направленные на удаление радионуклидов с мест первичного поступления. Это проведение санитарной обработки, удаление РВ из желудочно-кишечного тракта и т. д. При установлении факта внутреннего радиоактивного заражения или только предположении об его наличии в процессе частичной санитарной обработки прополаскивают полость рта 1% раствором соды или просто водой, промывают такими же жидкостями конъюнктивы, слизистые оболочки носа, принимают меры к удалению РВ из желудочно-кишечного тракта (промывание желудка, назначение рвотных средств, механическое раздражение задней стенки глотки, солевые слабительные, клизмы). Проведение этих мероприятий следует начинать на возможно ранних этапах эвакуации пораженных и завершать в специализированном стационаре. Все проведенные мероприятия должны быть зафиксированы в первичной медицинской карте, передаваемой в стационар.
22.3.2. Медицинские средства защиты и раннего (догоспитального) лечения при внутреннем заражении радиоактивными веществами
Медицинские средства защиты от поражающего действия РВ и специальные средства раннего (догоспитального) лечения пострадавших представлены препаратами трех групп:
• сорбенты;
• препараты, затрудняющие связывание РВ тканями;
• препараты, ускоряющие выведение РВ.
Сорбенты
Сорбентами называют вещества, предназначенные для связывания РВ в желудочно-кишечном тракте. Такие препараты должны быстро и прочно связывать РВ в среде желудка и кишечника, причем образовавшиеся соединения или комплексы не должны всасываться.
Применение в качестве сорбентов таких неспецифических средств, как животный уголь, каолин, крахмал, агар-агар, соли висмута, карбонаты, при поступлении РВ в желудочно-кишечный тракт малоэффективно.
Лучшие результаты дает применение средств селективного действия. Механизм действия препаратов этой группы может быть основан на явлениях молекулярной сорбции, на ионообменном поглощении или на образовании комплексных недиссоциирующих и нерастворимых соединений.
Сульфат бария, применяемый в рентгенодиагностике как контрастное средство, при приеме внутрь активно адсорбирует ионы радиоактивных стронция, бария, радия. Более эффективной лекарственной формой является адсобар — активированный сернокислый барий со значительно увеличенной адсорбционной поверхностью. Применение адсобара снижает всасывание радиоактивного стронция в 10—30 раз. При введении обычного сернокислого бария всасывание этого радионуклида снижается всего в 2—3 раза.
Альгинат кальция — слабокислый природный ионообменник. В его составе имеются соли Д-маннуроновой и Д-галактуроновой кислот, с которыми стронций, помимо ионного обмена, образует более устойчивые, чем кальций, комплексные соединения. Альгинаты несколько менее эффективны, но лучше переносятся, чем препараты сернокислого бария, и могут применяться в течение длительного времени.
Вокацит — препарат высокоокисленной целлюлозы. В процессе окисления целлюлозы в ней образуются карбоксильные группы и происходит размыкание колец в отдельных мономерах. Свободные концы разомкнутых колец представляют собой карбоксильные остатки, с которыми связываются ионы стронция. При этом кольца замыкаются и образуются соединения клешневидного типа. Катионы большей валентности образуют комплексы в виде внутри- или межмолекулярных циклических форм.
Существенным недостатком перечисленных средств является необходимость приема больших количеств препарата: разовые дозы и альгината, и вокацита, и адсобара составляют по 25,0 — 30,0 г ( в 1/2-3/4 стакана воды). В меньших дозах (4,0—5,0) применяют полисурьмин — натриевую соль неорганического ионообменника — кремний-сурьмянокислого катионита.
Адсобар, альгинат, вокацит, полисурьмин при профилактическом применении или введении в течение ближайших 10—15 мин после заражения снижают всасывание радиоизотопов стронция и бария в десять и более раз. Они мало эффективны по отношению к одновалентным катионам, в частности, к цезию.
Берлинская лазурь и другие соли переходных металлов и ферроциани-Да обладают хорошей способностью связывать цезий. Относящийся к этой группе препарат ферроцин рекомендуется принимать по 1,0 г 2—3 раза в день. При раннем применении ферроцина резорбция 137Cs из желудочно-кишечного тракта снижается на 92—99%. При уже состоявшейся инкорпорации этого радионуклида период его полувыведения у человека при лечении ферроцином снижается вдвое.
Возможность длительного применения сорбентов ограничивают их часто неудовлетворительная переносимость и недостаточная изученность хронического воздействия на организм.
Препараты, применяемые с целью предупреждения связывания тканями и ускорения выведения радионуклидов, проникших во внутреннюю среду организма
Калия йодид. В основе применения калия йодида при инкорпорации радиоактивного йода лежит принцип так называемого изотопного разбавления. Если радиоактивное вещество уже попало во внутреннюю среду, препятствовать процессу связывания его тканями, а иногда и способствовать освобождению уже связанного радионуклида может введение в организм стабильного изотопа того же элемента или другого элемента той же группы таблицы Менделеева, которые химически замещают попавшие в организм РВ.
Препарат выпускается в таблетках по 0,125 г для приема по 1 табл. в сутки. При профилактическом применении поглощение щитовидной железой радиоактивного йода удается снизить на 95—97%. Прием стабильного йода после окончания поступления в организм радиоактивного изотопа этого элемента значительно менее эффективен, а через четыре часа уже практически бесполезен. Однако при длительном поступлении радиоактивного йода существенный эффект достигается даже если прием стабильного йода начат с запозданием.
При отсутствии йодистого калия показан прием внутрь йодной настойки в молоке или даже воде (44 капли 1 раз в день или по 22 капли 2 раза в день после еды в 1/2 стакана жидкости), раствора Люголя (22 капли 1 раз в день после еды в 1/2 стакана молока или воды), а также смазывание кожи предплечья или голени настойкой йода. Защитный эффект наружного применения йода сопоставим с эффектом приема такого же его количества внутрь.
При идиосинкразии к йоду, калия йодид может быть заменен перхлоратом калия, ионы которого конкурируют с ионами йода. Таблетки калия перхлората в сочетании с калия йодидом рекомендуется при необходимости принимать также беременным женщинам.
Другим примером возможности применения метода изотопного разбавления является введение глюконата стабильного стронция в ранние сроки после инкорпорации радиоактивного изотопа. Менее эффективен в этом случае кальция глюконат.
Пентацин — тринатрийкальциевая соль диэтилентриаминпентаук-сусной кислоты (ДТПА) представляет собой препарат, относящийся к группе комплексонов, или хелатов. Это органические вещества, которые благодаря своей молекулярной конфигурации и наличию электрон-нодонорных атомов в молекуле способны образовывать прочные комплексы с 2- и 3-валентными металлами. Для связывания РВ в организме пригодны хелатные препараты, комплекс которых с металлом не разрушается в организме и быстро выводится из него.
Пентацин образует очень прочные комплексы со скандием, хромом, железом, цинком, иттрием, цирконием, рутением, кадмием, индием, свинцом, торием, лантаноидами, ураном и трансурановыми элементами. Препарат в организме человека стабилен и очень быстро (в течение 6 ч) выводится, в основном с мочой. Пентацин связывает РВ не только в крови, но частично и проникшие в органы. Рекомендуемая доза пентацина составляет до 1 г в сутки. Введение проводится либо путем внутривенного вливания в течение от 1/2 до 3 ч, либо очень медленно струйно. При поступлении радионуклидов, особенно плутония, через органы дыхания применяют ингаляции аэрозолей растворов пентацина. При этом рассчитывают на связывание попавшего в органы дыхания плутония пентацином, образование недиссо-циирующих комплексов, которые переходят через альвеолярные мембраны в кровь и выводятся с мочой. Возможно введение препарата через рот. Эффективность препарата в значительной мере зависит и от времени, прошедшего с момента инкорпорации до введения пентацина. Особенно это относится к остеотропным радионуклидам.
Выпускается препарат в форме 5% раствора и в таблетках по 0,5 г. На курс лечения в среднем идет 30—40 г препарата.
Если пентацин ввести в липосомах, то они, проникая через клеточные мембраны, облегчают препарату доступ к радионуклидам, связанным с клеточными структурами, что повышает выведение РВ.
Соли этилендиаминтетрауксусной кислоты (ЭДТА) — кальций-динат-риевая соль (тетацин-кальций) и динатриевая соль (трилон Б) — действуют во многом аналогично пентацину, но менее эффективны и несколько хуже переносятся.
Унитиол (для внутривенного введения по 10 мл 10% раствора 1—2 раза в сут). Этот препарат применяют при инкорпорации 210Ро, выведение которого не удается ускорить с помощью пентацина. Полоний связывается сульфгидрильными группами препаратов. Образовавшиеся комплексы выводятся с мочой. Применение комплексонов, содержащих сульфгидрильные группы, значительно эффективнее по сравнению с пентацином также при связывании ионов кобальта, меди, ртути.
Триметацин рекомендуется в качестве средства первой помощи при отравлениях ураном и бериллием. После введения препарата ускоряется также выведение плутония, иттрия, церия, циркония, ниобия. Разовая Доза триметацина содержится в виде лиофилизированного порошка во флаконах и разводится перед внутривенным введением 2,5% раствором кальция хлорида для инъекций.
 После проведения неотложных мероприятий пострадавший должен быть транспортирован в стационар, желательно специализированный.
После проведения неотложных мероприятий пострадавший должен быть транспортирован в стационар, желательно специализированный.
22.4. Ранняя диагностика и эвакуационные мероприятия при внутреннем заражении радиоактивными веществами
Диагностика при внутреннем радиоактивном заражении основывается на индикации и оценке количества инкорпорированных радиоактивных веществ. Сам факт наличия внутреннего радиоактивного заражения можно установить уже в процессе радиометрического обследования человека. Если обнаруженное излучение от тела не устраняется в процессе санитарной обработки, проводят измерения в двух вариантах: при открытом окне зонда (приборы типа ДП-5), когда определяется суммарная мощность дозы у- и р-излучения, и при закрытом окне, когда р-излучение отфильтровывается и определяется только у-излучение. В случае внутреннего заражения существенных различий показаний прибора при открытом и закрытом окне зонда не будет. В случае наружного заражения отклонение стрелки радиометра при открытом окне окажется значительно больше, чем при закрытом.
Для количественного определения содержания РВ в организме применяют прямые и косвенные методы измерения.
Прямые методы основаны на измерении мощности дозы у-излучения от тела (или от отдельного органа при избирательном накоплении в нем радионуклида). В последующем с помощью имеющихся в таблицах эмпирически установленных коэффициентов рассчитывают содержание радионуклида в организме (или органе) и поглощенную дозу внутреннего облучения. Наиболее точные результаты дает применение прямых методов при измерениях с помощью счетчиков излучения человека (СИЧ). Возможно также применение приборов радиационного контроля (СРП-69-01, ДП-5В и др.)
Косвенные методы основаны на радиометрических исследованиях активности биосред и выделений. Для наиболее важных радионуклидов установлены зависимости между количеством инкорпорированных РВ и их суточным выведением с мочой и калом на разные сроки после заражения. Эти данные, имеющиеся в справочных таблицах, позволяют произвести расчет поступившей в организм активности.
При поражениях в результате ядерных взрывов или аварий на ядерных энергетических установках внутреннее радиоактивное заражение не играет ведущей роли, а необходимость и сроки эвакуации будут определяться преимущественно другими факторами (тяжесть сопутствующей хирургической травмы, доза внешнего облучения).
В случае радиационных инцидентов, при которых имеется вероятность внутреннего заражения РВ, правильная оценка состояния пострадавшего и определение рациональных лечебных вмешательств в большой мере зависят от полноты информации. Поэтому с самых ранних этапов оказания медицинской помощи следует уточнить и зарегистрировать точное время инцидента, наименование радионуклида и пути его поступления в организм, в состав какого химического соединения входил радионуклид, в каком он был агрегатном состоянии (раствор, порошок и т. п.), сколько всего находилось радионуклида на рабочем месте.
Необходимо зафиксировать результаты первичного определения загрязненности кожных покровов. Следует собрать возможные пробы биосубстратов: рвотные массы, первые порции кала, мочи, промывные воды — с целью последующей их радиометрии.
| T.O<in.la-- . , ( 'if iV't*!"'*-'*} ••ГТ • «V - ', f'f 1 . i ,.'!««'. i »' :'Mi ■ ' • |
При инкорпорации высокотоксичных радионуклидов, таких как плутоний, полоний, америций, радий и другие, требуется срочная эвакуация в специализированное учреждение, где могут быть проведены эффективные мероприятия по выведению РВ из организма (бронхопульмональный лаваж, форсированный диурез, повторные введения комплексонов и т. п.).
, UH i '* ,'• r r,<?., tfWJSK'T Ф "*
 i-ч'" <> 4; . *'Ч«-Щ5Я!'
i-ч'" <> 4; . *'Ч«-Щ5Я!'
.г tjf> • '."/ f ^.5'4«.>$
• . ■ " /i.; <'.*.* -V№$&
?• < им u- " VIVO! X. : »'
Глава 23. СОЧЕТАННЫЕ И КОМБИНИРОВАННЫЕ РАДИАЦИОННЫЕ ПОРАЖЕНИЯ
23.1* Сочетанные радиационные поражения
Сочетанные радиационные поражения — это поражения, возникающие вследствие одновременного или последовательного воздействия внешнего излучения; аппликации на кожу или слизистые оболочки радионуклидов, их поступления внутрь организма через органы дыхания и пищеварения, а также раневые и ожоговые поверхности. Сочетанные поражения могут наблюдаться у людей, оказавшихся без средств защиты кожи и органов дыхания на местности, загрязненной радиоактивными продуктами ядерного взрыва или радионуклидами, попавшими в окружающую среду вследствие радиационных аварий. Считается, что сочетанные радиационные поражения (наряду с комбинированными) являются наиболее вероятными формами патологии, возникающей у пострадавших при применении ядерного оружия или при радиационных авариях. Так, массовые случаи сочетанных радиационных поражений наблюдались у жертв атомных бомбардировок городов Хиросимы и Нагасаки, а также у жителей Маршалловых островов, подвергшихся воздействию у-р-излучения в момент выпадения радиоактивных осадков, вызванных испытанием США термоядерного оружия. Этот вариант радиационных поражений часто регистрировался у пострадавших при авариях ядерных энергетических установок на атомных подводных лодках, а также у лиц, участвовавших в ликвидации последствий Чернобыльской катастрофы.
Ведущим фактором, определяющим течение сочетанного поражения, как правило, является доза общего внешнего облучения, однако и сопутствующие компоненты поражения ((3-ожоги кожных покровов и слизистых оболочек, поражения от внутреннего облучения) играют весьма существенную роль в усугублении общего состояния и перспектив лечения пострадавших, а в ряде случаев могут явиться непосредственной причиной их гибели.
Особенностями, отличающими течение острой лучевой болезни при сочетанном облучении от поражения, вызываемого изолированным внешним у- или у-нейтронным воздействием, являются:
• более выраженные симптомы первичной реакции на облучение, сопровождающиеся раздражением слизистых оболочек верхних дыхательных путей и конъюнктивы глаз, первичной эритемой на открытых участках тела;
• нарушение «классической» периодизации острого лучевого костномозгового синдрома: удлинение и неотчетливость границ периода первичной реакции на облучение, уменьшение продолжительности скрытого периода или его отсутствие, быстрое наступление периода разгара, более длительный период восстановления;
• изменение «классических» проявлений панцитопенического синдрома за счет разнонаправленного действия р- и у-излучения на кроветворение: менее выраженная лейкопения в период разгара при ОЛБ легкой и средней степени тяжести, изменение сроков наступления и темпов развития агранулоцитоза при тяжелых формах поражения, ранняя тромбоцитопения и анемия, замедленное восстановление уровня лейкоцитов в период выздоровления;
• более ранние и выраженные проявления геморрагического синдрома (носовые кровотечения в скрытом периоде, появление кровоизлияний в восстановительном периоде и т. д.), эндогенной интоксикации (за счет плазмореи и потери белков), более сильные нарушения функций сердечно-сосудистой, эндокринной и центральной нервной систем;
• усиление тяжести поражений, вызванных внутренним облучением организма при инкорпорации радионуклидов;
• более тяжелое течение местных радиационных поражений, частое инфицирование ран и удлинение сроков их заживления;
• большое число поздних летальных исходов у тяжелопораженных;
• длительный период клинического выздоровления, характеризующийся выраженными астено-вегетативными расстройствами, функциональной неустойчивостью, снижением толерантности к физическим и психическим нагрузкам;
• высокий риск отдаленных (главным образом онкологических) последствий облучения.
Диагностика сочетанных радиационных поражений заключается прежде всего в оценке степени тяжести внешнего лучевого поражения, а также в установлении характера, локализации и степени тяжести лучевых поражений, формирующихся при наружном радиоактивном загрязнении кожных покровов и слизистых оболочек или при инкорпорации радионуклидов. С этой целью используются данные физической и биологической Дозиметрии, анамнеза, объективного обследования, а также результаты клинико-лабораторных и радиометрических исследований (см. выше).
Основным принципом лечения сочетанных радиационных поражений является комплексное применение средств терапии острой лучевой болезни и местных повреждений кожи и слизистых оболочек. При оказании неотложной помощи существенную роль играют симптоматическая терапия, направленная на борьбу с болевым синдромом, обусловленным наличием лучевых ожогов, а также мероприятия по поддержанию функций сердечно-сосудистой системы. С учетом патогенетических механизмов взаимного отягощения общих и местных патологических процессов, при оказании помощи пораженным особое внимание должно быть уделено дезинтокси-кационным и противоинфекционным мероприятиям, борьбе с геморрагическими проявлениями, анемией, поражением печени и почек.
23.2. Комбинированные радиационные поражения
Комбинированные радиационные поражения (КРП) — это вид поражений, возникающий при одновременном или последовательном воздействии на организм ионизирующих излучений и поражающих факторов нелучевой этиологии, приводящем к выходу пострадавшего из строя, нарушению его трудо- и боеспособности или возникновению выраженных изменений клинико-лабораторных показателей. КРП характеризуются взаимным влиянием на организм всех факторов, участвующих в формировании общего патологического процесса и оказывающих влияние на его течение и исход, и отличаются по своему течению и исходам от изолированных поражений теми же факторами.
В зависимости от количества и сочетания этиологических факторов КРП подразделяются на:
• двухфакторные (радиационно-механические, радиационно-терми-ческие, радиационно-химические, радиационно-биологические);
• трехфакторные (радиационно-механо-термические, радиационно-механо-химические, радиационно-механо-биологические, ради-ационно-термо-химические, радиационно-термо-биологические, радиационно-химико-биологические);
• четырехфакторные (радиационно-механо-термо-химические, ра-диационно-механо-термо-биологические, радиационно-механо-хи-мико-биологические, радиационно-термо-химико-биологические);
• пятифакторные (радиационно-механо-термо-химико-биологи-ческие).
КРП могут являться результатом ядерного взрыва, быть следствием техногенных катастроф и террористических актов на объектах ядерной энергетики. В случае применения, наряду с ядерным, биологического и (или) химического оружия возможно возникновение радиационно-био-логических и радиационно-химических КРП или их сочетания.
Наиболее типичными являются КРП, возникающие при одновременном действии поражающих факторов ядерного взрыва, в результате которого могут возникать комбинации острых лучевых поражений с ожогами и (или) механическими травмами. При применении ядерного оружия среднего калибра (20—50 кт) на долю КРП приходится до 60—70% от всех санитарных потерь. При использовании ядерного оружия малых и сверхмалых калибров преимущественно возникают «чистые» у-нейтронные поражения. Однако остающаяся в строю часть облученных может впоследствии (спустя часы и сутки) получить поражения другими видами оружия. Это может произойти и при ведении боевых действий на следе радиоактивного облака, где также создаются условия для комбинации пролонгированного облучения с огнестрельными ранениями и ожогами огнем пожаров или огнесмесями (напалм, пирогели и т. п.). Кроме того, КРП могут возникать у раненых, обожженных и больных, находящихся на зараженной радиоактивными веществами местности.
Другими словами, возникновение КРП возможно не только в результате одновременного действия поражающих факторов ядерного взрыва, но и в тех случаях, когда действие ионизирующего излучения предшествует нелучевым воздействиям или нелучевые травмы возникают ранее радиационных. Вариант «облучение + травма» отличается более тяжелым течением по сравнению с одновременными поражениями или с последовательностью «травма + облучение». Следует помнить, что в случае неодновременного воздействия поражающих факторов комбинированными будут являться только те поражения, при которых время между действием лучевых и нелучевых поражающих факторов не превышает длительности течения первого поражения, иначе это будут уже независимые друг от друга последовательные поражения.
Наиболее характерная особенность КРП — наличие у пострадавшего признаков двух или более патологий. Поскольку ранние (симптомы первичной реакции на облучение) или поздние (признаки разгара ОЛБ) клинические проявления радиационной патологии сочетаются у одного и того же пораженного с местными и общими симптомами ожога, раны, перелома и т. д., формируется своеобразная пестрая клиническая картина радиационных и травматических или ожоговых симптомов (синдромов).
Вторая характерная особенность КРП — преобладание одного, наиболее тяжелого и выраженного в конкретный момент патологического процесса, вызванного действием одного из этиологических факторов КРП, так называемого «ведущего компонента». Ведущий компонент в клиническом смысле определяет наибольшую опасность для жизни и здоровья пострадавших, а в организационном — требует наиболее срочного оказания помощи в данный конкретный момент. По мере развития патологического процесса вид и значение ведущего компонента могут меняться.
Наконец, третья характерная особенность КРП — взаимовлияние (взаимное отягощение) его нелучевых и лучевых компонентов, проявляющееся в виде более тяжелого течения патологического процесса, чем это свойственно каждому компоненту в отдельности. В результате летальность при КРП оказывается значительно выше, чем при каждой из составляющих его травм, и превосходит их суммарный эффект.
Следует отметить, что даже изолированное воздействие одного из компонентов КРП, вызвавшее острую лучевую болезнь, обширные или глубокие ожоги, тяжелую механическую травму, нередко приводит к летальному исходу. Это связано с отсутствием эволюционно выработанных механизмов, способных привести к выздоровлению при тяжелом ожоге или механическом повреждении, в результате чего развивающиеся компенсаторно-приспособительные процессы отличаются неустойчивостью и заведомой неэффективностью. Сочетание нескольких поражающих факторов приводит к возникновению качественно нового состояния, характеризующегося не просто суммированием повреждений, а развитием синдрома взаимного отягощения.
Синдром взаимного отягощения представляет собой усиление (или утяжеление) патологического процесса при воздействии двух и более этиологических факторов КРП или комплекс симптомов, свидетельствующих о более тяжелом течении каждого компонента КРП, чем это следовало бы ожидать при изолированном течении таких же поражений. Причина его развития состоит в том, что адаптационные процессы при ожоговой и травматической болезни требуют высокой функциональной активности органов и систем, в значительной мере страдающих от воздействия радиации. С другой стороны, восстановление организма от радиационной травмы существенно затрудняется вследствие дополнительного инфицирования, токсемии и других проявлений травматической или ожоговой болезни.
Основной патогенетический механизм развития синдрома взаимного отягощения — ограничение или утрата способности организма противостоять инфекции, а также различным токсическим субстратам гистогенного и бактериального происхождения вследствие радиационного подавления иммунитета. Важную роль в патогенезе этого синдрома играют также генерализованные нарушения метаболизма, приводящие к нарушению энергообеспечения клеток и недостаточности ряда органов и систем (надпочечниковой, тиреоидной, почечной, печеночной).
Следует помнить, что синдром взаимного отягощения развивается лишь тогда, когда сочетаются компоненты КРП не ниже средней степени тяжести. Существенное значение имеет и очередность различных поражающих воздействий, если они произошли не одновременно. Так, если нелучевое повреждение пришлось на период разгара ОЛБ, синдром взаимного отягощения отличается максимальной выраженностью. При нанесении механической травмы или ожога в период выздоровления от ОЛБ в большинстве случаев синдром взаимного отягощения не возникает. В случае если нетяжелая механическая травма предшествует лучевому поражению, нередко отмечается более легкое течение ОЛБ. Это феномен объясняется тем, что предварительно нанесенная легкая травма вызывает активацию неспецифических адаптационных механизмов и, как следствие, повышает устойчивость организма к радиационному воздействию.
В случае развития синдрома взаимного отягощения большей тяжестью отличается клиническое течение каждого из компонентов КРП. По сравнению с «чистыми» радиационными поражениями клиническое течение КРП отличается отсутствием скрытого периода (он' «заполнен» клинической картиной нелучевых компонентов), раньше наступает и более тяжело протекает период разгара, в случае выздоровления дольше длится восстановительный период. Доза облучения, при которой можно рассчитывать на благоприятный исход, снижается в 1,5—2 раза. С другой стороны, для травматической и ожоговой болезни при КРП характерно более тяжелое клиническое течение, увеличение зон некроза ран, замедление репаративных процессов, закономерное развитие раневой инфекции и частая ее генерализация. К другим клиническим проявлениям синдрома взаимного отягощения относятся:
• более частое возникновение и более тяжелое течение ожогового и (или) травматического шока, осложнений постшокового периода;
• более раннее развитие и более тяжелое течение основных синдромов периода разгара ОЛБ — панцитопенического, инфекционного, геморрагического;
• увеличение частоты инфекционных осложнений, повышенная склонность к генерализации инфекции, развитию сепсиса;
• замедленное течение процессов регенерации поврежденных органов и тканей.
Несмотря на пестроту клинической картины КРП, обусловленную наличием проявлений сразу нескольких патологических процессов, в ней, как правило, в каждый конкретный момент удается выделить ведущий компонент, определяющий, в основном, клиническую картину поражения и тяжесть состояния пострадавшего. С течением времени происходит смена ведущего компонента и, как следствие этого, изменяются проявления клинической картины КРП. Однако, несмотря на то что его внешние проявления динамично меняются, этот процесс с начала и до исхода развивается по единому механизму, что позволяет выделить в клинической картине КРП четыре периода.
1. Острый период, или период первичных реакций на лучевые и нелучевые травмы, развивается в первые часы и сутки после воздействия этиологических факторов КРП. Этот период представлен главным образом клиническими проявлениями нелучевых компонентов КРП: у пострадавших развивается травматический или ожоговый шок с выраженным болевым синдромом, массивной кровопотерей, острой дыхательной недостаточностью, очаговыми и общемозговыми неврологическими нарушениями. Признаки первичной реакции на облучение (тошнота, рвота и др.) обычно маскируются более ярко выраженной симптоматикой нелучевых компонентов. Более характерны для нелучевых, чем для радиационных поражений, и ранние гематологические сдвиги: нейтрофильный лейкоцитоз, анемия (при массивной кровопотере), гемоконцентрация (при обширных ожогах или синдроме длительного сдавливания). Важным диагностическим признаком КРП является возникающая на фоне лейкоцитоза абсолютная лимфопения, в то время как при «чистых» ожогах и травмах наблюдается только относительная лимфопения.
2. Период преобладания нелучевых компонентов соответствует раннему постшоковому периоду травматической болезни или периоду острой ожоговой токсемии ожоговой болезни. Однако вследствие развития синдрома взаимного отягощения у пострадавших чаще развиваются и тяжелее протекают характерные для этих периодов осложнения (респираторный дистресс-синдром взрослых, жировая эмболия, острая почечная недостаточность, синдром диссеминированного внутрисосудистого свертывания) и более выражена постгеморрагическая анемия. В случае достаточной длительности скрытого периода ОЛБ (при ОЛБ легкой или средней степени тяжести) и нетяжелого течения нелучевых травм или ожогов в течение второго периода КРП возможно даже полное заживление ран. В то же время к концу этого периода у пострадавших обычно развиваются характерные для лучевых поражений гематологические изменения: лейкоцитоз сменяется лейкопенией, нарастает лимфопения. Именно в этот период и формируются наиболее серьезные патогенетические механизмы синдрома взаимного отягощения.
3. Период преобладания лучевого компонента характеризуется преобладанием симптомов, типичных для периода разгара ОЛБ. В этот период максимально проявляется синдром взаимного отягощения: усугубляются как признаки лучевого панцитопенического синдрома, инфекционных осложнений и кровоточивости, так и выраженность нелучевых компонентов КРП. На фоне замедления регенерации ран развивается раневая инфекция, возрастает вероятность возникновения токсико-септических осложнений и вторичных кровотечений, отмечается повышенная ранимость тканей при операциях и манипуляциях, подавляется демаркация некротизированных участков обожженной кожи, прогрессирует полиорганная недостаточность. Накапливаясь уже во втором периоде КРП, в периоде преобладания лучевого компонента эти изменения значительно увеличивают риск смертельных исходов. Третий период клинического течения КРП обычно является критическим.
4. Период восстановления характеризуется постепенной активизацией регенеративных процессов, восстановлением иммунитета, появлением положительной динамики заживления ран, переломов, ожогов. Вместе с тем многие последствия нелучевых травм (трофические язвы, остеомиелит, ложные суставы, контрактуры, рубцовые деформации и т. п.) могут сохраняться в течение длительного времени, поскольку протекают в условиях функционально неполноценного гемо- и иммунопоэза, что в свою очередь отрицательно сказывается на эффективности лечения пострадавших и увеличивает сроки их нетрудоспособности.
Диагностика КРП заключается в установлении характера и локализации, оценке степени тяжести механической и ожоговой травм, выявлении и установлении степени тяжести радиационного воздействия. При этом используются данные анамнеза, объективного обследования и лабораторных исследований.
В остром периоде основной проблемой в диагностике КРП является индикация и определение дозовых параметров лучевого компонента. Индикация лучевого поражения осуществляется на основании данных анамнеза (нахождение пострадавшего в зоне действия поражающих факторов ядерного взрыва или радиационной катастрофы), данных физической и биологической дозиметрии, в частности, времени появления и выраженности симптомов первичной реакции, особенно рвоты. Ориентировочные данные о частоте и сроках возникновения клинических проявлений эме-тической реакции в случае КРП представлены в табл. 74. Диагноз КРП уточняется по гематологическим показателям облучения (лимфопения, лейкопения), при возможности должны быть проведены кариологические и цитологические исследования.
Таблица 74
Ожидаемая частота и характеристика радиационно индуцированной эметической реакции при комбинированных радиационных поражениях (по Бритуну А. И. и др., 1992)
| Дозы облучения при КРП, Гр | Характеристика эметической реакции |
| 0,8-1,2 | Однократная рвота у 10% пораженных. Возникает в течение первых суток |
| 1,2-1,7 | Однократнвя или повторная рвота у 25% пораженных. Возниквет через 12-24ч |
| 1,7-2,2 | Повторная рвота у 50% пораженных. Возникает через 6-12 ч |
| 2,2-3,3 | Частая многократная рвота у 70-90% пораженных. Возникает через 4-6 ч |
| 3,3-4,5 | Неукротимая рвота у 100% пораженных. Возникает через 2-3 ч |
| Более 4,5 | Неукротимая рвота у 100% порвженных. Возникает через 0,5-1 ч. Могут отмечаться расстройства гемодинамики (коллапс) |
Кроме этого, важным признаком КРП является несоответствие клинической симптоматики и общей тяжести состояния характеру и степени тяжести нелучевых травм. В качестве примера в табл. 75 представлена зависимость степени тяжести КРП от площади термического ожога и степени тяжести острой лучевой болезни.
Таблица 75
Прогнозируемая тяжесть комбинированного радиационно-термического
поражения в зависимости от степени тяжести острой лучевой болезни
и площади глубокого термического ожога
(по Селидовкину Г. Д., Гусеву И. А., 2001) ___________________________________
| Степень тяжести ОЛБ | Площадь глубокого термического ожога, % от площади поверхности тела | |||
| I | Менее 10 | 10-20 | 20-30 | Более 30 |
| II—IV | Менее 1 | 1-5 | Более 10 | |
| Степень тяжести КРП | I (легкая) | II (средняя) | III (тяжелая) | IV (крайне тяжелая) |
Мероприятия медицинской защиты при КРП включают комплексное применение средств противолучевой защиты и методов оказания помощи при нелучевой травме.
На передовых этапах эвакуации при оказании первой и доврачебной помощи наличие или отсутствие радиационного поражения существенным образом не сказывается на обычном объеме мероприятий. В дополнение к обычному перечню внутрь вводятся противорвотные средства, при угрозе инкорпорации радиоактивных веществ — надевается респиратор.
На этапе первой врачебной помощи внутрипунктовая сортировка предусматривает выделение трех групп пострадавших:
• легкопораженные: не нуждающиеся, либо нуждающиеся в минимальной помощи на данном этапе;
• нуждающиеся в оказании первой врачебной помощи с последующей эвакуацией на этап квалифицированной или специализированной помощи;
• пораженные в крайне тяжелом состоянии, которым показана только симптоматическая терапия.
К обычному объему мероприятий первой врачебной помощи, определяемому характером и тяжестью нелучевых повреждений, добавляется проведение частичной санитарной обработки, смена повязок, загрязненных радиоактивными веществами, купирование проявлений первичной реакции.
Основные принципы медицинской сортировки при оказании квалифицированной и специализированной медицинской помощи совпадают. Только на этих этапах появляется возможность произвести исчерпывающую медицинскую сортировку по всем группам пораженных с КРП. Следует помнить, что пострадавшие с КРП легкой степени тяжести не нуждаются в специализированном лечении, а пострадавшие с крайне тяжелыми поражениями направляются для оказания симптоматической помощи.
Ключевым моментом лечения КРП является использование скрытого периода острой лучевой болезни для проведения хирургических мероприятий, что обусловлено невозможностью длительного открытого ведения ран и необходимостью добиться их заживления до начала периода разгара ОЛБ.
В первом периоде КРП (первичной реакции на лучевые и нелучевые травмы) основные усилия должны быть направлены на ликвидацию последствий нелучевых повреждений и профилактику их осложнений. С этой целью проводятся мероприятия, направленные на восстановление внешнего дыхания, окончательную остановку кровотечения, обезболивание, иммобилизацию, профилактику раневой инфекции и т. д., а если имеются признаки первичной реакции на облучение, необходимо их купировать с помощью противорвотных препаратов. Во втором периоде (преобладания нелучевых компонентов) проводится первичная хирургическая обработка ран и открытых переломов, лечение ожогов, а также все мероприятия квалифицированной и специализированной хирургической помощи, выполнение которых не может быть отсрочено до завершения периода разгара ОЛБ. В третьем периоде КРП (преобладания лучевого компонента) проводятся медицинские мероприятия, направленные на борьбу с панцитопеническим, инфекционным и геморрагическим синдромами. Хирургические вмешательства выполняются только по жизненным показаниям (наружные и внутренние кровотечения, перфорации полых органов и т. д.). В четвертом периоде (восстановления) осуществляется патогенетическая и симптоматическая терапия остаточных явлений лучевого поражения и лечение последствий нелучевых травм.
Часть Ш
СРЕДСТВА И МЕТОДЫ ПРОФИЛАКТИКИ ХИМИЧЕСКИХ И РАДИАЦИОННЫХ ПОРАЖЕНИЙ
 |  | ||
 |
H
»
Технические средства индивидуальной защиты подразделяются на средства защиты органов дыхания (СИЗОД), средства защиты глаз (СИЗГ) и средства защиты кожи (СИЗК).
24,1.1. Средства индивидуальной защиты органов дыхания
К средствам защиты органов дыхания относятся противогазы, респираторы, изолирующие дыхательные аппараты, часто называемые изолирующими противогазами, комплект дополнительного патрона. Средства защиты органов дыхания подразделяются на фильтрующие и изолирующие, а также на общевойсковые и специальные (табл. 77).
Таблица 77
Средства индивидуальной защиты органов дыхания
| Общевойсковые |
| Специальные |
| Противогаз ракетных войск универсальный ПРВ-У Противогаз ракетных войск модернизированный ПРВ-М Противогаз фильтрующий летного состава ПФЛ Респиратор морской РМ-2 Комплект дополнительного патрона КДП |
Принцип защитного действия
Фильтрующие
Противогаз малогабаритный ПМГ Противогаз малогабаритный ПМГ-2 Противогаз масочный коробочный ПМК
Противогаз масочный коробочный ПМК-2
Противогаз масочный коробочный ПМК-3
| Изолирующий дыхательный аппарат морской ИП-6 Портативный дыхательный аппарат ПДА-3 Шланговый дыхательный аппарат ШДА |
Респиратор Р-2 Респиратор общевойсковой универсальный РОУ
| Изолирующие |
Изолирующий дыхательный аппарат ИП-4
Изолирующий дыхательный аппарат ИП-4М
Изолирующий дыхательный аппарат ИП-5
24.1.1.1.
Эксплуатационная характеристика
Фильтрующие противогазы предназначены для защиты органов дыхания, зрения и кожи лица личного состава от отравляющих и высокотоксичных веществ (ОВТВ), радиоактивных веществ (РВ) и биологических средств (БС), а также для уменьшения интенсивности поражения световым излучением ядерных взрывов. Защитное действие фильтрующих противогазов основано на том, что используемый для дыхания воздух предварительно очищается от вредных примесей в результате процессов адсорбции, хемо-сорбции, катализа и фильтрации через зернистые поглотители.
4ВО
Общевойсковой фильтрующий противогаз состоит из фильтрующе-поглощающей системы, выполненной в виде фильтруюше-поглотитель-ной коробки или фильтрующе-поглотительного элемента, лицевой части и противогазовой сумки. При угрозе отравления угарным газом фильтрую-ще-поглощающая система выполняется в виде фильтрующе-поглотитель-ной коробки и комплекта дополнительного патрона. В фильтрующе-по-глощающей системе первым по току воздуха помещен противоаэрозоль-ный фильтр, а затем — специальный поглотитель (шихта), созданный на основе активированного угля с различными химическими добавками (дегазаторами, катализаторами и др.).
Лицевая часть противогаза изготовлена в виде шлем-маски или маски, конструктивными элементами которой являются очковый узел, обтекатели для предохранения стекол от запотевания, клапанно-распредели-тельная коробка и система крепления на голове. Правильно подобранная лицевая часть должна плотно прилегать краями к голове, обеспечивать необходимую герметизацию, не вызывая болевых ощущений. Для сохранения нормальной громкости речи в противогазе имеются лицевые части, которые содержат мембранное переговорное устройство, а специальная конфигурация стекол очков в противогазах позволяет работать с оптическими приборами. Кроме того, лицевая часть ряда противогазов оборудуется подмасочником, обтюратором и системой для приема жидкости. Подбор соответствующего размера лицевой части противогаза в каждом случае осуществляется индивидуально.
Герметичность противогаза проверяется в специальной палатке, предназначенной для проверки противогазов в атмосфере с учебными ОВТВ. Проверка технического состояния противогазов проводится в соответствии с Руководством по использованию средств индивидуальной защиты. В этом же Руководстве подробно описаны устройство и правила пользования всеми имеющимися в Вооруженных Силах РФ противогазами и другими техническими средствами индивидуальной защиты.
Защитная мощность фильтрующих противогазов по парам летучих отравляющих и высокотоксичных веществ, по аэрозолю радиоактивных веществ и биологических средств характеризуется динамической активностью (сорбционной емкостью), временем защитного действия и общим коэффициентом защиты. Защитная мощность зависит от физико-химических свойств, способа применения, концентрации ОВТВ, РВ или БС в воздухе, от метеорологических условий, а также от объема легочной вентиляции, который определяется прежде всего интенсивностью физической нагрузки.
Динамическая активность (сорбционная емкость) — это показатель, характеризующий поглощающую способность фильтрующе-поглощаю-щей системы. Она выражается массой пара ОВТВ, сорбированного за время защитного действия. Под временем защитного действия понимают время с момента начала прохождения через фильтрующе-поглощающую систему паровоздушной смеси, содержащей ОВТВ, до момента появления предельно-допустимой концентрации паров этого вещества, обнару-
живаемого специальным индикатором. Оба эти показателя связаны между собой следующим соотношением:
М = G х С х V,
где М — динамическая активность фильтрующе-поглощающей системы, г;
G — время защитного действия, мин; 11
С — концентрация ОВТВ, РВ или БС, г/м3; V — объем легочной вентиляции, м3/мин.
Показателем, характеризующим способность противоаэрозольного фильтра задерживать аэрозоли ОВТВ, РВ или БС, является коэффициент проскока. Коэффициент проскока (Кф) представляет собой отношение концентрации аэрозоля, прошедшего через фильтр (Сф), т. е. проникшего внутрь противогаза, к концентрации аэрозоля в атмосфере (Са), выраженное в процентах:
Кф = Сф/Сах 100.
Показателем, характеризующим правильность подбора лицевой части противогаза, а следовательно, его герметичность, является коэффициент подсоса. Коэффициент подсоса (Кподс) представляет собой отношение концентрации ОВТВ, РВ или БС, проникших под маску противогаза (См), к концентрации этих веществ в атмосфере (Са), выраженное в процентах:
Кподс. = СМ/Сах 100.
Из суммы коэффициента проскока (Кф) и коэффициента подсоса (Кподс.) и складывается общий коэффициент защиты (К3) фильтрующего противогаза:
К3 = Кф + кподс.
Фильтрующие противогазы обеспечивают эффективную защиту личного состава от ОВ при ведении боевых действий в течение одной-двух фронтовых операций, однако длительное использование противогазов в атмосфере маскирующих дымов может привести к ухудшению их защитных и физиолого-гигиенических свойств. Шлем-маски фильтрующих противогазов защищают человека от капельно-жидких ОВ в течение 6-10 ч, а отравляющие вещества, находящиеся в парообразном состоянии, так же как радиоактивные вещества и биологические средства, через резину лицевой части в боевых условиях не проникают. В то же время лицевые части общевойсковых противогазов обладают низкими термозащитными свойствами, поэтому для защиты от светового излучения ядерного взрыва их необходимо использовать совместно со средствами индивидуальной защиты кожи. Кроме того, в условиях применения ядерного оружия поверх противогаза необходимо надевать защитные очки ОФ или ОПФ. Время надевания противогаза в зараженной отравляющими и высокотоксичными веществами, радиоактивными веществами или биологическими средствами атмосфере не должно превышать 10 с.
В настоящее время на оснащении Сухопутных войск Вооруженных Сил состоят фильтрующие противогазы ПМГ, ПМГ-2, ПМК, ПМК-2, ПМК-3. В Ракетных войсках используются фильтрующие противогазы ПРВ-У и ПРВ-М, в Военно-Воздушных силах — противогаз ПФЛ.
Противогаз ПМГ состоит из фильтрующе-поглотительной коробки ЕО-18К, выполненной в форме цилиндра, и шлем-маски ШМГ, снабженной переговорным устройством и левосторонним или правосторонним узлом присоединения фильтрующе-поглощающей коробки с клапаном вдоха. Фронтальное расположение и размеры стекол очкового узла обеспечивают возможность работы с оптическими приборами.
В состав противогаза ПМГ-2 входит цилиндрической формы филь-трующе-поглотительная коробка ЕО-62К, которая присоединяется к подбородочной части шлем-маски ШМ-62. ПМГ-2 может выпускаться со шлем-маской ШМ-ббМу, в которой предусмотрено переговорное устройство и сквозные вырезы для ушных раковин, что обеспечивает нормальную слышимость.
Противогаз ПМК состоит из фильтрующе-поглотительной коробки ЕО. 1.08.01 в форме цилиндра и маски М-80 с переговорным устройством, системой для приема жидкости и наголовником. Маски М-80 выпускают с левосторонним (90%) и правосторонним (10%) расположением узла присоединения фильтрующе-поглощающей коробки.
Противогаз ПМК-2 является модернизированным образцом противогаза ПМК. В маске МБ-1-80, входящей в состав ПМК-2, в щечных областях имеются два отверстия — левое и правое, для удобного присоединения фильтрующе-поглотительной коробки правшам и левшам. После присоединения фильтрующе-поглотительной коробки к одному из отверстий, противоположное отверстие закрывают заглушкой.
В состав противогаза ПМК-3 входит маска МБ-2, имеющая два (левый и правый) узла для присоединения фильтрующе-поглотительной коробки, переговорное устройство и приспособление для приема воды, фильтрую-ше-поглотительная коробка КБ-2В (войсковая) или КБ-2У (универсальная) и капюшон. Фильтрующе-поглотительная коробка КБ-2У способна защищать органы дыхания не только от отравляющих веществ, биологических средств и радиоактивного аэрозоля, но и от воздействия хлора и аммиака.
Противогазы ракетных войск ПРВ-У и ПРВ-М предназначены для защиты органов дыхания, лица и глаз от отравляющих веществ, биологических средств и радиоактивного аэрозоля, а также от паров ракетных топ-лив и окислителей. Они состоят из шлем-маски ШМС-Р, гофрированной соединительной трубки, защищенной прорезиненным чехлом, и специальной фильтрующе-поглотительной системы. В противогазе ПРВ-У фильтрующе-поглотительная система представляет собой фильтруюше-по-глотительную коробку в виде цилиндра и дополнительную коробку для зашиты от воздействия компонентов ракетных топлив, которая навинчивается на фильтрующе-поглощаюшую коробку. В модернизированных образцах ПРВ-М фильтрующе-поглотительная система выполнена в виде одной коробки. Сумка противогаза изготовлена из прорезиненной ткани.
4Б2
Противогаз фильтрующий летный ПФЛ состоит из лицевой части, соединительной трубки и фильтрующе-поглотительной коробки КПЛ. В комплект противогаза ПФЛ также входят коробка с незапотевающими пленками НПН, полиэтиленовый пакет и сумка.
Фильтрующе-поглотительная коробка КПЛ является средством одноразового боевого применения. Ее масса составляет 180 г. Она изготовлена в виде изогнутого прямоугольника высотой 130 мм, шириной 100 мм, толщиной 35 мм с целью удобного ее размещения в кармане защитного снаряжения летчика. На верхней ее части размещена горловина с резьбой, предназначенная для присоединения коробки к соединительной трубке. Соединительная трубка состоит из двух частей, соединенных между собой замком байонетного типа. В случае необходимости байонет-ный замок расстыковывается и часть трубки, соединенная с маской, может быть подключена к кислородному прибору КП-98. Маска противогаза ПФЛ состоит из резинового корпуса объемного типа с независимым обтюратором, изготовленным за одно целое с корпусом, узла клапанов вдоха и выдоха, панорамного стекла, подмасочника, радиогарнитуры и пятилямочного наголовника.
Необходимо помнить, что в силу своих конструктивных особенностей фильтрующе-поглотительные коробки современных противогазов не способны обезвредить оксид углерода (угарный газ). В связи с этим для защиты от вредного воздействия оксида углерода применяется комплект дополнительного патрона (КДП), в состав которого входят соединительная трубка, патрон ДП-2, представляющий собой цилиндрическую коробку, снаряженную осушителем, гопкалитом и катализатором, противо-аэрозольный фильтр и сумка. Проходя через дополнительный патрон ДП-2, воздух с оксидом углерода в слое осушителя освобождается от влаги, а затем, взаимодействуя с гопкалитовой смесью, превращается в углекислый газ. Комплект дополнительного патрона эффективен в широком диапазоне температур: от — 40° С до + 40° С. При положительной температуре время защитного действия комплекта дополнительного патрона составляет до 400 мин, при температуре минус 40° С и наличии водорода — около 70 мин. Повышенная влажность воздуха практически не влияет на работу прибора.
Следует помнить, что при концентрации оксида углерода свыше 1%, при недостатке в воздухе кислорода (концентрация менее 17%) и при пожарах в закрытых помещениях комплект дополнительного прибора малоэффективен. В этих случаях необходимо пользоваться изолирующими дыхательными аппаратами (изолирующими противогазами).
Респираторы предназначены для защиты органов дыхания от аэрозолей радиоактивных веществ и биологических средств. Респираторы не защищают от паров ОВТВ и газов и не обогащают вдыхаемый воздух кислородом, в связи с чем их можно использовать только в атмосфере, свободной от ОВТВ и содержащей не менее 17% кислорода.
Респираторы представляют собой фильтрующую полумаску, снабженную клапанами вдоха и выдоха. Полумаска с помощью наголовника крепится на голове, а носовой зажим обеспечивает более герметичное прилегание полумаски в области носа. Современные респираторы выполнены на основе фильтрующего материала, предложенного в 1955 г. академиком И. В. Петряновым-Соколовым. Фильтры Петрянова представляют собой гидрофобный полимер из ультратонких волокон полихлорвиниловой, полистироловой или метилметакрилатной ткани. Эта ткань обладает большим и стойким электростатическим зарядом, притягивающим аэрозольные частицы. При увеличении скорости потока аэрозоля за счет возрастания трения заряд ткани увеличивается, что способствует лучшему удержанию частиц на фильтрах. При правильном хранении и использовании электростатический заряд на фильтрах Петрянова способен удерживаться в течение десяти лет. Хранится респиратор в полиэтиленовом пакете, так как при намокании респиратора его фильтрующая способность и, следовательно, его защитные свойства, значительно снижаются. Коэффициент проскока в респираторах не превышает 0,1%.
Респиратор Р-2 состоит из фильтрующей полумаски и наголовника. Фильтрующая полумаска изготовлена из трех слоев материалов. Внешний слой — пенополиуретан защитного цвета, внутренний — воздухонепроницаемая полиэтиленовая пленка с вмонтированными двумя клапанами вдоха, а между пенополиуретаном и пленкой расположен слой фильтрующего материала из полимерных волокон ткани Петрянова. Клапан выдоха размещен в передней части полумаски и закрыт снаружи экраном.
Респиратор морской РМ-2 является модификацией респиратора Р-2. Он предназначен для защиты органов дыхания от радиоактивных аэрозолей, а также от воздействия паров радиоактивного йода и полония. РМ-2 состоит из полумаски с наголовником, на которой размещены фильтрующая коробка с клапанами вдоха и выдоха и переговорное устройство.
Респиратор общевойсковой универсальный РОУ состоит из лицевой части в виде фильтрующе-сорбирующей маски с очковым узлом, которая выполняет одновременно функции лицевой части и фильтрующе-сорби-рующего элемента. В отличие от респиратора Р-2 респиратор РОУ предназначен также для защиты глаз от светового излучения ядерного взрыва и органов дыхания от паров отравляющих веществ.
Изолирующие дыхательные аппараты (изолирующие противогазы) предназначены для защиты органов дыхания, лица и глаз при наличии во внешней среде ОВТВ, которые не задерживаются фильтрующим противогазом, при полном отсутствии или недостатке кислорода в воздухе, а также при работах в очагах химического поражения в условиях высоких концентраций паров и плотностей заражения любых ОВТВ. Кроме того, изолирующие дыхательные аппараты могут использоваться при повышенном содержании в атмосфере оксида углерода (в концентрации более 1%), при форсировании водных преград или выполнении работ на небольших глубинах.
Защитные свойства изолирующих дыхательных аппаратов не зависят от природы отравляющих и высокотоксичных веществ, радиоактивных веществ, биологических средств или от их концентрации в воздухе; они способны защищать органы дыхания от любых вредных примесей, находящихся в воздухе. Они используются для проведения спасательных работ и лечебно-эвакуационных мероприятий в очагах химического поражения, для работ с высокотоксичными и агрессивными газообразными веществами, парами и аэрозолями ОВТВ и деятельности в условиях недостатка кислорода.
В изолирующих противогазах человек дышит газовой смесью с повышенным содержанием кислорода и углекислоты. Содержание кислорода обычно колеблется в пределах 70-90%, а углекислого газа 2-3%. Опасным пределом, за которым может наступить потеря сознания при выполнении физической нагрузки, считается 9-11% кислорода во вдыхаемом воздухе. Содержание углекислого газа во вдыхаемом воздухе до 1% практически не вызывает нарушения функций организма. Нарастание углекислого газа до 2% ведет к учащению дыхания и увеличению объема легочной вентиляции, а увеличение концентрации С02 свыше 3% опасно для организма человека.
По принципу обеспечения кислородом все средства защиты органов дыхания изолирующего типа делятся на пневматогены и пневматофоры.
К пневматогенам относятся изолирующие дыхательные аппараты ИП-46, ИП-46М, ИП-4, ИП-5, ИП-6, ПДА-3, в которых кислород получается химическим путем. В противогазах такого устройства дыхание осуществляется по маятниковому типу.
Изолирующие дыхательные аппараты из группы пневматогенов состоят из лицевой части, регенеративного патрона с пусковым приспособлением, дыхательного мешка и противогазовой сумки. В регенеративном патроне кислород содержится в химически связанном состоянии в виде надперекисей. Он высвобождается в процессе дыхания при взаимодействии с углекислотой и водяными парами выдыхаемого воздуха. Однако процесс развития реакции, особенно при низких температурах окружающий среды, происходит достаточно медленно, поэтому в работе пневматогенов имеется начальный период, в котором из-за медленного течения реакции не обеспечивается достаточно полная регенерация дыхательной смеси. В связи с этим для устранения опасности, связанной с недостатком кислорода в дыхательной смеси, используется специальное пусковое устройство, предназначенное для выделения необходимого для дыхания количества кислорода в период пуска регенеративного патрона.
К пневматофорам относятся противогазы КИП-5, ИПСА и шланговый дыхательный аппарат ИЩА. В приборах такого типа кислород находится в баллонах в сжатом виде.
В настоящее время на оснащение Вооруженных Сил приняты усовершенствованные образцы изолирующих дыхательных аппаратов ИП-4, ИП-4М и ИП-5. На Военно-Морском Флоте используются аппараты ИП-6, ПДА-3 и ШДА-
Изолирующий дыхательный аппарат ИП-4 предназначен только для работы на суше. Регенеративный патрон РП-4 имеет форму цилиндра, на верхней крышке которого имеется пусковое устройство винтового типа с чекой и пломбой. Шлем-маска ШИП-2б(к) состоит из корпуса с обтюратором и переговорным устройством, очкового узла и защищенной чехлом из прорезиненной ткани соединительной трубки, наглухо присоединенной к шлем-маске. Дыхательный мешок имеет форму прямоугольного параллелепипеда, защищенного каркасом из дюралюминия. Клапан избыточного давления находится в выворотном фланце мешка.
Изолирующий дыхательный аппарат ИП-5 предназначен для выхода из затонувших объектов бронетанковой техники и выполнения легких работ под водой на глубине не более 7 м, но может использоваться и на суше. Регенеративный патрон РП-5 имеет форму параллелепипеда со скругленными боковыми гранями, на верхней крышке которого имеется пусковое устройство рычажного типа. Шлем-маска ШИП-М состоит из корпуса с обтюратором, очкового узла и соединительной трубки, но, в отличие от ШИП-2б(к), не имеет переговорного устройства и используется с подма-сочником. Дыхательный мешок выполнен в виде емкости кольцевой формы, внутри которой проходит трубка для соединения шлем-маски с регенеративным патроном. При работе в ИП-5 дыхательный мешок в чехле надевается вокруг шеи и крепится к нагруднику.
Изолирующий дыхательный аппарат ИП-6 является модификацией аппарата ИП-4, предназначенной для личного состава Военно-Морского Флота. От ИП-4 отличается конструкцией лицевой части и дыхательного мешка: в ИП-6 используется маска МИА-1 с переговорным устройством, регенеративный патрон защищен футляром, который крепится поясным ремнем спереди на груди, дыхательный мешок имеет дугообразную форму, находится в защитном чехле и в положениях «наготове» и «боевом» надевается на шею сзади в виде воротника.
Портативный дыхательный аппарат ПДА-3 предназначен для экстренной защиты органов дыхания при эвакуации личного состава надводных и подводных кораблей из загазованной зоны в аварийных ситуациях, а также для выполнения кратковременных работ по предупреждению развития аварии в этих условиях. Он состоит из маски МПДА, регенеративного патрона, пускового устройства, дыхательного мешка, теплоизо-лятора и футляра. Маска МПДА представлена в виде корпуса с обтюратором, очкового узла, соединительной трубки, наглухо присоединенной к маске, и наголовника, имеющего пряжки для подгонки маски по размеру головы.
Шланговый дыхательный аппарат ШДА относится к пневматофорам и используется только в составе стационарной дыхательной системы. Он защищает органы дыхания, глаза и кожу лица от любых вредных примесей, а также применяется при недостатке кислорода в отсеке. В состав ШДА входят лицевая часть, выполненная в форме маски МИА-1 с переговорным устройством, легочной автомат, соединительный шланг длиной 3 м, приборный ящик с крышкой, транспортная заглушка и поясной ремень.
Маска служит для изоляции органов дыхания, глаз и кожи лица от окружающей атмосферы и подвода воздуха к органам дыхания. Легочный автомат обеспечивает редуцирование и подачу воздуха к органам дыхания, а также удаление выдыхаемого воздуха в окружающую атмосферу. Шланг служит для подвода сжатого воздуха от раздаточного трубопровода

стационарной дыхательной системы к легочному автомату. Поясной ремень предназначен для фиксации шланга при переводе ШДА в положение «боевое». Приборный ящик с крышкой служит для размещения и хранения ШДА на штатном месте.
Изолирующие дыхательные аппараты являются надежными средствами защиты в экстремальных ситуациях, однако несоблюдение мер безопасности и правил пользования ими может привести к тяжелым последствиям. При снятии маски в непригодной для дыхания атмосфере возможно отравление вредными веществами. Несрабатывание пускового брикета, повторное использование пневматогенов после перерыва в работе со снятием маски может привести к кислородному голоданию с внезапной потерей сознания или отравлению вредными веществами. При контакте органических веществ с перекисными соединениями, содержащимися в регенеративном патроне, происходит их возгорание, часто сопровождаемое взрывом. Практически все реакции, которые происходят в регенеративном патроне, экзотермические, т. е. идут с выделенем тепла, что может привести к ожогу верхних дыхательных путей. Наконец, удары или другие механические воздействия по дыхательному мешку могут вызвать резкое повышение давления воздушной смеси и привести к развитию баротравмы легких.
В целях оказания первой помощи пострадавших необходимо вынести из зоны заражения, снять маску и немедленно сделать искусственное дыхание. Несвоевременное оказание первой помощи, особенно при отравлении или кислородном голодании, как правило, приводит к смертельному исходу. В связи с этим, работа личного состава с использованием изолирующих дыхательных аппаратов должна проводиться под строгим медицинским контролем.
Время работы в изолирующих дыхательных аппаратах определяется физической нагрузкой (табл. 78).
24.1.1.2. Факторы, определяющие порядок использования средств защиты органов дыхания
Нахождение в СИЗОД сопровождается определенными изменениями физиологических функций организма. Степень их выраженности зависит от состояния здоровья, тренированности и характера деятельности личного состава. Основными неблагоприятно действующими на организм факторами фильтрующих и изолирующих противогазов и, в меньшей степени, респираторов являются сопротивление дыханию, воздействие вредного пространства и влияние лицевой части на кожу лица и органы чувств.
Сопротивление дыханию обусловлено трением воздуха при его движении через противогаз, особенно через респираторную и клапанную коробки. При слабой физической нагрузке сопротивление вдоху составляет 25—30 мм вод. ст., а при тяжелой оно может достигать 250-280 мм вод. ст. и более. Вследствие высокого сопротивления дыханию уменьшается объем легочной вентиляции, возрастает частота дыхания, дыхание становится поверхностным. Преодоление сопротивления дыханию на вдохе вызывает также понижение внутригрудного давления, которое может колебаться от 5 до 300 мм вод. ст. В свою очередь все это приводит к увеличению частоты сердечных сокращений, усиленному притоку крови к правому предсердию, затруднению систолы, застою в малом круге кровообращения и в портальной системе. Отрицательное влияние сопротивления дыханию прогрессирующе нарастает с увеличением физической нагрузки, а при высокой напряженности работы становится серьезным неблагоприятным фактором, влияющим на физиологические функции организма.
Вредное пространство представляет собой объем под маской противогаза, в котором задерживается выдыхаемый воздух с избыточным содержанием углекислого газа и водяных паров. В лицевых частях современных противогазов вредное пространство составляет около 200 см3. Негативное влияние вредного пространства на организм связано с тем, что избыточное содержание углекислого газа в подмасочном пространстве противогаза вызывает учащение дыхания и увеличение частоты сердечных сокращений. Особенно возрастает отрицательное влияние вредного пространства на организм при поверхностном и частом дыхании, в связи с чем дышать в противогазе следует реже и глубже. Необходимо учитывать, что сопротивление дыханию и вредное пространство действуют на организм совместно, но в покое более существенно влияние вредного пространства, а при тяжелой физической нагрузке — сопротивления дыханию.
Вредное влияние лицевой части противогаза на органы чувств связано с тем, что она вызывает уменьшение полей зрения (примерно на 30—50%), нарушение остроты и бинокулярности зрения, затруднение восприятия звуков (понижение слышимости), выключение функций вкусового анализатора и анализатора обоняния. Громкость речи в шлем-масках проти-
вогазов, не имеющих переговорных устройств, снижается на 35-40%, а при наличии подобных устройств — на 20-30%. Кроме того, лицевая часть противогаза оказывает выраженное давление на мягкие ткани лица и головы, сопровождающееся болезненными ощущениями и покраснением кожи лица. Неправильно подобранная лицевая часть противогаза может вызывать сильные болевые ощущения в области надбровных дуг, скул, подбородка и ушей, что также затрудняет длительное пребывание в нем. При пребывании в противогазе нарушается потоотделение, что наряду с механическим сдавливанием отдельных участков кожи лица в летнее время может приводить к возникновению мацерации кожи, наминов и рубцов, а в зимнее время способствовать развитию отморожений.
Таким образом, длительное пребывание в СИЗОД предъявляет к организму повышенные требования, прежде всего к органам дыхания и кровообращения, особенно к состоянию дыхательной мускулатуры. Определенные затруднения при выполнении профессиональных обязанностей в СИЗОД возникают вследствие ограничения функции различных анализаторов. В связи с этим, для уменьшения эффектов неблагоприятного влияния на организм вредных факторов противогазов необходимо проводить противогазовые тренировки. Их целью является выработка приспособительных физиологических реакций в организме, способствующих улучшению переносимости СИЗОД.
Противогазовая тренировка складывается из занятий для общего укрепления организма и специальных упражнений. Основу противогазовой тренировки составляет физическая подготовка, в частности, занятия бегом, лыжами, переползание по-пластунски, плавание и гребля. Все эти виды занятий повышают резервные возможности организма и способствуют увеличению запасов адаптационных резервов в дыхательных мышцах и в сердце. Специальные упражнения связаны с выполнением различных вариантов физических нагрузок в СИЗОД. Тренировка организуется по принципу планомерного усложнения физической нагрузки и увеличения времени пребывания в противогазе. Марш в противогазах с возрастающей скоростью и продолжительностью, кратковременный бег, переползание и выполнение земляных работ способствуют налаживанию правильного дыхания, адаптируют сердечно-сосудистую деятельность. Начальник медицинской службы консультирует командование части при разработке плана противогазовой тренировки, осуществляет медицинский контроль в ходе ее проведения, а также принимает участие в систематических тренировках физически ослабленных людей. Целью медицинского контроля является определение характера реакций организма в ответ на воздействие СИЗОД, что позволяет своевременно предупредить появление патологических изменений физиологических функций организма.
24.1.1.3. Использование СИЗОД для защиты раненых и больных
В условиях зараженной ОВТВ атмосферы своевременное применение противогазов имеет важное значение и для защиты раненых и больных.
В зависимости от характера ранения или заболевания и способности пострадавшего пользоваться СИЗОД раненых и больных на этапах медицинской эвакуации можно разделить на четыре группы:
I. Способные пользоваться общевойсковым противогазом и самостоя-
тельно надеть его.
II. Способные пользоваться общевойсковым противогазом, но требу-
ющие помощи при его надевании.
III. Нуждающиеся в противогазе со шлемом для раненных в голову.
IV. Нуждающиеся в размещении в объектах коллективной защиты, оборудованных в противохимическом отношении, поскольку надевание общевойскового противогаза пострадавшим этой категории противопоказано.
Сортировка раненых и больных по способу защиты осуществляется медицинским составом путем закрепления специальных маркировочных талонов или марок.
Раненые, способные пользоваться общевойсковым противогазом и самостоятельно надеть его, делают это по общим правилам.
Надевание противогаза на раненого, не способного самостоятельно это сделать, производится в порядке взаимной помощи товарищами, санитарами или санитарными инструкторами. При надевании противогаза учитываются состояние раненого, характер повреждения и боевая обстановка.
Вне сферы воздействия огня противника оказывающий помощь должен посадить раненого в удобное положение (между своих ног), снять с него каску (головной убор), вынуть шлем-маску (маску) из сумки, подвести ее к подбородку и, растягивая резину пальцами от подбородка к голове, надеть шлем на голову.
При надевании противогаза под огнем противника оказывающий помощь укладывает раненого на спину, ложится на живот рядом с ним и надевает шлем-маску (маску), выполняя последовательно все указанные выше приемы.
Если пострадавший лежит на животе, то оказывающий помощь также ложится рядом на живот, после чего достает шлем-маску (маску), подводит ее под лицо раненого, берет лицевую часть так, чтобы большие пальцы были внутри, а остальные снаружи, и указанными приемами надевает шлем на голову.
Для индивидуальной защиты раненых и обожженных с ранениями и повреждениями головы создана специальная лицевая часть — шлем для раненных в голову (ШР). Шлем для раненных в голову выпускается одного размера и используется в комплекте с фильтрующе-поглощающей коробкой общевойскового противогаза. Он применяется непосредственно на месте поражения и на путях медицинской эвакуации.
 |
Шлем для раненных в голову представляет собой резиновый мешок в виде капюшона, в который вмонтированы очки, вдыхательный и выдыхательный клапаны и соединительная трубка. На боковых поверхностях шлема имеются три пары тесемок, после завязывания которых уменьшается величина вредного пространства. Линия герметизации шлема находится на шее.
Шлем для раненных в голову надевается в определенной последовательности.
При надевании шлема на пострадавших с повреждениями головы нижнюю его часть подводят под подбородок, после чего развертывают и надевают шлем на голову.
При надевании шлема на раненного в челюстно-лицевую область подводят основание клиновидного клапана под затылок, добиваясь первичной герметизации. Затем переднюю часть шлема подтягивают к поверхности лица и головы, завязывая тесемки. Раненых с черепно-мозговой травмой после надевания шлема укладывают на левый бок, а с челюстно-лицевыми ранениями — на живот.
Снятие шлема с раненных в голову производится в обратном порядке. После использования шлема необходимо промыть его теплой водой с мылом, протереть тампоном, смоченным в 2% растворе формалина или спиртом, и высушить на воздухе.
Находящийся в противогазе раненый нуждается в систематическом наблюдении (осмотр кожи лица и состояния зрачков, контроль за частотой дыхания и пульса) и уходе. Необходимо следить за тем, чтобы не была зажата соединительная трубка, не была залита слюной и рвотными массами клапанная коробка. При появлении у раненых рвоты и засорении клапанов слюной и рвотными массами необходимо срочно заменить шлем-маску или маску ШР.
Определенная часть раненых и пораженных в силу своего состояния не может пользоваться СИЗОД. Медицинские противопоказания к использованию противогазов можно разделить на абсолютные и относительные. К абсолютным противопоказаниям относятся тяжелые ранения и заболевания, при которых даже в условиях покоя использование противогаза невозможно или связано с большой опасностью и риском:
• проникающие ранения грудной полости и все повреждения головы, связанные с повышением внутричерепного давления;
• легочные, носовые и желудочные кровотечения;
• бессознательное состояние;
• неукротимая рвота;
• судороги;
• органические заболевания сердца с явлениями декомпенсации;
• склероз венечных сосудов со стенокардией;
• тяжелые заболевания легких и плевры (пневмония, отек легких, абсцессы, экссудативные плевриты и др.);
• обильные выделения из носа, резко выраженный бронхоспазм при поражении ФОВ и др.
Такие раненые и больные должны размещаться в объектах коллективной защиты, оборудованных в противохимическом отношении.
К относительным противопоказаниям следует отнести заболевания, допускающие использование противогаза для защиты, но требующие осторожности или определенного ограничения, а иногда запрещения тренировок. К ним относятся функциональные заболевания сердца и сосудов, хронические заболевания дыхательных путей, болезни почек и др. Пораженным этой категории нужно использовать противогазы только для спасения жизни в. условиях зараженной среды.
24.1.2. Средства индивидуальной защиты кожи
Для защиты кожных покровов используются средства индивидуальной защиты кожи (СИЗК). Они защищают от отравляющих и высокотоксичных веществ, действующих на кожу и через кожу, радиоактивных веществ, бактериальных аэрозолей и токсинов, а также от светового излучения ядерного взрыва и зажигательных смесей. По принципу защитного действия все средства индивидуальной защиты кожи делятся на изолирующие и фильтрующие. По способу использования различают средства защиты кожи постоянного ношения, периодического применения и однократного использования.
К средствам индивидуальной защиты кожи относятся: общевойсковой комплексный защитный костюм фильтрующего типа (ОКЗК-М, ОКЗК-Д), комплект защитной фильтрующей одежды (КЗФО), общевойсковой защитный комплект фильтрующий (ОЗК-Ф), общевойсковой защитный комплект изолирующего типа (ОЗК) и специальная защитная одежда (костюм Л-1, комплекты защитные морские КЗМ-1 и КЗМ-2, комплект защитный № 6 и др.) (табл. 79).
24.1.2.1. Эксплуатационная характеристика
Защита кожи средствами индивидуальной защиты фильтрующего типа основывается на обезвреживании аэрозоля или паров отравляющих и высокотоксичных веществ при прохождении их через толщу бдлья и обмундирования, предварительно импрегнированного специальными дегазирующими рецептурами.
Общевойсковой комплексный защитный костюм (ОКЗК-М) предназначен для защиты кожных покровов личного состава от отравляющих и высокотоксичных веществ, радиоактивного аэрозоля, биологических средств и светового излучения ядерного взрыва, а также от неблагоприятных воздействий погодных условий на уровне и ниже летнего армейского обмундирования. Он состоит из пилотки с козырьком, позволяющим защитить глаза от светового излучения ядерного взрыва, куртки с отлетными козырьками на низках рукавов и брюк. На пилотку надевается подшлемник, а под куртку и брюки — защитная рубашка и кальсоны. В комплекте с ОКЗК-М могут использоваться фильтрующий противогаз и защитные чулки, а поверх него может надеваться костюм защитный сетчатый КЗС, представляющий собой куртку с капюшоном и брюки.
Защитные свойства ОКЗК-М от действия светового излучения ядерного взрыва обеспечиваются огнезащитными пропитками наружного слоя и головного убора, наличием воздушных зазоров между слоями и дополнительных элементов для защиты открытых участков кожи. Огнезащитные свойства костюма сохраняются в течение 5 месяцев.
Защита от ОВТВ достигается наличием пропитки на защитном белье, многослойностью костюма и его герметичностью. Время защитного действия зависит от типа ОВ и его концентрации, содержания «активного» хлора на защитном белье и температуры воздуха. В отношении паров ОВ оно составляет от 3 до 24 ч. При увлажнении костюма потом и водой защитные свойства снижаются, поэтому для предохранения ОКЗК-М от увлажнения при дожде необходимо использовать плащи или средства защиты кожи изолирующего типа. Защитные свойства увлажненного ОКЗК восстанавливаются после высыхания костюма. После носки ОКЗК-М в течение 2-2,5 месяцев, а также после дегазации и дезинфекции в подразделениях войск радиационной, химической и биологической защиты проводят восстановление защитных свойств костюма в отношении паров и аэрозолей ОВТВ путем перепропитки защитного белья и подшлемника машинным или другим способом.
Комплект защитной фильтрующей одежды КЗФО состоит из двухслойных куртки и брюк. За счет специальных пропиток верхний слой КЗФО позволяет защищаться от светового излучения ядерного взрыва и огня пожаров, а нижний слой предохраняет от действия боевых отравляющих веществ.
В состав общевойскового защитного комплекта фильтрующего ОЗК-Ф входят защитный комплект ПКР, состоящий из фильтрующего противогаза ПМК-3 с капюшоном и респиратора РОУ, и комплект защитной фильтрующей одежды КЗФО.
Комплект защитный морской КЗМ-2 состоит из фартука, нарукавников, защитных перчаток и бахил.
Защитное действие средств индивидуальной защиты изолирующего типа основано на способности некоторых материалов задерживать ОВТВ на своей поверхности и очень медленно пропускать их в жидком и парообразном состоянии через толщу тканей. Такие материалы не обладают воздухопроницаемостью и, при соответствующем покрое изготовленной из них одежды, изолируют организм от внешней среды.
Время от момента нанесения капли ОВТВ на изолирующий материал до появления на оборотной стороне паров ОВТВ в концентрации, достаточной для поражения кожи, называется временем защитного действия.
По назначению средства индивидуальной защиты кожи изолирующего типа делятся на общевойсковые и специальные.
К общевойсковым средствам защиты кожи относится общевойсковой защитный комплект (ОЗК), в состав которого входят защитный прорезиненный плащ ОП-1М, защитные чулки и защитные перчатки. Защитный плащ ОЗК может использоваться в виде накидки, надетым в рукава и в виде комбинезона.
В виде накидки плащ используется при внезапном применении противником отравляющих и высокотоксичных веществ, биологических средств, а также при выпадении радиоактивных веществ из облака ядерного взрыва. При преодолении на открытых машинах участков местности, зараженной отравляющими, высокотоксичными или радиоактивными веществами, при выполнении дегазационных и дезактивационных работ защитный плащ используется надетым в рукава. На местности, интенсивно зараженной отравляющими веществами, а также в очагах химических поражений при проведении спасательных работ и эвакуационных мероприятий защитный плащ используется в виде комбинезона.
Общевойсковой защитный комплект, зараженный отравляющими веществами или биологическими средствами, подвергают специальной обработке с помощью ИПП непосредственно на личном составе. ОЗК выдерживает 10 циклов специальной обработки с сохранением защитных свойств от капель отравляющих веществ.
Специальная защитная одежда изолирующего типа применяется при длительных действиях личного состава на зараженной местности, при особо опасных работах с ОВ, а также выполнении дегазационных работ. Специальные средства защиты кожи состоят на табельном оснащении в виде защитных комбинезонов и легкого защитного костюма (Л-1), изготовленного из прорезиненной ткани, обеспечивающей повышенную герметизацию.
К специальным средствам защиты кожи относится и комплект защитный морской КЗМ-1, состоящий из защитного костюма морского, охлаждающего костюма и защитных перчаток. В состав комплекта защитного № 6 входят костюм защитный изолирующий КЗИ-2, костюм хлопчатобумажный охлаждающий КХО-3 и защитные перчатки БЛ-1М.
24.1.2.2. Факторы, определяющие порядок использования средств защиты кожных покровов
При эксплуатации защитной одежды изолирующего типа вследствие изменения соотношения между теплопродукцией и теплоотдачей нарушается терморегуляция организма. Теплоотдача в изолирующей защитной одежде резко падает. Это имеет отношение ко всем путям теплоотдачи: теплопроведению и конвекции, теплоизлучению и испарению жидкости (пота) с поверхности тела.
В условиях высокой температуры воздуха и солнечной радиации интенсивная физическая работа человека может привести к перегреванию организма и вызвать тепловой удар. Основными признаками перегревания являются повышение температуры тела до 38—41° С, резкая слабость, головная боль, учащение пульса, гиперемия (а иногда бледность) лица. В тяжелых случаях наступает тепловой удар с потерей сознания.
| - Таблица 80 Допустимые сроки пребывания в средствах индивидуальной защиты при различной физической нагрузке, ч |
Во избежание перегревания организма научно обоснованы и официально рекомендованы предельно допустимые сроки непрерывной работы в защитной одежде изолирующего типа, которые приведены в табл. 80.
| — г Л—■•—, ■ Физическая нагрузка и температура воздуха, °С | ||||||||
| Средства защиты | Легкая (180 ккал/ч) | Тяжелая (450 ккал/ч) | ||||||
| 10° | 20° | 30е | 40е | 10° | 20° | 30° | 40° | |
| ОКЗК | 8,0 | 8,0 | 8,0 | 8,0 | 8,0 | 3,0 | 1,5 | 1.0 |
| ОКЗК + противогаз + чулки + перчатки | 8,0 | 8,0 | 8,0 | 6,0 | 8,0 | 2,0 | 1,0 | 0,6 |
| ОКЗК + ОЗК + противогаз | 8,0 | 2,0 | 1,0 | 0,7 | 4,0 | 0,5 | 0,4 | 0,3 |
Для сохранения наибольшей работоспособности в защитной одежде изолирующего типа рекомендуется:
• хранить ее в тени, избегая предварительного нагревания;
• надевать ее непосредственно перед работой;
• работать без лишних движений, соблюдать равномерный и умеренный темп;
• по возможности орошать защитную одежду водой;
• вести непрерывное наблюдение за работающими;
• систематически проводить тренировки личного состава в защитной одежде в целях выработки навыков, более рациональных движений и сноровки.
24*1.3. Средства индивидуальной защиты глаз
Средства индивидуальной защиты глаз (СИЗГ) предназначены для защиты глаз от светового излучения ядерного взрыва. К ним относятся защитные очки и пленочные средства защиты глаз.
Защитные очки противоожоговые фотохромные (ОПФ) и очки фото-хромные (ОФ) представляют собой очки со специальными стеклами, обрамленные в резиновый корпус. По внешнему виду, составу и устройству ОПФ и ОФ не отличаются друг от друга, а различие между ними состоит лишь в свойствах фотохромных материалов, применяемых в блоках светофильтров. Защита глаз от светового излучения ядерного взрыва достигается поглощением энергии светового импульса фотохромным или инфракрасным светофильтрами. Резиновый корпус очков сконструирован таким образом, чтобы исключить прямое попадание света в подочковое пространство.
Пленочные средства защиты глаз (ПСЗГ) представлены в виде пленок, которые вставляются в очковые узлы фильтрующих средств индивидуальной защиты органов дыхания. По своему предназначению и принципу действия они принципиально не отличаются от защитных очков.
24.2. Коллективные средства защиты
Коллективными средствами защиты (КЗС) являются специально оборудованные сооружения и объекты, предназначенные для защиты людей от воздействия ядерного, химического, биологического оружия, зажигательных и обычных средств поражения. Эти сооружения и объекты позволяют обеспечить бесперебойную работу медицинских пунктов и лечебных учреждений.
В связи с особенностями оборудования и эксплуатации объектов КСЗ их делят на два вида: стационарные фортификационные сооружения и подвижные объекты техники и вооружения.
Эффективность инженерно-технических сооружений, предназначенных для коллективной защиты, зависит от устройства и наличия специального оборудования.
Выделяют два основных типа сооружений — открытого и закрытого типов. Такие простейшие сооружения, как траншеи, ходы сообщения и щели, могут снижать потери от ударной волны ядерного взрыва и огнестрельного оружия, частично защищая от светового излучения и ионизирующего излучения, но не защищают от ОВТВ, биологических средств и токсинов. Более надежная защита личного состава войск, раненых и больных обеспечивается закрытыми сооружениями, к которым относятся блиндажи и убежища различных типов. Все закрытые сооружения, в зависимости от специального оборудования, делятся на вентилируемые и невентилируемые.
Наиболее полную и эффективную защиту личного состава войск от всех поражающих факторов средств массового поражения обеспечивают убежища. В них организуются бесперебойная работа медицинского состава и укрытие раненых и больных без средств индивидуальной защиты. Эти сооружения, для того чтобы они соответствовали своему назначению, должны противостоять воздействию ударной волны ядерного взрыва, не подвергаться возгоранию от светового излучения, исключать возможность проникновения отравляющих и высокотоксичных веществ, радиоактивного аэрозоля, биологических средств и токсинов, а также защищать от воздействия огнесмесей типа напалма.
Оборудование убежища в противоатомном отношении предусматривает создание надежной прочности и устойчивости от воздействие ударной волны всей конструкции убежища, защиту воздухозаборных отверстий, дымохода и входных дверей. Заглубление укрытий производится с учетом эффективного снижения проникающей радиации до безопасных величин, что практически достигается слоем отсыпки грунта около 1,5—2 м.
Противохимическое оборудование убежищ заключается в следующем:
• в герметизации основных помещений убежища и тамбуров;
• в герметизации входа путем применения легких герметических дверей, герметических перегородок и защитно-герметических дверей;
• в использовании фильтро-вентиляционных агрегатов для подачи очищенного от отравляющих и высокотоксичных веществ, радиоактивных аэрозолей и биологических средств воздуха в сооружения.
Специальное противохимическое оборудование убежищ состоит из фильтров-поглотителей, вентилятора, воздухозаборного устройства, воздуховодов и контрольно-измерительных приборов.
Противохимическое оборудование для убежищ медицинского назначе-
ния представлено в виде фильтровентиляционных комплектов ФВКП-М-1
и ФВКП-М-2. ,
Филыпровентиляционный комплект ФВКП-М-1 состоит из двух фильтров-поглотителей ФП-50у, вентилятора ЭРВ-49, указателя расхода воздуха УРВ-1, двух раздвижных герметических дверей, набора воздуховодов и монтажных деталей, в него входят также 100 м2 рулонной бумаги для герметизации покрытий сооружения. В фильтровентиляционном комплекте ФВКП-М-2 в отличие от комплекта ФВКП-М-1 имеется три поглотителя ФП-50у и четыре раздвижные герметические двери. Производительность фильтровентиляционной установки, собранной на основе комплекта ФВКП-М-1, — 100 м3/ч очищенного воздуха, а установки, собранной из ФВКП-М-2, - около 150 м3/ч.
На оснащение частей и подразделений медицинской службы могут также поступать фильтровентиляционные агрегаты ФВА-100/50 и ФВА-50/25.
Фильтровентиляционный агрегат ФВА-100/50 предназначен для оборудования командных и медицинских пунктов, а также войсковых убежищ вместимостью 20 человек и более. Этот агрегат обеспечивает подачу в сооружение 100-150 м3/ч очищенного воздуха. В комплект ФВА-100/50 входит вентилятор с электрическим и ручным приводом, фильтр-поглотитель ФП-100/50 с подставкой, вентиляционное защитное устройство, воздухозаборное устройство, указатель расхода воздуха, индикатор проскока ОВ, устройство для продувки тамбуров, набор монтажных деталей, две раздвижные герметические двери, два полотнища из прорезиненной ткани и 100 м2 рулонной водонепроницаемой бумаги. Вентиляционное защитное устройство предназначено для предотвращения проникновения ударной волны в убежище через воздухозаборное приспособление и для защиты фильтров-поглотителей от повреждения. Аналогичные устройства имеются и для предотвращения проникновения ударной волны в сооружение через дымоходы. В интересах поддержания температуры воздуха в убежище до 19—23° С используются обогревательные комплекты.
Фильтровентиляционный агрегат ФВА-50/25 предназначен для оборудования войсковых убежищ и блиндажей. Этот агрегат обеспечивает подачу в сооружение до 50 м3 очищенного воздуха в час.
Обогревательный комплект типа ОПП состоит из металлической печи, приспособлений для сжигания твердого топлива и набора дымовых труб.
Монтаж всех комплектов и их эксплуатация осуществляются в соответствии с инструкциями, прилагаемыми к каждому комплекту.
Убежища должны обеспечивать необходимые санитарно-гигиенические условия для нахождения в них людей, а также возможность входа и выхода личного состава при заражении воздуха отравляющими, радиоактивными веществами и бактериальными аэрозолями.
Вход в основное помещение убежища осуществляется путем шлюзования через тамбурное устройство. Тамбуры представляют собой небольшие по объему 2—3 помещения, отделенные одно от другого герметическими дверями. В тамбурах происходит снижение концентрации ОВ и других вредных примесей, вносимых с воздухом наружной атмосферы.
Убежища медицинского назначения имеют свои конструктивные особенности: тамбуры обычных сооружений имеют длину до 1 м, а в сооружениях медицинского назначения входы оборудуются тамбурами длиной не менее 3 м (размер носилок и место для санитаров-носильщиков); кроме того, сооружения медицинского назначения должны иметь два самостоятельных входа.
При включении фильтровентиляционного агрегата создается искусственная приточная вентиляция. Она способствует созданию необходимых санитарно-гигиенических условий в убежище. Вместе с тем создается избыточное давление (подпор) при подаче очищенного воздуха, что препятствует проникновению зараженного воздуха внутрь сооружения. Герметичность убежища определяется воздушным подпором — избыточным давлением внутри сооружения. Убежище считается герметичным, если избыточное давление поддерживается на уровне 2—5 мм вод. ст., при подаче воздуха, равной половине объема основного помещения.
Порядок входа личного состава, действующего на зараженной местности, в убежищах следующий.
Изолирующие средства защиты (ОП-1М, чулки, перчатки) снимаются в перекрытом участке траншеи и складываются в прорезиненный мешок.

Рис. 72. Площадка санитарной обработки отделения специальной обработки отдельного медицинского батальона:
1 — обменный фонд носилок; 2 — мешки для сбора средств индивидуальной защиты кожных покровов и обмундирования; 3 — ящик для оружия; 4 — стол для сортировочных марок, полиэтиленовых пакетов с пробирками, противохимических средств; 5 — стол для медицинских средств и регистратора; б — умывальник; 7 — подставка под носилки; 8 — скамейки для ходячих раненых и больных; 9 — комплект санитарной обработки (иногда
размещают в моечной); 10 — мешок (ящик) для сбора респираторов и противогазов; 11 — душевой прибор; 12 — ведро (тазик) для чистых мочалок и мыла; 13 — ведро (тазик) для грязных мочалок; 14 — специальные носилки на подставках для проведения санитарной обработки носилочных раненых и больных; 15 — переносные душевые сетки; 16 — поглощающий колодец; 17 — дезинфекционно-душевая установка ДДА (ДДП); 18 — резервуар для воды; 19 — цистерна для воды; 20 — полиэтиленовая пленка для моечной; 21 — кислородный ингалятор; 22 — стол для медикаментов, сортировочных марок, стерилизатора; 23 — стеллаж с обменным фондом обмундирования и белья; 24 — хозяйственный стол (ящик для имущества)
После снятия средств индивидуальной защиты кожных покровов и сортировки тяжелопораженных санитары-носильщики доставляют в раздевальную. Ходячие пораженные следуют туда самостоятельно. В раздевальной производится обработка открытых участков кожных покровов жидкостью ИПП при заражении ОВТВ или их обмывание водой при загрязнении РВ. Легкопораженные делают это в порядке само- и взаимопомощи, а тяжелопораженным обработку осуществляют санитары-раздевальщики. При наличии показаний в раздевальной пораженным оказывается неотложная медицинская помощь.
По окончании подготовки тяжелопораженные (носилочные) выносятся санитарами-раздевальщиками в тамбур, ведущий в моечную, и передаются там санитарам-душорам. В межтамбурном промежутке сред- ства индивидуальной защиты органов дыхания с пораженных снимаются и помещаются в специальный прорезиненный мешок для последующей обработки. Легкопораженные направляются в моечную самостоятельно.
Моечная размещается в отгороженной части палатки УСБ. Работают здесь два санитара-душора и юдитель-дезинфектор установки ДДА. Все они работают в защитных очках, нарукавниках, фартуках и чулках. В моечной проводится полная санитарная обработка, которая заключается в помывке всего тела теплой водой с мылом. Легкопораженные осуществляют это мероприятие самостоятельно, а тяжелопораженных моют санитары-душоры.
Из моечной пораженные направляются в одевальную, размещенную во второй части палатки УСБ. Здесь работают санитарный инструктор-дозиметрист, санитары-одевалыцики и 2 санитара-носильщика из приемно-сортировочного взвода. В одевальной проводятся контроль полноты санитарной обработки, одевание пораженных, выдача им обработанных на площадке специальной обработки обмундирования и имущества противогазов. Здесь же по показаниям могут осуществляться мероприятия неотложной помощи (повторно вводятся антидоты, симптоматические средства, проводятся отсос слизи из верхних дыхательных путей, кислородотерапия, укрепляются повязки и т. п.), после чего пораженные доставляются в приемно-сортировочный взвод.
Площадка специальной обработки обмундирования и имущества размещается не ближе 50 м от других функциональных подразделений отдельного медицинского батальона с подветренной стороны вблизи от площадки санитарной обработки. Размеры площадки зависят от количества имущества, подлежащего дегазации и дезактивации. На ней также выделяют грязную и чистую половины. На грязной половине размещают необходимые средства для проведения дегазации и дезактивации обмундирования и имущества, отрывают сточные канавы и поглощающие колодцы, устанавливают знаки ограждения. На чистой половине оборудуют места для размещения обработанного обмундирования и имущества. Основными задачами площадки специальной обработки обмундирования и имущества являются:
• дезактивация средств индивидуальной защиты, снаряжения, об-__мундирования и обуви;
• дегазация средств индивидуальной защиты органов дыхания;
• сбор обмундирования, обуви, снаряжения и средств индивидуальной защиты, зараженных ОВТВ, а также обмундирования, не поддающегося дезактивации до безопасных величин, для отправки на ПуСО;
• дегазация и дезактивация личного оружия;
• дегазация и дезактивация носилок и других предметов медицинского имущества;
• доставка обработанных средств индивидуальной защиты в оде-вальную.
На площадке специальной обработки обмундирования и имущества обычно работает санитарный инструктор-дезинфектор, в помощь которому выделяется несколько военнослужащих из команды выздоравливающих. Все они должны работать в средствах индивидуальной защиты органов дыхания и кожных покровов. Здесь с помощью дегазирующих и дезактивирующих растворов и технических средств проводится специальная обработка личного оружия, носилок, противогазов, отдельных видов медицинского имущества при малых масштабах заражения, а при возможности — и небольшого количества средств индивидуальной защиты кожных покровов и обмундирования. Вариант развертывания площадки специальной обработки обмундирования и имущества представлен на рис. 73.
На расстоянии 10—15 м от площадки санитарной обработки развертывается площадка специальной обработки транспорта (рис. 74). Она также делится на две части (грязную и чистую) и обозначается знаками ограждения. На зараженной части площадки выделяют места для стоянки транспорта и специальной обработки автомобилей и носилок, отрывают яму для сточных вод и продуктов дегазации, на чистой организуют место сбора и укомплектования транспорта. Основной задачей площадки является проведение полной дегазации и дезактивации транспорта, доставившего раненых и больных (пораженных). Здесь же могут дегазироваться и дезактивироваться носилки, которые необходимо вернуть вместе с транспортом.
 | |||
 | |||
1 — щит деревянный; 2 — комплект ДК-4; 3 — емкости для дегазирующих и дезактивирующих растворов; 4 — ящик с ветошью, веники; 5 — автомобиль; б — яма для сточных вод; 7 — знак «Заражено»
После дегазации и дезактивации обработанное обмундирование и имущество размещается на чистой половине площадки, после чего противогазы и обмундирование переносятся в одевальную площадки санитарной обработки. При необходимости дегазации или дезактивации большого количества медицинского имущества может дополнительно развертываться площадка специальной обработки медицинского имущества.
Под руководством выделенного на площадку санитара водители автомобилей самостоятельно проводят специальную обработку транспорта, используя комплекты ДК-4 (ДК-5) или ИДК-1. Для обеспечения работы площадки обычно выделяются еще 1—2 военнослужащих из команды выздоравливающих, которые участвуют в разведении дегазирующих и дезактивирующих растворов, снаряжении технических средств и т. д.
Полная санитарная обработка пораженных, поступивших в военно-полевой госпиталь непосредственно из очагов радиационного или химического заражения, проводится в отделении специальной обработки (ОСО). Принцип развертывания, силы и средства, организация работы ОСО военно-полевого госпиталя принципиально не отличаются от аналогичного подразделения отдельного медицинского батальона.
Дегазация и дезактивация медицинского имущества проводятся на площадке специальной обработки медицинского имущества (рис. 75). Малые количества зараженного ОВТВ медицинского имущества могут также подвергаться дегазации и дезактивации на площадке специальной обработки обмундирования и имущества отделения специальной обработки.

направление ветра

Рис. 75. Площадка специальной обработки медицинского имущества.
I — площвдкв для сосредоточения зврвженного имуществе: 1 — комплекты медицинского имущества (кроме комплектов перевязочных средств); 2 — комплекты перевязочных средств; 3 — отдельные предметы и оборудование (столы перевязочные, операционные, носилки и др.). II — площвдка для дегазвции и дезактиввции: 4 — место для обработки наружной поверхности комплектов; 5 — места для дегазационных приборов; б — места для дегазирующих растворов; 7 — водоотводные канавы; 8 — водосборные колодцы; 9 — место для извлечения имущества из комплектов и его сортировки; 10 — место для дегазации внутренней поверхности тары: 11 — место для обработки герметичной тары лекарственных средств; 12 — место для ветоши; 13 — место для емкостей с водой; 14 — место для сбора имущества, подлежащего уничтожению; 15 — место для замены этикеток; 16 — место для дегазации имущества кипячением; 77 — место для дегазации наружной поверхности комплектов перевязочных средств; 18 — место для извлечения и сортировки перевязочных средств; 19 — место для дегазации отдельных предметов; 20 — место для снятия средств индивидуальной защиты. Ill — площвдка выборочного контроля полноты дегазации и двзвктиввции: 21 — места для выборочного контроля полноты дегазации и дезактивации. IV — площвдка для сосредоточения обработанного имуществе: 22 — места для формирования комплектов; 23 — места для проветривания и просушки перевязочных средств; 24 — места для сосредоточения отдельных предметов; 25 — места для надевания средств индивидуальной защиты. / — площадке для сосредоточения имуществе, не подлежащего дегвзвции и двзвктиввции. VI — площвдка для естественной дегвзвции и дезактивации
Площадка специальной обработки медицинского имущества развертывается силами и средствами медицинской службы в местах сосредоточения зараженных запасов медицинского имущества, но не менее чем на 50 м от подразделений и частей медицинской службы, не подвергшихся заражению ОВТВ. Численность личного состава, работающего на площадке, определяется объемом зараженного имущества, степенью его заражения и т. д. Обычно для работы на ней выделяется санитарный инструктор или военнослужащие из команды легкораненых, а руководит их работой начальник аптеки.
Площадка специальной обработки медицинского имущества должна включать места сосредоточения зараженного имущества и его сортировки, дегазации, выборочного контроля, сбора дегазированного имущества, а также места для естественной дегазации и для сосредоточения имущества, подлежащего уничтожению. Площадка и пути подхода к ней обозначаются соответствующими предупредительными знаками.
Площадка специальной обработки медицинского имущества делится на грязную (для работы с зараженным имуществом) и чистую половины. Грязная половина площадки ограждается и обозначается знаками ограничения с надписью «заражено». На грязной половине оборудуются места для сосредоточения, сортировки, дегазации и выборочного контроля имущества; Места для естественной дегазации и для сбора имущества, подлежащего уничтожению, также развертываются на грязной половине на расстоянии не менее, соответственно, 50 и 100 м от основной площадки с учетом направления ветра.
Места для сосредоточения зараженного медицинского имущества оборудуются палатками, навесами, настилами из подручных средств и брезентов для предохранения имущества от атмосферных осадков. Места для сортировки зараженного имущества соединяются с чистой половиной дорожками, позволяющими передвигаться личному составу с тележками или носилками. На грязной половине площадки размещаются дегазирующие растворы, подставки под носилки, столы, запас ветоши и ватно-марлевых тампонов. В ходе развертывания площадки на грязной половине необходимо также предусмотреть поглощающий колодец для стока продуктов дегазации и яму для отработанной ветоши.
На чистой половине площадки оборудуются места для осмотра, проветривания, просушки и сосредоточения дегазированного медицинского имущества, формирования комплектов из обработанного имущества, а также место для надевания личным составом средств защиты. Обеззараженное имущество на чистой половине должно храниться в укладочных ящиках или другой транспортной таре, на носилках из досок, жердей или веток. Кроме того, на местах сбора и хранения оборудуются полевые укрытия, навесы, палатки для предохранения медицинского имущества от воздействия неблагоприятных факторов внешней среды.
Дегазацию медицинского имущества проводят в основном теми же способами и средствами, которые применяются для дегазации различных видов войскового имущества, учитывая при этом степень герметичности упаковки, характер заражения и вид ОВТВ (табл. 83).
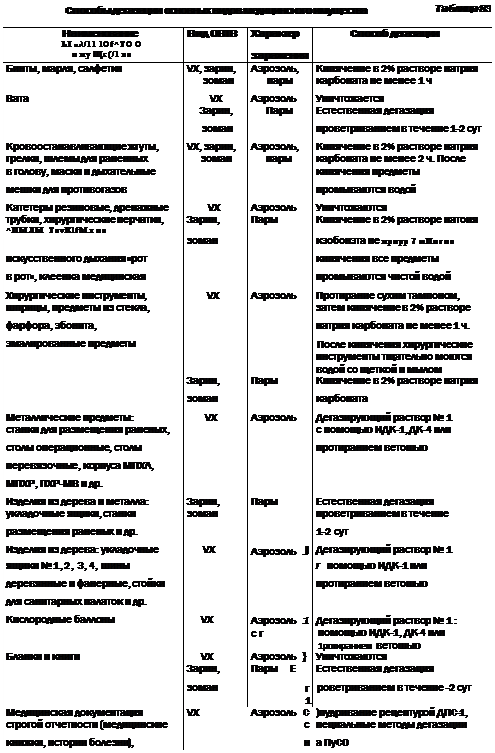 |  | ||
Так, при дегазации медицинского имущества, находящегося в комплектах, сначала обрабатывают наружную поверхность укладочных ящиков, затем извлеченное из них имущество и после этого — внутреннюю поверхность тары.
Лекарственные средства, находящиеся в герметичной упаковке (бутылки, банки, трубки и другая непроницаемая для ОВТВ потребительская тара, укупоренная полиэтиленовыми пробками с тремя и более уплотнительными кольцами, резиновыми пробками с навинчивающимися крышками из металла и т. п.), обрабатываются снаружи тампонами, смоченными полидегазирующей рецептурой РД-2, дегазирующим раствором № 1 (при заражении VX или ипритами) или дегазирующим раствором № 2 (при заражении зарином или зоманом) с последующим обмыванием тары водой. После этого неповрежденные формы лекарственных средств могут использоваться по назначению.
Лекарственные средства, находящиеся в негерметичной или проницаемой для ОВТВ таре, при заражении капельно-жидкими ОВТВ уничтожаются, а при заражении парами или аэрозолями — дегазируются по специальным режимам. После проведения дегазации такие лекарственные препараты подлежат тщательной проверке с последующим вынесением решения о возможности их дальнейшего использования.
Нестерильные перевязочные средства и другие предметы из хлопчатобумажной ткани кипятят в 2% растворе натрия карбоната в течение 1 ч, а затем прополаскивают в теплой воде. После высушивания, а при необходимости и стерилизации, перевязочный материал может быть использован по назначению.
Стерильные перевязочные средства в течение первых суток после заражения могут быть использованы без дегазации после снятия перга-
5DO
5D1
мента и двух-трех наружных слоев бинта. В случае нахождения этих перевязочных средств в своей упаковке более суток после заражения их дегазируют кипячением в 2% растворе натрия карбоната не менее часа.
Вату, зараженную парами ОВТВ, дегазируют проветриванием в течение 1—2 сут с последующим контролем полноты дегазации. Вата, зараженная капельно-жидкими ОВТВ или аэрозолем VX, подлежит уничтожению.
Все виды резиновых изделий (кровоостанавливающие резиновые жгуты, грелки, пузыри для льда и т. п.) дегазируют кипячением в 2% растворе натрия карбоната в течение 2 ч. После кипячения резиновые предметы промывают водой и используют по назначению.
Зараженные ОВТВ в капельно-жидком состоянии или в форме аэрозолей резиновые или пластмассовые медицинские предметы, используемые в хирургической практике (катетеры, дренажные трубки, перчатки, зонды, интубационные и дыхательные трубки, клеенка медицинская и т. п.), дегазации не подлежат и уничтожаются. При заражении указанных изделий парами зарина, зомана, иприта их кипятят в 2% растворе натрия карбоната не менее 2 ч, после чего промывают чистой водой.
Медицинские инструменты, шприцы, предметы из стекла, фарфора, эбонита и эмалированные предметы, зараженные ОВТВ, после снятия видимых капель ОВТВ тампонами промывают в органических растворителях, затем каждый предмет тщательно моют с мылом, протирают и кипятят в 2% растворе натрия карбоната в течение часа, а при необходимости стерилизуют.
Типовое медицинское оборудование, изготовленное из металла, проволочные шины и другие металлические предметы медицинского имущества, зараженные ОВТВ, обрабатывают полидегазирующей рецептурой РД-2 или дегазирующими растворами № 1 и № 2 с помощью ИДК-1, ДК-4, РДП-4 или протиранием ветошью, смоченной этим раствором.
Деревянные и металлические изделия, зараженные парами зарина или зомана, подвергаются естественной дегазации проветриванием в течение 1—2 сут с последующим контролем полноты дегазации. Изделия из дерева (шины, укладочные медицинские и другие ящики и т. п.), зараженные VX в форме аэрозоля, дегазируют полидегазирующей рецептурой РД-2 или дегазирующим раствором № 1. Шины деревянные и ящики тессчые, зараженные капельно-жидкими ОВТВ, подлежат уничтожению.
Аппараты кислородной терапии и искусственной вентиляции легких, зараженные VX, дегазируют по следующей схеме: обрабатывают корпус укладочного ящика ветошью, смоченной полидегазирующей рецептурой РД-2 или дегазирующим раствором № 1, и обмывают водой. В той же последовательности обрабатывают корпус кислородного баллона. Систему подачи кислорода (вентиль, редуктор, манометр) обеззараживают протиранием тампонами, смоченными рецептурой, состоящей из 3% водного раствора перекиси водорода с добавлением 3% натриевой или калиевой щелочи. Резиновые части аппаратуры (дыхательные мешки, соединительные гофрированные трубки, маски) снимают и дегазируют кипячением в 1% растворе натрия карбоната в течение 2 ч.
Бланки и книги медицинского учета, учета материальных средств, зараженные парами ОВТВ, проветривают в течение 1—2 сут с последующим контролем полноты дегазации. Документы и бланки, оказавшиеся зараженными после проветривания, уничтожают.
Медицинские документы строгой отчетности (медицинские книжки, истории болезни), так же как и личные документы военнослужащих, в случае невозможности полной дегазации припудриваются порошком ДПС-1 (ДПП-М), складываются в специальные прорезиненные мешки и оставляются для естественной дегазации или отправляются на ПуСО.
Пакеты перевязочные индивидуальные (ППИ) после снятия зараженной оболочки и дегазации могут использоваться в качестве перевязочного материала. После проведения дегазации и проверки качества ее выполнения выдаваться личному составу могут и индивидуальные противохимические пакеты ИПП-8 или ИПП-11.
Аптечки индивидуальные, хранящиеся в аптеке (на складе), дегазируют протиранием наружной части футляра полидегазирующей рецептурой РД-2, дегазирующими растворами № 1 или № 2. Футляр аптечки, выданной личному составу, дегазируется путем протирания тампоном, смоченным рецептурой индивидуального противохимического пакета ИПП.
Чехлы сумок (санитара, медицинской войсковой), полотнища носилок, лямки санитарные и другие брезентовые изделия, зараженные аэрозолем VX или ипритом, дегазируют полидегазирующей рецептурой РД-2 или дегазирующим раствором № 1 с последующим промыванием водой. Резину с ручек носилок срезают и уничтожают.
Медицинские палатки обрабатывают на дегазационных пунктах, развертываемых службой радиационной, химической и биологической защиты, или дегазируют на этапах медицинской эвакуации полидегазирующей рецептурой РД-2, дегазирующими растворами № 1 или № 2 с помощью ИДК-1, ДК-4, РДП, проветривают и просушивают. Сроки естественной дегазации палаток, зараженных парами зарина, составляют не менее 24 ч в летних и не менее 36 ч в зимних условиях.
Необходимо помнить, что зараженное ОВТВ медицинское имущество может использоваться только после правильно проведенной специальной обработки и последующего контроле полноты дегазации.
Медицинская техника, зараженная ОВТВ и продегазированная полидегазирующей рецептурой РД-2, водными рецептурами гипохлорита кальция, СН-50, СФ-2у или растворителями, может эксплуатироваться личным составом в течение 1—2 сут с соблюдением требований безопасности. Работать с медицинской аппаратурой, зараженной зоманом (зарином), даже после дегазации с помощью дегазирующего раствора № 2-бщ (ащ) или 1—1,5% водного раствора гипохлорита кальция, личный состав может только в противогазах. Следует учитывать, что при работе с зараженной медицинской техникой необходимо проводить периодический контроль за концентрацией паров ОВТВ с подветренной стороны про-дегазированных объектов с помощью приборов химической разведки (ВПХР, ПХР-МВ, МПХР).

Наименование имущества
Перевязочный материал, лямки санитарные
Вата
Хирургический инструментарий, шприцы
Резиновые изделия: жгуты, грелки, маски дыхательных аппаратов и др.
Резиновые предметы, используемые в хирургической практике
Предметы из стекла, эбонита, фарфора, пластмассы
Металлические предметы: столы операционные, столы перевязочные, стенки для раненых и др.
Носилки санитарные, сумки медицинские
Способ дезактивации
Стирка с моющими средствами; при целой упаковке — обметание ее щетками, обтирание влажными тампонами. Большие партии подлежат хранению до спада уровня загрязнения РВ до безопасных значений
При целой упаковке — обметание ее щетками, обтирание влажными тампонами. При нарушенной герметичности упаковки — уничтожается
Промывание дезактивирующими растворами, обтирание тампонами, смоченными дезактивирующими рестворами или растворами комплексообразователей (1% раствором ЭДТА, 10% раствором цитрата натрия)
Промывание водой или дезактивирующими растворами, обтирание влажными тампонами
Промывание водой или дезактивирующими растворами, обтирание влажными тампонами
Обмывание дезактивирующими растворами, обтирание тампонами, смоченными растворами комплексообразователей
Обмывание дезактивирующими растворами
с помощью РДП-4, ИДК-1, обтирание тампонами,
смоченными растворами комплексообразователей
Чистка щетками, обмывание водой или дезактивирующими растворами с помощью РДП-4, ИДК-1, автомакса
Медикаменты в не герметичной таре, загрязненные РВ, подлежат уничтожению. Перевязочный материал, лямки санитарные подвергаются стирке или сдаются на склад для естественной или специальной дезактивации.
Медицинский инструментарий, предметы из стекла, эбонита, фарфора и пластмассы протираются влажными тампонами или промываются в комплексообразователях. Резиновые предметы (катетеры, дренажные трубки, перчатки, зонды, интубационные и дыхательные трубки, маски дыхательных аппаратов, резиновые грелки, пузыри, жгуты, шлемы для раненных в голову, маски противогазов) и клеенка медицинская обмываются водой или дезактивирующими растворами, а затем протираются тампонами. Хирургический инструментарий после проведения дезактивации должен подвергаться стерилизации по общепринятым схемам.
Крупные металлические предметы обмываются дезактивирующими растворами с помощью технических средств специальной обработки (РДП-4В, ИДК-1, ДК-4). Носилки, загрязненные РВ, чистятся щетками, обмываются водой или обрабатываются дезактивирующими растворами с последующим промыванием водой.
После проведения дезактивации медицинское имущество должно подвергаться контролю уровней загрязненности РВ с помощью приборов радиационной разведки и контроля (рентгенометров-радиометров ДП-5). Личный состав, осуществляющий дезактивацию медицинского имущества, должен соблюдать меры безопасности, работать в средствах индивидуальной защиты кожных покровов и респираторах. Кроме того, при проведении дезактивации должен быть организован дозиметрический контроль облучения личного состава, работающего на площадке, а также проведение полной санитарной обработки личного состава после окончания дезактивационных работ.
При проведении санитарной обработки личного состава, раненых и больных, а также дегазации и дезактивации вооружения, военной техники (в том числе санитарного транспорта) и медицинского имущества необходимо принимать меры защиты от возможных поражений, а также строго соблюдать правила безопасности. Ответственность за соблюдение личным составом правил безопасности при проведении дегазационных и дезактивационных работ возлагается на начальников соответствующих подразделений медицинской службы.
Так, для дезактивации медицинского имущества на этапах медицинской эвакуации в основном применяют 0,075% или 0,15% водные растворы порошка СФ-2у или 1% водные растворы порошка СН-50. Кроме того, для этих целей могут использоваться водные растворы мыла и других моющих средств, а также обычная вода, горючее (бензин, керосин, дизельное топливо) и различные растворители (дихлорэтан и др.).
Глава 26. РАДИАЦИОННАЯ И ХИМИЧЕСКАЯ РАЗВЕДКА В ЧАСТЯХ И ПОДРАЗДЕЛЕНИЯХ МЕДИЦИНСКОЙ СЛУЖБЫ
Радиационная и химическая разведка является одним из важных мероприятий в обеспечении радиационной и химической безопасности медицинских подразделений, частей и учреждений в условиях применения оружия массового поражения и воздействия факторов радиационной и химической природы при авариях (разрушениях) на предприятиях атом-но-энергетического цикла и объектах по производству, хранению или транспортировке токсичных химических веществ.
Она проводится с целью своевременного установления уровня радиации на местности, обнаружения типа и вида отравляющих и высокотоксичных веществ и времени действия его опасных концентраций, оповещения личного состава о радиоактивном и химическом заражении и необходимости проведения мероприятий защиты. Составными частями радиационной и химической разведки являются радиационное и химическое наблюдение, позволяющее обеспечить непрерывность и своевременность изменения радиационного фона и обнаружения ОВТВ, а также радиационный и химический контроль, данные которого используются для оценки боеспособности войск и определения объема мероприятий по ликвидации последствий радиоактивного или химического заражения.
26.1. Средства и методы радиационной разведки и контроля
Обеспечение радиационной безопасности в зонах радиоактивного заражения местности достигается непрерывным ведением радиационного наблюдения и разведки, контролем доз облучения личного состава, а также проведением радиометрического контроля в зоне заражения и по выходу из зараженных районов.
Для обнаружения и измерения ионизирующих излучений используются дозиметрические приборы, которые подразделяются на измерители мощности дозы (индикаторы радиоактивности, рентгенометры, радиометры) и измерители дозы (дозиметры). Методы измерения ионизирующих излучений в этих приборах основаны на различных физико-химических принципах.
В основе ионизационного метода лежит явление ионизации газа в камере при взаимодействии излучения с веществом. Для измерения используются явления электропроводности ионизированного газа. В результате возникает ток между вмонтированными в камеру электродами, к которым подведено напряжение. В зависимости от режима работы приборы, основанные на появлении ионизационного тока в газах, могут использоваться для измерения плотности потоков частиц (пропорциональные счетчики, счетчики Гейгера-Мюллера) и для измерения мощности дозы и дозы излучения (ионизационные камеры).
Химические методы дозиметрии основаны на измерении выхода ра-диационно-химических реакций, возникающих под действием ионизирующих излучений. Так, при действии излучений на воду образуются свободные радикалы Н* и ОН*. Продукты радиолиза воды могут взаимодействовать с растворенными в ней веществами, вызывая различные окислительно-восстановительные реакции, сопровождающиеся изменением цвета индикатора (например, реактива Грисса для нитратного метода). В частности, в основе работы ферросульфатного дозиметра лежит реакция
Fe2+ + ОН' -» Fe3+ + ОН", а при работе нитратного дозиметра
N03" + 2Н" -» N02" + Н20.
Химические методы дозиметрии не обязательно связаны с водными растворами; для этих целей применяются также органические растворы, изменяющие цвет пленки или стекла. Химические методы используются, как правило, для измерения дозы излучения.
Одним из вариантов химического метода является фотографический метод. В его основе лежит восстановление атомов металлического серебра из галоидной соли под влиянием излучений. Плотность почернения фотопленки после проявления зависит от дозы излучения. Данный метод часто используется в приборах контроля профессионального облучения.
Сцинтилляционные методы основаны на регистрации вспышек света, возникающих при взаимодействии излучения с некоторыми органическими и неорганическими веществами (антрацен, стильбен, сернистый цинк и др.). Эти методы используют в приборах, предназначенных для измерения потоков фотонов и частиц.
Сущность люминесцентных методов состоит в том, что под действием ионизирующего излучения в некоторых твердотельных изоляторах (кристаллах и стеклах) носители электрических зарядов (электроны и дырки) изменяют свое положение и частично задерживаются в местах, где имеются дефекты кристаллической решетки с соответствующими максимумами или минимумами электрического поля. Центры, образованные в результате захвата носителей заряда, обладают некоторыми разрешенными энергетическими уровнями, между которыми возможны квантовые переходы носителя заряда, соответствующие испусканию или поглощению энергии. Это может отражаться в изменении оптических свойств (цвета и оптической плотности) стекла, в появлении способности к люминесцентному возбуждению под действием видимого и ультрафиолетового света (радиофотолюминесценции), в излучении световых квантов при освобождении носителей зарядов из центров-ловушек под действием теплового возбуждения (радиотермолюминесценции). Интенсивность возникающей люминесценции пропорциональна дозе излучения, в связи с чем эти методы применяются для измерения дозы излучения.
Для измерения доз нейтронов применяют наборы активационных детекторов, в которых поток и доза нейтронов определяются по наведенной в разных веществах активности. С той же целью применяются трековые детекторы, работа которых основана на регистрации следов тяжелых заряженных частиц, образующихся в веществе под действием нейтронов. Такими частицами могут быть осколки деления нептуния, изотопов урана в специальной пластинке — радиаторе, подвергнутой действию нейтронов. Следы образуют на специальной пленке — детекторе, находящейся в контакте с радиатором. Треки становятся видимыми после травления детектора (например, щелочью) и учитываются под микроскопом. Трековый метод, так же как и активационный метод, позволяет оценить флюенсы нейтронов в определенных энергетических диапазонах с последующим расчетным определением дозы. Из-за своей сложности эти методы применяются главным образом в лабораторных условиях.
Существуют и другие методы дозиметрии, применяемые в научных исследованиях и гигиеническом нормировании профессионального облучения. Некоторые из них, например, основанные на изменении электрических свойств полупроводников при действии излучения, перспективны для разработки полевых и индивидуальных средств дозиметрии.
Радиационное наблюдение в подразделениях, частях и учреждениях медицинской службы осуществляется с помощью индикаторов радиоактивности, предназначенных для обнаружения, сигнализации и измерения ионизирующих излучений, и рентгенометров, позволяющих осуществлять измерение уровня радиации на местности. Начинается оно с использования индикатора-сигнализатора ДП-64, пульт которого устанавливается в помещении дежурного по части. Индикатор-сигнализатор ДП-64 предназначен для постоянного радиационного наблюдения и оповещения о радиоактивной зараженности местности. Прибор работает в следящем режиме и при мощности дозы у-излучения 0,2 Р/ч и выше подает звуковой (раздаются щелчки) и световой (мигает лампочка) сигналы.
Измеритель мощности дозы ИМД-21 предназначен для измерения мощности экспозиционной дозы у-излучения и подачи светового сигнала о превышении порогового значения мощности экспозиционной дозы. Измеритель устанавливается в стационарных (ИМД-21 С) или подвижных (ИМД-21 Б) объектах.
Прибор ИМД-21 измеряет мощность экспозиционной дозы у-излучения от 1 до 10000 Р/ч с выводом информации на пульт управления. Время установления рабочего режима 5 мин, время измерения и срабатывания сигнализации до 10 с. Блок детектирования (датчик со счетчиком) благодаря наличию соединительного кабеля может выноситься за пределы помещения до 200 м. Прибор может работать круглосуточно в автоматическом режиме.
Для измерения зараженности личного состава, вооружения и военной техники, различных объектов, воды и продовольствия предназначены радиометры. Однако степень радиоактивной зараженности установить непосредственно в единицах активности технически трудно. Поэтому в ряде случаев о степени зараженности различных объектов судят косвенно, измеряя мощность дозы у-излучения от их поверхности, которая в определенных пределах пропорциональна степени радиоактивной зараженности. В полевых радиометрах единицей измерения мощности дозы у-излучения служит мР/ч.
Измеритель мощности дозы ДП-5В предназначен как для измерения уровней у-радиации на местности (т. е. является рентгенометром), так и для определения радиоактивной зараженности различных предметов по у-излучению (т. е. используется как радиометр). Мощность дозы у-излучения определяется в миллирентгенах в час для той точки пространства, в которой помещен при измерениях блок детектирования прибора. Кроме того, имеется возможность обнаружения р-излучения.
Прибор состоит из измерительного пульта, блока детектирования, часто называемого зондом, соединенного с пультом при помощи гибкого кабеля длиной 1,2 м и раздвижной штанги, на которую крепится зонд. На блоке детектирования вмонтирован контрольный источник. Диапазон измерений прибора по у-излучению составляет от 0,05 мР/ч до 200 Р/ч, погрешность измерений прибора в нормальных климатических условиях не превышает +30% от измеряемой величины.
Назначение и принцип действия модификаций прибора ДП-5А и ДП-5Б те же, что и ДП-5В. Различия состоят в некоторых конструктивных изменениях и частично в электрической схеме.
Измеритель универсальный НМД-12 позволяет провести измерение мощности дозы у-излучения в диапазоне от 10 мкР/ч до 999 Р/ч, а также измерение интенсивности р-излучения с поверхностей и измерение удельной р- и а-активности продовольствия, воды и фуража. Для осуществления каждой из этих функций к измерительному пульту прибора присоединяется соответствующий блок детектирования.
При воздействии на человека проникающей радиации ядерного взрыва, а также внешнего облучения в зонах радиоактивного заражения основным фактором, определяющим степень поражения, является доза облучения. Определение доз ионизирующих излучений, полученных личным составом, осуществляется с помощью измерителей доз или дозиметров.
Общевойсковые измерители дозы, к которым относятся приборы ДКП-50А (в составе комплекта ДП-22В) и ИД-1 (в комплекте того же названия), используются преимущественно для контроля доз облучения личного состава в подразделениях. Индивидуальные дозиметры ДП-70МП и ИД-11 применяются главным образом для диагностики лучевого поражения и определения степени его тяжести у раненых и больных на этапах медицинской эвакуации.
Комплект дозиметров ДП-22В состоит из зарядного устройства ЗД-5 и 50 дозиметров ДКП-50А. Дозиметры ДКП-50А обеспечивают измерение индивидуальных доз у-облучения в диапазоне от 2 до 50 рентген при мощности дозы от 0,5 до 200 Р/ч.
Отсчет измеряемых доз производится по шкале, расположенной внутри дозиметра и отградуированной в рентгенах. Саморазряд дозиметров в нормальных условиях не превышает 2 деления за сутки, а погрешность измерений — не более ±10% от максимального значения шкалы.
Во время работы в поле действия у-излучения дозиметр носят в кармане одежды. Периодически наблюдая в окуляр дозиметра, определяют по положению изображения нити на шкале величину дозы у-излучения, полученную во время работы.
Комплект измерителя дозы ИД-1 состоит из 10 индивидуальных дозиметров ИД-1 и зарядного устройства ЗД-6. Он предназначен для измерения поглощенных доз у-нейтронного излучения в диапазоне от 20 до 500 рад с мощностью дозы от 10 до 360 000 рад/ч.
Основная погрешность измерения поглощенных доз у-нейтронного излучения не превышает ±20%, а саморазряд дозиметра в нормальных условиях составляет не более 1 деления в сутки.
Индивидуальный измеритель дозы ИД-11 и измерительное устройство ИУ обеспечивает измерение поглощенной дозы у- и смешанного у-нейтронного излучения в диапазоне от 10 до 1500 рад. Доза нейтронов регистрируется по тепловой составляющей нейтронного спектра.
ИД-11 накапливает дозу при дробном (периодическом) облучении и сохраняет набранную дозу в течение длительного времени (не менее 12 мес). Измерительное устройство обеспечивает многократное измерение одной и той же дозы.
Регистратор предназначен для использования в стационарных и полевых условиях. Измерительное устройство дает показания в виде цифрового отсчета, соответствующего величине поглощенной дозы у-нейтронного излучения. Время прогрева регистратора — 30 мин, время непрерывной работы — 20 ч. Время измерения поглощенной дозы не превышает 30 с.
Химический у-нейтронный дозиметр ДП-70МП в комплекте с полевым колориметром ПК-56Мпредназначается для измерения в полевых условиях доз суммарного у-нейтронного излучения, а также «чистого» у-излучения в дозах от 50 до 800 Р в интервале мощностей доз от 1 до 250 000 Р/ч. Отсчет измеряемых доз производится по шкале передвижного ушка полевого колориметра ПК-56М непосредственно в рентгенах. Погрешность измерения полученной дозы у-излучения составляет ±25%. Время развития максимальной окраски в рабочем растворе дозиметра составляет 40—60 мин с момента прекращения воздействия у-излучения. Продолжительность сохранения окраски без изменения — не менее 30 сут.
26.2. Средства и методы химической разведки и контроля
Основой химической разведки является индикация отравляющих и высокотоксичных веществ, которая осуществляется с помощью средств периодического и непрерывного контроля зараженности ОВТВ воздуха, техники, воды, продовольствия, обмундирования и средств индивидуальной защиты личного состава, раненых и больных. На медицинскую службу возлагается индикация ОВТВ в воде, продовольствии, медикаментах, предметах медицинского и санитарно-технического имущества с целью предупреждения поражения личного состава, раненых и больных.
Термин «индикация» означает комплекс организационных и технических мероприятий, направленных на качественное обнаружение, количественное определение (установление концентрации и плотности заражения) и идентификацию химической природы ОВТВ в различных средах. Индикация ОВТВ может проводиться органолептическим, физическим, физико-химическим, химическим, биохимическим, биологическим, фотометрическим или хроматографическим методом.
Исторически первым, когда еще не было приборов для обнаружения химических веществ, возник органолептический метод индикации ОВТВ. Органолептический метод основан на использовании зрительного, слухового или обонятельного анализаторов людей. Например, можно услышать глухой звук разрыва химического боеприпаса, увидеть облако на месте его разрыва, обнаружить изменение окраски растительности, мертвых животных и рыб, на местности — капли или мазки жидкости, похожей на ОВ, почувствовать подозрительный запах. Этот метод может быть использован химическими наблюдательными постами, но лишь как вспомогательный, поскольку он недостоверен и субъективен.
Физический и физико-химический методы индикации основаны на определении некоторых физических свойств ОВТВ (например, температуры кипения или плавления, растворимости, удельного веса и др.) или на регистрации изменений физико-химических свойств зараженной среды, возникающих под влиянием ОВТВ (изменение электропроводности, преломление света). Физический метод можно применять только при определении констант химически чистого вещества. Физико-химический метод положен в основу работы автоматических газосигнализаторов и газоопределителей. Эти приборы позволяют вести постоянное наблюдение за воздухом и быстро сигнализировать о заражении ОВТВ.
Основными методами индикации ОВТВ в настоящее время являются химический и биохимический методы. Они положены в основу работы приборов химической разведки, полевых и базовых лабораторий.
Химический метод основан на способности ОВТВ при взаимодействии с определенным реактивом давать осадочные или цветовые реакции. Эти реакции должны обеспечивать обнаружение ОВТВ в концентрациях, не опасных для здоровья людей, т. е. должны быть высокочувствительными и, по возможности, специфичными.
Необходимость обнаружения незначительных количеств ОВТВ в воздухе и воде достигается применением адсорбентов и органических растворителей, с помощью которых ОВТВ извлекается их анализируемой пробы, а затем подвергается концентрированию.
Специфичность реакции определяется способностью реактива взаимодействовать только с одним определенным ОВТВ или определенной группой веществ, сходных по химической структуре и свойствам. В первом случае — это специфические реактивы, во втором — групповые. Большинство известных реактивов являются групповыми; они используются для установления наличия ОВТВ и степени заражения ими среды.
Химическую индикацию ОВ осуществляют путем реакции на бумаге (индикаторные бумажки), адсорбенте или в растворах.
При выполнении реакции на бумаге используют такие реактивы, которые при взаимодействии с ОВТВ вызывают изменение цвета индикаторной бумаги. При просасывании зараженного воздуха через индикаторную трубку ОВТВ поглощается адсорбентом, концентрируется в нем, а затем реагирует с реактивом с образованием окрашенных соединений. Это позволяет определять с помощью индикаторных трубок такие концентрации ОВТВ, которые нельзя обнаружить другими способами.
При выполнении индикации в растворах ОВТВ предварительно извлекается из зараженного материала, а затем переводится в растворитель, в котором и происходит взаимодействие ОВТВ со специфическим реактивом. В зависимости от исследуемого материала, типа ОВТВ и реактива в качестве растворителя используют воду или органические соединения, чаще всего — этиловый спирт или петролейный эфир.
Биохимический метод индикации основан на способности некоторых ОВТВ нарушать деятельность ряда ферментов. Практическое значение имеет холинэстеразная реакция для определения фосфорорганических соединений (ФОС). ФОС угнетают активность холинэстеразы — фермента, гидролизующего ацетилхолин. Это свойство ФОС и используется для индикации. Стандартный препарат холинэстеразы подвергают воздействию вещества с исследуемого объекта, а затем по изменению цвета индикатора сопоставляют время гидролиза ферментом определенного количества ацетилхолина в опыте и контроле. Главным преимуществом биохимического метода индикации является его высокая чувствительность. Например, в воздухе ФОС определяются в концентрации 0,0000005 мг/л.
Биологический метод индикации основан на наблюдении за развитием патофизиологических и патологоанатомических изменений у лабораторных животных, зараженных ОВТВ. Этот метод лежит в основе токсикологического контроля и имеет большое значение для индикации новых ОВТВ или токсических веществ, которые нельзя определить с помощью табельных индикационных химических приборов. Индикация биологическим методом осуществляется достаточно длительное время и требует специальной подготовки персонала и наличия лабораторных животных, в связи с чем его используют главным образом в санитарно-эпидемиологических учреждениях.
В основе фотометрического метода лежит определение оптической плотности различных химических веществ, по изменению которой и определяется концентрация ОВТВ. Для измерения светопоглощения используются фотометры и спектрофотометры, в основе работы которых лежит закон поглощения света окрашенными растворами (закон Ламберта— Бера).
Обычно для фотометрии используют область, в которой идет наибольшее поглощение света. Причем для аналитических целей пригодны только те цветовые реакции, в ходе которых развивается окраска, пропорциональная концентрации исследуемого вещества. Например, этими методами можно определить концентрацию карбоксигемоглобина в крови.
Хроматографический метод основан на разделении веществ по зонам их максимальной концентрации и определении их количества в различных фракциях. В практике нашли применение различные виды хроматографии: бумажная, тонкослойная, жидкостная, газожидкостная и др. Эти методы являются весьма перспективными, так как позволяют определить содержание различных химических веществ в исследуемых объектах в самых малых количествах.
Для осуществления мероприятий по индикации ОВТВ на оснащении подразделений, частей и учреждений медицинской службы имеются средства непрерывного и периодического контроля.
К средствам непрерывного контроля относятся индикаторные элементы, автоматические газосигнализаторы и газоопределители, к средствам периодического контроля — войсковой прибор химической разведки (ВПХР), прибор химической разведки медицинской и ветеринарной служб (ПХР-МВ), медицинский прибор химической разведки (МПХР) и медицинская полевая химическая лаборатория (МПХЛ).
Индикаторные элементы представлены комплектом КХК-2, позволяющим обнаруживать капли и оседающий аэрозоль VX, зомана и иприта дисперсностью 80—400 мкм за 30-80 с и индикаторными пленками АП-1, предназначенными для определения аэрозолей VX. Пленка АП-1 представляет собой ленту желтого цвета, которая прикрепляется к обмундированию, чаще всего к рукаву на предплечье. Признаком опасного заражения VX является появление на пленке сине-зеленых пятен.
Войсковой автоматический газосигнализатор ГСА-2 позволяет обнаружить фосфорорганические отравляющие вещества в воздухе в концентрации 5-8* Ю-5 мг/л в течение 2 с.
Автоматический газосигнализатор ГСП-11 предназначен для непрерывного контроля воздуха с целью определения в нем наличия паров фосфорорганических ОВ, при обнаружении которых прибор подает световой и звуковой сигналы. Прибор работоспособен в интервале температур от -40 до +40° С, продолжительность работы прибора от 1 до 6 ч в зависимости от температуры окружающей среды.
Для тех же целей предназначен и автоматический газосигнализатор ГСП-12. Он также оснащен звуковой и световой сигнализацией, которая срабатывает не позднее 4-5 мин после обнаружения фосфорорганических ОВ. Прибор работает на одном из двух режимов с обновлением информации о наличии ФОВ: в непрерывном — через 2 мин, в циклическом — через 16 мин. Время непрерывной работы с одной зарядкой индикаторных средств в непрерывном режиме 8 ч, в циклическом — 24 ч.
Газоопределитель ПГО-11 имеет набор индикаторных трубок, позволяющий в течение 1-6 мин определять в воздухе ФОВ, иприты, синильную кислоту, хлорциан и фосген.
Прибор химической разведки медицинской и ветеринарной служб (ПХР-МВ) используют для забора проб воды, продовольствия и сыпучих материалов и определения в них ОВТВ. Запас реактивов позволяет выполнить 10—15 качественных анализов проб воды и продовольствия.
Войсковой прибор химической разведки (ВПХР) предназначен для определения в воздухе, на местности, на поверхности вооружения и военной техники зарина, зомана, иприта, фосгена, дифосгена, синильной кислоты, хлорциана, а также паров VX и BZ. ВПХР является штатным прибором химической разведки и состоит на табельном оснащении любого этапа медицинской эвакуации.
Для этих же целей может быть использован медицинский прибор химической разведки (МПХР) и медицинская полевая химическая лаборатория (МПХЛ).
Медицинский прибор химической разведки (МПХР) предназначен для обнаружения зараженности отравляющими веществами водоисточников, фуража и сыпучих видов продовольствия. Предусмотренные в МПХР средства и методы индикации основных ОВТВ позволяют проводить определение ОВ типа VX, зарина, зомана, иприта и ОВ типа BZ на местности и на различных предметах. Кроме того, прибор предназначен для взятия проб, подозрительных на зараженность бактериальными средствами. Прибором оснащаются подразделения и учреждения медицинской и ветеринарной служб.
Прибор обеспечивает обнаружение следующих групп ОВТВ:
• в воде: зарина, зомана, VX, иприта, BZ, мышьяксодержащих соединений, синильной кислоты и ее солей, фосфорорганических пестицидов, алкалоидов и солей тяжелых металлов;
• в сыпучих видах продовольствия и фуража: зарина, зомана, VX, иприта;
• в воздухе, на местности и на различных предметах: зарина, зомана, VX, иприта, BZ, фосгена, дифосгена.
Запас реактивов рассчитан на 100-120 анализов и позволяет за 10 ч провести 20 качественных анализов проб воды или пищевых продуктов.
На оснащении санитарно-эпидемиологических учреждений стоит медицинская полевая химическая лаборатория (МПХЛ). Она предназначена для качественного и количественного определения ОВТВ в пробах воды, продовольствия, фуража, медикаментов, перевязочного материала и на предметах медицинского и санитарно-технического оснащения. В частности, возможности МПХЛ позволяют проводить:
• качественное обнаружение ОВТВ, алкалоидов и солей тяжелых металлов в воде и продовольствии;
• количественное определение ФОВ, ипритов и мышьяксодержа-щих веществ в воде;
• определять полноту проведения дегазации воды, продовольствия, фуража, медикаментов, перевязочного материала и предметов ухода;
• устанавливать зараженность воды, продовольствия и фуража неизвестными ОВТВ путем проведения биологических проб.
Запас реактивов, растворителей и материалов обеспечивает проведение лабораторией не менее 120 анализов. МПХЛ приспособлена для перевозки любыми видами транспорта, обслуживается одним лаборантом, производительность ее работы — 10-12 проб за 10 ч работы.
Главнейшим требованием к индикации ОВТВ является достоверность ее результатов и безопасность проведения работ. В связи с этим определение ОВТВ следует проводить в строгом соответствии с инструкцией или руководством, так как в них предусмотрены оптимальные условия для проведения исследования. Кроме того, индикацию ОВТВ должны проводить лица, прошедшие необходимую подготовку в объеме руководств или инструкций к используемым индикационным приборам, знающие свойства ОВТВ и меры безопасности при работе с ними. В частности, при работе в полевых условиях необходимо пользоваться техническими средствами индивидуальной защиты (противогаз, защитная одежда, резиновые перчатки и сапоги), а в процессе выполнения работы необходимо находиться с подветренной стороны от зараженного участка.
26.3. Организация и проведение радиационной и химической разведки в подразделениях и частях медицинской службы
Мероприятия радиационной и химической разведки и контроля в войсковых частях (соединениях) организуют и проводят начальник штаба и специалисты службы радиационной, химической и биологической защиты. Общее руководство радиационной и химической разведкой возлагается на начальника службы радиационной, химической и биологической защиты.
Основными задачами радиационной и химической разведки и контроля являются:
• обнаружение факта радиоактивного или химического заражения местности и воздуха и оповещение об этом личного состава;
• определение характера и степени радиоактивного или химического заражения (определение уровня радиации на местности, типа и концентрации отравляющих и высокотоксичных веществ);
• установление границ зараженных районов, поиск зон с наименьшими уровнями радиоактивного или химического заражения и установление маршрутов обхода зон опасного заражения;
• контроль за изменением степени радиоактивного или химического заражения местности и воздуха для установления времени снижения уровня радиации и концентрации ОВТВ во внешней среде до безопасных величин.
Радиационная и химическая разведка в подразделениях и частях медицинской службы, как правило, осуществляется собственными силами. Данные радиационной и химической разведки используются для выбора наиболее целесообразных маршрутов перемещения, районов развертывания, вариантов работы и мероприятий защиты медицинских подразделений и частей с целью минимизации вредного действия поражающих факторов радиационной и химической природы на личный состав медицинской службы, раненых и больных.
Кроме общих задач радиационной и химической разведки в подразделениях и частях медицинской службы решаются частные задачи:
• обнаружение радиоактивного или химического заражения личного состава медицинской службы, раненых и больных для определения необходимости проведения мероприятий санитарной обработки;
• определение степени радиоактивного или химического заражения медицинского имущества и техники для решения вопроса о необходимости проведения дезактивации и дегазации;
• установление факта зараженности воды и продовольствия радиоактивными, отравляющими и высокотоксичными веществами с целью решения вопроса о возможности и сроках их использования;
• определение дозы внешнего облучения и оценка степени внутреннего радиоактивного заражения раненых и больных, поступивших на этапы медицинской эвакуации;
• обнаружение отравляющих и высокотоксичных веществ в биосредах.
Для организации и проведения радиационной и химической разведки в районах постоянной дислокации медицинских подразделений, частей и учреждений начальник медицинской службы (начальник медицинского пункта, командир омедб, омедо) выделяет посты радиационно-химиче-ского наблюдения, оснащенные специальными приборами и средствами оповещения. Радиационно-химическое наблюдение осуществляется санитарным инструктором-дозиметристом, в помощь которому придаются два-три военнослужащих, обученных правилам работы с приборами радиационной и химической разведки. В задачи наблюдателей входит:
• установление факта радиационного или химического заражения в районе дислокации медицинских подразделений и частей;
• определение уровня радиации (мощности дозы) на местности, типа и концентрации отравляющих и высокотоксичных веществ в воздухе;
• доклад данных радиационной и химической разведки командиру (начальнику);
• подача сигналов оповещения о радиационном или химическом заражении.
При смене мест дислокации этапов медицинской эвакуации на маршруты движения и в места предстоящего развертывания высылаются рекогносцировочные группы в составе фельдшера, санитарного инструктора-дозиметриста и двух-трех военнослужащих, умеющих работать с приборами радиационной и химической разведки. На них возлагаются следующие обязанности:
• установление радиационной или химической зараженности маршрутов передвижения;
• выявление направлений с наименьшим уровнем зараженности или путей обхода сильно зараженных участков местности.
По мере приближения к новому району развертывания подразделений и частей медицинской службы радиационная и химическая разведка осуществляется дозором, входящим в состав рекогносцировочной группы. Дозор устанавливает наличие радиоактивного или химического заражения в местах развертывания и, если оно имеется, определяет изменение степени заражения местности и воздуха во времени.
Проведение радиационного и химического контроля в подразделениях и частях медицинской службы возлагается на сортировочный пост и дежурную службу.
Сортировочный пост развертывается силами и средствами приемно-сортировочных (сортировочно-эвакуационных) отделений. Он оснащается специальными приборами радиационной и химической разведки, знаками ограждения, средствами связи и оповещения. Работающий на сортировочном посту санитарный инструктор-дозиметрист проводит радиометрический и химический контроль заражения кожи, обмундирования, средств индивидуальной защиты раненых и больных, поступающих из радиационных и химических очагов, а также оценивает степень зараженности транспорта, доставившего пострадавших, и их личного оружия. Контроль радиоактивного или химического заражения проводится с целью определения необходимости в проведении специальной обработки: санитарной обработки личного состава, раненых и больных, поступивших на данный этап медицинской эвакуации, и дезактивации или дегазации вооружения, техники, имущества, обмундирования и средств индивидуальной защиты. В случае превышения установленных норм санитарный инструктор-дозиметрист направляет личный состав, раненых и больных и зараженный транспорт на площадку (в отделение) специальной обработки.
В обязанности санитарного инструктора-дозиметриста также входит осуществление постоянного радиационного и химического наблюдения в районе развертывания медицинского подразделения или части.
Контроль зараженности медицинского имущества радиоактивными, отравляющими и высокотоксичными веществами санитарный инструктор осуществляет на площадке специальной обработки. Определение зараженности воды и продовольствия производится, как правило, специально подготовленным фельдшером, а выдача заключений о возможности их использования — начальником медицинской службы.
26.4. Организация и проведение контроля доз облучения личного состава, раненых и больных на этапах медицинской эвакуации
Контроль облучения организуется в целях получения информации о дозах облучения личного состава, раненых и больных. Он осуществляется при действиях личного состава в условиях воздействия ионизирующих излучений: в мирное время — при проведении работ с источниками ионизирующих излучений, в военное время — при ведении боевых действий в условиях применения ядерного оружия, а также при авариях (разрушениях) на объектах ядерно-энергетического цикла.
Контроль облучения подразделяется на войсковой и индивидуальный. Войсковой (или групповой) контроль облучения осуществляется в военное время с целью получения информации об облученности личного состава и оценки боеспособности подразделений в ходе выполнения задачи. Групповой метод контроля заключается в том, что по показаниям 1—2 дозиметров делается вывод об облучении группы военнослужащих (отделение, экипаж) или группы раненых и больных, находящихся примерно в одинаковых условиях облучения.
Индивидуальный контроль основан на измерении дозы облучения каждого человека. В мирное время он проводится только в воинских частях, проводящих работы с источниками ионизирующих излучений, в военное время — во всех воинских частях. Индивидуальный контроль предусматривает получение информации об индивидуальных дозах облучения при медицинской сортировке раненых и больных на этапах медицинской эвакуации, при проведении медицинских обследований личного состава и при выполнении работ с источниками ионизирующих излучений.
Информация о дозах облучения личного состава используется как для предотвращения облучения личного состава свыше установленных предельно допустимых доз (в мирное время), так и для оценки поражающего действия ионизирующих излучений на личный состав войск. На основании информации о дозах облучения личного состава осуществляются:
• оценка боеспособности по радиационному фактору и определение порядка дальнейшего использования воинских частей (подразделений) и отдельных военнослужащих, подвергшихся воздействию ионизирующих излучений;
• планирование пополнения войск личным составом;
• ранняя диагностика степени тяжести острых лучевых поражений личного состава и медицинская сортировка раненых (пораженных) на этапах медицинской эвакуации;
• определение необходимого объема лечебно-эвакуационных мероприятий для лиц, подвергшихся воздействию ионизирующих излучений;
• оценка состояния радиационной безопасности при работах с источниками ионизирующих излучений и планирование этих работ;
• оценка состояния здоровья личного состава, работающего с источниками ионизирующих излучений.
Организация контроля облучения заключается в обеспечении личного состава измерителями дозы, в своевременном снятии показаний измерителей доз и их перезарядке, поддержании технической исправности приборов, систематическом учете доз облучения в подразделениях, в представлении вышестоящим командирам (начальникам) сведений и донесений о дозах облучения личного состава и боеспособности войск по радиационному фактору.
В качестве технических средств контроля облучения для проведения войскового контроля облучения применяются общевойсковые измерители дозы, для проведения индивидуального контроля облучения — индивидуальные измерители дозы. Общевойсковые и индивидуальные измерители дозы носятся, как правило, в нагрудном кармане обмундирования. Обеспечение войск техническими средствами контроля облучения и их ремонт осуществляются специалистами службы радиационной, химической и биологической защиты.
Войсковой контроль организуется групповым (один общевойсковой измеритель дозы на отделение) или индивидуальным (один общевойсковой измеритель дозы на каждого генерала и офицера) способами. Он проводится с помощью измерителей доз ИД-1 или ДКП-50А с целью получения информации об облученности личного состава и оценки боеспособности подразделений в ходе выполнения боевой задачи. Аналогичным образом проводится контроль облучения и личного состава медицинских подразделений и частей.
Дозы облучения, полученные личным составом, ежесуточно регистрируются в журнале учета доз. Периодически суммарная доза с указанием даты переносится в карточку учета доз, которая находится в военном билете или удостоверении личности военнослужащего. Кроме того, в вышестоящий штаб, при действиях войск в условиях применения ядерного оружия, ежесуточно представляется донесение об облучении личного состава и боеспособности подразделений в радиационном отношении.
На этапах медицинской эвакуации осуществляется индивидуальный контроль облучения. Индивидуальный контроль проводится с целью получения данных для установления тяжести лучевой болезни, последующей сортировки и определения необходимых лечебно-эвакуационных мероприятий. В некоторых случаях индивидуальный и групповой методы контроля не позволяют оценить дозу облучения пораженных, поступивших на этапы медицинской эвакуации, и использовать ее для оценки степени тяжести лучевой болезни. Поэтому при опасности облучения для ранней диагностики лучевого поражения, независимо от метода общевойскового контроля облучения, все военнослужащие обеспечиваются индивидуальными дозиметрами ИД-11 или ДП-70МП, а все медицинские подразделения, части и учреждения медицинской службы обеспечиваются измерительными устройствами для снятия показаний этих дозиметров.
Снятие показаний индивидуальных дозиметров ИД-11 или ДП-70МП осуществляется специально подготовленным фельдшером (санитарным инструктором) при медицинской сортировке раненых (пораженных) и при проведении медицинских обследований. Определение доз облучения раненых (пораженных) производится до осмотра врачом.
Доза облучения, полученная пораженным, записывается в первичную медицинскую карточку или историю болезни, а дозиметр возвращается пораженному. При выписке из медицинских частей (учреждений) суммарная доза облучения (полученная до поступления и за время пребывания в лечебном учреждении) переносится в карточку учета доз.
26.5. Организация и проведение экспертизы воды и продовольствия на зараженность отравляющими, высокотоксичными и радиоактивными веществами
При опасности воздействия отравляющих, высокотоксичных или радиоактивных веществ в подразделениях, частях и учреждениях медицинской службы осуществляется войсковой контроль химического и радиационного заражения воды и продовольствия. Войсковой химический и радиационный контроль воды и продовольствия — это установление их зараженности отравляющими, высокотоксичными или радиоактивными веществами с помощью приборов химической и радиационной разведки с целью решения вопроса о возможности использования по назначению, необходимости проведения специальной обработки воды и продовольствия или дальнейшего их исследования в ходе санитарно-токсикологиче-ской и санитарно-радиологической экспертизы. Он проводится под руководством командиров подразделений специально подготовленными для проведения радиационно-химической разведки фельдшерами или санитарными инструкторами. В тех случаях, когда медицинский состав не может сделать окончательное заключение на месте, производится отбор проб воды и продовольствия для направления их в санитарно-эпидемиологические учреждения для проведения санитарно-токсикологической или санитарно-радиологической экспертизы.
Войсковой контроль и экспертиза воды для питьевых и санитарно-технических нужд при подозрении на химическое или радиоактивное заражение проводится в обязательном порядке. Контроль и экспертиза продовольствия осуществляется, если продовольствие находилось в районах применения противником оружия массового поражения, в районах аварий (разрушений) радиационно и химически опасных объектов, если поступают трофейные продукты питания или имеется подозрение на заражение продовольствия диверсионным путем, а также при необходимости оценки остаточного заражения после специальной обработки продуктов питания.
Химический контроль и экспертиза воды и пищевых продуктов в подразделениях и частях медицинской службы (медицинском пункте полка, отдельном медицинском батальоне) производится с помощью прибора МПХР (ПХР-МВ), а в санитарно-эпидемиологических учреждениях — с помощью полевой лаборатории МПХЛ. Радиационный контроль осуществляют с помощью прибора ДП-5В, которым оснащаются все подразделения и части Вооруженных Сил (в том числе, и медицинские), а сани-тарно-радиологическую экспертизу — с помощью прибора ИМД-12.
Химическое заражение водоисточников возможно с помощью химических средств нападения (бомбы, снаряды, ракеты и т. п.), диверсионным путем, а также за счет попадания в них вод, стекающих с зараженной территории. Не исключено применение противником в целях морального воздействия так называемых денатурирующих веществ, которые в эффективных дозах не ядовиты, но могут делать воду непригодной для питья, придавая ей неприятный вкус и запах (вещества типа хлорфенола, многие водорастворимые красящие вещества).
Степень зараженности воды зависит от ряда факторов, главными из которых являются химическая природа и физическое состояние ОВТВ, гидролитическая устойчивость, количество яда, попавшего в водоем, характер водоснабжения.
Заражение открытых водоемов отравляющими и высокотоксичными веществами возможно при их применении в капельно-жидком и аэрозольном состоянии. Химическое заражение происходит при непосредственном попадании ОВТВ в источник воды, а также с дождевыми и талыми водами. Небольшие непроточные водоемы (озера, пруды, особенно колодцы) могут быть заражены ОВТВ на срок, исчисляемый неделями и месяцами, а заражение крупных и быстротекущих рек опасными концентрациями этих веществ практически не осуществимо. Вода в трубчатых и хорошо закрытых шахтных колодцах глубиной не менее 5—6 м практически остается незараженной, однако при значительных плотностях заражения местности ФОВ, а также при подозрении на диверсионные акции эти источники воды подлежат контролю на зараженность.
Химические вещества, гидролиз которых протекает с образованием нетоксичных продуктов (фосген, дифосген), практически не вызывают заражения воды. Трудно гидролизуемые ОВ, например, вещества типа VX, дают устойчивое и длительное заражение. Зоман и зарин быстро и полностью растворяются в воде, сохраняясь, как и VX, в водных растворах летом, весной и осенью неделями, а зимой — месяцами. Сернистый иприт в воде летом сохраняется около 1 ч, весной и осенью — 4—6 ч, зимой — 14—16 ч. Азотистый иприт и его соли могут сохраняться в воде более длительное время.
Плотность заражения пищевых продуктов зависит от физико-химических свойств, агрегатного состояния ОВТВ в момент контакта с пищевым продуктом, характера упаковки, длительности воздействия токсиканта и свойств конкретного продукта.
Отравляющие и высокотоксичные вещества могут заражать пищевые продукты в капельно-жидком, аэрозольном и парообразном состоянии. Капельно-жидкое заражение продовольствия возможно при разрыве химического боеприпаса вблизи места хранения продуктов, а также при разбрызгивании ОВТВ с помощью выливных авиационных приборов. Заражение продуктов питания парами и аэрозолями ОВТВ возможно при хранении их в складских помещениях и упаковках, проницаемых для аэрозолей и паров отравляющих веществ, как вблизи разрыва химического боеприпаса, так и на значительном удалении вследствие движения облака по направлению ветра. Не исключена возможность заражения запасов продовольствия диверсионным путем.
Отравляющие и высокотоксичные вещества хорошо сорбируются пищевыми продуктами и длительное время сохраняются в них. Особенно большую опасность представляют стойкие ОВТВ (VX, зоман, иприт), которые могут вызывать опасное заражение пищевых продуктов на несколько суток, недель и даже месяцев. Нестойкие ОВТВ типа фосгена в силу своей летучести сохраняются в пищевых продуктах недлительное время, однако такие продукты для немедленного использования могут оказаться непригодными. Большую опасность представляют продукты питания, зараженные жидкой синильной кислотой, в связи с образованием нелетучих солей синильной кислоты. Хлорацетофенон, бромбензилцианид и другие раздражающие вещества, включая и мышьяксодержащие, при воздействии на продукты питания долго оставляют в них свой неприятный запах, но не вызывают опасного заражения. Сернистый иприт в парообразном, тума-нообразном и капельно-жидком виде вызывает весьма устойчивое заражение пищевых продуктов, особенно жиросодержащих. Пары иприта проникают в зерно и крупы на глубину до 10 см, в муку — до 6 см, в твердые продукты (мясо, рыба, хлеб) — на 1—2 см. В жирах и маслах капельно-жид-кий иприт, а также его аэрозоли в силу своей липидофильности растворяются очень быстро, постепенно распространяясь по всей массе.
Стеклянная и металлическая тара полностью защищает от ОВТВ продукты, хранящиеся в ней (бидоны, бочки, консервные банки), а также в герметично закрытых емкостях (термосы, бидоны). Упаковка из картона и бумаги, полиэтиленовые мешки, деревянные и фанерные ящики не защищают продукты от ОВТВ. В незащищенные сыпучие пищевые продукты (крупа, мука, зерно и др.) ОВТВ в зависимости от агрегатного состояния проникают на глубину 1—7 см, в толщу мяса — на 2—5 см, в овощи — на 0,5—2 см, а в жиросодержащих продуктах очень быстро растворяются и заражают всю их массу. В ранние сроки после воздействия ОВТВ на неза-таренное продовольствие и продукты в наибольшей степени заражаются поверхностные слои. С течением времени зараженность этих слоев снижается, а более глубоких возрастает, в связи с чем необходимо избегать перемешивания поверхностных слоев с глубокими, так как это ухудшает условия для десорбции отравляющего вещества и увеличивает время сохранения его в продукте.
Заражение воды и продовольствия радиоактивными веществами возможно при выпадении радиоактивных осадков ядерного взрыва и при действиях на радиоактивно-зараженной местности, а также при совершении диверсионных или террористических актов. Наиболее опасно заражение открытых водоемов и незатаренного продовольствия. В воде и жидких пищевых продуктах радиоактивные вещества растворяются, заражая их на всю глубину, а в твердых и сыпучих пищевых продуктах чаще всего происходит заражение лишь поверхностных слоев.
При отборе проб воды и продовольствия в районе заражения отравляющими, высокотоксичными или радиоактивными веществами необходимо соблюдение мер предосторожности с использованием средств индивидуальной защиты. Отбор проб на экспертизу проводится со строгим учетом данных химической разведки: где, когда и с использованием какого ОВТВ был нанесен химический удар противника.
При взятии проб из источников воды и пищевых объектов тщательно обследуется прилегающая местность в целях выявления признаков заражения ОВТВ. Все подозрительные участки грунта, растительность, тара с признаками заражения капельно-жидкими или порошкообразными рецептурами неизвестных веществ подлежат исследованию. Грунт отбирается лопаткой, растительность срезается ножницами или ножом. Отобранные образцы перекладываются пинцетом в банки или полиэтиленовые мешочки.
В первые часы после заражения воды, а также, если сроки заражения неизвестны, пробы отбирают в верхнем слое с подветренной стороны непосредственно с поверхности, на глубине 20—30 см от поверхности воды и в нижнем слое (на 20—30 см от дна). В более поздние сроки заражения пробы отбирают из среднего слоя водоема и со дна. В каждом слое воды пробы отбирают из двух и более различных мест и смешивают их в общую пробу.
При взятии пробы из верхних слоев воду зачерпывают банкой или любым другим чистым сосудом. Для взятия пробы воды из придонного слоя используют батометр (табельный или приспособленный). Пробы воды из рек, озер берут ведром или банкой с поверхности вблизи берега, особенно в местах с видимыми маслянистыми пятнами и налетами.
Из артезианской скважины или водопровода воду предварительно выпускают в течение 10 мин, а затем наполняют бутыль. Каждая проба воды (из различных слоев источника воды, из колодца или водопровода) по объему должна быть не меньше 1,5—2 л.
Если проба воды будет доставлена на анализ позже 2 ч с момента ее взятия, ОВТВ извлекаются адсорбентом или органическим растворителем по специальной методике. Поэтому в санитарно-эпидемиологическое учреждение направляют 2 л воды и пробирку с осушенным углем, после фильтрования через него с помощью сорбционной колонки 1,5—2 л воды.
Для отбора проб пищевых продуктов необходимо оборудовать специальный металлический ящик с ячейками. В нем должны быть уложены: отборник проб почвы, щуп для отбора сыпучих продуктов, мерник или пружинные весы для измерения объема или массы пробы, банки по 500 мл с крышками и этикетками для проб жидких продуктов, полиэтиленовые мешочки для проб сухих продуктов, пинцет, нож, ножницы, совок, сачок для насекомых и банка с пробирками для отбора проб на биологическое исследование.
Предварительному лабораторному контролю подвергаются пищевые продукты, хранившиеся открыто или в недостаточно герметичной таре (полиэтилен, мешковина, картон, фанера, пергамент, бумага с полиэтиленовым покрытием). Пробы таких пищевых продуктов направляются на лабораторный контроль вместе с образцами тарного материала. Пищевые продукты, хранившиеся в стеклянной и металлической таре, после дегазации наружной поверхности тары пригодны к употреблению без проведения экспертизы.
Пробу сыпучих пищевых продуктов, находящихся в мешочной таре, берут с помощью металлического щупа или лопатки из наиболее подозрительных на заражение участков. Для этого делают П-образный разрез мешковины на площади 10x15 см, после чего берут пробу на глубину 1,0—1,5 см. В мешках с крупой, сахарным песком или мукой отбирают пробу на глубину до 3 см.
Пробу сухарей, галет, печенья, сухих овощей, пищевых концентратов, кускового сахара отбирают на глубину до 10 см с поверхности, прилегающей к участкам тары с наибольшим заражением.
Пробы мяса, рыбы, хлеба и твердых жиров отбирают с помощью скальпеля и пинцета, срезая слой толщиной 0,5—1,0 см с мест наибольшего заражения или тех отдельных участков, где видны следы ОВТВ (капли, пятна, мазки). Мелкую рыбу, свежие фрукты и овощи берут целыми экземплярами.
Пробу жидких продуктов (растительное масло, жидкая пища и др.) берут после тщательного перемешивания всей массы, находящейся в посуде (бутылке, банке, бидоне и т. п.); зачерпывается поверхностный слой до 5 см.
Масса пищевого продукта, направленного на анализ, должна быть не менее 150—200 г. Жидкие пищевые продукты, свежие овощи направляются на экспертизу по 500 г, твердые и сыпучие продукты — по 150—200 г, фасованные и штучные продукты с массой менее 500 г — поштучно.
Если пищевые продукты содержат значительное количество влаги, необходимо дублировать пробы путем извлечения ОВТВ из продукта органическим растворителем по специальной методике.
При отборе проб необходимо их пронумеровать, указать место взятия, время заражения и взятия пробы, фамилию взявшего пробу. Отобранные пробы должны быть плотно укупорены и уложены в специальный ящик вместе с сопроводительными бланками. Ящик опечатывают и с нарочным на отдельном транспорте отправляют в санитарно-эпидемиологическое учреждение. Доставку проб в химическую лабораторию медицинской службы подразделения и части осуществляют своими силами и средствами. Условия упаковки и транспортировки взятых проб воды и продовольствия должны обеспечить безопасность окружающих и сохранность ОВТВ в доставленном материале.
Сопроводительное донесение к пробам заполняет и подписывает представитель медицинской службы, ответственный за отбор проб. В нем указывают:
• адрес, по которому направляется проба;
• цель исследования (определение степени зараженности или полноты дегазации с указанием вида дегазации);
• место нахождения объекта, где взята проба;
• номер и время взятия пробы;
• наименование, масса (объем) и условия взятия пробы;
• результаты предварительного контроля и предположительно характер заражения пробы;
• время отправления пробы;
• адрес, по которому необходимо направить результаты анализа;
• должность, воинское звание и фамилия лица, направившего пробу.
Поступающие в санитарно-эпидемиологическое учреждение пробы воды и продовольствия, подозрительные на заражение отравляющими, высокотоксичными и радиоактивными веществами, подвергаются первичной обработке в отдельном помещении (отдельная палатка, комната). Первичная обработка осуществляется в условиях приточно-вытяжной вентиляции, исключающей попадание ОВТВ в органы дыхания, на кожные покровы, для чего в лабораторных условиях используются вытяжной шкаф, защитный фартук, нарукавники, перчатки, а в полевых условиях поднимается полог палатки, применяются противогаз и защитный костюм. Часть поступившей на первичную обработку пробы подлежит химико-токсикологическим исследованиям, вторая часть — после обезвреживания в ней ОВТВ, передается на радиометрическое исследование. Обез-
вреживание проб, направленных на радиометрические исследования, проводится путем выпаривания, проветривания или обработки дегазирующими растворами.
В том случае, когда нет информации о времени и виде примененного противником ОВТВ в районе обследуемого объекта или когда им применяются новые, неизвестные ОВТВ, проводится полный (или систематический) анализ проб воды и продовольствия. Кроме того, систематическому анализу на зараженность ОВТВ подвергаются пробы трофейного продовольствия, а также пробы воды из источников, ранее находившихся на территории противника. При наличии информации о природе примененного вещества анализ проб может производиться в определенном объеме, т. е. на зараженность конкретными ОВТВ.
Систематический анализ проб воды предусматривает непосредственное определение зараженности воды, извлечение ОВТВ из воды березовым активированным углем, органическими растворителями и постановку биопроб. Для систематического анализа продовольствия часть продукта помещают в цилиндр прибора для воздушной экстракции и подвергают предварительному исследованию на зараженность ОВТВ посредством индикаторных трубок, имеющихся в комплекте МПХЛ. После этого оставшаяся часть пробы подвергается анализу в растворах петролейного эфира, спирта и воды. Анализ пробы продовольствия завершается постановкой биопроб на животных.
Токсикологический (биологический) контроль проводится для установления факта заражения ОВТВ продовольствия, воды и других объектов внешней среды, когда химическими и биохимическими методами токсиканты не распознаются. Полученные результаты токсикологического контроля могут быть использованы для решения экспертных вопросов, связанных с организацией и проведением профилактических и лечебных мероприятий.
По результатам экспертизы воды и продовольствия могут быть приняты следующие решения:
• продовольствие или вода пригодны к использованию по назначению без ограничений;
• продовольствие или вода пригодны к использованию с ограничением сроков потребления (если их зараженность не превышает соответствующих максимально-допустимых концентраций);
• продовольствие пригодно к употреблению после проведения рекомендуемой кулинарной обработки;
• продовольствие и вода не пригодны к употреблению и подлежат дегазации с последующей повторной экспертизой с решением вопросов возможного использования по назначению;
• продовольствие не пригодно для употребления личным составом и подлежит уничтожению;
• вода пригодна для питья и хозяйственных нужд после ее очистки техническими средствами инженерных войск.
В соответствии с полученными рекомендациями командир части объявляет решение о дальнейшем использовании воды и продовольствия.
Продовольствие и вода, зараженные отравляющими, высокотоксичными или радиоактивными веществами выше предельно допустимых концентраций, подвергаются дегазации или дезактивации. В этом случае на медицинскую службу возлагаются повторная индикация ОВТВ в воде и продовольствии, подвергшихся дегазации, повторная оценка уровня их радиоактивного заражения, определение доброкачественности воды и пиши и проведение экспертизы для решения вопроса о их пригодности к употреблению.
При действиях в районах радиоактивного загрязнения приготовление и прием пищи организуются только на незараженных участках местности. Если по условиям обстановки это невозможно, приготовление пищи допускается на участках местности с уровнем радиации до 1 Р/ч, а при уровнях радиации до 5 Р/ч развертывание полевых кухонь производится в палатках. На местности с более высокими уровнями радиации приготовление пищи должно производиться в дезактивированных закрытых помещениях и сооружениях, местность вокруг которых необходимо дезактивировать или увлажнять. Прием пищи на открытой местности и в открытых оборонительных сооружениях разрешается при уровнях радиации до 5 Р/ч. При более высоких уровнях радиации пища должна приниматься на дезактивированной увлажненной территории или в специально оборудованных машинах и убежищах.
Приготовление пищи на зараженной ОВТВ местности не разрешается. Приготовление и прием пиши допускаются только в специально оборудованных укрытиях и военной технике. Готовая к употреблению горячая пища, подозреваемая на заражение ОВТВ, химическому контролю и экспертизе не подвергается и подлежит уничтожению.
Учебное издание
Сергей Алексеевич Куценко Николай Викторович Бутомо Александр Николаевич Гребенюк Юрий Юрьевич Ивницкий Валерий Павлович Мельничук Татьяна Николаевна Преображенская Виктор Михайлович Рыбалко Николай Васильевич Саватеев
ВОЕННАЯ ТОКСИКОЛОГИЯ, РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ ЗАЩИТА
Учебник
Под редакцией профессора С. А. Куценко
ISBN 5-93929-082-5
 |
Лицензия ИД № 01081 от 28.02.2000 ООО «Издательство ФОЛИАНТ»
Редактор Н. Д. Пылева Компьютерная верстка Н. Н. Сергиевской
ООО «Издательство ФОЛИАНТ»
190020, Санкт-Петербург, Нарвский пр., 18, оф. 501 тел./факс: (812) 325-39-86, 186-72-36 e-mail: foliant@peterlink.ru
Подписано в печать 23.10.2003. Формат 70x100 W Печ. л. 33. Гарнитура Тайме. Печать офсетная. Тираж 1000 экз. (II завод — 5001 — 10000). Заказ № 3055
Отпечатано с готовых диапозитивов в Академической типографии «Наука» РАН 199034, Санкт-Петербург, 9 линия, 12
Отсканировал Кипер Руслан
– Конец работы –
Используемые теги: Военная, Токсикология, радиобиология, медицинская, Защита0.077
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ВОЕННАЯ ТОКСИКОЛОГИЯ, РАДИОБИОЛОГИЯ И МЕДИЦИНСКАЯ ЗАЩИТА
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов