КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛО В
Металлы представляют собой поликристаллические тела, состоящие из большого числа мелких (10-1 – 10-5 см) кристаллов, разориентированных по отношению друг к другу.
Металлы и металлические сплавы



 Кристаллы с металлическим типом связи, наличие элек-
Кристаллы с металлическим типом связи, наличие элек-
тронного газа.
Кристаллы (кристаллическая решетка)
Наличие дальнего порядка в расположении атомов.
| Атомы | распола- |
| гаются | на рас- |
| стоянии, | когда |
| энергия | о тта л - |
| кивания | и при- |
| тяжения | равны. |







 Свойств а
Свойств а
Термоэлектронная эмиссия
Выс о к а я тепло- и электропроводность
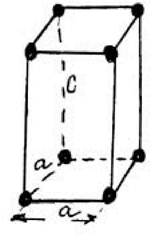
Строение кристаллической решетки описывается элементарной ячейкой. Элементарная ячейка - это наименьший объем кристалла, дающий представление о строении всего кристалла. Характеристики ячейки - ребра a, b, c и углы между ними ос, (3, у; отрезки a, b, c называются периодами решетки.





















 Металлический блеск, отражательная способность
Металлический блеск, отражательная способность
Элементарная ячейка
Повышенная способность пластического деформирования
Положительный тем -пературный коэффициент электросопротивления
 |  |
| i |
ИДЕАЛ ЬНОЕ СТРОЕНИЕ КРИСТАЛЛОВ
I
однородность, закономерность и симметричность в расположении атомов определяет тип кристаллической решетки.




 Характеристики решетки: координационное число к (число атомов, находящихся на равном и наименьшем расстоянии от данного атома), период, плотность упаковки, коэффициент к о м пак тно с ти η, число атомов на ячейку n). Наиболее часто встречающиеся типы решеток
Характеристики решетки: координационное число к (число атомов, находящихся на равном и наименьшем расстоянии от данного атома), период, плотность упаковки, коэффициент к о м пак тно с ти η, число атомов на ячейку n). Наиболее часто встречающиеся типы решеток
I
| Кубическая решетка «4=4=Vc объемно-центрированная |
| Тетрагональная решетка а = b ^ с а = |3 = у= 900С |
| е- |
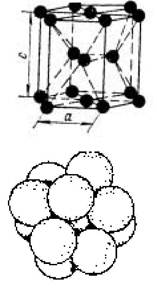
Гексагональная
шетка (ГПУ) (плотноупакованная)
а = Ь Ф с
|
| ^=И ^а '^ |
а = р = 90°С,у=120°
|

|
| n, η, k – зависит от отношения с/a – степени те тр а г о -нальнос ти. |
с/а = 1,633

Pb, Na, Tip, Feb-, W, Vflp.
| п = 6,л= 74 %, к = 12 Mg,a, Cd, Be, Tifoaa, йт,СОри др. |
 п = 2, л = 68 %, и = 8 гранецент ГЦК рованная
п = 2, л = 68 %, и = 8 гранецент ГЦК рованная

| FeY, Си, Ni, Со, Ag и др. п = 4, г| = 74 %, к = 12 |
^це л ые ра цио на л ь ные чис ла являющ ие ся величинами, обратными отрезку осей, отсекаемых данной плоскостью по осям координатх, у, z
Т
РЕАЛЬНОЕ СТРОЕНИЕ КРИСТАЛЛОВ
 |  | ||
 |
| I |
в решетке имеются нарушения строения - структурные несовершенства (дефекты)
I


 Точечные дефекты -малы во всех направлениях. 1. вакансии
Точечные дефекты -малы во всех направлениях. 1. вакансии
| L J | |||||||
| ^* | ft | ||||||
| ''! | |||||||
| X | Мн | ||||||
| (Н | |||||||
2. межузельные атомы (дефект Френкеля)

3. примесные атомы замещения

Линейные дефекты - дислокации - малые размеры в двух измерениях и большая протяженность в третьем.
1. Краевая (линейная)
дислокация (экстра
плоскость)
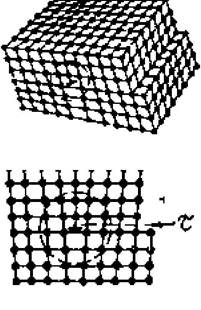
2. Винтовая дислокация - линия, вокруг которой атомные плоскости изогнуты по спирали.

Поверхностные дефекты - малы в одном измерении.
1. Границы зерен -больше угловые границы
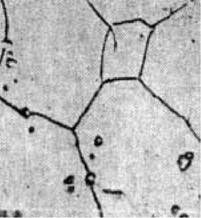
| субструктура |
2. Границы субзерен мало угловые гран ицы

Оказывают существенное влияние на свойства металлов и сплавов
Нал ич ие дефектов предопределяет возможность диффузии – перемещения атомов на расстояния, большие межатомных. Процесс диффузии, в первую очередь, зависит от температуры. Чем выше температура, тем интенсивнее процесс диффузии.
ДИФФУЗИЯ



 Самодиффузия – перемещение атомов, не связанное с изменением концентрации в отдельных объемах.
Самодиффузия – перемещение атомов, не связанное с изменением концентрации в отдельных объемах.
Гетеродиффузия сопровождается изменением концентрации в отдельных объемах, происходит в сплавах с повышенным содержанием примесей .
 Механизмы диффузии
Механизмы диффузии




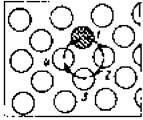
 вакансионный
вакансионный
обменный
циклический
межузельный

|

|
|
ТТППТТ]
| О. |
ш
диффузия С, N, Н
I
Характеристик и диффузии
 |  |  |  | ||||||
 |
| Скорость диффузии |
Коэффициент диффузии D – количество вещества, диффундирующего через единицу площади 1 см2 за единицу времени 1 с.
D = - A⋅e-Q / RT см2/с (градиент концентрации равен 1)
m = - D(dc/dx) - коли
чество вещества,
диффундирующего
через единицу площа
ди поверхности раз
дела за единицу вре
мени. По то к стацио
нарный.
I закон Фика.
Для нестационарного потока
dc/dτ = D(d2c/dx2) dc – концентрация; dx – расстояние в выбранном направлении; dτ - время; II закон Фика.
Наибо л ее легко процесс диффузии протекает по границам зерен, где сосредоточены дефекты кристаллического строения (вакансии, дислокации).
ВОПР ОСЫ ПО ТЕМЕ
1. Что определяет металлическое состояние металлов и сплавов? Какие свойства характеризуют металлы?
2. Что так о е кристаллическая решетка? Основные типы кристаллических решето к .
3. Что так о е координационное число?
4. Параметры кристаллической решетки.
5. Крис таллографичес кие плоскости и их индексификация.
6. Классификация дефектов кристаллического строения.
7. Что так о е точечные, линейные, поверхностные дефекты?
8. Что так о е диффузия? Самодиффузия, гетеродиффузия.
9. Механизмы диффузии.
10. Характеристики диффузии.
ЗАДАЧИ Задача № 1
Рассчитайте число атомов, приходящихся на одну элементарную ячейку в решетке ОЦК (рис. 1).
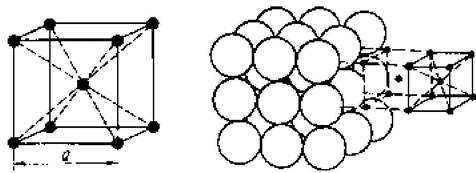
а) б)
Рис. 1 Решение:
Пронумеруем атомы в ячейке. Каждый атом в вершине куба (1-8) принадлежит восьми соседним ячейкам, следовательно данной ячейке приходит 1/8 атома. Таких атомов 8: 1/8⋅8 = 1 атом и один атом в центре решетки (9) 1+1 = 2. Ответ: 2 атома.
Задача № 2
Рассчитайте число атомов в решетке (рис. 2,а,б)
1) ГЦК (а); 2) ГПУ (б); 3) тетрагональная кубическая решетка (в)
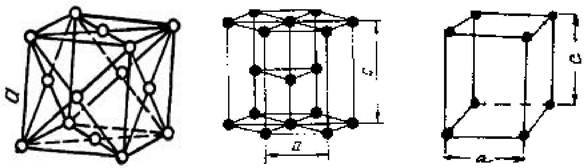
а) б) в)
Рис.2
Задача № 3
Определить какие дефекты кристаллического строения (1-8) имеются в решетке кристаллов, приведенных на рис. 3.
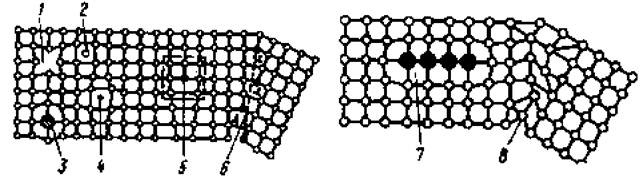
Рис. 3 Задача № 4
Рассчитайте и сравните коэффициенты диффузии для Feα и Feγ при 9110С, если
| для Feγ |
для Feα
| А = 0,6 см2/с Q = 68000 кал/г⋅ат |
А = 5,8 см2/с
Q = 59700 кал/г⋅ат
Задача № 5
Определить, насколько увеличится скорость диффузии в Feγ, если увеличить температуру с 9110С до 11000С.