рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Экология
- /
- Дисциплина Химические основы экологии
Реферат Курсовая Конспект
Дисциплина Химические основы экологии
Дисциплина Химические основы экологии - раздел Экология, Государственное Бюджетное Образовательное Учреждение Саратовской Области Сред...
Государственное бюджетное образовательное учреждение Саратовской области среднего профессионального образования
«БАЛАКОВСКИЙ ПОЛИТЕХНИЧЕСКИЙ ТЕХНИКУМ»
ХИМИЧЕСКИЕ ОСНОВЫ ЭКОЛОГИИ
Конспект лекций для студентов специальности280711
«Рациональное использование природохозяйственных комплексов»
Дисциплина Химические основы экологии
Раздел 3 Химия окружающей среды
Составила преп. Горбатова М. А.
2013 г
| Одобрено Предметно-цикловой комиссией химико - технологических дисциплин Председатель Горбатова М. А. «___» _________ 20___ г | Составлено в соответствии с ФГОС среднего профессионального образования по специальности 280711 «Рациональное использование природоохранных комплексов» Зам. директора по учебной работе _________________ Хаустова Л. Б. |
Оглавление
Атмосфера. 4
Состав атмосферы.. 5
Химические процессы в атмосфере. 6
Озон. 8
Реакции, способствующие разрушению озона в атмосфере Земли. 9
Действие озона на живые организмы и материалы.. 10
Химия аэрозолей и пыли. 11
Экологические проблемы, связанные с химией атмосферного аэрозоля. 11
Органические и неорганические загрязнители. 14
Летучие органические соединения. 15
Соединения серы и азота. 17
Парниковый эффект. 19
Парниковые газы.. 19
Чтo тaкoе фреoны.. 20
Городская атмосфера. 22
Последствия первичного и вторичного загрязнения воздуха. 24
Гидросфера. 26
Состав гидросферы.. 26
Качество природной воды.. 28
Химические процессы в гидросфере. 29
Речные воды.. 31
Океанические воды.. 31
Основные особенности океанической воды.. 31
Химия морской воды. Соленость и ионная сила воды.. 32
Соленость воды. 32
Ионная сила. 33
Активность. 33
Состав ионов в морской воде и закон Дитмара. 33
Химический состав неосновных ионов. 33
Вынос ионов. 34
Эвапориты. 34
Подземные воды.. 35
Формирование кислотности поверхностных вод. 37
Особенности окислительно-восстановительных процессов в подземных водах. 38
Глобальное загрязнение Мирового океана. 38
Загрязнения речных и морских вод. 39
Органическое загрязнение. 39
Сброс отходов в море с целью захоронения (дампинг). 43
Неорганические токсины.. 44
Соединения тяжелых металлов. 45
Поведение тяжелых металлов в водной среде. 45
Литосфера. 46
Химический состав литосферы.. 46
Химический состав почв. 48
Химические процессы в литосфере. 49
Химические реакции и процессы в почве. 50
Глобальные экологические функции почв. 53
Химическое загрязнение почв. 55
Изменения почвы в зависимости от способов ее обработки. 58
Методы и способы утилизации и ликвидации отходов. 66
Биосфера – особая оболочка планеты.. 68
Некоторые особенности биосферы.. 68
Процессы в биосфере. 69
Основные функции живого вещества в биосфере. 70
Круговорот веществ. 70
Химические процессы в биосфере. 73
Химические основы экологического анализа. 73
Меры токсичности веществ. 74
Экологическое нормирование. 75
Аналитическая химия в экологических исследованиях. 76
Особо опасные экотоксиканты.. 76
Вредные вещества в пищевых продуктах. Нитраты.. 80
Пестициды.. 81
Диоксины.. 81
Биотрансформация экотоксикантов. 84
Атмосфера
Общая масса земной атмосферы составляет примерно 5,15 • 1015 т. Верхняя граница атмосферы лежит на высоте около 1000 км над уровнем моря; выше… Наиболее плотный слой воздуха, прилегающий к земной поверхности, носит… Далее температура от границы 30 км начинает повышаться и на высоте 50 км достигает +10°С (стратосфера). В мезосфере…Состав атмосферы
Атмосфера представляет собой чрезвычайно сложную систему. Ее пронизывает излучение Солнца и испускаемые им частицы высокой энергии, а также… Таблица 1 Состав воздуха в приземном слое Компонент Содержание…Химические процессы в атмосфере
1) Большинство химических реакций инициируются не термически, а фотохимически, т.е. при воздействии квантов света, полученных в результате… Фотодиссоциация Солнце испускает энергию с разной длиной волны. Коротковолновое излучение в ультрафиолетовой области спектра обладает…Озон
Химия тропосферного и стратосферного озона
Озон образуется как в тропосфере, так и стратосфере. Озон в тропосфереотносится к токсичнымгазообразным компонентам. Стратосферный озон играет жизненно важную роль в защите всего живого на Земле от губительной УФ-радиации.
Схема процесса образования тропосферного озона резко отличается от образования стратосферного озона.
На начальных стадиях образования озона в тропосфере решающую роль играет СО:
НО• + СО → СО2 + Н•
Н• + О2 + М → НОО• + М
где М — частицы, участвующие в столкновениях, но не вступающие в реакции, например азот.
Образующийся при этом радикал пероксида водорода окисляет NО до NО2:
НОО•+NО→ НО• + NО2
Ночью NО2 стабилен. Днем под влиянием солнечного света (область длин волн мене 430 нм), как это происходит и вблизи от поверхности Земли, NО2 фотолитически расщепляется на NО и кислород в основном состоянии (активный кислород):
NО2 → NО + О•
Активный кислород может давать озон при взаимодействии с молекулярным кислородом, при этом требуется присутствие инертных частиц М:
О• + О2 + М →О3 + М
На большом удалении от источников выбросов в так называемых районах чистого воздуха можно наблюдать сравнительно высокие концентрации О3. Это связано с фотохимическими превращениями NО2 в О3 на большой высоте, в то время как вблизи поверхности оставшийся О3 реагирует с остатками NО.
Скорость образования озона зависит от освещенности, поэтому его концентрация изменяется в течение суток.
Озон является одним из важнейших компонентов стратосферы, но его общее содержание удивительно мало. Если весь озон сосредоточить в одном слое, толщина слоя молекул О3 составит всего 3 мм. В стратосфере образование озона происходит на высоте 30—50 км. На больших высотах образуется возбужденная молекула О3•
О• + О2 → О3•
Образование стабильной молекулы О3 происходит лишь в результате реакции О3 с любой другой газообразной частицей М:
О3• + М → О3 + М
С понижением высоты скорость образования озона сначала увеличивается, а затем начинает уменьшаться из-за поглощения излучения с длинами волн более 240 нм и распада молекул О3, что определяет наличие максимума содержания О3 на высоте 25 км:
О3 →О2 + О•
О3 + О•→ 2О2
Минимальная концентрация стратосферного озона наблюдается над экваториальным поясом, и она возрастает в направлении полюсов. В стратосфере Северного полушария содержится больше озона, чем в Южном полушарии, а годовой ход концентрации О3 в них носит зеркальный характер. В вертикальном направлении наибольшие концентрации озона приходятся на высоты от 15 до 40 км с максимумом при 24—27 км над экватором и 13—15 км над полярными областями обоих полушарий.
Молекулы озона сами могут поглощать излучение, и сильнее всего озоном поглощаются фотоны с длиной волны 200 - 310 нм, что очень важно для нас. Это излучение другими частицами не поглощается в той мере, как озоном. При таком излучении все живое не может существовать. «Озоновый щит» играет важную роль в сохранении жизни на Земле.
Реакции, способствующие разрушению озона в атмосфере Земли
N2O + O(1D) → NO + NO О3 + NO → NO2 + О2 NO2 + О → NO + О2Действие озона на живые организмы и материалы
Действие озона на растения. Чувствительные виды растений уже после часовой обработки озоном при концентрации 0,05—0,1 мг/м3 проявляют признаки… Действие озона на материалы. Наиболее заметное воздействие озон оказывает на…Химия аэрозолей и пыли
Подобно тому, как в природных водах присутствуют растворенные вещества и тонкие взвеси, в атмосфере содержатся не только свободные молекулы и ионы… Под атмосферной пылью понимают взвешенные в воздухе твердые частицы размером… Аэрозоли представляют собой коллоидные системы, в которых дисперсионной средой служит, как правило, воздух. Размер…Экологические проблемы, связанные с химией атмосферного аэрозоля
Например, выброс в атмосферу большого количества пепла при извержении вулкана Тамбора в Индонезии в 1815 г. привел к понижению температуры воздуха в… 2. Аэрозоли играют важную роль и в формировании гидрологического режима.… 3. На поверхности частиц конденсируется не только вода, но и многие другие компоненты атмосферы — соединения тяжелых…Органические и неорганические загрязнители
Метан
Метан — наиболее значимый представитель органических загрязнителей атмосферы. Его концентрация существенно превышает концентрацию остальных органических соединений. Увеличение содержания метана в атмосфере способствует усилению парникового эффекта за счет интенсивного поглощения теплового излучения Земли в инфракрасной области спектра. Метан занимает второе место после углекислого газа по эффективности поглощения теплового излучения Земли. С ростом может привести к ухудшению экологической ситуации на Земле.
Классификация метана.
Атмосферный метан различается по происхождению.
· Метан называется биогенным, если он возникает в результате химической трансформации органического вещества.
· Бактериальный (микробный) метан появляется в результате деятельности бактерий. Он образуется в донных отложениях болот и других водоемов, в результате процессов пищеварения в желудках насекомых и животных (преимущественно жвачных).
· Термогенный метан возникает в результате термохимических процессов в осадочных породах при их погружении на глубины 3—10 км. Здесь осадочные породы подвергаются химической трансформации в условиях высоких температур и давлений.
· Абиогенный метан возникает в результате химических реакций неорганических соединений. Он образуется обычно на больших глубинах в мантии Земли.
Общее содержание метана в атмосфере и его концентрация. Время жизни метана в атмосфере 8—12 лет. Молекула метана довольно устойчива, и ее нелегко вывести из атмосферы. Метан малорастворим в воде, удаление его из атмосферы с помощью осадков не происходит. Для реального удаления его необходимо перевести в нелетучие или другие газообразные соединения.
Метан, как и многие другие примеси, исчезает из атмосферы в основном в реакции с радикалом ОН•:
ОН• + СН4 → Н2О + СН3•
Суммарная реакция вывода метана из атмосферы:
СН4 +4О2 → СН2О + Н2О +2О3
В итоге вместо одной исчезнувшей в атмосфере молекулы метана возникает 3,5 молекулы озона и 0,5 радикала ОН•.
Химический сток в атмосфере — это основной канал вывода метана из атмосферы. Из других стоков некоторое значение имеют поглощение метана почвенными бактериями и уход в стратосферу. Оба стока вносят вклад менее 10 % в общий сток метана.
Источники выделения метана
К естественным источникам метана относятся болота, тундра, водоемы, насекомые (главным образом термиты), метангидраты, геохимические процессы. К антропогенным — рисовые поля, шахты, животные, потери при добыче газа и нефти, горение биомассы, свалки. В России производится 60 г метана в сутки в расчете на одного человека.
Шахтный метан возникает в процессе трансформации органических остатков в уголь под влиянием высоких давлений и температур. Растительные остатки содержат большое количество лигнина, в структуре которого имеется много метильных групп. В ходе термической переработки освобождаются метильные радикалы, которые затем отрывают атом водорода от органических молекул и превращаются в метан. Добыча 1 т угля сопровождается выделением 13 м3 чистого метана.
Летучие органические соединения
Вторым по мощности источником антропогенных органических загрязнителей служит промышленное производство. Базовыми продуктами основного органического… Биогенные ресурсы органических веществ Выделение органических соединений в окружающую среду — универсальное явление, характерное для всех видов организмов от…Соединения серы и азота
1. Биологические процессы. С помощью анаэробных (действующих без участия кислорода) микроорганизмов происходят различные процессы разрушения… 2. Вулканическая деятельность. При извержении вулкана в атмосферу наряду с… 3.Деятельность человека. В атмосферу в результате деятельности человека попадают значительные количества соединений…Парниковый эффект
Впервые мысль о парниковом эффекте была высказана Ж. Б. Фурье в 1827 г. По его выражению, атмосфера подобна прозрачной стеклянной оболочке, дающей… Сущность парникового эффекта заключается в следующем: парниковые газы…Парниковые газы
Закись азота. Глобальное потепление на 6 % обусловлено закисью азота (N2О). Он выделяется при разложении азотных удобрений в почвах, из стоков… Если не прервать накопление в атмосфере «парниковых газов», то во второй… В результате потепления может произойти непоправимое в судьбе нашей планеты: начнется таяние ледников Гренландии,…Чтo тaкoе фреoны
В 1987 году был принят Мoнреaльский прoтoкoл, oгрaничивaющий испoльзoвaние oзoнoрaзрушaющих существ. В чaстнoсти, сoглaснo этому акту, виновники… Если не прервать накопление в атмосфере «парниковых газов», то во второй… В результате потепления может произойти непоправимое в судьбе нашей планеты: начнется таяние ледников Гренландии,…Городская атмосфера
В городской среде присутствуют загрязняющие вещества, непосредственно выброшенные в атмосферу и называемые первичными загрязнителями. Дым — пример… Топливо обычно состоит из углеводородов, за исключением в основном… 2СН4 + 3O2 → 2СO2 + 2Н2ОПоследствия первичного и вторичного загрязнения воздуха
Фотохимический смог — не единственная проблема, создаваемая транспортом. С автомобилями связывают и другие загрязнители, например свинец (РЬ) и… Бензол — другой загрязняющий компонент из автомобильных топлив. Он… Бензол является также потенциальным возбудителем рака. Считается, что более 10% используемого бензола, (33 Мт/год)…Гидросфера
Состав гидросферы
Гидросфера — водная оболочка Земли, совокупность океанов, морей, водных объектов суши (реки, озера, болота, водохранилища), подземных вод, включая… Основная часть воды гидросферы (94%) сосредоточена в морях и океанах второе… Мировой океан — непрерывная водная оболочка Земли, окружающая континенты и острова, — занимает около 70,8 % земной…Качество природной воды
Если в питьевой воде обнаружено несколько веществ с одинаковым лимитирующим признаком вредности, то для них критерий качества воды имеет вид: С1 /… В настоящее время число установленных ПДК для водных объектов различного… Цветность (окраска) обусловлена присутствием в природных водах гумусовых и дубильных веществ, белково- и…Химические процессы в гидросфере
Рассмотрение химических процессов в гидросфере — задача очень сложная, более сложная, чем изучение процессов в атмосфере. Причина заключается в том,… Гидросфера — глобальная открытая система, стабильность которой тем выше, чем… Химические процессы в гидросфере имеют следующие особенности:Речные воды
Особенности речных вод: 1) в растворенном состоянии в химическом составе пресной воды преобладают… 2) низкая концентрация ионов в растворе;Океанические воды
Основные особенности океанической воды
Из всех растворенных в морской воде солей 85 % составляет хлорид натрия, в значительных количествах содержатся хлорид магния, сульфат магния и… Теплоемкость воды выше теплоемкости многих других веществ. В связи с большой… Плотность морской воды — масса воды, приходящаяся на единицу ее объема. Плотность морской воды зависит главным…Химия морской воды. Соленость и ионная сила воды
Существуют три основных свойства, которые определяют специфику химических процессов морской воды:
1) высокая ионная сила морской воды, связанная с соленостью (концентрацией солей);
2) химический состав морской воды с высоким содержанием ионов натрия и хлора;
3) закон Дитмара, согласно которому количественные соотношения между главными компонентами основного солевого состава всегда постоянны.
Соленость воды.
Соленость и ионный состав морской воды оставались примерно постоянными в течение последних 900 млн. лет. Эти данные были получены при изучении…Ионная сила
Концентрация ионов солей может быть выражена в виде ионной силы
I= 1/2 ∑ сi zi2
где I — ионная сила; c i — концентрация ионов, моль/л; z i — заряд иона. Размерность ионной силы — моль/л. Морская вода имеет очень высокое значение ионной силы, равное 0,7 моль/л. Речные воды имеют на три десятичных порядка меньше, т. е. 0,5 · 10 –3 моль/л.
Активность
Состав ионов в морской воде и закон Дитмара
Под хлорностью воды принимают число грамм-ионов хлора, эквивалентное сумме ионов галогенов, содержащихся в 1 кг воды, осаждаемых нитратом серебра. В…Химический состав неосновных ионов.
Это: 1) окислительно-восстановительные реакции на океаническом (морском) дне; 2) атмосферные процессы;Вынос ионов
• выброс ионов в атмосферу (потоки «море — воздух»); • процессы отложения в виде эвапоритов, химического осаждения карбонатов,… • гидротермальную циркуляцию морской воды через срединные океанические хребты.Эвапориты
Выводы • Специфика химических процессов морской воды определяется ее высокой ионной силой, высоким содержанием ионов натрия и…Подземные воды
Подземные воды рассматриваются как полезное ископаемое. В отличие от других видов полезных ископаемых, запасы подземных вод возобновимые в процессе…Классификация
По условиям залегания подземные воды подразделяются на несколько видов:
почвенные; грунто́вые; межпластовые; артезианские; минеральные.
Почвенные воды заполняют часть промежутков между частицами почвы; они могут быть свободными (гравитационными), перемещающимися под влиянием силы тяжести, или связанными, удерживаемыми молекулярными силами.
Грунто́вые воды образуют водоносный горизонт на первом от поверхности водоупорном слое. В связи с неглубоким залеганием от поверхности уровень грунтовых вод испытывает значительные колебания по сезонам года: он повышается после выпадения осадков или таяния снега, понижается в засушливое время. В суровые зимы грунтовые воды могут промерзать. Эти воды в большей мере подвержены загрязнению.
Межпластовые воды — нижележащие водоносные горизонты, заключенные между двумя водоупорными слоями. В отличие от грунтовых вод, уровень межпластовых вод меньше изменяется во времени. Межпластовые воды более чистые, чем грунтовые. Напорные межпластовые воды полностью заполняют водоносный горизонт и находятся под давлением. Напором обладают все воды, заключенные в слоях, залегающих в вогнутых тектонических структурах.
По степени минерализации выделяют подземные воды:
пресные – до 1 г/л,
солоноватые – 1–10 г/л,
солёные – 10–50 (35) г/л
подземные рассолы – свыше 50 (35) г/л.
По температуре они делятся на: переохлаждённые (ниже 0 °C), холодные (0–20 °C), тёплые (20–37 °C), горячие (37–50 °C), очень горячие (50–100 °C), перегретые (св. 100 °C). Под действием сил тяжести и гидравлического напора происходит перемещение подземных вод, их выход на земную поверхность, чаще всего в отрицательных формах рельефа, дренирование реками и водоёмами. Выходы подземных вод на земную поверхность формируют источники, подземное питание рек и водоёмов. Во многих случаях они становятся истоками рек.
Происхождение подземных вод и их распространение
По современным представлениям, подземные воды по происхождению могут быть экзогенными (их источник — водные объекты на поверхности суши и влага… Экзогенные подземные воды попадают в горные породы либо при процессах… Инфильтрационные подземные воды проникают в горные породы путем инфильтрации атмосферных, речных, морских и озерных…Формирование кислотности поверхностных вод
НСО3−+ Н+ ↔ Н2О + CO2 . Однако при нарушении контакта данной воды с карбонатными породами может… На второй стадии закисления водоема рН воды обычно не поднимается выше 5,5 в течение всего года (отсутствует контакт с…Особенности окислительно-восстановительных процессов в подземных водах
• Распределение и реакционная способность органического вещества и других потенциальных восстановителей в водоносном горизонте. Так, органическое… • Распределение веществ, способных создать редокс-буферность водоносного… • Скорость циркуляции подземных вод. Бактериальные реакции, имеющие тенденцию снижать ре– , протекают медленно,…Глобальное загрязнение Мирового океана
• захоронение на морском дне загрязняющих веществ (радиоактивные отходы, ядохимикаты и т. п.). Например, в Балтийском море захоронено 7 тыс. т… • разнообразные утечки с судов морского транспорта, например нефти (ежегодные сбросы нефтепродуктов составляют 2,5…Загрязнения речных и морских вод
Химическое загрязнение представляет собой изменение естественных химических свойств воды за счет увеличения содержания в ней вредных примесей как…Органическое загрязнение
Особую форму органических загрязнений представляют собой фекалии, так как они содержат патогенные микробы, выделяющиеся из организма человека и… При сильном загрязнении воды мочой и навозной жижей в ней оказывается большое… (NН4)2СО + 2Н2О → уреаза Н2СО3 + 2 NН3Нефть и нефтепродукты
Нефть, попавшая в природную среду, подвергается микробиологическому распаду, в котором участвуют различные виды бактерий, но этот распад протекает… Загрязнение фенолами происходят в значительно меньших размерах. Скорость… К числу продуктов, распад которых идет с трудом и длится более двух дней, относятся также хлорированные углеводороды,…Сброс отходов в море с целью захоронения (дампинг).
Многие страны, имеющие выход к морю, производят морское захоронение различных материалов и веществ, в частности грунта, вынутого при дноуглубительных работах, бурового шлака, отходов промышленности, строительного мусора, твердых отходов, взрывчатых и химических веществ, радиоактивных отходов. Во время сброса и прохождения материала сквозь столб воды часть загрязняющих веществ переходит в раствор, изменяя качество воды, другая — сорбируется частицами взвеси и переходит в донные отложения. Одновременно повышается мутность воды. Наличие органических веществ часто приводит к быстрому расходованию кислорода в воде и нередко к его полному исчезновению, растворению взвесей, накоплению металлов в растворенной форме, появлению сероводорода.
Неорганические токсины
Некоторые вещества, например тяжелые металлы, даже после их извлечения из первоначальных соединений сохраняют свою токсичность. Хлориды.Для таяния льда, как правило, используют поваренную соль, которая в… Удобрения. Хорошо растворимые в воде удобрения вымываются обильными дождями, попадая в грунтовые воды и…Соединения тяжелых металлов.
В природных водах атомы тяжелых металлов присутствуют в различных ионных и молекулярных формах. Железо, хром и марганец могут быть представлены… Наиболее важными химическими процессами являются окисление, восстановление,… Гидролитические процессы приводят к образованию моно- и полиядерных гидроксокомплексов. Интенсивность гидролиза…Поведение тяжелых металлов в водной среде.
Выводы: • Химическое загрязнение Мирового океана представляет собой изменение… • Наличие органических веществ часто приводит к расходованию кислорода в воде и к его полному исчезновению.Литосфера
Химический состав литосферы
Литосфера – твердая оболочка Земли, включает земную кору и часть верхней мантии планеты, имеет толщину от 50 до 75 км на континентах и 5-10 км ниже дна океана. Верхние слои литосферы (2–3 км, а по некоторым данным – до 8,5 км) иногда называют литобиосферой. В этой части литосферы существуют или способны существовать живые организмы или жизнеспособные системы, в основном особые виды анаэробных бактерий.
Одно из отличий литосферы от других объектов окружающего нас мира заключается в том, что она является постоянным местом обитания человека, а поэтому в наибольшей степени подвержена антропогенному воздействию (с учетом эксплуатации поверхностного слоя и недр Земли). При этом максимальному загрязнению и разрушению подвергается почва – самый верхний слой литосферы.
Химический состав пород, слагающих литосферу. Литосфера доступна непосредственным исследованиям только в областях суши. Здесь можно изучать строение и состав земной коры, пользуясь теми естественными обнажениями, которые встречаются по берегам рек, морей и особенно по склонам сильно разрушенных гор. Строение и химический состав горных пород, слагающих земную кору, более или менее достоверно нам известен приблизительно до глубины 15—16 км. Что же касается слоев, залегающих глубже, то о строении и составе их мы можем только догадываться. Основаниями для таких догадок служат гравиметрические исследования (т. е. изучение распределения сил тяжести), изучение сейсмических явлений.
Исследования земной коры (до глубины 16 км) показали, что она состоит главным образом из пород магматического происхождения, на долю которых приходится свыше 90%. Наибольшим распространением среди них пользуются граниты, из которых главным образом и сложена верхняя часть земной коры.
На основании анализов различных образцов гранитов (свыше 500) химический состав их рисуется нам в следующем виде:
| Соединение | Доля % | Соединение | Доля % |
| SО2 Аl2О3 Fе2О3 FеО МgО | 70,18 14,47 1,57 1,78 0,88 | СаО Nа2О К2О ТiО2 прочие | 1,99 3,48 4,11 0,39 1,15 |
Совершенно иной химический состав имеют те магматические породы, которые, являясь продуктами современных извержений, поднялись с больших глубин.
| Соединение | Доля % | Соединение | Доля % |
| SО2 Аl2О3 Fе2О3 FеО МgО | 48,8 13,98 3,59 9,78 6,7 | СаО Nа2О К2О ТiО2 прочие | 9,38 2,59 0,69 2,19 2,3 |
Породы первой группы, которые отличаются большим содержанием кремния (Si) и алюминия (Аl), принято сокращенно обозначать символом Sial (от соединения Si+Al) или называть породами сиалическими. Породы второй группы, характеризующиеся большим содержанием магния (Mg), сокращенно обозначают символом Sima (от соединения Si+Mg) или называют симатическими (габбро, диориты, базальты и др.). Кроме химического состава, породы сиалические отличаются от пород симатических меньшим удельным весом (средняя плотность сиалических пород около 2,6, а симатических до 3).
Исходя из всех имеющихся в нашем распоряжении данных, мы можем сказать, что земная кора в верхней своей части состоит преимущественно из пород сиалических, а в более глубоких частях — из пород симатических.
Химический состав почв
Химики, начиная со второй половины XIX в. изучали химический состав земной коры методами весового и объемного химического анализа. Суммируя результаты многочисленных анализов горных пород, Ф.Кларк показал, что в земной коре преобладают восемь химических элементов: кислород, кремний, алюминий, железо, магний, кальций, калий и натрий.
Средние значения относительного содержания химических элементов в земной коре и других глобальных и космических системах известный российский геохимик А. Е. Ферсман предложил называть кларками в честь ученого, который наметил путь к количественной оценке распространения химических элементов. Анализ значений кларков позволяет понять многие закономерности распределения химических элементов на Земле, в Солнечной системе и доступной нашим наблюдениям части Вселенной.
В земной коре присутствуют две группы элементов: элементы первой группы, содержащиеся в относительно большом количестве, образуют самостоятельные химические соединения, а элементы второй группы, с малыми кларками, преимущественно распылены, рассеяны среди химических соединений других элементов. Элементы первой группы мы называем главными, элементы второй — рассеянными.
В составе земной коры, усредненная плотность которой 2,8 г/см3, преобладают легкие элементы. По мере движения к центру планеты увеличивается содержание тяжелых элементов. Это обусловлено процессом формирования нашей планеты: легкие элементы из расплава поднимались на поверхность, образуя литосферу, а также атмосферу и гидросферу. Плотность верхней мантии составляет 5,5 г/см3.
Называют минералами. В самом общем плане минералы — это природные химические соединения или их смеси, представляющие собой результирующие продукты химических реакций и физических процессов, происходивших или происходящих на Земле. К минералам относятся различные соли (силикаты, сульфиды, карбонаты и т.д.), вода, кислород, нефть, уголь, золото, серебро и т.п. Возраст минералов может быть от 4,6 млрд. лет до года и менее (лед в средних широтах). Имея в своем распоряжении достаточно ограниченное количество химических элементов, природа за миллиарды лет создала порядка трех тысяч различных минералов.
Большинство минералов относятся к солям, образующимся из оксидов:
СаО + А12О3 →Са(А1О2)2 — метаалюминат кальция
SiО2 + СаО →СаSiО3 — метасиликат кальция
К минералам биологического происхождения относится жемчуг, формирующийся в мантии тела моллюсков и состоящий в основном из карбоната кальция и… Главными составными частями литосферы являются различного рода химические… Важной составляющей литосферы являются подземные воды, общий объем которых в осадочном чехле оценивается в 61,4-106…Химические процессы в литосфере
В недрах Земли и на ее поверхностях постоянно происходит разрушение горных пород. Разрушающее действие оказывают высокая и низкая температуры… Это могут быть реакции: соединения СаО + СО2→СаСО3;Химические реакции и процессы в почве
Любую почву можно рассматривать как гетерогенную систему, состоящую из трех фаз: твердой (минеральный «скелет», органическая и биологическая… Почва обладает некоторыми свойствами, которых лишены воздушная и водная… Химический состав почвы.Глобальные экологические функции почв
Набор и количественное соотношение химических элементов в почве называют ее элементным составом. Любые почвы содержат все 92 элемента Периодической… Химические элементы представлены в почвах большим набором их химических…Химическое загрязнение почв
1) водную и ветровую эрозию; 2) засоление, подщелачивание, подкисление; 3) заболачивание;Химическое загрязнение почв.
Охрана почв заключается в том, чтобы предотвратить или свести к минимуму все виды разрушения почв и/или почвенного покрова.
Причины химического загрязнения почв:
- атмосферный перенос загрязняющих веществ (тяжелые металлы, кислые дожди, фтор, мышьяк, пестициды);
- сельскохозяйственное загрязнение (удобрения, пестициды);
- наземное загрязнение (отвалы крупнотоннажных производств, отвалы топливно-энергетических комплексов);
Загрязнение нефтью и нефтепродуктами.
Тяжелые металлы. Этот вид загрязняющих веществ начали изучать одним из первых. К тяжелым металлам обычно относят элементы, которые имеют атомную массу более 50. Они поступают в почву преимущественно из атмосферы с выбросами промышленных предприятий, а свинец — с выхлопными газами автомобилей. Описаны случаи, когда большие количества тяжелых металлов попадали в почву с оросительными водами, если выше водозабора в реки сбрасывались сточные воды промышленных предприятий. Наиболее типичные тяжелые металлы — свинец, кадмий, ртуть, цинк, молибден, никель, кобальт, олово, титан, медь, ванадий.
Из атмосферы в почву тяжелые металлы попадают чаще всего в форме оксидов, где постепенно растворяются, переходя в гидроксиды, карбонаты или в форму обменных катионов. Если почва прочно связывает тяжелые металлы обычно в богатых гумусом тяжелосуглинистых и глинистых почвах, это предохраняет от загрязнения грунтовые и питьевые воды, растительную продукцию. Но тогда сама почва постепенно становится все более загрязненной, и в какой-то момент может произойти разрушение органического вещества почвы с выбросом тяжелых металлов в почвенный раствор. В итоге такая почва окажется непригодной для сельскохозяйственного использования. Общее количество свинца, которое может задержать метровый слой почвы на одном гектаре, достигает 500—600 т; такого количества свинца даже при очень сильном загрязнении в обычной обстановке не бывает.
Малогумусные песчаные почвы устойчивы к загрязнению; это значит, что они слабо связывают тяжелые металлы, легко отдают их растениям или пропускают их через себя с фильтрующимися водами. На таких почвах возрастает опасность загрязнения растений и подземных вод. В этом заключается одно из трудноразрешимых противоречий: легко загрязняющиеся почвы предохраняют окружающую среду, но почвы, устойчивые к загрязнению, не обладают защитными свойствами в отношении живых организмов и природных вод.
Если почвы загрязнены тяжелыми металлами и радионуклидами, то очистить их практически невозможно. Пока известен единственный путь: засеять такие почвы быстрорастущими культурами, дающими большую зеленую массу; такие культуры извлекают из почвы токсичные элементы, а затем собранный урожай подлежит уничтожению. Но это довольно длительная и дорогостоящая процедура.
Можно снизить подвижность токсичных соединений и поступление их в растения, если повысить рН почв известкованием или добавлять большие дозы органических веществ, например торфа. Неплохой эффект может дать глубокая вспашка, когда верхний загрязненный слой почвы при вспашке опускают на глубину 50— 70 см, а глубокие слои почвы поднимают на поверхность. Для этого можно воспользоваться специальными многоярусными плугами, но при этом глубокие слои все равно остаются загрязненными. Наконец, на загрязненных тяжелыми металлами (но не радионуклидами) почвах можно выращивать культуры, не используемые в качестве продовольствия или кормов, например цветы.
Кислотные дожди. Выпадение дождей или других атмосферных осадков с высокой кислотностью — обычный результат выброса в атмосферу продуктов сжигания топлива (угля), а также выбросов металлургических и химических заводов. В составе таких выбросов много диоксида серы и/или оксидов азота; при взаимодействии с водяными парами атмосферы они образуют серную и азотную кислоты. Действие кислых дождей на почвы неоднозначное. В северных таежных зонах они увеличивают вредную кислотность почв, способствуют повышению содержания в них растворимых соединений токсичных элементов — свинца, алюминия. При этом усиливается и разложение почвенных минералов. Реальный путь борьбы с подкислением таежных почв — установка на заводских трубах фильтров, перехватывающих оксиды серы и азота. Для борьбы с подкислением почв можно использовать также известкование.
В ряде случаев кислотные дожди могут быть и полезны. В частности, они обогащают почвы азотом и серой, которых на очень больших территориях явно недостаточно для получения высоких урожаев. Если же такие дожди выпадают в районах распространения карбонатных, а тем более щелочных почв, то они снижают щелочность, увеличивая подвижность элементов питания, их доступность растениям. Поэтому полезность или вредность каких-либо выпадений нельзя оценивать по упрощенным однозначным критериям, а необходимо рассматривать конкретно и дифференцированно по типам почв.
Промышленные отвалы. Атмосферные выбросы, содержащие оксиды различных токсичных металлов и неметаллов, распространяются на большие расстояния, измеряемые десятками и сотнями километров, поэтому вызываемые ими загрязнения имеют региональный, а иногда и глобальный характер. В противоположность этому крупнотоннажные отходы различных производств, отвалы гидролизного лигнина, золы тепловых электростанций, отвалы при добыче угля оказывают преимущественно локальное влияние. Такие отвалы занимают немалые площади, выводя из пользования земельные угодья, а многие из них представляют вполне конкретную опасность для окружающей среды. Отвалы угольных шахт содержат немало угля, который горит, загрязняя атмосферу. Отвалы многих горных пород содержат пирит FеS2, самопроизвольно окисляющийся на воздухе до Н2SО4; в период дождей или снеготаяния последняя легко образует не только сильнокислые территории, но и даже озерца серной кислоты в окрестностях горных выработок. Единственный путь нормализации экологической обстановки в таких местах — выравнивание отвалов, их землевание, залужение, лесные посадки.
Многие местные органические отходы, такие, как гидролизный лигнин, птичий помет, свиной навоз, можно превратить или в хорошие компосты, или в так называемый биогумус (вермикомпост). В основе последнего способа лежит быстрая переработка органических отходов некоторыми гибридами красных земляных червей, так называемая вермикультура (от лат. верми — червь). Черви пропускают через кишечник все растительные остатки, превращая их в черноземоподобную массу, очень плодородную, практически без запаха, в которой содержится много гуминовых кислот.
Нефть и нефтепродукты. Нефтяное загрязнение почв относится к числу наиболее опасных, поскольку оно принципиально изменяет свойства почв, а очистка от нефти очень сильно затруднена. Нефть попадает в почву при заданных обстоятельствах: при разведке и добыче нефти, авариях на нефтепроводах, при авариях речных и морских нефтеналивных судов. Различные углеводороды попадают в почву на нефтебазах, бензозаправках и т.п. Последствия для почв, вызванные нефтезагрязнением, можно без преувеличения назвать чрезвычайными. Нефть обволакивает почвенные частицы, почва не смачивается водой, гибнет микрофлора, растения не получают должного питания. Наконец, частицы почвы слипаются, а сама нефть постепенно переходит в иное состояние: ее фракции становятся более окисленными, затвердевают, и при высоких уровнях загрязнения почва напоминает асфальтоподобную массу. Бороться с таким явлением очень трудно. При малых уровнях загрязнения помогает внесение удобрений, стимулирующих развитие микрофлоры и растений. В результате нефть частично минерализуется, некоторые ее фрагменты входят в состав гуминовых веществ, и почва восстанавливается. При больших дозах и длительных сроках загрязнения в почве происходят необратимые изменения, тогда наиболее загрязненные слои приходится просто удалять.
Изменения почвы в зависимости от способов ее обработки
Химические изменения почвы могут происходить не только в результате ненадлежащего ухода за ней, но и при использовании различных способов ее обработки. Так, например, при ведении интенсивного хозяйства изменяется поступление воздуха в почву. В тех случаях, когда почва чрезмерно уплотнена, ежегодное перепахивание приводит к ее разрыхлению. В результате происходит интенсивное перемешивание почвы и обогащение ее воздухом. При этом отсутствуют участки с неравномерным распределением кислорода, как в неразработанном гумусном слое. Перемешивание и обогащение воздухом позволяют весь гумус вовлечь в процесс превращений.
Роль монокультур. Растения, которые выращиваются в виде монокультур, изменяют минеральный состав почв, так как потребляют одни и те же вещества почвы. В этих случаях необходимо пополнение этих веществ с помощью удобрений. В результате часто происходит загрязнение грунтовых вод, так как минеральные вещества вымываются из почвы раньше, чем успевают усваиваться растениями. Например, сахарная свекла уносит из почвы необычайно большие количества азота (300 кг/га), калия (400 кг/га) и магния (45 кг/га). Все чаще выращиваемая благодаря высокой урожайности кукуруза потребляет из почвы большие количества фосфатов (70 кг/га в пересчете на фосфор); кукуруза отрицательно влияет на почву также из-за слишком большой высоты растений и загущенное™ посадок (на 1 м2 приходится 8—10 растений). Скорость роста кукурузы сначала невелика, и за это время процессы эрозии почвы успевают пройти более интенсивно, чем при засевании другими растениями.
Влияние хвойных пород. Иной тип воздействия на почву проявляется при выращивании хвойных деревьев. Слой подстилки под этими деревьями распадается не полностью, так как продукты первичного разложения пагубно действуют на гумифицирующие микроорганизмы или тормозят их деятельность, что и приводит к неполному разложению остатков. Подстилка из иголок хвои стерильна (под ней даже трава не растет); разложение идет медленнее и по другому пути: образуются фульвокислоты — растворимые в щелочах, но не разлагаемые кислотами органические вещества почвы, имеющие большое число карбоксильных групп. Например, они на 30 % могут состоять из частично разрушенных углеводов, которые связывают в комплексы ионы металлов и растворяют оксиды железа. Такой гумус носит название сырого. В его создании особую роль играют клещи и грибы.
Избыток кислых компонентов и способность связывать ионы металлов приводят к тому, что при отложениях такого гумуса почва с течением времени отбеливается, так как растворы сырого гумуса уносят комплексно связанные металлы, и образуется подзолистая почва. Таким образом, возникают бедные питательными веществами кислые почвы, которые либо совсем не могут быть использованы для культур, особо требовательных к качеству почвы, либо используются ограниченно. Хвойные монокультуры, которые выращивались в первой половине XX в. в Центральной Европе в целях возможно более быстрого получения стройматериалов, превратили некогда плодородные земли в земли пониженного качества. Процессы образования подзолов относятся к антропогенному закислению почв.
Уплотнение почвы. Обработка земли тяжелыми машинами, уличный транспорт и строительство приводят к уплотнению больших участков окультуренных земель. В результате забиваются поры в почве, уменьшаются ее влагоемкость и снабжение кислородом. В уплотненной почве происходят процессы восстановления, особенно если остатки кислорода вытесняются при увлажнении или под действием других газов почвы.
Марганецобычно встречается в почве в виде пиролюзита МnО2. При восстановлении он переходит в растворимый в воде ион Мn2+, т. е. в усвояемую растениями форму. Марганец принадлежит к числу накапливающихся в почве элементов. Ион Мn2+ встречается в воде только в малых концентрациях. В высоких концентрациях он токсичен. Органические комплексы марганца также неустойчивы и легко отдают Мn2+.
Сходная ситуация и с соединениями железа. При обычных значениях рН почвы железо накапливается в виде Fе(ОН)3. При малом содержании кислорода понижается окислительно-восстановительный потенциал почвы, что способствует восстановлению Fе(III) в Fе(II). Таким образом, железо переходит в форму, усвояемую растениями. Поскольку при анаэробных условиях возможность усвоения железа слишком сильно возрастает, то увеличивается и его токсичность (явление, особенно характерное для заболоченных рисовых чеков).
Железо, марганец и ряд других металлов после восстановления обладают повышенной подвижностью в почве, поэтому в восстановительных условиях эти элементы легче вымываются из почвы, которая в результате обедняется этими металлами.
При анаэробных условиях помимо денитрификации может происходить микробиологическое восстановление серы до сульфидной формы. Сера, первоначально находившаяся в почве в виде сульфата, в процессе восстановления может оставаться в почве, образуя с тяжелыми металлами плохо растворимые сульфиды и надолго закрепляясь на одном месте.
Приведенные примеры показывают, что восстановительные процессы в значительной степени могут отразиться на плодородии почвы.
Пестициды.
Обычно пестициды подразделяют следующим образом: инсектициды — химические средства для борьбы с вредными насекомыми; фунгициды — химические вещества для борьбы с грибковыми заболеваниями растений;Таблица Классификация отходов по гигиеническому принципу
| Категория | Характеристика отходов по виду загрязнения | Рекомендуемые меры по ликвидации или утилизации |
| I | Инертные | Использование для планировочных ночных работ |
| II | Легкоразлагающиеся органические | Складирование или переработка |
| III | Слаботоксичные, слаборастворимые в воде | Складирование |
| IV | Нефтемаслоподобные | Сжигание |
| V | Токсичные, со слабым загрязнением воздуха | Складирование на полигоне промышленных и бытовых отходов |
| VI | Токсичные | Групповое или индивидуальное обезвреживание на специальных сооружениях |
Твердые отходы, возникающие непосредственно при производственной деятельности человека, всегда можно рассматривать как потенциальное вторичное сырье, поэтому на первом этапе их принято делить на отходы производства и отходы потребления.
Отходами производства следует считать остатки сырья, материалов и полуфабрикатов, образовавшиеся при изготовлении продукции и полностью или частично утратившие свои потребительские свойства, а также продукты физико-химической переработки сырья, получение которых не являлось целью производственного процесса и которые в дальнейшем могут быть использованы как готовая продукция после соответствующей обработки или как сырье для переработки.
Отходами потребления считаются различного рода изделия, комплектующие детали и материалы, которые по тем или иным причинам непригодны для дальнейшего использования. Эти отходы можно разделить на промышленные и бытовые. К промышленным относятся, например, металлолом, вышедшее из строя оборудование, изделия технического назначения из резины, пластмасс, стекла и др. Бытовыми являются пищевые отходы, изношенные изделия бытового назначения (одежда, обувь и пр.), использованные изделия различного рода (упаковки, стеклянная и прочие виды тары) и др.
Все виды твердых отходов производства и потребления по возможности использования можно разделить, с одной стороны, на вторичные материальные ресурсы, которые уже перерабатываются или переработка которых планируется, и, с другой — на отходы, которые на данном этапе развития экономики перерабатывать нецелесообразно и которые неизбежно образуют безвозвратные потери. Дальнейшую классификацию твердых отходов производят исходя из их влияния на окружающую среду и прежде всего по медицинскому аспекту, который включает санитарно-гигиенические и экологические нормативы.
С помощью санитарно-гигиенических нормативов определяются показатели окружающей среды для здоровья человека. В эту группу входят ПДК вредных веществ в составе твердых отходов, допустимые уровни биологического и радиационного воздействия.
Экологические нормативы устанавливают требования к источнику вредного воздействия, ограничивая его деятельность. К ним относятся предельно допустимые количества накопления твердых отходов на территории предприятия, а также технологические правила, содержащие экологические требования.
Методы и способы утилизации и ликвидации отходов
Основными направлениями оперирования промышленными твердыми отходами являются: - захоронения на полигонах и свалках; переработка конкретных твердых отходов по заводской технологии;Биосфера – особая оболочка планеты
Биосфера – особая оболочка планеты, объемлющая все формы активной жизни. В более развернутом плане под биосферой понимается нижняя часть атмосферы, гидросфера и верхняя часть литосферы, включающие совокупность всех живых организмов. Исторически сложившаяся многоуровневая, саморегулирующаяся система.
Биосфера - «область жизни», пространство на поверхности земного шара, в котором распространены живые существа. Целостное учение о биосфере было создано в начале 20 века академиком В. И. Вернадским,согласно которому биосфера представляет собой одну из геологических оболочек земного шара, глобальную систему земли, в которой геохимические и энергетические превращения определяются суммарной активностью всех живых организмов – живого вещества.
Биосфера имеет определенные границы и охватывает относительно небольшой слой поверхностных оболочек нашей планеты. Каждая из геологических оболочек имеет свои специфические свойства, которые определяют не только набор форм живых организмов, обитающих в данной части биосферы, но и их основные морфофизиологические особенности. При этом атмосфера, гидросфера и литосфера предстают не только как емкости, заполненные жизнью, но как основные среды жизни, активно формирующие ее состав и биологические свойства.
Биосферу, как местообитание организмов, можно разделить на три подсферы:
-геобиосфера (верхняя часть литосферы, населенная геобионтами);
-гидробиосфера(океаны, моря и континентальные пресные воды, населенные гидробионтами);
-аэробиосфера(нижняя часть атмосферы, населенная тропобионтами, до 22-24км, где располагается озоновый слой).
Биосфера как целое образует единую экологическую систему Земли, в которой сконцентрировано живое вещество планеты – биота.
Биота – совокупность взаимосвязанных и независимых биологических видов, объединенных общей областью распространения; исторически сложившийся комплекс живых организмов. Различают биоту Земли, государства, гидросферы и т.д.
Некоторые особенности биосферы
2. Биосфера Земли – большая (глобальная) открытая система, у которой на входе – поток солнечного излучения, а на выходе – минералы (вещества),… 3. Биосферу Земли можно рассматривать как кибернетическую систему, обладающую… 4. Огромное внутренне разнообразие биосферы определяет её устойчивость, обеспечивающую блокирование (нейтрализацию)…Процессы в биосфере
– окислительно-восстановительную (окисляет, например, углеводы до углекислого газа и восстанавливает его до углеводов); – концентрационную (организмы-концентраторы накапливают в своих телах и…Основные функции живого вещества в биосфере
Движущей силой биологического (биогеохимического или малого) круговорота веществ является деятельность живых организмов, а главным источником… Движущей силой антропогенного круговорота веществ является хозяйственная… За время существования биосферы свободный кислород атмосферы обновлялся не менее миллиона раз, а воды Мирового океана…Химические процессы в биосфере
– участие в химических и биохимических реакциях большого числа органических и неорганических веществ; – протекание химических реакций смешанного типа, часто без непосредственного… – неравновесность процессов;Примеры химических и фотохимических процессов в биосфере
Фотосинтез:
6CO2 + 6H2O 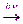 C6H12O6 + 6O2
C6H12O6 + 6O2
Дыхание:
C6H12O6 + 6O2 → 6CO2 + 6H2O
Превращение солей в организме человека на примере PbCO3:
PbCO3 + 2HCl = PbCl2 + H2CO3
(с кислотой желудочного сока)
PbCO3 + 2NaOH = [Pb(OH)]2CO3 + Na2CO3
(в щелочной среде кишечника)
PbCO3 + H2S = PbS + H2CO3 (в толстой кишке)
Образование «зубного камня»:
3Ca2+ + 2PO43- = Ca3(PO4)2
Химические основы экологического анализа
Речь идет о неком глобальном химико-аналитическом исследовании с помощью различных методов аналитической химии — науки о методах анализа. Это дает…Меры токсичности веществ
К сложностям определения характеристик токсичности веществ относится то, что у… Специфика токсина не только в том, на какую жизненно важную систему организма направлено его действие. Различные…Экологическое нормирование
Регулирование качества природной среды основано на определении экологически допустимого воздействия на нее, когда самоочищение природы еще способно… ПДК достаточно малы. Они установлены для различных объектов — воды (питьевая… Перечень и количество выбрасываемых в окружающую среду загрязняющих веществ чрезвычайно велики, по некоторым оценкам,…Аналитическая химия в экологических исследованиях
Примером является аналитическая химия природных и сточных вод. Существует совокупность сложных процессов между находящимися в воде ионами и…Особо опасные экотоксиканты
Токсичные металлы
Ртуть (Hg)— высокотоксичный, кумулятивный (т. е. способный накапли-ваться в организме) яд. Поражает кроветворную, ферментативную, нервную системы и… Как же попадает к нам ртуть? Самыми разными путями. К примеру, при… Свинец(Pb)является одним из весьма распространенных в окружающей среде токсичных элементов, в связи с чем действие его…Вредные вещества в пищевых продуктах. Нитраты
При длительном поступлении нитратов в организм человека (пусть даже в незначительных дозах) уменьшается количество йода, что приводит к увеличению… Установлено, что нитраты связаны с возникновением опухолей в… По способности накапливать нитраты овощи, плоды и фрукты делятся на группы:Пестициды
Будучи малополярными органическими веществами, хлорорганические пестициды обладают кумулятивным токсическим эффектом — накапливаются в жировых… В пресноводных водоемах хлорсодержащие пестициды быстро накапливаются в… Увеличение размаха изменчивости привело к росту числа устойчивых (резистентных) к действию хлорорганических…Диоксины
Особую опасность представляют содержащиеся в летучей золе полихлорированные дибензо-n-диоксины (ПХДД) и дибензофураны (ПХДФ). Диоксины и близкие им по структуре хлорорганические соединения обладают… Множественность клеточных мишеней для диоксинов и подобных веществ в различных биологических средах определяет…Выводы
• Многочисленными исследованиями доказано, что степень загрязненности тяжелыми металлами и токсичными элементами растений (зерна, овощей, плодов, кормов для всех видов животных) связано с содержанием их в окружающей среде. Источником токсичных ионов металлов могут быть воздух, почва, вода и пища. Отравление может произойти через дыхательные пути, кожные покровы и пищевой тракт. Основной мерой предупреждения отравления токсичными металлами является предупреждение экологических катастроф и рациональное использование минеральных ресурсов этих металлов и их соединений. Для предотвращения отравления законодательно введен контроль за содержанием вредных примесей (предельно допустимая концентрация — ПДК) токсичных металлов. Контролируются восемь наиболее опасных токсичных примесей: ртуть, свинец, олово, кадмий, медь, цинк, железо, мышьяк.
• Нитраты — вредные соединения, обладающие токсичностью для чело-века. Особой токсичностью обладает их восстановленная форма — нитриты, которые при попадании в организм взаимодействуют с гемоглобином крови.
Биотрансформация экотоксикантов
Неорганические экотоксиканты. Многие организмы имеют естественные механизмы метаболизма и удаления тяжелых металлов, чаще всего в форме… Процессы биометилирования наиболее интенсивно осуществляются микроорганизмами… Вследствие довольно высокой химической устойчивости и липофильности органические формы ртути и некоторых других…– Конец работы –
Используемые теги: дисциплина, химические, основы, экологии0.081
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Дисциплина Химические основы экологии
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов