Твердые отходы металлургии и теплоэнергетического комплекса, их утилизация.
Металлургия.
В результате взаимодействия золы топлива, компонентов пустой породы и флюсов образуются металлургические шлаки. В зависимости от состава различают основные, в которых преобладают оксиды кальция и магния; кислые, отличающиеся повышенным содержанием оксидов кремния и алюминия, и нейтральные – доменные шлаки. Шлаки содержат богатый спектр химических соединений, поэтому являются ценным сырьем для получения строительных материалов и изделий, являющихся более качественными и дешевыми, чем получаемые из природного сырья.
Основным способом переработки шлаков в настоящее время является их грануляция.
Сталеплавильные шлаки содержат железо, MnO, различные оксиды и сульфиды. Около половины перерабатываемой массы этих шлаков идет на изготовление щебня, около трети используется в качестве оборотного продукта, примерно пятая часть перерабатывается в удобрения для сельского хозяйства. При переработке этих шлаков с помощью электромагнитных сепараторов из них извлекается металл.
Согласно химическому составу шлаки цветной металлургии могут быть условно объединены в три группы:
- шлаки никелевых заводов и часть шлаков медных заводов, отличающихся малым содержанием цветных металлов и железа.
- медные шлаки, отличающиеся значительным содержанием железа, малым содержанием меди и наличием ≤5% Zn и Pb.
- оловянные, свинцовые и часть медных шлаков, отличающихся значительным содержанием Zn, Pb и Sn.
Технологическая схема переработки шлаков выбирается в зависимости от их состава и физико-химических свойств и может включать как гидрометаллургические, так и пирометаллургические способы извлечения металлов. При пирометаллургическом способе осуществляют восстановление металлов из их безводных соединений в условиях высоких температур. Гидрометаллургический метод связан с восстановлением металлов из водных растворов их соединений различными методами.
Энергетические установки.
Основными компонентами, выбрасываемыми в атмосферу при сжигании различных видов топлива в энергоустановках, являются CO2 и H2O, продукты неполного сгорания топлива – оксид углерода, сажа, углеводороды, несгоревшие частицы твердого топлива, зола, шлаки и прочие механические примеси. По объему образования и составу твердые отходы сжигания топлив-золы и шлаки – близки к металлургическим шлакам. На 80-90% химический состав золошлаковых отходов представлен оксидами Si, Al, Fe, Ca и Mg, помимо этого в них присутствуют соединения Ti, V, Ge, Ga, S, а также несгоревшие частицы топлив. Золы сланцев и торфа содержат значительные количества CaO и используются для известкования кислых почв вследствие содержания значительных количеств К и Р, а также микроэлементов, необходимых ряду с/х культур, они применяются практически без какой-либо дополнительной обработки в качестве удобрений. Некоторые виды золошлаковых отходов используют в качестве агентов очистки промстоков.
Золы углей и нефтей содержат многие металлы. Максимальные концентрации Sr, V, Zn, Ge в золе углей могут достигать 10 кг/т. В золе нефтей содержание V2O5 в отдельных случаях достигает по массе 65%. Зола торфа содержит значительные количества U, Co, Cu, Ni, Zn, V, Pb.
Экологическое совершенствование теплоэнергетики идет по различным взаимодополняющим направлениям.
– улавливание, обезвреживание и целевая переработка газообразных выбросов, использование твердых отходов в других производствах и минимизация водопотребления.
– "улучшение" топлива путем предварительного удаления из него вредных примесей или переработки твердого горючего на жидкие продукты.
– использование принципиально отличных от реакции горения источников энергии.
24. озоновый слой.+ См. вопрос 21.
В атмосфере на высоте около 40 км (стратосфера) расположен озоновый защитный слой Земли, определяющий верхний предел жизни в биосфере.
Озон обладает очень сильным поглощением. Озоновый слой полностью поглощает всю энергию ультрафиолетовой радиации – губительную для всего живого. Также озон поглощает инфракрасное излучение Земли, препятствуя ее охлаждению.
Влияние солнечного света проявляется и в механизме образования озоновых дыр.
В течение холодной антарктической зимы, когда температура нижней атмосферы падает до -80°С, холодных воздух падает вниз. В результате на высоте 10-20 км образуется полярный вихрь, который изолирует воздух внутри своего объема от остального пространства. В этом воздухе образуются стратосферные полярные облака, соединения молекул H2O и HNO3. На поверхности частиц облаков протекают реакции, достаточно устойчивых соединений хлора. Процессы идут в течении всей зимы. В результате чего к е концу в полярном вихре накапливается достаточное количество этих компонентов. С восходом солнца в начале весны они легко распадаются и образуются активные частицы, которые начинают разрушать озоновый слой цепным путем. Т.к. вихрь еще существует, то обмена с соседними, богатыми озоном областями стратосферы нет, содержание озона быстро падает. Далее происходит разогрев воздуха, распад вихря и расползание остатков дыры по южному полушарию
Основными загрязнителями атмосферы на сегодняшний день являются окись углерода и сернистый газ. Но, конечно, нельзя забывать и о фреонах, или хлорфторуглеводородах. Именно их большинство ученых считают причиной образования так называемых озоновых дыр в атмосфере. Фреоны широко используются в производстве и в быту в качестве хладореагентов, пенообразователей, растворителей, а также в аэрозольных упаковках. А именно с понижением содержания озона в верхних слоях атмосферы медики связывают рост количества раковых заболеваний кожи.
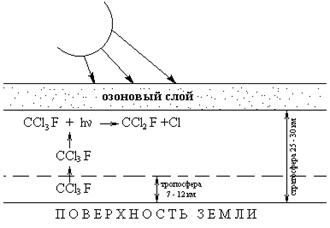 |
Известно, что атмосферный озон образуется в результате сложных фотохимических реакций под воздействием ультрафиолетовых излучений Солнца. Хотя его содержание невелико, его значение для биосферы огромно. Озон, поглощая ультрафиолетовое излучение, предохраняет все живое на земле от гибели. Фреоны же, попадая в атмосферу, под действием солнечного излучения распадаются на ряд соединений, из которых окись хлора наиболее интенсивно разрушает озон.
ФРЕОНОВАЯ ГИПОТЕЗА
Фреоны - это галогенсодержащие органические соединения (CFCl3, CF2Cl2, CF3Cl, CF4, CF3CF3, CF2Cl CF2Cl).
Cl* + O3 ® ClO* + O2
ClO* + O3 ® Cl* + 2O2
Одна молекула фреона способна разрушить 10 000 молекул О3.