Прилади та обладнання
Балон, рідинний манометр, мікрокомпресор.
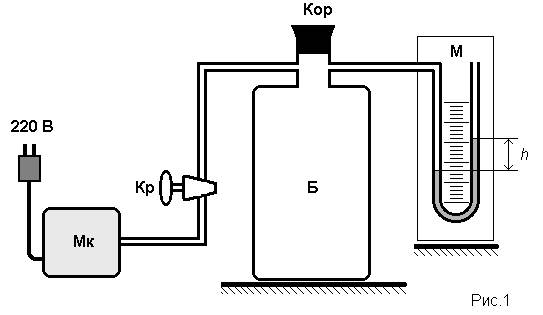
Опис вимірювального пристрою та виведення розрахункової формули
|
· скляного балона Б,закритого коркомК;
· рідинного манометра М, під’єднаного до балона Б;
· мікрокомпресора Мк, який сполучається з балоном краном Кр.
Досліджуваним газом є повітря.
На початку досліду газ знаходиться у балоні при атмосферному тиску po і кімнатній температурі Т1, а під час експерименту послідовно проходить через 3 стани (рис.2):
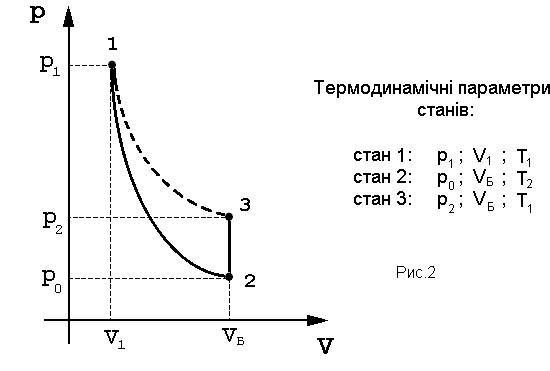
Стан 1.Система перейде у стан 1, якщо при закритому корку Кі
відкритому крані Кр у балон мікрокомпресором нагнітати
повітря до тиску
p1=po + ρgh1. (1)
Надлишковий над атмосферним тиск ρgh1 визначають у
міліметрах водяного стовпа (h1 –виміряна в мм різниця
рівнів води у колінах манометра).
Стан 2.Якщо повністю відкрити корок К, повітря з балону буде
швидко розширюватися в атмосферу до вирівнювання тиску
у балоні з атмосферним. Цей процес можна приблизно вважа-
ти адіабатним, він супроводжується охолодженням повітря
до температури Т2< Т1. Газ, що залишився у балоні займав до
розширення деяку частину об’єму балона V1 < VБ,після
розширення його об’єм дорівнює VБ.
Перехід газу із стану 1 в стан 2 ілюструє крива 1–2 (адіабата).
Стан 3.Якщо закрити балон, газ у ньому внаслідок теплообміну буде
ізохорно нагріватися до кімнатної температури Т1, при цьому
тиск зросте до значення
p2=po + ρgh2 . (2)
Перехід газу із стану 2 в стан 3 ілюструє крива 2–3 (ізохора).
Зауважимо, що стани 1 і 3 відповідають одній температурі Т, отже і одній ізотермі (крива 1–3), тому згідно з законом Бойля-Маріотта:
p1V1=p2VБ. (3)
Адіабатне розширеня 1–2 опишемо рівнянням Пуассона:
 . (4)
. (4)
Поділимо рівняння (3) у степені γна рівняння (4)
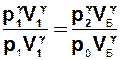 , (5)
, (5)
звідки випливає:
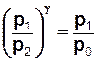 . (6)
. (6)
Пролоґарифмувавши (6), знайдемо γ
γ .(7)
.(7)
Перетворимо знаменник (7), додавши і віднявши lnp0, а також підставимо значення p1 і p2 з формул (1), (2):
γ  . (8)
. (8)
Атмосферний тиск po >> ρgh1;  gh2, отже
gh2, отже 
 << 1;
<< 1;
 << 1,
<< 1,
тому, використовуючи наближення ln(1+x) » x,з (8) будемо мати:
γ  , або γ
, або γ  . (9)
. (9)
Отже, для знаходження γтреба експериментально визначити h1 та h2.
При підготовці до виконання роботи використати: