Способы выражения составов фаз
При изучении массообменных процессов приходится иметь дело со смесью различных компонентов, находящихся в жидкой или паровой фазе. Свойства такой смеси зависит от её состава, т.е. относительного содержания (концентрации) тех или иных компонентов.
Принято для выражения состава смесей пользоваться различной системой концентраций и наиболее распространёнными являются массовые, молярные и объёмные концентрации.
а) массовые концентрации (обозначим хi)
Рассмотрим систему, состоящую из n компонентов. Обозначим массы 1-го, 2-го и n-го компонентов через g1, g2,……gn соответственно. Общая масса системы будет  ; тогда массовые концентрации компонентов, входящих в состав смеси определяются следующим образом:
; тогда массовые концентрации компонентов, входящих в состав смеси определяются следующим образом:
х1 = 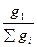 ; х2 =
; х2 = 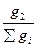 ;……….; хn =
;……….; хn =  .
.
Очевидно, что сумма массовых концентраций всех компонентов смеси равна единице:
x1 + x2 +……+ xn = 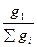 +
+ 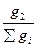 + ……+
+ ……+  =
=  .
.
б) молярные концентрации (мольные доли) (обозначим х’) – это отношение числа молей i – го компонента к общему числу молей системы
х1’ = 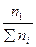 ; х2’ =
; х2’ = 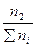 ;……….; хn’ =
;……….; хn’ =  .
.
Очевидно, что и сумма мольных долей системы равна 1
x1’ + x2’ +……+ xn’ =
в) объёмные концентрации (обозначим vi) – это отношение объёма отдельного компонента Vi к общему объёму системы 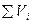
v1 = 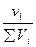 ; v2 =
; v2 =  ; ……; vn =
; ……; vn = 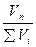 .
.
При условии, что в процессе смешения компонентов их объём не изменяется , т.е.
V1 + V2 + ….. + Vn = ∑Vi,
Сумма объёмных концентраций также будет равна 1
v1 + v2 + …..+ vn = 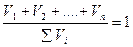
∑vi = 1.