Дослiд 5.5. Окиснення ненасичених вуглеводнів
Ациклічні вуглеводні окиснюються повітрям у рідкій фазі (140-150°С) в присутності солей кобальту або мангану. При окисненні циклогексану утворюються циклогексан й циклогексанон.
Етиленові вуглеводні дуже чутливі до дії окисників. Будова продуктів окиснення визначається природою окисника. При дії кисню на етиленові вуглеводні в рідкій фазі подвійний зв'язок не використовується. Окисненню підлягає група, що знаходиться в α-положенні до подвійного зв'язку, при цьому утворюється гідроксид:
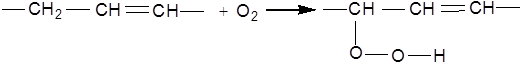
Каталітичне окиснення ненасичених вуглеводнів застосовується для отримання α-оксидів. Окиснення етилену киснем повітря над дрібнороздробленим сріблом при 270-290°С призводить до утворення оксиду етилену:
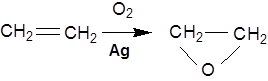
При дії марганцевокислого калію в нейтральному або лужному розведеному водному розчині на етиленові вуглеводні утворюється α-гліколі:

При цьому спостерігається знебарвлення лужного розчину перманганату й осадження MnO2. Дана реакція використовується як якісна на подвійний зв'язок.
Реакція Вагнера йде через стадію утворення циклічного ефіру. Механізм утворення гліколю можна подати такою схемою:
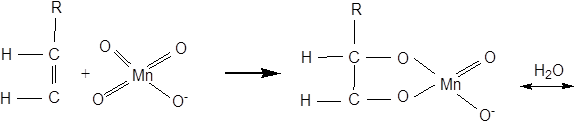
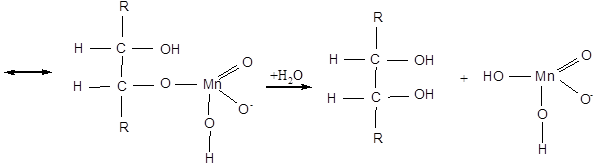
При більш енергійному окисненні (KMnO4 в кислому розчині, HNO3, хромова суміш) відбувається розрив за подвійним зв'язком та в залежності від будови ненасичені сполуки утворюються кислоти або кетони й кислота:
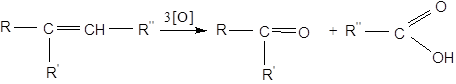
Цей метод дає можливість отримувати гліколі, кетони й кислоти з ненасичених вуглеводнів, а також встановлювати їхню будову. Для окиснювального розщеплення етиленових вуглеводнів використовується реакція озонування. Реакція озонування використовується для встановлення будови сполуки з подвійним зв'язком.
| Реактиви та матеріали: | рідкі алкени, перманганат калію KMnO4, 0,1Н розчин, карбонат натрію Na2CO3, 1Н розчин. |
У пробірку вводять 1 краплю рідкого алкену, 1 краплю розчину вуглекислого натрію й додають при енергійному струшуванні 2-3 краплі розчину перманганату калію. Фіолетовий колір зникає, й з'являється коричневе забарвлення від утвореного діоксиду марганцю:
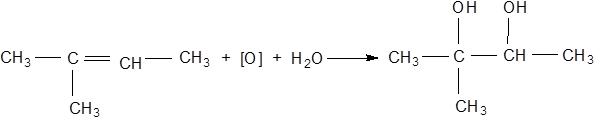
2-метил-2,3-бутандіол
Реакція окиснення алкенів перманганатом калію в нейтральному або лужному водних розчинах є аналітичною реакцією на подвійний зв'язок. У більш жорстких умовах – у кислому середовищі при нагріванні – відбувається розщеплення молекули за подвійним зв'язком. За продуктами окиснення встановлюють структуру алкену й положення подвійного зв'язку.