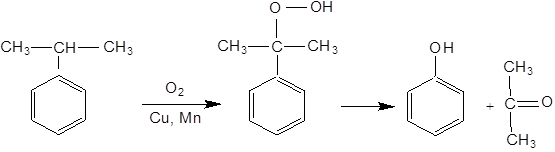Окиснення аренів
Незаміщені ароматичні вуглеводні дуже стійкі щодо різних окисників (перманганат калію, триоксид хрому, нітратна кислота), але кисень повітря в присутності V2O5 окиснює бензол в малеїновий ангідрид з гарним виходом:

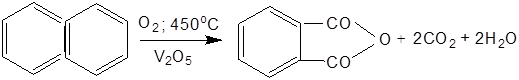
а нафталін – у фталевий ангідрид:
Гомологи бензолу при дії окисників (KMnO4, HNO3, CrO3) перетворюються в ароматичні кислоти. Боковий ланцюг у гомологів бензолу легко окиснюється при кип'ятінні з розведеною HNO3 (1 об'єм концентрованої HNO3 густиною 1,4 г/см3 на 2-3 об'єми води). При наявності декількох бокових ланцюгів нітратна кислота більшою частиною окиснює тільки одну алкільну групу, наприклад з о-ксилолу отримують о-толуїлову кислоту:

Легкість окиснення залежить від їх взаємного розташування, так, наприклад, п-ізомер окиснюється легше м-ізомеру.
Окиснення бокового ланцюга залежить також від характеру замісників у ядрі. Так, п-нітротолуол легше окиснюється в п-нітробензойну кислоту, ніж толуол в бензойну кислоту.
Найбільше практичне значення має каталітичне окиснення ароматичних вуглеводнів з боковим ланцюгом. При пропусканні парів толуолу й інших гомологів бензолу в суміші з киснем над V2O5 при 400-500°C утворюються відповідні альдегіди:
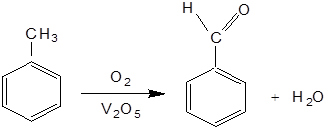
Якщо реакцію окиснення проводити в присутності лугів при 210°С й підвищенні тиску, толуол й етилбензол окиснюються в бензойну кислоту.
Для отримання фенолу використовується рідиннофазове окиснення кумолу киснем повітря в присутності мідних або марганцевих каталізаторів. Гідропероксид кумолу, що утворився, розкладають сульфатною кислотою на фенол й ацетон: