Дослiд 16.5. Утворення солей анiлiну та їхній розклад
| Реактиви та матеріали: | анiлiн; соляна кислота (d=1,19 г/см3); вода; їдкий натр, 2Н розчин; 1%-ний спиртовий розчин фенолфталеїну; червоний лакмусовий папiрець |
| Обладнання: | мікроскоп пробiрки, скляна паличка, предметне скло |
1. У пробірку вміщують 1 краплю аніліну, 8 крапель води та збовтують вміст пробірки. Одну краплю емульсії наносять на лакмусовий папірець. Колір червоного лакмусу не змінюється.
2. Приготовлену емульсію аніліну ділять на дві частини. До однієї частини додають краплями розчин сульфатної кислоти. Утворюється осад сульфатнокислого аніліну. Нагрівають пробірку до розчинення осаду та повільно охолоджують. Голчасті кристали, які випали, переносять на предметне скло і роздивляються їхню форму в мікроскопі.
Хімізм процесу:
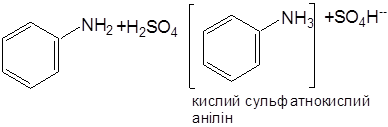
3.У пробiрку наливають 5 мл анiлiну i приблизно такий же об'єм соляної кислоти. Реакцiя проходить з видiленням тепла. Охолоджують пробiрку в холоднiй водi. Видiляються кристали солi - солянокислий анiлiн.
Хiмiзм процесу:
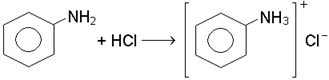
солянокислий анілін
До прозорого розчину солянокислого анiлiну додають 1-2 краплi фенолфталеїну i краплями - розчин лугу. Рiдина каламутнiє ще до появи малинового забарвлення:

Основнi властивостi амiногрупи, з'єднаної з ароматичним ядром, значно ослабленi порiвняно з амiнами жирного ряду. Водний розчин анiлiну при дiї на лакмус не дає синього кольору. Анiлiн утворює солi тiльки з сильними мiнеральними кислотами. Воднi розчини цих солей мають кислу реакцiю.