Масса и размеры молекул
Для характеристики масс атомов и молекул применяются следующие величины:
Атомная масса – масса атома вещества, выраженная в а.е.м.
Молекулярная масса – масса молекулы вещества, выраженная в а.е.м.
Атомная единица массы (а.е.м.) – единица массы, равная 1/12 массы атома изотопа углерода С12.
Количество вещества, в котором содержится число частиц (атомов или молекул), равное числу атомов в 0,012 кг изотопа углерода С12, называется молем
Масса 1 моля вещества называется молярной массой М.
Число частиц, содержащихся в 1 моле вещества, называется числом Авогадро:
NA = 6,023 × 1023 моль-1
Зная молярную массу М и число Авогадро NA, можно найти массу 1 молекулы:
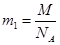 .
.
Так в случае углерода С12:
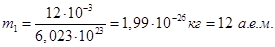 ,
,
откуда следует значение 1 а.е.м.
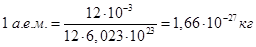 .
.
Теперь произведем оценку размеров молекул. Естественно предположить, что в жидкости молекулы располагаются довольно близко друг к другу. Поэтому приближенную оценку объема одной молекулы можно получить, разделив объем киломоля какой либо жидкости, например, воды, на число молекул в киломоле. Киломоль (т.е. 18 кг) воды занимает объем 18×10-3 м3. Следовательно, на долю одной молекулы приходится объем, равный
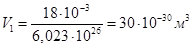 .
.
Отсюда следует, что линейные размеры молекул воды приблизительно равны 3×10-10 м.
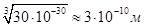 .
.
Молекулы других веществ также имеют размеры такого же порядка.