Построение диаграмм состояния сплавов. Критические точки. Изотермы свободной энергии.
Строение сплава определяет его свойства, поэтому важно знать, как будет изменяться строение при изменении t и состава сплава. Зависимость между структурой сплава, его температурой, составом описывается с помощью диаграмм состояния. Другими словами диаграмма состояния представляет собой графическое изображение состава сплава. Диаграмма состояния показывает устойчивое состояние, т.е состояние, которое при данных условиях имеет минимум свободной энергии, поэтому диаграмма состояния – диаграмма равновесия. По диаграмме состояния можно определить для конкретного сплава температуры кристаллизации и превращение в твердое состояние при заданной температуре, что позволяет примерно определить механические, физические и другие свойства сплавов и правильно назначить режимы ТО, ОМД, сварки. Диаграмма состояния строится по критическим точкам, получаемых на кривых охлаждения сплавов данной системе. Критические точки при этом стараются получить при очень медленном нагреве или охлаждении, т.е почти в равновесном состоянии.
Диаграмма состояния для сплавов с неограниченной растворимостью в твердом и жидком состоянии, не образующих химических соединений.
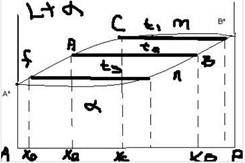
А* - t плавления чистого компонента А
В* - t плавления чистого компонента В
А*mВ* - линия ликвидус, окончание плавления при нагревании , начало кристаллизации – при охлаждении, выше этой линии жидкое состояние,
А*nВ* - солидус. Начало плавления – при нагревании, конец кристаллизации при охлаждении, ниже этой линии твердый раствор.
Фазы две – жидкость и твердый раствор. Эта диаграмма возможна тогда, когда оба компонента имеют одинаковую кристаллическую решетку и их параметры отличаются на 10 – 15 % Диаграмма состоит из двух линий, ликвидус и солидус пересекаются в точке кристаллизации. Эти диаграммы типичны для системы медь – никель, молибден – ванадий, молибден – волфрам и т.п Жидкий раствор начинает кристаллизоваться при tплавления t1. Из жидкости начнут выпадать кристаллы, обогащенные более тугоплавкими компонентами В, т.е их состав XL, при этом оставшаяся жидкость будет обедняться этим компонентом В.при достижении t2 из жидкости буду выделяться кристаллы ХВ, а жидкость при этой температуре будет ХА. При достижении температуры t будет разный состав. При достижении t3 оставшаяся жидкость будет иметь состав ХF.Состав жидкости меняется по линии В*mА* от t1 до f, а состав твердой фазы по B*nA*от l до t3.