Способы выражения состава растворов
Растворами называют гомогенные системы, состоящие из двух и более компонентов. Компонент, агрегатное состояние которого не изменяется при образовании раствора, принято называть растворителем, а другой компонент – растворенным веществом. При одинаковом агрегатном состоянии компонентов растворителем считают то вещество, которое преобладает в растворе.
Способы выражения состава раствора:
Массовая доля С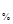 (Х) или W(X) –число граммов растворенного вещества, содержащееся в 100 г раствора.
(Х) или W(X) –число граммов растворенного вещества, содержащееся в 100 г раствора.
С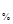 (Х) =
(Х) = 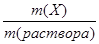 100% или С
100% или С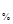 (Х) =
(Х) =  100%,
100%,
где m(Х) – масса растворенного вещества Х, г
m (раствора) - масса раствора, г
V - объем раствора, см
- объем раствора, см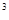
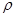
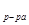 - плотность раствора, г/см
- плотность раствора, г/см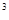 .
.
Молярная концентрация С или С(Х)– число моль растворенного вещества Х, содержащееся в 1дм
или С(Х)– число моль растворенного вещества Х, содержащееся в 1дм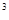 или 1 л раствора ( молярность М ).
или 1 л раствора ( молярность М ).
С(Х) =  или С(Х) =
или С(Х) = 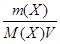 [
[ ],
],
где n(Х) – количество растворенного вещества, моль
V – объем раствора, дм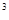 или л
или л
М(Х) – молярная масса растворенного вещества, г/моль.
Раствор, содержащий 1 моль растворенного вещества в 1 дм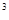 , называется одномолярным (1М), содержащий 0,1 моль вещества – децимолярным (0,1М), содержащий 0,01 моль вещества – сантимолярным (0,01М) и т. д..
, называется одномолярным (1М), содержащий 0,1 моль вещества – децимолярным (0,1М), содержащий 0,01 моль вещества – сантимолярным (0,01М) и т. д..
Молярная концентрация эквивалента С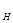 или С (
или С ( Х) –число моль эквивалентов растворенного вещества, содержащееся в 1 дм
Х) –число моль эквивалентов растворенного вещества, содержащееся в 1 дм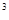 или 1 л раствора (нормальность раствора Н).
или 1 л раствора (нормальность раствора Н).
С ( Х) =
Х) =  или С (
или С ( Х) =
Х) = 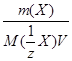 ,
,
где n(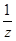 X) – количество эквивалентов вещества Х, моль;
X) – количество эквивалентов вещества Х, моль;
V- объем раствора, дм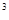 (л);
(л);
М ( Х) – молярная масса эквивалента вещества Х, г/моль.
Х) – молярная масса эквивалента вещества Х, г/моль.
Раствор, содержащий 1 моль эквивалентов растворенного вещества в 1 дм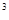 раствора, называется однонормальный (1Н), содержащий 0,1 моль эквивалентов – децинормальным (0,1Н) и т.д..
раствора, называется однонормальный (1Н), содержащий 0,1 моль эквивалентов – децинормальным (0,1Н) и т.д..
Для перевода одного способа выражения концентрации раствора в другой используются соотношения: