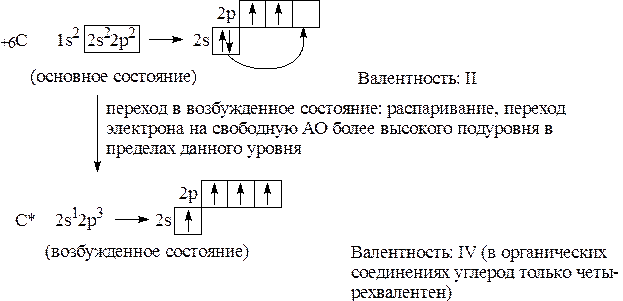К вопросу электронного строения атома
Согласно современным представлениям атом – нейтральная делимая частица, в центре которой находится положительно заряженное ядро. Заряд ядра равен порядковому номеру элемента и числу электронов вокруг ядра.
Электрон (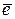 ) имеет заряд –1 и обладает одновременно свойствами волны и частицы. С точки зрения квантовой механики нельзя дать строго координаты электрона в атоме, а можно говорить только о пространстве его наиболее вероятного нахождения вокруг ядра, которое называется атомной орбиталью (АО).
) имеет заряд –1 и обладает одновременно свойствами волны и частицы. С точки зрения квантовой механики нельзя дать строго координаты электрона в атоме, а можно говорить только о пространстве его наиболее вероятного нахождения вокруг ядра, которое называется атомной орбиталью (АО).
Формы АО: 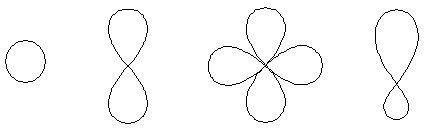
s-АО p-АО d-АО гибридная АО
Заполнение электронами АО подчиняется трем основным правилам.
Принцип Паули. Каждый электрон в атоме имеет свое энергетическое состояние (в атоме нет двух одинаковых электронов).
Чем же электроны в атоме могут различаться?
1) Запасом энергии (Е). По запасу Е все электроны в атоме распределяются по энергетическим уровням или электронным слоям.
Номер уровня обозначают n = 1, 2, 3, …
Самый малый запас Е у электронов первого уровня.
2) Внутри уровня электроны различаются формой АО и по этому признаку объединяются в подуровни: s-, p-, d-, f-.
На первом уровне – только s-подуровень; на 2-ом – s- и p-; на 3-ем – s-, p- и d-; на 4-ом – s-, p-, d- и f-.
3) Внутри подуровня электроны различаются расположением АО в пространстве. По этому признаку определяется количество АО на подуровне:
s-подуровень – 1 АО; p-подуровень – 3 АО (px, py, pz); d-подуровень – 5 АО,
f-подуровень – 7 АО.
4) На данной АО электроны отличаются друг от друга направлением вращения вокруг собственной оси (спином) и их может быть только два: один – по часовой, а другой – против часовой стрелки.
Принцип наименьшей Е. Электроны в атоме заполняют вначале наиболее энергетически выгодные АО: 1s < 2s < 2p < 3s < 3p < 4s < 3d… Таким образом d-подуровни энергетически невыгодны и заполняются после s-подуровня вышестоящего уровня.
Правило Гунда. Электроны располагаются на АО так, чтобы сохранялось наибольшее число электронов с параллельными спинами, т.е. поодиночке.
В ПСЭ все элементы по заполнению подуровней делятся на блоки: s-, p-, d-… Для s- и p-элементов число электронов на внешнем уровне равняется номеру группы; для d-элементов – сумме электронов с внешнего s- и предвнешнего d-подуровня. Эти электроны называются валентными, так как могут принимать участие в образовании химической связи.
Валентность – число связей, которые дает атом в данном состоянии.
Задача № 1. Показать электронное состояние атома углерода и возможные валентности.
|
С – элемент II периода и его 6 электронов распределяются по двум энергетическим уровням.