рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Образующийся сульфат свинца PbSO4 нерастворим и остается на поверхности электрода.
Реферат Курсовая Конспект
Образующийся сульфат свинца PbSO4 нерастворим и остается на поверхности электрода.
Образующийся сульфат свинца PbSO4 нерастворим и остается на поверхности электрода. - раздел Образование, Гальванические элементы Зарядка Аккумулятора. Анод Цепи Аккумулятора Соединяют С Анодом Генератора По...
ЗАРЯДКА АККУМУЛЯТОРА. Анод цепи аккумулятора соединяют с анодом генератора постоянного тока, а катод с катодом генератора. При этом происходят реакции:
К (-) PbSO4 + 2 е => Pb0 + SO42 - на катоде образуется губчатый свинец Pb и концентрация кислоты увеличивается.
А (+) PbSO4 + SO42 - 2 е => Pb (SO42-) 2. Образующаяся на аноде соль Pb (SO42-) 2, подвергается гидролизу:
Pb (SO42-) 2 + 4 H2O => Pb (OH) 4 + H2SO4
Pb (OH) 4 => PbO2 + 2 H2O
Или суммарно: Pb SO4 + 2 H2O - 2 е => PbO2 + 2 H2SO4.
В результате на одной пластине образуется губчатый свинец (катод аккумулятора), на другой - пористый PbO (анод аккумулятора).
Образовался гальванический элемент:
(-) Pb | H2SO4 | PbO2 (+).
При соединении металлическим проводником - РАЗРЯДКА:
K (+) PbO2 + 2 e + 4 H+ + SO42 - = > PbSO4 + 2 H2O(-) Pb0 - 2 e + SO42 - = > PbSO4.
Или суммарно:

ЭДС = 2 вольта. Напряжение меньшее 1.85 В недопустимо, при этом аккумулятор портится и считается разряженным.
Схема зарядки и разрядки свинцового аккумулятора:

Применяется в автомобилях, тракторах, электрохимических лабораториях. Недостаток - большая масса. Выгодно отличаются от свинцового - щелочные аккумуляторы: они более просты в уходе, у них больше срок службы и меньше масса. Используются для питания телефонных, телеграфных станций, радиоустановок и др.
3.2 Щелочные аккумуляторы
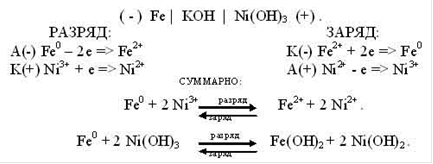
В железо-никелевом аккумуляторе активной массой анода является губчатое железо, спрессованное со специальными добавками HgO; катода - гидроксид никеля Ni (OH) 3, который частично дегидратируется до NiOOH; электролитом - 23-30% раствор КОН с плотностью 1.21 г/мл. ЭДС = 1.35 вольт.
Схема зарядки и разрядки железо-никелевого аккумулятора:

Недостаток - низкий коэффициент отдачи (50%), т.к. энергия поглощается при зарядке. Более высокий коэффициент отдачи имеет кадмиево-никелевый аккумулятор.
Схема зарядки и разрядки кадмиево-никелевого аккумулятора:
В последнее время широкое использование получили серебряно-цинковые аккумуляторы, у которых при малом весе значительно больше емкость и они работают в широком интервале температур (от - 60 до + 800С), кроме того они могут долго хранится в заряженном состоянии и работать в широком интервале атмосферного давления. ЭДС = 1.85 вольта.
Емкость аккумулятора - это количество электричества, выраженное в ампер-часах, которое может быть получено от заряженного аккумулятора. Емкость свинцового аккумулятора выше, чем щелочных аккумуляторов.
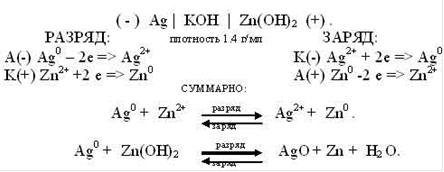
Схема зарядки и разрядки серебряно-цинкового аккумулятора:
Особой разновидностью химических источников тока являются электрохимические генераторыилитопливные элементы.
3.3 Топливные элементы
В топливном элементе химическая реакция горения топлива непосредственно превращается в электрическую энергию, поэтому КПД его превышает 80%. Как и в любом химическом источнике тока, реакция между восстановителем (топливом) и окислителем протекает на двух пространственно разделенных электродах. Однако в отличие от обычных источников тока запасы топлива и окислителя находятся не с самом элементе, а подаются в электроды извне. Это элемент непрерывного действия, т.к. реагирующие вещества непрерывно подводят к электродам, а продукты горения - отводят.
В топливных элементах используется жидкое (метиловый, этиловый спирт, формальдегид, гидразин) или газообразное топливо (водород, оксид углерода, пары бензина, этилен, бутан, пропан и др. горючие газы). В качестве окислителя применяют воздух, кислород, хлор, бром. Электролиты - водные растворы кислот, щелочей, расплавленные карбонаты, гидроксиды металлов.
– Конец работы –
Эта тема принадлежит разделу:
Гальванические элементы
В окислительно восстановительных реакциях происходит переход электронов от... Гальваническим элементом называется прибор в котором происходит превращение химической энергии в электрическую за...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Образующийся сульфат свинца PbSO4 нерастворим и остается на поверхности электрода.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов