Получение алкадиенов-1,2 (аллены)
2.1 Отщепление галогена из дигалогеналкенов:
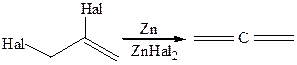
2.2 Изомеризация ацетиленовых углеводородов:

3. Получение алкадиенов-1,3 (сопряженные).
3.1 Пиролиз нефти:
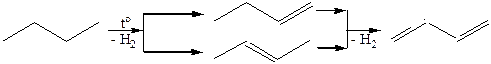
3.2 Дегидрирование алканов и алкенов:

3.3 Дегидратация гликолей и оксаланов (синтез В.Реппе):


3.4 Каталитическое превращение этилового спирта (синтез С.В. Лебедева, 1927 г., осуществляеся на смешанном катализаторе (ZnO, MgO):
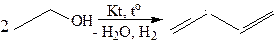
3.5 Метод Принса:

3.6 Метод А.Е.Фаворского:

Физические свойства и строение алкадиенов. Аллены представляют собой бесцветные газы (С3, С4) или бесцветные жидкости со слабым запахом. Четыре атома водорода молекулы аллена находятся в двух взаимно перпендикулярных плоскостях:
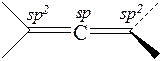
Углеродные атомы в молекуле аллена находятся в различных состояниях гибридизации – sp2, sp, sp2. Благодаря строению двузамещенных алленов для них возможна стереоизомерия, например:

Структура I является зеркальным изображением структуры II. Эти молекулы хиральны.
Алкадиены-1,3 представляют собой бесцветные вещества. Первые члены гомологического ряда являются газами или низкокипящими жидкостями (табл. 22).
Таблица 22 – Физические свойства некоторых алкадиенов
| Соединение | 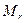
| Формула | Т, °С | Плотность, 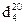
| |
| пл. | кип. | ||||
| бутандиен-1,3 | СН2=СНСН=СН2 | –108,4 | –4,5 | 0,6206 | |
| 2-метилбутандиен-1,3 | СН2=С(СН3)СН=СН2 | –136 | 34,1 | 0,6810 | |
| 2,2-диметилбутандиен-1,3 | СН2=С(СН3)2СН=СН2 | –76 | 68,6 | 0,7262 |
Для алкадиенов-1,3 характерна повышенная молекулярная рефракция. Экзальтация рефракции связана с увеличением поляризуемости электронной системы, что характерно для сопряженных систем двойных связей.
При сравнении экспериментальных значений теплоты образования с полученной суммированием термохимических энергий связей для молекул алкадиенов-1,3 экспериментальная величина получается больше на 13. . .16 кДж/моль. Т. е. при образовании сопряженной системы выделяется больше энергии, чем при образовании несопряженной системы и, следовательно, сопряженные системы являются более стабильными. Эта энергия называется энергией сопряжения (делокализации, резонанса).
Молекула бутадиена планарная, наиболее вероятным расположением двойных связей является транс-расположение по отношению к ординарной связи. Длины С–С-связей отличаются от таковых в этилене (0,133 нм) и этане (0,154 нм).
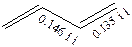
Сопряженные алкадиены обнаруживают ряд заметных отличий в параметрах молекулы, строении и свойствах в сравнении с алкадиенами двух других классов и классическими алкенами.