Реакции электрофильного присоединения.
1.1.1 Гидрирование (катализатор Ni, Pt, Pd):

1.1.2 Галогенирование. Присоединение галогенов по тройной связи протекает как анти-присоединение, реакция протекает медленнее, чем для алкенов за счет меньшей стабильности винильного катиона и более притянутого к ядрам атомов углерода π-молекулярного облака за счет повышенной электроотрицательности и, следовательно, труднее поляризуемого:

1.1.3 Гидрогалогенирование:

На второй стадии образуются геминальные дигалогеналканы:

Дестабилизирующее влияние атома галогена в карбкатионе (а) ослаблено за счет +М-эффекта. Атом галогена своей НЭП р-электронов участвует в делокализации "+" заряда. Вследствие большей стабильности карбокатион (а) образуется быстрее и его взаимодействие с нуклеофилом приводит к получению геминального дигалогенпроизводного.
1.1.4 Гидратация (реакция М.Г. Кучерова, 1881 г.):

На первой стадии образуются енолы, которые перегруппировываются в карбонильные соединения (правило Эльтекова – Эленмеера). Перегруппировку обеспечивает эффект р,π-сопряжения, вследствии которого электронная плотность перемещается от кислорода к углеродному атому к которому направляется протон гидроксильной группы:

1.1.5 Присоединение Н – электрофилов (НХ, где Х= CN, SR, RCOO):

1.2 Реакции нуклеофильного присоединения:
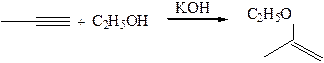
Механизм реакции нуклеофильного присоединения (АN) состоит в том, что алкин атакует частица или молекула, в результате присоединения которой образуется карбоанион, который как сильное основание стабилизируется, отрывая подвижный протон от реагента:

1.3 Гидроборирование. Образующиеся при этом алкенилбораны обрабатывают уксусной кислотой при низкой температуре превращая их в алкены:
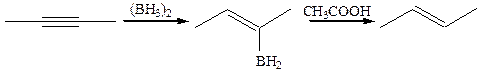
1.4. Карбонилирование (оксосинтез, гидроформилирование):

2. Реакции окисления.
2.1 Ацетиленовые углеводороды обесцвечивают щелочной растворKMnO4 на холоду:

2.2 Реакция с озоном:

2.3 Жесткое окисление. Сильные окислители (КMnO4, K2Cr2O7, CrO3) в кислой среде расщепляют ацетиленовые углеводороды по тройной связи:

2.4 Реакция горения:
С2Н2 + 2,5О2  СО2 + Н2О
СО2 + Н2О
С2Н2 + 1,5О2  СО2 + Н2О + С
СО2 + Н2О + С
3. Реакции алкинов по терминальной связи.Согласно протолитической теории, под кислотностью понимают способность отдать протон. В алкинах, благодаря повышенной электроотрицательности sp-гибридного С-атома, терминальная связь обладает заметной полярностью. Поэтому в присутствии сильных оснований возможна ионизация терминальных алкинов с образованием ацетиленид-ионов и передачей протона основанию.
3.1 Образование ацетиленидов: