Циклоприсоединение в синтезе производных циклобутана
[2 + 2)-Циклоприсоединенис относится к категории важнейших синтетических методов, поскольку эта реакция позволяет получать различные производные циклобутана по схеме сборки из двух алкеновых фрагментов. Этот процесс может протекать как по согласованому механизму через образование циклического переходного состояния (а), так и по стадиям, включающим промежуточное образование бирадикального (B) или биполярного (с) интермедиата (схема 2.126). Реализация того или иного из этих механизмов зависит как от строения реагентов, так и от условий проведения реакции.
 Схема 2.126
Схема 2.126
|
В случае термически индуцированного процесса согласованный механизм реализуется лишь для ограниченной категории реакций, таких, как взаимодействие кетенов с алкенами или алкинами. Результатом реакции всегда является образование продуктов чис-присоединения [32а]. Сам кетен в силу своей неустойчивости относительно редко используется в этой реакции, и чаще всего для синтеза циклобутанонов применяют более стабильные а-хлоркетены, которые генерируются in situ (действием триэтиламина на хло-рангидриды а-хлорзамещенных кислот) в присутствии второго компонента циклоприсоединения. На схеме 2.127 приведены типичные примгры этой реакции — образование циклоаддуктов 378[32Ь] и 379[32с]. Отметим, что, хотя в последнем случае реакция протекала с довольно скромным выходом (около 20%), однако она оказалась самым удобным методом синтеза аддукта 379,из которого в одну стадию был получен микотоксин монилиформин (380),природное соединение уникальной структуры, которую довольно затруднительно получить другим способом.
 Схема 2.127
Схема 2.127
|
а-Хлорциклобутаноны, образующиеся в рассматриваемой реакции, достаточно просто могут быть превращены в соответствующие циклобутаноны (восстановительным дехлорированием) или их можно непосредственно использовать в дальнейших превращениях в качестве субстратов, содержащих хорошую уходящую группу (а-хлорзаместитель) (см. далее).
Важным для синтеза является внутримолекулярное [2 + 21-циклопри-соединение кетенов к алкенам. Для этой реакции оптимальное расстояние между двумя кратными связями соответствует мостику из трех звеньев [32d]. Поэтому этот путь особенно удобен для получения различных структур, содержащих 4,5-сочлененный бициклический фрагмент. Типичными примерами являются показанные на схеме 2.128 превращения 381-> 382[32е] и 383-> 384[32f]. В этих превращениях генерация кетеновой функции также проводится in situ, но в этом случае, благодаря легкости протекания внутримолекулярной циклизации, уже не требуется наличия а-хлорзаместителя в кетеновом фрагменте (см. структуры интермедиатов 381аи 383а).Очевидным достоинством метода является легкость получения требуемых предшественников, как это показано на примере синтеза эфира 383.
 Схема 2.128
Схема 2.128
|
Фотохимически индуцированное [2 + 21-циклоприсоединение относится к категории важнейших реакций, особенно б синтезе стерически затрудненных соединений самых экзотических структурных типов [32g|. Эта реакция может протекать в соответствии с правилами сохранения орбитальной симметрии по согласованному механизму, но чаще реализуется бирадикальный механизм (пугьЬ, схема 2.126). В препаративной практике чаще всего применяется фотохимически индуцированное [2 + 2]-циклоприсоединение оле-фина к енону. Для этой реакции характерны высокая региоселективность, но подчас довольно низкая стереоселективность, что вполне согласуется с упомянутым бирадикальным механизмом.
Один из первых примеров, показавших полезность этой реакции для получения полициклических соединений, был описанный Кори [32h] синтез природного сесквитерпсна, а-кариофиллена (385)(схема 2.129). В качестве исходного вещества здесь был использован бициклический аддукт 386,полученный с высоким выходом по схеме фотоциклоприсоединения изобутиле-на к циклогексенону.
 Схема 2.129
Схема 2.129
|
В структуре адцукта 386уже содержался требуемый фрагмент 1,1-диме-тилциклобутана. Наличие в этом адцукте карбонильной функции позволило далее относительно легко достроить третий цикл и получить таким образом аддукт 387,уже содержавший 14 из 15 требуемых атомов углерода молекулы 385.Дальнейшая последовательность превращений, помимо трансформаций функциональных групп, включала также стадии разрыва центральной связи гидриндановой системы (по реакции фрагментации) с образованием 9-членного цикла и метиленирования по Виттигу,
Синтез а-кариофиллена наглядно продемонстрировал богатые синтетические возможности фотоциклоприсоединия олефина к енону, и вслед за ним последовало еще множество полных синтезов, в которых эта реакция использовалась на той или иной из ключевых стадий [32i].
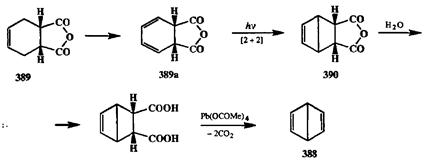 Схема 2.130
Схема 2.130
|
Фотохимически индуцированное [2 + 2]-циклоприсоединение во внутримолекулярном варианте проведения реакции оказалось незаменимым методом построения высоконапряженных молекул. Именно с помощью этой реакции за последние несколько десятилетий удалось получить «во плоти» множество структур, возникших «на кончике пера» как плод творческого воображения химиков-органиков. Одним из первых достижений такого рода был выполенный ван Тамеленом [laj удивительно короткий синтез бензола Дьюара (388),показанный на схеме 2.130.
На начальной стадии этого синтеза легко доступный продукт реакции Дильса—Альдера 389с помощью последовательности бромирование/дегидробромирование превращался в диен 389а.При облучении последнего легко протекало [2 + 2]-циклоприсоединение с образованием трициклического продукта 390.Завершающие стадии синтеза 388включали омыление ангидридного цикла и окислительное декарбоксилирование полученной дикислоты.
Отметим также, что в уже упоминавшемся синтезе баскетена (357)(схема 2.123) образование последней недостающей связи каркасной системы было также осуществлено с помощью [2 + 2]-фотоциклоприсоединения.
Внутримолекулярное [2 + 2]-фотоциклоприсоединение олефина к енону находит широкое применение в синтезе полициклических соединений как ключевая стадия, обеспечивющая быстрое усложнение скелета собираемой молекулярной конструкции [32j]. Хорошей иллюстрацией эффективности такого подхода могут служить превращения, показанные на схеме 2.131.
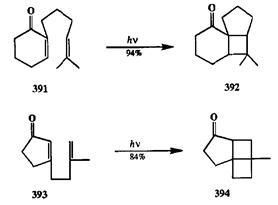 Схема 2.131
Схема 2.131
|
Действительно, превращения 391->392[32k] и 393->394[321] (равно как и многие другие, им подобные, см., например [32т]) протекают при комнатной температуре достаточно быстро с хорошим выходом, с высокой регио- и стереоселективностью и не требуют никаких реагентов или катализаторов, а только облучения. К этому следует добавить, что синтез требуемых диенонов типа 391или 393также несложен и легко может быть выполнен с помощью последовательности хорошо отработанных реакций, таких, как реакция Михаэля и ачкилирование енолятов. Таким образом, вырисовывается общая схема синтеза полициклических соединений, содержащих разные комбинации линейно и ангулярно сочлененных циклов, который включает две основные стадии, а именно: синтез полифункционального субстрата и его [2 + 2]-фотоциклоприсоединение. Дополнительная препаративная ценность такого протокола обусловлена тем, что получаемые напряженные системы могут легко претерпевать реакции с раскрытием циклобутанового фрагмента, а также скелетные перегруппировки [32т] (см. ниже, разд. 2.7.3.2.).
В последующих разделах этой, а также других глав, будет приведено еще немало примеров использования [2 + 2]-фотоциклоприсоединення (как в варианте алкен+ачкен, так и в варианте алкен+енон) для решения задач построения самых различных структур. Здесь уместно сделать еще одно замечание более общего характера. Структуры типа баскетена (357)или бензола Дьюара (388)относятся к числу богатых энергией жестких структур с системой напряженных связей С—С. По сути дела в ходе образования подобного рода систем происходит преобразование лучистой энергии в энергию химической связи. Ясно также, что превращения таких соединений, протекающие с разрывом напряженных фрагментов (например, под действием катализаторов), должны сопровождаться выделением энергии, запасенной при их синтезе. Поэтому внутримолекулярное фотоциклоприсоединение рассматривается сейчас не только как один из полезнейших инструментов органического синтеза, но и как перспективный путь создания систем, способных аккумулировать лучистую (в том числе солнечную) энергию в форме химической энергии, удобной для практического использования.