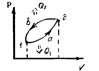
Адиабатный процесс. Уравнение адиабаты. Политропный процесс.
Адиабатическим наз. процесс при котором отсутствует теплообмен (dQ=0) между системой и окружающей средой. dА = -dU , т.е. внешняя работа совершается за счет изменения внутренней энергии системы. Для произвольной массы газа :
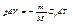 продифференцировав уравнение состояния для идеального газа, получим:
продифференцировав уравнение состояния для идеального газа, получим: 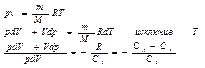 разделив переменные и учитывая, что Ср/Сv= g найдем
разделив переменные и учитывая, что Ср/Сv= g найдем
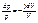 интегрируя это выражение в пределах от р1 до р2 и соответственно от V1 до V2, а затем потенцируя получим:
интегрируя это выражение в пределах от р1 до р2 и соответственно от V1 до V2, а затем потенцируя получим: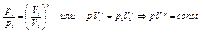
- уравнение адиабатического процесса.(уравнение Пуассона) g- показатель адиабаты
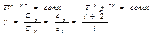
Работа в адиабатическом процессе:
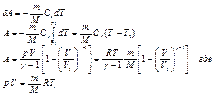
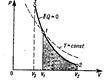 Процесс в котором теплоёмкость остаётся постоянной наз. политропным.
Процесс в котором теплоёмкость остаётся постоянной наз. политропным.
cm = const
cm – молярная теплоемкость.
Найдем уравнение политропы для идеального газа. Из первого начала термодинамики следует
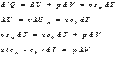
Из уравнения состояния идеального газа следует
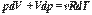
Поэтому можно записать
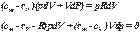 | ||
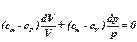 |
Поскольку cP = cV + R то
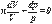
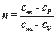
Обозначив получаем
Интегрируем
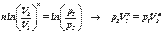 | |||||
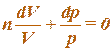 | |||||
 | |||||
Значит уравнение политропы
n - показатель политропы
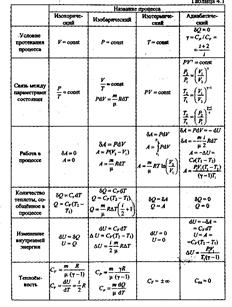
Все предыдущие процессы являются частными случаями политропического процесса:
n = 0 изобара cm = cP, n = 1 изотерма cm = ¥
n = ¥ изохора cm = cV n = g изобара cm = 0 .