Приготування розчину кислоти заданої концентрації
Студент одержує у викладача індивідуальне завдання для приготування певного об'єму (V, см3) кислоти (HCl чи H2SO4) заданої концентрації (С, M) з більш концентрованого розчину кислоти густиною ρ (г/ см3).
Щоб приготувати заданий об'єм розчину кислоти (V), необхідно розрахувати об’єми кислоти V1(кислоти) з густиною ρ і води V2(Н2О), які необхідно змішати (див. приклад розрахунку, с. 7).
Одержані результати записують у таблицю.
| Індивідуальне завдання | Результат | ||||
| Кислота | С, М | V, см3 | ρ, г/ см3 | V1 (кислоти) , см3 | V2 (H2O) , см3 |
Розчин кислоти готують у пронумерованих склянках місткістю 1 дм3. Розраховані об'єми кислоти V1(кислоти) і води V2(H2O) відмірюють мірними циліндрами і переносять у склянку, причому спочатку наливають воду, а потім доливають кислоту.
Приклад розрахунку. Обчислити, який об’єм (см3) сульфатної кислоти з густиною ρ(H2SO4) = 1,14 г/см3 необхідно взяти, щоб приготувати 700 см3 розчину H2SO4 з концентрацією  .
.
Об’єм H2SO4 з густиною 1,14 г/см3, необхідний для приготування заданого об’єму розчину, можна розрахувати двома способами.
І спосіб.
Розраховуємо масу чистої кислоти, потрібну для приготування 700 см3 розчину H2SO4 з концентрацією  за формулою:
за формулою:
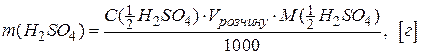 .
.
Оскільки сульфатна кислота є сильним двохосновним електролітом, то обидва йони гідрогену беруть участь в реакціях нейтралізації. Тому фактор еквівалентності сульфатної кислоти 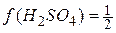 , а молярна маса еквівалента
, а молярна маса еквівалента 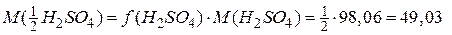 г/моль.
г/моль.
Використавши дані задачі отримаємо:
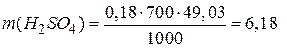 г.
г.
Користуючись довідником [4] знаходимо, що у розчині сульфатної кислоти з густиною 1,14 г/см3 міститься 20,08 % H2SO4. Враховуючи масову частку, розраховуємо масу розчину за формулою:
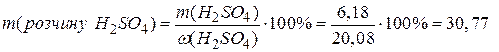 г.
г.
Знаючи густину розчину, знаходимо його об’єм:
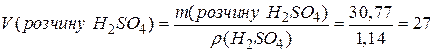 см3.
см3.
ІІ спосіб.
У довіднику [4] також вказано, що молярна концентрація розчину сульфатної кислоти з густиною 1,14 г/см3 дорівнює 2,334 моль/дм3. Оскільки 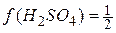 , то молярна концентрація еквівалента
, то молярна концентрація еквівалента 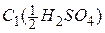 дорівнює:
дорівнює:
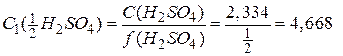 моль/дм3.
моль/дм3.
Використаємо закон еквівалентів:
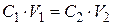 ,
,
звідки знайдемо об’єм V1 розчину кислоти, потрібний для приготування 700 см3 (V2) розчину H2SO4 заданої концентрації (С2).
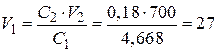 см3.
см3.
В обох випадках об’єм води V(H2O), до якого треба долити 27 см3 сульфатної кислоти з густиною 1,14 г/см3, дорівнює:
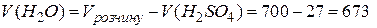 см3.
см3.
Відповідь: щоб приготувати 700 см3 розчину H2SO4 з концентрацією  необхідно змішати 673 см3 води і 27 см3 H2SO4 з густиною ρ(H2SO4) = 1,14 г/см3.
необхідно змішати 673 см3 води і 27 см3 H2SO4 з густиною ρ(H2SO4) = 1,14 г/см3.
Лабораторна робота № 2
Стандартизація розчину кислоти (HCl або H2SO4)