Классификация ОВР.
1)Реакции межмолекулярного окисления-восстановления(окислитель и восстановитель - в разных молекулах):
Zn + CuSO4 = ZnSO4 + Cu
H2 + Br2 = 2HBr
2) Реакции диспропорционирования (самоокисления - самовосстановления):
а) 2H2O2–1  O20 + 2H2O–2
O20 + 2H2O–2
│H2O2 + 2ē = 2OH‾
│H2O2 - 2ē = O2↑ + 2H+
б) 3Se0 + 6KOH = K2Se+4O3 + 2K2Se–2 + 3H2O
1│Se + 6OH– – 4ē = SeO32– + 3H2O
2│Se + 2ē = Se2–
3) Реакции внутримолекулярного окисления-восстановления(окислитель и восстановитель находятся в одной молекуле):
(N–3H4)2Cr2+6O7 = Cr2+3O3 + N20 + 4H2O
Факторы, влияющие на протекание ОВР:
- природа взаимодействующих веществ;
- температура;
- катализаторы;
- концентрация:
- рН среды.
Влияние рН среды на протекание ОВР.
KMnO4 в кислой, нейтральной и щелочной средах:

Участие частиц среды в переносе кислорода в ОВР.
| рН среды | Акцептор кислорода | Донор кислорода | Схема процесса | ||
| рН < 7 | Н+ | Н2О | 2Н+ | 
| Н2О |
| рН > 7 | Н2О | ОН– | 2ОН– | 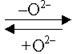
| Н2О |
| рН = 7 | Н2О | Н2О | Н2О | 
| 2ОН– |
| Н2О | 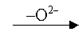
| 2Н+ |