рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Физика
- /
- Вид работы: Лабораторные Работы
- /
- ОБЩАЯ ТЕОРИЯ
Реферат Курсовая Конспект
ОБЩАЯ ТЕОРИЯ
ОБЩАЯ ТЕОРИЯ - Лабораторная Работа, раздел Физика, Методическое пособие для выполнения лабораторных работ по физике часть III Исследования Английского Физика Э. Резерфорда (1911Г.) Установили Так Называе...
Исследования английского физика Э. Резерфорда (1911г.) установили так называемую планетарную модель строения атома. Согласно этой модели весь положительный заряд и почти вся масса атома (> 99.94%) сосредоточены в атомном ядре, размер которого ничтожно мал (10-15м) по сравнению с размером атома (10-10м). Вокруг ядра по замкнутым круговым орбитам движутся электроны, образуя электронную оболочку атома.
Заряд ядра равен по абсолютному значению суммарному заряду электронов и может быть найден по формуле:
q = Ze, (501.1)
где е = 1.6×10-19Кл –– элементарный заряд, Z –– порядковый номер элемента в периодической системе Д.И. Менделеева.
Однако эта модель не укладывалась в рамки законов классической физики, согласно которым, электрон, двигаясь равноускоренно, должен непрерывно излучать (терять) энергию и, в конце концов, упасть на ядро. Атом должен давать сплошной спектр излучения, так как частота вращения электрона по мере приближения к ядру непрерывно изменяется (соответственно, так же меняется и частота излучения).
В действительности атом весьма устойчив и излучает линейчатый спектр, что говорит о том, что частота вращения электрона может принимать лишь определенные значения.
В нашей работе мы будем рассматривать спектр излучения атома водорода, как самого простого вещества.
В видимой части этого спектра обнаружены четыре линии со следующими длинами волн:
· λк = 0.656мкм –– красная линия;
· λг = 0.486мкм –– голубая линия;
· λс = 0.434мкм –– синяя линия;
· λф = 0.410мкм –– фиолетовая линия.
Швейцарский физик И. Бальмер и шведский физик И. Ридберг установили эмпирическую формулу для определения длин волн этих линий (серия Бальмера):
 , (501.2)
, (501.2)
где n = 3, 4, 5, 6,…, R = 1.0974×107м-1 –– постоянная Ридберга, вычисляемая теоретически по формуле:
 , (501.3)
, (501.3)
где т, е –– масса и заряд электрона, h = 6.625×10-34Дж∙с–– постоянная Планка,
 –– электрическая постоянная,
–– электрическая постоянная, 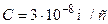 - скорость света в вакууме.
- скорость света в вакууме.
Существуют и другие серии излучений (Лаймана, Пашена и др.), которые к нашему опыту не имеют прямого отношения.
Датский физик Н. Бор (1913г.) усовершенствовал атомную модель Резерфорда и создал другую модель строения атома, в основу которой положил три постулата (постулаты Бора):
- Электроны могут двигаться в атоме только по орбитам определенного радиуса, на которых момент импульса электрона кратен постоянной Планка
 .
.
Это условие квантования радиуса орбиты выражается формулой:
 , (501.4)
, (501.4)
где т –– масса электрона, v –– скорость электрона, r –– радиус орбиты, n = 1,2,3,… –– главное квантовое число.
- Движение электрона по таким стационарным орбитам не сопровождается излучением (поглощением) энергии.
- Переход электрона с одной орбиты на другую сопровождается излучением или поглощением кванта энергии:
 , (501.5)
, (501.5)
где W1 и W2 –– энергии стационарного состояния атома.
Таким образом, частота излучения определяется разностью энергий, а не частотой вращения электрона в атоме.
В атоме изотопа водорода  один электрон вращается вокруг одного протона. Заряды электрона и протона равны по модулю величине элементарного заряда е=1,6·10-3 Кл.
один электрон вращается вокруг одного протона. Заряды электрона и протона равны по модулю величине элементарного заряда е=1,6·10-3 Кл.
Пусть электрон вращается по круговой орбите радиуса r, тогда на него будет действовать кулоновская сила, направленная к центру орбиты, которая будет также центростремительной силой. Уравнение движения электрона запишется в виде:
 , (501.6)
, (501.6)
откуда
 , (501.7)
, (501.7)
где т = 9.11×10-31кг –– масса электрона, ε0 = 8.85×10-12Ф/м –– электрическая постоянная.
Решим совместно уравнения (501.4) и (501.7), исключая скорость. Из (501.4) имеем:
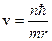 .
.
Подставив скорость в формулу (501.7), получим

а радиус орбиты электрона равен
 . (501.8)
. (501.8)
Полная энергия электрона в атоме есть сумма кинетической энергии и потенциальной энергии притяжения электрона к ядру:
 . (501.9)
. (501.9)
Из (501.7) следует, что
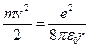 ,
,
тогда полная энергия
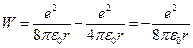 . (501.10)
. (501.10)
Таким образом, полная энергия электрона отрицательна и равна по модулю его кинетической энергии. Подставляя (501.10) в (501.8), получаем
 . (501.11)
. (501.11)
Для ближайшей к ядру орбите (п = 1) полная энергия электрона, находящегося на этой орбите, равна:
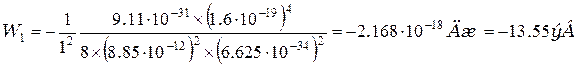 .
.
[1эВ = 1.6×10-19Дж].
Полная энергия электронов в атоме называется энергетическим уровнем атома. На рис. 501-1 схематически изображены уровни энергии атома водорода.


Атом может излучать и поглощать электромагнитные волны только вполне определенных частот (длин волн), чем и обусловлен линейчатый характер водородного спектра.
Серия Бальмера соответствует переходу атома на второй уровень энергии с более высокого. А именно, красная линия соответствует переходу с третьего уровня на второй (п=3 → п=2). При этом частота излучения, согласно (501.5), равна:
 [Гц],
[Гц],
а соответствующая длина волны
 [м].
[м].
Подставляя константы, получим
 .
.
Для переходов с четвертого, пятого и шестого энергетических уровней на второй мы будем иметь в спектре излучения атома водорода длины волн, соответствующие голубому (λгол = 489нм), синему(λсин = 437нм) и фиолетовому(λфио = 414нм) цветам, соответственно. При этом расхождения этих длин волн со значениями, полученными в результате эксперимента, не превышают 0,8%.
– Конец работы –
Эта тема принадлежит разделу:
Методическое пособие для выполнения лабораторных работ по физике часть III
Кафедра физики... Методическое пособие для выполнения лабораторных работ по физике...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ОБЩАЯ ТЕОРИЯ
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов