Расчет изменеия термодинамических функций в химических реакциях
По закону Гесса теплоту реакции можно представить в виде суммы изменения внутренней энергии всех веществ, участвующих в реакции
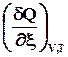 =
=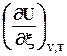 =
= 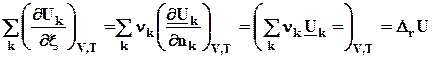
(2.14)
Оператор Drозначаетдействие над любой функцией состояния, сводя-щееся к суммированию мольных значений этой функции для реагентов и продкутов химической реакции, умноженных на соответствующий стехи-ометрический коэффициент. Результат действия оператора Dr на функцию выражает изменение данной фунции в химической реакции. В старых учебниках, в которых не используется знаки стехиометрических коэффициентов для различения реагентов и продуктов, последняя формула выглядит более громоздко
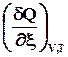 = DrU =
= DrU =
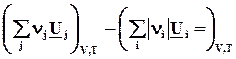 , (2.15)
, (2.15)
где индекс i относится к реагентам, а индекс j - к продуктам.
| Qv = DrU, при V=const, T = const, W’ = 0, x = 1. |
При постоянном давлении теплота химической реакции будет выражаться через действие оператора Drна энтальпию системы
Qр= 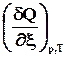 = Dr Н =
= Dr Н =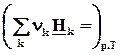 =
=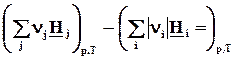 (2.16)
(2.16)
при р=const, T = const, W’ = 0, x = 1.