Коэффициент летучести. Стандартные состояния.
 m
m
 1
1
 m0 2
m0 2
 m*
m*
0  ln p
ln p
Рис.8.2. Зависимость химического потенциала идеального (1) и реального(2)газов от давления.
Химический потенциал идеального газа линейно зависит от логарифма давления (Рис.8.2). Для реального газа зависимость будет криволинейной. За стандартное состояние идеального газа принимают его состояние при давлении 1 атм (ln p˚= 0). Казалось бы на основании уравнения (8.25), что для реального газа – стандартным будет состояние при летучести, рав-ной единице (ln f ˚= 0,точкаm*) . На самом деле стандартное состояние одно и то же для обоих газов: f0 = p0 = 1. Для того, чтобы придти к стандартному состоянию реальный газ нужно расширить по изотерме до бесконечно малого давления, где реальный и идеальный газы имеют одинаковые свойства, в том числе и химические потенциалы, а затем сжать до р = 1 по изотерме идеального газа. Такое сложное определение стандартного состояния позволяет все отклонения реального газа от идеального выразить через коэффициент летучести g,который связывает летучесть и давление:
f = gp, или g = f/p. (8.26)
Свойства реальных и идеальных газов сближаются по мере уменьше-ния давления lim f/p p®0 = 1. g p®0 = 1. (8.27)
Таким образом, именно коэффициент активность выражает отклонение реального газа от идеального и связан с взаимодействиями, существующими в реальном газе. Отношение летучести к стандартному давлению называется активностью
a = f/f0 = p/p0. (8.28)
8.6.4. Методы определения летучести и коэффициента летучести.
8.6.4.1. Летучесть и коэффициенты летучести можно определять эксперименталь-но, измеряя мольные объемы реального газа в зависимости от давления. Эти объемы отличаются от молных объемов идеального газа на величину α:
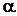 = Vид.–Vреал. Þ(8.29)
= Vид.–Vреал. Þ(8.29)
Vреал. = Vид.- 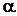 = RT/p -
= RT/p - 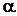 (8.30)
(8.30)
dmT = dG = RT d(lnf) = V dp = (RT/p -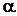 ) dp,(8.31)
) dp,(8.31)
Проинтегрируем уравнение (8.31), приняв за нижний предел бесконечно малое давление, когда f1 ® p1® 0
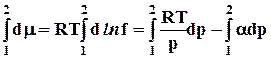 Þ
Þ
RT ln(f2/p1) = RT ln(p2 /p1) - 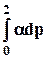 Þ RT lnp2 + RT lng = RT ln p2 -
Þ RT lnp2 + RT lng = RT ln p2 -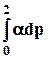
RT lng = - 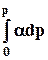 ; ln g = - 1/RT
; ln g = - 1/RT 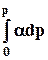 .(8.32)
.(8.32)
По экспериментальной зависимости величины α от давления графически рассчитывают интеграл в уравнении (8.32) и таким образом находят ln gдля разных давлений
 | |||||
 |  | ||||


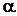 g1.5 t
g1.5 t
0.8 t
0.5 t
 0 р p
0 р p
а) б)
Рис.8.3. Методы определения коэффициентов летучести: а) по уравнению 9.10, б) методом соответственных состояний.
8.6.4.2.Метод соответственных состояний
Как уже указывалось в разделе 8.6.1. разные газы ведут себя одинаково при одинаковых приведенных параметрах p, t. В справочниках имеются номограммы которые позволяют определить коэффициенты летучести разных газов по их приведенным параметрам, т.е. отнесенным критическим.
Таблица 8.1. Летучести и коэффициентов летучести азота при 0 С
| р, атм | ||||||||
| f | 0.9995 | 9.956 | 49.06 | 97.03 | 194.4 | 424.8 | 743.4 | 1.839 |
| g | 0.9995 | 0.9956 | 0.981 | 0.970 | 0.972 | 1.062 | 1.269 | 1.839 |
Лекция № 9