Общее условие химического равновесия в закрытой системе
В химической реакции происходит изменение числа молей компонентов в соответствии со стехиометрическим уравнением 0 =S nkAk. Этим системы с химическими реакциями напоминают открытые системы, которые обмениваются веществом с окружающей средой, поэтому полные дифференциалы характеристических функций следует записывать как для открытых систем, например, dG = - SdT + Vdp + Smkdnk .
При p,T = const dGр,Т = Smk dnk. (9.1)
Так же будут выглядеть дифференциалы других характеристических функций при постоянных значениях их естественных параметров. В самопроизвольных процессах при p,T = const энергия Гиббса должна убывать dGр,Т< 0, а в состоянии равновесия достигать минимального значения dGр,Т=0. Следовательно, в самопроизвольной химической реакции при p,T = const Smk dnk < 0. Но если в истинно открытой системе изменения чисел молей веществ независимы друг от друга, то в закрытой системе с химической реакцией они связаны между собой и могут быть все выражены через химическую переменную
dnk/nk = dx и dnk = nk dx
dGpT = Smk nk dx.
В самопроизвольном процессе при p,T = const производная по степени протекания химической реакции должна убывать, а в состоянии химического равновесия равняться 0:
самопроизвольный процесс 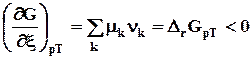 ; (9.2)
; (9.2)
химическое равновесие 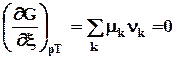 . (9.3)
. (9.3)
В принципе химическое равновесие можно выражать через любую характеристическую функцию, но наиболее просто это можно сделать через энергию Гиббса.
DrGpT = Smk nk = S G k∙ nk = S G j∙ nj - Sçni ç∙ G i = 0.(9.4)
Величина 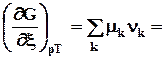 DrGpTпоказывает изменение энергии Гиббса за 1 пробег (
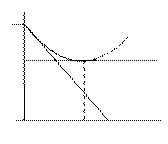
DrGpTпоказывает изменение энергии Гиббса за 1 пробег (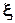 =1), т.е. при полном превращении реагентов в продукты в мольных количествах, соответствующих стехиометрическим коэффициентам, при р,T = const и заданном составе системы по сравнению с равновесным состоянием, для которого DrGpT = 0. Поэтому ее можно рассматривать как меру химической неравновесности системы, а -DrGpTназывают химическим сродством. На графике 9.1 эта величина определяет угловой коэффициент наклона касательной. По мере увеличения химической переменной этот коэффициент уменьшается в связи с изменением состава реакционной смеси, достигая нуля при равновесии.
=1), т.е. при полном превращении реагентов в продукты в мольных количествах, соответствующих стехиометрическим коэффициентам, при р,T = const и заданном составе системы по сравнению с равновесным состоянием, для которого DrGpT = 0. Поэтому ее можно рассматривать как меру химической неравновесности системы, а -DrGpTназывают химическим сродством. На графике 9.1 эта величина определяет угловой коэффициент наклона касательной. По мере увеличения химической переменной этот коэффициент уменьшается в связи с изменением состава реакционной смеси, достигая нуля при равновесии.
 ξ
ξ
Рис. 9.1. Химическое сродство.
Поскольку нет возможности определить абсолютное значение энергии Гиббса какого-либо вещества, вводится понятие изменение ее в реакции образования (так же как энтальпии), т.е. получения данного соединения из простых веществ.
ТогдаDrGpT = S Df G k∙ nk = SDf G j∙ nj - Sçni ç∙Df G i = 0.(9.5)
Для простых веществ DfG˚ = 0.