Равновесие
Классическая термодинамика обычно ограничивается рассмотрением равновесных состояний ТДС. Равновесие - это такое состояние, к которому самопроизвольно приходит ТДС, и в котором она может существовать бесконечно долго в отсутствие внешних воздействий. Для определения равновесного состояния всегда требуется меньшее количество параметров, чем для неравновесных систем.
2.2.3. Уравнение соcтояния связывает параметры состояния и относится к фазе. Общий вид его f (p,V, T) = 0. Простейший вид уравнения состояния имеет идеальный газ pV = nRT, (1.1)
где R = 8.314 Дж/(моль.К) = 1,987 кал/(моль.К) = 0,082 л.атм/(моль.К) .
[p] = Па, 1атм = 1,013*105 Па = 760 мм рт.ст.,
[V ] = м3, 1 м3 = 103 л,
[T] = К,
[n] = моль, N = 6.02*1023 моль-1= 6,02*1026 кмоль-1 .
2.2.4. Функции сост ояния – это характеристики системы, которые зависят только от параметров состояния, но не зависят от способа его достижения.
 ∙ F (x,y), например, F(V,T)
∙ F (x,y), например, F(V,T)
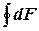 = 0, dF– полный дифференциал
= 0, dF– полный дифференциал
 dF =
dF = 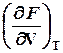 dV+
dV+ 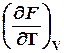 dT, (1.2)
dT, (1.2)
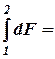 F2 – F1 = DF.(1.3)
F2 – F1 = DF.(1.3)
Изменение функции состояния не зависит от пути перехода, а определяется только начальным и конечным состоянием, DF – всегда разность между конечным (F2)и начальным (F1)состоянием.