Калорические коэффициенты
Внутренняя энергия системы U, будучи функцией состояния, является функцией независимых переменных (параметров состояния) системы.
В простейших системах будем рассматривать внутреннюю энергию как функцию двух переменных — объёма и температуры:
U = f (V, T) (I, 23)
Третья переменная (давление) в этом случае является зависимой переменной и однозначно определяется из уравнения состояния по значениям первых двух.
Тогда полный дифференциал dU будет равен:
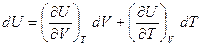 (1, 24)
(1, 24)
Подставив значение dU из уравнения (I, 24) в уравнение (I, 9), находим:
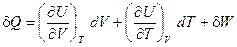 (I, 25)
(I, 25)
Если в изучаемой системе имеет место только работа расширения и отсутствуют работы электрическая, силы тяготения, поверхностных сил и т. д., то dW = PdV. Тогда
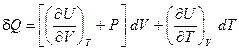 (I, 26)
(I, 26)
Обозначив коэффициенты при дифференциалах независимых переменных в уравнении (I, 26) символами l и CV , получим:
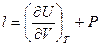 (I, 27)
(I, 27)
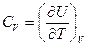 (I, 28)
(I, 28)
Тогда окончательно получим:
δQ = ldV + CVdT (1, 29)
Коэффициент l, размерность которого совпадает с размерностью давления, складывается из внешнего давления и члена 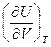 , который отражает взаимное притяжение молекул. Слагаемое
, который отражает взаимное притяжение молекул. Слагаемое 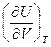 мало для реальных газов и очень велико (по сравнению с обычными значениями внешнего давления) для жидкостей и твёрдых тел.
мало для реальных газов и очень велико (по сравнению с обычными значениями внешнего давления) для жидкостей и твёрдых тел.
Для δQ запишем выражение, аналогичное (I, 24):
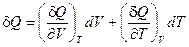 (I, 30)
(I, 30)
Т. к. в уравнениях (I, 26) и (I, 30) равны левые части, то равны и правые части:
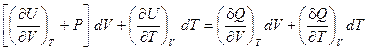
Поскольку V и T — независимые переменные, коэффициенты при соответствующих дифференциалах в правой и левой частях уравнения равны (так называемый метод сравнения коэффициентов). Следовательно:
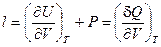 и
и 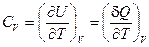
Нетрудно заметить, что CV есть не что иное, как теплоёмкость при постоянном объёме, что следует из определения (I, 16).
Коэффициент l характеризует теплоту изотермического расширения или, иначе говоря, он равен теплоте, необходимой для изменения объёма системы на единицу при T = const.
Выбрав в качестве независимых переменных P и Т, аналогично можно получить:
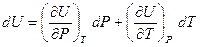
Тогда:
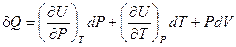 (I, 31)
(I, 31)
Чтобы избавиться от dV, объём также представим как функцию Р и Т:
V = f (P,T).
Тогда:
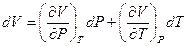 (I, 32)
(I, 32)
Подставив полученное выражение в (I,31), получим:
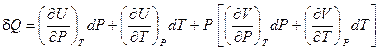
Раскрыв скобки и сгруппировав слагаемые, имеем:
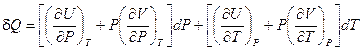 (I, 33)
(I, 33)
Введём обозначения, как мы уже делали ранее:
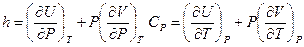 (I, 34)
(I, 34)
Тогда окончательно имеем:
dQ = hdP + CPdT (I, 35)
Уравнение, аналогичное (I, 30) запишется в следующем виде:
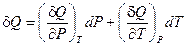
Сравнив его с уравнением (I, 33), получим:
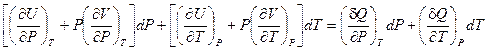
Поскольку P и T — независимые переменные, коэффициенты при соответствующих дифференциалах в правой и левой частях уравнения равны. Следовательно:
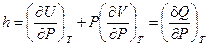 и
и 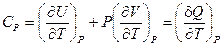 (I, 36)
(I, 36)
CP в соответствии с определением (I, 16) есть теплоёмкость при постоянном давлении.
Коэффициент h характеризует теплоту изотермического сжатия или, иначе говоря, он равен теплоте, необходимой для изменения давления системы на единицу при T = const.
Он является существенно отрицательной величиной.
Попробуем найти ответ на ещё один важный вопрос — о соотношении между CP и CV . Для этого используем уравнения (I, 29) и (I, 35).
δQ = ldV + CVdT
dQ = hdP + CPdT
Т. к. левые части этих уравнений равны, можно приравнять и их правые части:
ldV + CVdT = hdP + CPdT (I, 37)
Из трёх переменных P,V и T одна есть функция двух других. Рассматривая объём V как функцию P и T (мы уже делали это ранее): 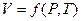 , используем выражение для полного дифференциала dV (I, 32). Тогда получим:
, используем выражение для полного дифференциала dV (I, 32). Тогда получим:
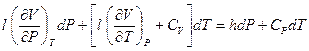
Так как P и T — независимые переменные, коэффициенты при соответствующих дифференциалах в правой и левой частях уравнения равны. Следовательно:
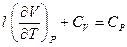 или
или 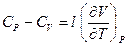 и
и 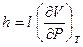 (I, 38)
(I, 38)
Следует отметить, что для конденсированных (твердых или жидких) фаз их объём очень мало зависит от температуры, следовательно, производная 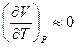 и разность CP – CV
и разность CP – CV 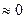 , поэтому изобарная и изохорная теплоёмкости в указанном случае практически равны CP ≈ CV .
, поэтому изобарная и изохорная теплоёмкости в указанном случае практически равны CP ≈ CV .
Коэффициенты l, h, CV, и CP называются калорическими коэффициентами. Имея самостоятельный физический смысл (особенно CP, CV и l), они являются также полезными вспомогательными величинами при термодинамических выводах и расчётах.