Зависимость теплового эффекта от температуры. Уравнение Кирхгофа.
По закону Гесса можно вычислить тепловой эффект реакции при той температуре, при которой известны теплоты образования или теплоты сгорания всех реагентов (обычно это 298К). Однако, часто возникает необходимость в том, чтобы знать тепловые эффекты реакций при различных температурах. Для вывода такой температурной зависимости воспользуемся уравнением
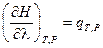
Если qT,P — тепловой эффект химической реакции, протекающей до конца (Dl = 1), при T = const и P = const, то тогда qT,P просто равен ΔН реакции (смотри (I, 68)):
ΔН = Н2 – Н1 = 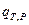
Здесь и в дальнейшем индекс «2» отнесён к продуктам реакции, а индекс «1» — к исходным веществам.
Запишем уравнение химической реакции в общем виде:
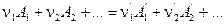
Через Hi обозначим энтальпию i-ого реагента, отнесённую к 1 моль вещества. Так как в результате одного пробега реакции исчезает 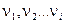 моль исходных веществ и появляется
моль исходных веществ и появляется 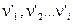 моль продуктов реакции, то общее изменение энтальпии в процессе будет:
моль продуктов реакции, то общее изменение энтальпии в процессе будет:
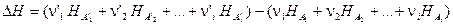
Продифференцируем это уравнение по температуре при P = const:
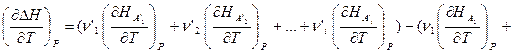
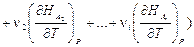
Если теперь ввести обозначения:
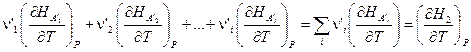
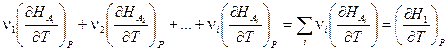
и принять во внимание, что 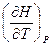 есть истинная теплоёмкость CP (смотри (I,63)), то тогда
есть истинная теплоёмкость CP (смотри (I,63)), то тогда
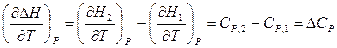
где 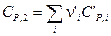 и
и 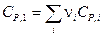
Или окончательно 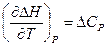
Как для идеальной системы, так и для реальных систем при невысоких давлениях частную производную от теплового эффекта по температуре можно заменить полной производной:
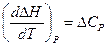 (I, 73)
(I, 73)
Это уравнение впервые было выведено Кирхгофом и называется его именем.
Из уравнения (I,73) получаем:
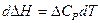
Интегрирование полученного соотношения от 0К до Т дает следующее выражение:
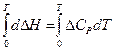 или
или
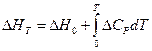 (I, 74)
(I, 74)
где DHT — тепловой эффект реакции при заданной температуре, а DH0 — константа интегрирования, которую иногда ошибочно называют тепловым эффектом реакции при абсолютно нуле. DH0 имела бы этот смысл, если бы при интегрировании (I, 73) использовалась функция, сохраняющая своё значение до температур, близких к абсолютному нулю. В большинстве же практических случаев при интегрировании используются зависимости теплоёмкостей, действительные для относительно высоких температур и совершенно непригодные в области абсолютного нуля.
В первом приближении можно считать, что 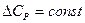 , тогда интегрирование
, тогда интегрирование
(I, 73) дает следующее выражение:
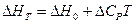
Если при интегрировании использовать температурную зависимость теплоемкостей в виде степенных рядов (смотри уравнение (I, 17)), то получим следующие более точные соотношения:
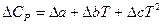
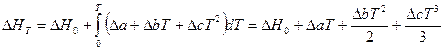 (I, 75),
(I, 75),
где
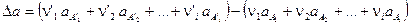
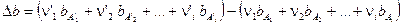
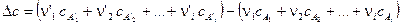
От трудностей, связанных с необходимостью вычисления константы интегрирования DH0, легко избавиться, если уравнение Кирхгофа проинтегрировать в интервале температур 298 ÷ Т :
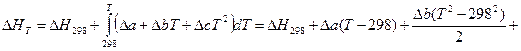
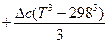 .
.
Тепловой эффект реакции при 298К DH298 может быть рассчитан с использованием четвертого или пятого следствий из закона Гесса.
Расчет тепловых эффектов по уравнению Кирхгофа с использованием температурных рядов для теплоёмкостей является относительно трудоемким. Вычисления значительно упрощаются, если использовать значения средних теплоёмкостей реагентов.
Если принять во внимание уравнение (I, 21), то можно записать:
 , тогда
, тогда
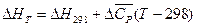 (I, 76)
(I, 76)
Разности DCP и 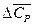 могут иметь как положительный, так и отрицательный знак. При этом изменение DHT с температурой определяется видом зависимости DCP (T) или
могут иметь как положительный, так и отрицательный знак. При этом изменение DHT с температурой определяется видом зависимости DCP (T) или 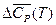 .
.