рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Оксиды и гидроксиды данного химического элемента.
Реферат Курсовая Конспект
Оксиды и гидроксиды данного химического элемента.
Оксиды и гидроксиды данного химического элемента. - раздел Химия, Химический элемент № 42, Мо 6.1. Запишите Ряд Оксидов Данного Химического Элемента (Прогноз По Электронно...
6.1. Запишите ряд оксидов данного химического элемента (прогноз по электронной формуле и ковалентности).
Для молибдена были идентифицированы оксиды с химической формулой МоО3, и МоО2. Ковалентность молибдена в оксидах равна 3 и 2. Кроме того, получены оксиды промежуточного между МоО3 и МоО2 состава: Мо8О23, Мо9О26, Мо4О11, Мо17О47. характер связи в оксидах в основном ионный, частично ковалентный.
МоО и Мо2О3 не выделены в свободном состоянии, хотя ранее в литературе и упоминалось о их выделении (8, ст. 162). Рентгенографически идентифицирована фаза, содержащая кислород в количестве, соответствующему составу Мо3О. оксид МоО2 более туго плавок и термодинамически устойчив чем оксид МоО3.
6.2. Прогнозируйте характер оксидов (основной, кислотный, амфотерный) по величине Э.О. и правилу химических свойств ряда оксидов.
Поскольку молибден относится к металлам, то его оксиды должны проявлять основные свойства. Но оксиды МоО3, и МоО2 проявляют не основные свойства, а кислотные. Они дают ряд соединений общей формулой Н2МоО4 и Н2МоО3. основные свойства проявляет оксид Мо2О3.
По химическим свойствам оксид проявляет тем более основные свойства, чем больше разница электроотрицательностей между элементом и кислородом. Электронегативность молибдена по Полингу равна 1,8 а кислорода 3,5. как видно разница электроотрицательностей элементов равна 3,5 – 1,8 = 1,7.
Основные свойства оксидов молибдена можно подтвердить их взаимодействием с растворами кислот и щелочей.
6.3. Запишите соответствующие гидроксиды (основания и кислоты). Определите принадлежность к сильным или слабым электролитам.
МоО3, и МоО2, как наиболее стойким оксидам молибдена, запишем формулы гидратов.
МоО3 характерен гидрат состава Н2МоО4 и Н2МоО4 ×Н2О. Н2МоО4 - белые мелкие кристаллы гексагональной формы. Дигидрат Н2МоО4 ×Н2О образуется при стоянии подкисленного раствора молибдатов в течении нескольких недель, а также при внесении затравки Н2МоО4 ×Н2О в сильно подкисленный раствор парамолибдата аммония. Н2МоО4 - молибденовая кислота, кислота средней силы, например, она более сильная чем угольная кислота и вытесняет ее из ее солей:
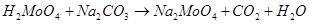
Гидраты окислов с валентностью металла между VI и IV получены в виде соединений МоО(ОН)3 и Мо(ОН)5. сила этих электролитов очень слабая, они малорастворимы в воде.
МоО2 характерен гидрат состава Н2МоО3, который в свободном состоянии не выделен, выделен только в растворах, также получены его соединения состава Ме2МоО3. слабый электролит.
Также при действии аммиака на растворы молибдатов получен Мо(ОН)3 - аморфный порошок черного цвета, не растворим в воде и растворах щелочей, легко растворяется в минеральных кислотах и при отсутствии окислителей дает ионы Мо+3.
6.4. Составьте уравнения реакций, подтверждающих характер гидроксидов о молекулярном и ионном виде.
Рассмотрим свойства Н2МоО4
Молибденовая кислота реагирует при повышенной температуре с оксидами, гидроксидами, карбонатами щелочных и щелочноземельных металлов давая соответствующие молибдаты.






Состояние молибденовой кислоты в растворах зависит от кислотности и разбавлености последних. При большом разбавлении (<10-4 моль/л, РН>6,5) молибденовая кислота находится в растворе в виде простых молекул. В более концентрированных растворах и при РН меньше шести: РН<6 происходит полимеризация молекул. Степень сложности образованных комплексов также зависит от температуры.
Рассмотрим свойства Мо(ОН)3
Сухой Мо(ОН)3 - это аморфный порошок, не растворимый в воде и растворах щелочей. Он проявляет основные свойства. Легко растворяется в растворах минеральных кислот, при этом образуются соли Мо3+.

6.5. Напишите уравнения реакций электролитической диссоциации гидроксидов.

7. Может ли данный химический элемент образовывать комплексные соединения? Если да, то, какие (кислоты, основания, соли)? Приведите примеры.
8. Напишите уравнения реакций гидролиза соли  по 1-ой стадии в молекулярном и ионном виде с учетом всех равновесий. Рассчитайте рН среды при гидролизе этой соли (0,01 моль/л). Как усилить гидролиз?
по 1-ой стадии в молекулярном и ионном виде с учетом всех равновесий. Рассчитайте рН среды при гидролизе этой соли (0,01 моль/л). Как усилить гидролиз?
Гидролиз солей молибдена (IІI) протекает ступенчато, в основном, по первой ступени.

Как видно из записи уравнения гидролиза  РН раствора будет кислым, поскольку будут синтезироваться ионы водорода.
РН раствора будет кислым, поскольку будут синтезироваться ионы водорода.
Для гидроксида молибдена  ПР =
ПР =  , поскольку он не растворим в воде.
, поскольку он не растворим в воде.


Тогда РН раствора при гидролизе будет равен:  . Но мы нашли концентрацию ионов водорода в растворе, поэтому:
. Но мы нашли концентрацию ионов водорода в растворе, поэтому:  .
.


В аналитической практике часто приходится встречаться с гидролизом солей. Гидролиз может способствовать выполнению реакции, а иногда мешает проведению анализа. Имеются следующие способы подавления и усиления гидролиза солей.
1. Прибавление к раствору соли другого электролита, кислоты или основания.
Для усиления гидролиза солей (в т.ч.  ) добавляют основания для связывания в процессе гидролиза ионов H+:
) добавляют основания для связывания в процессе гидролиза ионов H+:
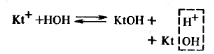

Равновесие реакции смещается в сторону гидролиза соли.
Для подавления гидролиза указанных солей к раствору добавляют кислоты, тогда:


В такой ситуации увеличивается количество ионов H+ и реакция смещается в обратную сторону, т.е. уменьшается гидролиз соли.
Для изменения гидролиза можно прибавлять и другие ионы электролитов: HCO3-, HPO42-, HSO4-. Для связывания OH- ионов используют их способность образовывать комплексные ионы: [Co(OH)]+, [Al(OH)]2+, [Al(OH)2]+ и др.
– Конец работы –
Эта тема принадлежит разделу:
Химический элемент № 42, Мо
ЗАДАНИЕ Электронное строение атома Дайте объяснение... Соединение данного химического элемента с неметаллами... С водородом...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Оксиды и гидроксиды данного химического элемента.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов