рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Растворимость газов в жидкостях
Реферат Курсовая Конспект
Растворимость газов в жидкостях
Растворимость газов в жидкостях - раздел Химия, Лекция № 5. Фазовые равновесия. Растворы неэлектролитов Растворимость Газов В Жидкостях Зависит От Ряда Факторов: Природы Газа И Жидк...
Растворимость газов в жидкостях зависит от ряда факторов: природы газа и жидкости, давления, температуры, концентрации растворенных в жидкости веществ (особенно сильно влияет на растворимость газов концентрация электролитов).
Наибольшее влияние на растворимость газов в жидкостях оказывает природа веществ. Так, в 1 литре воды при t = 18 °С и P = 1 атм. растворяется 0.017 л. азота, 748.8 л. аммиака или 427.8 л. хлороводорода. Аномально высокая растворимость газов в жидкостях обычно обусловливается их специфическим взаимодействием с растворителем – образованием химического соединения (для аммиака) или диссоциацией в растворе на ионы (для хлороводорода). Газы, молекулы которых неполярны, растворяются, как правило, лучше в неполярных жидкостях – и наоборот.
Поскольку растворимость характеризует истинное равновесие для определения влияния температуры и давления можно использовать принцип Ле-Шателье, влияние Т и р определяется знаком DН и DV.
Р-рение газов всегда сопровождается выделением теплоты (из-за сольватации молекул), поэтому при повышении температуры растворимость понижается.
При р-рении газов в жидкостях V уменьшается => повышение давления увеличивает растворимость (Зависимость растворимости газов от давления выражается законом Генри – Дальтона):
Растворимость газа в жидкости прямо пропорциональна его давлению над жидкостью.
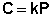 (III.7)
(III.7)
Здесь С – концентрация раствора газа в жидкости, k – коэффициент пропорциональности, зависящий от природы газа. Закон Генри – Дальтона справедлив только для разбавленных растворов при малых давлениях, когда газы можно считать идеальными. Газы, способные к специфическому взаимодействию с растворителем, данному закону не подчиняются.
Растворимость твердых веществ в жидкостях.
На растворимости твердых веществ давление значительно не сказывается (так как DV»0). Влияние становится ощутимым лишь при очень высоких давлениях. Например, лишь при давлении порядка 109 Па растворимость нитрата аммония в воде снижается (DVр > 0) почти вдвое.
Температура влияет на растворимость твердых веществ по-разному, что определяется, как сказано выше, знаком и величиной теплового эффекта растворения. Температурную зависимость растворимости твердых веществ часто выражают графически в виде кривых растворимости (рис. 2.23). Растворимость рубидия RbNO3 и хлората калия КClO3 при нагревании от 0 до 100 "С увеличивается в несколько раз (процесс растворения протекает с поглощением теплоты). Для кристаллогидрата сульфата иттербия Yb2(SO4)3*8Н20 теплота гидратации преобладает над теплотой разрушения кристаллической решетки и процесс растворения экзотермичен, поэтому растворимость его при повышении температуры снижается. У YCl3*7H2O растворимость не зависит от Т, т.к. у него практически нулевой эффект растворения.
Коллигативные свойства растворов (не зависят от природы, а только от количества вещества)
В результате образования раствора изменяются свойства не только растворенного вещества, но и растворителя. Для разбавленных растворов эти изменения м.б. разбиты на два типа: зависящие от природы растворенного вещества ( изменение цвета, объема) и от нее не зависящие. Во втором случае изменения свойств вызвано уменьшением концентрации молекул самого растворителя при распределении в нем другого вещества.
– Конец работы –
Эта тема принадлежит разделу:
Лекция № 5. Фазовые равновесия. Растворы неэлектролитов
Газообразное состояние вещества характеризуется слабым взаимодействием между частицами и большими расстояниями между ними Поэтому газы смешиваются... Общее давление газовой смеси равно сумме парциальных давлений всех входящих в...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Растворимость газов в жидкостях
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов