рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Тема: Типы химических реакций.
Реферат Курсовая Конспект
Тема: Типы химических реакций.
Тема: Типы химических реакций. - раздел Химия, Часть I Ключевые Слова И Словосочетания: Реакция; Химическа...
Ключевые слова и словосочетания:
Реакция; химическая реакция; процесс; образование связи; разрыв связи; степень окисления элемента; заряд иона; осадок; твердое вещество; газ; электронейтральный.
Прочитайте текст и выполните задания 1 и 2:
Текст:
Химические реакции – это процесс разрыва связей между атомами в исходных веществах и образование новых связей между атомами в продуктах реакции.
Различают такие типы химических реакций:
1) Реакции обмена – это реакции, которые идут без изменения степени окисления (заряда атома) элементов;
2) Окислительно-восстановительные реакции – это реакции, в результате которых степень окисления элементов меняется.
Реакции обмена сопровождаются образованием нового, более прочного соединения. Это осадок, газ или вода.
Например: а)  ;
;
б)  ;
;
газ
в) 
осадок
В этих реакциях степень окисления (заряд) элементов не меняется.
Степень окисления – это условный заряд атома элемента в молекуле. Условно считаем, что связь между атомами ионная.
Для определения степени окисления элемента в химическом соединении необходимо знать, что:
1) степень окисления водорода почти всегда +1. Степень окисления водорода может быть -1, если водород связан с металлами. Например,  ;
;  и др.;
и др.;
2) степень окисления атома кислорода почти всегда -2. Исключение – пероксиды типа  ,
, ,
,  . Здесь степень окисления кислорода -1;
. Здесь степень окисления кислорода -1;
3) атомы 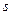 -элементов I группы в соединениях всегда имеют степень окисления +1, а
-элементов I группы в соединениях всегда имеют степень окисления +1, а 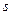 -элементы II группы – всегда +2;
-элементы II группы – всегда +2;
4) алюминий во всех соединениях имеет степень окисления +3;
5) фтор всегда имеет степень окисления -1; 0 0
6) в простых веществах степень окисления элементов равна0.(F2, Fe)
Остальные элементы могут иметь разные степени окисления и их надо уметь рассчитывать, помня правило:
- в молекуле сумма положительных зарядов должна быть равна сумме отрицательных зарядов, т.к. молекула электронейтральна.
- в ионе сумма положительных и отрицательных зарядов равна заряду иона.
Пример 1. Рассчитаем степень окисления атома азота в молекуле  . Для этого поставим известные степени окисления (ставят над символом химического элемента):
. Для этого поставим известные степени окисления (ставят над символом химического элемента):
 , так как в молекуле три атома кислорода, то сумма отрицательных зарядов равна
, так как в молекуле три атома кислорода, то сумма отрицательных зарядов равна  .Значит, положительных зарядов тоже должно быть 6. Один «+» у атома водорода, значит, у азота должен быть заряд +5. Проверка:
.Значит, положительных зарядов тоже должно быть 6. Один «+» у атома водорода, значит, у азота должен быть заряд +5. Проверка:

Пример 2: Рассчитаем степень окисления хрома и серы в соединении  . Это соль, которая состоит из катионов хрома и кислотного остатка серной кислоты
. Это соль, которая состоит из катионов хрома и кислотного остатка серной кислоты  .
.
В кислотном остатке сумма всех степеней окисления элементов равна заряду иона 2- .


 , т.е. степень окисления серы равна +6.
, т.е. степень окисления серы равна +6.
Так как кислотных остатков три, то их общий заряд равен  , следовательно, и положительных зарядов в молекуле соли тоже должно быть +6, т.к. атомов хрома два, то +6/2 = +3, т.е. степень окисления хрома равна +3.
, следовательно, и положительных зарядов в молекуле соли тоже должно быть +6, т.к. атомов хрома два, то +6/2 = +3, т.е. степень окисления хрома равна +3.
Задание 1.Рассчитайте степени окисления элементов в соединениях:
– Конец работы –
Эта тема принадлежит разделу:
Часть I
И НАУКИ УКРАИНЫ... КРИВОРОЖСКИЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ... Кафедра химии...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Тема: Типы химических реакций.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов