Понятие о скорости химических реакций
Скоростью химической реакции называется число элементарных актов реакции, происходящих в единицу времени в единице объема (в случае гомогенных реакций) или на единице поверхности раздела фаз (в случае гетерогенной реакции). Скорость реакции обычно характеризуются изменением концентрации какого-либо из исходных или конечных продуктов реакции в единицу времени и чаще всего выражают в моль/л · с.
Различают среднюю скорость химической реакции за данный промежуток времени и истинную скорость реакции в данный момент времени. Если в момент времени 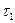 концентрация вещества была C1, а для момента
концентрация вещества была C1, а для момента 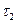 она стала C2, то средняя скорость реакции для интервала времени τ2 – τ1 будет равна
она стала C2, то средняя скорость реакции для интервала времени τ2 – τ1 будет равна
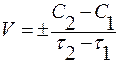
Знак минус пишут в том случае, если концентрация вещества во времени уменьшается (исходное вещество), а знак плюс – если концентрация увеличивается (продукт реакции). Скорость реакции всегда положительна. Истинная скорость в данный момент 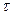 определяется пределом, к которому стремится выражение при ∆τ → 0, т.е. первой производной от концентрации по времени:
определяется пределом, к которому стремится выражение при ∆τ → 0, т.е. первой производной от концентрации по времени:
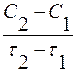
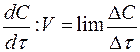
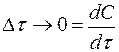
Измерить среднюю и истинную скорость химической реакции можно, найдя зависимость изменения концентрации реагирующих веществ в системе от времени.
Об изменении концентрации веществ в системе можно судить или непосредственно, или определяя какое-либо свойство реакционной системы. Это может быть вес осадка, образующегося в ходе реакции, объем реакционной системы, давление, цвет, электропроводность и т.п.
Скорость химических реакций зависит от многих факторов, основные из которых — концентрация (давление) реагентов, температура и действие катализатора. Эти же факторы определяют и достижение равновесия в реагирующей системе.