Озоновый защитный слой - раздел Химия, Предмет и задачи химии окружающей среды Как Известно, В Атмосфере На Высоте Около 15-25 Км (В Зависимости От Широты) ...
Как известно, в атмосфере на высоте около 15-25 км (в зависимости от широты) расположен озоновый защитный слой Земли, определяющий верхний предел жизни в биосфере. Озоновый слой появился вместе с появлением в земной атмосфере кислорода. Озона в атмосфере очень мало, всего 4*10-7 об. %. Если собрать весь озон атмосферы в один слой, то при нормальных условиях, т. е. при давлении 1 атм. и температуре 273оС он будет иметь толщину всего лишь 0,3 см. Однако этого количества вполне достаточно, чтобы говорить о защитных свойствах озонового слоя, поскольку озон обладает очень сильным поглощением. Он полностью поглощает всю энергию ультрафиолетовой радиации Солнца в полосе от 290 до 220 нм, что совершенно исключает попадание на поверхность Земли губительных для всего живого солнечных лучей короче 290 нм. Кроме того, озон поглощает также инфракрасное излучение Земли, препятствуя ее охлаждению. Определяя верхний предел жизни в биосфере, озоновый защитный слой естественно привлекает к себе особое внимание. Однако химия озона, особенно атмосферного, весьма сложна, и в ней еще многое остается неясным.
Синтез и разложение озона в атмосфере представляют собой сложный процесс, поскольку поведение самой атмосферы переменчиво. Так, облучение ее Солнцем периодически изменяется по суткам и по временам года.
Рассмотрим механизм образования озона в стратосфере. Расчеты по термодинамическим данным реакции 3О2 ↔ 2О3 (1.39)
I
показывают, что при низких температурах газ в основном состоит из молекулярного кислорода, а при высоких - из атомарного, и при давлении 1 атм. нет никакой области температур, где равновесное парциальное давление озона было бы сколько-нибудь существенным. Поэтому правомочен вопрос: каковы же причины наблюдаемых на опыте сравнительно больших концентраций озона? В yстановлении равновесия (1.39) большую роль играют реакция образования озона, из атомарного и молекулярного кислорода и обратная ей реакция бимолекулярного разложения продукта:
О2 + О + М ↔ О3 + М. (1.40)
Здесь М означает любую частицу, присутствующую в системе и необходимую для отвода энергии от образующейся молекулы озона.
При высоких температурах, когда содержание атомарного кислорода велико, равновесие реакции (1.39) сильно сдвинуто влево и образования озона не происходит. При низких же температурах, когда равновесие по реакции (1.39) сдвинуто вправо, парциальное давление атомарного кислорода слишком низкое, что также препятствует образованию озона. Для получения значительных концентраций озона необходимо сочетание двух условий: сравнительно низкой температуры, обеспечивающей достаточный сдвиг равновесия в сторону образования озона, и больших концентраций атомарного кислорода. Выполнение этих условий возможно, когда диссоциация молекул кислорода обеспечивается в результате нетермического воздействия на систему, например за счет облучения или потока быстрых частиц. Для получения представлений о механизме образования атмосферного озонав первомприближении условимся, что в расчет берется только кислород. Кроме того, кислород и озон под влиянием коротковолнового излучения Солнца подвергаются диссоциации на атомы, которые могут вновь соединяться, образуя кислород и озон. В то же время озон может снова разлагаться и под влиянием более длинноволнового облучения. Есть еще и другие причины, осложняющие процесс, в частности наличие в атмосфере, кроме кислорода, азота и других газов. Диссоциация или ионизация молекул азота приведут к образованию атомов или ионов азота, которые могут соединяться с другими различными атомами. То же происходит и с другими газами, которые содержатся в воздухе в виде примесей. Все эти процессы могут происходить во время облучения воздуха солнечным светом и будут идти с разной скоростью, зависящей от интенсивности света. Ночью, когда атмосфера будет находиться в тени Земли, все процессы идут в обратном направлении или затормаживаются вплоть до полного прекращения. На их течение влияет также высота над уровнем моря. Все это происходит постоянно, и потому ни равновесие, ни стационарное состояние не достигаются. Тем не менее при некоторых упрощениях можно получить определенное представление о механизме образования озона в атмосфере и об условиях равновесия образования и разложения озона.
В атмосфере на больших высотах концентрация озона с увеличением высоты должна убывать из-за уменьшения концентрации третьих частиц (М) и кислорода. С уменьшением высоты она должна убывать за счет снижения интенсивности облучения. Расчет показывает, что концентрация озона должна быть максимальной на высоте 25-30 км.
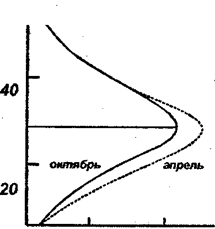
В атмосфере существует распределение озона по времени, широте и высоте. В соответствии с суточными колебаниями послеобеденное содержание озона больше утреннего. Максимального значения содержание озона достигает весной, а осенью падает до минимума. В полярных широтах озона содержится в два раза больше, чем у экватора. Наибольшего внимания заслуживает вертикальное распределение озона. На рис. 8 видно, что концентрация озона проходит через максимум на высоте 25 км. С повышением широты высота озонового слоя падает с 25 км до 13 км
h,км
СН3
0,01 0,02 С,см3/км3
Рис. 8. Схема вертикального распределения озона
Постоянно возникающий и разрушающийся слой озона обусловливает явление, названное «озоновым дождем». Как уже отмечалось, атомарный кислород образуется на больших высотах благодаря коротковолновому излучению. Процесс его образования распространяется вниз до 25 км высоты. На этой высоте атмосферное давление обеспечивает достаточное парциальное давление молекулярного кислорода для начала реакции образования сравнительно тяжелых молекул озона:
О2 + О + М ↔ О3 + М.
На более низких высотах благодаря уменьшению высокочастотного облучения и сохранению длинноволнового начинается обратный процесс - все большее разложение озона. Образующиеся при этом молекулярный и атомарный кислород, будучи легче озона, поднимаются вверх. Таким образом, существует постоянный поток озона вниз, как бы «дождь» озона. Можно считать, что от этого потока из стратосферы в тропосферу зависит годовое изменение содержания озона. Так как за период с октября по апрель солнечная радиация слабее, чем с апреля по октябрь, содержание озона в весенне-летний период заметно уменьшается. Так же можно объяснить и сезонное содержание озона в зависимости от широты. В тропосфере, в земном слое содержится лишь 10% от общего атмосферного озона. Повышенное содержание озона отмечается на берегах морей и над лесами.
Озон имеет многочисленные, полосы поглощения, простирающиеся от длинноволновой инфракрасной до коротковолновой ультрафиолетовойобласти. Спектрпоглощения озона вультрафиолетовойобласти, как видно из рис. 9, хорошо коррелирует со спектрами поглощения нуклеиновых кислот и белка.

'230 250 270 290 310 λ, нм
Рис. 9. Спектры поглощения озона (1); нуклеиновых кислот (2) и белков (3) в ультрафиолетовой области
По своему биологическому действию солнечное излучение, достигающее поверхности Земли, обычно делится на более активное, с λ= 280 - 315 нм, называемое УФ - А, и менее активное, с λ= 315 - 400 нм, называемое УФ - В. Количество ультрафиолетового излучения зависит от многих физико-химических, метеорологических, геофизических и других условий. В частности, оно зависит от широты местности, высоты над уровнем моря, прозрачности атмосферы и т. д. Годовая доза УФ - А изменяется на порядок при переходе от Арктики (360 Вт • ч/м2) к тропикам (3600 Вт • ч/м2). В небольших дозах ультрафиолетовое облучение сказывается благоприятно на человеке, животных и растительности, в частности способствует выработке в организме человека, животных и птиц витамина D3, регулирующего процесс кальциевого обмена. Совершенно противоположно действие повышенных или больших доз УФ. Под их влиянием происходит распад важнейших частей клетки. В ней возникают вещества, блокирующие процессы воспроизводства ДНК и синтеза РНК. У человека высокие дозы УФ-облучения вызывают сильные ожоги и раковые заболевания. Отмечается также отрицательное влияние повышенных доз УФ на растительный мир.
Поглощение озоном коротковолнового ультрафиолетового излучения, корреляция его с поглощением белка и нуклеиновых кислот предопределяют защитные функции озонового слоя для всего живого на земле.
Все темы данного раздела:
Предмет и задачи химии окружающей среды
Проблема охраны окружающей среды сложна и многопланова. Она включает не только чисто научные аспекты, но и экономические, социальные, политические, правовые, эстетические.
В основе процесс
Происхождение и эволюция Земли
Принято считать, что Вселенная возникла в один момент в результате огромного взрыва, обычно называемого Большим взрывом. Планеты нашей Солнечной системы образовались, по-видимому, из облака
Образование земной коры и атмосферы
Земная кора, гидросфера и атмосфера образовались в основном результате высвобождения веществ из верхней мантии молодой Земли. За счет этих процессов сформировалась оболочка из породы толщиной менее
Эволюция атмосферы и происхождение жизни
Аккреция вещества Земли привела к временному его разогреву и легких молекул первичной атмосферы, прежде всего водорода и гелия, рассеянных в космическом пространстве. Последующее понижение
Гидросфера
Вода - ключевой компонент в поддержании жизни на Земле. Вода в своих трех состояниях - жидкость, лед и водяные пары широко распространена на поверхности Земли и занимает объем 1,4 млрд. кмЗ
Состав атмосферы
Общий состав атмосферы почти одинаков по всей Земле в результате высокой степени перемешивания в пределах атмосферы. В горизонтальном направлении перемешивание осуществляется благодаря вращению Зем
Микрокомпонентные примеси в атмосфере
Многие микрокомпонентные примеси в атмосфере имеют постоянные концентрации, тo есть существует баланс между поступлением и выходом вещества в атмосферу
Fвх = Fвы
Геохимические источники
Самыми мощными геохимическими источниками служат переносимая ветром пыль и морские брызги, поставляющие огромные количества твердых веществ в атмосферу. Пыль — это в основном почва регионов Земли.
Биологические источники.
В отличие от геологических источников биологические не являются крупным прямым источником поступления частиц в атмосферу, за исключением лесных пожаров (лесные пожары служат значительным источнико
Антропогенные источники
Антропогенные факторы предопределяют существенные изменения в нормальном функционировании атмосферы, причем как в самых нижних, так и в высотных ее частях. Изменения, вызванные человеком, значител
Радиоактивное загрязнение атмосферы
К опасным, факторам антропогенного характера, способствующим серьезному ухудшению качества атмосферы, следует отнести радиоактивность.
Радиоактивностью называется, самопро
Основные радиоактивные изотопы, обнаруживаемые в атмосфере после ядерного взрыва
Изотоп
8938Sr
9038Sr
9540Zr
13153I
Механизмы разрушения озона
Выше рассматривался механизм образования озона в атмосфере только на основе кислорода как компонента воздуха. Между тем в образовании и разрушении озона атмосферы играют существенную роль и другие
Состав и строение литосферы
Сейсмические исследования свидетельствуют о том, что при землетрясениях возникают различные сейсмические волны, распространяющиеся в породах Земли с разными скоростями. Наиболее быстрые из них - пе
Процессы выветривания
Поверхность земной коры подвержена действию атмосферы, что делает ее восприимчивой к физическим и химическим процессам.
Физическое выветривание является механическим проце
Общие для большинства почв реакции
При характеристике почв наиболее информативны не отдельные индивидуальные соединения, а их группы, то есть совокупность соединений со сходными строениями и свойствами. Такими группами могут быть мо
Катионный обмен
Для почв наиболее характерны реакции катионного обмена между твердой частью почвы, которая поглощает катионы, и почвенным раствором, который можно рассматривать как раствор электролитов. Если твёрд
Потенциальная кислотность почв
Обменные катионы участвуют также в формировании потенциальной кислотности почв. Такая кислотность встречается в кислых дерново-подзолистых, серых лесных, красноземных почвах. Проявляется о
Щелочность почв
Щелочными считают почвы, водная суспензия которых имеет рН 7,5 — 8,0 или выше. Эти почвы формируются в степных и сухо-степных природных зонах; к ним относятся солонцы, некоторые солончаки. Щелочно
Окислительно-восстановительные режимы
Практически в каждой почве происходят реакции окисления или восстановления химических соединений или элементов. Эти реакции являются сопряженными, и если какой-либо компонент почвы окисляется, то
Гумификация
Это один из самых важных почвенных биохимических процессов. Сущность его заключается в трансформации растительных остатков в своеобразные, темноокрашенные органические гуминовые вещества преимуще
Химическое загрязнение и охрана почв
В последние десятилетия человек стал причиной быстрой деградации почв, хотя потери почв имели место на протяжении всей человеческой истории. Во всех странах мира сейчас распахивают около 1,5 млрд.
Пресные воды подземной гидросферы
Существенную роль в процессах биосферы играет и так называемая подземная гидросфера. Пресные воды после ледников вносят основной вклад в общий баланс пресной воды на планете. Обширные запасы
Химия пресных поверхностных вод
Озера. Озера— это водоемы, не имеющие прямой связи с системой Мирового океана. Они распространены на равнинных и горных территориях, во влажных и засушливых, холодных и жарких ги
Химия воды и режимы выветривания
Состав растворенных ионов в пресных водах зависит от: варьирующего состава дождевых осадков и сухих атмосферных выпадений; изменений в поступлениях в атмосферу вследствие эвапотранспирации; варьи
Растворенные твердые вещества пресных вод
Кремний высвобождается при выветривании силикатов и переносится в природных водах в виде недиссоциированной кремниевой кислоты H4SiО4. Силикаты выветриваются медленно, поэто
Биологические процессы
В ручьях и небольших реках биологическая активность в воде слабо влияет на ее химический состав из-за быстрого течения. В крупных же реках и озерах, со слабым течением основные изменения в химическ
Диаграммы Eh-pH
Кислотность (рН) и окислительно-восстановительный потенциал (Eh) могут определять поведение элементов и их соединений в окружающей среде. Теоретически возможно бесконечное разнообразие сочетаний
Питательные вещества и эвтрофикация
Кроме СO2, воды и света растениям для роста нужны определенные ионы (питательные вещества). Некоторых из этих ионов, на пример Mg2+ , довольно много в пресной воде, однако др
Кислотные осадки
Кислотными называют атмосферные осадки (дождь, снег, роса) с рН<5,5. Естественная дождевая вода имеет слабокислую реакцию (рН=б), так как находится в контакте с СО2 и растворяет ее, о
Процессы в дельтах и эстуариях
Очень интересна химия морской воды вблизи континентальных областей — в переходной зоне между средами обитания суши и открытого океана.
Дельта - устьевая часть реки, в которой происходит р
Изменения веществ в окружающем среде
Для целостного понимания биосферы как глобальной системы важно изучение как природных, так и антропогенных процессов, происходящих в ней.
Для предсказания того, как эта система может измен
Изменения во времени
Естественные (природные) изменения. Изменения геохимических, геофизических и метеорологических параметров за геологические периоды времени, эволюция живых организмов, обитающих в воде и н
Пространственные изменения
Критериями оценки природных и антропогенных веществ по степени их воздействия на изменение окружающей среды являются их количество, объем запасов, частота появления и распространенность. Учет изме
Распространение в окружающей среде
Оценка распространения в окружающей среде синтезированных человеком веществ включает физико-химические свойства этих веществ, физические процессы, связанные с их переносом, биологические п
Перенос между различными средами
Рис. 19. Схема процессов переноса вещества между различными средам
Перенос почва — вода
Перенос веществ на границе раздела почва — вода играет важную роль в процессе загрязнения вод в результате применения химических препаратов или их поступления в почву с дождем, в результате искус
Перенос вода — воздух
Переход вещества в природных условиях из водного раствора в атмосферу называют летучестью; этот процесс осуществляется в результате диффузии, обратный перенос называют сухим осаждением в воду.
Перенос почва -—воздух
В миграционных процессах между почвой и воздухом большое значение имеют обменные процессы жидкость/твердая фаза, жидкость/газ и твердая фаза/газ.
Переход вещества из почвы в атмосферу пут
Поступление и накопление в живых организмах
В принципе любое химическое вещество поглощается и усваивается живыми организмами. Равновесное состояние или состояние насыщения в процессе усвоения достигается в том случае, если его поступлени
Сравнение содержания химических элементов в морской воде и теле рачка Calanus finmarchicue
Химические элементы
Морская вода,
масс,%
Calanus finmarchicus, масс.%
Коэффициент обогащения
Кислород
Географический и биотический перенос
После того как произошло распределение поступивших в окружающую среду химических веществ между воздухом, водой и почвой, необходимо проследитьих дальнейшую миграцию на более или менее далекие рас
Геохимические барьеры
Участки биосферы, на которых в миграционном потоке на коротком расстоянии резко уменьшается интенсивность миграции химических элементов, и как следствие этого процесса, повышается их концентрация
Круговороты макроэлементов
Солнечная энергия обеспечивает на Земле два круговорота веществ: большой, или геологический (абиотический) и малый, или биологический (биотический). Большой круговорот наиболее четко проявляется в
Вещества, попавшие в окружающую среду исключительно в результате.человеческой деятельности
ДДТ(2,2-ди (р-хлорфенил) - 1,1,1 -трихлорэтан)
Пестицид
Неселективный ряд, концентрируется в пищевой цепи
ПХД (полихлориро-ванные
Углерод
Самым важным компонентом природного цикла углерода является газообразный диоксид углерода СО2. Сейчас запасы углерода в атмосфере в виде СО2 относительно невелики в сравнении
АТМОСФЕРА
СО2
Круговороты второстепенных элементов
Микроэлементы, как и макроэлементы, мигрируют между организмами и средой. Многие из них концентрируются в тканях благодаря химическому сходству с какими-либо важными биогенными элементами, что мо
Соединения хлора
Химия соединений хлора в биосфере сравнительно проста. Практически все встречающиеся в почвах хлориды легко растворимы: NaCl, KC1, СаСl2, MgCl2. Растворимы также хлориды боль
Соединения йода
Содержание йода в земной коре колеблется от 0,01 до 6 мг/ кг, достигая максимума в обогащенных органическим веществом сланцах. Минеральные соединения йода легкорастворимы, поэтому йод энергично вы
Соединения брома
Содержание брома в земной коре колеблется от 0,2 до 10 мг/кг, причем максимальные концентрации характерны для глинистых отложений. Бром — сильнолетучий элемент, его соли легкорастворимые. К числу
Соединения фтора
Свойства соединений фтора значительно отличаются от свойств других галогенопроизводных.
Фториды щелочных металлов растворимы в воде и их растворимость уменьшается в ряду KF > NaF >
Тяжелые металлы
Металлы в очень высокой степени вовлечены в антропогенную деятельность, они отличаются настолько высокой технофильностью, что нередко говорят о современной «металлизации» биосферы. Особое значение
Атмосфера
Общий запас 15,6*109 г
Стронций
Sr -хороший пример ранее малоизученного элемента, который теперь служит объектом особого внимания в связи с большой опасностью его радиоактивного изотопа для человека и животных. По свойствам стро








Новости и инфо для студентов