Окислители и восстановители - раздел Химия, Химия. Полный справочник для подготовки к ЕГЭ
Окислительно‑восстановительные Реакции П...
Окислительно‑восстановительные реакции протекают с одновременным повышением и понижением степеней окисления элементов и сопровождаются передачей электронов:
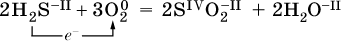
Повышение степени окисления элемента в ходе реакции, отвечающее потере электронов атомами этого элемента, называют окислением : S‑II – 6е‑ = SIV. В данном примере S‑II окисляется до SIV.
Понижение степени окисления элемента в ходе реакции, отвечающее присоединению электронов атомами этого элемента, называется восстановлением : O0 + 2е‑ = О‑II. В данном примере О0 восстанавливается до O‑II.
Вещество, частицы которого содержат окисляющиеся атомы, выполняет в реакции функцию восстановителя. В данном примере восстановитель – сероводород H2S.
Вещество, частицы которого содержат восстанавливающиеся атомы, выполняет в реакции функцию окислителя. В данном примере окислитель – молекулярный кислород O2.
Вещества, являющиеся окислителями или восстановителями во многих реакциях, называются типичными (сильными).
Многие вещества могут проявлять как окислительные, так и восстановительные свойства. К таким веществам принадлежат соединения, содержащие элементы в промежуточной (для них) степени окисления:
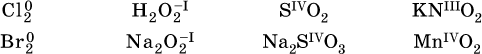
Окислительно‑восстановительные свойства веществ связаны с положением элементов в Периодической системе Д. И. Менделеева. Простые вещества – неметаллы обладают бóльшими окислительными свойствами, а металлы – бóльшими восстановительными свойствами (O2, Cl2 – окислители; Na, Ва, Al и Zn – восстановители).
В каждой группе Периодической системы элемент с большим порядковым номером будет обладать и бóльшими восстановительными свойствами в своей группе, а элемент с меньшим порядковым номером – бóльшими окислительными свойствами. Так, кальций Са – более сильный восстановитель, чем магний Mg, молекулярный хлор Cl2 – более сильный окислитель, чем иод I2.
Соединения, содержащие атомы элементов в низкой степени окисления, будут восстановителями за счет этих атомов, например: NH3 – восстановитель за счет азота (‑III), H2S – за счет серы (‑II), KI – за счет иода (‑I) и т. д.
Соединения, включающие атомы элементов в высокой степени окисления, будут окислителями , например: HNO3 – окислитель за счет азота (+V), КMnO4 – за счет марганца (+VII), К2Cr2O7 – за счет хрома (+VI) и т. д.
Все темы данного раздела:
Распространенные элементы. строение атомов. Электронные оболочки. Орбитали
Химический элемент – определенный вид атомов, обозначаемый названием и символом и характеризуемый порядковым номером и относительной атомной массой.
В табл. 1 перечи
В каждой орбитали может разместиться не более двух электронов.
Один электрон на орбитали называется неспаренным, два электрона – электронной парой:
Свойства элементов находятся в периодической зависимости от порядкового номера.
Периодически повторяющийся характер изменения состава электронной оболочки атомов элементов объясняет периодическое изменение свойств элементов при движении по периодам и группам Пе
Молекулы. Химическая связь. Строение веществ
Химические частицы, образованные из двух или нескольких атомов, называются молекулами (реальными или условными формульными единицами многоатомных веществ). Атомы в мол
Кальций
Кальций – элемент 4‑го периода и IIA‑группы Периодической системы, порядковый номер 2O. Электронная формула атома [18Ar]4s2, степени окислен
Алюминий
Алюминий – элемент 3‑го периода и IIIA‑группы Периодической системы, порядковый номер 13. Электронная формула атома [10Ne]3s23p1,
Марганец
Марганец – элемент 4‑го периода и VIIB‑группы Периодической системы, порядковый номер 25. Электронная формула атома [18Ar]3d54s2;
Общие свойства металлов. Коррозия
Элементы с металлическими свойствами расположены вIA – VIA группах Периодической системы (табл. 7).
Водород
Водород – первый элемент Периодической системы (1‑й период, порядковый номер 1). Не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к како
Хлор. Хлороводород
Хлор – элемент 3‑го периода и VII А‑группы Периодической системы, порядковый номер 17. Электронная формула атома [10Ne]3s23p5, ха
Хлориды
Хлорид натрия NaCl. Бескислородная соль. Бытовое название поваренная соль. Белый, слабогигроскопичный. Плавится и кипит без разложения. Умеренно раствори
Гипохлориты. Хлораты
Гипохлорит кальция Са(СlO)2. Соль хлорноватистой кислоты HClO. Белый, при нагревании разлагается без плавления. Хорошо растворим в холодной воде (обр
Бромиды. Иодиды
Бромид калия КBr. Бескислородная соль. Белый, негигроскопичный, плавится без разложения. Хорошо растворим в воде, гидролиза нет. Восстановитель (более слабый, ч
Кислород
Кислород – элемент 2‑го периода и VIA‑группы Периодической системы, порядковый номер 8, относится к халькогенам (но чаще рассматривается отдельно). Электронная фо
Сера. Сероводород. Сульфиды
Сера – элемент 3‑го периода и VIA‑группы Периодической системы, порядковый номер 16, относится к халькогенам. Электронная формула атома [10Ne]3s
Диоксид серы. Сульфиты
Диоксид серы SO2. Кислотный оксид. Бесцветный газ с резким запахом. Молекула имеет строение незавершенного треугольника [: S(O)2] (sр
Серная кислота. Сульфаты
Серная кислота H2SO4. Оксокислота. Бесцветная жидкость, очень вязкая (маслообразная), весьма гигроскопичная. Молек
Азот. Аммиак
Азот – элемент 2‑го периода и VA‑группы Периодической системы, порядковый номер 7. Электронная формула атома [2He]2s22p3, характе
Оксиды азота. Азотная кислота
Монооксид азота NO. Несолеобразующий оксид. Бесцветный газ. Радикал, содержит ковалентную σπ‑связь ( N=O), в твердом состоянии димер N2
Нитриты. Нитраты
Нитрит калияKNO2. Оксосоль. Белый, гигроскопичный. Плавится без разложения. Устойчив в сухом воздухе. Очень хорошо растворим в воде (образуется бесцв
Углерод в свободном виде
Углерод – элемент 2‑го периода и IVA‑группы Периодической системы, порядковый номер 6. Химия углерода – это в основном химия органических соединений; неорганическ
Оксиды углерода
Монооксид углерода СО. Несолеобразующий оксид. Бесцветный газ, без запаха, легче воздуха. Молекула слабополярна, содержит ковалентную тройную σππ
Карбонаты
Карбонат натрия Na2CO3. Оксосоль. Техническое название кальцинированная сода. Белый, при нагревании плавится и разлагается. Чувстви
Кремний
Кремний – элемент 3‑го периода и IVA‑группы Периодической системы, порядковый номер 14. Электронная формула атома [10Ne]3s23p2. Х
Алканы. Циклоалканы
Алканы (парафины ) – это соединения углерода с водородом, в молекулах которых атомы углерода соединены между собой одинарной связью (предельные углеводоро
Алкены. Алкадиены
Алкены (олефины ) – это углеводороды, в молекулах которых содержатся атомы углерода, соединенные между собой двойной связью (непредельные углеводороды ряд
Спирты. Простые эфиры. Фенолы
Спирты – производные углеводородов, содержащие функциональную группу ОН (гидроксил). Спирты, в которых имеется одна группа ОН, называются одноат
Альдегиды и кетоны
Альдегиды и кетоны – это производные углеводородов, содержащие функциональную карбонильную группу СО . В альдегидах карбонильная группа связана с а
Карбоновые кислоты. Сложные эфиры. Жиры
Карбоновые кислоты – это производные углеводородов, содержащие функциональную группу СООН (карбоксил).
Формулы и названия некоторых распространенных ка
Углеводы
Углеводы (сахара ) – важнейшие природные соединения, состоящие из углерода, водорода и кислорода. Углеводы подразделяются на моносахариды, дисахариды и полис
Нитросоединения. Амины
Очень важны в народном хозяйстве азотсодержащие органические вещества. Азот может входить в органические соединения в виде нитрогруппы NO2, аминогруппы NH2 и а
Аминокислоты. Белки
Аминокислоты – органические соединения, содержащие в своем составе две функциональные группы – кислотную СООН и аминную NH2
Скорость реакций
Количественной характеристикой быстроты течения химической реакции А + B → D + E является ее скорость, т. е. скорость взаимодействия частиц реагентов А
Скорость химической реакции прямо пропорциональна произведению молярных концентраций реагентов
если для реакции необходимо столкновение двух реагирующих молекул. Эта зависимость носит название кинетического закона действующих масс (К. Гулльберг, П. Вог
Энергетика реакций
Любая реакция сопровождается выделением или поглощением энергии в форме теплоты. В исходных веществах химические связи разрываются, и на это энергия затрачивается (т. е. она при это
Обратимость реакций
Химическая реакция называется обратимой, если в данных условиях протекает не только прямая реакция (→), но также и обратная реакция т. е. из исходных веществ образуются
При воздействии на равновесную систему химическое равновесие смещается в сторону, противодействующую этому воздействию.
Рассмотрим подробнее влияние таких факторов, как температура, давление, концентрация, на смещение равновесия.
1. Температура. Повышение температуры сме
Растворимость веществ в воде
Раствор – это гомогенная система, состоящая из двух или более веществ, содержание которых можно изменять в определенных пределах без нарушения однородности.
Электролитическая диссоциация
Растворение любого вещества в воде сопровождается образованием гидратов. Если при этом в растворе не происходит формульных изменений у частиц растворенного вещества, то такие вещест
Диссоциация воды. Среда растворов
Сама вода – это очень слабый электролит:
Реакции ионного обмена
В разбавленных растворах электролитов (кислот, оснований, солей) химические реакции протекают обычно при участии ионов . При этом все элементы реагентов могут сохра
Гидролиз солей
Гидролиз соли – это взаимодействие ее ионов с водой, приводящее к появлению кислотной или щелочной среды, но не сопровождающееся образованием осадка или газа (ниже
Подбор коэффициентов методом электронного баланса
Метод состоит из нескольких этапов.
1. Записывают схему реакции; находят элементы , повышающие и понижающие свои степени окисления, и выпи
Ряд напряжений металлов
В ряду напряжений металлов стрелка отвечает уменьшению восстановительной способности металлов и увеличению окислительной способности их катионов в водном растворе (кислотная среда):
Электролиз расплава и раствора
Электролизом называется окислительно‑восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через растворы или
Массовая доля растворенного вещества. Разбавление, концентрирование и смешивание растворов
Массовая доля растворенного вещества В
(ω в) – это отношение массы вещества В (т в) к массе раствора (m (р)
Объемное отношение газов
Для химической реакции a A + b B = c C + d D выполняется соотношение
Масса (объем, количество вещества) продукта по реагенту в избытке или с примесями
Избыток и недостаток реагентов. Количества, массы и объемы (для газов) реагентов не всегда берутся стехиометрическими, т. е. в соответствии с уравнениями реакции. Ч
Нахождение молекулярной формулы органического соединения
При выведении формул веществ, особенно в органической химии, часто используют относительную плотность газа.
Относительная плотность газа X – отношение абсолютной пло
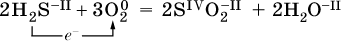
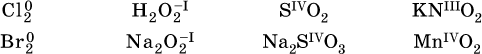







Новости и инфо для студентов