В зависимости от pH раствора
| Название | Окраска индикатора в среде | ||
| Кислая [H+] > [OH-] рН < 7 | Нейтральная [H+] = [OH-] рН = 7 | Щелочная [OH-] > [H+] рН > 7 | |
| Лакмус | красный | фиолетовый | синий |
| Фенолфталеин | бесцветный | бесцветный | малиновый |
| Метилоранж | розовый | оранжевый | желтый |
Для более точного определения значения pH растворов используют сложную смесь нескольких индикаторов, нанесенную на фильтровальную бумагу (так называемый "Универсальный индикатор Кольтгоффа"). Полоску индикаторной бумаги обмакивают в исследуемый раствор, кладут на белую непромокаемую подложку и быстро сравнивают окраску полоски с эталонной шкалой для pH.
2. Электрохимический метод. Этот метод позволяет более точно определять значение рН среды. Он основан на измерении разности потенциалов двух электродов, помещенных в анализируемый раствор. Один из этих электродов – электрод сравнения – в процессе измерения имеет более постоянный потенциал, а потенциал второго электрода (обычно стеклянного) зависит от величины 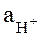 в анализируемом растворе. Потенциал стеклянного электрода относительно электрода сравнения измеряется рН-метром, показывающая шкала которого градуирована в единицах рН и позволяет производить непосредственный отсчет измеряемой величины. Электрохимический метод определения водородного показателя называют еще методом рН-метрии.
в анализируемом растворе. Потенциал стеклянного электрода относительно электрода сравнения измеряется рН-метром, показывающая шкала которого градуирована в единицах рН и позволяет производить непосредственный отсчет измеряемой величины. Электрохимический метод определения водородного показателя называют еще методом рН-метрии.
Гидролиз солей.
Гидролиз - это химическая реакция ионного обмена между водой и растворённым в ней веществом с образованием слабого электролита. В большинстве случаев гидролиз сопровождается изменением pH раствора.
Большинство реакций гидролиза - обратимы
Pb(NO3)2 + H2O « Pb(OH)(NO3) + HNO3