РАСЧЕТ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА ЦИНКА.
1. Приводим объем выделившегося водорода к нормальным условиям (V он.у.) по уравнению Бойля-Мариотта и Гей-Люссака
 Þ V0(H2) =
Þ V0(H2) = 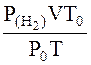
где  - давление водорода, кПа; То – абсолютная температура, 273 К; Ро – давление при н.у., кПа (760 мм рт.ст. = 101,325 кПа); Т – комнатная температура, К.
- давление водорода, кПа; То – абсолютная температура, 273 К; Ро – давление при н.у., кПа (760 мм рт.ст. = 101,325 кПа); Т – комнатная температура, К.
2. Рассчитываем массу выделившегося водорода для V0(H2), с точностью до четвертого знака после запятой:
1 моль H2 2г - 22,4 л
m (H2) - V0 (H2), л
3. Вычисляем молярную массу эквивалента цинка по закону эквивалентов двумя способами
I способ расчета: 

 ,
,
II способ расчета: 
где 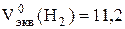 дм3 – объем 1 моль-эквивалента H2 при н. у.
дм3 – объем 1 моль-эквивалента H2 при н. у.
4. Рассчитываем теоретическое значение молярной массы эквивалента цинка
Мэ(Zn)теор. =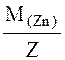 ,
,
где Z – валентность цинка, М(Zn) – молярная масса атома цинка.
5. Расчет погрешности опыта в процентах
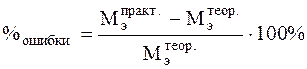
6. Вывод и анализ ошибки.
Лабораторная работа №2