рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Влияние температуры на скорость химических реакций.
Реферат Курсовая Конспект
Влияние температуры на скорость химических реакций.
Влияние температуры на скорость химических реакций. - раздел Химия, Кинетика, катализ, химическое равновесие Закон Вант-Гоффа При Повышении T На Каждые 10О Ско...
Закон Вант-Гоффа
При повышении t на каждые 10о скорость химической реакции увеличивается в 2-4 раза.

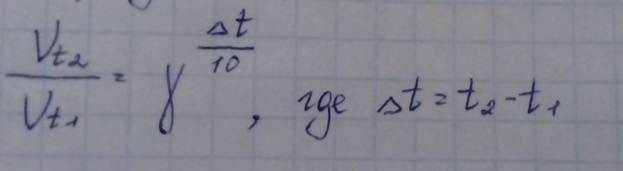 Энергия активации – та минимальная дополнительная энергия, которую необходимо собирать, молекулам сверх среднего ее значения.
Энергия активации – та минимальная дополнительная энергия, которую необходимо собирать, молекулам сверх среднего ее значения.
Уравнение Аррениуса:
 Влияние катализатора на скорость химических реакций
Влияние катализатора на скорость химических реакций
Катализаторы – это вещества, изменяющие скорость химических реакций, остающиеся при этом в химически неизменном виде.
Катализ – это процесс изменения скорости химических реакций под действием катализатора.
Катализ:
- гомогенный (катализатор и реагирующие вещества находятся в одной фазе)
- гетерогенный (катализатор и реагирующие вещества находятся в разных фазах)
Особенности биокатализаторов:
- высокая эффективность:
А) 2H2O2 → 2H2O + O2 (Ea = 75 кДж/моль)
Б) 2H2O2 → 2H2O + O2 (Ea = 23 кДж/моль)
V химической реакции увеличивается в 3*1011 раз
- ориентационный эффект (повышает скорость биохимических реакций примерно в 1000 раз)
- действует в условиях постоянных температур (10о-60оС)
- действие ферментов зависит от рН среды (рН = 4-10)
Механизм положительного действия катализатора
Роль катализатора – уменьшение Еа

 Смещение химического равновесия называется сдвигом химического равновесия.
Смещение химического равновесия называется сдвигом химического равновесия.
– Конец работы –
Эта тема принадлежит разделу:
Кинетика, катализ, химическое равновесие
Если на систему находящуюся в равновесии оказывать внешнее воздействие то равновесие сместится в сторону той из двух реакций которая...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Влияние температуры на скорость химических реакций.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов