Виды напряжений в органических молекулах
1. Торсионное напряжение (напряжение Питцера) вызвано электростатическим взаимодействием противостоящих связей.
2. Напряжение Ван-дер-Ваальса, возникающее при расположении заместителей на расстоянии, приблизительно равном сумме их ван-дер-ваальсовых радиусов.
3. Угловое напряжение (напряжение Байера),вызванное отклонением валентного угла в цикле от нормального угла для данного валентного состояния.
Геометрия реальной молекулы соответствует той конформации, в которой энергия внутримолекулярных взаимодействий имеет минимальное значение.
Конформациямимолекулы определенной конфигурации называются состояния молекулы с различным расположением ее атомов в пространстве, возникающие в результате вращения вокруг связей. Конформер это молекула в конформации, в которую ее атомы самопроизвольно возвращаются после небольших сдвигов. Наиболее стабильными являются конформации, в которых атомы испытывают наименьшее межмолекулярное отталкивание. Их называют заторможенными. И наоборот, конформации в которых атомы располагаются близко, являются нестабильными и называются заслоненными. Возможность перехода одной конформации в другую определяется барьером вращения.
Свободному вращению вокруг одинарной связи препятствуют при сближении групп наряду с взаимным ван-дер-ваальсовым отталкиванием изменения:
· торсионного (питцеровского) напряжения (квантово-химическое взаимодействие соседних σ-связей, например, в конформации «ванна» циклогексана);
· углового, или байеровского, напряжения (в циклоалканах);
· дипольных взаимодействий или водородных связей;
· энергии сольватации (в растворителе при смене растворителя);
· напряжения связей вследствие их растяжения или сжатия (при изменении температуры);
· взаимодействия несвязных атомов.
Структура конформеров часто оказывает решающее влияние на физические и химические свойства соединений, поэтому так интенсивны исследования в этой области в настоящее время.
Для изображения процесса вращения по связи С–С удобно пользоваться двумерными изображениями соединений, которые предложил М. Ньюмен (1955 г.):
Торсионный угол (j) – двугранный угол, образованный плоскостями, в которых лежат связи соседних атомов четырехатомного фрагмента.
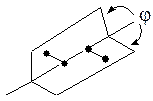
За минимальный отсчет торсионного угла принято считать 60о. В результате полного оборота возникает бесконечное множество конформаций, шесть из них с торсионными углами, кратными 60о, соответствуют максимумам и минимумам на энергетической кривой.
Энергетический барьер вращения – разность потенциальных энергий двух крайних конформаций (1 и 5); для этана – 12 кДж/моль, для н-бутана – 25,5 кДж/моль.
Конформеры – относительно устойчивые конформации (4, 5, 6).
Названия конформаций:
· синперипланарная (syn – вместе, plan – плоскость) – (1);
· антиперипланарная (anti – напротив), трансоидная – (5);
· синклинальная (гр. klino – выгибаю) – (4, 6);
· антиклинальная – (2, 3).
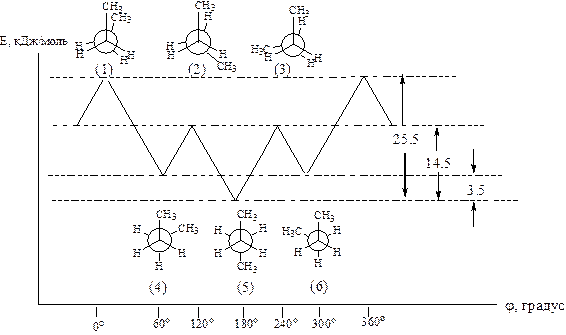
Рисунок 12 – Потенциальная энергия конформации н-бутана

анти- гош-
Рисунок 13 – Стабилизация конформации за счет внутримолекулярной водородной связи

конформационные энантиомеры н-бутана
Рисунок 14 – Конформационная энантиомерия
С удлинением углеродных цепей возникают различные конформации цепи. Например:
· зигзагообразная:

· клешневидная:

d-гидроксивалериановая d-валеролактон
кислота (5-гидроксипента- (пентанолид-1,5)
новая кислота)
· нерегулярная:
Особенно сложна картина цепной конформации у полимерных молекул с длинной цепей. В жидких и твердых алканах с большим значением Сn наиболее устойчива регулярная зигзагообразная конформация, обеспечивающая максимальное межмолекулярное взаимодействие соседних СН2 -групп.
Конформации циклов возникают за счет изменения колебательных состояний атомов и атомных группировок, что создает возможность образования многих неустойчивых форм.
Низшие циклоалканы (циклопропан и циклобутан) сравнительно жесткие и малоустойчивые образования, способные размыкаться при взаимодействии со многими реагентами.
Причина необычного поведения малых циклов заключается в особенностях электронного строения. Полагают, что в молекуле циклопропана из-за углового напряжения, т. е. значительного отклонения валентного угла от нормального для sp3-гибридизации (109°28'), при образовании связей С–С не достигается максимальное перекрывание атомных орбиталей. Из-за сближенности (угол равностороннего треугольника – 60°) электронные облака испытывают сильное взаимное отталкивание. В результате эти облака перекрываются не по прямой, соединяющей центры ядер, а под углом, вне треугольника молекулы:
Таким образом, С–С-связи в циклопропане отличаются от обычных σ-связей при sp3-гибридизации: они изогнуты и не обладают цилиндрической симметрией. Такие связи называют «банановыми», или τ-связями. Они занимают промежуточное положение между σ- и π-связями. Поскольку в такой связи не достигается максимальное перекрывание атомных орбиталей, она достаточно слаба, что и проявляется в легкости раскрытия цикла и образовании продуктов присоединения.
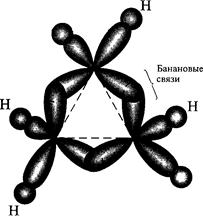
Рисунок 15 – Схема перекрывания АО в молекуле циклопропана
Поэтому циклопропан и напоминает по свойствам олефины, хотя он значительно пассивнее последних.
Средние и макроциклы достаточно устойчивы и близки по свойствам к алканам.
В 1885 г. А. Байер предположил, что неустойчивость малых циклов объясняется так называемым угловым напряжением – отклонением угла между связями от нормального валентного угла при sp3-гибридизации.
В 1890 – 1919 гг. Г. Сакс и Е. Мор предположили и обосновали возможность неплоского расположения атомов в циклах. Циклические углеводороды изгибаются в пространстве таким образом, чтобы отклонение валентного угла от нормального было минимальным. Напряжение, выводящее молекулу из плоскости, называется торсионным напряжение Питцера, напряжение заслоненных связей (от англ. слова «torsion» - кручение).
Циклы изгибаются в пространстве, образуя конформации, в которых угол между связями соответствует или приближается к нормальному валентному углу насыщенного атома углерода. Конформационная изомерия циклоалканов обеспечивает устойчивость средних и больших циклов.
Устойчивость той или иной конформации определяется угловым напряжением и торсионным эффектом, возникающим, когда заместители у соседних атомов углерода отклоняются от заторможенной конформации.
Например:
· молекула циклобутана может перейти из плоского состояния в неустойчивое неплоское:
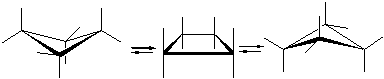
· молекула циклопентана может находится в конформациях “конверт” и “полукресло”:
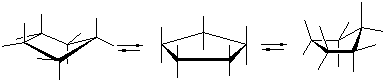
· молекула циклогексана может находится в конформациях “кресло”(от англ. chаir-кресло), “ванна” (лодка, от англ. boat-лодка) и “твист”:
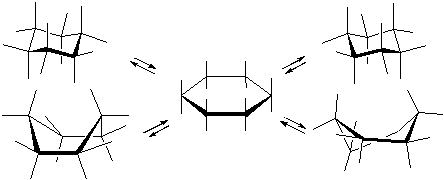
Разделить конформации циклогексана невозможно, так как при обычных температурах они быстро превращаются друг в друга. Однако конформация кресла, как более стабильная, составляет при обычных условиях более 99 % равновесной смеси.

Конформация кресло имеет ось симметрии третьего порядка. Атомы углерода в ней располагаются в двух параллельных плоскостях. Шесть связей С–Н параллельны оси симметрии и называются аксиальными (а). Остальные располагаются почти перпендикулярно оси и занимают так называемое экваториальное положение (е).

Рисунок 16 – Расположение оси симметрии в молекуле циклогексана
1,3-Диаксиальное взаимодействие – ван-дер-ваальсово взаимодей-ствие между объемными заместителями, расположенными на аксиальных связях в положении – 1,3.

Рисунок 17 – 1,3-Диаксиальное взаимодействие заместителей

Рисунок 18 – Стабилизация аксиального конформера за счет водородной связи
Таблица 3 – Конформационный анализ дизамещенных циклогексанов.
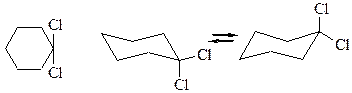
| а, е = е, а | |

| е, а = а, е | |

| е, е > a, a | |

| e, e > a, a | |

| e, a = a, e | |

| e, a = a, e | |

| e, e > a, a |
Вывод: Термодинамическая устойчивость
цис – 1, 2 < транс – 1, 2
цис – 1, 3 > транс – 1, 3
цис – 1, 4 < транс – 1, 4
Конформации играют большую роль в химии средних (С7 – С10) и больших (С12 и больше) циклов. Здесь положения атомов водорода, которые замещаются при синтезе функциональных производных, еще более неэквивалентны, чем у циклогексана. Так, молекула циклодекана в конформации “алмаз” имеет четыре атома водорода, расположенные внутри цикла, которые сильно сближены друг с другом:
Это приводит к необычным свойствам циклоалканов. Введение в циклоалканы гетероатомов (O, N, S, P и т. д.) приводит к гетероциклам. Гетероатом изменяет свойства конформаций и, нередко, конформации устойчивые для циклоалканов становятся неустойчивыми, и наоборот.
Геометрическая изомерия (π-диастереомерия) – стереомерия, обусловленная различным расположением заместителей в пространстве относительно плоскости π-связи.
π-связь
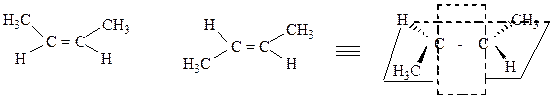
цис-бутен-2 (Z) транс-бутен-2 (E)
Условия, необходимые для π-диастереомерии:
· наличие π-связи;
· у атомов углерода, соединенных двойной связью наличие разных заместителей.
Е-изомеры, в которых старшие заместители у углеродных атомов двойной связи находятся по разные стороны (нем. entgegen– напротив) относительно плоскости связи. Z-изомеры, в которых старшие заместители располагаются по одну сторону относительно плоскости двойной связи (нем. zusammen – вместе).
Превращение изомеров друг в друга в обычных условиях не возможно без разрыва двойной связи и цис–, транс– изомеры существуют как индивидуальные соединения.
Оптическая изомерия обусловлена возможностью пространственной асимметрии молекул. Я. Вант-Гофф и независимо от него Ж. Ле Бель в 1874 г. выдвинули гипотезу о пространственной конфигурации насыщенного углеродного атома – тетраэдрическом расположении заместителей. Асимметрические молекулы называют хиральным (от греч. χειρ (хиро) – рука). Молекула хиральна, если отсутствуют плоскость и центр симметрии. Ось симметрии может быть.
Хиральные молекулы обладают способностью поворачивать плоскость поляризованного света на определенный угол. Это явление называют оптической активностью, а соответствующие молекулы оптически активными.
Оптические изомеры, вращающие плоскость поляризации вправо, называют правовращающими и обозначают знаком “+”, влево – левовращающимии обозначают знаком “–“.
Плоскость симметрии – это воображаемая плоскость, которая рассекает объект на две зеркально противоположные половины.
Центр симметрии – это точка, относительно которой на прямой, проходящей через нее, можно встретить тождественные точки на одном и том же расстоянии.

| Молекула ахиральна | Молекула хиральна | Плоскость симметрии – молекула ахиральна |

Рисунок 19 – Схемы зеркальных изомеров производных дифенила
Хиральный центр – sp3-гибридизованный атом (C, N, Si, P) с четырьмя разными лигандами.
Асимметрический атом углерода – хиральный атом, т. е. sp3-гибридизованный с четырьмя разными партнерами. В структурной формуле обозначается С*.
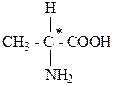
2-аминопропановая кислота
Два стереоизомера, относящиеся друг к другу как предмет и его зеркальное отражение, называют антиподами или энантиомерами. Например молочная кислота:

В поисках универсального способа для выражения абсолютной конфигурации была разработана система Кана – Ингольда – Прелога (1956 г.) или система абсолютной R, S – конфигурации (от лат. rectus – правый, sinister – левый). Система основана на старшинстве заместителей при асимметричном атоме углерода:
· атом или атом заместителя, непосредственно связанный с хиральным центром, с большим атомным номером является старшим относительно атома с меньшим атомным номером;
· большее массовое число имеет преимущество перед меньшим, в том числе и изотопов;
· неподеленные пары электронов имеют самый низкий порядок, в том числе и по сравнению с водородом;
· если с хиральным центром связаны два идентичных атома, то старшим считается тот, который связан с атомом с большим атомным номером (процедура может повторяться);

· если атом двоесвязан, то по старшинству он приравнивается к атому, связанному с двумя эквивалентными группами, т. е. атомный номер удваивается.
Однако для углеводов и аминокислот используют D (+), L (–) номенклатуру. В качестве стандарта при использовании D, L номенклатуры Э. Фишер предложил правовращающую, т. е. (+) – глюкозу.