Сu u Hg
2) Al u Fe
3) Zn u Cr
4) Mg u Pb
Тесты по разделу «Строение атома и периодическая система Д.И.Менделеева»
1.Ядерную планетарную модель атома предложил
1) Бор
2) Зоммерфельд
3) Резерфорд
4) Планк
5) Томсон
2.Принцип неопределенности Гейзенберга описывается уравнением
1) 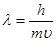
2) 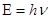
3)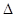 q
q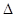 V
V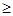 h/m
h/m
4) 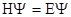
5) E = mc2
3.Уравнение Де-Бройля имеет вид
1) 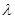 =h/mv
=h/mv
2) 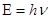
3) 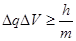
4) 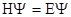
5) E = mc2
4. Уравнение Шредингера имеет вид
1) 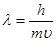
2) 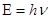
3) 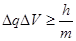
4) H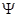 =E
=E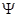
5) E = mc2
5. Изотопами являются
1) 40Ca и 42Ca
20 20
2)40Ar и 40K
18 19
3) 40Ca и 40K
20 19
4) 136Xe и 138Ba
54 56
5) 23Na и 39K
11 19
6. Ядро атома состоит из
1) протонов и электронов
2) протонов и нейтронов
3) нейтронов и электронов
4) протонов
5) протонов, нейтронов и электронов
7. Энергию и размер орбитали характеризует
1) главное квантовое число n
2) орбитальное квантовое число l
3) магнитное квантовое число ml
4) спиновое квантовое число ms
5) количество находящихся на ней электронов
8. Форму атомной орбитали определяет
1) главное квантовое число n
2) орбитальное квантовое число l
3) магнитное квантовое число ml
4) спиновое квантовое число ms
5) порядковый номер атома в таблице Менделеева
9. Магнитное квантовое число ml характеризует
1) энергию орбитали
2) размер орбитали
3) форму орбитали
4) собственный механический момент движения электрона
5) ориентацию орбитали в пространстве
10. Все возможные значения магнитного квантового числа для d-орбиталей
1) 1,2,3
2) –1,0,1
3) –2,-1,0,1,2,3
4) –3,-2,-1,0,1,2,3
5) 1,2,3,4
11. Все возможные значения магнитного квантового числа для p-орбиталей
1) 1,2,3
2) –1,0,1
3) –2,-1,0,1,2
4) –3,-2,-1,0,1,2,3
5) 1,2,3,4
12. Какие орбитали имеют форму гантели
1) s-орбитали
2) p-орбитали
3) d-орбитали
4) f-орбитали
5) гибридные орбитали
13. В атоме не может быть …… электронов с одинаковым набором четырех квантовых чисел
1) двух
2) трех
3) пяти
4) семи
5) четырех
14. Какое электронное состояние возможно
1) 2s3
2) 3p7
3) 4d11
4) 3f 5
5) 5d 6
|

|



 15. Строение внешней электронной оболочки в устойчивом состоянии имеет
15. Строение внешней электронной оболочки в устойчивом состоянии имеет
1) кислород
2) кремний
3) азот
4) алюминий
5) фтор
16. В невозбужденном состоянии число электронов на четвертом энергетическом уровне равно пяти у
1) технеция
2) брома
3) германия
4) мышьяка
5) ванадия
17. Способность атомов притягивать к себе электронную плотность
1) потенциал ионизации
2) электроотрицательность
3) сродство атома к электрону
4) электростатическое притяжение
5) электрохимический потенциал
18. Энергия, выделяющаяся при присоединении электрона к свободному атому
1) потенциал ионизации
2) электроотрицательность
3) сродство атома к электрону
4) электростатическое притяжение
5) энергия Гиббса
19. Величина I в процессе

 A(атом) + I A+ + 1 e 1) потенциал ионизации
A(атом) + I A+ + 1 e 1) потенциал ионизации
2) электроотрицательность
3) сродство атома к электрону
4) внутренняя энергия
5) стандартный электродный потенциал
20. Количество протонов, нейтронов и электронов в атоме 52Cr
1) 52,24,52 24
2) 24,52,24
3) 24,24,28
4) 28,24,24
5) 24,28,24
21. В атоме 127J …. Нейтронов 53
1) 53
2) 127
3) 180
4) 74
5) 85
22. Электроотрицательность элементов в таблице Д.И. Менделеева в периодах слева направо …., а в группах сверху вниз ….
1) уменьшается, уменьшается
2) увеличивается, уменьшается
3) увеличивается, увеличивается
4) уменьшается, увеличивается
5) увеличивается, не изменяется
23. В атоме 51V …. Протонов 23
1) 23
2) 51
3) 74
4) 28
5) 25
24. Возможные валентности серы с точки зрения строения атома
1) 3, 5
2) 2, 4, 6
3) 1, 3, 5
4) 5, 7
5) 1, 3
25. Возможные валентности хлора с точки зрения строения атома
1) 1,7
2) 1,5,7
3) 1,3,5,7
4) 1,2,7
5) 1,2,4,7
Тесты по разделу «Химическая термодинамика»
1. Энергия Гиббса рассчитывается по формуле:
1)S = k ∙ ln w
2)Δ G = Δ H – T Δ S
3) Δ F = Δ U – T Δ S
4)Q = Δ U + A
5) Δ S = Δ H/T
2. Процесс, протекающий при постоянной температуре, называется
1)изобарическим
2)изохорическим
3)изотермическим
4)адиабатическим
5)изобарно-изотермичечким
3. Характеристическая функция H = U + p∙V называется
1)энтропией
2)энтальпией
3)изобарно-изотермическим потенциалом
4)свободной энергией Гиббса
5)свободной энергией Гельмгольца
4) Мерой неупорядоченности состояния системы служит термодинамическая функция, получившая название
1)энтальпии
2)энтропии
3)энергии Гельмгольца
4)теплового эффекта реакции
5)энергии Гиббса
5. Согласно второму закону термодинамики, в изолированных системах самопроизвольно идут процессы, которые сопровождаются возрастанием
1)энтальпии
2)энтропии
3)внутренней энергии
4)объёма
5)температуры
6 Экзотермическими являются реакции:
1)CH4 + 2H2O = CO2 + 4H2 ΔH0 реакции = +164,9 кДж/моль
2)C3H8 + 5O2 = 3CO2 + 4H2O ΔH0 реакции = -103,9 кДж/моль
3)H2O2 = H2O + 1/2O2 ΔH0 реакции = -98,8 кДж/моль
4)1/2Na2O + 1/2H2O = NaOH ΔH0 реакции= -68,4 кДж/моль
5)2Cu2O = Cu2O + 1/2O2 ΔH0 реакции = +163,2 кДж/моль
7. «Тепловой эффект реакции зависит от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути реакции, то есть от числа и характера промежуточных стадий».
Приведённое выражение представляет собой:
1)закон Ома
2)закон Ньютона
3)закон Гесса
4)закон Авогадро
5)закон Фарадея
8. Тепловой эффект образования 1 моль вещества из простых веществ, устойчивых при температуре 298К и давлении 100 кПа, называется
1)свободной энергией Гиббса
2)свободной энергией Гельмгольца
3)энтальпией образования
4)энтальпией сгорания
5)энтропией
9. Самопроизвольный процесс в любом температурном интервале возможен при условии:
1)ΔH < 0,ΔS > 0
2) Δ H < 0, Δ S < 0
3) Δ H > 0, Δ S > 0
4) Δ H > 0, Δ S < 0
5) Δ H > 0, Δ S=0
10. Процесс, протекающий при постоянном давлении, называется:
1)изотермическим
2) изобарным
3)изохорным
4)адиабатным
5)изобарно-изотермическим
11. В условиях постоянства температуры и давления химическая реакция не может протекать самопроизвольно, если
1) Δ G < 0,
2) ΔG> 0,
3) Δ H < 0,
4) Δ H > 0,
5) Δ S < 0
12. Первый закон термодинамики:
1) ΔG = Δ H – T Δ S
2) Q =ΔU + A
3) ΔU = U2 – U1
4)S = k ∙ lnw
5) Δ S = Δ H/T
13. Веществом, для которого стандартная энтальпия образования равна нулю, является
1)этанол
2)кислород
3)хлороводород
4)сероводород
5)серная кислота
14. Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:
2NO2 = N2O4
ΔH0обр. 33,9 9,4 кДж/моль
Изменение энтальпии указанной реакции составляет:
1) ΔH0реакции= +58,4 кДж
2)ΔH0реакции= -58,4 кДж
3) ΔH0реакции= -24,5 кДж
4) ΔH0реакции = +24,5 кДж
5) ΔH0реакции = +28,4 кДж
15. Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:
PtCl2 + Cl2 = PtCl4
Δ H0обр -118,0 -226,0 кДж/моль
Изменение энтальпии в указанной реакции составляет:
1) Δ Н0 реакции =108,0 кДж
2) ΔН0 реакции = 344,0 кДж
3) ΔН0 реакции = -344,0 кДж
4) ΔН0 реакции = 25,0 кДж
5)ΔН0 реакции = -108 кДж
16. Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:
С2Н2 + Н2 = С2Н4
Δ Н0 обр. 226,8 52,3 кДж/моль
Изменение энтальпии в указанной реакции составляет
1)+174,5 кДж
2)-174,5 кДж/моль
3)+279,1кДж/моль
4)-279,1кДж/моль
5)-87,2 кДж/моль
17. Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции
СО + Сl2 = СОСl2
ΔН0обр. 110,6 -220,3 кДж/моль
Изменение энтальпии в данной реакции составляет
1) + 109,7 кДж
2) –109,7 кДж
3)-330,9 кДж
4) +330,9 кДж
5) –210,1 кДж
18. Для реакции, протекающей в стандартных условиях, известны значения энтропии исходных веществ и продуктов реакции:
N2(г) + 3H2(г) = 2NH3(г)
S0298 199,9 130,5 192,6 Дж/моль ∙ К
Изменение энтропии в указанной реакции составляет
1) +206,2 Дж/К
2) –137,8 Дж/К
3) –206,2 Дж/К
4) +137,8 Дж/К
5) –398,9 Дж/К
19. Процесс испарения воды протекает в стандартных условиях:
Н2О (жидк.) = Н2О(газ)
ΔН0обр. –286,0 -242,0 кДж/моль
Энтальпия процесса испарения равна:
1)-44,0 кДж/моль
2)+44,0 кДж/моль
3)-528,0 кДж/моль
4)+528,0 кДж/моль
5)-88,0 кДж/моль
20. Реакция протекает в стандартных условиях:
2Cu(NO3)2 = 2CuO = 4NO2 + O2
Изменение энтальпии в данной реакции равно +420,4 кДж, изменение энтропии в реакции равно +1033.6 Дж/К. Рассчитать изменение свободной энергии Гиббса.
1)+112,3 кДж
2) –112,3 кДж
3) 613,2 кДж
4) –613 кДж
5) +1454,0 кДж
21. Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:
СО2 + Н2 = СО + Н2О
ΔН0обр. –393,8 -110,6 -286,0 кДж/моль
Изменение энтальпии в указанной реакции составляет: