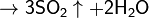Химические свойства
 Горение серы
Горение серы
На воздухе сера горит, образуя сернистый ангидрид — бесцветный газ с резким запахом:
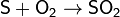
С помощью спектрального анализа установлено, что на самом деле процесс окисления серы в двуокись представляет собой цепную реакцию и происходит с образованием ряда промежуточных продуктов: моноокиси серы S2O2, молекулярной серы S2, свободных атомов серы S и свободных радикалов моноокиси серы SO[6].
Восстановительные свойства серы проявляются в реакциях серы и с другими неметаллами, однако при комнатной температуре сера реагирует только со фтором:
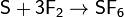
Расплав серы реагирует с хлором, при этом возможно образование двух низших хлоридов[7]:
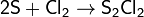
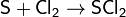
При нагревании сера также реагирует с фосфором, образуя смесь сульфидов фосфора[8], среди которых — высший сульфид P2S5:
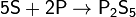
Кроме того, при нагревании сера реагирует с водородом, углеродом, кремнием:
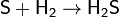 (сероводород)
(сероводород)
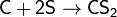 (сероуглерод)
(сероуглерод)
При нагревании сера взаимодействует со многими металлами, часто — весьма бурно. Иногда смесь металла с серой загорается при поджигании. При этом взаимодействии образуются сульфиды:
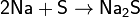
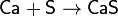
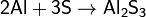
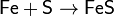 .
.
Растворы сульфидов щелочных металлов реагируют с серой с образованием полисульфидов:
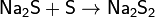
Из сложных веществ следует отметить прежде всего реакцию серы с расплавленной щёлочью, в которой сера диспропорционирует аналогично хлору:
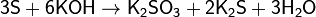 .
.
Полученный сплав называется серной печенью.
С концентрированными кислотами-окислителями (HNO3, H2SO4) сера реагирует только при длительном нагревании:
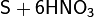 (конц.)
(конц.) 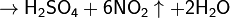
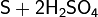 (конц.)
(конц.)