Галоидирование.
На свету алканы могут последовательно замещать атомы водорода на атомы галоида, например:
CH4 + Cl2 ® CH3Cl + HCl хлористый метил
CH3Cl + Cl2 ® CH2Cl2 + HCl хлористый метилен
CH2Cl2 + Cl2 ® CHCl3 + HCl хлороформ
CHCl3 + + Cl2 ® CCl4 + HCl четыреххлористый углерод.
В.В.Марковников установил, что после замещения одного атома водорода хлором, замещение оставшихся атомов водорода облегчается.
Реакции галоидирования алканов протекают по радикальному цепному механизму. Этот механизм был открыт и доказан советским ученым Семёновым (Нобелевская премия).
Для начала реакции необходимо образование свободного радикала.
Энергия диссоциации связей при 25°С:
С–С – 345,6 кДж×моль-1;
С–Н – 413,0 кДж×моль-1;
Cl–Cl – 242,7 кДж×моль-1.
Легче других разрывается связь Cl–Cl. При подведении энергии извне (тепло, электрическое поле, солнечный свет) образуются два радикала Cl×.
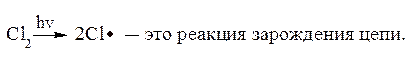
Далее:
| CH4 + Cl× ® CH3× + HCl CH3× + Cl2 ® CH3Cl + Cl× CH3Cl + Cl× ® CH2Cl× + Cl CH2Cl× + Cl2 ® CH2Cl2 + Cl× | – это реакция роста цепи |
| и т.д., до CCl4. |
При этом получаются довольно длинные цепи – порядка 1000 звеньев (актов взаимодействия) на один атом хлора.
Обрыв цепи происходит вследствие рекомбинации атомов хлора:
Cl× + Cl× ® Cl2
или вследствие реакции атома хлора со свободным радикалом (что вероятнее):
Cl× + CH3×® CH3Cl
Хлорирование метана, особенно с целью получения CCl4, проводится в промышленном масштабе. Галогеналканы служат исходными веществами для многих органических синтезов.