ИОНООБМЕННЫЕ РЕАКЦИИ. ГИДРОЛИЗ СОЛЕЙ
При взаимодействии растворов электролитов реакции происходят между ионами растворенных веществ. Химический процесс можно записать в молекулярной и ионно-молекулярной формах. Однако ионная форма отражает его точнее. При составлении ионных уравнений реакций вещества малодиссоциированные, малорастворимые (выпадающие в осадок) и газообразные изображаются в виде молекул.
Пример 1.Записать в молекулярной и ионно-молекулярной формах уравнения реакций между следующими веществами: H2SO4 и BaCl2; Na2СО3 и НCl.
Решение:
1) H2SO4 + BaCl2= Ва SO4 ↓+ 2 НCl – молекулярное уравнение,
2Н + + SO4 2-_+ Ва2+ + 2Cl- = ВаSO4 ↓ + 2Н+ + 2Cl- – полное ионно-молекулярное уравнение;
Ва2+ + SO4 2- = ВаSO4 ↓ – сокращенное ионно-молекулярное уравнение.
Сокращенное ионно-молекулярное уравнение показывает, что в реакции участвуют только ионы Ва2+ и SO4 2-.
2) Na2СО3 + 2НCl = 2NaCl + Н2О + СО2↑
2 Na + + СО3 2-_+ 2Н++ 2Cl- = 2 Na + + 2Cl- + Н2О + СО2↑
СО3 2-_+ 2Н+ = Н2О + СО2↑
Гидролизомназывается взаимодействие солей и воды с образованием слабодиссоциирующих веществ, одновременно сопровождающееся смещением ионного равновесия воды. Отсюда следует, что не всякое взаимодействие соли с водой является гидролизом, а следовательно, не все соли гидролизу подвергаются.
Гидролизу подвергаются соли, образованные катионом сильного основания и анионом слабой кислоты (Na2CO3, CH3COOK), катионом слабого основания и анионом сильной кислоты ( ZnCl2, Al2(SO4)3), катионом слабого основания и анионом слабой кислоты (CH3COONH4, Al2S3).
Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются.
При анализе состава солей нужно помнить, что:
| 1. К сильным основаниям относятся: LiOH, KOH, NaOH, CsOH, RbOH, Ca(OH)2, Ba(OH)2, Sr(OH)2, Rа(OH)2. 2. К сильным кислотам относятся: H2SO4, H2SеO4, HNO3, HClO4, HBr, HI, HCl. | 3. Слабые основания образуют катионы всех остальных металлов и NH4+. 4. К слабым кислотам относятся: H2SO3, HNO2, HClO, HF, H3PO3, H2CO3, H2S, H2SiO3,CH3COOH и др. |
Соли, образованные многокислотными основаниями или многоосновными кислотами, подвергаются ступенчатому гидролизу. Более легко протекает первая ступень гидролиза, и на ней, как правило, при обычных условиях гидролиз солей завершается. Скорость гидролиза зависит от растворимости солей, оснований и кислот, поэтому необходимо учитывать этот фактор (прил. 7).
Гидролизу подвергается не все количество находящейся в растворе соли, а только часть ее. Иначе говоря, в растворе устанавливается равновесие между солью и образующими ее кислотой и основанием. Доля вещества, подвергающаяся гидролизу, - степень гидролиза, - зависит от константы этого равновесия, а также от температуры и концентрации соли.
Запишем уравнение гидролиза в общем виде. Пусть НА – кислота, МОН – основание, МА – образованная ими соль. Тогда уравнение гидролиза будет иметь вид:
МА + Н2О ↔НА + МОН
Этому равновесию отвечает константа
 .
.
Концентрация воды в разбавленных растворах представляет собой практически постоянную величину. Обозначая К·[ Н2О] =Кг, получим
 .
.
Величина Кг называется константой гидролиза соли. Ее значение характеризует способность данной соли подвергаться гидролизу; чем больше Кг, тем в большей степени (при одинаковых температуре и концентрации соли) протекает гидролиз. Для соли, образованной катионом сильного основания и анионом слабой кислоты, константа гидролиза связана с константой диссоциации кислоты Ккисл зависимостью:


 .
.
Это уравнение показывает, что Кг тем больше, чем меньше Ккисл . Иными словами, чем слабее кислота, тем в большей степени подвергаются гидролизу ее соли.
Для солей, образованных катионом слабого основания и анионом сильной кислоты, аналогичное выражение связывает константу гидролиза с константой диссоциации основания Косн:
 .
.
Поэтому, чем слабее основание, тем в большей степени подвергаются гидролизу образованные им соли.
Степень гидролиза определяется природой соли, ее концентрацией и температурой. Природа соли проявляется в величине константы гидролиза.
Зависимость степени гидролиза (h) от концентрации выражается через закон разбавления:
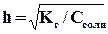 ,
,
то есть с разбавлением раствора степень гидролиза увеличивается.
Влияние температуры на степень гидролиза вытекает из принципа Ле-Шателье. Все реакции нейтрализации протекают с выделением теплоты, а гидролиз с поглощением теплоты. Поскольку выход эндотермических реакций с ростом температуры увеличивается, то и степень гидролиза растет с повышением температуры.
Пример 1.Составить молекулярное и ионное уравнение гидролиза соликарбоната натрия.
Решение. Соль Na2СO3 образована сильным основанием (NaOH) и слабой кислотой (H2СO3), таким образом,гидролиз соли будет протекать по аниону. Так как ион СO32- содержит 2 заряда, то гидролиз возможен в 2 ступени: первая ступень протекает в обычных условиях, вторая – при нагревании или разбавлении. Рассмотрим гидролиз по первой ступени:
Сокращенное ионное уравнение гидролиза:
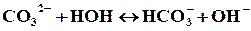
полное ионное уравнение гидролиза:

молекулярное уравнение:

Так как в растворе накапливаются гидроксид-ионы, то среда щелочная, т.е. рН>7.
Пример 2. Составить молекулярное и ионное уравнение гидролиза соли хлорида алюминия.
Решение.Гидролиз солей, образованных слабым основанием (Al(OH)3) и сильной кислотой (HCl) протекает по катиону:

В обычных условиях гидролиз протекает по первой ступени, незначительно – по второй. Третья ступень практически не протекает, однако разбавление или нагревание усиливают гидролиз.
Первая ступень:

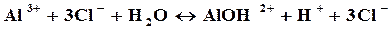
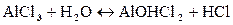
Так как в растворе накапливаются ионы водорода, то среда кислая, т.е. рН<7.
Пример 3. Составить молекулярное и ионное уравнение гидролиза соли, образованной слабым основанием и слабой кислотой.
Решение.Гидролиз солей, образованных слабым основанием и слабой кислотой, протекает полностью и с достаточно большой скоростью, например:
Al2 (CO3)3+3Н2О=2Al(OH)3+3CO2 .
Подобный процесс наблюдается при смешивании растворов Na2CO3 и AlCl3, в которых соответственно имеются избыток ионов ОН- и Н+:

