Таблиця 1
Стандартні потенціали деяких окисно-відновних систем
| Система | Е’0, вольт |
| Кисень / вода | + 0,82 |
| Цитохром a: Fe3+ / Fe2+ | + 0,29 |
| Цитохром с: Fe3+ / Fe2+ | + 0,22 |
| Убіхінон: окислений / відновлений | + 0,10 |
| Цитохром b: Fe3+ / Fe2- | + 0,08 |
| Фумарат / сукцинат | + 0,03 |
| Флавопротеїн («жовтий фермент»): окислений / відновлений | – 0,12 |
| Оксалоацетат / малат | – 0,17 |
| Піруват / лактат | – 0,19 |
| Ацетоацетат / b-гідроксибутират | – 0,27 |
| Ліпоат: окислений / відновлений | – 0,29 |
| НАД+ / НАДН | – 0,32 |
| Н+ / Н2 | – 0,42 |
| Сукцинат / a-кетоглутарат | – 0,67 |
1) Оксидази. Істинні оксидази каталізують видалення водню із субстрату, використовують як акцептор тільки кисень. Вони обов’язково містять мідь, продуктом реакції є вода (виключення складають реакції, які каталізуються уриказою і монооксидазою, в результаті яких утворюється Н2О2 ):

Цитохромоксидаза – гемопротеїн, широко розповсюджений в рослинних і тваринних тканинах. Вона служить кінцевим компонентом ланцюга дихальних переносників, локалізованих в мітохондріях, і каталізує реакцію, в результаті якої електрони, вивільняються із молекул субстрату при їх окисленні дегідрогеназами, переносяться на кінцевий акцептор – кисень. Даний фермент отруюється оксидом вуглецю, ціанідом сірководнем. Інколи цитохромоксидазу називають цитохромом аа3. Спочатку припускали, що цитохром а і цитохром а3 – це автономні гемопротеїни, оскільки кожний з них характеризується визначеним спектром, крім того, вони виявляють різну чутливість до дії оксиду вуглецю і ціаніду. Однак було доведено, що вони входять до складу комплексу, який одержав назву цитохром аа3. Він містить дві молекули гема, у кожній з який атом заліза може переходити зі стану Fe2+ у стан Fe3+ і назад у ході окислення і відновлення, а також два атоми Сu, кожний з яких взаємодіє з одним з гемів.
Фенолаза (тирозиназа, поліфенолоксидаза, катехолоксидаза) – це мідьвмісний фермент із широкою специфічністю. Він каталізує перетворення монофенолу (у присутності о-дифенолу) у о-хінон. Мідь виявлена в ряді інших ферментів, зокрема в уриказі, яка каталізує окислення сечової кислоти в алантоїн, і в моноамінооксидазі, яка окислює адреналін і тирамін у мітохондріях.
2) Аеробні дегідрогенази – ферменти, які каталізують видалення водню із субстрату; на відміну від оксидаз вони як акцептор водню можуть використовувати не тільки кисень, а і штучні акцептори, такі, як метиленовий синій. Ці дегідрогенази відносяться до флавопротеїнів, і продуктом реакції, яку вони каталізують є пероксид водню, а не вода:
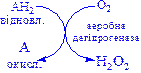 ,
,