ФЕРМЕНТЫ
Ферменты (энзимы) – биологические катализаторы, ускоряющие химические реакции обмена веществ в организме.
Катализ – это процесс изменения скорости химической реакции под действием различных веществ – катализаторов, участвующих в химическом процессе, но к концу реакции остающихся химически неизменными.
Механизм действия катализаторов заключается в следующем.
Молекулы вступают между собой в реакцию, если они находятся в т.н. «активном» или «возбужденном» состоянии, т.е. имеют определенный запас потенциальной энергии, которой достаточно для преодоления сил отталкивания или сцепления между ними, т.е. для преодоления «энергетического барьера».
Скорость химической реакции можно увеличить 2-мя путями:
- увеличить число активных молекул, сообщив определенное дополнительное количество энергии, которое называют «энергия активации». Активировать молекулы можно путем нагревания, повышения давления, облучения и т.д.;
- уменьшить высоту энергетического барьера..
Сущность катализа заключается в том, что катализаторы снижают энергетический барьер, т.е. снижают уровень энергии активации реакции. Это справедливо как для неорганических катализаторов, так и для ферментов.
Происходит это следующим образом.
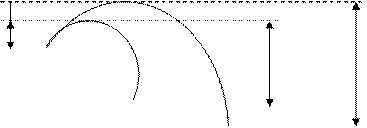
При наличии катализатора взаимодействие молекул происходит в несколько этапов. Энергетический барьер промежуточных реакций значительно ниже энергетического барьера исходной реакции.
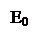
 |

 |
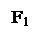
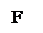
 | |||
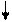 |

 |
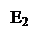
 |
 А+ В АВ Для этой некатализируемой реакции энергетический барьер F, энергия активации Е0.
А+ В АВ Для этой некатализируемой реакции энергетический барьер F, энергия активации Е0.
При введении катализатора:
 А + К АК Энергетический барьер F1, энергия активации Е1.
А + К АК Энергетический барьер F1, энергия активации Е1.
F1 < F; Е1 < Е0
 АК + В АВ + К Энергетический барьер F2< F, энергия активации Е2 < Е0.
АК + В АВ + К Энергетический барьер F2< F, энергия активации Е2 < Е0.
Более того, F1 + F2 < F и Е1 + Е2 < Е0, т.е. с энергетической точки зрения катализируемая реакция более выгодна, чем некатализируемая, т.к. снижается энергия активации, следовательно химическая реакция пойдет быстрее.
Так, энергия активации разложения Н2О2 без катализатора составляет 75,6 кДж/моль, в присутствии неорганического катализатора (коллоидной платины) – 48,14 кДж/моль и скорость ее увеличивается в 2*104 раз.
Рассмотренные закономерности неферментативного катализа справедливы и для действия ферментов. Однако, ферментативный катализ гораздо более интенсивен. Так, в присутствии фермента каталазы энергия активации разложения Н2О2 снижается до 23,1 кДж, а скорость реакции увеличивается в 2*1011 раз.
Общие черты ферментов и неорганических катализаторов:
1. Участвуют в реакции и остаются неизменными после завершения реакции (хотя в последние годы получены данные, что некоторые ферменты после реакции подвергаются модификации и даже распаду);
2. Действуют в малых количествах (например, 1 молекула фермента реннина в желудке теленка створаживает 106 молекул казеина за 10 мин.);
3. Не сдвигают химическое равновесие реакции и не влияют на величину свободной энергии.