рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Энергетика
- /
- Вид работы: Лекции
- /
- Реальные газы
Реферат Курсовая Конспект
Реальные газы
Реальные газы - Лекция, раздел Энергетика, Лекция 1. Основные понятия. Совокупность макроскопических тел, которые обмениваются энергией друг с другом и с окружающей средой, называются термодинамической системой ТС Для Реальных Газов Необходимо Учитывать Взаимодействие Между ...
Для реальных газов необходимо учитывать взаимодействие между молекулами, т.к. обычно это достаточно плотные газы.
Различные способы задания уравнения состояния реальных газов.
1 способ. Уравнение состояния с коэффициентом сжимаемости:
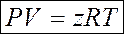 (2.7)
(2.7)
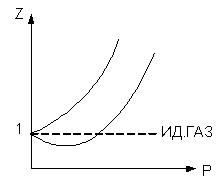
Здесь z - коэффициент сжимаемости (иногда его называют сверхсжимаемостью газа).
Недостаток этого способа в том, что коэффициент z находится чисто экспериментально, притом он зависит не только от природы газа, но и от давления и температуры.
2 способ. Параметрические уравнения. Одно из первых таких уравнений:
 (2.8)
(2.8)
(2.8) - уравнение Ван-дер-Ваальса,
где a, b - параметры, которые зависят только от природы газа.
Это уравнение описывает свойства реальных газов с погрешностью 10-20%.
В настоящее время появились аналогичные уравнения - Редлиха-Квонга,
Пенга-Робинсона и т.д., которые дают меньшую погрешность.
3 способ. Уравнения с вириальными коэффициентами.
 (2.9)
(2.9)
А,В,С - вириальные коэффициенты, 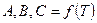
Уравнение (2.9) считается наиболее точным для определения свойств реальных газов.
Помимо этих трех аналитических способов существуют графические методы расчета реальных газов с помощью различных диаграмм: P-V, T-S, i-S.
– Конец работы –
Эта тема принадлежит разделу:
Лекция 1. Основные понятия. Совокупность макроскопических тел, которые обмениваются энергией друг с другом и с окружающей средой, называются термодинамической системой ТС
Лекция Основные понятия... Совокупность макроскопических тел которые обмениваются энергией друг с другом...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Реальные газы
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов