PH воды
Для удобства, концентрации [H+] и [HO-] выражают в виде водородного показателя pH и гидроксильного показателя pOH. pH и pOH - это отрицательные десятичные логарифмы концентраций [H+] и [HO-] (правильнее использовать не концентрацию, а активность) соответственно:
pH = -lg[H+]
pOH = -lg[OH-]
Прологарифмируя уравнение [H+] • [HO-] = 10-14 получим:
lg[H+] + lg[OH-] = -14
-lg[H+] - lg[OH-] = 14
pH + pOH = 14
Получившаяся сумма pH и pOH, также как и произведение, которое логарифмировали, является постоянной и равна 14, так если pH=3 то pOH=11 (pH и pOH могут быть и отрицательными, и если pH=-1 тогда pOH=15).
В зависимости от pH растворы делят на нейтральные, кислые и щелочные. При pH=7 раствор нейтральный, при pH<7 - кислый, при pH>7 - щелочной.
От pH раствора очень сильно зависит протекание многих химических реакций, как на уровне процессов проводящихся в лаборатории и на производстве, так и на уровне реакций в живых организмах, поэтому химикам и биологам с водородным показателем иметь дело приходится очень часто. Все обитатели природных вод и почв адаптированы к определенному водородному показателю, и в случаи его изменения могут погибнуть. Большинство живых организмов могут существовать лишь в средах, близких к нейтральным. Отчасти это связано с тем, что под действием ионов H+ и OH- многие белки, содержащие кислотные или основные группы, изменяют свою конфигурацию и заряд. А в сильнокислой и сильнощелочной средах рвётся пептидная связь, которая соединяет отдельные аминокислотные остатки в длинные белковые цепи. Из-за этого ультраосновные (сильнощелочные) растворы вызывают щелочные ожоги кожи и разрушают шёлк и шерсть, состоящие из белка. Все живые организмы вынуждены поддерживать во внутриклеточных жидкостях определённое значение рН. От величины водородного показателя почвенного раствора зависит урожайность различных культурных растений. На кислых почвах с pH=5-5,5 не развиваются проростки ячменя, но хорошо развивается картофель.


КH2O = 1.10-4 Данная константа для воды называется ионным произведением воды, которое зависит только от температуры.
При диссоциации воды на каждый ион Н+ образуется один ион ОН-, следовательно, в чистой воде концентрации этих ионов одинаковы: [Н+] = [ОН-]. Используя значение ионного произведения воды, находим:
[H+] = [ОН-] = 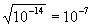 моль/л.
моль/л.
Таковы концентрации ионов Н+ и ОН- в чистой воде. Рассмотрим, как изменится концентрация при добавлении других веществ, например, соляной кислоты, которая диссоциирует в воде на ионы Н+ и Сl-. Концентрация ионов Н+ в растворе станет увеличиваться, но ионное произведение воды от концентрации не зависит - в таком случае уменьшается концентрация [ОН-].
Напротив, если к воде добавить щелочь, то концентрация [ОН-] увеличится, а [Н+] уменьшится. Концентрации [Н+] и [ОН-] взаимосвязаны: чем больше одна величина, тем меньше другая, и наоборот.
Кислотность растворов обычно выражают через концентрацию ионов Н+. В кислых растворах [Н+] > 10-7 моль/л, в нейтральных [Н+] = 10-7 моль/л, в щелочных [Н+] < 10-7 моль/л.
Чтобы не писать числа с показателем степени, кислотность раствора часто выражают через отрицательный логарифм концентрации ионов водорода, называя эту величину водородным ателем и обозначая ее рН:
pН = -lg[Н+].
Величина рН впервые была введена датским химиком С. Серенсоном. Буква “р” - начальная от датского слова potenz (степень), “Н” - символ водорода.
В кислых растворах рН < 7, в нейтральных рН = 7, в щелочных pH > 7.
25. Водородный показатель pH среды для растворов электролитов. Шкала pH. Формулы для расчёта pHдля сильных и слабых кислот и оснований.
Если разбавленный раствор содержит больше ионов водорода, чем 10-7 моль/л, то соответственно концентрация гидроксид-ионов уменьшится во столько раз, во сколько увеличилась концентрация ионов Н+.
Концентрация ионов водорода и гидроксид-ионов важна в химии растворов, поэтому была введена специальная величина — водородный показатель, или pH. По определению, водородный показатель есть обратный логарифм концентрации ионов H+:
pH=-lg[H+].
pH чистой воды равен -lg10-7=7. Если в растворе концентрация ионов Н+ больше, чем 10-7 моль/л, то pH такого раствора будет меньше 7, что является показателем кислой среды раствора, Если же [Н+]<10-7 моль/л, то pH>7, и раствор имеет щелочную реакцию.

Для определения среды растворов используются приборы, называемые pH-метрами. Быстрый анализ можно провести, если в исследуемый раствор добавить одну-две капли кислотно-основного индикатора, т.е. такого вещества, которое под действием ионов Н+ и ОН- может резко изменять свою окраску. Изменения окрасок наиболее распространенных индикаторов приведены ниже.

| Раствор | Формула для расчета рН |
| Общий случай | pН = –lg[H+] pH = 14 + lg[OH–] |
| Раствор сильной одноосновной кислоты | [H+] = с(кислоты) pН = –lgс(кислоты) |
| Раствор сильной двухосновной кислоты | [H+] = 2с(кислоты) pН = –lg[2с(кислоты)] |
| Раствор слабой кислоты | pН = ½рКА – ½lgс(кислоты) |
| Раствор сильного однокислотного основания | [OH–] = с(основания) pH = 14 – lgс(основания) |
| Раствор сильного двухкислотного основания | [OH–] = 2с(основания) pH = 14 + lg[2с(основания)] |
| Раствор слабого основания | pН = 14 – ½рКВ + ½lgс(основания) |
| Буферный раствор | 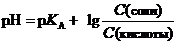
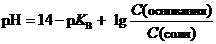
|