ПРЕДМЕТ И ЗАДАЧИ ТОКСИКОЛОГИИ
Аннотация_ 14
ПРЕДИСЛОВИЕ АВТОРА_ 15
РАЗДЕЛ 1. ВВЕДЕНИЕ_ 16
ГЛАВА 1.1. ПРЕДМЕТ И ЗАДАЧИ ТОКСИКОЛОГИИ_ 16
1. Предмет изучения_ 16
1.1. Попытка определения 16
1.2. Токсичность 18
1.3. Токсический процесс 19
1.3.1. Формы проявления токсического процесса на разных уровнях организации жизни_ 19
1.3.2. Основные характеристики токсического процесса, выявляемого на уровне целостного организма 21
1.3.2.2. Другие формы токсического процесса_ 23
2. Цель и задачи токсикологии_ 24
3. Структура токсикологии_ 25
ГЛАВА 1.3. ТОКСИКАНТ (ЯД) 25
1.Общая характеристика токсикантов_ 25
2. Краткая характеристика отдельных групп токсикантов_ 27
2.1. Токсиканты биологического происхождения 27
2.1.1. Бактериальные токсины_ 27
2.1.2. Микотоксины_ 27
2.1.3. Токсины высших растений_ 29
2.1.4. Токсины животных (зоотоксины) 32
2.2. Неорганические соединения естественного происхождения 33
2.3. Органические соединения естественного происхождения 34
2.4. Синтетические токсиканты_ 34
2.4.1. Пестициды_ 34
2.4.2. Органические растворители_ 37
2.4.3. Лекарства, пищевые добавки, косметика_ 38
2.4.4. Боевые отравляющие вещества (БОВ) 39
ГЛАВА 1.2. БИОСИСТЕМЫ - МИШЕНИ ДЕЙСТВИЯ ТОКСИКАНТОВ_ 40
1. Уровни организации биологических систем_ 40
2. Термодинамика биосистем. Термодинамические аспекты токсичности_ 41
3. Фундаментальные свойства живых систем. 42
4. Степени свободы токсического воздействия_ 43
ГЛАВА 1.4. СВОЙСТВА ТОКСИКАНТА, ОПРЕДЕЛЯЮЩИЕ ТОКСИЧНОСТЬ_ 43
1. Размеры молекулы_ 44
2. Геометрия молекулы токсиканта_ 45
3. Физико-химические свойства вещества_ 46
4. Стабильность в среде 48
5. Химические свойства. 48
5.1. Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма_ 48
РАЗДЕЛ 2. ТОКСИКОДИНАМИКА_ 52
ГЛАВА 2.1. МЕХАНИЗМЫ ТОКСИЧЕСКОГО ДЕЙСТВИЯ_ 52
1. Определение понятия "рецептор" в токсикологии_ 52
2. Действие токсиканта на элементы межклеточного пространства_ 54
3. Действие токсикантов на структурные элементы клеток_ 55
3.1. Взаимодействие токсикантов с белками. 55
3.1.1. Энзимы_ 56
3.1.1.1. Усиление каталитической активности_ 57
3.1.1.2. Угнетение каталитической активности_ 57
3.1.1.3. Биологические последствия действия токсикантов на энзимы_ 60
3.2. Взаимодействие токсикантов с нуклеиновыми кислотами. 60
3.3. Взаимодействие токсикантов с липидами_ 61
3.4. Взаимодействие токсикантов с селективными рецепторами_ 61
3.4.1. Селективные рецепторы клеточных мембран_ 61
4. Изучение локализации рецепторов в биообъекте 64
5. Понятие полирецепторного профиля связывания токсиканта_ 64
6. Радиолигандные методы изучения процесса взаимодействия токсиканта с рецепторами 65
ГЛАВА 2.2. МЕХАНИЗМЫ ЦИТОТОКСИЧНОСТИ_ 67
1. Нарушение процессов биоэнергетики_ 68
1.1. Системы энергообеспечения клетки_ 68
1.2. Механизмы токсического повреждения систем энергообеспечения клетки_ 70
2. Нарушение гомеостаза внутриклеточного кальция_ 72
2.1. Повреждение цитоскелета_ 74
2.2. Активация фосфолипаз 76
2.3. Активация протеаз 76
2.4. Активация эндонуклеаз 76
3. Активация свободно-радикальных процессов в клетке 76
3.1. Сущность явления 76
3.2. Механизмы клеточной антирадикальной защиты_ 78
3.3. Механизмы активации ксенобиотиков и образования свободных радикалов 79
3.4. Биологические последствия активации свободно-радикального процесса в клетке 81
4. Повреждение мембранных структур_ 82
4.1. Основные свойства и функции биологических мембран_ 82
4.2. Действие токсикантов на мембраны_ 84
4.2.1. Прямое действие на мембраны_ 84
4.2.2. Активация перекисного окисления липидов_ 84
4.2.3. Активация фосфолипаз 85
4.3. Биологические последствия действия токсикантов на мембраны_ 86
5.2. Синтез РНК. Транскрипция 88
5.3. Синтез белков. Трансляция 89
5.4. Биологические последствия действия токсикантов на нуклеиновый обмен и синтез белка_ 90
ГЛАВА 2.3. ДЕЙСТВИЕ ТОКСИКАНТОВ НА МЕХАНИЗМЫ РЕГУЛЯЦИИ КЛЕТОЧНОЙ АКТИВНОСТИ_ 91
1. Прямое межклеточное взаимодействие 91
2. Механизмы гуморальной регуляции_ 92
3. Механизмы нервной регуляции_ 92
4. Особенности токсического повреждения механизмов регуляции клеточной активности 94
4.1. Изменение числа рецепторов, вызываемое действием ксенобиотиков. 95
4.1.1. Уменьшение количества рецепторов при воздействии токсикантов_ 95
4.1.2. Увеличение числа мембраносвязанных рецепторов при воздействии токсикантов_ 96
4.2. Десенсибилизация рецепторов 96
РАЗДЕЛ 3. ТОКСИКОМЕТРИЯ_ 96
ГЛАВА 3.1. ЗАВИСИМОСТЬ "ДОЗА-ЭФФЕКТ" В ТОКСИКОЛОГИИ_ 96
1. Общие замечания_ 96
2. Зависимость "доза-эффект" на уровне отдельных клеток и органов_ 97
2.1. Предварительные замечания 97
2.2. Основные понятия 98
2.3. Афинность 98
2.3.1. Описание взаимодействия "токсикант-рецептор" в соответствии с законом действующих масс 98
2.3.2. Более сложные модели взаимодействия "токсикант-рецептор" 99
2.4. Эффективность 100
2.4.1. Оккупационные теории_ 100
2.4.2. Теория "скорости взаимодействия" 102
2.4.3. Теории конформационных изменений рецептора_ 103
3. Зависимость "доза-эффект" на уровне организма_ 104
3.1. Предварительные замечания 104
3.2. Кривая "доза-эффект" 104
3.2.1. Среднеэффективная доза (ЕД50) 104
3.2.2. Относительная активность_ 105
3.3. Биологическая изменчивость 105
3.4. Совместное действие нескольких токсикантов на биообъект 106
3.4.1. Параллельный сдвиг кривой "доза-эффект" 106
3.4.2. Снижение максимальных значений кривой "доза-эффект" 107
3.4.3. Параллельный сдвиг с одновременным снижением максимальных значений_ 108
3.5. Определение кажущихся констант диссоциации комплекса "агонист-рецептор" 109
4. Зависимость "доза-эффект" в группе 110
4.1. Зависимость "доза-эффект" для одного токсиканта_ 110
4.1.1. Анализ зависимости "доза-эффект" методом формирования подгрупп_ 110
4.1.2. Анализ зависимости "доза-эффект" без формирования подгрупп_ 113
4.1.3. Зависимость "доза-эффект" по показателю летальность_ 113
4.1.3.1. Общие представления_ 113
4.1.3.2. Определение безопасных доз действия токсикантов_ 116
4.1.3.3. Интерпретация и практическое использование результатов_ 117
4.2. Зависимость "доза-эффект" при комбинированном действии нескольких веществ 119
ГЛАВА 3.2. ЭПИДЕМИОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ В ТОКСИКОЛОГИИ 120
1. Основные категории и типы эпидемиологических исследований_ 121
2. Основные показатели, привлекаемые для организации эпидемиологических исследований 123
2.1 Классификация показателей_ 123
2.1.1. Показатели состояния обследуемой популяции_ 123
3. Замысел эпидемиологического исследования_ 125
3.1. Метод регистрации серии событий_ 125
3.2. Исследование типа "случай-контроль" (болезнь - контроль). 125
3.3. Метод когортных исследований_ 127
3.4. Метод "поперечного среза" 128
3.5. Другие методы_ 130
4. Интерпретация результатов (принципы формирования выводов) 130
ГЛАВА 3.3. ОЦЕНКА РИСКА ДЕЙСТВИЯ ТОКСИКАНТА_ 132
1. Исторические аспекты_ 132
2. Что такое оценка риска?_ 133
3. Процесс оценки риска_ 136
3.1. Идентификация опасности_ 137
3.2. Оценка воздействия 137
3.3. Оценка токсичности_ 138
3.4. Характеристика риска_ 139
4. Недостатки методологии оценки риска_ 139
4.1. Экстраполяция данных_ 139
4.2. Неадекватные исследования 140
4.3. Различия в механизмах токсического действия 140
4.4. Популяционные различия 141
4.5. Неопределенность при оценке воздействия 141
4.6. Неопределенность, связанная с комбинированным действием токсикантов 141
Заключение 142
РАЗДЕЛ 4. ТОКСИКОКИНЕТИКА_ 142
ГЛАВА 4.1. ОБЩИЕ ЗАКОНОМЕРНОСТИ_ 142
1. Растворение и конвекция_ 144
2. Диффузия в физиологической среде 145
2.1. Проникновение веществ через биологические барьеры_ 146
2.2. Диффузия веществ через липидные мембраны_ 147
2.3. Диффузия через поры_ 148
2.4. Межклеточный транспорт химических веществ 150
2.5. Диффузия растворенных газов 150
3. Осмос 151
4. Фильтрация_ 151
4.1. Капиллярная фильтрация 152
5. Специфический транспорт веществ через биологические барьеры_ 153
5.1. Активный транспорт 154
5.2. Каталитическая (облегченная) диффузия 154
5.3. Транспорт веществ путем образования мембранных везикул_ 154
ГЛАВА 4.2. РЕЗОРБЦИЯ КСЕНОБИОТИКОВ_ 155
1. Факторы, влияющие на резорбцию_ 156
2. Резорбция через кожу_ 157
2.1. Способы резорбции_ 157
2.2 Факторы, влияющие на скорость резорбции_ 158
2.2.1. Площадь и область резорбции_ 158
2.2.2. Кровоснабжение_ 158
2.2.3. Свойства действующих веществ_ 159
2.3.4. Экзогенные факторы_ 159
3. Резорбция через слизистые оболочки_ 159
3.1. Резорбция в ротовой полости_ 161
3.2. Резорбция в желудке 161
3.2.1. Растворимость в жирах и рН_ 161
3.2.2. Растворимость в воде_ 162
3.2.3. Содержимое желудка_ 162
3.3. Резорбция в кишечнике 162
3.3.1. Значение рКа 163
3.3.2. Коэффициент распределения в системе масло/вода_ 164
3.3.3. Размеры молекулы_ 164
3.3.4. Заряд молекулы_ 164
3.3.5. Отделы кишечника_ 164
3.3.6. Кровоснабжение_ 164
3.3.7. Содержимое кишечника_ 164
3.4. Резорбция в легких_ 165
3.4.1. Резорбция газов_ 167
3.4.1.1. Вентиляция легких_ 167
3.4.1.2. Поступление в кровь_ 168
3.4.1.3. Переход газов в ткани_ 169
3.4.2. Резорбция аэрозолей_ 170
3.5. Резорбция слизистыми глаз 170
4. Резорбция из тканей_ 170
4.1. Свойства тканей_ 171
4.1.1. Стенка капилляра_ 171
4.1.2. Капиллярная и лимфатическая система_ 171
4.1.3. Кровоснабжение_ 171
4.2. Свойства токсиканта_ 171
5. Квота резорбции_ 172
ГЛАВА 4.3. РАСПРЕДЕЛЕНИЕ КСЕНОБИОТИКОВ В ОРГАНИЗМЕ_ 172
1. Принципы распределения_ 173
1.1. Проникновение веществ через стенку капилляра_ 173
1.2. Значение особенностей кровоснабжения органов 173
1.3. Проникновение через клеточную мембрану_ 175
1.4. Относительная растворимость в системе масло/вода_ 175
1.5. Распределение в соответствии с химическим сродством_ 175
2. Объем распределения_ 176
3. Связывание с белками крови_ 177
3.1. Белки плазмы крови_ 177
3.2. Характеристики связывания ксенобиотиков 178
3.3. Конкурентные отношения при взаимодействии ксенобиотиков с белками_ 180
4. Связывание клетками крови_ 182
5. Проникновение ксенобиотиков в ЦНС_ 183
5.1. Гематоэнцефалический и гематоликворный барьеры. 183
5.1.1. Некоторые свойства гематоэнцефалического и гематоликворного барьеров_ 184
6. Гематоофтальмический барьер_ 184
7. Проникновение ксенобиотиков в печень_ 185
7.1. Сосудистое русло_ 185
7.2. Активный транспорт 186
7.3. Мембранная диффузия 186
7.4. Фагоцитоз 187
8. Поступление ксенобиотиков в экзокринные железы_ 187
9. Проникновение ксенобиотиков через плаценту_ 187
9.1. Плацентарный барьер_ 187
9.2. Характеристика проникновения токсикантов через плаценту и распределение их в тканях плода_ 188
10. Депонирование 188
10.1. Депонирование вследствие химического сродства и растворимости в липидах_ 189
10.2. Депонирование вследствие активного захвата ксенобиотика_ 189
ГЛАВА 4.4. МЕТАБОЛИЗМ КСЕНОБИОТИКОВ_ 189
1. Концепция l и ll фазы метаболизма ксенобиотиков_ 191
2. Локализация процессов биотрансформации_ 192
3. Первая фаза метаболизма_ 194
3.1. Окислительно-восстановительные превращения 196
3.1.1. Оксидазы смешанной функции_ 196
3.1.1.1. ЦитохромР-450-зависимая монооксигеназная система_ 196
3.1.1.1.1. Реакции, катализируемые цитохромомР-450_ 198
3.1.1.2. Флавинсодержащие монооксигеназы (ФМО) 200
3.1.2. Простогландинсинтетаза-гидропероксидаза и другие пероксидазы_ 201
3.1.3. Дегидрогеназы_ 201
3.1.4. Флавопротеинредуктазы_ 202
3.1.5. Восстановление_ 202
3.2. Гидролитические превращения 203
3.2.1. Расщепление эфиров_ 203
3.2.2. Расщепление амидов кислот 203
3.2.3. Эпоксидгидролазы_ 203
3.2.4. Другие гидролазы_ 203
4. Вторая фаза метаболизма. Конъюгация_ 204
4.1. Ацетилирование 205
4.2. Другие реакции ацилирования 205
4.3. Конъюгация с глюкуроновой кислотой_ 205
4.4. Конъюгация с сульфатом_ 206
4.5. Конъюгация с глутатионом и цистеином_ 207
4.6. Метилирование 208
5. Энзимы кишечной флоры_ 208
6. Факторы, влияющие на метаболизм ксенобиотиков_ 209
6.1. Генетические факторы_ 209
6.2. Пол и возраст 209
6.3. Влияние химических веществ 210
6.3.1. Индукция энзимов_ 210
6.3.1.1. Индукторы метаболизма_ 210
6.3.1.2. Механизмы индукции_ 211
6.3.1.3. Влияние индукторов на токсичность ксенобиотиков_ 212
6.3.2. Угнетение активности энзимов_ 212
6.3.3. Двухфазный эффект: угнетение и индукция_ 214
7. Активные метаболиты и их роль в инициации токсического процесса_ 214
ГЛАВА 4.5. ВЫДЕЛЕНИЕ КСЕНОБИОТИКОВ ИЗ ОРГАНИЗМА (ЭКСКРЕЦИЯ) 219
1. Выделение через легкие 219
2. Почечная экскреция_ 221
2.1. Фильтрация 222
2.2. Канальцевая реабсорбция 223
2.3. Канальцевая секреция 224
2.4. Совместное действие механизмов почечной экскреции_ 224
3. Выделение печенью_ 226
4. Выделение через кишечник_ 229
5. Другие пути выведения_ 229
ГЛАВА 4.6. КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ТОКСИКОКИНЕТИКИ_ 230
1. Скорость элиминации. Константа скорости элиминации. Время полуэлиминации_ 230
2. Объем распределения. 231
3. Клиаренс 232
4. Биодоступность_ 233
5. Соотношение между значениями клиаренса, объема распределения и времени полувыведения вещества_ 234
6. Компартменты_ 235
6.1. Однокомпартментная модель 236
6.1.1. Моделирование поведения ксенобиотика при однократном внутривенном введении_ 236
6.1.2. Моделирование поведения ксенобиотика с параллельными путями выведения_ 237
6.1.3. Моделирование поведения ксенобиотика полностью резорбирующегося из места введения 238
6.2. Многокомпартментные модели_ 239
6.3. Нелинейные токсикокинетические процессы_ 240
6.3.1. Нелинейная однокомпартментная модель распределения с ограниченным характером процесса элиминации_ 240
7. Физиологические токсикокинетические модели_ 241
РАЗДЕЛ 5. ФАКТОРЫ, ВЛИЯЮЩИЕ НА ТОКСИЧНОСТЬ_ 244
ГЛАВА 5.1. ВНУТРИ- И МЕЖВИДОВЫЕ ОСОБЕННОСТИ ОРГАНИЗМОВ И ИХ ВЛИЯНИЕ НА ЧУВСТВИТЕЛЬНОСТЬ К КСЕНОБИОТИКАМ_ 244
1. Генетически обусловленные особенности реакций организма на действие токсикантов 244
1.1. Межвидовые различия 244
1.1.1. Особенности токсикокинетики_ 245
1.1.1.1. Резорбция_ 245
1.1.1.2. Распределение_ 246
1.1.1.3. Биотрансформация_ 246
1.1.1.4. Экскреция_ 247
1.1.2. Особенности токсикодинамики_ 248
1.1.2.1. Связывание с рецептором_ 248
1.1.2.1. Эффекторные реакции_ 248
1.2. Внутривидовые различия 248
1.2.1. Генетические особенности личности_ 248
1.2.2. Различия связанные с полом_ 249
2. Не обусловленные генетически особенности реакции организма на действие токсикантов 250
2.1. Возрастные различия 250
2.2. Влияние массы тела_ 252
2.3. Влияние беременности_ 252
ГЛАВА 5.2. ВЛИЯНИЕ УСЛОВИЙ ПРОВЕДЕНИЯ ЭКСПЕРИМЕНТА И КАЧЕСТВА СРЕДЫ ОБИТАНИЯ НА ТОКСИЧНОСТЬ_ 253
1. Питание 253
2. Условия содержания экспериментальных животных_ 254
3. Содержание в стерильных условиях_ 254
4. Периодические изменения чувствительности к токсикантам_ 255
4.1. Циркадные ритмы_ 255
4.2. Годичные ритмы_ 255
5. Температура окружающего воздуха_ 256
ГЛАВА 5.3. ЯВЛЕНИЯ, НАБЛЮДАЕМЫЕ ПРИ ДЛИТЕЛЬНОМ ВОЗДЕЙСТВИИ ТОКСИКАНТОВ 257
1.Толерантность_ 258
1.1. Виды толерантности_ 258
1.2. Некоторые механизмы толерантности_ 259
1.2.1. Ослабление резорбции_ 259
1.2.2. Усиление метаболизма ксенобиотиков_ 259
1.2.3. Усиление экскреции. 260
1.2.4. Изменение распределения_ 260
1.2.5. Изменение рецепторов и реактивных систем_ 260
1.2.6. Индукция веществ-антагонистов_ 261
1.2.7. Истощение запасов нейромедиаторов_ 261
1.3. Тахифилаксия 261
1.4. Хроническая форма толерантности_ 262
1.5. Биологическое значение толерантности_ 262
2.Химическая зависимость_ 263
2.1. Психическая зависимость 263
2.2. Физическая зависимость 264
2.3 Механизм химической зависимости_ 264
3.Привыкание 265
4.Хроническое отравление 265
ГЛАВА 5.4. КОЕРГИЗМ КСЕНОБИОТИКОВ_ 266
1. Механизмы коергизма_ 267
1.1. Взаимодействие в период аппликации_ 267
1.2. Токсикокинетические механизмы коергизма. 268
1.2.1. Взаимодействие веществ при резорбции_ 268
1.2.2. Коергизм веществ, в процессе распределения_ 269
1.2.2.1. Модификация связывания белками плазмы крови_ 269
1.2.2.2. Изменение свойств тканей_ 269
1.2.2.3. Мобилизация биологически активных веществ_ 270
1.2.3. Коергизм в процессе биотрансформации_ 270
1.2.3.1. Угнетение активности энзимов, метаболизирующих ксенобиотики_ 270
1.2.3.2. Повреждение органов и тканей, метаболизирующих ксенобиотики_ 271
1.2.3.3. Индукция энзимов, метаболизирующих ксенобиотики_ 272
1.2.3. Коергизм веществ при их выведении_ 273
1.2.3.1. Выведение через почки_ 273
1.2.3.1.1. Канальцевая реабсорбция_ 273
1.2.3.1.2. Канальцевая секреция_ 273
1.2.3.2. Печеночная экскреция_ 274
1.3. Токсикодинамические механизмы коергизма_ 274
1.3.1. Взаимодействие на уровне рецепторов_ 274
1.3.1.1. Конкуренция за рецепторы одного типа_ 275
1.3.1.2. Коергизм при действии ксенобиотиков на разные участки рецепторной молекулы_ 276
1.3.2. Коергизм на уровне реактивных систем и целостного организма_ 277
2. Представление данных, получаемых в ходе изучения явления коергизма_ 277
3. Токсикологическое значение явления коергизма_ 279
ГЛАВА 5.5. АНТИДОТЫ (ПРОТИВОЯДИЯ) 279
1. История вопроса. 281
2. Характеристика современных антидотов_ 281
2.1. Краткая характеристика механизмов антидотного действия 282
2.1.1. Антидоты, связывающие токсикант (химические антагонисты) 283
2.1.1.1. Прямое химическое взаимодействие_ 283
2.1.1.2. Опосредованная химическая нейтрализация. 285
2.1.2. Биохимический антагонизм_ 286
2.1.3. Физиологический антагонизм. 289
2.1.4. Противоядия, модифицирующие метаболизм ксенобиотиков. 290
2.2. Применение противоядий_ 292
3. Разработка новых антидотов. 294
3.1. Оценка эффективности. 295
3.1.1. Опыты in vitro_ 295
3.1.2. Опыты in vivo. 296
3.2. Создание комплексных антидотных рецептур_ 299
3.3. Внедрение новых антидотов в практику_ 299
3.4. Перспективы_ 300
РАЗДЕЛ 6. СПЕЦИАЛЬНЫЕ ФОРМЫ ТОКСИЧЕСКОГО ПРОЦЕССА_ 300
ГЛАВА 6.1. ИММУНОТОКСИЧНОСТЬ_ 300
1. Краткая характеристика морфологических и функциональных особенностей иммунной системы млекопитающих_ 302
1.1. Иммунокомпетентные клетки_ 302
1.2. Органы и ткани иммунной системы_ 304
1.3. Особенности функционирования системы_ 305
1.4. Иммунокомпетентность 306
2. Действие токсикантов на иммунную систему_ 306
2.1. Понятие иммунотоксичности_ 306
2.2. Иммуносупрессия 307
2.2.1. Иммуносупрессия и инфекция_ 308
2.2.2. Иммуносупрессия и канцерогенез 309
2.3. Гиперчувствителность (аллергия) 309
2.3.1. Характеристика состояния гиперчувствительности_ 309
2.3.2. Псевдоаллергические реакции_ 312
2.3.3. Иммуногены и аллергены_ 312
2.4. Аутоиммунные процессы_ 316
3. Краткая характеристика токсикантов_ 317
3.1. Бериллий. 317
4. Определение иммунотоксичности ксенобиотиков_ 318
5. Выявления иммунотоксических эффектов_ 320
5.1. Оценка иммунологического статуса_ 321
ГЛАВА 6.2. ХИМИЧЕСКИЙ МУТАГЕНЕЗ_ 324
1. Точечные мутации_ 324
1.1. Замещение нуклеотида_ 324
1.2. Выпадение или включение дополнительного нуклеотида_ 326
1.3. Репарация ДНК_ 326
2. Хромосомные аберрации_ 327
3. Условия действия мутагенов на клетки_ 327
4. Изучение мутагенной активности_ 328
4.1. Исследования в опытах на прокариотах. Тест Эймса_ 328
4.2. Исследования в опытах на клетках млекопитающих_ 329
4.3. Оценка индукции синтеза ДНК клетками млекопитающих_ 329
4.4. Исследование ковалентного связывания токсикантов 330
4.5. Изучение хромосомных аберраций_ 330
ГЛАВА 6.3. ХИМИЧЕСКИЙ КАНЦЕРОГЕНЕЗ_ 330
1.Краткая характеристика канцерогенов_ 331
2.Классификации канцерогенов_ 337
3.Стадии химического канцерогенеза_ 340
4.Механизмы действия_ 342
5.Коканцерогены_ 344
6.Метаболизм и биоактивация канцерогенов_ 345
7.Краткая характеристика токсикантов_ 347
7.1. Бензол_ 347
7.2. 1,3-бутадиен_ 349
8.Выявление канцерогенной активности веществ_ 349
8.1. Экспериментальная оценка_ 349
8.2. Эпидемиологические исследования 352
9.Оценка риска химического канцерогенеза_ 354
9.1. Проблемы оценки риска_ 354
9.2. Математические модели, описывающие зависимость доза - эффект 354
8.3. Процедуры определения пороговых уровней риска_ 356
ГЛАВА 6.4. ТОКСИЧЕСКИЕ ВЛИЯНИЯ НА РЕПРОДУКТИВНУЮ ФУНКЦИЮ. ТЕРАТОГЕНЕЗ 357
1. Краткая характеристика анатомо-физиологических особенностей репродуктивных органов 358
2. Развитие плода_ 359
3. Особенности действия токсикантов на репродуктивные функции_ 359
3.1. Тератогенез 361
3.1.1. Закономерности тератогенеза_ 362
3.1.2. Особенности токсикокинетики тератогенов_ 364
3.1.3. Механизмы действия тератогенов_ 365
4. Характеристика некоторых токсикантов, влияющих на репродуктивные функции_ 366
4.1. Талидомид_ 366
4.2. Ртуть 366
4.3. Свинец_ 367
4.4. Кадмий_ 367
4.5. Полигалогенированные бифенилы (ПГБ) 367
4.6. Органические растворители_ 368
4.7. Цитостатики_ 368
5. Выявление действия токсикантов на репродуктивную функцию. 368
5.1. Экспериментальное изучение 368
5.2. Оценка риска поражения 373
5.3. Эпидемиология токсического действия 374
5.3.1. Анализируемые показатели_ 374
5.3.2. Методы сбора информации_ 375
5.3.3. Контроль тератогенеза в популяции_ 376
РАЗДЕЛ 7. ИЗБИРАТЕЛЬНАЯ ТОКСИЧНОСТЬ_ 377
ГЛАВА 7.1. РАЗДРАЖАЮЩЕЕ ДЕЙСТВИЕ_ 377
1. Краткая характеристика химических и физико-химических свойств токсикантов_ 377
2. Патогенез токсического эффекта_ 379
3. Основные проявления раздражающего действия_ 380
4. Экспериментальное выявление раздражающего действия ксенобиотиков_ 381
ГЛАВА 7.2. ДЕРМАТОТОКСИЧНОСТЬ_ 381
1. Химические дерматиты_ 382
1.1. Контактные химические дерматиты_ 382
1.2. Аллергические дерматиты_ 384
2. Фотодерматиты_ 385
3. Токсидермии_ 385
4. Краткая характеристика некоторых токсикантов_ 387
4.1. Поражение органическими растворителями_ 387
4.2. Поражения мышьякорганическими соединениями_ 387
4.3. Поражение сернистым ипритом_ 388
4.4. Поражение альдегидами_ 389
4.5. Поражение эпоксидными смолами_ 389
4.6. Поражение щелочами_ 389
4.7. Поражение кислотами_ 390
4.7.1. Поражение хромовой кислотой_ 390
4.7.2. Поражение плавиковой кислотой. 390
5. Оценка дерматотоксичности ксенобиотиков в эксперименте 391
ГЛАВА 7.3. ПУЛЬМОНОТОКСИЧНОСТЬ_ 392
1. Краткая характеристика морфологии дыхательной системы_ 393
1.1. Назофарингиальный отдел_ 393
1.2. Трахеобронхиальный отдел_ 393
1.3. Паренхима легких_ 394
1.4. Циркуляция крови и лимфы в лёгких_ 394
2. Физиология дыхательной системы_ 395
2.1. Вентиляция 395
2.1.1. Легочные объемы_ 395
2.1.2. Рефлексы, влияющие на дыхание_ 396
2.1.3. Механизмы регуляции тонуса бронхов_ 397
2.2. Газообмен_ 398
2.3. Метаболизм ксенобиотиков и биологически активных веществ 399
2.4. Депонирование и клиаренс ксенобиотиков в легких_ 400
3. Основные формы патологии дыхательной системы химической этиологии_ 401
3.1. Острые ингаляционные поражения 402
3.1.1. Локализация поражения_ 403
3.1.1.1. Верхние дыхательные пути_ 404
3.1.1.2. Глубокие дыхательные пути_ 405
3.1.1.3. Паренхима легких_ 405
3.1.1.3.1. Пневмонии_ 405
3.1.1.3.2. Отек легких_ 406
3.1.2. Острая дыхательная недостаточность_ 409
3.1.3. Диагностика_ 410
3.1.4. Оказание помощи_ 411
3.1.5. Краткая характеристика некоторых пульмонотоксикантов_ 412
3.1.5.1. Хлор_ 412
3.1.5.2. Паракват 413
3.1.5.3. Цинк 414
3.2. Хронические патологические процессы химической этиологии_ 415
3.2.1. Аллергические и гиперреактивные заболевания легких_ 416
4. Оценка пульмонотоксичности ксенобиотиков в эксперименте 417
5. Выявления пульмонотоксического действия профессиональных и экотоксикантов_ 418
5.1. Профессиональный анамнез 419
5.2. Биологический мониторинг 420
5.3. Обследование рабочего места_ 421
ГЛАВА 7.4. ГЕМАТОТОКСИЧНОСТЬ_ 421
1. Гемопоез 421
2. Нарушение функций гемоглобина_ 422
2.1. Метгемоглобинообразование 423
2.1.1. Причины метгемоглобинообразования_ 424
2.1.1.1. Врожденная метгемоглобинемия_ 425
2.1.1.2. Приобретённая метгемоглобинемия_ 426
2.1.2. Краткая характеристика некоторых токсикантов_ 426
2.1.2.1. Анилин_ 426
2.1.2.2. Дапсон (4,4-диаминодифенилсульфон) 427
2.1.2.3. Нитриты_ 427
2.1.3. Проявления метгемоглобинемии_ 428
2.1.4. Лабораторная диагностика_ 429
2.1.5. Принципы оказания помощи_ 430
2.2. Образование карбоксигемоглобина_ 430
3. Изменение числа форменных элементов_ 432
3.1. Гемолитические анемии_ 432
3.1.2. Краткая характеристика некоторых токсикантов_ 434
3.1.2.1. Мышьяковистый водород (Арсин - AsH3) 434
3.1.2.2. Сурмянистый водород (Стибин - SbH3) 435
3.1.2.3. Тринитротолуол_ 435
3.1.3. Биомониторинг 435
3.2. Аплазия костного мозга_ 436
3.2.1. Основные проявления интоксикаций_ 437
3.2.1.1. Панцитопения. 437
3.2.1.2. Агранулоцитоз 437
3.2.1.3. Тромбоцитопения_ 437
3.3. Лейкемии_ 438
3.3.1. Распространённость_ 438
3.3.2. Диагноз 438
3.3.3. Профессиональные воздействия и лейкемии_ 438
3.4. Характеристика наиболее известных токсикантов, вызывающих патологию крови_ 439
3.4.1. Бензол_ 439
3.4.2. Свинец_ 440
3.4.3. Мышьяк 441
3.4.4. Этиленоксид_ 441
3.4.5. Эфиры гликолей_ 441
3.4.6. Производные феноксиуксусной кислоты_ 441
4. Мониторинг состояния системы крови лиц, работающих в условиях опасных производств 442
ГЛАВА 7.5. НЕЙРОТОКСИЧНОСТЬ_ 442
1. Структурно-функциональная организация нервной системы_ 442
1.1. Нейроны_ 443
1.2. Синапсы_ 445
1.3. Глиальные клетки_ 445
1.4. Цереброспинальная жидкость. 445
1.5. Гематоэнцефалический барьер. 445
1.6. Энергетический обмен_ 446
1.7. Мозговой кровоток 446
1.8. Внутричерепное давление 446
2. Причины уязвимости нервной системы для токсикантов_ 447
3. Характеристика нейротоксикантов и нейротоксических процессов. 447
3.1. Нейротоксиканты_ 447
3.2. Нейротоксические процессы_ 450
3.2.1. Механизмы действия нейротоксикантов_ 450
4. Проявления нейротоксических процессов_ 452
4.1. Острые нейротоксические процессы_ 455
4.1.1. Судорожный синдром. Конвульсанты_ 455
4.1.1.1. Конвульсанты, активирующие возбуждающие процессы в ЦНС_ 459
4.1.1.1.1. Вещества, действующие на возбудимые мембраны и нарушающие механизмы ионного транспорта_ 459
4.1.1.1.2. Вещества, активирующие холинэргические структуры мозга_ 462
4.1.1.1.3. Вещества, активирующие глютаматэргические структуры мозга_ 465
4.1.1.2. Конвульсанты, блокирующие тормозные процессы в ЦНС_ 466
4.1.1.2.1. Конвульсанты, действующие на ГАМК-ергический синапс. 466
4.1.1.2.2. Конвульсанты, действующие на глицинергические синапсы_ 473
4.1.1.3. Вещества, нарушающие процессы биоэнергетики в мозге_ 475
4.1.2. Седативно-гипнотическй эффект. Наркотики_ 476
4.1.2.1. Неэлектролиты_ 477
4.1.3. Психодислептический синдром. Психодислептики_ 482
4.1.3.1. Эйфориогены_ 486
4.1.3.2. Галлюциногены_ 486
4.1.3.3. Делириогены_ 488
4.1.4. Нарушение нервной регуляции периферических органов и систем_ 490
4.1.4.1. Нарушение механизмов синаптической передачи_ 491
4.1.4.2. Блокаторы ионных каналов_ 494
4.2. Хронические нейротоксические процессы. Токсические нейропатии_ 496
4.2.1. Токсическая сегментарная миелинопатия_ 498
4.2.2. Токсическая дистальная аксонопатия_ 498
4.2.3. Перикариальная токсическая нейронопатия_ 501
5. Оценка нейротоксичности в эксперименте 506
6. Диагностическая стратегия в нейротоксикологии_ 507
6.1. Сбор анамнестических данных_ 507
6.2. Исследование специалистами_ 508
6.3. Функциональные исследования 508
ГЛАВА 7.6. ГЕПАТОТОКСИЧНОСТЬ_ 508
1. Анатомо-физиологияческие особенности печени_ 511
2. Патологические состояния, формирующиеся при действии гепатотоксикантов_ 511
2.1. Стеатоз 511
2.2 Некроз 512
2.3. Холестаз 512
2.4. Фиброз (цирроз) 513
2.5. Канцерогенез 513
3. Морфологические формы токсического повреждения печени_ 514
4. Краткая характеристика гепатотоксикантов_ 515
4.1. Облигатные гепатотоксиканты_ 515
4.2. Идиосинкратические гепатотоксиканты_ 516
5. Условия воздействия гепатотоксикантов. 517
6. Факторы, влияющие на гепатотоксичность_ 518
7. Краткая токсикологическая характеристика отдельных гепатотоксикантов_ 518
7.1. Токсины бледной поганки_ 518
7.2. Дихлорэтан_ 519
8. Изучение гепатотоксичности ксенобиотиков_ 520
8.1. Определение активности энзимов в плазме крови. 520
8.2. Функциональные пробы_ 521
8.2.1. Оценка метаболической активности печени_ 521
8.2.2. Оценка синтетической активности печени_ 522
8.3. Структурные исследования 522
9. Принципы выявление токсических гепатопатий у человека_ 522
9.1. Острые гепатопатии химической этиологии. 522
9.2. Подострые и хронические токсические гепатотопатии_ 523
9.3. Выявление гепатотоксичности в популяции лиц, контактирующих с опасными химическими агентами. 523
10. Заключение 525
ГЛАВА 7.7. НЕФРОТОКСИЧНОСТЬ_ 525
1. Анатомо-физиологические особенности органа_ 526
2. Характеристика нефротоксического действия_ 528
2.1. Механизмы действия 528
2.1.1. Биохимические механизмы_ 528
2.1.2. Иммунологические механизмы_ 528
2.1.3. Гемодинамические механизмы_ 529
2.2. Проявления токсического действия 529
3. Краткая характеристика отдельных нефротоксикантов_ 531
3.1. Металлы_ 531
3.1.1. Свинец_ 531
3.1.2. Кадмий_ 531
3.1.3. Ртуть_ 532
3.1.4. Мышьяк 532
3.2. Технические жидкости_ 533
3.2.1. Этиленгликоль_ 533
4. Оценка нефротоксичности ксенобиотиков_ 534
5. Выявление токсических поражений почек у человека_ 534
РАЗДЕЛ 8. ЭКОТОКСИКОЛОГИЯ_ 535
8.1. ОСНОВЫ ЭКОТОКСИКОЛОГИИ_ 535
1. Ксенобиотический профиль среды_ 537
2. Экотоксикокинетика_ 538
2.2. Персистирование 538
2.3. Трансформация 539
2.3.1. Абиотическая трансформация_ 539
2.3.2. Биотическая трансформация_ 540
2.4. Процессы элиминации, не связанные с разрушением_ 541
2.5. Биоаккумуляция 541
2.5.1. Факторы, влияющие на биоаккумуляцию_ 542
2.5.2. Значение биоаккумуляции_ 543
2.6. Биомагнификация 543
3. Экотоксикодинамика_ 543
3.1. Общие понятия 543
3.2. Экотоксичность 544
3.2.1. Острая экотоксичность_ 545
3.2.2. Хроническая экотоксичность_ 545
3.2.3. Механизмы экотоксичности_ 547
4. Экотоксикометрия_ 549
4.1. Общая методология 549
4.2. Оценка экологического риска_ 550
5. Характеристика некоторых экотоксикантов, опасных для человека_ 552
5.1. Полигалогенированные ароматические углеводороды_ 552
5.1.1. Диоксины_ 552
5.1.2. Полихлорированные бифенилы (ПХБ) 554
5.1.3. Хлорированные бензолы (ХБ) 556
5.2. Металлы_ 557
5.2.1. Кадмий_ 557
ГЛАВА 8.2. СИНДРОМ НЕСПЕЦИФИЧЕСКОЙ ПОВЫШЕННОЙ ХИМИЧЕСКОЙ ВОСПРИИМЧИВОСТИ_ 559
1. Состояние проблемы_ 559
2. Неспецифическая повышенная химическая восприимчивость, как заболевание 561
3. Клиническая экология_ 561
4. Диагностика СПХВ_ 563
5. Лечение синдрома ПХВ_ 563
ЛИТЕРАТУРА ПО ТЕМЕ_ 563
Аннотация
Книга рассчитана на ознакомление читателя с фундаментальными проблемами современной токсикологии, сущностью феномена токсичности и токсического процесса, проявляющимися при взаимодействии разнообразных химических веществ с живыми системами на различных уровнях их структурно-функциональной организации: от молекулы, до популяции. Раскрывается содержание основных разделов дисциплины - токсикометрии, токсикокинетики, токсикодинамики. Представлены особенности повреждающего действия высокотоксичных веществ, профессиональных вредностей, загрязнителей окружающей среды, лекарств и др. на отдельные органы и системы организма человека и экспериментальных животных (нейротоксичность, гепато -, нефро- , иммунотоксичность и т.д.). Обсуждены факторы, влияющие на токсичность веществ, свойства и механизмы действия антидотов, применяемых при острых отравлениях. Даны характеристики специальных форм токсического процесса: мутагенеза, канцерогенеза, нарушений репродуктивных функций химической природы.
Книга предназначена главным образом для студентов медицинских институтов. Однако приведенный в монографии фактический материал и рассматриваемые теоретические проблемы носят в значительной степени универсальный характер, что существенно расширяет круг лиц, для которых она может представлять интерес (врачи различных специальностей, биологи, экологи и т.д.).
The summary
The book is intended mainly for students of medical institutes. However the actual material represented in the textbook and considered theoretical…ПРЕДИСЛОВИЕ АВТОРА
В этой книге изложены основные представления современной токсикологии. Цель, к которой я стремился при её написании - ознакомить читателей с учением о токсичности химических веществ и токсическом процессе, проблемами химической опасности, столь актуальными в современном мире, для каждого из нас, отдельных коллективов и населения в целом. Книга рассчитана главным образом на студентов-медиков, врачей и других специалистов, чьи интересы и потребности лежат в области медицины, биологии, экологии, а также смежных областях. Её основная задача - подготовить читателя к решению клинических, профилактических и организационных проблем здравоохранения, а также защиты окружающей среды с учетом представлений о химических веществах, как о важнейших потенциальных этиологических факторах, действие которых на организм может инициировать широчайший спектр патологических состояний.
В ХХ веке, в связи с бурным развитием промышленности и внедрением бесчисленного количества химических веществ практически во все сферы человеческой деятельности, возникла острая необходимость защиты человека от химической опасности. Это явилось объективной причиной появления в России и за рубежом больших коллективов специалистов, плодотворно работавших и работающих в настоящее время в трех направлениях практической токсикологии: экспериментальном, профилактическом, клиническом. Масштабы, сложность и значимость решаемых задач привлекли к проблемам ученых, ставших гордостью отечественной науки: Н.С. Правдина, Н.В. Лазарева, Н.Н., Савицкого, С.В. Аничкова, С.Н. Голикова, Л.А. Тиунова, оставивших после себя большие школы исследователей и многочисленные глубокие научные труды.
Однако, давно занимаясь преподаванием и имея в своем распоряжении обширную литературу по предмету, я не мог порекомендовать моим ученикам, желающим познакомиться с токсикологией, книг, где просто, без излишней детализации излагалось бы то, что представляется самым важным и необходимым для современного врача или биолога - общая методология процесса познания потенциальной опасности, таящейся в бесконечном многообразии химических веществ окружающего мира, в чем эта опасность состоит, в каких формах проявляется. Все, что я мог - это предложить ознакомиться с многочисленными справочниками, либо литературой по клинической и профилактической токсикологии, в которой рассматриваются, подчас достаточно глубоко, сугубо специальные, прикладные проблемы этой области знаний. Это, естественно, не удовлетворяло.
"Основы токсикологии" сформировались в результате примерно двадцати лет преподавания курса в стенах Военно-медицинской академии врачам различных специальностей, включая специалистов в области токсикологии. Некоторые разделы не преподавались ранее, но включены в книгу, поскольку без них токсикологические знания на современном этапе нельзя считать полными, а полнота охвата проблемы, целостность, структурированность содержания были моими основными ориентирами. Напротив, некоторые вопросы, обычно включаемые в традиционные курсы по клинической, профилактической, военной токсикологии, по причине их специального характера, мне пришлось либо существенно сократить, либо опустить вовсе.
Предлагаемая книга не справочник и не практическое руководство, она рассчитана на ознакомление с фундаментальными проблемами предмета. Тем, кто предпочитает более строгое изложение материала, следует обратиться к методическим документам, издаваемым ВОЗ и Минздравом России.
При написании книги я исходил из того, что читатель знаком с основами органической химии, биохимии, физиологии, общей патологии. Впрочем, глубокие знания по этим вопросам не обязательны. Минимум сведений, где в этом есть необходимость, включен в содержание глав и разделов.
Прекрасно понимая, что современная токсикология это слишком большая область человеческих знаний для того, чтобы один человек мог её полностью освоить и, тем более, изложить, я, тем не менее, решился на это, полагая, что неизбежные при этом недостатки будут хотя бы отчасти компенсированы единством подхода к предмету, определенной позицией в отношении к имеющемуся огромному фактическому материалу, известной уравновешенностью и сбалансированностью включенных в книгу разделов. Поскольку субъективная трактовка некоторых вопросов и различного рода неточности в этих условиях неизбежны, я с удовольствием приму критические замечания и предложения по поводу книги, поскольку они могли бы послужить руководством при её последующей переработке. Я был бы особенно признателен читателям, если бы они смогли указать на ошибки, оставшиеся незамеченными при чтении корректуры.
В заключении мне хотелось бы выразить глубокую благодарность моему дорогому учителю профессору Николаю Васильевичу Саватееву за уроки честного отношения к жизни и специальности, за его бескорыстную помощь в моем становлении как ученого и педагога, без чьего доброго и внимательного слова, эта книга, кто знает, могла бы и не родиться вовсе.
С. Куценко
РАЗДЕЛ 1. ВВЕДЕНИЕ
ГЛАВА 1.1. ПРЕДМЕТ И ЗАДАЧИ ТОКСИКОЛОГИИ
Предмет изучения
Попытка определения
Так, в "Энциклопедическом словаре медицинских терминов" (1982) читаем: "Токсикология - область медицины, изучающая физические,… В качестве примеров можно привести и другие определения: "Токсикология - наука, изучающая ядовитые вещества и их влияние на растительный и животный организм"…Накопленные человечеством знания давно привели к осознанию того факта, что практически любое химическое вещество, в зависимости от действующего количества, может быть безразличным, полезным, вредным для организма (т.е. выступать в качестве яда).
Впервые на это указал еще в ХV веке выдающийся врач, химик, основоположник ятрохимии Теофраст Бомбаст фон Гогенгейм (Парацельс). В своей оправдательной речи, сказанной им по поводу обвинения в отравлении больных ядами (солями металлов, которые он применял в качестве лекарств), Парацельс произнес: "Все есть яд. Ничто не лишено ядовитости. И только доза отличает яд от лекарства".
Таким образом, понятие о яде никак не может быть положено в основу определения токсикологии. Не удивительно, что ученые пытаются исключить этот термин из своих определений. Так, Олдридж (1980) пишет: "Токсикология - наука о веществах, дезорганизующих биологические системы". Но мы уже знаем, что дезорганизовать биосистемы могут практически любые вещества, действуя в достаточном количестве, и в таком случае токсикология - это наука практически обо всех веществах окружающего мира.
Не смотря на общую критику, приведенных выше определений, следует признать, что все они содержат, несомненно, правильные элементы. Так, токсикология действительно изучает механизмы вредного действия веществ на организм человека и животных, закономерности развивающихся при этом патологических процессов, разрабатывает методы диагностики, лечения и профилактики отравлений и т.д.
Однако все сказанное выше призвано подчеркнуть важнейшее обстоятельство - химические вещества, обладают неким свойством, в силу которого их контакт с биологическими системами может иметь пагубные последствия для последних. Это свойство - токсичность.
Токсичность
Вещества существенно различаются по токсичности. Чем в меньшем количестве вещество способно вызывать повреждение организма, тем оно токсичнее… Таблица 1. Сравнительная токсичность некоторых веществ для белых мышей (доза, вызывающая гибель при внутрибрюшинном способе введения) Вещество Источник Токсичность…Токсикология - наука о токсичности - свойстве, присущем практически всем химическим веществам окружающего мира.
Действие веществ, приводящее к нарушению функций биологических систем, называется токсическим действием. В основе токсического действия лежит взаимодействие вещества с биологическим объектом на молекулярном уровне. Химизм взаимодействия токсиканта и биологического объекта на молекулярном уровне называется механизмом токсического действия.
Следствием токсического действия веществ на биологические системы является развитие токсического процесса.
Токсический процесс
Формирование и развитие реакций биосистемы на действие токсиканта, приводящих к её повреждению (т.е. нарушению её функций, жизнеспособности) или… Механизмы формирования и развития токсического процесса, его качественные и… + Щелкните для загрузки увеличенной копии (2,93кб, 561x153 GIF) …Формы проявления токсического процесса на разных уровнях организации жизни
Проявления токсического процесса определяются уровнем организации биологического объекта,на котором токсичность вещества изучается: - клеточном; - органном;Основные характеристики токсического процесса, выявляемого на уровне целостного организма
Токсические процессы, выявляемые на уровне организма, можно отнести к одной из следующих групп:
А. Процессы, формирующиеся по пороговому принципу.
Б. Процессы, развивающиеся по беспороговому принципу.
1.3.2.1. Интоксикация (отравление) Из всех форм проявления токсического процесса наиболее изученной и в… 1. В зависимости от продолжительности взаимодействияхимического вещества и организма интоксикации могут быть острыми,…Другие формы токсического процесса
Транзиторные токсические реакции наиболее часто развиваются вследствие раздражающего и седативно-гипнотического действия токсикантов.
При действии наркотических средств, многих лекарств, органических растворителей, пищевых продуктов (спирт) в малых дозах проявляется их… Транзиторные токсические реакции могут стать следствием только острого… Аллобиоз.К числу аллобиотических состояний можно отнести:Цель и задачи токсикологии
Цель токсикологии, как области человеческой деятельности - непрерывное совершенствование системы мероприятий, средств и методов, обеспечивающих сохранение жизни, здоровья и профессиональной работоспособности отдельного человека, коллективов и населения в целом в условия повседневного контакта с химическими веществами и при чрезвычайных ситуациях.
Эта цель достигается путем решения фундаментальных и прикладных токсикологических задач:
1. Установление количественных характеристик причинно-следственных связей между фактом воздействия каждого из известных человеку химических веществ и развитием различных форм токсического процесса; оценка токсичности веществ. Раздел токсикологии, в рамках которого совершенствуется методология и осуществляется оценка токсичности химических веществ, называется "токсикометрия". Результаты токсикометрических исследований в медицинской практике используют для разработки системы нормативных и правовых актов, обеспечивающих химическую безопасность населения; оценки риска действия ксенобиотиков в условиях производства, экологических и бытовых контактов с токсикантами; сравнительной оценки эффективности средств и методов обеспечения химической безопасности населения и т.д.
2. Изучение механизмов, лежащих в основе токсического действия различных химических веществ, закономерностей формирования токсического процесса, его проявлений. Эта задача решается с помощью методических приемов, разрабатываемых и совершенствуемых в рамках раздела токсикологии "токсикодинамика". Токсикодинамические характеристики веществ необходимы для разработки медикаментозных средств профилактики и терапии интоксикаций, средств и методов предупреждения и минимизации пагубных последствий развития иных форм токсического процесса; совершенствования методов диагностики интоксикаций и оценки функционального состояния лиц, подвергшихся воздействию сверхнормативных доз токсикантов; совершенствования методов оценки токсичности ксенобиотиков и биотестирования исследуемых проб.
3. Выяснение механизмов проникновения токсикантов в организм, закономерностей их распределения, метаболизма и выведения. Совокупность методических приемов, используемых для решения задачи, и накопленных сведений формируют раздел токсикологии - "токсикокинетика". Знания токсикокинетики ксенобиотиков необходимы для разработки надежной системы профилактики токсических воздействий; диагностики интоксикаций, выявления профессиональной патологии, проведения судебно-медицинской экспертизы; они широко используются в процессе создания новых противоядий и схем их оптимального использования; совершенствования методов форсированной детоксикации организма и т.д.
4. Установление факторов, влияющих на токсичность вещества: свойств токсикантов, особенностей биологических объектов, условий их взаимодействия, состояния окружающей среды и т.д.
Все упомянутые задачи решаются в ходе экспериментальных исследований на животных, в процессе лечения острых и хронических отравлений человека в условиях клиники, эпидемиологических исследований среди профессиональных групп и населения, подвергшихся действию токсикантов.
Структура токсикологии
Экспериментальная токсикологияизучает общие закономерности взаимодействия веществ и биологических систем (зависимости: "доза токсиканта -… Профилактическая токсикология изучает токсичность новых химических веществ;… Клиническая токсикология - область практической медицины, связанная с оказанием помощи при острых токсических…ГЛАВА 1.3. ТОКСИКАНТ (ЯД)
Общая характеристика токсикантов
Помимо термина яд в токсикологии используют и другие термины, характеризующие химические вещества, как потенциальную или реализовавшуюся причину… Токсикант - более широкое понятие, употребляющееся не только для обозначения… Нередко в токсикологической литературе используют термин ксенобиотик, подчеркивая тем самым, что некое химическое…В качестве токсикантов (ядов) могут выступать практически любые соединения различного строения, если, действуя на биологические системы не механическим путем, они вызывают их повреждение или гибель.
В настоящее время известны тысячи химических веществ, используемых человеком в быту, медицине, на производстве, в сельском хозяйстве. Поскольку, как следует из определения, по сути, любое из химических веществ при тех или иных условиях может вызвать токсический процесс, полная классификации токсикантов возможна только на принципе их химического строения. Она-то и положена в основу наиболее подробных справочных пособий по токсикологии как у нас в стране, так и за рубежом ("Вредные вещества в промышленности"; "Вредные химические вещества"). Однако такая классификация не позволяет составить общего представления о содержании проблемы химической опасности. Предлагаемая читателю структура токсикантов является рубрикатором, позволяющим идентифицировать химическую опасность по ряду принципов:
По происхождению
1.1. Токсиканты естественного происхождения
1.1.1. Биологического происхождения
1.1.1.1. Бактериальные токсины
1.1.1.2. Растительные яды
1.1.1.3. Яды животного происхождения
1.1.2. Неорганические соединения
1.1.3. Органические соединения небиологического происхождения
1.2. Синтетические токсиканты
По способу использования человеком
2.1. Ингредиенты химического синтеза и специальных видов производств
2.2. Пестициды
2.3. Лекарства и косметика
2.4. Пищевые добавки
2.5. Топлива и масла
2.6. Растворители, красители, клеи
2.7. Побочные продукты химического синтеза, примеси и отходы
По условиям воздействия
3.1. Загрязнители окружающей среды (воздуха, воды, почвы, продовольствия)
3.2. Профессиональные (производственные) токсиканты
3.3. Бытовые токсиканты
3.4. Вредные привычки и пристрастия (табак, алкоголь, наркотические средства, лекарства и т.д.)
3.5. Поражающие факторы при специальных условиях воздействия
3.5.1. Аварийного и катастрофального происхождения
3.5.2. Боевые отравляющие вещества и диверсионные агенты
Краткая характеристика отдельных групп токсикантов
Токсиканты биологического происхождения
Бактериальные токсины
Таблица 1. Бактериальные токсины белковой и полипептидной природы Общее число Продуцируемые: -Грам-позитивными организмами … (J.E. Alouf, 1982) Многие бактериальные токсины относятся к числу самых ядовитых из известных веществ. Это, прежде всего, ботулотоксин,…Микотоксины
Рисунок 2. Структура некоторых микотоксинов Аналоги эрготамина действуют на центральную нервную систему, вызывают спазм кровеносных сосудов и сокращение…Токсины высших растений
Рисунок 4. Структура некоторых фитотоксинов Особенно многочислен класс алкалоидов (табл. 2).Токсины животных (зоотоксины)
Химическое строение зоотоксинов чрезвычайно разнообразно. Это и энзимы, и другие протеины, олиго- и полипептиды, липиды, биогенные амины, гликозиды,… Высокотоксичные соединения относительно простого строения обнаружены в тканях…Неорганические соединения естественного происхождения
В естественных условиях металлы встречаются в форме руд и минералов. Они определяются в воздухе, почве и воде. Выплавка металлов из руд и… Большую опасность представляют некоторые органические соединения металлов… В группу газообразных поллютантантов входят вещества, находящиеся в газообразном состоянии при нормальной температуре…Органические соединения естественного происхождения
Рисунок 7. Структура отдельных представителей полициклических ароматических… Поскольку отдельные ПАУ являются канцерогенами, их рассматривают как опасные экотоксиканты.Синтетические токсиканты
Пестициды
Таблица 4. Классы пестицидов Классы Основные химические группы Альгициды оловоорганические соединения… Структура некоторых из них представлены на рисунке 7.Органические растворители
1. Алифатические углеводороды (пентан, гексан, октан и др.); 2. Галогенированные алифатические углеводороды (хлороформ: CHCl3;… 3. Алифатические алкоголи (этанол, метанол и т.д.);Лекарства, пищевые добавки, косметика
Рисунок 10. Структура некоторых препаратов - частых причин острых… Еще одна токсикологическая проблема, связанная с использованием лекарств, это наличие у многих из них так называемых…Боевые отравляющие вещества (БОВ)
В годы 2-й Мировой войны химическое оружие применяли в крайне ограниченных масштабах. Тем не менее работы по созданию новых образцов ОВ не… Рисунок 11. Структура некоторых боевых отравляющих веществГЛАВА 1.2. БИОСИСТЕМЫ - МИШЕНИ ДЕЙСТВИЯ ТОКСИКАНТОВ
Уровни организации биологических систем
Молекулярная организация живого чрезвычайно сложна. В состав организма входят молекулы различного строения. Это и простые вещества (кислород, азот,… Молекулярные системы состоят из нескольких молекул, изменяющих в процессе… В процессе ассоциации отдельных молекул и молекулярных систем образуются функциональные комплексы, цепи, сети.…Термодинамика биосистем. Термодинамические аспекты токсичности
Клетки, или тем более, многоклеточные организмы, являются высокоорганизованными структурами, в сравнении с окружающей их средой, то есть… Это возможно лишь при условии открытости биологической системы, т.е.… Таким образом развитие высокоорганизованных биологических структур есть процесс, в ходе которого понижается энтропия…Фундаментальные свойства живых систем.
1. Потребление из окружающей среды и превращение питательных веществ (подсистем) с низкой энтропией (метаболизм). Это необходимо для поддержания… 2. Обмен веществом и энергией с окружающей средой. Таким путем обеспечивается… 3. Регуляция. Поддержание структурно-функциональной организации биологической системы требует упорядоченности течения…Степени свободы токсического воздействия
Высшие организмы, характеризующиеся большой массой и высокой степенью организации, имеют специальные анатомо-физиологические образования,… С увеличением сложности организации живого эволюционно формируются… И так, суммируя сказанное: по мере совершенствования организации живой материи возрастает многообразие её форм,…ГЛАВА 1.4. СВОЙСТВА ТОКСИКАНТА, ОПРЕДЕЛЯЮЩИЕ ТОКСИЧНОСТЬ
Токсичность разных веществ не одинакова. Поскольку она проявляется во взаимодействии ксенобиотика с биологической системой, её величина зависит от свойств как токсиканта, так и биосистемы и в конечном итоге определяется:
1. Способностью вещества достичь структуры-мишени, взаимодействие с которой инициирует токсический процесс;
2. Характером и прочностью связи, образующейся между токсикантом и структурой-мишенью;
3. Значением структуры-мишени для поддержания гомеостаза в организме.
Строение биологических систем, особенности их морфо-функциональной организации в значительной степени неизменны в масштабах исторически обозримого времени. В этой связи, поскольку вещество обладает вполне определенными свойствами, оно оказывает на организм (биологическую систему) воспроизводимый с известным постоянством эффект. Изменение свойств действующего фактора (воздействие другим веществом) будет сопровождаться качественными и/или количественными изменениями развивающихся эффектов. Важнейшим принципом токсикологии является зависимость качественных и количественных характеристик развивающегося токсического процесса от строения действующего вещества.
Строение вещества определяет размеры молекулы, её массу, растворимость, летучесть, агрегатное состояние при нормальных условиях и химическую активность. Все эти свойства влияют на токсичность вещества, вместе с тем, ни одно из них не является единственно значимым.
Размеры молекулы
а). С увеличением молекулярной массы затрудняется процесс поступления токсиканта в организм и распределения его в органах и тканях. Низкомолекулярные, инертные в химическом отношении вещества в виде газа или в… Для высокомолекулярных соединений процесс прохождения через барьерные структуры, как правило, затруднен. С другой…Геометрия молекулы токсиканта
Молекулы веществ могут быть ригидными и гибкими. Ригидные молекулы имеют постоянную пространственную организацию. Это прежде всего вещества,… Рисунок 1. Цис- и транс-форма дихлорэтанаФизико-химические свойства вещества
А. Растворимость в воде. Растворимость токсиканта в воде - необходимое условие его резорбции во… Таблица 1. Растворимость некоторых производных бензола в воде (г/100г; С300)Стабильность в среде
После попадания в организм большая часть ксенобиотиков с различной скоростью подвергается биотрансформации. Так, при поступлении в…Химические свойства.
Большинство высоко токсичных соединений - инертные в химическом отношении молекулы. Сила межмолекулярного взаимодействия между токсикантом и… Иногда между токсикантом и молекулой-мишенью образуются прочные связи. В этих…Типы химических связей, образующихся между токсикантами и молекулами-мишенями организма
Таблица 3. различные типы связей, формирующихся между токсикантами и молекулами-мишенями организма Вид связи Пример Энергия… Ионная связь. В водных растворах многие вещества диссоциируют с образованием… А- + В+ АВРАЗДЕЛ 2. ТОКСИКОДИНАМИКА
ГЛАВА 2.1. МЕХАНИЗМЫ ТОКСИЧЕСКОГО ДЕЙСТВИЯ
Взаимодействие токсиканта или продуктов его превращения в организме со структурными элементами биосистем, лежащее в основе развивающегося токсического процесса, называется механизмом токсического действия. Взаимодействие осуществляется за счет физико-химических и химических реакции.
Токсический процесс, инициируемый физико-химическими реакциями, как правило, обусловлен растворением токсиканта в определенных средах (водной или липидной) клеток и тканей организма. При этом существенно изменяются физико-химические свойства среды-растворителя (рН, вязкость, электропроводность, сила межмолекулярных взаимодействий и т.д.). Особенность данного типа взаимодействия - отсутствие строгой зависимости качества развивающегося эффекта от химических свойств молекулы токсиканта. Таким образом, действуют на ткани все кислоты, щелочи, сильные окислители, некоторые органические растворители и лишенные специфической активности высокомолекулярные соединения.
Чаще в основе токсического действия лежат химические реакции токсиканта с определенным структурным элементом живой системы. Структурный компонент биологической системы, с которым вступает в химическое взаимодействие токсикант, называется его "рецептором" или "мишенью".
Механизмы токсического действия подавляющего большинства химических веществ в настоящее время неизвестны. В этой связи, очень многие описываемые ниже классы молекул и молекулярных комплексов, образующих организм, рассматриваются, по большей части, лишь как вероятные рецепторы (мишени) действия ядов. Рассмотрение их в этом ракурсе правомочно, поскольку в основе действия некоторых хорошо изученных токсикантов лежит взаимодействие с представителями именно этих классов биомолекул.
1. Определение понятия "рецептор" в токсикологии
Понятие "рецептор" весьма емкое. Наиболее часто в биологии его используют в следующих смыслах:
1. Общее понятие. Рецепторы - это участки относительно специфического связывания на биосубстрате ксенобиотиков (или эндогенных молекул), при условии, что процесс связывания подчиняется закону действующих масс. В качестве рецепторов могут выступать целые молекулы белков, нуклеиновых кислот, полисахаридов, липидов или их фрагменты. В отношении фрагмента биомолекулы, которая непосредственно участвует в образовании комплекса с химическим веществом, часто используют термин - "рецепторная область". Например, рецептором оксида углерода в организме является молекула гемоглобина, а рецепторной областью - ион двухвалентного железа, заключенный в порфириновое кольцо гема.
2. Селективные рецепторы. По мере эволюционного усложнения организмов формируются специальные молекулярные комплексы - элементы биологических систем, обладающие высоким сродством к отдельным химическим веществам, выполняющим функции биорегуляторов (гормоны, нейромедиаторы и т.д.). Участки биологических систем, обладающие наивысшим сродством к отдельным специальным биорегуляторам, получили название "селективные рецепторы". Вещества, взаимодействующие с селективными рецепторами в соответствии с законом действующих масс, называются лигандами селективных рецепторов. Взаимодействие эндогенных лигандов с селективными рецепторами имеет особое значение для поддержания гомеостаза.
Многие селективные рецепторы состоят из нескольких субъединиц, из которых лишь часть имеет участки связывания лигандов. Нередко термин "рецептор" используют для обозначения только таких лиганд-связывающих субъединиц.
3. Постоянные рецепторы - это селективные рецепторы, строение и свойства которых кодируется с помощью специальных генов или постоянных генных комплексов. На уровне фенотипа изменение рецептора путем генной рекомбинации развивается чрезвычайно редко. Возникающие порой в ходе эволюции вследствие полигенетических трансформаций изменения аминокислотного состава белка, формирующего селективный рецептор, как правило, слабо сказывается на функциональных характеристиках последнего, его сродстве к эндогенным лигандам и ксенобиотикам.
К числу постоянных рецепторов относятся:
- рецепторы нейромедиаторов и гормонов. Как и другие селективные рецепторы, эти рецепторы способны избирательно взаимодействовать и с некоторыми ксенобиотиками (лекарствами, токсикантами). Ксенобиотики могут при этом выступать как в качестве агонистов, так и антагонистов эндогенных лигандов. В итоге активируется или подавляется некая биологическая функция, находящаяся под контролем данного рецепторного аппарата;
- энзимы - белковые структуры, селективно взаимодействующие с субстратами, превращение которых они катализируют. Энзимы также могут взаимодействовать с чужеродными веществами, которые в этом случае становятся либо ингибиторами, либо аллостерическими регуляторами их активности;
- транспортные протеины - избирательно связывают эндогенные лиганды определенного строения, осуществляя их депонирование или перенос через различные биологические барьеры. Токсиканты, взаимодействующие с транспортными протеинами, также выступают либо в качестве их ингибиторов, либо аллостерических регуляторов.
4. Рецепторы с изменяющейся структурой. В основном это антитела и антигенсвязывающие рецепторы Т-лимфоцитов. Рецепторы данного типа формируются в клетках предшественниках зрелых клеточных форм вследствие индуцированной внешними воздействиями рекомбинации 2 - 5 генов, контролирующих их синтез. Если рекомбинация осуществилась в процессе дифференциации клеток, то в зрелых элементах будут синтезироваться рецепторы только определенного строения. Таким способом формируются селективные рецепторы к конкретным лигандам, а пролиферация приводит к появлению целого клона клеток, содержащих эти рецепторы.
Как следует из приведенных определений, в биологии термин "рецептор" в основном используется для обозначения структур, принимающих непосредственное участие в восприятии и передаче биологических сигналов, и способных избирательно связывать помимо эндогенных лигандов (нейромедиаторов, гормонов, субстратов) некоторые чужеродные соединения.
В токсикологии (как и фармакологии) термином "рецептор" обозначают любой структурный элемент живой (биологической) системы, с которым вступает в химическое взаимодействие токсикант (лекарство). В таком прочтении это понятие ввел в химеобиологию в начале ХХ века Пауль Эрлих (1913).
Спектр энергетических характеристик рецептор-лигандного взаимодействия необыкновенно широк: от формирования слабых, легко разрушающихся связей, до образования необратимых комплексов (см. выше). Характер взаимодействия и структура сформировавшегося комплекса зависят не только от строения токсиканта, конформации рецептора, но и от свойств среды: рН, ионной силы и т.д. В соответствии с законом действующих масс, количество образовавшихся комплексов вещество-рецептор определяется энергией взаимодействия (сродством) и содержанием обоих компонентов реакции (вещества и рецептора к нему) в биологической системе.
Рецепторы могут быть "немыми" и активными. "Немой" рецептор - структурный компонент биологической системы, взаимодействие которого с веществом не приводит к формированию ответной реакции (например, связывание мышьяка белками, входящими в состав волос, ногтей). Активный рецептор - структурный компонент биологической системы, взаимодействие которого с токсикантом инициирует токсический процесс. Для того, чтобы избежать терминологических трудностей, для обозначения структурных элементов, взаимодействуя с которыми токсикант инициирует токсический процесс, вместо термина "рецептор", часто используют термин "структура-мишень".
Принимаются постулаты:
- токсическое действие вещества выражено тем сильнее, чем большее количество активных рецепторов (структур-мишеней) вступило во взаимодействие с токсикантом;
- токсичность вещества тем выше, чем меньшее его количество связывается с "немыми" рецепторами, чем эффективнее оно действует на активный рецептор (структуру-мишень), чем большее значение имеет рецептор и повреждаемая биологическая система для поддержания гомеостаза целостного организма.
Любая клетка, ткань, орган содержат огромное количество потенциальных рецепторов различных типов ("запускающих" различные биологические реакции), с которыми могут вступить во взаимодействие лиганды. С учетом вышесказанного, связывание лиганда (как эндогенного вещества, так и ксенобиотика) на рецепторе данного типа является избирательным лишь в определенном диапазоне концентраций. Увеличение концентрации лиганда в биосистеме приводит к расширению спектра типов рецепторов, с которыми он вступает во взаимодействие, а следовательно, изменению его биологической активности. Это также одно из фундаментальных положений токсикологии, доказанное многочисленными наблюдениями.
Мишенями (рецепторами) для токсического воздействия могут быть:
- структурные элементы межклеточного пространства;
- структурные элементы клеток организма;
- структурные элементы систем регуляции клеточной активности.
Действие токсиканта на элементы межклеточного пространства
Попав в межклеточную жидкость, токсикант может изменять её физико-химические свойства, вступать в химическое взаимодействие с её структурными… 1. Электролитные эффекты. Нарушение электролитного состава наблюдается при… 2. рН-эффекты. Интоксикация рядом веществ, не смотря на высокую буферную емкость межклеточной жидкости, может…Действие токсикантов на структурные элементы клеток
Структурными элементами клеток, с которыми взаимодействуют токсиканты, как правило, являются:
- белки;
- нуклеиновые кислоты;
- липидные элементы биомембран;
- селективные рецепторы эндогенных биорегуляторов (гормонов, нейромедиаторов и т.д.).
Взаимодействие токсикантов с белками.
Нарушение свойств белков химическим веществом возможно различными способами, зависящими как от структуры токсиканта, так и от строения и функций… К числу веществ, денатурирующих белки, относятся крепкие щелочи, кислоты,… Особое значение в токсикологии придают действию ксенобиотиков на энзимы.Энзимы
Роль энзимов в обеспечении процессов жизнедеятельности огромна. Неудивительно, что вещества, модулирующие их активность, обладают высокой биологической активностью, порой являются высокотоксичными веществами.
Энзимы - это белки, выполняющие функции биологических катализаторов. Они ускоряют достижение состояния равновесия обратимых экзергических реакций, типа: АВ  А + В, путем снижения энергии активации субстратов. Высокая энергия активации многих экзергических реакций препятствует их протеканию в условиях температурного режима организма. Примером таковых является расщепление перекиси водорода. in vitro предварительное нагревание увеличивает кинетическую энергию молекул Н2О2, что и инициирует процесс, который, будучи экзотермическим, в дальнейшем сам поддерживает свое течение. В условиях организма связывание перекиси водорода энзимом пероксидазой приводит к снижению энергии активации, что обеспечивает прохождение реакции в условиях температуры тела.
А + В, путем снижения энергии активации субстратов. Высокая энергия активации многих экзергических реакций препятствует их протеканию в условиях температурного режима организма. Примером таковых является расщепление перекиси водорода. in vitro предварительное нагревание увеличивает кинетическую энергию молекул Н2О2, что и инициирует процесс, который, будучи экзотермическим, в дальнейшем сам поддерживает свое течение. В условиях организма связывание перекиси водорода энзимом пероксидазой приводит к снижению энергии активации, что обеспечивает прохождение реакции в условиях температуры тела.
Скорость каталитических превращений веществ в организме определяется специфической активностью энзимов, их содержанием в клетках и тканях, наличием субстратов и регуляторов активности в среде. При нормальных условиях интенсивность процессов поддерживается на определенном уровне. Регуляция осуществляется различными механизмами, среди которых основные - модуляция количества энзимов, их специфической активности, изменение биодоступности субстратов и т.д. Основные пути регуляции ферментативных процессов представлены на рисунке 1.
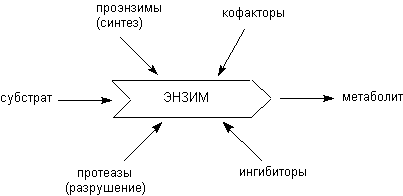
Рисунок 1. Пути регуляции ферментативных процессов
Возможные механизмы модуляции активности энзимов химическими веществами представлены в таблице 1.
Таблица 1. Механизмы изменения каталитической активности энзимов в условиях действия токсикантов
| Усиление каталитической активности - усиление синтеза энзимов - блокада разрушения энзимов - активация энзимов |
| Угнетение каталитической активности - угнетение синтеза энзимов - ускорение разрушения энзимов - угнетение специфической активности |
| Изменение конформации энзимов |
Усиление каталитической активности
Физиологическими индукторами синтеза энзимов являются многие субстраты и вещества, повышающие содержание коэнзимов в биосредах. Некоторые гормоны… Особое значение для токсикологии имеет явление индукции энзимов, участвующих в… К числу индукторов относятся барбитураты, циклические углеводороды, полигалогенированные полициклические углеводороды…Угнетение каталитической активности
К числу наиболее распространенных кофакторов, помимо металлов, относятся железопорфирины, флавины, никотинамид-адениндинуклеотид (НАД),… Некоторые токсиканты нарушают образование коферментов, предшественники которых поступают в организм с пищей. Так,…Биологические последствия действия токсикантов на энзимы
Поскольку все процессы в живых организмах протекают при участии энзимов, и все фундаментальные свойства живых систем неразрывно связаны с нормальным течением этих процессов, теоретически любые проявления жизни могут быть нарушены теми или иными токсикантами, изменяющими активность энзимов.
Взаимодействие токсикантов с нуклеиновыми кислотами.
1. Химическая модификация нуклеиновых кислот. К числу веществ, вступающих в химическое взаимодействие с нуклеиновыми…Взаимодействие токсикантов с липидами
Взаимодействие токсикантов с селективными рецепторами
Селективные рецепторы клеточных мембран
- формирующие ионные каналы; - связанные с G-протеинами; - обладающие тирозинкиназной активностью;Изучение локализации рецепторов в биообъекте
Часто для выявления рецепторов в органах и тканях используют метод авторадиографии. При этом о характере их распределения часто судят по… Метод компьютерной томографии, в частности позитронно-эмиссионная компьютерная…Понятие полирецепторного профиля связывания токсиканта
Сказанное выше относится к токсикантам с различными механизмами токсического действия, в том числе и влияющим на нейромедиаторный аппарат. В малых… В связи с изложенным, важным, при изучении механизмов токсического действия…Радиолигандные методы изучения процесса взаимодействия токсиканта с рецепторами
Количественно оценить сродство токсиканта к рецептору можно с помощью радиолигандных методов исследования. При этом, однако, эффекты, развивающиеся… а). Принцип метода с полным насыщением рецептора состоит в добавлении в… KD = [ R] [ L] /[ RL] (1)ГЛАВА 2.2. МЕХАНИЗМЫ ЦИТОТОКСИЧНОСТИ
В основе токсического действия веществ лежит повреждение клеток, сопровождающееся их функциональными, либо структурно-функциональными изменения. Разнообразие формирующихся при этом эффектов со стороны целостного организма обусловлено сложностью организации клеток, многообразием клеточных форм, составляющих организм. Сформировавшиеся в процессе эволюции особенности структуры и функции отдельных клеточных типов, формирующих различные органы и ткани, настолько существенны, что чувствительность различных клеток к токсикантам может отличаться в тысячи раз. Тем не менее, живое объединено общностью фундаментальных свойств (см. выше), а это позволяет выделить и некоторые общие механизмы, лежащие в основе цитотоксического действия ксенобиотиков. К числу важнейших можно отнести следующие:
- нарушение энергетического обмена;
- нарушение гомеостаза внутриклеточного кальция;
- активация свободно-радикальных процессов в клетке;
- нарушение процессов синтеза белка и клеточного деления;
- повреждение клеточных мембран;
Необходимо отметить, что все эти механизмы тесно связаны друг с другом. Порой один из них является пусковым, но в дальнейшем особую значимость для судьбы поврежденной клетки приобретают другие. Очень часто два или несколько из упомянутых механизмов связаны между собой по типу "порочного круга". В этой связи их выделение носит искусственный характер и оправдывается только целями данного издания.
Нарушение процессов биоэнергетики
Системы энергообеспечения клетки
А + В АВ, то существует и некая константа равновесия, характеризующая силу этого… К = [ АВ] /([ А] + [ В] ).Механизмы токсического повреждения систем энергообеспечения клетки
Рисунок 2. Механизмы действия токсикантов на биоэнергетические процессы Мышьяк, ртуть, их органические и неорганические соединения, другие тяжелые металлы, иодацетат и проч., могут…Нарушение гомеостаза внутриклеточного кальция
В норме низкая концентрация кальция в цитоплазме поддерживается механизмами его активного транспорта через биомембраны и системой его… Рисунок 5. Схема регуляции содержания ионов кальция в цитоплазме.Повреждение цитоскелета
Велика роль структур, формирующих цитоскелет в нервных клетках. Здесь микрофиламенты и микротрубочки принимают участие в монтаже системы… При действии разнообразных веществ на изолированные клетки (культура ткани)…Активация фосфолипаз
Активация протеаз
Идентифицированы две изоформы энзимов - с высоким и низким сродством к кальцию, обе активируемые этим ионом. В эксперименте показано, что стойкая,…Активация эндонуклеаз
Установлено, что кальций участвует в активации эндонуклеаз. Вызванная глюкокортикоидами фрагментация ДНК тимоцитов и гибель этих клеток связаны со… Активация эндонуклеаз может быть причиной гибели клеток печени, миокарда,…Активация свободно-радикальных процессов в клетке
Сущность явления
Рисунок 8. Примеры простых свободных радикалов Хорошо доказана возможность образования радикалов при метаболизме ацетаминофена, адриамицина (и других цитостатиков…Механизмы клеточной антирадикальной защиты
Механизмы антирадикальной защиты включают как ферментативные, так и неферментативные процессы. Самым простым примером некаталитического разрушения… Наиболее важной неферментативной реакцией "обезвреживания" радикалов… Гомеостаз в клетке поддерживается за счет равенства скоростей образования и связывания радикалов. В случае повреждения…Механизмы активации ксенобиотиков и образования свободных радикалов
Рисунок 11. Вещества, инициирующие свободно-радикальные процессы путем… Ионы металлов с переменной валентностью (медь, железо) облегчают процесс аутоокисления, а восстановители, например…Биологические последствия активации свободно-радикального процесса в клетке
Характер повреждающего действия активных радикалов во многом определяется их стабильностью и расстоянием, на которое они могут мигрировать от места… Наивысшей реакционной способностью обладают промежуточные продукты,… Следующими по реакционной способности являются вещества, покидающие область локализации фермент-субстратного…Повреждение мембранных структур
Основные свойства и функции биологических мембран
Мембрана образована двумя слоями молекул липидов, гидрофобные части которых направлены друг к другу, а гидрофильные в сторону окружающей и… В мембрану встроены белковые молекулы, которые часто пронизывают всю ее толщу,… Плазматические мембраны, несмотря на преимущественно липидный состав, способны пропускать низкомолекулярные…Действие токсикантов на мембраны
Прямое действие на мембраны
В результате неспецифического действия многочисленных токсикантов (бензола, толуола, динитробензола, хлороформа, мылов, сапонинов, смачивающих… Действуя в малых дозах на возбудимые мембраны нервных клеток ЦНС, органические… Многие токсиканты избирательно действуют на мембраносвязанные энзимы, транспортные системы, рецепторные комплексы к…Активация перекисного окисления липидов
Не смотря на многочисленные исследования до настоящего времени нет четких представлений о значении активации перекисного окисления липидов для… Для развития патологического процесса важно, чтобы… Для развития процесса важна степень насыщенности тканей кислородом. В полностью аэробной среде образующийся из…Активация фосфолипаз
Результатом действия фосфолипазы А2 на липиды биологических мембран является высвобождение арахидоновой кислоты. Последняя является, в свою очередь,… Еще одним продуктом энзиматического расщепления липидов мембран является… + Щелкните для загрузки увеличенной копии (8,23кб, 595x576 GIF) Рисунок 16.…Биологические последствия действия токсикантов на мембраны
1. Проницаемость. Изменяется поступление субстратов в клетки и отток продуктов метаболизма. Действие проявляется изменением интенсивности обмена… 2. Электрический заряд. Нарушается раздражимость возбудимых клеток. 3. Структурная организация. Нарушается структура клетки, возможна клеточная гибель.Синтез РНК. Транскрипция
1. Нарушение конформации и свойств ДНК (см. выше). На поврежденной ДНК синтезируется измененные молекулы РНК, не свойственные… 2. Угнетение активности РНК-полимераз.Синтез белков. Трансляция
1. Нарушение конформации рибосом и организации полисом. Этот механизм экспериментально показан для целого ряда антибиотиков,… 2. Угнетение процесса образования полипептидной цепи.Биологические последствия действия токсикантов на нуклеиновый обмен и синтез белка
Повреждающее действие химических веществ на ДНК называется генотоксическим. Наиболее чувствительны к генотоксическому действию клетки, способные к… Таблица 5. Условия воздействия генотоксиканта, определяющие форму развития… Существует представление, согласно которому проникновение в организм даже единственной молекулы генотоксиканта (в…ГЛАВА 2.3. ДЕЙСТВИЕ ТОКСИКАНТОВ НА МЕХАНИЗМЫ РЕГУЛЯЦИИ КЛЕТОЧНОЙ АКТИВНОСТИ
Существование высших форм организации живого стало возможным только благодаря кооперативному взаимодействию частей в рамках целостного организма. Так как состояние клеток, в силу их специфических свойств, определяет функциональное состояние организма в целом, клеточная активность должна регулироваться в соответствии с потребностями макроорганизма. Таким образом, кооперация, прежде всего, означает регуляцию. Можно выделить три основных механизма регуляции клеточной активности: прямое межклеточное взаимодействие, нервный и гуморальный контроль. Каждый из этих механизмов может стать объектом токсического воздействия.
1. Прямое межклеточное взаимодействие
Самая простая форма взаимодействия - влияние на соседние клетки продуктами собственного метаболизма. Межклеточное пространство для большинства тканей составляет около 15 нм, поэтому метаболиты за счет простой диффузии преодолевают это расстояние с большой скоростью. Кроме того между отдельными клетками возможен прямой обмен веществом через области межклеточных контактов, так называемые коннексоны. Во многих тканях клетки вырабатывают специальные биологически активные вещества, влияющие на функциональное состояние соседних структур. Особенно богато такими локальными биорегуляторами сосудистое русло. Здесь синтезируются и действуют оксид азота, эндотелины, лейкотриены, тромбоксаны, простогландины, фактор агрегации тромбоцитов. К числу таких веществ относится большая группа цитокинов и т.д. Механизм действия некоторых токсикантов может быть связан с активацией процесса образования этих веществ, ингибированием разрушения, имитацией их действия (агонисты). Так, полагают, что в основе регулирующего действия оксида азота на тонус сосудов лежит его способность образовывать с некоторыми эндогенными SH-содержащими веществами нестабильные нитрозотиолы. Период полусуществования такого соединения в организме 3 - 5 секунд:
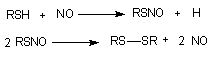
Падение артериального давления, наблюдаемое при отравлении такими веществами, как NaNO2, нитропруссид, органические нитраты и нитриты может быть обусловлено образованием нитрозотиолов, т.е. вещества в данном случае могут проявлять свойства агонистов NO.
Тесный контакт между клетками обеспечивает сдерживание их размножения. Механическое разобщение клеток (пороз) провоцирует клеточный рост. Установлено, что у клеток злокачественных опухолей повреждены структуры, воспринимающие сигналы контактного ингибирования, поэтому даже в условиях полного окружения другими клетками они продолжают бурно размножаться. Не исключено, что в этом состоит один из механизмов канцерогенного действия токсикантов.
2. Механизмы гуморальной регуляции
С увеличением массы тела и сложности организации многоклеточного организма механизмы межклеточного взаимодействия становятся недостаточными для обеспечения регуляции его функций. Формируются специальные типы клеток, функция которых состоит в контроле за физиологической активностью других клеточных систем (эндокринные железы). Их влияние передаётся через кровь и межклеточную жидкость. В качестве переносчиков информации (веществ-регуляторов) выступают продукты метаболизма этих специальных клеток (гормоны). В регулируемых же клетках формируется специальный рецепторный аппарат, чутко реагирующий на изменение концентрации в окружающей среде соответствующих регуляторов (см. раздел "Селективные рецепторы"). Активация рецепторов приводит к изменению функциональной активности клеток. Рецепторная система усиливает воспринимаемый сигнал. Так, инсулин или глюкагон, концентрация которых в плазме составляет около 0,1 нМ, регулирует уровень глюкозы, содержание которой в крови - около 5 мМ. Гормоны модулируют специфическую активность определенных энзимов, влияют на скорость их синтеза и разрушения, регулируют транспорт химических веществ через биологические мембраны.
Действие гормона на органы и системы определяется его концентрацией в крови, а также наличием и количеством рецепторов чувствительных к нему в данной ткани. Концентрация гормона, в свою очередь, зависит от интенсивности процессов его синтеза и разрушения. Возможна интоксикация гормональными препаратами при их необоснованном введении или применении в дозах, существенно превышающих рекомендуемые.
Так как поступивший в кровь гормон разносится по всему организму, специфичность действия определяется характером распределения в тканях соответствующих рецепторов. Если рецепторы к гормону имеются у всех клеток организма, то и действие он оказывает на все органы и ткани (инсулин, катехоламины и т.д.).
Можно выделить две основные группы гормонов с учетом механизма их действия.
1. Гормоны, регулирующие процессы синтеза белка. К числу таких относятся эстроген, андроген, тироксин, трииодтиронин, соматотропин, глюкокортикоиды, инсулин, АКТГ и некоторые другие. Эти гормоны усиливают белковый синтез. Их действие нарушается блокаторами синтеза белка: актиномицином, пуромицином и др. (см. выше). Индуцирующая активность гормонов по-разному реализуется в разных тканях. Эффект наступает после продолжительного латентного периода (от нескольких часов, до суток). Практически значимыми являются проблемы, связанные с хроническим отравлением этими гормонами или их синтетическими аналогами.
2. Гормоны, регулирующие содержание вторичных месенджеров (цАМФ, цГМФ, диацилглицерол, фосфоинозитиды и др.) в клетках. К числу гормонов, действующих подобным образом относятся катехоламины, окситоцин, вазопрессин, инсулин, глюкогон, паратгормон и другие. Аналогичным образом действуют такие биологически активные вещества, как простогландины, серотонин, гистамин, ангиотензин и др. Эти гормоны взаимодействуют с соответствующими рецепторами, локализующимися на клеточной поверхности, что и приводит к изменению содержания в клетках регуляторов клеточной активности (см. выше). Распределение этих рецепторов в тканях определяет характер действия на них гормонов.
Гормоны, относящиеся к этой группе, действуют быстро. Латентный период продолжается несколько минут. Эффект не блокируется ингибиторами синтеза белка, но усиливается некоторыми веществами, например ингибиторами фосфодиэстераз (энзимы, активирующие процесс разрушения циклических нуклеотидов в клетках). Возможно острое отравление гормонами данной группы или их синтетическими аналогами. Например, в эксперименте острое отравление инсулином (острую гипогликемию) можно вызвать у крыс, предварительно голодавших в течение нескольких суток.
3. Механизмы нервной регуляции
Высший уровень регуляции функционального состояния клеток, органов, систем появляется с формированием у живых организмов нервной системы. Структурной единицей нервной системы является нервная клетка (нейрон), осуществляющая контакт, как с большим количеством других нейронов, так и клетками периферических органов. Мозг человека, по некоторым данным состоит из 1010 нейронов, каждый из которых имеет около 104 контактов с другими клетками. Под контролем нервной системы находятся все органы и системы организма. Так как скорость передачи сигнала по нервным волокнам велика, то и эффект реализуется с минимальным латентным периодом. Это свойство нервной системы чрезвычайно важно, поскольку позволяет организму быстро реагировать на изменяющиеся условия окружающей среды, используя органы чувств, управляя двигательной активностью, регулируя состояние внутренних органов.
Между собой и с периферическими структурами нервные клетки связаны нервными волокнами. Передача информации по волокнам осуществляется с помощью электрического и химического механизмов. Распространение сигнала по волокну имеет электрическую природу. Область контакта между окончанием нервного волокна и иннервируемой клеткой называется синапсом. Нервный импульс, достигнув нервного окончания (пресинаптические структуры), вызывает высвобождение химического вещества (нейромедиатора), которое, диффундируя через пространство, отделяющее нервное окончание от поверхности иннервируемой клетки (синаптическая щель), действует на селективные рецепторы (постсинаптические) и вызывает их возбуждение. Возбуждение рецептора приводит к изменению потенциала постсинаптической мембраны. Таким образом, инициируется ответная реакция клетки, находящейся под контролем нейрона. Выделившийся в синаптическую щель нейромедиатор взаимодействует с постсинаптическими рецепторами, подвергается энзиматическому расщеплению либо обратному захвату пресинаптическими структурами. Часть высвободившегося нейромедиатора взаимодействует с пресинаптическими рецепторами, возбуждая их, и по механизму обратной связи прерывает дальнейший выброс и активирует обратный захват.
Для передачи нервного импульса в синапсах в качестве медиаторов различные нейроны используют различные химические вещества. Нейромедиаторы синтезируются в пресинаптических структурах и находятся здесь в связанной форме, главным образом в специальных клеточных органелах, так называемых синаптических везикулах. В каждой везикуле, в среднем, содержится до 104 молекул нейромедиатора.
В настоящее время в ЦНС и на периферии идентифицировано более 17 типов регуляторных систем (классификация по строению нейромедиатора), на которые оказывают влияние, в том числе, и токсиканты: холинергическая (мускариночувствительная - 4 подтипа, никотиночувствительная - 2 подтипа), адренергическая (9 подтипов), дофаминергическая (5 подтипов), серотонинергическая (5 подтипов), ГАМК-ергическая (2 подтипа), глутаматергическая (4 подтипа), глицинергическая (1 подтип), гистаминергическая (3 подтипа), опиоидная (4 подтипа), пуринергическая (6 подтипов), пептидергическая (более 5 типов) и т.д.
Помимо "классических" медиаторов нервного импульса в нервной ткани определяются другие вещества, как правило пептидной природы, модулирующие эффекты нейромедиаторов на синаптические рецепторы. В настоящее время таких нейромодуляторов в ЦНС млекопитающих идентифицировано более 60 (таблица 1). Помимо ЦНС эти вещества определяются и в других органах (сосуды, желудочно-кишечный тракт и др.). Некоторые из них одновременно являются гормонами (см. выше).
Таблица 1. Некоторые пептидные модуляторы нервной системы млекопитающих
| Рилизинг-гормоны (РГ) гипоталамуса - тиреотропин-РГ - гонадотропин-РГ - соматотропин-РГ - кортикотропин-РГ |
| Гормоны нейрогипофиза - вазопрессин - окситоцин - нейрофизин |
Пептиды гипофиза - АКТГ - пролактин - лютеинизирующий гормон - соматотропин - 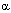 -меланотропин - -меланотропин - 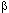 -эндорфин
- тиреотропин - глицил-глутамин -эндорфин
- тиреотропин - глицил-глутамин
|
| Гастро-интестинальные пептиды - гастрин - субстанция Р - нейротензин - энкефалины - инсулин - глюкагон - секретин - бомбезин - соматостатин - мотилин |
| Другие пептиды - ангиотензин 11 - брадикинин - карнозин - кальцитонин - нейропептид Y |
В основе действие токсикантов на передачу нервного импульса лежат следующие механизмы (рис. 1):
- влияние на синтез, хранение, высвобождение и обратный захват нейромедиатора;
- непосредственное действие на селективные рецепторы;
- изменение сродства рецепторных структур к нейромедиаторам;
- изменение скорости синтеза, разрушения и распределения рецепторов в тканях;
- модификация состояния механизмов сопряжения между рецептором и эффекторной системой клеток.
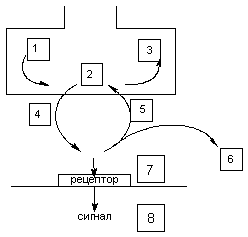
Рисунок 1. Места действия токсикантов на синапс. Схема этапов оборота нейромедиатора, воздействуя на которые токсикант может инициировать токсический процесс:
1 - синтез
2 - хранение
3 - метаболизм
4 - выделение
5 - обратный захват
6 - разрушение
7 - рецептор
8 - механизм проведения сигнала
4. Особенности токсического повреждения механизмов регуляции клеточной активности
В результате токсического действия ксенобиотиков на регуляторные механизмы формируются нарушения восприятия, памяти, мышления, двигательной активности, гемодинамики, дыхания, вегетативных процессов, метаболизма в органах и тканях и др. При этом обращают на себя внимание следующие закономерности:
1. Чем в большей степени токсикант структурно напоминает естественный биорегулятор, тем специфичнее его действие на организм, при этом, в зависимости от свойств, он либо имитирует эффект биорегулятора (агонист), либо блокирует его (антагонист). Таким образом, влияют на синаптические механизмы нервной регуляции многие алкалоиды (атропин, никотин, анабазин, мускарин, скополамин, курарин и т.д.) и огромное количество синтетических ядов.
2. Будучи аналогом биологически активного вещества, токсикант, тем не менее, может оказывать влияние лишь на часть эффектов, контролируемых в организме этим биорегулятором. Лучше всего этот феномен изучен для веществ, действующих на холинэргические синапсы (нейромедиатор - ацетилхолин). С помощью ацетилхолина нервный импульс передается в центральной нервной системе, вегетативных ганглиях, нервно-мышечных синапсах, нервных окончаниях парасимпатических волокон, иннервирующих гладкомышечные образования и железистую ткань. Однако рецепторы, взаимодействующие с медиатором, в перечисленных структурах имеют существенные особенности и оказываются чувствительными лишь к некоторым токсикантам. Так, алкалоид атропин действует преимущественно на нервные окончания парасимпатических волокон и некоторые виды холинергических синапсов ЦНС. При этом нервно-мышечные и ганглионарные синапсы остаются интактными. Алкалоид никотин, напротив, преимущественно действует на нервно-мышечные и ганглионарные синапсы.
Помимо различий структурно-функциональной организации рецепторов неодинаковое сродство органов и тканей к токсикантам - аналогам биорегуляторов, может быть обусловлено особенностями токсикокинетики ксенобиотиков.
3. Вещества, изменяющие количество нейромедиатора, находящегося в синаптической щели в момент передачи нервного импульса, как правило, обладают высокой токсичностью. Это обусловлено тем обстоятельством, что степень возбуждения постсинаптических рецепторов определяется количеством образующихся комплексов медиатор - рецептор в единицу времени, а, следовательно, зависит от концентрации медиатора в синаптической щели. В основе токсического действия таких веществ лежит нарушение механизмов синтеза нейромедиаторов (гидразин и его производные), их высвобождения (тетанотоксин, ботулотоксин) и разрушения (ФОС, карбаматы).
Действие токсикантов на рецепторы не редко сопровождается существенным изменением количественных и качественных характеристик последних.
4.1. Изменение числа рецепторов, вызываемое действием ксенобиотиков.
Число селективных рецепторов на клеточной мембране определяется соотношением скоростей процессов их разрушения и синтеза. Период полуобращения известен для очень ограниченного количества рецепторов. В среднем это время для различных рецепторов колеблется от трех суток до нескольких недель.
Поскольку рецепторы представляют собой белковые молекулы, их биосинтез ничем не отличается от синтеза других белков. Достаточно подробно, например, изучен процесс синтеза никотинэргического рецептора. После "сборки" полипептидной цепи на соответствующих полисомах белковая молекула встраивается в мембрану шероховатого эндоплазматического ретикулума, а затем с фрагментами этой мембраны переходит в везикулы аппарата Гольджи. Везикулы перемещаются в окончания нервных отростков с цитоплазматическим током, сливаются с клеточной мембраной, а в следствие экзоцитоза, молекула оказывается на поверхности клетки. Время синтеза рецепторной структуры составляет около 150 минут.
Некоторые ксенобиотики (особенно при длительном воздействии на организм) в состоянии оказывать влияние на синтез, биодоступность и разрушение тех или иных рецепторов. В итоге изменяются свойства как биорецепторных систем, так и организма в целом, в частности, его чувствительность к токсикантам.
4.1.1. Уменьшение количества рецепторов при воздействии токсикантов
Уменьшение количества рецепторов, как правило, является следствием длительного действия токсиканта - агониста эндогенного лиганда рецептора, либо самого лиганда в несвойственных организму концентрациях. Примерами рецепторов, для которых экспериментально доказана возможность такой реакции, являются рецепторы к ацетилхолину, инсулину, пролактину, а также рецепторы с тирозинкиназной активностью. В данном случае разрушение интернализировавшегося рецептора и его синтез идут параллельно. При хроническом стимулировании структуры развивается постепенное, но стойкое снижение числа рецепторов за счет неспособности процессов синтеза компенсировать усиленный распад рецептора.
Указанный эффект имеет особое значение при длительном использовании некоторых лекарств. Так, прием агонистов  2-адренорецепторов (изопреналин) лицами, страдающими бронхиальной астмой, со временем приводит к нарушению механизмов нервной регуляции дыхательных путей. Систематический прием психофармакологических препаратов может приводить к нарушению функций ЦНС.
2-адренорецепторов (изопреналин) лицами, страдающими бронхиальной астмой, со временем приводит к нарушению механизмов нервной регуляции дыхательных путей. Систематический прием психофармакологических препаратов может приводить к нарушению функций ЦНС.
4.1.2. Увеличение числа мембраносвязанных рецепторов при воздействии токсикантов
Противоположным, описанному выше, является процесс увеличения числа рецепторов при действии ксенобиотиков. Это может быть следствием длительной блокады рецепторов антагонистом эндогенного лиганда (нейромедиатора, гормона), либо повреждения токсикантом проводящих путей, по которым нервный импульс поступает к клеткам-мишеням. До настоящего времени не ясно, является ли увеличение числа рецепторов следствием угнетения процесса их разрушения или усиления синтеза.
Для клеток, способных к дифференциации (клетки иммунной системы), имеет значение индукция экспрессии рецепторов. В этой связи хорошо изученной является модуляция числа рецепторов интерлейкина-2. Количество этих рецепторов может быть оценено как путем определения количества связывающегося клетками вещества, так и с помощью специфических моноклональных антител. В процессе индукции иммунного ответа незрелые Т-лимфоциты стимулируются таким образом, что начинают синтезировать рецепторы интерлейкина и встраивать их в клеточную мембрану. Вследствие этого у клеток и появляется способность взаимодействовать с этими биологически активными веществами, что необходимо для дальнейшей дифференциации и специализации Т-клеток.
4.2. Десенсибилизация рецепторов
Термин "десенсибилизация" используют в нескольких смыслах. Иногда это понятие применяют для обозначения явления снижения выраженности реакции клеток на токсикант, развивающегося вследствие уменьшения числа рецепторов к нему (см. выше). Более правильно этим термином обозначать явление быстро развивающегося понижения реактивности рецепторно-эффекторного комплекса клеток вследствие действия на него агониста. То есть, в узком смысле слова, десенсибилизация - это переход рецептора в новое состояние (иную конформацию) после его взаимодействия с агонистом, при котором продолжение действия вещества не приводит к дополнительной активации эффекторной системы. Рецептор, находящийся в этой конформации переходит в неактивное состояние. Этот феномен в эксперименте выявляется при действии на биологический объект различных ксенобиотиков в возрастающей концентрации.
Каково значение явления десенсибилизации в обычных физиологических условиях остаётся не ясным. Между тем известно, что в нормальных условиях в активном состоянии находится лишь малая часть рецепторов к эндогенным лигандам.
РАЗДЕЛ 3. ТОКСИКОМЕТРИЯ
ГЛАВА 3.1. ЗАВИСИМОСТЬ "ДОЗА-ЭФФЕКТ" В ТОКСИКОЛОГИИ
1. Общие замечания
Спектр проявлений токсического процесса, определяются строением токсиканта. Однако выраженность развивающегося эффекта является функцией количества действующего агента.
Для обозначения количества вещества, действующего на биологический объект, используют понятие - доза. Например, введение в желудок крысе весом 250 г и кролику весом 2000 г токсиканта в количестве 500 мг, означает, что животным введены дозы равные соответственно 2 и 0,25 мг/кг (более подробно понятие "доза" будет рассмотрено ниже).
Зависимость "доза-эффект" может быть прослежена на всех уровнях организации живой материи: от молекулярного до популяционного. При этом в подавляющем большинстве случаев будет регистрироваться общая закономерность: с увеличением дозы - увеличивается степень повреждения системы; в процесс вовлекается все большее число составляющих её элементов.
В зависимости от действующей дозы практически всякое вещество в определенных условиях может оказаться вредным для организма. Это справедливо для токсикантов, действующих как местно (таблица 1), так и после резорбции во внутренние среды (таблица 2).
Таблица 1. Зависимость между концентрацией формальдегида во вдыхаемом воздухе и выраженностью токсического процесса
| Концентрация (см3/м3 - ppm) | Клинические проявления |
| 0,01 - 0,05 | Раздражение глаз |
| 0,05 - 1,00 | Непереносимый запах |
| 0,05 - 3,00 | Раздражение верхних дыхательных путей |
| 3,00 - 10,00 | Сильное раздражение слизистой дыхательных путей |
| 10,00 - 30,00 | Раздражение глубоких дыхательных путей |
| 50,00 - 100,00 | Воспалительный процесс в легких; токсический отек |
(P.M. Misiak, J.N. Miceli, 1986)
Таблица 2. Зависимость между концентрацией этанола в крови и выраженностью токсического процесса
| Концентрация мг/100 мл | Клинические проявления |
| 20 - 99 | Изменение настроения; прогрессирующее нарушение координации движений, сенсорных функций; изменение поведения |
| 100 - 199 | Выраженные нарушения мышления; увеличение времени реакции на внешние раздражители; атаксия |
| 200 - 299 | Тошнота; рвота; выраженная атаксия |
| 300 - 399 | Гипотермия; дизартрия; амнезия; 1 стадия анестезии |
| 400 - 700 | Кома; угнетение дыхания; смерть |
(T.G. Tong, D. Pharm, 1982)
На проявление зависимости "доза-эффект" оказывает существенное влияние внутри- и межвидовая изменчивость организмов. Действительно, особи, относящиеся к одному и тому же виду, существенно отличаются друг от друга по биохимическим, физиологическим, морфологическим характеристикам. Эти отличия в большинстве случаев обусловлены их генетическими особенностями. Еще более выражены, в силу тех же генетических особенностей, межвидовые различия. В этой связи дозы конкретного вещества, в которых оно вызывает повреждение организмов одного и того же и, тем более, разных видов, порой очень существенно различаются. Следовательно, зависимость "доза-эффект" отражает свойства не только токсиканта, но и организма, на который он действует. На практике это означает, что количественную оценку токсичности, основанную на изучении зависимости "доза-эффект", следует проводить в эксперименте на различных биологических объектах, и обязательно прибегать к статистическим методам обработки получаемых данных.
2. Зависимость "доза-эффект" на уровне отдельных клеток и органов
Предварительные замечания
2.2. Основные понятияГЛАВА 3.2. ЭПИДЕМИОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ В ТОКСИКОЛОГИИ
В ряде случаев, очевидно, что причина того или иного заболевания - действие химического вещества. Например, отек легких после действия хлора или фосгена, развитие судорожного синдрома вследствие воздействия фосфорорганического вещества, угнетение кроветворения как итог контакта с ипритом и т.д. Однако нередко трудно доказать наличие причинно-следственной связи между действием токсиканта и развитием конкретной патологии у человека. Огромное число симптомов и синдромов заболеваний неспецифично, и их возникновение возможно в результате пример инфекционных, факторов. Это является причиной неопределенности суждений как в случае выявления заболеваний (связаны ли они с воздействием токсикантов?), так и в случае оценки возможных последствий воздействия токсикантов (выявляются ли неблагоприятные для здоровья эффекты?). Затруднения часто возникают также, когда недуг развивается в результате длительного действия вещества в малых дозах, а проявлению патологического процесса предшествует длительный скрытый период (канцерогенез). Задачи подобного свойства усложняются еще и тем, что реакция людей на токсикант в определенной дозе колеблется в очень широких пределах: от практически не диагностируемых субклинических эффектов, до отчетливо выраженных заболеваний.
доказательства значения химического вещества, как этиологического фактора, в токсикологии используют ряд методических приемов:
- экспериментальное изучение зависимости "структура-активность";
- полномасштабные исследования на лабораторных животных токсичности, механизма действия, особенностей повреждения отдельных органов и систем, канцерогенной, мутагенной, тератогенной активности;
- краткосрочные скрининговые исследования для уточнения отдельных сторон токсического действия;
- глубокий анализ случаев острых и хронических интоксикаций в условиях клиники;
- компьютерное моделирование;
- эпидемиологические исследования популяций людей, подвергающихся действию токсикантов.
Ни один из указанных приемов не лишен недостатков. Поэтому конечное решение вырабатывается с учетом данных, получаемых всеми методами. В последние годы, как весьма продуктивный, зарекомендовал себя метод эпидемиологических исследований.
Эпидемиологические исследования в токсикологии основываются на выявлении различий в состоянии здоровья отдельных людей и популяций, находящихся в условиях воздействия химических соединений, в сравнении с контрольными группами. Подобные исследования строятся на наблюдениях над естественно складывающимися событиями. Поэтому основное различие между экспериментом и эпидемиологическим анализом состоит в том, каким образом формируется база анализируемых данных. В ходе экспериментального исследования сам экспериментатор активно создает группу объектов будущего анализа, воздействуя на организм оцениваемым фактором в требуемых условиях. В ходе эпидемиологических исследований воздействие изучаемого фактора никак не регулируется исследователем. Под его контролем находятся только этапы выбора из генеральной совокупности репрезентативных групп обследуемых и подбор адекватных методов анализа полученной информации.
По указанной причине эпидемиологический анализ позволяет сформировать гипотезы, выявить важные тенденции, но не даёт исчерпывающих доказательств наличия причинно-следственных связей между воздействием и наблюдаемым эффектом, и в этом его ограниченность. Тем не менее в медицинской науке этот метод играет все возрастающую роль. По всей видимости, при изучении влияния факторов среды на здоровье людей, эпидемиологический анализ может оказаться единственно полезным методом, поскольку эксперимент на людях не возможен. Но в этой связи совершенно недопустимы скоропалительные выводы по итогам исследований, а ответственность исследователей перед обществом весьма велика.
Принципиально возможны два типа ошибок в ходе эпидемиологических исследований. Ошибка первого типа: ложно позитивный результат - декларация наличия причинно-следственной связи между оцениваемым фактором и эффектом там, где её реально нет; ошибка второго типа: ложно отрицательный результат - декларация отсутствия связи при её реальном наличии.
Любое эпидемиологическое исследование включает следующие этапы:
- уяснения задачи предстоящей работы;
- выбор замысла исследования;
- сбор фактического материала;
- выбор математического аппарата анализа баз данных;
- обработка данных;
- анализ полученных результатов;
- формулировка выводов и предложений.
Основные категории и типы эпидемиологических исследований
- описательные; - аналитические (этиологические); - интервенционные.Основные показатели, привлекаемые для организации эпидемиологических исследований
Классификация показателей
Можно выделить четыре группы показателей, используемых в эпидемиологическом исследовании:
- показатели состояния обследуемой популяции (группы);
- характеристики исследуемого фактора (строение токсиканта, концентрация в окружающей среде или биосредах, продолжительность воздействия, колебания интенсивности воздействия во времени и т.д.);
- показатели, характеризующие другие факторы, модулирующие действие основного (вредные привычки: курение, прием лекарств, отношение к алкоголю и т.д., производственные условия, характер работы, место жительства и т.д.);
- "запутывающие" факторы (социальная принадлежность, пол, возраст, раса и др.). Влияние "запутывающих" факторов можно исключить, путем составления программы исследования, в которой предусмотрено равномерное распределение этих факторов в сравниваемых группах, использования соответствующих статистических методик. Важно представлять, что "запутывающий" фактор в одном исследовании может являться основным в другом.
Получаемые и анализируемые данные, в зависимости от условий, могут представляться: а) в альтернативной (категорийной) форме (типа "да - нет"); б) в виде шкалы непрерывных количественных показателей (концентрация токсиканта в среде, величина артериального давления у обследуемых); в) в форме порядковых показателей (уровень воздействия: - отсутствует - низкий - средний - высокий).
Показатели состояния обследуемой популяции
Заболеваемость в популяции является показателем риска развития заболевания. Она определяется числом новых случаев заболеваний (появление эффекта) в… Распространенность анализируемого эффекта характеризует долю лиц с… В эпидемиологических исследованиях часто используют производные характеристики заболеваемости и распространенности,…Замысел эпидемиологического исследования
Метод регистрации серии событий
В тех случаях, когда наблюдаемый эффект является следствием действия нескольких факторов, выводы, построенные только на результатах исследования… 3.2. Исследование типа "случай-контроль" (болезнь - контроль). Исследования типа "случай-контроль" позволяют сравнительно надежно определять относительный риск,…Метод когортных исследований
При формировании когорт важно учитывать, что многие виды патологии имеют длительный скрытый период, поэтому продолжительность проспективного… Исходя из сказанного, для решения неотложных задач по установлению… В известном смысле метод когортных исследований является обратным методу исследований типа "случай-контроль"…Другие методы
Экотоксикологические исследования предполагают анализ функционального состояния не отдельных лиц, а целых групп населения, находящихся в условиях…Интерпретация результатов (принципы формирования выводов)
В настоящее время в токсикологии признано, что степень научной обоснованности вывода о наличии причинно-следственных связей между действием… - достоверностью и выраженностью математических характеристик силы связи между… - специфичностью выявленной связи;ГЛАВА 3.3. ОЦЕНКА РИСКА ДЕЙСТВИЯ ТОКСИКАНТА
Человек подвержен действию огромного количества вредных химикатов, следовательно, всегда имеется риск возможного вреда, причиняемого ими. Очень часто общество нуждаются в разумных, обоснованных предложениях о путях снижения риска. Такие предложения могут быть сделаны только на основе информации о вероятности и характере вредного действия. Это и послужило поводом для разработки методологии оценки риска, которая предназначена для его идентификации, характеристики и измерения.
Исторические аспекты
2. Что такое оценка риска? Риск - это вероятность ущерба здоровью, или более точно, вероятность травмы,… Базовой информацией для проведения исследования является токсикологическая характеристика вещества, риск от…Процесс оценки риска
1. Идентификация опасности; 2. Оценка воздействия; 3. Оценка токсичности;Идентификация опасности
Все доступные данные по токсикантам собираются, систематизируются и используются для оценки токсического потенциала веществ. Если в среде…Оценка воздействия
В ходе работы желательно выявить часть населения с повышенной чувствительностью к ксенобиотику. Необходимо тщательно проанализировать пути… В результате получают данные, позволяющие оценить количество вещества,… I = C R D / W T , где:Оценка токсичности
Фактор безопасности является своеобразным допущением, учитывающим неполноту или недостаточность наших знаний о токсичности вещества. Фактор… Таблица 2. Величины фактора безопасности, используемые при оценке риска и…Характеристика риска
Если вещество проявляет свойства канцерогена в документе должно быть представлено значение риска развития новообразований в конкретных условиях,…Недостатки методологии оценки риска
Каждый этап оценки риска предполагает формирование определенных выводов при отсутствии исчерпывающей информации, необходимой для этого. В этой связи… Существует четыре основных источника появления неопределенности в методологии… - влияние свойств и особенностей окружающей среды на эффекты, вызываемые токсикантами;Экстраполяция данных
Необходимость экстраполяции диктуется объективными причинами. Так, оценка токсичности осуществляется в опытах на лабораторных животных. Вместе с тем… Таблица 3. Сравнительная токсичность некоторых веществ для человека и… (А. Rowan, 1983)Неадекватные исследования
Различия в механизмах токсического действия
Популяционные различия
В последнее время в токсикологических лабораториях часто используют инбредных животных. Получаемые в этом случае результаты варьируют не в столь…Неопределенность при оценке воздействия
Уровень воздействия, частота, продолжительность, способ воздействия никогда в полной мере не являются неизменными. Источник воздействия, например… Факторы окружающей среды, такие как температура, влажность воздуха, скорость… Изложенные обстоятельства - важные источники неопределенности, поскольку не могут быть полностью учтены.Неопределенность, связанная с комбинированным действием токсикантов
Заключение
До настоящего времени многие ученые противятся распространению методологии оценки риска, поскольку считают его не в полной мере адекватным решаемым задачам. Причина этого в высокой степени неопределенности получаемых результатов, в основе которой - скудость наших знаний в области токсикологии огромного количества токсикантов, окружающих современного человека, общих законов науки токсикологии, несовершенство методологии определения токсичности и т.д.
Конечно хотелось бы, основываясь на строгом научном подходе, идентифицировать и устранить все источники риска для здоровья человека. Поэтому следует уделять пристальное внимание развитию методологии оценки риска, но при этом каждому должно быть понятно, что нулевой риск, в частности от действия химических веществ - недостижимая иллюзия.
РАЗДЕЛ 4. ТОКСИКОКИНЕТИКА
ГЛАВА 4.1. ОБЩИЕ ЗАКОНОМЕРНОСТИ
Токсикокинетика - раздел токсикологии, в рамках которого изучаются закономерности, а также качественные и количественные характеристики резорбции, распределения, биотрансформации ксенобиотиков в организме и их элиминации (рисунок 1).

Рисунок 1. Этапы взаимодействия организма с ксенобиотиком
С позиций токсикокинетики организм представляет собой сложную гетерогенную систему, состоящую из большого числа компартментов (отделов): кровь, ткани, внеклеточная жидкость, внутриклеточное содержимое, с различными свойствами, отделенных друг от друга биологическими барьерами. К числу барьеров относятся клеточные и внутриклеточные мембраны, гистогематические барьеры (например, гематоэнцефалический), покровные ткани (кожа, слизистые оболочки). Кинетика веществ в организме - это, по сути, преодоление ими биологических барьеров и распределение между компартментами (рисунок 2).

Рисунок 2. Схема движения веществ в основных компартментах организма
В ходе поступления, распределения, выведения вещества осуществляются процессы его перемешивания (конвекция), растворения в биосредах, диффузии, осмоса, фильтрации через биологические барьеры.
Конкретные характеристики токсикокинетики определяются как свойствами самого вещества, так и структурно-функциональными особенностями организма.
Важнейшими характеристиками вещества, влияющими на его токсикокинетические параметры, являются:
- коэффициент распределения в системе масло/вода - определяет способность накапливаться в соответствующей среде: жиро-растворимиые - в липидах; водо-растворимые - в воде;
- размер молекулы - влияет на способность диффундировать в среде и проникать через поры биологических мембран и барьеров;
- константа диссоциации - определяет относительную часть молекул токсиканта, диссоциировавших в условиях внутренней среды организма, т.е. соотношение молекул, находящихся в ионизированной и неионизированной форме. Диссоциировавшие молекулы (ионы) плохо проникают через ионные каналы и не проникают через липидные барьеры;
- химические свойства - определяют сродство токсиканта к химическим и биохимическим элементам клеток, тканей и органов.
Свойства организма, влияющие на токсикокинетику ксенобиотиков.
- соотношение воды и жира в клетках, тканях и органах. Биологические структуры могут содержать либо мало (мышечная ткань), либо много жира… - наличие молекул, активно связывающих токсикант. Например в костях имеются… Свойства биологических барьеров:Растворение и конвекция
Конвекция.Без явления конвекции жизнь организма была бы невозможна, так как только благодаря ей осуществляется быстрый обмен веществами между… Так, через органы с общей массой 7% от массы тела (мозг, легкие, сердце,… Движущей силой конвекции является градиент давления крови р, создаваемый периодическим сокращением сердечной мышцы.…Диффузия в физиологической среде
Диффузия веществ в воде описывается уравнением Фика: Y = -Дp C/ l S t, где Y - количество диффундирующего вещества;Диффузия веществ через липидные мембраны
Многочисленные исследования проницаемости биологических барьеров для химических веществ (модель - эритроциты, эпителиальные слои и т.д.) показывают,… Процесс проникновения жирорастворимых веществ через липидные мембраны можно… 1. Переход молекулы из водной фазы в гидрофобную фазу биологической мембраны;Диффузия через поры
Рисунок 3. Зависимость проницаемости биологических барьеров от размеров… Можно представить, что с увеличением размеров молекул их взаимодействие со стенками белковых каналов все в большей…Межклеточный транспорт химических веществ
Диффузия растворенных газов
Количество газа, растворенного в жидкости, определяется: 1. Величиной его парциального давления в газовой смеси над жидкостью; 2. Свойствами жидкости;Осмос
Осмос - процесс перемещения растворителя через мембрану, не проницаемую для растворенного вещества, в сторону его более высокой концентрации.
Биологические жидкости представляют собой многокомпонентные растворы, в которых осмотическое давление всех растворенных частиц пропорционально их общей концентрации. При интоксикациях осмотическое давление внутри и вне клеток за счет попадания во внутреннюю среду молекул токсикантов практически не изменяется. Тем не менее это явление имеет определенное токсикологическое значение.
Клетки организма ведут себя, как осмометр, снабженный полупроницаемой мембраной. Если они взаимодействуют с гипоосматической средой, внутрь клеток поступает вода. В результате увеличивается их объем. При значительном увеличении объема клеточная мембрана разрушается, клеточное содержимое выходит в среду. Это явления называется цитолизом (для эритроцитов - гемолизом). Вещества, нарушающие эластичность биологических мембран (мышьяковистый водород, сурьмянистый водород и др.), снижают резистентность клеток к колебаниям осмотического давления среды и вызывает гемолиз. Реакция антиген-антитело может приводить к существенному изменению проницаемости клеточных мембран, а это в свою очередь также становится причиной лизиса клеток. В гиперосмотической среде клетки отдают воду, и объем их уменьшается (в крови появляются "звездчатые" эритроциты).
В целом явление осмоса оказывает несущественное влияние на токсикокинетические характеристики ксенобиотиков. Однако при назначении осмотических диуретиков удается существенно повысить интенсивность процесса отделения мочи путем увеличения осмотического давления жидкости внутри почечных канальцев, и затруднения тем самым реабсорбции воды. В этих условиях ускоряется процесс элиминации выделяемых через почки некоторых ксенобиотиков и продуктов их метаболизма.
Фильтрация
Скорость фильтрации или объем жидкости, проходящий через пористую мембрану за единицу времени зависит от: 1. Различия гидростатического давления по обе стороны мембраны, т.е. градиента… 2. Вязкости жидкости, которая в свою очередь, зависит от температуры;Капиллярная фильтрация
- давление крови в капиллярном русле (рк); - давление жидкости вне капиллярного русла (ртк); - колоидосмотическое давление крови ( к);Специфический транспорт веществ через биологические барьеры
Эволюционно специфический транспорт возник из физиологических процессов переноса через мембраны относительно простых, жизненно необходимых клетке… Таблица 5. Признаки специфического транспорта 1. Связывание… Некоторые ксенобиотики могут изменять активность и свойства молекул-переносчиков и, тем самым, влиять на течение…Активный транспорт
Первичный активный транспорт - это процесс, при котором энергия макроэргов (АТФ) непосредственно расходуется на перемещение молекулы или иона через… Вторичный активный транспорт состоит из двух структурно разделенных…Каталитическая (облегченная) диффузия
Транспорт веществ путем образования мембранных везикул
Таблица 6. Транспорт веществ путем цитозов 1. Эндоцитозы: захват вещества клеткой 1.1. Фагоцитоз: захват корпускулярных частиц 1.2.… Путем фагоцитоза клетка захватывает большие частицы или макромолекулярные… Под пинозитозом понимают захват клеткой капель жидкостей. Капли жидкости, с растворенными в ней веществами, окружаются…ГЛАВА 4.2. РЕЗОРБЦИЯ КСЕНОБИОТИКОВ
Термином "резорбция" обозначают процесс проникновения вещества из окружающей среды или ограниченного объема внутренней среды организма в лимфо- и кровоток. Действие вещества, развивающееся вслед за его резорбцией, называется резорбтивным (системным). Некоторые вещества оказывают действие на месте аппликации, главным образом на барьерные ткани: кожу, слизистые оболочки, не проникая в кровоток (процесс резорбции отсутствует). Такое действие называется местным. Многие токсиканты способны как к местному, так и резорбтивному действию.
В настоящее время известно, что подавляющее большинство веществ могут проникать в организм через один или несколько тканевых барьеров: кожные покровы, дыхательные пути, желудочно-кишечный тракт, хотя скорость резорбции при этом различна. В зависимости от того, какой из барьеров преодолевает вещество, говорят об ингаляционном, чрезкожном или пероральном пути поступления токсиканта в организм.
Путь проникновения вещества в организм во многом определяется его агрегатным состоянием, локализацией в элементах окружающей среды, площадью и свойствами "входных ворот" (таблица 1). Так, вещество в форме пара имеет очень высокую вероятность резорбироваться в дыхательных путях, но то же вещество, растворенное в воде, сможет попасть во внутренние среды организма преимущественно через желудочно-кишечный тракт и с меньшей вероятностью через кожу.
Таблица 1. Площадь "всасывающих" поверхностей тела человека (м2)
| Кожа Полость рта Желудок Тонкий кишечник Толстый кишечник Прямая кишка Полость носа Легкие | 1,2 - 2 0,02 0,1 - 0,2 100 0,5 - 1,0 0,04 - 0,07 0,01 70 |
Способность многих химических веществ переходить из одного агрегатного состояния в другое и локализоваться вследствие этого в разных средах, порой затрудняет предсказание, каким будет основной способ резорбции токсиканта. Например, многие летучие вещества, способные действовать ингаляционно, вместе с тем растворяются и в воде и в продовольствии и, следовательно, могут действовать различными путями (боевые отравляющие вещества: иприт, люизит, зоман; металлы и их соединения и т.д.).
Факторы, влияющие на резорбцию
- обусловленные особенностями организма; - обусловленные количеством и свойствами апплицируемого вещества; - обусловленные параметрами среды.Резорбция через кожу
Поверхностный слой кожи состоит из ороговевших эпидермоцитов. Его толщина равна 20 - 40 мкм, поверхность покрыта жировой смазкой. В роговом слое… Кожа не просто пассивный барьер, отделяющий организм от окружающей среды.…Способы резорбции
При трансэпидермальном проникновении веществ возможно как прохождение их непосредственно через клетки, так и через межклеточные пространства. При рассмотрении процесса прохождения веществ через кожу следует различать… В силу того, что многие токсиканты проникают через кожу чрезвычайно медленно, орган может выполнять функции…Факторы, влияющие на скорость резорбции
- площадь и локализация резорбирующей поверхности; - интенсивность кровоснабжения кожи; - свойства токсиканта.Площадь и область резорбции
Анатомическая локализация области контакта с веществом существенно влияет на скорость резорбции (таблица 2). Наибольшей способностью к резорбции… Таблица 2. Скорость проникновения паратиона через кожу различных областей тела…Кровоснабжение
Свойства действующих веществ
Газы, такие как кислород, азот, диоксид углерода, сероводород, аммиак, гелий, водород - способны к кожной резорбции. На скорости процесса, прежде…Экзогенные факторы
Увлажненная кожа лучше всасывает токсиканты, чем сухая. На скорость резорбции веществ, апплицируемых в виде эмульсий, растворов, мазей… Параметры резорбции некоторых веществ через кожу человека представлены на таблице 3.Резорбция через слизистые оболочки
Резорбция веществ через слизистые определяется главным образом следующими факторами: - агрегатным состоянием вещества (газ, аэрозоль, взвесь, раствор); - дозой и концентрацией токсиканта;Резорбция в ротовой полости
Проникать через слизистые могут лишь вещества, находящиеся в полости рта в молекулярной форме. Поэтому растворы лучше резорбируются, чем взвеси.… Оттекающая от слизистой полости рта кровь поступает в верхнюю полую вену и…Резорбция в желудке
Таблица 5. Резорбция некоторых производных барбитуровой кислоты в желудке Вещество рКа Коэффициент распределения %… Алкалоиды (морфин, атропин и др.) резорбируются здесь лишь в следовых…Растворимость в жирах и рН
Для веществ - слабых кислот и слабых оснований большое значение имеет величина рКа, определяющая, какая часть растворенного вещества будет… Для слабых кислот кислая среда способствует превращению вещества в… Поскольку неионизированные молекулы более липофильны они легче проникают через биологический барьер. Поэтому в желудке…Растворимость в воде
Необходимым условие резорбции вещества в желудке является его растворимость в желудочном соке. Потому практически не растворимые в воде вещества, даже в случае высокой растворимости в жирах, здесь не всасываются (дикумарол).
Взвеси химических соединений перед всасыванием должны перейти в раствор. Поскольку время нахождения в желудке ограничено взвеси действуют слабее, чем растворы того же вещества.
Содержимое желудка
Резорбция в кишечнике
Таблица 6. Некоторые характеристики слизистой тонкой кишки человека Структуры Количественные характеристики Площадь… Перистальтика кишечника обеспечивает перемешивание содержимого, вследствие… Молекулы-субстраты обмена веществ и структурные элементы живого (глюкоза, аминокислоты, электролиты, нуклеотиды и…Размеры молекулы
Заряд молекулы
Отделы кишечника
Резорбция в толстой кишке происходит сравнительно медленно. Этому способствует не только меньшая площадь поверхности слизистой этого отдела, но и,…Кровоснабжение
Кишечник хорошо кровоснабжаемый орган. Вещества, проникающие через слизистую оболочку, быстро уносятся оттекающей кровью, поэтому скорость кровотока здесь не является фактором, лимитирующим процесс резорбции.
Содержимое кишечника
Желчные кислоты, обладая свойствами эмульгаторов, способствуют всасыванию жиров, однако, усиливают ли они резорбцию жирорастворимых ксенобиотиков… Микрофлора кишечника может вызвать химическую модификацию молекул токсикантов.… E. coli содержит ферменты, имеющие значение для судьбы токсикантов в организме. Так, под влиянием этих энзимов, в…Резорбция в легких
ДM = Др 1/2 (SA + SC) n-1 , где ДM - скорость диффузии (мл/мин); - абсорбционный коэффициент Бунзена;Резорбция газов
Рисунок 2. Процесс проникновения и распространения газов в организме В конечном итоге в тканях (в частности в ЦНС) аккумулируется определенная концентрация токсиканта, при которой…Вентиляция легких
При нормальной частоте и глубине дыхания легочная вентиляция достаточна для того, чтобы альвеолярную концентрацию газа (Са) в течение 2 минут от… Таким образом, вентиляция обеспечивает очень быструю доставку газа из… В тот момент, когда парциальное давление газа в окружающем, а затем и альвеолярном воздухе становиться ниже, чем в…Поступление в кровь
1. Растворимости газа в крови; 2. Градиента концентрации газа между альвеолярным воздухом и кровью; 3. Интенсивности кровотока;Переход газов в ткани
Таблица 11. Коэффициенты распределения трихлорэтилена в тканях крысы и человека Коэффициент распределения Крыса: … Диффузия газов в ткани определяется следующими факторами: 1. Растворимостью газов в тканях;Резорбция аэрозолей
Пенетрация в кровь осуществляется в соответствии с физико-химическими законами. Эпителий дыхательного тракта и стенки капиллярного русла обладают… Квота резорбции вещества в легких является функцией количества,…Резорбция слизистыми глаз
Резорбция из тканей
Свойства тканей
Стенка капилляра
Стенки капилляров мышц млекопитающих имеют поры диаметром 3 - 4 нм, поэтому они не проницаемы для гемоглобина (r = 3,2 нм) и сывороточных альбуминов…Капиллярная и лимфатическая система
Кровоснабжение
Охлаждение конечности вызывает замедление в ней кровотока, нагревание - ускорение.Свойства токсиканта
Высокомолекулярное вещество инулин (МВ 5500)используют в эксперименте для изучения закономерностей резорбции веществ в тканях. Так, установлены… Жирорастворимые соединения хорошо резорбируются в тканях, поскольку клетки…Квота резорбции
Более простым и надежным является способ определения величины квоты резорбции. Для этого после нанесения веществ на кожные покровы или введения его… QR = (SR)/(SIV). Чем ближе значение QR к 1, тем лучше резорбируется данное вещество исследуемым путем.ГЛАВА 4.3. РАСПРЕДЕЛЕНИЕ КСЕНОБИОТИКОВ В ОРГАНИЗМЕ
После резорбции в кровь вещество в соответствии с градиентом концентрации распределяется по всем органам и тканям. Распределение - динамический процесс, его направленность во многом определяется соотношением содержания ксенобиотика во внешней среде, на месте аппликации, в крови и тканях. По большей части вещества распределяются в организме неравномерно. Неодинаково и время пребывания ксенобиотиков в различных органах и тканях. Некоторые избирательно накапливаются в том или ином органе, ткани, даже клетках определенного типа. Так, ботулотоксин избирательно связывается с нервными окончаниями холинэргических нервных волокон, 6-гидроксидофамин - накапливается в катехоламинэргических нейронах ЦНС, свинец, стронций - в костях и т.д. Причем если время нахождения первых двух токсикантов в соответствующих клетках насчитывает несколько часов - суток, то последние агенты могут сохраняться в костной ткани годами. Однако строение, физические свойства и химически состав клеток во многом одинаковы, поэтому такое неравномерное распределение ксенобиотика в организме или избирательное накопление в отдельных тканях встречается не так часто.
Токсический процесс далеко не всегда характеризуется повреждением именно тех структур, в которых вещество накапливается в наибольшем количестве. Выраженность токсического эффекта пропорциональна концентрации ксенобиотика в месте действия на биологически значимую "структуру-мишень". Для того, чтобы эффект был сильным необходима высокая концентрация вещества в "биофазе" чувствительных рецепторов. Например, чтобы вызвать отравление, в основе которого лежит нарушение деятельности сердца, буфотоксин должен накопиться в сердечной мышце. Его содержание в мозге, печени, поджелудочной железе практически не имеет значение для развития острого токсического процесса. При интоксикации диэтиламидом лизергиновой кислоты (ДЛК) менее 1% вещества поступает в мозг, но именно со стороны ЦНС выявляются изменения, составляющие основу острого отравления. Свинец, накопившийся в костях, практически не обладает биологической активностью.
Принципы распределения
- свойства стенок их капиллярного русла; - степень вазкуляризации и интенсивность кровоснабжения органов; - свойства клеток, формирующих орган, и особенно клеточных мембран;Проникновение веществ через стенку капилляра
Значение особенностей кровоснабжения органов
Объем крови, протекающей через различные органы в единицу времени далеко не одинаков (рисунок 1). Рисунок 1. Интенсивность кровоснабжения различных органов и тканейПроникновение через клеточную мембрану
Водо-растворимые соединения могут попасть в клетки лишь через поры клеточных мембран. Размер пор клеточных мембран значительно меньше пор стенок… На способность веществ проникать через клеточные мембраны влияет величина их… 1.4. Относительная растворимость в системе масло/водаРаспределение в соответствии с химическим сродством
Стронций и свинец - металлы, в известном отношении близкие кальцию. При поступлении в организм они первоначально накапливаются в паренхиматозных… Распределение веществ модифицируется внешними условиями. Так, CN- обладает…Объем распределения
Сравнивая Vd с объемами различных компартментов, можно ориентировочно оценить, в каком из них будет преимущественно накапливаться вещество. У… Таблица 2. Относительный объем компартментов организма Компартмент … Если вещество не растворимо в липидах, оно будет накапливаться в водной фазе: плазме крови VК или одновременно…Связывание с белками крови
Токсикант, попавший в кровоток, может вступать во взаимодействие с белками и клетками крови, при этом изменяются его токсикокинетические характеристики. В практическом отношении особый интерес представляет взаимодействие ксенобиотиков с протеинами плазмы крови.
Белки плазмы крови
Таблица 4. Потенциальные участки связывания ионизированных молекул ксенобиотиков белками Участки связывания (аминокислота) Строение… Tanford et al. 1955 Альбумины плазмы крови человека хорошо растворяются в воде. Их молекулярная масса - около 66000 Д. Они состоят из 585…Характеристики связывания ксенобиотиков
Таблица 5. Связывание некоторых лекарственных препаратов белками плазмы крови Вещество Связывание (%) Вещество … ( цит. по Марковой И.В., 1998) Связь веществ с белками - спонтанно протекающая реакция, не требующая затрат энергии и зависящая только от их…Конкурентные отношения при взаимодействии ксенобиотиков с белками
Известна способность веществ к взаимному вытеснению из связей с протеинами. Это особенно характерно для слабых кислот, например таких лекарственных… Значение рассматриваемого явления определяется следующими факторами: - относительным сродством вещества и его конкурента к белкам плазмы крови с одной стороны, и тканям - с другой;Связывание клетками крови
Фиксация веществ на поверхности эритроцитов отчасти обусловлена наличием отрицательного заряда на внешней поверхности мембраны. Он формируется… Прохождение ксенобиотиками клеточной мембраны эритроцитов подчиняется общим…Проникновение ксенобиотиков в ЦНС
Проникновение в ЦНС целого ряда химических соединений, в основном водорастворимых и тем более заряженных, затруднено или даже невозможно. Это обусловлено особенностями строения гистогематического барьера между кровью и тканью мозга, носящего здесь название "гематоэнцефалический барьер", и барьера, отделяющего цереброспинальную жидкость от кровяного русла (гематоликворный барьер).
Гематоэнцефалический и гематоликворный барьеры.
Гематоэнцефалический барьер формируется благодаря уникальным особенностям анатомических структур головного мозга. Во-первых, эндотелий капиллярного русла головного мозга отличается от… Во-вторых, капилляры мозга плотно окутаны отростками астроцитарной глии. Астроцитарная оболочка препятствует…Некоторые свойства гематоэнцефалического и гематоликворного барьеров
Свойства веществ, влияющие на их способность проникать в мозг, по сути, идентичны свойствам, регулирующим проникновение соединений через клеточные… Необходимые мозгу вещества: субстраты обменных процессов, биорегуляторы… Проницаемость ГЭБ в значительной степени изменяется с возрастом и при различных патологических состояниях…Гематоофтальмический барьер
Первый регулирует обмен веществ между кровью и внутриглазной жидкостью (камерами глаза). Главную роль здесь играет цилиарное тело, продуцирующее… Вторым является гематоретинальный барьер, оделяющий кровь от сетчатки глаза.…Проникновение ксенобиотиков в печень
Сосудистое русло
Печеночная артерия, портальная вена и желчевыводящий проток образуют тесно связанный пучок, называемый портальной триадой. Кровь, поступающая по… Именно через стенки синусоидов ксенобиотики проникают из крови в гепатоциты.… Между фенестрированным эндотелием синусоида и мембраной гепатоцита имеется пространство, шириной от 60 нм до 0,5 мкм…Активный транспорт
Мембранная диффузия
Проницаемость биологического барьера для ксенобиотика может быть рассчитана по формуле: KP = - 1/t ln [ 1 - (Ct/Cmax)] , где KP - константа проницаемости барьера;Фагоцитоз
Поступление ксенобиотиков в экзокринные железы
Переход токсикантов из крови в клетки желез определяется уже рассматривавшимися ранее общими характеристиками: величиной коэффициента распределения… При анализе процесса распределения веществ необходимо учитывать, что секрет…Проникновение ксенобиотиков через плаценту
Если химическое вещество поступает в организм беременной женщины, оно может оказаться опасным не только для будущей матери, но и для плода, а иногда и исключительно для плода. Такая опасность обусловлена способностью многих чужеродных соединений проходить через плацентарный барьер. Особую опасность, в этой связи, представляют лекарственные препараты, вредные привычки (курение табака, прием алкоголя и т.д.), профессиональные вредности.
Плацентарный барьер
Характеристика проникновения токсикантов через плаценту и распределение их в тканях плода
Особенностью плацентарного барьера является его способность пропускать некоторые высокомолекулярные вещества, некоторые белки и даже материнские… Таблица 9. Примеры веществ, проникающих в кровь плода через плацентарный… После прохождения барьера вещества оказываются в крови плода. Отсюда, в соответствии с общими закономерностями, они…Депонирование
Депонирование имеет три основные причины: 1. Активный захват клетками ксенобиотика с последующим его удержанием; 2. Высокое химическое сродство… Количественные характеристики процесса депонирования существенно зависят от…Депонирование вследствие химического сродства и растворимости в липидах
Другой механизм депонирования - накопление липофильных веществ в жировой ткани. Таким образом, в организме в течение многих лет сохраняются… Существуют возможности влиять на процесс депонирования путем: - прекращения поступления вещества в организм;Депонирование вследствие активного захвата ксенобиотика
Если вещество поступает в клетки против градиента концентрации, то оно может накапливаться в них. Это имеет место в определенных органах и тканях в отношении лишь очень ограниченного количества веществ. Механизм депонирования выявлен для некоторых аналогов биогенных аминов (5-ОН-триптамина, хлорфенилаланина и др.), белковых токсинов (холерного, дифтирийного, столбнячного, ботулотоксина), йода и др.
ГЛАВА 4.4. МЕТАБОЛИЗМ КСЕНОБИОТИКОВ
Многие ксенобиотики, попав в организм, подвергаются биотрансформации и выделяются в виде метаболитов. В основе биотрансформации по большей части лежат энзиматические преобразования молекул. Биологический смысл явления - превращение химического вещества в форму, удобную для выведения из организма, и тем самым, сокращение времени его действия.
Метаболизм ксенобиотиков проходит в две фазы (рисунок 1).

Рисунок 1. Фазы метаболизма чужеродных соединений
В ходе первой фазы окислительно-восстановительного или гидролитического превращения молекула вещества обогащается полярными функциональными группами, что делает ее реакционно-способной и более растворимой в воде. Во второй фазе проходят синтетические процессы конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, в результате чего образуются полярные соединения, которые выводятся из организма с помощью специальных механизмов экскреции.
Разнообразие каталитических свойств энзимов биотрансформации и их низкая субстратная специфичность позволяет организму метаболизировать вещества самого разного строения. Вместе с тем, у животных разных видов и человека метаболизм ксенобиотиков проходит далеко не одинаково, поскольку энзимы, участвующие в превращениях чужеродных веществ, часто видоспецифичны.
Следствием химической модификации молекулы ксенобиотика могут стать:
1. Ослабление токсичности;
2. Усиление токсичности;
3. Изменение характера токсического действия;
4. Инициация токсического процесса.
Метаболизм многих ксенобиотиков сопровождается образованием продуктов существенно уступающих по токсичности исходным веществам. Так, роданиды, образующиеся в процессе биопревращения цианидов, в несколько сот раз менее токсичны, чем исходные ксенобиотики. Гидролитическое отщепление от молекул зарина, зомана, диизопропилфторфосфата иона фтора, приводит к утрате этими веществами способности угнетать активность ацетилхолинэстеразы и существенному понижению их токсичности. Процесс утраты токсикантом токсичности в результате биотрансформации обозначается как "метаболическая детоксикация".
В процессе метаболизма других веществ образуются более токсичные соединения. Примером такого рода превращений является, в частности, образование в организме фторуксусной кислоты при интоксикации фторэтанолом.
В ряде случаев в ходе биотрансформации ксенобиотиков образуются вещества, способные совершенно иначе действовать на организм, чем исходные агенты. Так, некоторые спирты (этиленгликоль), действуя целой молекулой, вызывают седативно-гипнотический эффект (опьянение, наркоз). В ходе их биопревращения образуются соответствующие альдегиды и органические кислоты (щавелевая кислота), способные повреждать паренхиматозные органы и, в частности, почки. Многие низкомолекулярные вещества, являющиеся факультативными аллергенами, подвергаются в организме метаболическим превращениям с образованием реакционноспособных промежуточных продуктов. Так, соединения, содержащие в молекуле амино- или нитрогруппу в ходе метаболизма превращаются в гидроксиламины, активно взаимодействующие с протеинами крови и тканей, формируя полные антигены. При повторном поступлении таких веществ в организм помимо специфического действия развиваются аллергические реакции.
Порой сам процесс метаболизма ксенобиотика является пусковым звеном в развитии интоксикации. Например, в ходе биологического окисления ароматических углеводородов инициируются свободно-радикальные процессы в клетках, образуются ареноксиды, формирующие ковалентные связи с нуклеофильными структурами клеток (белками, сульфгидрильными группами, нуклеиновыми кислотами и т.д), активирующие перекисное окисление липидов биологических мембран (рисунок 2). В итоге инициируется мутагенное, канцерогенное, цитотоксическое действие токсикантов.

Рисунок 2. Образование ареноксидов в процессе метаболизма ароматических полициклических углеводородов при участии оксидаз смешанных функций (ОСФ)
Аналогично ареноксидам на клетки действуют N-оксиды, нитрозамины, гидроксиламины, также являющиеся канцерогенами и мутагенами. В опытах на собаках установлена прямая зависимость между канцерогенной активностью (рак мочевого пузыря) и концентрацией в моче продуктов N-окисления веществ в ряду: 1-нафтиламин, 2-нафтиламин, 4-аминодифенил.
По такому же механизму действуют на организм галогенированный бензол, нафтанол и многие другие ксенобиотики.
Процесс образования токсичных продуктов метаболизма называется "токсификация", а продукты биотрансформации, обладающие высокой токсичностью - токсичными метаболитами. Во многих случаях токсичный метаболит является не стабильным продуктом, подвергающимся дальнейшим превращениям. В этом случае он также называется промежуточным или реактивным метаболитом. Реактивные метаболиты это как раз те вещества, которые часто и вызывают повреждение биосистем на молекулярном уровне. Общим свойством практически всех реактивных метаболитов является их электродефицитное состояние, т.е. высокая электрофильность. Эти вещества вступают во взаимодействие с богатыми электронами (нуклеофильными) молекулами, повреждая их. К числу последних относятся макромолекулы клеток, в структуру которых входят в большом количестве атомы кислорода, азота, серы. Это, прежде всего, белки и нуклеиновые кислоты. Реактивные метаболиты либо присоединяются к нуклеофильным молекулам, образуя с ними ковалентные связи, либо вызывают их окисление. В обоих случаях структура макромолекул нарушается, следовательно, нарушаются и их функции.
Биоактивация далеко не всегда сопровождается повреждением биосубстрата, поскольку одновременно в организме протекают процессы детоксикации и репарации. Интенсивность этих процессов может быть достаточной для компенсации ущерба, связанного с образованием реактивных метаболитов. Тем не менее при введении высоких доз токсиканта, повторном воздействии защитные механизмы могут оказаться несостоятельными, что и приведет к развитию токсического процесса.
Концепция l и ll фазы метаболизма ксенобиотиков
Фаза ll - этап биологической конъюгации промежуточных продуктов метаболизма с эндогенными молекулами, такими как глутатион, глюкуроновая кислота,… В ходе биопревращений липофильный и, следовательно, трудновыводимый… Классическим примером биотрансформации ксенобиотиков является метаболизм бензола в организме (рисунок 3)Локализация процессов биотрансформации
Рисунок 5. Локализация этапов метаболических превращений ксенобиотиков в… Продукты l фазы метаболизма поступают в общий кровоток и могут оказывать действие на органы и системы. Печень…Первая фаза метаболизма
Энзимы l фазы, участвующие в процессе биотрансформации ксенобиотиков, можно классифицировать в соответствии с типом активируемой ими реакции: 1. Оксидазы смешанной функции: цитохромР-450 (Р-450) и флавинсодержащие… 2. Простогландинсинтетазы - гидропероксидазы (ПГС) и другие пероксидазы;Оксидазы смешанной функции
ЦитохромР-450-зависимая монооксигеназная система
Р-450 представляют собой семейство энзимов, локализующихся в эндоплазматическом ретикулуме, которые могут быть разделены с помощью иммунологических… Реакции микросомального окисления, протекающие при участии Р-450, как правило,…Реакции, катализируемые цитохромомР-450
Эпоксидирование и гидроксилирование ароматических соединений.
Эпоксид, возникающий в процессе метаболизма, может подвергаться…Эпоксидирование алифатических и алициклических соединений.
Многие алифитические и алициклические соединения, содержащие в молекуле непредельные связи метаболизируют с образованием чрезвычайно стабильных эпоксидов (превращение алдрина в диалдрин). Это же превращение лежит в основе образования канцерогенных продуктов метаболизма афлатоксинов:
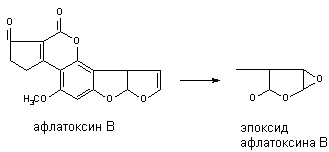
N-окисление.
Превращению могут подвергаться такие вещества, как анилин и его производные, ацетаминофлюорен и др. В результате окисления атома азота могут образовываться гидроксиламины, оксимы и N-оксиды:
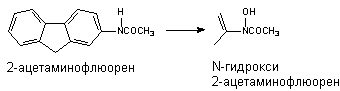
Оксимы образуются в процессе гидроксилирования иминов или первичных аминов:
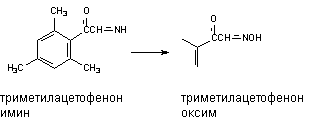
Десульфурирование и расщепление эфиров.
Х = О (1); Х = S (2). Процесс разрушения эфирных связей при атоме фосфора ФОС также во многом обусловлен действием Р-450, хотя процесс может…Оксилительное деалкилирование.
Другим примером может служить метаболизм инсектицида этоксихлора:Окисление тиоэфиров.
При участии цитохромаР-450 и других монооксигеназ происходит окисление тиоэфирных связей, в молекулах таких ксенобиотиков как хлорпромазин, альдикарб, метиокарб и др. Этот вид превращения характерен также для метаболизма сернистого иприта:

Установлено, что при этом токсичность вещества возрастает (сульфон иприта токсичнее исходного вещества).
Флавинсодержащие монооксигеназы (ФМО)
Рисунок 8. Превращение ксенобиотиков при участии флавинмонооксигеназПростогландинсинтетаза-гидропероксидаза и другие пероксидазы
Например, лейкоцитарная пероксидаза, пероксидаза эозинофилов разрушают… Простогландинсинтетаза активирует образование простогландинов (гидроперекисей жирных кислот) из арахидоновой кислоты.…Дегидрогеназы
НАД-зависимая алкогольдегидрогеназа печени обладает невысокой субстратной специфичностью. Так, под влиянием этого энзима метаболизируют не только… Алкогольдегидрогеназа существует в множественной форме с перекрестной субстратной специфичностью. Ее активность…Флавопротеинредуктазы
Рисунок 9. Образование кислородных радикалов в результате окислительно-восстановительного цикла хинона,…Восстановление
В тканях человека и других млекопитающих содержатся ферменты, восстанавливающие молекулы некоторых ксенобиотиков. К их числу относятся, в частности, нитрозоредуктазы (превращают группы NO2- в NH2-), нитроредуктазы (восстанавливают нитраты до нитритов), азоредуктазы (активируют восстановительное расщепление азогрупп с образованием первичных аминогрупп), дегалогеназы (контролируют восстановительное дегалогенирование таких веществ как гексахлоран, ДДТ и др.).
Гидролитические превращения
Расщепление эфиров
Расщепление амидов кислот
Некоторые ткани содержат энзимы, разрушающие и амидные группировки (печень:…Эпоксидгидролазы
Диэпоксиды являются более активными канцерогенами, чем исходные моноэпоксиды.Другие гидролазы
Рисунок 10. Гидролиз зарина при участии флюорогидролазы Наивысшая активность энзима определяется в печени, наименьшая в мозге. Ионы Mg+2, производные пиридина и имидазола…Вторая фаза метаболизма. Конъюгация
Рассматриваемую группу энзимов можно классифицировать следующим образом: 1. Энзимы, формирующие эфирные или амидные связи с промежуточными… - ацетил КоА: амин N-ацетилтрансфераза;Ацетилирование
Ацетилированию могут подвергаться ариламингруппы, сульфамидные группы,…Другие реакции ацилирования
Конъюгация с глюкуроновой кислотой
Рисунок 11. Глюкуроновая кислота Она активно присоединяется к молекулам алифатических и ароматических спиртов, органических кислот, серосодаржащих…Конъюгация с сульфатом
В зависимости от строения молекулы-акцептора в процесс вовлекаются различные…Конъюгация с глутатионом и цистеином
Реакции конъюгации восстановленного глутатиона с электрофильными субстратами катализируют энзимы глутатион-S-трансферазы (GST). Хотя GST обнаружены… Рисунок 13. Биоактивация дибромэтана при участии глутатион-S-трансферазыМетилирование
Метилированию могут подвергаться молекулы, содержащие гидроксильные, сульфгидрильные и аминогруппы в структуре. В качестве донора метильной группы… Среди эндогенных веществ, таким образом, при участии фермента катехол-О-метилтрансферазы (КОМТ) метаболизируют…Энзимы кишечной флоры
Рисунок 15. Взаимодействие печеночных энзимов и энзимов флоры кишечника в…Факторы, влияющие на метаболизм ксенобиотиков
Таблица 5. Факторы, влияющие на метаболизм ксенобиотиков ЕСТЕСТВЕННЫЕ: вид, пол, возраст, питание ИНДУКТОРЫ ФЕРМЕНТОВ: …Генетические факторы
Полиморфизм метаболизма ксенобиотиков отмечен для процессов ацетилирования ароматических веществ, содержащих амино-, сульфо-, амидную группу. Лица…Пол и возраст
Отличия метаболизма ксенобиотиков, обусловленные возрастом, наиболее отчетливо проявляются у новорожденных и лиц пожилого возраста. Хорошо известно,… В старческом возрасте наблюдается снижение клиаренса ксенобиотиков отчасти…Влияние химических веществ
1. Практически не влияющие на активность энзимов метаболизма; 2. Повышающие активность энзимов - индукторы; 3. Угнетающие активность энзимов - ингибиторы.Индукция энзимов
Индукторы метаболизма
Фенобарбитал вызывает выраженную пролиферацию гладкого эндоплазматического ретикулума в гепатоцитах и увеличение активности Р-450. В результате… Индукция, вызываемая полициклическими углеводородами не сопровождается… Некоторые индукторы способны специфично активировать отдельные изоформы Р-450. К числу таковых относятся, в частности,…Механизмы индукции
Механизм феномена полностью не изучен. Одна из первых гипотез была предложена S. Granick в 1966 году для объяснения индукторных свойств стероидов.… в соответствие с более поздними представлениями механизм действия стероидных… Другие индукторы, такие как барбитураты, вероятно действуют с помощью иного механизма. Хотя известно, что в основе…Влияние индукторов на токсичность ксенобиотиков
Другим последствием индукции может быть изменение соотношения интенсивности метаболизма ксенобиотиков в разных органах и тканях, в результате чего… Индукторы из группы производных барбитуровой кислоты способны одновременно… У человека индукция микросомальных ферментов нередко становится следствием различных привычек (курение, прием алкоголя…Угнетение активности энзимов
Группа ингибиторов метаболизма включает: - конкурентные ингибиторы ферментов (альтернативные субстраты). Например,… - неконкурентные ингибиторы. Это, как правило, алкилирующие агенты, угнетающие активность энзима, но не конкурирующие…Активные метаболиты и их роль в инициации токсического процесса
Некоторые вещества активируются уже в ходе однократного превращения, другие в результате многоэтапных превращений, локализующихся порой в разных… Модель N1. Эта модель является наиболее простой (рисунок 18). Орган - мишень…ГЛАВА 4.5. ВЫДЕЛЕНИЕ КСЕНОБИОТИКОВ ИЗ ОРГАНИЗМА (ЭКСКРЕЦИЯ)
Биологические эффекты, вызываемые химическими веществами, как правило, ограничены во времени. Одной из основных причин этого является элиминация их из организма. Под элиминацией понимают процесс, приводящий к снижению концентрации веществ в крови, органах и тканях. Элиминация осуществляется путем:
1. Экскреции - выведения вещества из организма в окружающую среду;
2. Биотрансформации - химических превращений молекул ксенобиотика, его метаболизма. Метаболиты ксенобиотика удаляются из организма путем экскреции.
Биотрансформация сопровождается либо усилением, либо потерей веществом биологической активности. Если токсичность метаболита ниже токсичности исходного агента, говорят о детоксикации или инактивации вещества, если токсичность повышается - токсификации или активации токсиканта. В любом случае исходный действующий агент элиминируется.
При выделения веществ в окружающую среду, организм использует те же механизмы, что и при резорбции. Поэтому общие закономерности, определяющие качественные и количественные характеристики экскреции, не отличаются от закономерностей, управляющих резорбцией и распределением токсикантов в организме. Однако ведущим процессом здесь часто является не диффузия или активный транспорт, а фильтрация чужеродных веществ через биологические барьеры. Местом фильтрации ксенобиотиков, а следовательно и основным органом выделения являются почки. Другие органы, через которые экскретируются вещества - это легкие, печень и в значительно меньшей степени - железы кишечника и кожи. Способ выделения вещества во многом зависит от строения выделяющего органа.
Выделение через легкие
- объем распределения ксенобиотика; - растворимость в крови; - эффективность легочной вентиляции;Почечная экскреция
- фильтрация через гломерулярно-капиллярный барьер; - секреция эпителием почечных канальцев; - реабсорбция клетками эпителия.Фильтрация
Диаметр пор базальной мембраны составляет у разных видов млекопитающих 2 - 4 нм; общая площадь пор: 4 - 10% от общей фильтрационной поверхности (для… Движущая сила фильтрации складывается из артериального давления в… Скорость фильтрации зависит от ряда факторов и может увеличиваться при:Канальцевая реабсорбция
Таблица 2. Площади поверхности различных отделов нефрона. Часть нефрона Площадь (м2) Гломерулы Канальцы 1 порядка … Первичная моча (фильтрат плазмы крови) в значительной части распространяется… Проницаемость канальцевого барьера почти тождественна проницаемости слизистой кишечника, поэтому вещества, легко…Канальцевая секреция
Иногда процессу активной секреции из крови в просвет канальцев противодействует простая диффузия вещества в противоположном направлении. Например,… В почечных канальцах существует система активного выведения и веществ со… Механизмы активной секреции обнаруживаются у большинства позвоночных.Совместное действие механизмов почечной экскреции
GFR Cp = V Cn , где GFR - скорость гломерулярной фильтрации (мл/мин) Cp - концентрация вещества в плазме кровиВыделение печенью
Выделяющиеся вещества должны проходить через барьер, образуемый эндотелием печеночных синусов, базальной мембраной и гепатоцитами. Структура барьера… В процессе экскреции ксенобиотиков осуществляется в два этапа: - захват гепатоцитами;Выделение через кишечник
а) в результате неполного всасывания в желудочно-кишечном тракте; б) в результате билиарной экскреции без последующей реабсорбции в кишечнике; … в) в результате выделения слизистой желудочно-кишечного тракта.Другие пути выведения
Элиминация ксенобиотиков в молоко зависит от степени их персистентности в организме. Быстро элиминируемые, хорошо растворимые в воде ксенобиотики…ГЛАВА 4.6. КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ТОКСИКОКИНЕТИКИ
Важнейшим этапом изучения токсикокинетики ксенобиотика является определение количественных характеристик процессов резорбции, распределения, элиминации. Методология определения токсикокинетических констант постоянно совершенствуется. Её развитие сопряжено с внедрением в практику исследований новых методов количественного определения веществ в биосредах и развитием математического аппарата анализа данных. Ниже будет представлена характеристика некоторых, наиболее часто встречающихся, методических приемов.
Скорость элиминации. Константа скорости элиминации. Время полуэлиминации
dC/dt = -КЕС, т.е. скорость процесса в каждый момент времени пропорциональна концентрации… Мерой скорости элиминации вещества является величина угла наклона касательной к кривой, проведенной в интересующей…Объем распределения.
Начальная концентрация вещества СО в плазме крови не доступна для непосредственного измерения, поскольку необходимо время перемешивания ксенобиотика… Vd = Д/СО Отнеся полученную величину к массе тела (М) получаем значение (VR):Клиаренс
Cltot = ClR + ClH + Cl ... Определение общего клиаренса осуществляется на основе данных, полученных в… Cltot = Д/ППКБиодоступность
Под биодоступностью понимают способность вещества, находящегося в определенном агрегатном состоянии и связи с инертными носителями (почва, пища, растворитель и т.д.), абсорбироватся во внутренние среды организма и достигать места взаимодействия с системами-мишенями.
Поскольку место действия для подавляющего большинства токсикантов не определено, или недоступно для экспериментального анализа, принято допущение, согласно которому содержание вещества в крови линейно связано с величиной его биодоступности.
В соответствии с принципом Доста мерой биодоступности вещества в водимой дозе может являться величина ППК, которая не зависит от временных характеристик процесса резорбции. Чем больше ППК вещества при различных способах введения, тем выше его биодоступность, тем более выражено действие данного ксенобиотика на организм. Сравнение ППК при внутривенном способе и иных способах аппликации (например, ингаляционном, трансдермальном и т.д.) позволяет определить квоту резорбции токсиканта через различные "входные ворота" - частный случай характеристики биодоступности:
QR = ППКинг/ППКв/в и т.д.
Фракция (F) апплицированной дозы вещества (в конкретном примере равна QR) определяет то количество действующего агента, которое достигло общего кровотока. При иных, кроме внутривенного, способах введения ксенобиотиков F < 1. В основе этого лежат неполная абсорбция вещества или/и его метаболизм в органах поступления (коже, легких, кишечнике, печени).
При поступлении вещества через рот следует выделять несколько фракций токсиканта в крови:
FG - фракция токсиканта в крови портальной системы;
FL - фракция токсиканта экстрагируемая печенью;
F - фракция токсиканта, попавшая в общий кровоток. Причем:
F = FG (1 - FL)
Так, если 80% вещества достигает портальной системы, а 30% при этом еще и экстрагируется печенью, то общего кровотока достигает: F = 0,8 0,7 = 0,56, т.е. 56% от введенного количества.
Однако в таком прочтении величина биодоступности не может в полной мере отражать последствия действия токсиканта на организм. Дело в том, что ППК при разных способах воздействия может быть одинаковой, но различная скорость поступления и одновременно протекающая элиминация соединения могут привести к совершенно разным эффектам одного и того же вещества. Пример такой ситуации приведен на рисунке 3.

Рисунок 3. Кривые динамики концентрации вещества Д в плазме крови экспериментального животного при различных способах воздействия:
N1 - внутривенное введение
N2 - введение через желудочно-кишечный тракт
N3 - введение через желудочно-кишечный тракт в форме, адсорбированной на ионно-обменной смоле
Как показано на рисунке, площадь под кривыми 1, 2, 3 после воздействия вещества в дозе Д различными способами практически одинакова, однако формирующиеся эффекты различны.
Соотношение между значениями клиаренса, объема распределения и времени полувыведения вещества
t1/2 = ln2 Vd/Cltot Из уравнения следует, что чем больше объем распределения при одном и том же… Клиаренс может быть определен, как произведение константы элиминации на объем распределения:Компартменты
При определении и расчетах упомянутых в предыдущих разделах характеристик исходили из представления о наличии в организме лишь одного компартмента… Рисунок 4. Токсикокинетические модели:Однокомпартментная модель
Моделирование поведения ксенобиотика при однократном внутривенном введении
-b* = KЕb и bt = b0 e-Kеt , где b* - изменение содержания вещества в крови; b0 - содержание вещества в крови в момент времени t = 0 (т.е. величина, равная дозе вещества Д, введенной…Моделирование поведения ксенобиотика с параллельными путями выведения
b* = - (К1 + К2)b; u* = К1 b; G* = К2 b. При этом для характеристики количества вещества, выделяющегося с мочой или… u0/D = K1/K2 ; G0/D = K2/K1 , гдеМоделирование поведения ксенобиотика полностью резорбирующегося из места введения
Предположим в момент времени t = 0 вещество в дозе Д быстро попало в депо М и начался процесс его резорбции в кровь с одновременной элиминацией… Все процессы, приводящие к повышению содержания вещества в крови, вследствие… Динамика концентрации вещества в плазме крови при этом может быть описана функцией Батемана (Bateman):Многокомпартментные модели
Нелинейные токсикокинетические процессы
К числу нелинейных токсикокинетических процессов могут быть отнесены так называемые "насыщающиеся процессы": канальцевая секреция… Основные последствия кинетики насыщающихся процессов следующие: - увеличение дозы вводимого вещества не приводит к пропорциональному увеличению его концентрации в объеме…Нелинейная однокомпартментная модель распределения с ограниченным характером процесса элиминации
С* = - Vmax C /(KM + C) = - KE KM C /(KM + C), где С* - изменение концентрации вещества в системе; С - концентрация вещества в системе;Физиологические токсикокинетические модели
Эти трудности удается отчасти преодолеть, используя физиологические модели, разрабатываемые с учетом анатомо-физиологических особенностей органов и… Таблица 3. Сравнительная характеристика некоторых биометрических параметров… (По Oser B.L., 1981)РАЗДЕЛ 5. ФАКТОРЫ, ВЛИЯЮЩИЕ НА ТОКСИЧНОСТЬ
ГЛАВА 5.1. ВНУТРИ- И МЕЖВИДОВЫЕ ОСОБЕННОСТИ ОРГАНИЗМОВ И ИХ ВЛИЯНИЕ НА ЧУВСТВИТЕЛЬНОСТЬ К КСЕНОБИОТИКАМ
Представители различных видов живых существ по-разному, как в количественном, так и качественном отношении, реагируют на действие химических веществ (межвидовые различия). Это позволяет создавать с утилитарными целями вещества с "избирательным" действием, т.е. такие, токсичность которых в отношении определенного вида (видов) живых существ во много раз превосходит токсичность для других видов. На этом принципе строится разработка многочисленные пестицидов, антибиотиков и т.д. Представители одного и того же вида также, порой, неодинаково чувствительны к токсикантам (внутривидовые различия).
Неодинаковая токсичность одного и того же соединения для различных организмов обусловлена как наследуемыми, так и благоприобретенными особенностями их морфо-функциональной организмции, сказывающимися на токсикокинетике и токсикодинамике веществ.
Генетически обусловленные особенности реакций организма на действие токсикантов
Помимо генетических механизмов, чувствительность отдельного организма к токсиканту определяется взаимодействием внутренних факторов (гормональный…Межвидовые различия
Таблица 1. Токсичность (ЛД50 мг/кг) некоторых веществ для животных различных видов Вид Строфантин (подкожно) Гексахлор … Большие различия выявляются при оценке на лабораторных животных токсичности… Таблица 2. Токсичность 2,3,7,8-тетрахлодибензопарадиоксина (ТХДД) для разных видов животных. Вид животного …Особенности токсикокинетики
Резорбция
Квота резорбции вещества через аналогичные пути поступления у представителей различных видов далеко не одинакова. Так, 6-азауридин разорбируется кожными покровами целого ряда лабораторных животных, но не человека. Напротив, актиномицин хорошо всасывается в желудочно-кишечном тракте человека, но не лабораторных животных.
Распределение
Заслуживает внимания такая характеристика, как диаметр пор гломерулярной мембраны. Так, у человека в почках через барьер не проникают молекулы с…Биотрансформация
Таблица 3. Чувствительность животных различных видов к гексобарбиталу (вводимые дозы -100 мг/кг; для собаки - 50 мг/кг). Вид Время… Кошки являются исключением из этого правила. Они метаболизируют вещества… Активность энзимов отдельных органов и тканей, участвующих в метаболизме чужеродных соединений у разных видов живых…Экскреция
Особенности токсикодинамики
Связывание с рецептором
Содержание рецепторов определенного вида в аналогичных тканях животных различных видов также не одинаково. Например выносящий семенной канатик мыши…Эффекторные реакции
Внутривидовые различия
Генетические особенности личности
У некоторых лиц с очень низкой скоростью протекает реакция ацетилирования ксенобиотиков и их метаболитов. Так, обычно период полупревращения… Дефект N-ацетилтрансферазы лежит в основе неблагоприятных реакций на целый ряд…Различия связанные с полом
Кастрация или введение самцам эстрогенов нивелируют различия в скорости метаболизма ксенобиотиков в организме животных разных полов. Напротив,… В связи с изложенным токсичность многих ксенобиотиков для самцов и самок… Различия токсичности веществ при остром и хроническом введении могут иметь разную направленность. Так, при остром…Не обусловленные генетически особенности реакции организма на действие токсикантов
Возрастные различия
Таблица 7. Некоторые функционально-морфологические различия между организмами, находящимися в различных периодах развития и жизни Различия…Влияние массы тела
Более высокая, в сравнении с нормой, масса тела как правило является следствием избыточного накопления жировой ткани. Вещества, накапливающиеся в жире в этом случае действуют слабее. Ожирение нередко сопровождается нарушением функций печени, поэтому у тучных людей характер токсического действия некоторых ксенобиотиков может существенно изменяться.
Влияние беременности
Достаточно подробно изучался метаболизм ксенобиотиков в организме беременных крыс. Установлено, что активность анилингидроксилазы,…ГЛАВА 5.2. ВЛИЯНИЕ УСЛОВИЙ ПРОВЕДЕНИЯ ЭКСПЕРИМЕНТА И КАЧЕСТВА СРЕДЫ ОБИТАНИЯ НА ТОКСИЧНОСТЬ
Биологические системы постоянно обмениваются с окружающей средой веществом, энергией, информацией и потому их функциональное состояние находится в полной зависимости от состояния среды. В определенных границах биосистемы способны приспосабливаться к изменению свойств окружающей среды. При этом изменяются их биохимические, физиологические, морфологические характеристики, а, стало быть, и чувствительность к ксенобиотикам. Колебания чувствительности к ядам в зависимости от условий, в которых яд действует, отмечаются на всех уровнях организации жизни: клеточном, органном, организменном, популяционном. Наибольшее количество данных по этому вопросу получено в эксперименте применительно к целостному организму лабораторных животных различных видов. Имеются отдельные наблюдения на людях. Проблема практически не изучена на уровне популяций, хотя в будущем это может иметь очень большое значение для решения практических экотоксикологических задач.
Свойства среды влияют на все звенья цепи формирования и развития токсического процесса: резорбцию, распределение, метаболизм, элиминацию ксенобиотика, взаимодействие его с рецепторами, активацию патологических и репаративных процессов. Наиболее значимые факторы представлены в таблице 1.
Таблица 1. Факторы, оказывающие влияние на токсичность ксенобиотиков
| 1. Биологические или биосоциальные - питание - условия содержания (для лабораторных животных) - окружение |
| 2. Физические - геофизическая периодичность - температура - давление - влажность воздуха - концентрация ионов и Рн - апплицируемый объем - концентрация действующего агента и его агрегатное состояние |
| 3. Химические - ксенобиотики в окружающей среде - ксенобиотики в воде и пище - совместное воздействие нескольких веществ |
Между действием отдельных факторов в реальных условиях трудно провести границу. Так, временная периодичность в изменении чувствительности организма к ксенобиотику зависит как от геофизических факторов (смена дня и ночи, времен года), так и от биосоциальныхъ факторов, генетических особенностей организма и т.д.
Питание
Хроническое недоедание понижает резорбцию веществ в желудочно-кишечном тракте и скорость их метаболизма. Развивающаяся гипоальбуминемия приводит к… Голод редуцирует активность энзимов печени, разрушающих чужеродные соединения.…Условия содержания экспериментальных животных
Таблица 2. Токсичность некоторых веществ (мг/кг; через рот) для мышей при изолированном и групповом содержании Вещества Групповое… Иногда механизмы, лежащие в основе явления, затрагивают глубинные… Однако часто можно обнаружить и достаточно простые причины наблюдаемых эффектов. Например, при изолированном…Содержание в стерильных условиях
У животных, рожденных и выращенных в стерильных условиях, отсутствует кишечная флора. Это является причиной полного прекращения у них процессов внутрикишечного метаболизма ксенобиотиков, в частности деглюкуронидирования конъюгатов, и подавления внутрипеченочной циркуляции некоторых чужеродных веществ. Полагают, что этим можно объяснить значительное снижение (в сравнении с контролем) частоты появления опухолей кишечника и молочной железы, развивающихся при введении животным 3,2-диметил-4-аминофенола. В обычных условиях канцероген подвергается в печени N-гидроксилированию, а затем и глюкуронидированию. После попадания метаболита в кишечник с желчью происходит его расщепление под влиянием 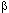 -глюкуронидазы кишечной флоры и образование исходного вещества, активно реабсорбирующегося слизистой ЖКТ. Длительная внутрипеченочная циркуляция диметил-аминофенола и, следовательно, продолжительное пребывание в организме, способствуют реализации канцерогенного действия токсиканта. У животных, содержащихся в стерильных условиях, внутрипеченочная циркуляция подавлена. Вследствие этого существенно ускоряется экскреция вещества из организма, снижается вероятность развития патологических процессов.
-глюкуронидазы кишечной флоры и образование исходного вещества, активно реабсорбирующегося слизистой ЖКТ. Длительная внутрипеченочная циркуляция диметил-аминофенола и, следовательно, продолжительное пребывание в организме, способствуют реализации канцерогенного действия токсиканта. У животных, содержащихся в стерильных условиях, внутрипеченочная циркуляция подавлена. Вследствие этого существенно ускоряется экскреция вещества из организма, снижается вероятность развития патологических процессов.
Периодические изменения чувствительности к токсикантам
Циркадные ритмы
Так, токсичность ингибиторов холинэстеразы для крыс коррелирует с содержанием ацетилхолина в ткани мозга животных. В те периоды, когда содержание… Поскольку чувствительность организма к различным токсикантам изменяется… С учетом сказанного, исследования по оценке острой токсичности веществ следует проводить в одно и тоже время суток.Годичные ритмы
Годичные изменения чувствительности к токсикантам особенно характерны для холоднокровных животных. Однако некоторые колебания чувствительности отмечаются и у теплокровных. Например, у крыс линии Wistar в течение года определяются достоверные изменения чувствительности к токсическому действию никотина. Не исключено, что это связано с колебаниями среднесуточной температуры и влажности воздуха. Максимальная токсичность выявляется в теплое время года.
Температура окружающего воздуха
Q10 = Vt/V(t-10) Q10 для физико-химических процессов находится в интервале 1,1 - 1,5,… Таблица 3. Содержание метадона в тканях экспериментальных животных (мкг/г), через 30 минут после подкожного введения,…ГЛАВА 5.3. ЯВЛЕНИЯ, НАБЛЮДАЕМЫЕ ПРИ ДЛИТЕЛЬНОМ ВОЗДЕЙСТВИИ ТОКСИКАНТОВ
Реакция живых систем на ксенобиотик может существенно изменяться при его повторном или длительном воздействии. Выделяют четыре основные формы проявления этого феномена: толерантность, химическая зависимость, привыкание и хроническое отравление. Первые три формы развиваются при контакте с веществом, поступающим в организм в действующей дозе, т.е. первоначально вызывающей отчетливый эффект. Эти формы интересуют токсиколога прежде всего при оценке действия веществ, которые человек как правило принимает умышленно: лекарственные препараты, наркотические средства, вредные привычки (курение, прием алкоголя) и т.д. Последняя развивается в результате длительного контакта с токсикантом в малых, близких к пороговым, или даже подпороговых, дозах. Эта форма рассматриваемого явления интересует токсиколога применительно к проблеме профессиональной патологии и экотоксикологии.
Толерантность
Толерантность формируется лишь в отношении ограниченного круга веществ. Скорость и выраженность феномена также не одинаковы при действии различных…Виды толерантности
- острую форму (тахифилаксия) - возникает после однократного или повторного действия вещества; - хроническую форму - развивается при частом и длительном контакте с… По механизму формирования:Некоторые механизмы толерантности
Ослабление резорбции
Например, толерантность к хроническому пероральному приёму мышьяка объясняют нарушением его всасывания слизистой кишечника. Изменения слизистой… Прямой зависимости между способностью провоцировать воспалительные процессы в… Возможно формирование перекрестной толерантности к действию различных раздражающих газов.Усиление метаболизма ксенобиотиков
В некоторых случаях токсиканты являются индукторами собственного метаболизма. Хорошо известно, что хроническое потребление этанола приводит к… Таблица 1. Изменение скорости элиминации этанола из организма шимпанзе и… 1 - время потребления 6 - 14 недель: максимальное количество этанола - 5,5 - 7,7 г/кг/сутки;Усиление экскреции.
Аналогичные наблюдения сделаны и для некоторых других веществ. Так, при повторном введении ускоряется выведение из организма пенициллина.…Изменение распределения
Изменение характера распределения токсиканта можно рассматривать как одну из причин формирования толерантности. Однако экспериментальные и клинические данные, подтверждающие это предположение, практически отсутствуют. Для отдельных веществ (например, хлордиазепоксида) у толерантных животных отмечается снижение проницаемости гематоэнцефалического барьера. Однако клиническое значение этого явления остается не ясным.
Изменение рецепторов и реактивных систем
- снижение способности связываться с рецептором; - увеличение числа рецепторов; - снижение эффективности реактивных систем, связанных с рецептором-мишенью для токсиканта.Индукция веществ-антагонистов
Еще одним механизмом развития толерантности может явиться экранирование биомишени для токсиканта продуктами его метаболизма или другими веществами, синтезируемыми в организме. Сюда же можно отнести синтез гаптенов или специальных антител, связывающих исходное вещество, при его продолжительном введении.
Истощение запасов нейромедиаторов
Тахифилаксия
Формирование тахифилаксии - дозо-зависимый феномен. В ряде случаев повторное действие токсиканта в малых и даже умеренных дозах не приводит к… Эффект можно вызвать как на целом животном, так и на изолированных органах.… На препарате изолированной стенки аорты собаки тахифилаксию можно вызвать в отношении ацетилхолина, гистамина,…Хроническая форма толерантности
При развившейся толерантности к морфину и морфиноподобным веществам организм в состоянии переносить очень высокие дозы вещества. Анальгетическая… Толерантность к морфину формируется на клеточном уровне. Поскольку в крови у… В настоящее время полагают, что действие опиатов на рецепторы мозга приводит к повышению синтеза в ЦНС естественных…Биологическое значение толерантности
Толерантность можно рассматривать как защитную реакцию организма на действие ксенобиотиков, при которой снижается чувствительность к веществам, и, не редко, лишь в отношении части эффектов, вызываемых токсикантом. Последнее обстоятельство является одной из причин существенных различий в проявлениях острой, подострой и хронической интоксикаций одним и тем же веществом.
Химическая зависимость
В соответствии с положением, разработанным ВОЗ в 1964 году, лекарственная зависимость определяется как состояние психической или физической… Нередко говорят о пристрастии, рассматривая этот термин, как синоним… - непреодолимое стремление к потреблению вещества;Психическая зависимость
Психическая зависимость - центральный признак химической зависимости, развивающийся при всех её формах. Она характеризуется непреодолимым стремлением к продолжению, сделавшегося привычкой, потребления вещества. Психические проявления синдрома отмены состоят в появлении страха, беспокойства, депрессии вплоть до суицидных попыток, стремлении к поиску веществ. Как указывалось ранее, психическая зависимость не всегда связана с физической зависимостью и развитием толерантности.
Физическая зависимость
Физическая зависимость может развиваться не только у человека. Это явление достаточно глубоко изучается и на экспериментальных животных. В основе… Характерными признаками физической зависимости являются: - повторное введение вещества в течение нескольких недель;Механизм химической зависимости
В качестве нейробиологических механизмов развития химической зависимости рассматриваются следующие: 1.Вещество-агонист рецептора (фенамин, наркотический анальгетик и др.)… 2.Токсикант повышает выброс нейромедиатора из пресинаптических структур (например, усиление выделения дофамина при…Привыкание
Хроническое отравление
1.Токсикокинетические; 2.Токсикодинамические. В основе токсикокинетических механизмов развития хронической интоксикации лежат процессы, приводящие к накоплению…ГЛАВА 5.4. КОЕРГИЗМ КСЕНОБИОТИКОВ
В реальных условия биологические системы, как правило, подвергаются воздействию более чем одного вещества. При этом большинство соединений (действуя в достаточной дозе) таким образом изменяют состояние организма, что последующий контакт с другими ксенобиотиками приводит к формированию эффектов качественно и количественно отличающихся, от вызываемых ими у интактных организмов, т.е. вызывают аллобиотические состояния. Например, уже однократный прием хлорорганического инсектицида алдрина мышами приводит к существенному изменению их чувствительности к фосфорорганическим инсектицидам (таблица 1).
Таблица 1. Влияние алдрина (16 мг/кг, однократно через рот, за 4 суток до испытания) на чувствительность белых мышей к некоторым ФОС
| Вещество | Смертность в группе (%) | |
| (мг/кг) | Контроль | После потребления алдрина |
| Паратион (22) | ||
| Параоксон (40) | 44,4 | |
| ТЭПФ (10) | ||
| ДФФ (50) | 66,6 | |
| Гутион (15) | 84,6 | 15,4 |
| ТОКФ (2000) | ||
| ОМФА (25) |
(A.J. Triolo, J.M. Coon, 1966)
Для обозначения всех форм эффектов, развивающихся при совместном действии химических веществ, не зависимо от их строения и вида подвергающейся воздействию биологической системы, используют термин - коергизм. Проявления коергизма возможно как вследствие одномоментного (комбинация), так и последовательного (сукцессия) действия веществ на организм (рисунок 1).
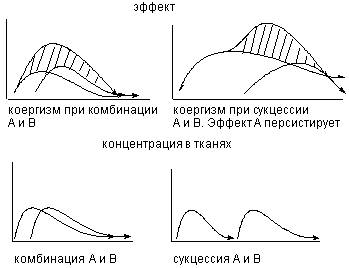
Рисунок 1. Коергизм при одномоментном и последовательном поступлении веществ "А" и "В" в организм.
Проявления коергизма по показателям качества и интенсивность развивающихся эффектов можно представить в форме трех основных типов: аддитивный синергизм (суммация), потенцирующий синергизм (потенцирование), антагонизм (таблица 2).
Таблица 2. Виды коергизма
| Аддитивный синергизм | Совместный эффект А и В равен сумме эффектов каждого из веществ. Вещества имеют либо близкую структуру, либо одинаковый механизм действия |
| Потенцирующий синергизм | Совместный эффект А и В больше суммы эффектов каждого из веществ. Вещества имеют различные механизмы действия. Возможно действие одного из веществ, как аллостерического активатора рецептора другого вещества |
| Антагонизм | Совместный эффект А и В существенно ниже суммы эффектов каждого из веществ вплоть до полного устранения эффектов |
Механизмы коергизма
Взаимное влияние химических веществ на развивающиеся эффекты может осуществляться во все периоды их действия и даже после выведения одного из них из организма.
Взаимодействие в период аппликации
Адсорбция на поверхности. Наиболее изученным примером подобного рода взаимодействия является процесс связывания токсиканта активированным углем.… Химическое взаимодействие. В ряде случаев в основе коергизма лежит химическое… В ряде случаев химическое взаимодействие ксенобиотиков может приводить к образованию более опасных соединений. Так,…Токсикокинетические механизмы коергизма.
- изменять абсорбцию вещества "А" вследствие модификации проницаемости биологических барьеров или гемодинамики в органе (ткани). Алкалоз и… -вступать в химическое или физико-химическое взаимодействие с веществом… - вытеснять вещество "А" из связи с транспортными белками плазмы крови и увеличивать содержание токсиканта в…Взаимодействие веществ при резорбции
Поверхностно-активные вещества повышают всасываемость в желудочно-кишечном тракте жирорастворимых веществ. В опытах на крысах показана способность… В ряде случаев коергизм веществ при поступлении их в желудочно-кишечном тракте… Веществом с выраженными "проводниковыми" свойствами, облегчающим проникновение веществ через биологические…Коергизм веществ, в процессе распределения
Модификация связывания белками плазмы крови
Таблица 3. Процент связывания плазмой крови и токсичность фосфакола для мышей предварительно отравленных хлорорганическими инсектицидами … (A.J. Triolo et al., 1970) Напротив, введение крысам три-о-крезил фосфата (ТОКФ), вещества полностью блокирующего места связывания ФОС с…Изменение свойств тканей
Вещества, обладающие свойствами -адреноблокаторов и одновременно высоким коэффициентом распределения в системе масло/вода (более 20), значительно…Мобилизация биологически активных веществ
Таблица 4. Эффективность некоторых комплексообразователей при интоксикации металлами. Комплексон Mn Co Zn Cu … (Wirth et al, 1971)Коергизм в процессе биотрансформации
- конкурентное и неконкурентное угнетение активности энзимов, участвующих в биотрансформации веществ; - повреждение субклеточных структур, ответственных за метаболизм ксенобиотиков… - угнетение синтеза или активация разрушения метаболизирующих энзимов;Угнетение активности энзимов, метаболизирующих ксенобиотики
Реакции I фазы метаболизма. Два токсиканта или продукты их метаболизма могут взаимодействовать с одним и тем же метаболизирующим энзимом. В… Угнетение активности микросомальной этанолметаболизирующей окислительной… Большая группа химических веществ является ингибиторами микросомальной биотрансформации ксенобиотиков (таблица 5).Повреждение органов и тканей, метаболизирующих ксенобиотики
Индукция энзимов, метаболизирующих ксенобиотики
Таблица 6. Некоторые лекарственные препараты, обладающие свойствами индукторов и ингибиторов энзимов, метаболизирующих ксенобиотики … Благодаря низкой специфичности энзимов, метаболизирующих ксенобиотики, многие индукторы повышают скорость метаболизма…Коергизм веществ при их выведении
Выведение через почки
Вещества, повышающие артериальное давление и усиливающие почечный кровоток (дофамин, пурины, сердечные гликозиды и др.) ускоряют процесс почечной фильтрации ксенобиотиков, несвязанных с белками плазмы крови. Вытеснение коергистом ксенобиотика из связи с протеинами крови также увеличивает скорость их выведения.
Канальцевая реабсорбция
Решающим фактором, определяющим скорость выведения многих веществ через почки, является рН мочи, изменяющаяся в норме от 4,5 до 7,5. При длительном…Канальцевая секреция
В таблице 8 представлены данные, демонстрирующие замедление элиминации почками пенициллина при одновременном назначении ряда других веществ. Таблица 8. Влияние некоторых веществ на скорость элиминации почками… Переносчики соединений свойствами слабых оснований участвуют элиминации таких веществ как хинин, хинидин, имипрамин,…Печеночная экскреция
Токсикодинамические механизмы коергизма
Взаимодействие на уровне рецепторов
- путем действия на один и тот же рецептор биологически активной макромолекулы (энзима, ионного канала, рецептора эндогенного биорегулятора);… - путем действия на разные сайты связывания одного и того же рецептора… Интерпретация феномена коергизма на уровне рецепторов возможна с нескольких позиций.Конкуренция за рецепторы одного типа
Рисунок 3. Механизмы конкуренции двух токсикантов на уровне рецептора В качестве рецептора для токсикантов (А, В) могут выступать активный (Е) и аллостерический (R) центры энзима,…Коергизм при действии ксенобиотиков на разные участки рецепторной молекулы
Показано, что морфин и N-аллилморфин очевидно реагируют с различными участками одной и той же молекулы опиатного рецептора. Антагонизм между… N-этилмалеинимид, р-хлормеркуробензоат, цистеин, ионы ртути и мышьяка и другие… В холинэргических рецепторах пункт связывания ацетилхолина соседствует с -S-S- связью белковой молекулы,…Коергизм на уровне реактивных систем и целостного организма
Представление данных, получаемых в ходе изучения явления коергизма
Изучается соотношение доз коергистов "А" и "В" при их совместном действии, по показателю - способность вызывать некий… Рисунок 4. Комбинационный квадрат Loewe с 4 изоболами:Токсикологическое значение явления коергизма
2. Явление коергизма лежит в основе разработки средств этиотропной (антидоты), патогенетической и симптоматической терапии отравлений. В качестве…ГЛАВА 5.5. АНТИДОТЫ (ПРОТИВОЯДИЯ)
В клинической токсикологии, как и в других областях практической медицины, в качестве лечебных, используют симптоматические, патогенетические и этиотропные средства терапии (таблица 1). Поводом для введения этиотропных препаратов, является знание непосредственной причины отравления, особенностей токсикокинетики яда. Симптоматические и патогенетические вещества назначают, ориентируясь на проявления интоксикации, при этом одно и то же лекарство порой можно вводить отравленным совершенно разными токсикантами.
Таблица 1. НЕКОТОРЫЕ МЕХАНИЗМЫ ДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРИМЕНЯЕМЫХ ПРИ ОСТРЫХ ИНТОКСИКАЦИЯХ
| СРЕДСТВА | НЕКОТОРЫЕ МЕХАНИЗМЫ ДЕЙСТВИЯ |
| Этиотропные | А. Химический антагонизм - нейтрализация токсиканта Б. Биохимический антагонизм - вытеснение токсиканта из связи с биосубстратом; - другие пути компенсации, нарушенного токсикантом количества и качества биосубстрата В, Физиологический антагонизм - нормализация функционального состояния субклеточных биосистем (синапсов, митохондрий, ядра клетки и др.) Г. Модификация метаболизма токсиканта |
| Патогенетические | - модуляция активности процессов нервной и гуморальной регуляции; - устранение гипоксии; предотвращение пагубных последствий нарушений биоэнергетики; - нормализация водно-электролитного обмена и кислотно-основного состояния; - нормализация проницаемости гисто-гематических барьеров; - прерывание патохимических каскадов, приводящих к гибели клеток и др. |
| Симптоматические | - устранение боли судорог психомоторного возбуждения - нормализация дыхания - нормализация гемодинамики и др. |
Специфичность лекарств, в отношении действующих токсикантов убывает в ряду: этиотропное - патогенетическое - симптоматическое средство. В такой же последовательности убывает эффективность применяемых средств. Этиотропные препараты, введенные в срок и в нужной дозе, порой практически полностью устраняют проявления интоксикации. Симптоматические средства устраняют лишь отдельные проявления отравления, облегчают его течение (Таблица 2).
Таблица 2. Различия ожидаемых эффектов от использования средств этиотропной, патогенетической и симптоматической терапии острых интоксикаций
| Средства | Ожидаемый эффект | Примеры |
| Этиотропные | Ослабление или устранение всех проявлений интоксикации | Устранение (или полное предотвращение развития) признаков отравления цианидами при своевременном введении метгемоглобинообразователей (азотистокислого натрия, диметиламинофенола) |
| Патогенетические | Ослабление или устранение проявлений интоксикации, в основе которых лежит данный патогенетический феномен | Временное улучшение состояние (частичное устранение признаков гипоксии головного мозга) пораженных удушающими веществами (хлором) при ингаляции кислорода |
| Симптоматические | Ослабление или устранения отдельного проявления интоксикации | Устранение судорожного синдрома, вызванного фосфорорганическим соединением, с помощью больших доз диазепама |
В токсикологии, термину этиотропное средство терапии, тождествен термин антидот (противоядие).
Антидотом (от Antidotum, "даваемое против") - называется лекарство, применяемое при лечении отравлений и способствующее обезвреживанию яда или предупреждению и устранению вызываемого им токсического эффекта (В.М. Карасик, 1961).
История вопроса.
Другое распространенное воззрение на отравление зиждилось на гуморальной теории патологии. В классификации ядов, предложенной ещё Галеном,… Бытовало представление, что противоядие должно изгонять яд из тела, поскольку… Следует упомянуть о противоядиях, которым столетиями приписывалась сказочная сила. Такими считались знаменитые териаки…Характеристика современных антидотов
В настоящее время антидоты разработаны лишь для ограниченной группы токсикантов. В соответствии с видом антагонизма к токсиканту они могут быть… Таблица 3. Противоядия, используемые в клинической практике Вид…Краткая характеристика механизмов антидотного действия
1. Химический; 2. Биохимический; 3. Физиологический;Антидоты, связывающие токсикант (химические антагонисты)
В настоящее время антидоты с химическим антагонизмом широко используют в практике оказания помощи отравленным.Прямое химическое взаимодействие
- химическая нейтрализация свободно циркулирующего токсиканта; - образование малотоксичного комплекса; - высвобождение структуры-рецептора из связи с токсикантом;Опосредованная химическая нейтрализация.
К числу таких противоядий относятся метгемоглобинообразователи - антидоты цианидов и сульфидов, в частности: азотистокислый натрий, амилнитрит,… Как известно, основным механизмом токсического действия цианидов и сульфидов,…Биохимический антагонизм
Данный вид антагонизма лежит в основе антидотной активности кислорода при отравлении оксидом углерода, реактиваторов холинэстеразы и обратимых… Кислородиспользуют при интоксикациях различными веществами, однако…Физиологический антагонизм.
Впервые возможность использовать противоядия с таким механизмом действия была установлена Шмидебергом и Коппе (1869), выделившими из мухомора… - гетерогенностью синаптических рецепторов, на которые воздействуют токсикант… - неодинаковым сродством и внутренней активностью веществ в отношении различных субпопуляцый рецепторов;Противоядия, модифицирующие метаболизм ксенобиотиков.
Используемые в практике оказания помощи отравленным препараты могут быть отнесены к одной из следующих групп: А. Ускоряющие детоксикацию. - тиосульфат натрия - применяется при отравлениях цианидами;Применение противоядий
Лекарственные формы и схемы применения основных противоядий представлены в таблице 5. Таблица 5. Лекарственные формы и схемы применения некоторых противоядий …Разработка новых антидотов.
После выявления антагониста начинается планирование и проведение целенаправленных, порой длительных исследований по выбору из большого числа… - высокая эффективность, - хорошая переносимость,Оценка эффективности.
3.1.1. Опыты in vitro Некоторые свойства антидотов могут быть оценены in vitro. Особенно это… Так, в опытах с простыми биологическими объектами (простейщие, примитивные ракообразные, культуры клеток и т.д.)…Создание комплексных антидотных рецептур
При разработке рецептур сталкиваются с дополнительными трудностями. Входящие в рецептуру препараты должны быть химически совместимы и иметь близкие…Внедрение новых антидотов в практику
Порядок проведения исследований на переносимость, организация и проведение клинических испытаний новых антидотов осуществляется по общим правилам, в…Перспективы
1. Противоядия могут быть разработаны лишь для ограниченного количества ксенобиотиков. Во-первых, маловероятна разработка лечебных антидотов в отношении токсикантов,… Во-вторых, антидоты к малотоксичным (но порой весьма опасным) токсикантам редко оказываются достаточно эффективными.…РАЗДЕЛ 6. СПЕЦИАЛЬНЫЕ ФОРМЫ ТОКСИЧЕСКОГО ПРОЦЕССА
ГЛАВА 6.1. ИММУНОТОКСИЧНОСТЬ
Иммунотоксичность следует рассматривать в двух аспектах: как собственно повреждающее действие веществ на иммунную систему и как участие иммунной системы в реализации механизмов токсического действия ксенобиотиков. Первый аспект прослеживается, например, в явлении снижения резистентности организма, подвергшегося действию токсиканта, к инфекции; второй - превалирует в феномене сенситизации кожных покровов, дыхательных путей и т.д. к химическим веществам (см. разделы "Дерматотоксичность", "Пульмонотоксичность"). Оба аспекта неразрывно связаны между собой.
Иммунная система включает кровеносное русло и лимфатические сосуды, пронизывающие все ткани организма, по которым перемещаются мириады иммунокомпетентных клеток. Функция системы - выявить чужеродные элементы (антигены), проникшие во внутренние среды, изолировать их и уничтожить. Это реализуется в несколько этапов:
а) накопление чужеродных элементов в лимфоидной ткани;
б) прохождение иммунокомпетентных клеток через лимфоидные структуры и их трансформация в антиген-специфичные за счет контакта с чужеродными элементами (антигенами);
в) диссеменация продуктов иммунологической трансформации (антиген-специфичных клеток и гуморальных факторов иммунитета) в крови и тканях;
г) взаимодействие продуктов трансформации с антигеном;
д) манифестация процесса, который может быть местным и общим, острым и хроническим, обратимым и необратимым, отчетливо проявляющимся и скрытым.
Иммунная система является высоко специализированной, сложно регулируемой системой, её клеточные элементы находятся в состоянии постоянной пролиферации. В этой связи любое токсическое воздействие обязательно амплифицируется. При этом повреждение иммунной системы может проявляться усилением или супрессией иммунных функций организма, либо вообще не проявляться клинически. Подавление иммунитета приводит к учащению инфекционных заболеваний, ослаблению механизмов противоопухолевой защиты организма. Усиление иммунного ответа приводит к формированию аутоиммунных процессов, аллергизации организма или патологической гиперчувствительности к определенным антигенам.
Огромное количество веществ обладает иммунотоксичностью. Полагают, что практически любая интоксикация в той или иной степени может стать причиной нарушения иммунного статуса организма. Однако к числу иммунотоксикантов, т.е. веществ, нарушающих иммунные реакции организма, действуя в минимальных дозах, можно отнести лишь ограниченное количество соединений. Перечень иммунотоксикантов, достаточно широко используемых в хозяйственной деятельности, представлен в таблице 1.
Таблица 1. Перечень наиболее известных промышленных токсикантов, обладающих выраженной иммунотоксичностью
| Бериллий Платина Хром Кадмий Никель Этиленоксид Формальдегид Полигалогенированные ароматические углеводороды ДДТ Диэльдрин Карбарил 2,3,7,8-тетрахлордибензофуран 2,3,7,8-тетрахлордибенз-р-диоксин Метилртуть Оловоорганические соединения Эпоксидные смолы Изоцианаты Эфиры гликоля |
Для выявления действия веществ на иммунную систему разработаны многочисленные методы исследования, выполняемые in vivo и in vitro. Иммунные клетки легко изолировать, а их функции изучить in vitro. Антитела также легко выделить и их количество оценить. Информация об иммунотоксичности веществ может быть использована для оценки риска, которому подвергаются лица, контактирующие с ними.
Краткая характеристика морфологических и функциональных особенностей иммунной системы млекопитающих
Иммунокомпетентные клетки
Помимо упомянутой, существует популяция тимуснезависимых лимфоцитов (В-лимфоциты). Хотя вопрос окончательно не решён, полагают, что в организме… Таблица 2. Некоторые свойства иммуноглобулинов человека Свойства … В отличие от пролиферации лимфоцитов в первичном лимфоидном органе, их пролиферация во вторичных органах зависит от…Органы и ткани иммунной системы
Селезёнка.Селезёнка - основной фильтр антигенов, циркулирующих в крови, а также место формирования иммунного ответа на чужеродные элементы. Помимо… Лимфатические узлы.В организме человека насчитывается 500 - 600 лимфатических… Печень.Нормальная печень взрослого человека весит 1400 - 1600 грамм и состоит из левой и правой доли. Строение органа…Особенности функционирования системы
Характерными особенностями функционирования иммунной системы являются: 1. Специфичность. Известно, что устойчивость в отношении отдельных заболеваний… 2. Память. Если антиген определенного вида уже являлся причиной иммунной реакции, то элементы системы навсегда…Иммунокомпетентность
Помимо иммунной системы резистентность к указанным факторам обеспечивается механическими барьерами (кожа, слизистые), выделением секретов,… В отличие от врожденной резистентности, механизмы приобретенной резистентности… 1. Образовывать функциональные барьеры, обеспечивающие его единство и изоляцию от окружающей среды.Действие токсикантов на иммунную систему
Понятие иммунотоксичности
В основе нарушений могут лежать разнообразные эффекты, от грубого повреждения стволовых клеток костного мозга, до изменения продукции цитокинов и… Нормальной считается сбалансированная иммунная реакция организма на антигены.… - угнетение иммунного ответа (иммуносупрессия);Иммуносупрессия
К числу алкилирующих агентов относятся, помимо отравляющих веществ (сернистый, азотистый, кислородный иприты), профессиональных вредностей… Наиболее известные иммуносупрессоры - аналоги пуриновых оснований, это…Иммуносупрессия и инфекция
Иммуносупрессия и канцерогенез
Таблица 4. Некоторые показатели иммунного статуса мышей, отравленных бенз(а)пиреном Показатели Выраженность (% от нормы) …Гиперчувствителность (аллергия)
Характеристика состояния гиперчувствительности
1. Термин "аллергия" введен Pirquet в 1906 году. Этим термином обозначалась изменённая реакция организма на повторное действие фактора. В… 2. Термин "анафилаксия" предложен Porter и Richet в 1902 году для… 3. Термин "атопия" предложен Coca в 1920 году для описания многочисленных необычных реакций, развивающихся у…Псевдоаллергические реакции
Иммуногены и аллергены
Еще со времен Ландштейнера известно, что при определенных условиях возможно формирование иммунной реакции на введение низкомолекулярного вещества,… В настоящее время установлено, что в иммунном ответе на комплексный антиген… Как указывалось выше, в качестве носителя гаптена могут выступать различные макромолекулы: белки, полипептиды,…Аутоиммунные процессы
Имеющиеся данные свидетельствуют, что аутоиммунные заболевания являются следствием количественных нарушений отдельных сторон и в норме протекающих… Аутоиммунные заболевания подразделяются на орган-специфичные и… Таблица 9. Аутоиммунные болезни. Патология, обусловленная антителами Синдромы Соответствующие…Краткая характеристика токсикантов
Бериллий.
В 1945-50 годах в США регистрировались эпидемические вспышки острых и хронических интоксикаций бериллием на предприятиях по его производству,… Заболевание, возникающее в результате длительно воздействия бериллием,… Нарушения функций легких при хроническом бериллиозе могут протекать в нескольких формах:Определение иммунотоксичности ксенобиотиков
Таблица 10. Двухэтапный пакет тестов оценки иммунотоксичности ксенобиотика Этап Параметры Методы исследования 1.… Исследования первого этапа предназначены для выявления потенциальных… Для изучения иммуносупрессорных свойств токсикантов в лабораторных условиях могут быть применены животные, зараженные…Выявления иммунотоксических эффектов
Исследования должны начинаться с тщательного обследования и сбора анамнеза. Необходимо особое внимание уделять выявлению классических проявлений и…Оценка иммунологического статуса
Таблица 11. Тесты клинического иммунологического скрининга - Подсчет числа форменных элементов крови. Формула крови - Количественный… Гуморальный иммунитет: - Количество иммуноглобулинов (IgG,… Клеточный иммунитет: - Кожные тесты на отсроченную гиперреактивностьГЛАВА 6.2. ХИМИЧЕСКИЙ МУТАГЕНЕЗ
Мутации - это наследуемые изменения генетической информации, хранящейся в ДНК клеток. Различные факторы химической и физической природы способны вызывать мутации. Наиболее изученными являются последствия действия ионизирующей радиации и таких веществ, как сернистый и азотистый иприты, эпоксиды, этиленимин, метилсульфонат и т.д. Химические вещества, способные вызывать мутации называются мутагенами.
Далеко не всякая модификация молекулы ДНК (мутация) является опасной для организма. Более того, эволюция была бы не возможна без мутаций, поскольку именно она лежит в основе изменчивости. Опасность представляет случайный, ненаправленный мутагенез, как правило, несущий для организма негативные последствия. Неблагоприятные эффекты мутагенеза определяются тем, в клетках какого типа он реализуется: половых или соматических, стволовых и делящихся или созревающих и зрелых. Результатом грубых мутаций половых клеток и делящихся клеток развивающегося плода являются: стерильность особи, врожденная патология у потомства, тератогенез, гибель плода. Мутации стволовых и делящихся соматических клеток сопровождаются структурно-функциональными нарушениями тканей с непрерывной физиологической регенерацией (система крови, иммунная система, эпителиальные ткани) и канцерогенезом. Повреждение токсикантом ДНК зрелой соматической клетки не приводит к пагубным последствиям для организма.
Основными видами мутаций, вызываемых химическими веществами, являются: 1) точечная мутация, связанная с модификацией одного нуклеотида в структуре ДНК, (замещение нуклеотида, выпадение нуклеотида из цепи, включение дополнительного нуклеотида в цепь); 2) хромосомные аберрации, т.е. изменение структуры хромосом (разрывы молекул ДНК, транслокации фрагментов ДНК) или числа хромосом в клетке.
Точечные мутации
Замещение нуклеотида
Примером химической модификации является изменение нуклеотида азотистой кислотой.HNO2 способна превращать цитозин в урацил или аденин в гипоксантин… Рисунок 1. Превращение цитидина в уридин под влиянием азотистой кислотыВыпадение или включение дополнительного нуклеотида
Рисунок 4. Выпадение аденина (А*) приводит к сдвигу цепи нуклеотидов влево и… Некоторые токсиканты, например производные акридина, способны вызывать подобные изменения в структуре ДНК.Репарация ДНК
Ряд ферментов, участвующих в репарации поврежденных ДНК, в настоящее время хорошо изучен (см. выше). Например, метилтрансферазы принимают участие в…Хромосомные аберрации
В ходе "сшивания" двунитевых разрывов хромосом весьма вероятны ошибки. Основные виды нарушений, возникающих при этом, это делеция,… Увеличение числа хромосом в клетке может явиться следствием нарушения процесса…Условия действия мутагенов на клетки
1. Покоя (фаза G0): клетка функционирует или покоится (большинство соматических неделящихся клеток); 2. Синтеза клеточных компонентов, необходимых для последующего синтеза ДНК… 3. Синтеза ДНК (фазаS): осуществляется "сборка" новой молекулы ДНК из наличествующих в клетке компонентов.…Изучение мутагенной активности
Изучение мутагенной активности химических веществ осуществляется в опытахin vitro на прокариотических и эукариотических клетках, путем непосредственного изучения степени повреждения ДНК, и выявления хромосомных аберраций у животных, подвергшихся действию токсикантов.
Исследования в опытах на прокариотах. Тест Эймса
Тест осуществляется на суспензии бактериальных клеток в расплавленном при 450 агаре. В инкубационную среду (не содержащую гистидин) добавляют… В настоящее время тестирование проводят и на других биологических объектах…Исследования в опытах на клетках млекопитающих
Исследования по оценке мутагенности обычно проводят, изучая изменения резистентности клеток к: 8-азагуанину или 6-тиогуанину (определяется… ГГФРТ регулирует инкорпорацию пуринов из среды в клетку. Мутация локуса ДНК,… ТК активирует транспорт пиримидинов. Мутация лкуса ДНК, ответственного за синтез ТК, делает клетку не чувствительной к…Оценка индукции синтеза ДНК клетками млекопитающих
Исследования обычно выполняются на гепатоцитах взрослых крыс самцов, диспергированных в инкубационной среде с последующей спонтанной адгезией на… Недостатком метода является то, что с его помощью невозможно оценить, приводит…Исследование ковалентного связывания токсикантов
Изучение хромосомных аберраций
Одним из широко используемых методов выявления генотоксичности является так называемый "микронуклеарный тест". Микроядра представляют… Повреждение герменативного эпителия (нарушения сперматогенеза) токсикантом… Наследуемые мутации могут быть выявлены путем прямого исследования клеток потомства (на различных стадиях развития)…ГЛАВА 6.3. ХИМИЧЕСКИЙ КАНЦЕРОГЕНЕЗ
Канцерогенами называются химические вещества, воздействие которых достоверно увеличивает частоту возникновения опухолей или сокращает период их развития у человека или животных.
Судьба этих веществ в организме, как и других ксенобиотиков, подчиняется общим законам токсикокинетики. Однако в действии на организм им присущ ряд особенностей. Так, развивающиеся под их влиянием эффекты носят отсроченный характер и являются следствием, как правило, длительного кумулятивного действия в малых дозах. Активность рассматриваемой группы веществ в отношении молекул - носителей наследственности в известной степени уникальна.
Первым, кто осознал возможность химической этиологии рака, был Percival Pott. В 1775 году им описан рак мошонки у ряда пациентов. Все они били трубочистами, что и натолкнуло доктора Pott на мысль, что длительный контакт кожи с сажей, может приводить к развитию рака. 100 лет спустя высокая частота рака кожи была выявлена у немецких рабочих, имевших длительный контакт с каменноугольной смолой - основным ингредиентом сажи. Позже было установлено, что веществами, содержащимися в смолах, и обладающими канцерогенной активностью, являются полициклические ароматические углеводороды (ПАУ). Характерные особенности строения этих соединений отражают структуры классических представителей группы: бензо(а)пирена и дибенз(а,h)антрацена (рисунок 1).
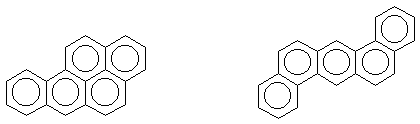
бнезо(а)пирен дибензо(а,h)антрацен
Рисунок 1. Типичные представители группы полициклических углеводородов
В 1935 году была доказана канцерогенная активность целого ряда азокрасителей. В 1937 году в опытах на собаках удалось показать, что ароматические амины, и в частности 2-нафтиламин, способны вызывать опухоли мочевого пузыря. Высокая частота случаев этого новообразования у рабочих, контактировавших с некоторыми красителями, была показана ещё в 19 веке.
Следует различать понятия "канцерогенная активность" ("канцерогенность") и "канцерогенная опасность" вещества. Канцерогенная активность свидетельствует о способности вещества индуцировать развитие злокачественных новообразований, позволяет осуществлять сравнение веществ по этому признаку при непосредственном воздействии их на биологический объект. Канцерогенная опасность включает в себя дополнительные условия: распространенность вещества, возможность контакта с ним, его стабильность в окружающей среде или в местах потенциальных контактов и др.
Краткая характеристика канцерогенов
В ряде случаев канцерогенез есть результат сочетанного действия ксенобиотиков. Так, ведущим канцерогенным фактором для человека является табачный… Канцерогенными свойствами обладают некоторые вещества природного… В материалах, опубликованных Международной Ассоциацией Исследований Рака (МАИР), содержится указание на более чем 60…Классификации канцерогенов
Предложено классифицировать канцерогены по происхождению, химической структуре, степени участия в различных стадиях развития рака, по степени доказанности их канцерогенной активности и т.д.
1.Происхождение канцерогенов.
Природные канцерогены, это вещества, содержание которых в среде не зависит от деятельности человека. Их вклад в онкозаболеваемость считается незначительным. Так, установлено, что ежесуточно на поверхность Земли выседает около 170 т метеоритной пыли, в составе которой обнаруживаются полициклические ароматические углеводороды (ПАУ).
На планете в настоящее время действует около 520 вулканов, их ежегодный выброс составляет 3-6 млрд. т химических веществ (аэрозоли, пепел, лава, газы). С пеплом в атмосферу может поступить до 12-24 т только одного бенз(а)пирена, не считая других ПАУ.
Обнаружены и описаны природные источники таких канцерогенов как мышьяк, асбест, афлатоксины, радионуклиды и др. Так, значительное число злокачественных новообразований кожи наблюдается на юго-западном побережье острова Тайвань, где население потребляет воду с высоким содержанием мышьяка - до 1,8 мг/л (ПДК в России - 0,05 мг/л).
Иногда канцерогены естественного происхождения могут накапливаться в организмах живых существ и растениях и по пищевым цепям попадать в организм человека (токсины сине-зеленых водорослей, афлатоксины).
Канцерогены антропогенного происхождения появились тогда, когда люди научились пользоваться огнем (около 500 тыс. лет назад). По-видимому, первыми искусственными канцерогенами были продукты пиролиза белков. Накопление канцерогенов в биосфере возрастало параллельно интенсификации промышленного производства. Процесс ускорился в последние десятилетия ХХ века. Например, производство бензола, вызывающего у людей лейкозы, составляет ежегодно 12 млн. т. Полихлорированных бифенилов произведено к настоящему времени 1,2 млн. т. Несмотря на запрещение выпуска и использования ПХБ их концентрация во всех средах биосферы и биообъектах не снижается. Суммарное поступление этих токсикантов в окружающую среду достигает 35% от произведенной массы. Из этого количества лишь 4% подвергается естественной деградации.
2.Химическая структура.
К канцерогенам относятся вещества, имеющие совершенно различное химическое строение (рисунок 2). Среди них ПАУ и гетероциклические соединения, ароматические азосоединения, ароматические аминосоединения, нитрозоамины и нитроамины, металлы, металлоиды и неорганические соли и др.

Рисунок 2. Структура некоторых канцерогенов, синтетических и естественного происхождения
3.Участие в различных стадиях развития рака (см. ниже).
4.Степень доказанности канцерогенной активности вещества.
Наиболее полный перечень веществ, исследованных на их канцерогенную активность, и соответственно их классификация принадлежит Международному Агентству Изучения Рака (МАИР, Лион, Франция). В нем представлены данные по более чем 800 соединениям. Список непрерывно пополняется.
Первая группа включает вещества, производственные или иные факторы, для которых имеются безусловные доказательства опасности возникновения опухолей у человека, то есть как минимум убедительные эпидемиологические данные (список веществ 1-й группы приведен выше). В эту группу вошло более 60 факторов, причем не только отдельные соединения, применяющиеся в быту, медицине, сельском хозяйстве, промышленности, но и сами производственные условия.
Вторая группа включает те факторы, которые "вероятно" (т.е. с высокой степенью доказанности) или "возможно" (с меньшей степенью доказанности) канцерогенны для человека. Эта группа делится на 2 подгруппы: 2А - 51 фактор (акрилонитрил, формальдегид, диметилсульфат, нитрозодиэтиламин и др.) и 2Б - 192 фактора (кобальт, ДДТ, акриламид, нитропирены, ПХБ и др.).
Третья группа включает 446 химических веществ, которые сегодня, на основании имеющихся данных, не могут быть отнесены к факторам канцерогенного риска для человека.
Четвертая группа - агенты, для которых существуют убедительные доказательства отсутствия канцерогенной опасности для человека (до недавнего времени здесь числилось только одно вещество - капролактам).
Перечень МАИР постоянно изменяется в результате проведения все новых и новых исследований. Он носит рекомендательный, а не обязательный характер. На территории Российской Федерации действует иной список канцерогенов, утвержденный Минздравом (приводится выше).
Стадии химического канцерогенеза
Инициация опухолевого роста. Процесс непосредственного действия канцерогена на клетки, запускающий их трансформацию, называется инициацией опухолевого роста.
Впервые термин инициация был предложен в 1941 году Rous и Kidd для обозначения манипуляции, состоящей в аппликации смолы на кожу уха кролика, с целью вызвать в дальнейшем опухолевый рост. Как правило, в эксперименте для провокации неоплазмы, лишь инициации недостаточно. Необходимы и другие условия, которые определяются видом экспериментального животного, факторами окружающей среды.
Стадия инициации включает быстрое, практически необратимое повреждение генетического материала клеток, предрасполагающее их к последующему неопластическому развитию (см. разделы "Механизм действия", "Мутагенез"). Поврежденные клетки называются "инициированными" и нуждаются в периоде репликации генетического материала, с тем, что бы зафиксировать вызванные изменения (мутации). В соответствии с существующими представлениями, инициированная клетка может длительное время оставаться в состоянии покоя, не проявляя агрессии, до тех пор, пока не подействует другой (другие) фактор, побуждающий клетку к делению, клонообразованию и, тем самым, формированию опухоли.
Характерными особенностями действия инициаторов являются:
- необратимость;
- куммулятивность;
- отсутствие морфологических проявлений;
- зависимость эффекта от особенностей метаболизма клетки и фаз её клеточного цикла;
- беспороговость.
Промоция опухолевого роста. Процесс, в ходе которого инициированная клетка завершает неопластическую трансформацию называется промоцией.
Рисунок 3. Примеры химического строения некоторых промоторов Многие промоторы являются органо-специфичными. Так, сахарин - промотор… Классический пример действия промоторов может быть представлен в эксперименте. На кожу спины мышам апплицируют…Механизмы действия
Таблица 3. Некоторые примеры генотоксических и эпигенотоксических канцерогенов Генотоксические канцерогены Эпигенотоксические… Для многих канцерогенов, действующих на геном клетки, первичной мишенью… В пользу того, что молекула ДНК является критической структурой канцерогенеза, говорят следующие факты:Коканцерогены
Таблица 4. Предполагаемы механизмы коканцерогенеза - Увеличение скорости и объема захвата канцерогенов клетками - Интенсификация… Действие некоторых коканцерогенов является доказанным в эксперименте.… Вещества, содержащиеся в табачном дыму, являются коканцерогенами асбеста. Так, у рабочих профессионально…Метаболизм и биоактивация канцерогенов
Рисунок 5. Роль цитохрома Р450 в процессах химического канцерогенеза Общим свойством многих канцерогенов является их способность к биотрансфомации с образованием высоко…Краткая характеристика токсикантов
Бензол
Бензол является исходным продуктом синтеза большого количества веществ и входит в первую десятку наиболее потребляемых промышленностью соединений.
Это бесцветная летучая жидкость со своеобразным ароматическим запахом; температура кипения около 800, давление пара 100 мм Hg. Легко воспламеняется. Вещество ограниченно растворяется в воде (1 : 1420), но хорошо смешивается с маслами и спиртами. Впервые описано Фарадеем в 1825 году. Промышленное производство налажено в 1849 году.
Впервые случаи лейкозов, обусловленные действием бензола, описаны в 1897 году (Le Noir, Claud, 1897). Однако процент заболеваний, индуцированных веществом, в сравнении с общим количеством лейкемий был невелик. Повышение значения этого феномена связано с широким распространением бензола в современных технологических процессах. Анализ показывает, что многие вещества, угнетающие костный мозг, могут одновременно вызывать и лейкемии. В 60-е годы было отмечено существенное увеличение числа лейкемий у турецких рабочих, занятых в обувной и кожевенной промышленности и контактировавших с клеящими материалами на основе бензола. Публикация этих данных и сообщение об аналогичных наблюдениях на итальянских предприятиях, послужили поводом проведения серьёзных токсико-эпидемиологических исследований среди лиц, контактирующих с бензолом. В ходе этих исследований удалось подтвердить лейкемогенное действие бензола.
Помимо производства бензол оказывает действие на человека и через окружающую среду. Бензол нередко выделяется при горении различных веществ и является составной частью дыма при пожарах, сигаретного дыма, выхлопных газов. Содержание его в бензине от 0,5 до 2%. Бензол - естественный компонент овощей, фруктов, мяса, яиц. Содержание его в продуктах питания от 2 до 2100 мкг/ кг. Вещество не способно к материальной кумуляции и потому его экологическое значение определяется количеством потребляемых продуктов, содержащих это соединение. С позиций концепции пороговости в действии токсикантов на организм значение бензола, как экологического фактора, ничтожно. Если допустить беспороговый характер действия вещества, хотя бы по способности вызывать лейкемию, можно говорить о некоторой его опасности, как "средового" фактора.
Спорным остаётся вопрос о вредном действии бензола, как компонента табачного дыма (последний содержит массу других токсичных веществ, среди которых: полиароматические углеводороды, 1,3-бутадиен и т.д.). Курильщик, в среднем, в сутки потребляет примерно в 10 раз больше бензола (1800 мкг/ день для выкуривающего пачку сигарет), чем некурящий. Однако, если основываться на пороговости в действии токсиканта, это количество составляет ничтожную часть от дозы, вызывающей токсический эффект.
В настоящее время представления о пороговости лейкемогенного действия бензола не однозначны. По мнению ряда специалистов, способность вещества вызывать лейкемии носит стохастический беспороговый характер. При этом полагают, что кумуляция эффекта и развитие лейкемии могут произойти не зависимо от действующей концентрации токсиканта. Риск развития лейкемии от контакта с веществом в той или иной дозе устанавливается путем экстраполяции данных, получаемых при действии высоких концентраций бензола, к условиям контакта с малыми дозами вещества (см. ниже).
Согласно другой точке зрения, порог лейкемогенного действия существует. В этой связи контакт с веществом в малых концентрациях объявляется неопасным. Накопилось немало клинических и экспериментальных данных, подтверждающих эту точку зрения. Показана высокая степень корреляции между возникновением лейкемии и наличием в анамнезе данных об интоксикации бензолом, проявившимся нарушениями со стороны системы крови. В многочисленных работах описаны случаи перерастания панцитопении, угнетения костного мозга, его гипоплазии и апластической анемии, вызванных бензолом, в острый миелоидный лейкоз. С другой стороны, практически отсутствуют описания случаев лейкемий, вызванных бензолом, без предшествовавшего им этапа (в анамнезе) панцитопении. Вместе с тем хорошо известно, что у лиц, перенёсших лучевую или химеотерапию по поводу новообразований, изменения со стороны костного мозга регистрируются в течение длительного времени, иногда годами после полной нормализации показателей периферической крови. Из этого следует, что нормальные показатели крови у лиц, контактирующих (контактировавших) с бензолом, ещё не являются свидетельством отсутствия его пагубного действия на организм.
Каким образом токсическое действие бензола перерастает в лейкемогенное остаётся неясным.
Как следует из имеющихся (порой противоречивых и не всегда в полной мере доказанных) наблюдений, наиболее частым типом лейкемий, вызываемых бензолом, являются острые миелоидные лейкозы (ОМЛ), особенно острая миелобластная лейкемия, мономиелоцитарная лейкемия и эритролейкемия. При диагностике последней формы следует проводить дифференциальный диагноз с компенсаторной эритроидной гиперплазией. Другие типы лейкемий встречаются при действии бензола значительно реже.
Не выяснен и механизм формирования лейкемии. Вероятными механизмами действия бензола могут быть мутации, возникающие либо в результате образования ДНК-аддуктов, либо хромосомной делеции или анеуплоидии вследствие нарушения процесса редубликации нитей ДНК и их распределения между дочерними клетками в процессе митоза. Строение бензола, его метаболитов и их химическая активность делают более вероятным второй механизм действия токсиканта. Так, в отличии от активных алкилирующих агентов бензол и его метаболиты не являются цикло-неспецифичными мутагенами или тератогенами. Не смотря на целенаправленные поиски, в клетках костного мозга отравленных не удалось обнаружить бензольных аддуктов ДНК. С другой стороны, установлена способность бензола блокировать клеточное деление на стадии G2/ М митоза, угнетая процесс формирования клеточного веретена (объясняют действием метаболитов бензола на сульфгидрильные группы тубулина).
У рабочих, хронически подвергающихся действию бензола, обнаружено увеличение числа хромосомных аберраций, в частности, количества анеуплоидных клеток.
Бутадиен
В эксперименте показана высокая степень видовых различий в чувствительности животных к канцерогенному действию вещества. Крысы - относительно…Выявление канцерогенной активности веществ
Вывод о канцерогенной активности того или иного вещества основывается на результатах двух видов исследований. Во-первых, это эксперименты на различных биологических объектах и лабораторных животных. Во-вторых - данные эпидемиологического обследования групп лиц, контактирующих или контактировавших с токсикантами.
Экспериментальная оценка
Таблица 5. Протокол изучения канцерогенной активности вещества А. Оценка химического строения вещества Б. Исследования в опытах in… Исследование предполагает выявление мутагенной, тератогенной активности у… Изучение канцерогенной активности в хроническом эксперименте предполагает длительное (1,5 - 2 года) введение веществ…Эпидемиологические исследования
- выявленное увеличение частоты новообразований в обследованной популяции не может быть объяснено действием случайных причин; - аналогичные результаты получены в ходе нескольких независимых… - доказано, что частота появления опухолей изменяется при изменении дозы канцерогена и времени прошедшего от момента…Оценка риска химического канцерогенеза
Проблемы оценки риска
Противоречие состоит в следующем. Исследователя интересуют количественные характеристики увеличения частоты опухолевого роста при длительном…Математические модели, описывающие зависимость доза - эффект
- достаточное количество изученных доз (минимум четыре) и животных, протестированных на каждой дозе; - учет "фоновых" значений оцениваемых параметров; - математическая форма представления зависимости "доза-эффект";Процедуры определения пороговых уровней риска
- на основе эмпирически найденных параметров принятой математической модели; - линейной экстраполяции к малым дозам без учета математической модели… Процедура поиска параметров кривой зависимости "доза-эффект" аналогична для всех упомянутых ранее моделей.…ГЛАВА 6.4. ТОКСИЧЕСКИЕ ВЛИЯНИЯ НА РЕПРОДУКТИВНУЮ ФУНКЦИЮ. ТЕРАТОГЕНЕЗ
Репродуктивная функция осуществляется как сложноорганизованная последовательность физиологических процессов, протекающих в организме отца, матери, плода. Токсиканты могут оказывать неблагоприятное воздействие на любом этапе реализации функции. Сложность феномена репродукции делает его весьма уязвимым для ксенобиотиков. Трудность познания феномена состоит в том, что нарушение репродукции может быть следствием даже острого токсического действия на различные органы и системы одного из "участников" процесса, в различные временные периоды, а проявляться лишь спустя многие месяцы, а иногда и годы, дефектами зачатия, вынашивания, развития плода и несостоятельностью растущего организма (таблица 1).
Таблица 1. Периоды реализации репродуктивной функции, уязвимые для действия токсикантов.
| Предконцептивный период - половое созревание - половое влечение - формирование половых клеток (гамет) - транспорт гамет |
| Концептивный период - оплодотворение - имплантация яйцеклетки - развитие плаценты |
| Беременность - развитие эмбриона - созревание плода |
| Рождение - роды - постнатальный период - лактация |
| Рост и развитие ребенка - развитие половых органов - формирование интеллекта Трансплацентарный канцерогенез |
Краткая характеристика анатомо-физиологических особенностей репродуктивных органов
Яичники представляют собой миндалевидный парный орган, локализующийся по обе стороны матки. Функции яичников - овогенез, т.е. образование женских… Фаллопиевы трубы - каналы, связывающие яичник с просветом матки. Это место… Матка - полый орган, с мощными мышечными стенками, расположенный в полости таза. Анатомически матка подразделяется на…Развитие плода
Особенности действия токсикантов на репродуктивные функции
Неблагоприятное действие токсикантов (и их метаболитов) на мужские и женские органы репродуктивной системы может быть обусловлено либо нарушением… Цитотоксичность, как правило лежит в основе поражения половых клеток отца или… Механизм действия многих токсикантов остается неизвестным (сероуглерод, углеводороды). Некоторые из опасных веществ,…Тератогенез
Современная тератология как наука начала формироваться в сороковых годах двадцатого века после работ Warknay и сотрудников, показавших, что влияние… Тератогенным называется действие химического вещества на организм матери, отца… Существует четыре типа патологии развития плода: гибель, уродства, замедление роста, функциональные нарушения.Действие токсиканта, сопровождающееся гибелью эмбриона, чаще обозначается как эмбриотоксическое.
Закономерности тератогенеза
Особенности токсикокинетики. Тератогенным действием на плод обладают лишь вещества, хорошо проникающие через плацентарный барьер. Многие тератогены… Генетическая предрасположенность. Чувствительность к тому или иному тератогену… Отчасти этот феномен связан с существенными различиями токсикокинетики ксенобиотиков.Особенности токсикокинетики тератогенов
Токсический эффект ксенобиотиков может зависеть от действия на структуры-мишени их метаболитов, образующихся в организме матери или/и плода.… Попав в кровоток плода, токсиканты распределяются в его органах и тканях в…Механизмы действия тератогенов
Генерация мутаций (мутагенез) - явление модификации токсикантом последовательности нуклеотидов в молекуле ДНК (см. выше). Установлено, что около 20… Повреждение хромосом - явление разрыва хромосом или их слияния (нерасхождение… Повреждение механизмов репарации. Нарушение свойств генетического аппарата клетки может быть следствием угнетения…Характеристика некоторых токсикантов, влияющих на репродуктивные функции
Талидомид
Рисунок 2. Структура талидомида В 60х годах этот препарат использовали в медицинской практике Германии, Великобритании, других странах Европы и…Ртуть
Это вещество является выраженным тератогеном для экспериментальных животных. Для человека этот вид токсического действия окончательно не доказан. Хлорид ртути вызывает аборты, однако, трансплацентарное поступление неорганических соединений ртути в организм плода не приводит к врожденным аномалиям. Пары ртути, действуя ингаляционно, вызывают нарушения менструального цикла. Элементарная ртуть также обладает способностью проникать через плацентарный барьер. Повышенное содержание ртути в плаценте и тканях плода обнаружено при обследовании женщин стоматологов, имевших контакт с ртутными амальгамами.
Метилртуть вызывает серьёзное поражение мозга плода, сопровождающееся нейрональной дегенерацией и пролиферацией глии, особенно выраженной в коре мозжечка и конечного мозга. Глубина нарушений зависит от сроков беременности. Особенно опасно воздействие токсиканта во втором и третьем триместре беременности. Некоторые проявления патологических изменений выявляются сразу после рождения, другие, спустя несколько месяцев. Основные симптомы поражения: спастичность, гипотония, микроцефалия, нарушение движения глазных яблок (нистагм, стробизм), умственная отсталость, нарушение роста зубов. Отсутствуют данные о дозовой нагрузке, приводящей к патологии.
Свинец
То, что металл влияет на репродуктивные функции, известно более 100 лет. На 12 - 14 неделях беременности вещество начинает проникать через плаценту. При длительном действии на организм матери свинец накапливается и в тканях плода. Последствиями этого являются: аборты, преждевременные роды, перинатальная гибель. Имеются сообщения о неврологических нарушениях у детей, рожденных женщинами, в крови которых содержание свинца более 10 мг/ дл. Данные о способности свинца вызывать врожденные уродства отсутствуют.
Действие свинца на отцов также пагубным образом сказывается на развитии плода, однако пока не ясно, является ли это следствием прямого влияния на сперматогенез (хромосомные аберрации, снижение числа сперматозоидов, изменение их формы и активности). Не исключено, что в ряде случаев, причина нарушений - поражение матери в домашних условиях свинцовой пылью, приносимой отцом с производства.
Дети, подвергшиеся воздействию свинца в утробе матери, требуют длительного и постоянного контроля состояния их здоровья. Необходимо контролировать количество свинца в плазме крови, протопорфиринов в эритроцитах, оценивать неврологический статус.
Кадмий
В лабораторных условиях периодически наблюдаются эффекты, связанные с действия кадмия на репродуктивные функции экспериментальных животных. Эффект зависит от дозы вещества, вида лабораторного животного, периода воздействия. Экстраполяция данных, в этой связи, на человека весьма затруднена. Основываясь на экспериментальных данных, полагают, что тератогенное действие Cd-содержащих веществ может быть связано с ингибированием активности карбоангидразы. Установлено также, что кадмий способен накапливаться в плаценте и вызывать её повреждение.
Данные, полученные при обследовании людей менее убедительны. Только при действии вещества в высоких дозах иногда отмечается повреждение семенников, тератогенез.
Полигалогенированные бифенилы (ПГБ)
В условиях лаборатории тератогенное действие ПГБ выявляется постоянно. Имеются данные, согласно которым поступление веществ в организм женщины в…Органические растворители
Имеются единичные наблюдения, когда действие органических растворителей на женщин в период беременности приводит к появлению ряда врожденных…Цитостатики
С другой стороны отсутствуют убедительные данные, указывающие на неблагоприятное действие цитостатиков (по показателю "увеличение риска…Выявление действия токсикантов на репродуктивную функцию.
Экспериментальное изучение
1. Изучение оплодотворяемости и общей репродуктивности - в опытах на одномпоколении животных; 2. Изучение оплодотворяемости и общей репродуктивности - в опытах на… 3. Изучение тератогенной активности веществ;Оценка риска поражения
В этой связи оценка риска поражения и диагностика действия токсиканта на репродуктивную функцию людей строятся на комплексном изучении состояния… Признаки нарушения репродуктивных функций могут быть различными, но всегда… Во всех подобных случаях врачу необходимо обследовать пациента, документировать все предъявляемые жалобы, выявить…Эпидемиология токсического действия
Анализируемые показатели
Одним из часто оцениваемых показателей является оплодотворяемость, т. е. характеристика способности женщины стать беременной. Оплодотворяемость… Оплодотворяемость и вынашиваемость (так называемые интенсивные характеристики… Таблица 9. Вероятность спонтанных абортов в различные сроки беременности Время после овуляции …Методы сбора информации
В ходе ретроспективных исследований формируют группы сравнения, в одной из которых, у обследуемых, выявлены нарушения репродукции, в другой -… Проспективные исследования предполагают сравнительное обследование лиц,… Интервенционные исследования предназначены для установления частоты развития исследуемых нарушений в контрольной…Контроль тератогенеза в популяции
Уместность. Учитываемые дефекты развития должны быть клинически значимыми. Небольшие нарушения морфологии лица, конечностей и т.д. могут являться… Временная корректность. Большинство уродств является следствием действия… Чувствительность. Предлагаемые методы обследований должны быть достаточно чувствительными для выявления умеренного…РАЗДЕЛ 7. ИЗБИРАТЕЛЬНАЯ ТОКСИЧНОСТЬ
ГЛАВА 7.1. РАЗДРАЖАЮЩЕЕ ДЕЙСТВИЕ
Раздражающим называется избирательное действие химических веществ на нервные окончания, разветвляющиеся в покровных тканях, сопровождающееся рядом местных и общих рефлекторных реакций и субъективно воспринимаемое, как неприятное чувство покалывания, жжения, рези, боли и т.д.
Наиболее чувствительными к раздражению являются покровные ткани, в которых плотность нервных окончаний выше, где они более доступны действию химических веществ. Это, прежде всего, конъюнктива глаз, слизистая дыхательных путей. Покровные ткани этих органов имеют особенности строения, иннервации и потому неодинаково чувствительны к различным веществам. Отдельные токсиканты вызывают преимущественное раздражение органа зрения и условно обозначаются как слезоточивые (лакриматоры), другие - слизистой дыхательных путей (стерниты).
Краткая характеристика химических и физико-химических свойств токсикантов
Вещества, обладающие раздражающим действием, как правило, плохо растворимы в воде, но хорошо в органических растворителях. Они могут быть… К числу веществ с высокой раздражающей активностью, прежде всего, относятся:… По способности сообщать галогенированной молекуле кетона свойства лакриматора атомы галогенов располагаются в…Патогенез токсического эффекта
Первичным звеном в этой цепи являются чувствительные нейроны языкоглоточного, тройничного и блуждающего нервов при действии веществ на орган зрения,… Возможны два способа действия химических веществ на нервные окончания: - прямое (ингибирование арсинами SH-групп структурных белков и ферментов; действие капсаицина на ионные каналы…Основные проявления раздражающего действия
При воздействии на человека аэрозоля CS с размером частиц в среднем 1 мкм в течение 60 сек и концентрации 0,01 - 0,04 г/м3 развивается поражение… При действии раздражающих веществ в очень высоких концентрациях возможно… При тяжелых поражениях адамситом явления раздражения слизистых сопровождаются мучительными ощущениями. Поражаются…Экспериментальное выявление раздражающего действия ксенобиотиков
Недостатками метода являются: необходимость испытывать вещества в объемах и концентрациях, значительно превосходящих реально действующие; высокая… Попытки модифицировать метод, сопряжены с использованием в качестве…ГЛАВА 7.2. ДЕРМАТОТОКСИЧНОСТЬ
Дерматотоксичность - это свойство химических веществ, действуя на организм немеханическим путем, вызывать повреждение кожных покровов.Воздействие ксенобиотиков осуществляется двумя способами: путем прямого контакта кожных покровов с парообразными, жидкими, твердыми веществами (формальдегид, фенолы, амины, кислоты, щелочи, кантаридин, этиленоксид, металлы и т.д.) и резорбтивного действия, вследствие проникновения веществ во внутренние среды организма с развитием системных эффектов (полигалогенированные диоксины, дибензофураны, никель, бериллий и т.д.). Кожа - самый объемный орган тела человека, составляющий около 15% от массы тела и с площадью поверхности около 2 м2 (у взрослого). С учетом большой поверхности и ранимости кожи не удивительно, что она очень часто страдает при действии токсикантов. Кожа состоит из двух основных слоев: дермы и эпидермиса. Толщина эпидермиса на разных участках тела не одинакова, но в среднем - около 100 - 200 мкм. Большая часть эпидермиса формируется из сквамозных, активных в метаболическом отношении, клеток, синтезирующих структурные протеины, которые составляют основу наружного, рогового, слоя эпидермиса. Роговой слой формирует барьер на пути токсикантов, действующих из окружающей среды. Элементы рогового слоя, обладая высокой липофильностью, не позволяют проникнуть в организм водо-растворимым соединениям. Буферная активность молочной кислоты, амфотерных аминов, слабых оснований, находящихся в ороговевших клетках, обеспечивают известную защиту от кислот и оснований. Базальный слой эпидермиса, представленный постоянно делящимися клетками с высокой митотической активностью, является ростковым слоем. Остальная часть ощутимой на ощупь толщины кожи образована волокнистой соединительной тканью дермального слоя (основные белки: коллаген, эластин, ретикулан) и межуточным веществом.
Токсический процесс может носить характер острого и хронического воспаления, функциональных нарушений кожи и её придатков (волосяных фоликулов, потовых и сальных желез), неопластических изменений. Токсический процесс, развивающийся в результате местного действия токсикантов, и сопровождающийся воспалительной реакцией, называется химическим дерматитом. Патологические процессы в коже, формирующиеся вследствие резорбтивного действия токсикантов называются токсидермиями.
Химические дерматиты
Контактные химические дерматиты
С точки зрения профессиональной патологии наибольшего внимания заслуживают контактные дерматиты, развивающиеся в результате прямого цитотоксического… Цитотоксический эффект возможен лишь при взаимодействии токсикантов с… В отличие от раздражающего, прижигающее действие характеризуется альтерацией покровных тканей, формирующейся…Аллергические дерматиты
Тот факт, что сенсибилизация развивается лишь у отдельных людей, свидетельствует об их генетической предрасположенности к подобной патологии (см.…Фотодерматиты
Рисунок 2. Структура некоторых фотосенсибилизирующих агентовТоксидермии
К облигатным токсикантам относятся, в частности, полигалогенированные полициклические углеводороды (ППУ) следующих химических групп (рисунок 3): 1) хлорнафталены; 2) полихлорированные бифенилы;Краткая характеристика некоторых токсикантов
Поражение органическими растворителями
Органические растворители, будучи липофильными соединениями, легко проникают в кожу и всасываются в кровь. Они обладают раздражающим действием на… На клеточном уровне органические растворители действуют как сосудистые яды,… При попадании растворителей на кожу их следует удалить путем обмывания пораженного участка водой с мылом. С целью…Поражения мышьякорганическими соединениями
При действии люизита на кожу уже в течение 30 минут на месте аппликации появляется эритема. Через 12 часов формируются мелкие пузырьки, которые,… С целью оказания помощи с пораженного участка кожи удаляют токсическое…Поражение сернистым ипритом
Иприт является алкилирующим агентом, т.е. это вещество способно образовывать ковалентные связи с нуклеофильными, реакционно-способными группами… При контакте иприта с кожей человека до 80% испаряется, 20% пенитрирует, из… Поражения развиваются в две стадии. Острая стадия включает разрушение фибробластов, эндотелия поверхностных капилляров…Поражение альдегидами
Действие альдегидов на кожу сопровождается явлениями раздражения, эритемой. Повторные контакты с веществами вызывают сенсибилизацию тканей.… Акролеин и глютаровый альдегид - сильно раздражают слизистые оболочки глаз и…Поражение эпоксидными смолами
Основной формой патологии, вызываемой смолами, являются контактные аллергические дерматиты. Более 90% лиц, имеющих контактную аллергию на клеи,…Поражение щелочами
Помимо кожи, щелочи могут вызывать поражение глаз, дыхательных путей, ЖКТ. Травма глаз может оказаться очень сильной, включая разрушение… Некоторые коммерческие сорта цемента представляют собой комбинацию силиката… Оказание помощи начинается на догоспитальном этапе. Необходимо снять загрязненную одежду и обувь, а пораженную кожу…Поражение кислотами
Поражение хромовой кислотой
Относительно кратковременный контакт с кожей быстро приводит к её поражению и абсорбции вещества во внутренние среды организма. Если поражение… Оказание помощи начинается немедленно. Пораженный участок необходимо тщательно…Поражение плавиковой кислотой.
Пораженные плавиковой кислотой участки кожи имеют белесоватый цвет. Область - болезненна. Постепенно развивается отек, а затем и некроз тканей. Если… Пострадавшие жалуются на сильную боль в области ожога. Не смотря на… Оказание помощи при поражении плавиковой кислотой помимо общих мероприятий (см. выше) включает немедленную обработку…Оценка дерматотоксичности ксенобиотиков в эксперименте
В эксперименте эффекты оцениваются путем аппликации ксенобиотика на поверхность кожи. Выделяют четыре категории исследований, направленных на… - непосредственного раздражающего (прижигающего) действия; - сенситизирующего действия;ГЛАВА 7.3. ПУЛЬМОНОТОКСИЧНОСТЬ
Пульмонотоксичность - это свойство химических веществ, действуя на организм немеханическим путем вызывать структурно-функциональные нарушения со стороны органов дыхания.
Обладая огромной площадью поверхности, лёгкие находятся в состоянии постоянного воздействия ксенобиотиков, содержащихся во вдыхаемом воздухе. В подавляющем большинстве случаев, когда концентрации веществ малы, такие воздействия никак не проявляют себя. Если же уровень воздействия достаточно высок, формируется токсический процесс, тяжесть которого колеблется в широких пределах от незначительных явлений раздражения (транзиторная токсическая реакция) до тяжелейших расстройств со стороны многих органов и систем (интоксикация). Пульмонотоксичность может проявляться как при местном, так и при резорбтивном действии токсикантов. Более того, не все вещества, действующие ингаляционно, обладают пульмонотоксичностью. Для многих токсикантов легкие лишь входные ворота, которые они проходят, не вызывая повреждений (монооксид углерода, мыщьяковистый водород, стибин, ТЭС и т.д.). Вместе с тем к некоторым соединениям, проникающим в организм и другими путями (например, через желудочно-кишечный тракт) ткань легких чрезвычайно чувствительна. Вещества, порог чувствительности к которым органов дыхания существенно ниже, чем других органов и систем, и клиника поражения которыми характеризуется нарушениями со стороны, прежде всего, органов дыхания, условно можно отнести к группе пульмонотоксикантов.
Как следует из определения, не все вещества, вызывающие нарушения со стороны дыхательной системы обладают пульмонотоксичностью. Так, ксенобиотики, вмешивающиеся в механизмы центральной регуляции дыхания (наркотические аналгетики, неэлектролиты, барбитураты и др.), отравление которыми сопровождаются выраженными функциональными нарушениями со стороны дыхательной системы, к числу пульмонотоксикантов в строгом смысле слова не относятся.
По большей части пульмонотоксичность проявляется при ингаляционном способе воздействия ксенобиотиков в форме газов, паров и аэрозолей. Перечень веществ, действующих на организм ингаляционно, очень велик и включает загрязнители атмосферного воздуха и воздуха рабочей зоны, гербициды, пестициды, сильнодействующие и ядовитые вещества (СДЯВ - при нештатных ситуациях на производствах), отравляющие вещества (ОВ - в ходе военных конфликтов) и т.д.
Некоторые вещества вызывают поражение уже вследствие однократного воздействия, другие провоцируют патологию только при длительной экспозиции или повторных воздействиях.
Каким бы образом не формировался токсический процесс, клинические эффекты группируются вокруг достаточно ограниченного числа типических патологических состояний. К их числу относятся: явления обратимого раздражения верхнего и нижнего отделов дыхательных путей; стойкое поражение дыхательных путей; повреждение терминальных респираторных единиц легких (ацинусов) в форме воспалительных, пролиферативных процессов и нарушения проницаемости альвеолярно-капиллярного барьера; новообразования. Некоторые токсиканты способны вызывать множественные нарушения со стороны дыхательной системы. Так, асбест вызывает не только фиброз легочной ткани, но и рак легких. Сигаретный дым вызывает самый широкий спектр патологических состояний от хронического бронхита до эмфиземы и рака легких.
Краткая характеристика морфологии дыхательной системы
Назофарингиальный отдел
Трахеобронхиальный отдел
Дыхательные пути подразделяются на три основные категории: бронхи, содержащие хрящ, респираторные бронхиолы, участвующие в газообмене, альвеолярные… Респираторные бронхиолы представляют собой короткие трубочки диаметром около…Паренхима легких
Газообмен, в основном, осуществляется в альвеолах. Барьер на пути диффундирующих газов образуют мембраны, состоящие из слоя альвеолярного эпителия,… Интерстициальное вещество обычно представлено несколькими эластическими и… При патологических процессах с вовлечением любого компонента терминальной респираторной единицы - эпителия, эндотелия,…Физиология дыхательной системы
С точки зрения токсиколога интерес представляют три аспекта физиологии дыхательной системы. Это вентиляция, газообмен, метаболизм ксенобиотиков и биологически активных веществ.
Вентиляция
Патологические процессы, развивающиеся в лёгких в ходе токсического процесса, могут вызвать три типа изменений процесса вентиляции: - структурно-механические. Состояния, сопряженные со снижением способности… - повреждающие дыхательные пути. Повреждение дыхательных путей в форме острой (химический ожег, интоксикация ипритом,…Легочные объемы
Рисунок 1. Жизненные ёмкости и объемы легких При развитии токсических процессов развиваются патологические состояния, сопровождающиеся изменением легочных объёмов…Рефлексы, влияющие на дыхание
Рефлексы глубоких дыхательных путей. Раздражение нервных окончаний глубоких дыхательных путей инициирует кашель. Наличие этого рефлекса при… Бронхоальвеолярные рефлексы. В 1868 году Герингом и Брейером описан рефлекс,… Краткая характеристика рефлексов, лежащих в основе реакций внешнего дыхания, на возможные токсические воздействия…Механизмы регуляции тонуса бронхов
Ингаляция пыли, а у сенсибилизированных людей, целого ряда других веществ (см. ниже) может приводить к выраженному бронхоспазму. Причина явления -… Таблица 2. Механизмы регуляции тонуса бронхов Эффект …Газообмен
Рисунок 2. Процесс газообмена между воздухом и кровьюМетаболизм ксенобиотиков и биологически активных веществ
При анализе токсичности необходимо учитывать способность лёгких к селективному захвату ряда веществ (прежде всего органических аминов). Так, активно…Депонирование и клиаренс ксенобиотиков в легких
Рисунок 3. Схема движения ксенобиотика (депонирование и клиаренс) в организме… Сайт депонирования ингалируемых газов определяется степенью их растворимости в тонком слое жидкости, выстилающей…Основные формы патологии дыхательной системы химической этиологии
Острые отравления веществами, действующими непосредственно или опосредованно на органы дыхания, сопровождаются рядом респираторных синдромов, среди… Последствиями подострых воздействий, а также результатом длительного контакта…Острые ингаляционные поражения
Немедленные реакции организма на действие токсикантов изучены достаточно хорошо. Прежде всего, это кашель, секреция слизи, бронхоспазм, умеренный… Афферентные нервы в дыхательных путях, участвующие в кашлевом рефлексе,… Стимуляция выделения слизи подслизистыми железами дыхательных путей и бокаловидными клетками - еще одна защитная…Локализация поражения
Верхние дыхательные пути
Таблица 4. Перечень наиболее известных токсикантов, вызывающих раздражение и воспалительные процессы в дыхательных путях Ацетон …Глубокие дыхательные пути
Большинство случаев трахеобронхитов химической этиологии разрешаются практически без последствий (в случае поражения раздражающими ОВ в течение… Необходимо учитывать, что проявления острого трахеобронхита могут развиваться… Мероприятия по оказанию помощи включают использование средств защиты органов дыхания, немедленный (по возможности)…Паренхима легких
Пневмонии
Таблица 5. Вещества, вызывающие острую химическую пневмонию Акролеин Аммиак Бензин Бериллий Диоксид серы Кадмий Хлористый… Токсиканты повреждают паренхиму лёгких, захватывая как альвеолярную стенку… Лечение пневмоний химической этиологии осуществляется по общим правилам лечения этого недуга. К числу специфических…Отек легких
Выделяют три типа отёка лёгких: - гемодинамический отек лёгких, в основе которого лежит повышение давления… - собственно токсический отек лёгких, развивающийся в результате первичного поражения альвеолярно-капиллярной…Острая дыхательная недостаточность
В целом, основными причинами дыхательной недостаточности легочного типа при отравлениях являются: - альвеолярная гиповентиляция вследствие угнетения дыхательного центра,… - нарушение свойств альвеолярно-капиллярной мембраны (отёк легких, фиброз);Диагностика
Поскольку транзиторные токсические реакции быстро исчезают, а стойкие признаки острого ингаляционного поражения формируются постепенно, диагностика… Определенную помощь в диагностике может оказать обычная спирометрия или… Во всех случаях интоксикаций при пожарах следует определять содержание карбоксигемоглобина в крови. Как правило,…Оказание помощи
Система оказания помощи при развивающемся токсическом отеке легких включает следующие мероприятия: 1. Снижение потребления кислорода (покой, тепло, назначение успокаивающих и… 2. Борьба с гипоксией (вынужденное положение тела, ингаляция противовспенивающих средств, кислородотерапия);Краткая характеристика некоторых пульмонотоксикантов
Хлор
Хлор - газ желтовато-зеленого цвета с характерным удушливым запахом, примерно в 2,5 раза тяжелее воздуха, хорошо растворяющийся в воде. Является сильным окислителем. Он сохраняется и транспортируется в сжиженном виде под повышенным давлением. В случае аварий возможно массовое поражение людей.
Уже в минимальных концентрациях (10 мл/м3) хлор раздражает дыхательные пути, действуя в более высоких концентрациях, вызывает тяжелое поражение. По данным А.А. Лихачева (1931) при регистрации гибели экспериментальных животных (собак) в течение трех суток LCT50 составляет около 70 г мин/м3 (при 15 - 30 минутной экспозиции).
Хлор был первым веществом, примененным на войне в качестве ОВ. 22 апреля 1915 г близ Ипра германские части выпустили его из баллонов (около 70 т), направив поток газа, движимый ветром, на позиции французских войск. Позже вещество широко применялось на фронтах 1-й Мировой войны и потому клиника поражения хорошо изучена.
В редких случаях смерть может наступить уже при первых вдохах зараженного воздуха. Причина смерти - рефлекторная остановка дыхания и сердечной деятельности. Другой причиной быстрой гибели пострадавших (в течение 20 - 30 минут после вдыхания вещества) является ожег легких. В этих случаях окраска кожных покровов пострадавшего имеет зеленоватый оттенок. При вскрытии обнаруживаются сухие на ощупь, спавшиеся легкие, зеленовато-серого цвета. Левое сердце пусто, правое расширено и наполнено густой кровью.
Чаще в случаях тяжелого отравления в момент воздействия пострадавший ощущает резкое жжение в области глаз и верхних дыхательных путей, стеснение дыхания. Отравленный стремится облегчить дыхание, разрывая ворот одежды. Одновременно отмечается крайняя слабость, вследствие этого отравленные падают и лишаются возможности бежать из пораженной зоны. Практически с начала воздействия появляется надрывный, мучительный кашель, позже присоединяется одышка, причем в дыхании участвуют добавочные дыхательные мышцы. Пораженный старается занять положение, облегчающее дыхание. Речь невозможна. Иногда наблюдается рвота.
Через некоторое время после выхода из зоны поражения может наступить некоторое облегчение состояния (скрытый период), однако чаще (в отличие от поражения фосгеном) полная ремиссия не наступает: сохраняется кашель, болезненные ощущения по ходу трахеи и в области диафрагмы.
Через некоторое время (от нескольких часов до суток) состояние вновь ухудшается, усиливаются кашель и одышка (до 40 дыхательных актов в минуту), лицо приобретает синюшную, а в крайне тяжелых случаях пепельную, окраску. Над легкими прослушиваются хрипы. Пострадавший постоянно отхаркивает пенистую желтоватую или красноватую жидкость (более 1 л за сутки). Наблюдаются сильнейшие головные боли, температура тела понижается. Пульс замедлен. Артериальное давление падает. Пострадавший теряет сознание и погибает при явлениях острой дыхательной недостаточности. Если отек легких не приводит к гибели, то через несколько часов (до 48) состояние начинает улучшаться, отечная жидкость рассасывается. Однако заболевание постепенно переходит в следующий период - осложнений, во время которого обычно развиваются явления бронхопневмонии.
Как правило, отравленные, не погибшие в первые 24 часа после воздействия, выживают. Явления бронхита и пневмонии могут наблюдаться в течение нескольких недель, а легочная эмфизема оказывается стойким последствием интоксикации. Часто в качестве осложнения регистрируются длительные нарушения со стороны деятельности сердца.
В подавляющем большинстве случаев поражений легкой и средней степени тяжести через известное время наблюдается полное восстановление здоровья.
Паракват
Паракват - кристаллическое вещество белого цвета, без запаха. Хорошо растворяется в воде и спиртах; температура кипения 300о С (при этом препарат… При воздействии коммерческих растворов вещества возможны местные обратимые… Таблица 9. Токсичность параквата для грызунов (ЛД50 , мг/кг) Путь введения Крысы Мыши …Цинк
Цинк представляет собой голубовато-белый металл, находящийся в группе II периодической таблицы элементов. При нагревании выше 5000 цинк окисляется и испаряется в форме мельчайших частиц оксида цинка, которые в холодном воздухе подвергаются флокуляции с образованием дыма.
С древнейших времен человек использовал сплав цинка с медью и оловом (бронза), но вероятно не был знаком с чистым металлом вплоть до 15 века.
Мировая продукция металла в настоящее время составляет более 7 млн. тонн в год. Цинк и его соединения широко используется в хозяйственной деятельности.
Цинк является эссенциальным элементом организма. Высокое содержание его отмечается в предстательной железе, мышцах, поджелудочной железе, костях, почках.
Токсичность металла и его соединений мала. Наибольшую опасность представляют ингаляционные поражения дымами, содержащими соединения цинка, и аэрозолем оксида цинка. Так, после вдыхания ZnO в концентрации около 600 мг/м3 в течение 45 минут у кошек сразу после извлечения из камеры отмечаются нарушение координации движений, тремор, затруднение дыхания, понижение температуры тела.
Вследствие своих раздражающих свойств, хлорид цинка вызывает воспалительное повреждение кожи и поражения глаз. Ингаляция пыли, содержащей соли цинка, сопровождается раздражением слизистой оболочки верхних дыхательных путей.
Ингаляция паров и дыма, содержащего металлический цинк в высоких концентрациях приводит к формированию респираторного дистресс-синдрома, который может развиться спустя несколько суток после ингаляции, а в малых концентрациях - состояния, называемого "лихорадка литейщиков". Проявления синдрома включает: металлический вкус во рту, сухой кашель, учащение дыхания, утомляемость, миалгии, лихорадку, озноб, развивающиеся спустя 4 - 12 часов после воздействия. Температура может подниматься до 400. Количество лейкоцитов достигает 20000. Продолжительность приступа 1 - 3 часа. Со стороны ЦНС наблюдаются неспецифические эффекты типа ощущения усталости, вялости. Полная нормализация состояния - в течение 24-48 часов. Осложнения не наблюдаются. Достаточно быстро (в течение суток от начала контакта) формируется толерантность к действию металла, однако столь же быстро (1-2 дня) она исчезает. В этой связи характерно приступообразное течение этого вида профессиональной патологии. Наблюдаемая картина проявляется особенно ярко в начале трудовой недели, после перерыва в действии вещества в выходные дни. Отсюда еще один термин, обозначающий процесс - "утренняя лихорадка понедельника".
При ингаляционном поражении соединениями цинка необходимы мероприятия, направленные на профилактику токсического отека легких. При развившемся респираторном дистресс-синдроме взрослых - оказание помощи по общим правилам.
Хронические патологические процессы химической этиологии
Таблица 10. Перечень токсикантов, вызывающих патологические состояния дыхательной системы при длительном воздействии Диффузный…Аллергические и гиперреактивные заболевания легких
- вызывающие неспецифические вялотекущие воспалительные процессы в лёгких; - обладающие антигенными свойствами, в том числе, способные образовывать… Итогом таких воздействий являются:Оценка пульмонотоксичности ксенобиотиков в эксперименте
В настоящее время опыты, как правило, выполняют на белых крысах, кроликах, беспородных собаках (преимущественно самцах), хотя для этой цели подходит… Условия аппликации веществ следует выбирать исходя из их свойств, целей и… Действие жидких веществ изучают либо в паровой фазе (летучие агенты), либо в форме аэрозолей с различной степенью…Выявления пульмонотоксического действия профессиональных и экотоксикантов
Таблица 11. Выявление профессиональных и экологических причин лёгочной патологии химической этиологии Профессиональный анамнез: -…Профессиональный анамнез
Важно собрать сведения о возможном воздействии токсикантов, не связанных с профессиональной деятельностью: путем длительного приёма лекарств,…Биологический мониторинг
Примеры профессиональной патологии лёгких химической этиологии, выявляемой физиологическими методами исследования, представлены в таблице 12. Таблица 12. Патологические состояния, сопровождающиеся нарушением…Обследование рабочего места
В большинстве случаев рабочие не знают всего перечня химических веществ, с которыми им приходится контактировать в процессе работы, и,… В случае необходимости выполняются замеры концентраций интересующих веществ в… Итогом обследования является не только уточнение диагноза, но и рекомендации по улучшению условий труда.ГЛАВА 7.4. ГЕМАТОТОКСИЧНОСТЬ
Гематотоксичность это свойство химических веществ, действуя на организм немеханическим путём, избирательно нарушать функции клеток крови или её клеточный состав (как в сторону уменьшения, так и увеличения числа форменных элементов). Важнейшими функциями клеток крови являются: кислородтранспортная, гемостатическая, обеспечение иммунитета. Нарушение числа форменных элементов может явиться следствием прямого разрушения клеток в кровяном русле, повреждения процессов клеточного деления и созревания в кроветворных органах, поступления зрелых элементов в кровь.
Частыми проявлениями гематотоксичности являются: нарушение свойств гемоглобина (метгемоглобинемия, карбоксигемоглобинемия), анемии (в том числе гемолитические), тромбоцитопении, лейкопении, лейкемии. По большей части клеточные дискразии, вызванные токсикантами, обратимы и исчезают после прекращения действия вещества. Однако встречаются и персистирующие формы, заканчивающиеся летальным исходом в случае тяжелого повреждения костного мозга.
Гемопоез
Нарушение функций гемоглобина
- в форме соединения - гемоглобином; - в форме раствора - плазмой. В растворенном состоянии плазмой крови переносится около 0,2 мл О2 на 100 мл крови. В связанной с гемоглобином форме…Метгемоглобинообразование
Поддержание метгемоглобина на уровне менее 1% обеспечивается двумя физиологическими механизмами. Первый связан с восстановлением или связыванием ксенобиотиков-окислителей до… Второй механизм обеспечивает восстановление образовавшегося в крови метгемоглобина до гемоглобина при участии двух…Причины метгемоглобинообразования
Таблица 1. Перечень основных метгемоглобинобразователей аллоксон альфа нафтиламин аминофенол (и его производные) аммония нитрат … Скорость образования метгемоглобина у различных экспериментальных животных при… Таблица 2. Способность некоторых ароматических аминов вызывать метгемоглобинэмию у разных экспериментальных животных …Врожденная метгемоглобинемия
Наиболее частой причиной врождённых метгемоглобинемий является дефицит НАДН - метгемоглобинредуктазы. Лица с дефектом этого энзима справляются с… Уровень метгемоглобина в крови у пациентов с гомозиготной недостаточностью… Врождённый дефицит НАДфН - редуктазы встречается редко. Поскольку энзим имеет небольшое функциональное значение, в…Краткая характеристика некоторых токсикантов
Анилин
Анилин - вязкая, бесцветная жидкость, темнеющая на свету и воздухе. Применяется в производстве лекарственных веществ, антиоксидантов, фотоматериалов, красителей и др.
Действуя ингаляционно, через кожу и желудочно-кишечный тракт анилин может вызывать тяжелую патологию. По мимо метгемоглобинемии развивается гемолитическая анемия с образованием телец Гейнца.
Механизм действия анилина до конца не установлен. Известно, что in vitro, при инкубации с суспензией эритроцитов, вещество не вызывает метгемоглобинообразования. Вместе с тем, метаболиты анилина: фенилгидроксиламин, 2-аминофенол, 4-аминофенол - вызывают образование метгемоглобина in vitro. Полагают, что с учетом скорости накопления каждого из упомянутых метаболитов в организме и их индивидуальной активности, относительное значение фенилгидроксиламина, 2-аминофенола и 4-аминофенола в образовании метгемоглобина при отравлении анилином может быть оценено соответственно, как 100:4:1 (рисунок 3).

Рисунок 3. Схема метаболизма анилина
Поскольку анемия развивается спустя несколько суток после острой интоксикации анилином, по завершения лечебных мероприятий по поводу метгемоглобинемии, отравленные анилином должны находиться под наблюдением врача в течение относительно длительного времени.
Дапсон (4,4-диаминодифенилсульфон)
Рисунок 4. Структура дапсона Препарат используют для лечения лепры, герпетиформных дерматитов, профилактики малярии (комбинированный препарат…Нитриты
Приём нитроглицерина может приводить к образованию метгемоглобина. Обычная доза препарата (4,8 мг. под язык) не вызывает клинически значимого… Встречаются токсикомании, обусловленные пристрастием к ингаляции амилнитрита,… Определённую опасность представляют также нитраты - производные азотной кислоты (азотнокислый натрий - NaNO3),…Проявления метгемоглобинемии
Необходимо отличать периферический и центральный цианоз. Периферический цианоз является следствием нарушения гемодинамики и… Центральный цианоз развивается при повышенном содержании в крови сульфогемоглобина (более 0,5г на децилитр),…Лабораторная диагностика
Результаты анализа газового состава крови следует оценивать с большой осторожностью. Часто данные о сатурации крови кислородом получаются на основе… С помощью спектрофотометрических исследований можно отличить (как указывалось)…Принципы оказания помощи
Антидотом метгемоглобинообразователей является метиленовый синий (тетраметилтионин хлорид). Препарат назначают лицам с уровнем метгемоглобинемии… Рисунок 5. Восстановление метгемоглобина при участии метиленового синего и метгемоглобинредуктазыОбразование карбоксигемоглобина
СО представляет собой бесцветный газ, лишенный запаха. Основным источником его являются процессы неполного сгорания топлива (древесины, угля, газа,… Сродство монооксида углерода к гемоглобину в 200 - 300 раз выше, чем у…Изменение числа форменных элементов
Токсическое действие некоторых веществ может сопровождаться существенным нарушением клеточного состава крови. Наиболее значимыми проявлениями интоксикаций являются: анемии (гемолитическая, апластическая), лейкопении, тромбоцитопении, лейкемии.
Гемолитические анемии
Среди анемий химической этиологии, гемолитические - встречаются наиболее часто. Вещества, вызывающие внутрисосудистый гемолиз можно разделить на три группы (таблица 4):
1. Разрушающие эритроциты (при определённой дозе) у всех отравленных;
2. Гемолизирующие форменные элементы у лиц с врождённой недостаточностью Г-6Ф-ДГ;
3. Вызывающие иммунные гемолитические анемии.
Таблица 4. Вещества, вызывающие гемолиз
Общие гемолитики
| анилин сурма арсин (мышьяковистый водород) бромат калия бензол хлорат калия (натрия) хлористый метил хлороформ медь динитробензол фенол гидрохинон лецитин мезантоин | нафтален нитриты нитраты свинец сульфоны толуол трибромметанол тринитробензол тринитротолуол нитробензол цинкэтиленбисдитиокарбамат Яды пауков Яды змей (кобра) |
Токсиканты, вызывающие гемолиз у лиц с дефицитом Г-6Ф-ДГ
| ацетанилид ацетилсалициловая кислота аскорбиновая кислота гидразин метиленовый синий хлорамфеникол дифенилсульфон фенилгидразин фуразолидин | Н-ацетилсульфамид нафтален нитрофурантион примахин сульфаметоксипиридазин сульфаниламиды сульфапиридин тиозосульфон |
Токсиканты, вызывающие иммуноаллергические гемолитические анемии
В основе иммунологических анемий лежат два механизма. Первый связан с фиксацией токсиканта на мембране эритроцита с образованием комплексного… Гемолитики разрушают эритроциты и гемоглобин выходит в плазму крови.… - существенным повышением коллоидно-осмотических свойств крови (содержание белка в плазме возрастает с 7 до 20%);Краткая характеристика некоторых токсикантов
Арсин - бесцветный газ, без запаха. Используется в химическом синтезе, а также выделяется при зарядке аккумуляторных батарей. Острое воздействие… В опытах на мышах показано, что воздействие арсином в течение 1 часа в… Снижение осмотической стойкости эритроцитов отмечается лишь при действии арсина в высоких концентрациях (15ppm -…Тринитротолуол
Отравления тринитротолуолом встречаются на производствах взрывчатых веществ и при воздействии пороховых газов. Основные пути поступления в организм: ингаляционный и через кожу. Проявления гематотоксического действия вещества: анемия смешанного типа (апластическая с элементами гемолитической), метгемоглобинообразование. Одновременно отмечаются дерматит, гастрит, токсический гепатит.
Биомониторинг
Для выявления действия стибина можно использовать выявление сурьмы в крови и моче. Нормальным содержанием элемента в цельной крови является 3 мкг/…Аплазия костного мозга
Сокращение числа форменных элементов крови может быть результатом действия огромного числа токсикантов, как лекарственных веществ, так и… В зависимости от воспроизводимости наблюдаемого эффекта вещества делятся на… Таблица 5. Химические агенты, нарушающие клеточный состав крови А. Алкилирующие агенты: -сернистый иприт …Основные проявления интоксикаций
Панцитопения.
Агранулоцитоз
Тромбоцитопения
Тромбоцитопения, связанная с действием токсикантов, проявляется кровотечениями различной степени тяжести. Признаки геморрагии: петехии, пурпура, геморрагические пузыри на слизистой полости рта, желудочно-кишечные кровотечения. При аллергических процессах количество тромбоцитов в тяжелых случаях падает до 1000 и менее в мм3 крови, при этом число мегакариоцитов в костном мозге снижается несущественно. Геморрагическому синдрому сопутствует анемизация организма.
Лейкемии
В США ежегодно регистрируется около 24000 новых случаев лейкемий, что составляет примерно 3% от общего количества новообразований. Острая миелоидная… Вторичная острая миелоидная лейкемия - достаточно хорошо установленный… Попытки установить причинно-следственные связи между фактом действия токсиканта и возникновением лейкемий связаны с…Диагноз
При проведении исследований необходимо иметь в виду существенные различия в частоте миелодисплазий у представителей различных возрастных групп. Так,…Профессиональные воздействия и лейкемии
Увеличение числа лейкемий, преимущественно ОМЛ, отмечается среди рабочих металлургической промышленности, других сфер деятельности, при которых…Характеристика наиболее известных токсикантов, вызывающих патологию крови
До настоящего времени бензол остаётся основным этиологическим фактором, вызывающим патологию крови. Однако в последнее время большое внимание уделяется и другим токсикантам, среди которых: свинец, мышьяк, радий, этиленоксид, некоторые пестициды (хлордан, гептахлор, 2,4-Д; 2,4,5-Т) этиленгликоль, 1,3-бутадиен.
Бензол
Помимо химического синтеза, бензол широко используется в качестве растворителя особенно в производстве клеев, в кожевенной промышленности, при производстве резины и резиновых изделий, в нефтеперерабатывающей промышленности, производстве химикалиев, пестицидов и пластмасс. Интоксикация веществом возможна, кроме того, на складах горюче-смазочных материалов, в фармацевтической промышленности. После установления токсического действия бензола на костный мозг его по возможности стали заменять на менее токсичные ксилол и толуол. Установление гигиенических нормативов и контроля за их соблюдением существенно сократили последствия токсического действия вещества, тем не менее полностью устранить неблагоприятное действие токсиканта на здоровье людей при контакте с бензолом пока не удаётся. Особенно велик риск поражения при транспортировке бензола, замене и чистке химических реакторов, клапанов, трубопроводов и т.д.
Основной путь поступления бензола в организм человека на производстве - ингаляционный. Кожа обычно не является значимыми входными воротами для токсиканта, хотя длительное воздействие на кожу чистого вещества и его аэрозоля могут привести к интоксикации.
Поступившее во внутренние среды организма вещество быстро выводится из организма практически в неизменённом виде через лёгкие и в форме конъюгатов с мочой. Хотя молекула бензола проста, метаболизм его достаточно сложен. В настоящее время доказано, что угнетение костного мозга обусловлено действием метаболитов токсиканта. Начальные этапы метаболических превращений проходят в основном в печени при участии цитохром-Р450-зависимых оксидаз. Продуктом этих превращений является фенол. Превращение фенола под влиянием все тех же цитохром-Р450-зависимых оксидаз приводит к образованию полифенольных метаболитов, в основном гидрохинонов, а также, под влиянием пероксидаз, - бифенолов, гидрохинона, р-бензохинона. Долгое время полагали, что муконовый альдегид и муконовая кислота (НООССН=СНСН=СНСООН), в небольшом количестве выделяющиеся с мочой отравленных, играют ключевую роль в механизме токсического действия бензола. В настоящее время вопрос о механизме действия бензола полагают целесообразным считать открытым.
Ключевым ферментом, обеспечивающим токсическое действие бензола на костный мозг, вероятно следует считать миелопероксидазу, активность которой чрезвычайно высока в гранулоцитарных элементах костного мозга. Энзим катализирует превращение одного из метаболитов бензола - гидрохинона в высокоактивный 1,4-бензохинон. В процессе метаболизма активируются свободно-радикальные процессы в клетках.
В эксперименте показано, что одновременное с бензолом введение индометацина (антиоксидант и противовоспалительное средство) существенно ослабляет миелотоксическое действие вещества. Это указывает на значение простагландинсинтетазы (циклооксигеназы) для развития индуцируемого бензолом миелотоксического эффекта. Однако показано, что индометацин угнетает активность и миелопероксидазы (блокируется окисление гидрохинона).
Эффекты, связанные с хроническим действием бензола, практически полностью ограничиваются нарушениями со стороны гемопоэза и иммунной системы. Способность бензола угнетать кроветворение была обнаружена в начале 20 века. Это свойство вещества первоначально даже пытались использовать для лечения лейкемий, но безуспешно.
Признаками хронической интоксикации бензолом являются: анемия, тромбоцитопения, лимфоцитопения, панцитопения, сопровождающиеся слабостью, петехиальной сыпью, пурпурой, частыми инфекционными заболеваниями. Наиболее частое проявление - лейкопения, сопровождающаяся тромбоцитопенией. Часто, на фоне уменьшения числа форменных элементов в крови, выявляется гиперплазия костного мозга с признаками задержки созревания клеточных элементов эритроидного и миелоидного ряда. При обследовании рабочих типографий, контактировавших с бензолом в относительно высоких концентрациях, выявлены существенные нарушения со стороны системы крови (Greenberg, 1939; Goldwater et al, 1941). В крови обнаруживается относительная и абсолютная лимфопения, предшествующая анемии и тромбоцитопении. Гранулоциты, по-видимому оказываются более резистентными к действию токсиканта: гранулоцитопения, как самостоятельное проявление интоксикации, развивается редко.
По современным наблюдениям нарушения со стороны крови развиваются при хроническом действии бензола в концентрациях более 100ррм.
Бензол действует на клетки костного мозга, находящиеся в фазе G2 митоза. Эти представления находятся в соответствии с данными о высокой чувствительности цитоскелета (микротрубочки) к метаболитам бензола (гидрохинон, п-бензохинон), которые взаимодействуют с ГТФ-зависимыми структурами, вступая в ковалентную связь с сульфгидрильными группами белков. Эффекты метаболитов бензола не ограничиваются действием на клетки, находящиеся в фазе митоза. В сублетальных дозах возможно действие хинольных метаболитов на вхождение клеток в период клеточного деления.
Повторное введение бензола сопровождается уменьшением числа клеточных элементов в костном мозге. Эффект достигает максимума на 3 - 10 сутки и характеризуется исчезновением пула дифференцирующихся клеток средней степени зрелости. Характерной особенностью действия бензола является наличие рефрактерного периода, проявляющегося в том, что не смотря на продолжение его введения к 10 - 15 суткам отмечается нормализация клеточного состава костного мозга.
Путем введения метаболитов не удаётся воспроизвести клинику отравления бензолом. Так, введение даже больших доз фенола сопровождается лишь кратковременным угнетением кроветворения. Тем не менее, совместное введение фенола с гидрохиноном приводит к значимой супрессии клеточного деления в костном мозге. Вероятно, для воспроизведения полной картины интоксикации необходимо действие всего комплекса продуктов биотрансформации токсиканта.
Свинец
В прежние века свинец был доминирующей причиной хронических интоксикаций человека. Имеются данные, что конец Римской империи во многом связан с хронической интоксикацией населения свинцом, широко применявшимся для изготовления водопроводов и посуды. Изменившийся характер использования вещества в современном обществе, изменил и роль патологии, вызываемой токсикантом. В последние годы частота острых и хронических отравлений свинцом, сопровождающихся развитием выраженной патологии, существенно уменьшилась. И тем не менее полностью опасность поражения свинцом не исчезла. Особую проблему представляют красители на основе соединений свинца, свинецорганические соединения, такие как тетраэтил- и тетраметилсвинец, широко используемые в качестве добавок к горючим.
Одним из характерных проявлений хронической интоксикации свинцом является нарушения со стороны крови. Как в эксперименте, так и в клинике показано, что действие свинца на кровь ограничивается нарушениями со стороны эритроидного ростка. Характерный признак хронической интоксикации свинцом - анемия различной степени тяжести. В основе патологии лежат два основных механизма, это (1) угнетение эритропоэза в следствие нарушения процесса синтеза гема, опосредованное подавления активности дегидрогеназы 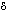 -аминолевулиновой кислоты и (2) повреждение мембраны эритроцитов. Второй механизм может быть количественно оценён только с помощью прецизионных методов исследования, он проявляется снижением стойкости эритроцитов. При исследовании костного мозга лиц, отравленных свинцом, отмечается выраженное угнетение созревания клеток эритроидного ряда, что сопровождается значительным увеличением числа эритробластов. В полихроматофильных эритробластах нередко выявляется базофильная исчерченность - достаточно надёжный признак интоксикации, хотя и не столь специфичный, как представлялось некоторое время тому назад.
-аминолевулиновой кислоты и (2) повреждение мембраны эритроцитов. Второй механизм может быть количественно оценён только с помощью прецизионных методов исследования, он проявляется снижением стойкости эритроцитов. При исследовании костного мозга лиц, отравленных свинцом, отмечается выраженное угнетение созревания клеток эритроидного ряда, что сопровождается значительным увеличением числа эритробластов. В полихроматофильных эритробластах нередко выявляется базофильная исчерченность - достаточно надёжный признак интоксикации, хотя и не столь специфичный, как представлялось некоторое время тому назад.
В условиях производства, связанного с воздействием свинца, у работающих порой отмечается незначительная анемия гипохромного характера с умеренным ретикулоцитозом. На ранних этапах развития интоксикации анемизации может предшествовать повышение содержания порфирина в клетках костного мозга и эритроцитах. Появление порфирина в моче, как правило, поздний признак интоксикации. В сомнительных случаях надёжными диагностическими признаками хронической интоксикации являются появление в моче 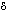 -аминолевулиновой кислоты и повышенный уровень свинца в плазме крови. В литературе отсутствуют данные о способности свинца вызывать лейкемии.
-аминолевулиновой кислоты и повышенный уровень свинца в плазме крови. В литературе отсутствуют данные о способности свинца вызывать лейкемии.
Мышьяк
Острые отравления мышьяком редко случаются в условиях производства. Основной путь поступления токсикантов, содержащих мышьяк, - с зараженной водой и пищей. Одним из признаков острой интоксикации, хотя и не основным, является нарушение созревания миелобластов, проявляющееся лейкопенией.
Скорость элиминации мышьяка из организма относительно высока. Период полувыведения составляет 1 - 3 суток. Основной путь выведения - через почки. В этой связи важным диагностическим признаком интоксикации в первые сутки является обнаружение элемента в плазме крови и моче.
Имеются сообщения, что хроническое действие мышьяка может приводить к развитию лейкемий, болезни Ходжкина.
Этиленоксид
Эфиры гликолей
Производные феноксиуксусной кислоты
В последние годы проведено немало исследований направленных на установление неблагоприятного действия гербицидов. В некоторых работах показана…Мониторинг состояния системы крови лиц, работающих в условиях опасных производств
В качестве дополнительных методов обследования часто рекомендуют проводить: - оценку количества хромосомных аберраций в клетка периферической крови (в… - изучение распределения эритроцитов по их размерам, чувствительный тест, позволяющий выявить макро- и микроцитоз…ГЛАВА 7.5. НЕЙРОТОКСИЧНОСТЬ
Нейротоксичность - это свойство химических веществ, действуя на организм немеханическим путем, вызывать нарушение структуры и/или функций нервной системы. В основе развивающегося токсического процесса может лежать повреждение любого структурного элемента нервной системы путем модификации пластического, энергетического обменов, нарушения генерации, проведения нервного импульса по возбудимым мембранам, передачи сигнала в синапсах. Нейротоксичность может быть проявлением прямого, и опосредованного повреждением других органов и систем, действия токсикантов на нервную систему. Нейротоксичность присуща большинству известных веществ. Поэтому практически любая острая интоксикация в той или иной степени сопровождается нарушениями функций нервной системы. Вещества, для которых порог чувствительности собственно нервной системы (отдельных её гистологических и анатомических образований) существенно ниже, чем других органов и систем, и в основе интоксикации которыми лежат нарушения моторных, сенсорных функции нервной системы, памяти, мышления, эмоций, поведения, условно относят к нейротоксикантам, даже если не известны механизмы их токсического действия. Например, интоксикация свинцом у детей приводит к замедлению умственного развития, ухудшает способности к обучению. Механизм этого феномена неизвестен, но принято считать, что нейротоксичность - свойство свинца. Изучение особенностей действия отдельных нейротоксикантов позволяет понять механизмы феномена нейротоксичности в целом.
Структурно-функциональная организация нервной системы
Нервная система представлена двумя отделами - центральным (центральная нервная система - ЦНС) и периферическим (периферическая нервная система -… Таблица 1. Основные образования центрального и периферического отделов нервной… Клеточное строение ЦНС, её функции чрезвычайно сложны и многообразны. Клетки, составляющие нервную систему и…Нейроны
Аксон у нервной клетки только один. Это отросток, предназначенный для проведения нервного импульса от тела нервной клетки к другим клеткам. Диаметр… Тела, дендриты и аксоны нервных клеток окружены клеточной мембраной, толщина… Таблица 2. Распределение ионов внутри и вне возбудимых клеток (Katz, 1971). (мМ/л) ионы мышечная…Синапсы
Глиальные клетки
Олигодандроциты в ЦНС и Шванновские клетки (леммоциты) ПНС окружают аксоны нейронов и образуют миелин. Миелинизирующие клетки, наряду с нейронами,… Микроглия это фагоцитарная система ЦНС. Значение этих элементов глии для…Цереброспинальная жидкость.
Гематоэнцефалический барьер.
ЦНС защищена от действия многих токсикантов гематоэнцефалическим барьером. Аналогичный барьер окружает периферический отдел нервной системы (гематоневральный барьер). Также как и в ЦНС здесь имеются анатомические структуры с повышенной проницаемостью барьера для токсикантов. К числу таких структур относятся корешки дорзальных ганглиев спинного мозга и вегетативные (автономные) ганглии.
Энергетический обмен
Окисление глюкозы - единственный источник энергии в нервной ткани. Резервы глюкозы и кислорода в мозге ничтожно малы. Поэтому обеспечение ими…Мозговой кровоток
Кровоснабжение мозга - саморегулирующаяся система. Это означает, что в интервале давления церебральной гемоперфузии 6,65 - 20,0 кРа (50 - 150 мм…Внутричерепное давление
Внутричерепное давление определяется объёмом цереброспинальной жидкости, протекающей через мозг крови и объёмом самого мозга. В нормальных условиях увеличение одного из указанных объёмов компенсируется уменьшением других.
Причины уязвимости нервной системы для токсикантов
- многие химические вещества легко проникают через ГЭБ, а также действуют на нервные образования, не защищенные ГЭБ; - длинные нервные отростки (аксоны и дендриты) значительно увеличивают площадь… - для нормального течения физиологических процессов в ЦНС необходимо поддержание электрохимического баланса в…Характеристика нейротоксикантов и нейротоксических процессов.
Нейротоксиканты
Важнейшим условием прямого действия нейротоксиканта на ЦНС является его способность проникать через гематоэнцефалический барьер. Вещества, не… Отдельные токсичные соединения, не способные преодолевать ГЭБ, тем не менее… Некоторые широко используемые промышленные агенты и экополлютанты, обладающие высокой нейротоксичностью, представлены…Нейротоксические процессы
Механизмы действия нейротоксикантов
Классификация наиболее известных в настоящее время высокоспецифичных нейротоксикантов, часто используемых в эксперименте для изучения явления… Таблица 6. Классификация "избирательных" нейротоксикантов в… Как видно из таблицы, в основе токсичности большинства известных нейротоксикантов лежит способность действовать на…Проявления нейротоксических процессов
Последствия действия химических веществ на нервную систему представлены в таблице 7. Таблица 7. Некоторые проявления нейротоксического действия ксенобиотиков … В зависимости от условий действия, строения токсиканта, его нейротоксического потенциала развивающиеся процессы…Острые нейротоксические процессы
Судорожный синдром. Конвульсанты
Механизмы, посредством которых токсиканты вызывают судороги, могут быть классифицированы на несколько логических категорий, исходя из представлений,… Таблица 10. Возможные общие механизмы генерации судорожного синдрома … Тормозные процессы в ЦНС осуществляются с помощью пресинаптических и постсинаптических механизмов. В обоих механизмах…Конвульсанты, активирующие возбуждающие процессы в ЦНС
Рисунок 1. Структура некоторых конвульсантов Пентилентетразол (ПТЗ) является представителем группы тетразолиевых конвудьсантов, непосредственно действующих на…Вещества, действующие на возбудимые мембраны и нарушающие механизмы ионного транспорта
В серии производных тетразола от триметилентетразола до гептаметилентетразола, судорожная активность возрастает с увеличением числа метиленовых… Таблица 12. Дозы производных тетразола, вызывающие судорожный синдром у мышей…Вещества, активирующие холинэргические структуры мозга
Процесс передачи сигнала в холинэргических синапсах может быть представлен несколькими этапами: - синтез медиатора из холина и ацетата при участии энзима холин-ацетил… - выделение ацетилхолина в синаптическую щель (спонтанно и при поступлении в нервное окончание возбуждающего…Вещества, активирующие глютаматэргические структуры мозга
Основными глютаматергическими нейрональными трактами ЦНС являются: кортико-стриатный, энторинал-гипокампальный; первичные слуховые волокна… Деполяризация постсинаптической мембраны, развивающаяся после действия… Токсические проявления системного действия глютамата в больших дозах у млекопитающих - это судороги (крысы, кошки) и…Конвульсанты, блокирующие тормозные процессы в ЦНС
- нарушающие проведение импульса в ГАМК-ергических синапсах; - нарушающие проведение нервного импульса в глицинергичесих синапсах.…Конвульсанты, действующие на ГАМК-ергический синапс.
ГАМК обнаружена во всех структурах ЦНС. Концентрация аминокислоты в разных областях мозга колеблется в пределах от 2 до 10 мкМ/г ткани. Наивысшее её… В нервных окончаниях ГАМК обнаруживается главным образом в цитоплазме в… ГАМК образуется из глютамата под влиянием пиридоксальфосфат-зависимого энзима глютаматдекарбоксилазы (ДГК) (рисунок…Конвульсанты, действующие на глицинергические синапсы
Прерывание нервного импульса в глицинергических синапсах осуществляется путем высокоафинного обратного захвата медиатора пресинаптическими нервными… Антагонисты глицина в действии на глицинергический синапс обладают свойствами… СтрихнинВещества, нарушающие процессы биоэнергетики в мозге
Важной, с практической и теоретической точек зрения, группой веществ, вызывающих судороги, путем нарушения энергетики мозга, являются… Фторорганические соединения Синтез фторорганических соединений стал в середине ХХ века необходимым элементом крупномасштабного производства…Седативно-гипнотическй эффект. Наркотики
- агонисты тормозных нейромедиаторных систем мозга (в основном ГАМК-ергической); - вещества с неспецифическим, так называемым "неэлектролитным" (по… К первой группе относятся седативные, снотворные средства, препараты для внутривенной анестезии, широко используемые в…Неэлектролиты
Группы веществ, обладающих наркотической активностью и их отдельные представители, приведены в таблице 13. Таблица 13. Химическая классификация веществ, обладающих наркотической… Отравление "неэлектролитами" любого строения сопровождается быстрым развитием практически одинаковых…Психодислептический синдром. Психодислептики
Используемые в качестве медикаментов средства обычно подразделяют на следующие группы: - нейролептики; - антидепрессанты;Эйфориогены
В процессе развития транзиторной токсической реакции выделяют два периода действия. В первом, коротком, наблюдается эйфория, возбуждение, усиление… Повторный прием приводит к развитию толерантности (в том числе к этанолу) и…Галлюциногены
Большинство галлюциногенов - вещества животного и растительного происхождения, используемые человеком с древних времён для самоотравления с… Классическим представителем группы является диэтиламид лизергиновой кислоты. … Диэтиламид лизергиновой кислоты (ДЛК)Делириогены
Наряду с веществами, представленными на таблице 17, к числу делириогенов могут быть отнесены лекарственные препараты из группы нейролептиков… - спутанность сознания; - нарушение оценки своего состояния;Нарушение нервной регуляции периферических органов и систем
Существуют вещества, в основе действия которых на организм лежит способность "избирательно" нарушать периферические механизмы нервной…Нарушение механизмов синаптической передачи
Яды змей Яды змей, относящихся к семейству Elapidae (тигровая змея, тайпан, морские… Таблица 22. Свойства основных нейротоксинов ядов змей Токсин Молекулярная масса Масса…Блокаторы ионных каналов
Сакситоксин В 1957 году Schantz et al. удалось выделить и изучить свойства так называемого… Сине-зелёные водоросли пресноводных водоемов также синтезируют сакситоксин. Имели место случаи отравления скота водой,…Хронические нейротоксические процессы. Токсические нейропатии
Таблица 23. Характеристика хронических нейротоксических процессов Тип Поражаемая структура Патологическая реакция … Частыми формами хронического процесса являются токсические нейропатии. Однако… В основе хронических процессов, как правило, лежат нарушения пластического обмена в нервной системе, сопровождающиеся…Токсическая сегментарная миелинопатия
Ключевыми характеристиками сегментарной миелинопатии являются: преимущественное поражение отростков миелинобразующих клеток и малая чувствительность… При интоксикациях некоторыми веществами (ацетилэтил-тетраметил-тетралин -…Токсическая дистальная аксонопатия
Перечень некоторых веществ, способных вызывать токсические аксонопатии у человека представлены на таблице 25. Таблица 25. Вещества, вызывающие токсические аксонопатии у человека … В большинстве случаев проявления отравлений мало специфичны и характеризуются знаками симметричной сенсомоторной…Перикариальная токсическая нейронопатия
Метилртуть Благодаря высокой растворимости в липидах, метилртуть легко проникает через… Первые упоминания о массовых отравления метилртутью относятся к 1914 году, когда препарат стали использовать в…Оценка нейротоксичности в эксперименте
Поведенческие исследования предполагают наблюдение за животными, подвергающимися острому, подострому, хроническому действию веществ, с целью… Если такие признаки выявляются и есть необходимость определить эффективные… Возможность химических веществ вызывать отсроченные нейропатии желательно оценивать в опытах на курах, у которых этот…Диагностическая стратегия в нейротоксикологии
Сбор анамнестических данных
Таблица 27. Перечень вопросов, рассматриваемых при сборе данных профессионального анамнеза 1. Где работает пациент и как давно? 2. Какой… В тех случаях, когда сбор анамнеза не позволяет прийти к определенному… Если не удаётся выявить действующий агент на производстве, необходимо ознакомиться с бытовыми условиями, привычками,…Исследование специалистами
Более того, один и тот же токсикант, как указывалось, может вызвать различные формы поражения нервной системы, и вместе с тем разные токсиканты…Функциональные исследования
Электоромиографические исследования позволяют оценить выраженность денервации мышечных волокон, развивающейся вследствие гибели нервных волокон,… Методами оценки степени тяжести токсических энцефалопатий являются…ГЛАВА 7.6. ГЕПАТОТОКСИЧНОСТЬ
Гепатотоксичность - это свойство химических веществ, действуя на организм немеханическим путем, вызывать структурно-функциональные нарушения печени.
Таблица 1. Вещества, обладающие гепатотоксичностью 1. Производственные токсиканты - Алифатические углеводолроды: гептан;Анатомо-физиологияческие особенности печени
Функциональной единицей печени является ацинус. Область вокруг портальной триады (печеночная артерия, воротная вена, желчный ход) называется… 1 зона - основная функциональная область печени. В крови, притекающей к… Метаболизм ксенобиотиков в гепатоцитах рассмотрен ранее (см. выше).Патологические состояния, формирующиеся при действии гепатотоксикантов
Стеатоз
- нарушение синтеза белка в клетках печени; - нарушение процессов конъюгации триглицеридов с белками и образования… - повреждение механизмов транспорта липопротеинов через клеточные мембраны;Некроз
Некроз - это дегенеративный процесс, приводящий к клеточной гибели. Некротические изменения, развивающиеся под действием токсикантов, могут затрагивать лишь отдельные участки печени (фокальный некроз) либо всю массу органа (тотальный некроз). Гибель клеток сопровождается повреждением плазматических мембран; ей предшествует ряд морфологических изменений гепатоцитов: отек цитоплазмы, дилятация цитоплазматического ретикулума, набухание митохондрий с разрывом крист, деградация полисом, разрушение органел и ядра клетки, стеатоз.
Биохимические изменения, предшествующие гибели клетки включают: инициацию свободно-радикальных процессов, связывание токсикантов или их метаболитов с белками, нуклеиновыми кислотами и ненасыщенными жирными кислотами мембран клеток, нарушение пластических и биоэнергетических процессов, резкое повышение содержания в клетке свободного кальция.
Полагают, что фатальным, необратимым этапом развития гепатоцеллюлярного некроза является нарушение гомеостаза внутриклеточного Са+2. Повышение концентрации кальция в цитоплазме клетки вторично приводит к повреждению клеточных мембран и органел (митохондрий, эндоплазматического ретикулума, лизосом), денатурации структурных протеинов, инактивации энзимов. Интимный механизм, приводящий к нарушению клеточного метаболизма Са+2 до конца неясен (см. раздел "Механизмы цитотоксичности").
Гибель клеток может являться следствием реализации регулируемых биологических механизмов (контролируемая клеточная смерть - апоптоз) - физиологического "противовеса" процессу непрерывного клеточного деления. Хотя апоптоз - нормальный процесс, он может быть существенно усилен при действии ряда экзогенных факторов, таких как, оксидативный стресс, аноксия, ионизирующее излучение, токсиканты.
Имеются морфологические критерии (световая и электронная микроскопия), позволяющие отличить некроз от апоптоза. Однако в действии токсикантов, как правило, практически не возможно четко определить какой из процессов, некроз или активированный апоптоз лежит в основе гибели клетки. По большей части, при интоксикациях, прослеживаются признаки обоих процессов.
Угнетение апоптоза может приводить к накоплению в органе постоянно размножающихся клеток. Например, клональная экспансия малигнизировавшихся клеток и последующий рост опухоли, могут быть следствием угнетения апоптоза.
Наиболее изученными токсикантами, вызывающими стеатоз и некроз гепатоцитов, являются четырёххлористый углерод, хлороформ, бромбензол, фосфор, афлатоксины, диметилнитрозамин, пуромицин, алкалоиды пирролизидинового ряда, бериллий.
Холестаз
Среди веществ, вызывающих холестаз - известные лекарстывенные препараты: тиоридазин, амитриптилин, диазепам, эстрадиол, сулфаниламиды, а также…Фиброз (цирроз)
Канцерогенез
Таблица 2. Гепатоканцерогены А. Гепатоканцерогены человека доказано предполагаемые … Б. Гепатоканцерогены животных ВЕЩЕСТВО ВИД ЖИВОТНОГО 1. Азокрасителт и их предшественники: …Морфологические формы токсического повреждения печени
Таблица 3. Морфологические типы заболеваний печени, вызываемых химическими веществами ТИП ПРИМЕР Фокальный некроз …Краткая характеристика гепатотоксикантов
Облигатные гепатотоксиканты вызывают дозо-зависимый эффект, как правило, воспроизводимый в опытах на экспериментальных животных. Идиосинкратические… В основе прямого цитотоксического действия веществ обеих групп на печень лежат… - повреждение механизмов транспорта веществ через мембраны гепатоцитов и клеточных органелл;Облигатные гепатотоксиканты
Некоторые токсиканты в процессе метаболизма инициируют в гепатоцитах генерацию свободных радикалов, активных форм кислорода. Эти продукты вызывают… В условиях эксперимента показано, что сероуглерод вызывает жировое… Большинство гепатотоксикантов вызывают повреждение печени путём прямого взаимодействия со структурами клеток. В основе…Идиосинкратические гепатотоксиканты
Аллергические гепатопатии развиваются спустя несколько (1 - 5) недель после воздействия и при повторном контакте с веществом. Как правило, им… Необходимо отметить, что далеко не всегда, аллергическая гепатопатия… Идиосинкратические поражения печени могут встречаться у лиц, работающих на химических и фармацевтических…Условия воздействия гепатотоксикантов.
Целый ряд широко используемых инсектицидов из группы хлорированных ароматических углеводородов в высоких дозах вызывают поражение печени. Патология… Наиболее частыми причинами острых гепатопатий в производственных условиях… В ходе обследования типографских рабочих, имевших длительный контакт с толуолом, у большой группы лиц выявлена…Факторы, влияющие на гепатотоксичность
Хронический приём алкоголя повышает токсичность четырёххлористого углерода, трихлорэтилена, метиленхлорида, винилхлоида, ксилола, стирола,… Наряду с химическими, гепатотоксичность модифицируется и другими факторами. К… 1. Состояние питания: кальций, медь, железо, цинк, магний, - необходимы для реализации функций ОСФ. Их дефицит…Краткая токсикологическая характеристика отдельных гепатотоксикантов
Токсины бледной поганки
Рисунок 1. Строение -аманитина Аматоксины являются ингибиторами ядерной РНК-полимеразы В. Угнетая активность фермента, токсины нарушают синтез белка…Дихлорэтан
Отравление может наступить при поступлении ДХЭ через дыхательные пути, желудочно-кишечный тракт и кожные покровы. Картина тяжелой интоксикации… Попав во внутренние среды организма, ДХЭ достаточно быстро исчезает из крови,… Продолжительность скрытого периода при ингаляционных поражениях составляет 1 - 12 часов. При приеме вещества внутрь…Изучение гепатотоксичности ксенобиотиков
При этом необходимо иметь в виду, что патогенез острого и хронического поражений печени одним и тем же токсикантом может быть различным. Поэтому… Совершенствование методов выявления гепатотоксичности также осуществляется в…Определение активности энзимов в плазме крови.
ТГГК - специфичный для печени энзим и чувствительный индикатор её состояния. Повышение активности ТГГК также отмечается при отравлении самыми… Уровень ЛДГ, хотя и отражает состояние печени, однако не является… При подострых и хронических интоксикациях активность энзимов может повышаться лишь транзиторно. Кроме того, постепенно…Функциональные пробы
Оценка метаболической активности печени
С помощью неинвазивных методов исследования информация о состоянии метаболической активности печени может быть получена при постановке… Возможны и другие методы оценки состояния метаболизирующих свойств печени.… Определение уровня желчных кислот в плазме крови не требует при оценке экскреторных функций введения экзогенных…Оценка синтетической активности печени
В печени осуществляется синтез многих, циркулирующих в крови веществ. Их содержание является косвенным показателем синтетической активности органа. Наиболее часто определяют альбумины, протромбин, холестерол, транспортные белковые молекулы, например, трансферин. Следует отметить, что печень имеет огромный резерв синтетических функций и вследствие этого лишь при очень существенном дефиците массы паренхимы органа следует ожидать изменение показателей.
Структурные исследования
Функциональные исследования высоко специфичны, но, как правило, мало чувствительны при выявлении патологии печени на ранних стадиях её развития. Методы изучения морфологии органа лишены этих недостатков. Однако следует учитывать, что результаты морфологических исследований также не всегда легко интерпретировать, поскольку в органе, в ответ на действие различных этиологических факторов, развивается относительно небольшое количество типических патологических изменений.
Принципы выявление токсических гепатопатий у человека
С помощью используемых проб порой бывает сложно отличить поражения печени с асимптотическим течением от нормы. В целом ряде случаев, выявляемые…Острые гепатопатии химической этиологии.
Основой диагностики гепатопатий химической этиологии является тщательно собранный анамнез. В ходе беседы уясняются особенности профессиональной… Диффузная паренхиматозная дегенерация органа с минимальным некрозом… Холестатические поражения печени клинически манифестируются желтухой, кожным зудом. В крови определяется умеренное…Подострые и хронические токсические гепатотопатии
Выявление нарушений функций печени, развивающихся вследствие длительного действия токсикантов, особенно в начальном периоде развития патологического процесса, является сложной задачей. Особенно трудно выявлять, индуцированные токсикантами новообразования печени. Эти задачи могут быть успешно решены лишь в специализированных учреждениях с использованием современных методов диагностики.
Выявление гепатотоксичности в популяции лиц, контактирующих с опасными химическими агентами.
Однако, как уже указывалось, попытка применения существующих методов исследования состояния печени для массового обследования людей сталкивается с… Мировая практика формулирует ряд требований к проведению рассматриваемых… 1. Перед проведением анализа необходимо по возможности строго очертить понятие нормы для обследуемой популяции. Размер…Заключение
Поражение печени по-прежнему одно из наиболее частых последствий перенесённых острых, подострых и хронических интоксикаций. Высокая чувствительность органа к токсикантам обусловлена его анатомо-физиологическими особенностями. Печень - основной орган, где происходит метаболизм чужеродных соединений. Результат метаболизма - образование веществ, легко выделяющихся из организма. Однако в ходе биопревращений часто образуются реактивные промежуточные продукты, которые и повреждают ткань печени.
В зависимости от строения токсиканта, дозы, кратности введения, длительности воздействия формы поражения различны. Действуя в высокой дозе, ксенобиотик может вызвать острое цитотоксическое поражение печени. Интермитирующее, подострое, хроническое действие токсиканта сопровождается формированием вяло текущего процесса, приводящего нередко к фиброзу, рубцовым изменениям в органе, новообразованиям.
Выявление острых форм гепатотоксического действия возможно с помощью широко используемых методов исследования. В большинстве случаев они оказываются достаточно информативными. Важная задача, стоящая перед токсикологией - разработка чувствительных, специфичных тестов, позволяющих выявлять начальные и вяло текущие, не манифестирующиеся формы токсических гепатопатий. Только широкое внедрение в практику таких методов и их корректное использование может обеспечить профилактику заболеваний, обусловленную профессиональным контактом с токсикантамти.
ГЛАВА 7.7. НЕФРОТОКСИЧНОСТЬ
Нефротоксичность - это свойство химических веществ, действуя на организм немеханическим путем вызывать структурно-функциональные нарушения почек. Нефротоксичность может проявляться, как вследствие прямого взаимодействия химических веществ (или их метаболитов) с паренхимой почек, так и опосредованного действия, главным образом через изменения гемодинамики, кислотно-основного равновесия внутренней среды, массивное образование в организме продуктов токсического разрушения клеточных элементов, подлежащих выведению через почки (гемолиз, рабдомиолиз).
В строгом смысле нефротоксикантамимогут быть названы лишь те, непосредственно действующие на почки вещества, к которым порог чувствительности органа существенно ниже, чем у других органов и систем. Однако на практике часто нефротоксикантами называют любое вещество, обладающее нефротоксичностью.
В таблице 1 представлен перечень токсикантов с относительно высокой прямой нефротоксической активностью. Перечень известных веществ, оказывающих опосредованное токсическое действие на почки значительно шире и включает более 300 наименований.
Таблица 1. Вещества, вызывающие острые и хронические формы повреждения почек
| Металлы | Технические жидкости | Разные |
| Мышьяк Висмут Кадмий Медь Золото Свинец Литий Ртуть Платина Серебро Талий Хром | Четырёххлористый углерод Дихлорэтан Трихлорэтилен Хлороформ Толуол Стирол Метанол Этиленгликоль Диэтиленгликоль Эпихлоргидрин Эфиры этиленгликоля Гексахлор-1,3-бутадиен Дихлорацетилен Сероуглерод Диоксан | Паракват Микотоксины (в том числе токсины бледной поганки) Силикон Кантаридин Рицин Пенициллин Производные ацетилсалициловой кислоты Цефалоридин Пуромицин Аминонуклеозид |
Вследствие лекарственной терапии, случайных или преднамеренных интоксикаций, работы или проживания в условиях зараженной среды значительная часть населения постоянно подвергается воздействию потенциальных нефротоксикантов. Количественно определить вклад каждой из указанных причин в общее число регистрируемых хронических и острых нефропатий в настоящее время не представляется возможным.
По некоторым данным в мире более 10 миллионов человек имеют постоянный контакт с веществами, обладающими выраженной нефротоксичностью. Частота регистрируемых случаев острой почечной недостаточности около 2 на 1000. По мнению некоторых исследователей примерно 20% - следствие химических воздействий, главным образом, лекарственных средств. Лекарства являются и основной, среди прочих химических факторов, причиной хронических нефропатий. По некоторым данным только злоупотребление ненаркотическими аналгетиками лежит в основе трети случаев хронической почечной недостаточности. При этом следует отметить, что в половине выявляемых случаев заболеваний органа, причины патологии остаются не выясненными. Не исключено, что патология почек возникает вследствие хронических воздействий экополютантов, производственных вредностей (тяжелых металлов, органических растворителей и др.) значительно чаще, чем принято считать. Отдельные наблюдения подтверждают это предположение. Так, среди лиц, постоянно подвергающихся воздействию тяжелых металлов (свинца, кадмия) частота смертей от почечной недостаточности достоверно выше среднестатистической.
Анатомо-физиологические особенности органа
Парный орган, весящий всего около 300 граммов (менее 1% от массы тела человека), получает около 25% минутного объёма сердечного выброса крови.… Капиллярный клубочек, окруженный капсулой Боумена, это сложно организованный… В области сосудистого полюса почечного клубочка в месте впадения в него приносящей артериолы располагается…Характеристика нефротоксического действия
Механизмы действия
По мнению некоторых авторов (Наумова В.И., Папаян А.В., 1991) причины острой почечной недостаточности могут быть отнесены к одной из следующих… - преренальные; - ренальные;Биохимические механизмы
В зависимости от физико-химических свойств веществ, происходит их взаимодействие с молекулами-рецепторами (мембранные структуры, энзимы, структурные… Для многих органических соединений, этапу их нефротоксического действия…Иммунологические механизмы
Точный механизм, с помощью которого токсикант инициирует реакцию гипериммунной реакции, приводящей к поражению почек в большинстве случаев… Повреждение почечной ткани происходит путём реализации определённой цепи…Гемодинамические механизмы
При остром поражении токсикантом почечных канальцев функции органа могут нарушаться вследствие закупорки просвета канальцев продуктами распада… В тех случаях, когда объём гломерулярной фильтрации снижается более чем на…Проявления токсического действия
- появление крови в моче (гематурия) вследствие повреждения стенки капилляров клубочков; - появление белка в моче более 0,5 г в суточной пробе (протеинурия).… - уменьшение количества отделяемой мочи - менее 600 мл в сутки (олигурия);Краткая характеристика отдельных нефротоксикантов
Металлы
Свинец
В недалёком прошлом свинец являлся частой причиной острых и хронических нефропатий. В литературе описаны многочисленные случаи некроза канальцевого эпителия вследствие случайного или преднамеренного приёма больших доз солей свинца. Случаи хронической почечной недостаточности регистрировались у лиц, принимавших алкоголь, хранившийся в сосудах, содержавших свинец, у рабочих, постоянно контактирующих со свинец-содержащими веществами, у взрослых, в детстве перенесших острую интоксикацию свинцовыми красителями и т.д. В настоящее время случаи поражения свинцом регистрируются значительно реже.
Хроническая свинцовая нефропатия проявляется прогрессивным тубулоинтерстициальным нефритом, который характеризуется отсутствием протеинурии и альбуминурии на начальном этапе формирования патологии и обнаруживающим себя при исследовании скорости гломерулярной фильтрации. Накопление свинца в ткани почек, особенно в клетках эпителия проксимального отдела канальцев, сопровождается на ранних стадиях заболевания повреждением митохондрий клеток и нарушением абсорбционных функций клеток. Позже в ядрах этих клеток появляются включения, образованные комплексами свинца с кислыми протеинами. Эти внутриядерные тельца, как правило, исчезают по мере прогрессирования патологии. Патологии почек при свинцовой интоксикации часто сопутствуют гипохромная анемия, гипертензия, нейропатии.
С помощью хелатирующих агентов (ЭДТА или димеркаптосукцината) удаётся мобилизовать кумулируемый в тканях свинец и ускорить тем самым его выведение из организма. Содержание свинца в моче пациента более 800 мкг в суточной пробе после внутривенного введения ЭДТА в дозе 0,5 грамм указывает на высокое содержание металла в тканях организма.
Кадмий
Хроническая интоксикация кадмием нередко сопровождается развитием прогрессирующего тубулоинтерстициального нефрита.
Поражения людей, как правило, является следствием потребления контаминированной пищи или, в производственных условиях, ингаляции пыли, содержащей кадмий. Эпидемиологические исследования среди лиц, профессионально контактирующих с кадмием, позволили выявить высокую частоту почечной патологии. Описаны случаи хронической интоксикации людей, проживающих в регионах с высоким содержанием элемента в воде и почве. Так, в Японии, среди женщин, употребляющих в пищу рис, произрастающий на почвах с высоким содержанием кадмия, отмечается заболевание (Итаи-итаи), которое проявляется анемией, разрушением костной ткани, нарушением функций почек (поражение эпителия проксимальных канальцев). Заболевание начинается с выделения с мочой специфических низкомолекулярных белков, таких как 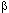 2-микроглобулины или ретинол-связывающий протеин, а также кадмия, главным образом, в виде комплекса с белком металлотионенином. Связывание кадмия металлотионеином по-видимому позволяет защитить некоторые органы от поражения. В тоже время именно в форме такого комплекса вещество захватывается почками и депонируется в органе (период полувыведения кадмия из организма человека составляет 10 - 20 лет).
2-микроглобулины или ретинол-связывающий протеин, а также кадмия, главным образом, в виде комплекса с белком металлотионенином. Связывание кадмия металлотионеином по-видимому позволяет защитить некоторые органы от поражения. В тоже время именно в форме такого комплекса вещество захватывается почками и депонируется в органе (период полувыведения кадмия из организма человека составляет 10 - 20 лет).
У лиц с начальными формами поражения почек концентрация кадмия в моче обычно составляет более 10 мкг на 1 г выделяющегося с мочой креатинина.
При острых интоксикациях кадмием достаточно эффективным средством выведения вещества из организма является ЭДТА-Са,Na. При хронической интоксикации мобилизовать элемент с помощью имеющихся в распоряжении врача комплексообразователей пока не удаётся.
Механизм токсического действия металла окончательно не установлен. По-видимому, он заключается во взаимодействии металла с карбокси-, амино-, SH-руппами белковых молекул, нарушении функций структурных белков и энзимов. Показано также, что, Сd во многом следует метаболическим путям Zn+2 и Сa+2. Например, захватывается клетками с помощью механизмов, предназначенных для захвата Zn. Полагают, что на молекулярном уровне механизм токсического действия Сd также может быть обусловлен его способностью замещать Zn и другие двухвалентные ионы в биологических системах. Дефицит цинка модифицирует характер распределения Сd и существенно потенцирует его токсичность.
Ртуть
Острая интоксикация некоторыми неорганическими и органическими соединениями ртути сопровождается развитием некроза эпителия проксимального отдела почечных канальцев и почечной недостаточности. Хорошо известно, что приём ртутных мочегонных в малых дозах сопровождается связыванием Hg2+ с ферментами клеточных мембран, содержащими сульфгидрильные группы в молекуле и участвующими в реабсорбции натрия, угнетая их активность. Введение препаратов в неоправданно высоких дозах может привести к острому гломерулонефриту с характерной протеинурией и нефротическим синдромом.
Действуя в умеренных дозах, пары и соли ртути могут вызвать различные субклинические формы нарушения функций почек, сопровождающиеся протеинурией, экскрецией с мочой некоторых низкомолекулярных энзимов. У лиц с тяжёлой профессиональной интоксикацией ртутью, как правило, регистрируется хронический гломерулонефрит.
Содержание в моче ртути более 50 мкг на 1 г креатинина, как правило, свидетельствует о поражении почек.
Для ускорения выведения вещества из организма используют различные хелатирующие агенты. Наиболее часто применяют димеркапрол, Д-пенициламин, димеркаптосукцинат.
Мышьяк
Некроз канальцевого эпителия почек - частое осложнения острого отравления соединениями трехвалентного и пятивалентного мышьяка. Для ускорения выведения мышьяка из организма с успехом применяют хелатирующие агенты из группы дитиолов (2,3-димеркаптопропанол, унитиол и т.д.).
Отравления арсином (AsH3) приводит к вторичному поражению почек гемоглобином, выделяющимся в плазму крови, вследствие массивного гемолиза. Острая почечная недостаточность, развивающаяся при этом, является основной причиной гибели отравленных. Применение комплексообразователей при интоксикации этим веществом нецелесообразно.
Технические жидкости
Нередко поражение почек развиваются у токсикоманов, ингалирующих, с целью получения удовольствия, клеи, красители, содержащие в качестве… Субхронические и хронические интоксикации углеводородами (бензины) могут стать… В зависимости от типа растворителя в патологический процесс помимо почек часто вовлекаются и другие органы, главным…Этиленгликоль
Вещество быстро всасывается в желудочно-кишечном тракте. Наибольшее количество накапливается в печени и почках, где ксенобиотик подвергается… Действуя целой молекулой этиленгликоль проявляет свойства типичного… Признаки поражения почек, как правило, развиваются на 2 - 3 сутки интоксикации (вслед за периодом мозговых явлений). В…Оценка нефротоксичности ксенобиотиков
В ходе скрининга ксенобиотиков с успехом используют такие тесты, как определение плотности мочи, содержание в ней сахара, крови (с помощью… Важно иметь в виду, что ни один из этих тестов не позволяет однозначно судить… К числу наиболее простых и часто выполняемых исследований, позволяющих более определенно судить о механизме…Выявление токсических поражений почек у человека
В ходе плановых обследований лиц, контактирующих с потенциальными нефротоксикантами, для целей диагностики рекомендуют использовать относительно… У отравленного необходимо: изучить химический состав мочи; провести её… В настоящее время, в силу распространённости элементарных гигиенических мероприятий, защищающих человека от массивных…РАЗДЕЛ 8. ЭКОТОКСИКОЛОГИЯ
ОСНОВЫ ЭКОТОКСИКОЛОГИИ
Еще несколько десятков лет назад химические отходы производства просто сбрасывали в окружающую среду, а пестициды и удобрения практически… Однако уже в 1962 году появляется книга Рашель Карсон УМолчаливая веснаФ, в… В самостоятельную науку экотоксикологию (ecotoxicology) выделил Рене Траут, который впервые, в 1969 году, связал…Ксенобиотический профиль среды
Для экотоксикологии интерес представляют лишь молекулы, обладающие биодоступностью, т.е. способные взаимодействовать немеханическим путем с живыми… Часть биодоступных соединений утилизируется организмами, участвуя в процессах… Совокупность чужеродных веществ, содержащихся в окружающей среде (воде, почве, воздухе и живых организмах) в форме…Экотоксикокинетика
2.1. Формирование ксенобиотического профиля. Источники поступления поллютантов в среду К числу природных источников биодоступных ксенобиотиков, по данным ВОЗ (1992),… Важнейшим элементом экотоксикологической характеристики поллютантов является идентификация их источников. Решить эту…Персистирование
Таблица 2. Период полуразрушения некоторых ксенобиотиков в окружающей среде Поллютант Период полуразрушения Среда … Постоянный выброс в окружающую среду персистирующих поллютантов приводит к их… К числу веществ, длительно персистирующих в окружающей среде, относятся тяжелые металлы (свинец, медь, цинк, никель,…Трансформация
Подавляющее большинство веществ подвергаются в окружающей среде различным превращениям. Характер и скорость этих превращений определяют их стойкость.
Абиотическая трансформация
Фотолиз. Свет, особенно ультрафиолетовые лучи, способен разрушать химические связи и, тем самым, вызывать деградацию химических веществ. Фотолиз… Гидролиз.Вода, особенно при нагревании, быстро разрушает многие вещества.… Процесс деградации инсектицида паратиона представлен на рисунке 1.Биотическая трансформация
Процессы элиминации, не связанные с разрушением
Перемещение ветром и атмосферными течениями частицтоксикантов или почвы, на которых адсорбированы вещества, также важный путь перераспределения… Сорбция веществ на взвешенных частицах в воде, с последующим осаждением… Перераспределению водо-растворимых веществ способствуют дожди и движение грунтовых вод. Например, гербицид атразин,…Биоаккумуляция
Водная среда обеспечивает наилучшие условия для биоаккумуляции соединений. Здесь обитают мириады водных организмов, фильтрующих и пропускающих через… Таблица 3. Биоаккумуляция некоторых поллютантов в организме рыб … *Фактор биоаккумуляции - соотношение концентрации поллютанта в тканях рыб и в воде в состоянии равновесия (Le Blanс,…Факторы, влияющие на биоаккумуляцию
Так, синильная кислота, хотя и токсичное соединение, в силу высокой летучести не является, по мнению многих специалистов, потенциально опасным… После поступления веществ в организм их судьба определяется… Вещества, метаболизирующие в организме, накапливаются в меньшем количестве, чем можно было бы ожидать, исходя из их…Значение биоаккумуляции
Биомагнификация
В уже упоминавшейся ранее книге Рашель Карсон УМолчаливая веснаФ приводится такой пример. Для борьбы с переносчиком Уголландской болезниФ,…Экотоксикодинамика
Общие понятия
Механизмы, посредством которых вещества могут вызывать неблагоприятные эффекты в биогеоценозах, многочисленны и, вероятно, в каждом конкретном… Прямое действие - это непосредственное поражение организмов определенной… Опосредованное- это действие ксенобиотического профиля среды на биотические или абиотические элементы среды обитания…Экотоксичность
В соответствии с представлением об уровнях организации биологических систем в экологии принято выделять три раздела (Г.В. Стадницкий, А.И. Родионов,… - аутэкологию - описание экологических эффектов на уровне организма; - демэкологию - экологические эффекты на уровне популяции;Острая экотоксичность
Истории уже известны такие события. Так, в 1984 году в г. Бхопал (Индия) на заводе американской химической компании по производству пестицидов… Другой известный случай острой токсикоэкологической кататстрофы имел место в… В 2000 году в Румынии, на одном из предприятий по добыче драгоценных металлов, в результате аварии произошла утечка…Хроническая экотоксичность
Проявления действия экотоксикантов на человека могут быть самыми разнообразными и при определенных уровнях интенсивности воздействия оказываются… Таблица 5. Влияние тяжелых металлов питьевой воды и атмосферы окружающей среды… В большинстве случаев экотоксиколог сталкивается со случаями именно хронической экотоксичности. По сути, хроническое…Механизмы экотоксичности
1. Прямое действие токсикантов, приводящее к массовой гибели представителей чувствительных видов. Применение эффективных пестицидов приводит к… При оценке экологической обстановки необходимо иметь в виду основной закон… 2. Прямое действие ксенобиотика, приводящее к развитию аллобиотических состояний и специальных форм токсического…Взрыв численности популяции вследствие уничтожения вида-конкурента.
Нетрудно заметить, что приведенные в качестве примеров механизмы экотоксического действия веществ на животных при иных условиях вполне могут реализоваться и в отношении человека.
Экотоксикометрия
Общая методология
Экотоксикометрия - раздел экотоксикологии, в рамках которого рассматриваются методические приемы позволяющие оценить (перспективно или ретроспективно) экотоксичнсоть ксенобиотиков.
Все виды классических количественных токсикологических исследований в полной мере используются для определения экотоксичности ксенобиотиков (см раздел УТоксикометрияФ).
Острая токсичность экополлютантов определяется экспериментально на нескольких видах, являющихся представителями различных уровней трофической организации в экосистеме (водоросли, растения, беспозвоночные, рыбы, птицы, млекопитающие). Агентство по защите окружающей среды США требует при определении критериев качества воды, содержащей некий токсикант, определения его токсичности, по крайней мере, на 8 различных видах пресноводных и морских организмов (16 тестов).
Неоднократно делались попытки ранжировать виды живых существ по их чувствительности к ксенобиотикам. Однако для различных токсикантов соотношение чувствительности к ним живых существ различно. Более того, использование в экотоксикологии Устандартных видовФ представителей определенных уровней экологической организации, для определения экотоксичности ксенобиотиков, с научной точки зрения, не корректно, поскольку чувствительность животных даже близких видов, порой отличается очень существенно.
Условные данные для оценки токсичности веществ для биоты представлены в таблице 6.
Таблица 6. Группы токсичности ксенобиотиков для позвоночных животных
| LC50 для рыб (мг/л) | LD50 для птиц и млекопитающих (мг/кг) | Степень токсичности | Пример |
| более 100 10 - 100 1 - 10 менее 1 | более 5000 500 - 5000 50 - 500 менее 50 | мало токсичные умеренно токсичные токсичные высоко токсичные | барий кадмий дихлорбензол алдрин |
При оценке экотоксичности необходимо учитывать, что хотя практически все вещества могут вызывать острые токсические эффекты, хроническая токсичность выявляется далеко не у каждого соединения. Косвенной величиной, указывающей на степень опасности вещества при его хроническом действии, является соотношение концентраций, вызывающих острые (ЛК50) и хронические (порог токсического действия) эффекты. Если это соотношение менее 10, вещество рассматривается как малоопасное при хроническом воздействии (таблица 7).
Таблица 7. Острая и хроническая токсичность пестицидов для рыб (условия лаборатории)
| Пестицид | ЛК50 (мкг/л) | Токсичность | Порог действия* (мкг/л) | Коэффициент опасности |
| эндосульфан хлордекон малатион карбарил | высокая высокая токсичен умеренная | 4,3 0,3 | 8,8 |
*Пороговая концентрация вещества, по критерию Ухроническая токсичностьФ
При оценке хронической экотоксичности вещества необходимо учитывать следующие обстоятельства:
1. Определение коэффициента опасности является лишь самым первым шагом по определения экотоксического потенциала вещества. В условиях лаборатории пороговые концентрации хронического действия токсикантов определяют, оценивая показатели летальности, роста, репродуктивных способностей группы. Изучение других последствий хронического действия веществ порой может привести к иным числовым характеристикам.
2. Исследования токсичности проводят на животных, пригодных для содержания в условиях лаборатории. Получаемые при этом результаты нельзя рассматривать как абсолютные. Токсиканты могут вызывать хронические эффекты у одних видов, и не вызывать - у других.
3. Взаимодействие токсиканта с биотическими и абиотическими элементами окружающей среды может существенно сказаться на его токсичности в естественных условиях (см. выше). Однако это не подлежит изучению в условиях лаборатории.
Специфическим методом экотоксикометрии является метод оценки экологического риска.
Оценка экологического риска
Оценка экологического риска - это процесс определения вероятности развития неблагоприятных эффектов со стороны биогеоценозов (включая популяции… Как правило оценка экологического риска проводится в форме заказного… Методология оценки экологического риска до конца не разработана. В подавляющем большинстве случаев её выводы носят…Характеристика некоторых экотоксикантов, опасных для человека
Наибольшую опасность, как экотоксиканты, для человека представляют вещества, длительно сохраняющиеся в окружающей среде и организме и способные, действуя в малых дозах, инициировать хронические интоксикации, аллобиотические состояния и специальные формы токсического процесса. К числу таких прежде всего относятся полигалогенированные ароматическкие углеводороды и некоторые металлы.
Полигалогенированные ароматические углеводороды
Галогенированные токсиканты, содержащие один атом кислорода в молекуле, называют дибензофуранами, два атома - диоксинами, если вещества не содержит… Рисунок 4. Структура молекул некоторых полициклических углеводородовДиоксины
2,3,7,8-тетрахлордибензо-пара-диоксин (ТХДД, УдиоксинФ) - самый токсичный представитель группы. При оценке токсичности 2,3,7,8-тетрахлордибензо-пара-диоксина выявляются… Таблица 8. Токсичность диоксина для разных видов животных. Вид животного ЛД50, мкг/кг …Полихлорированные бифенилы (ПХБ)
Такое широкое использование ПХБ было обусловлено их высокой термостойкостью, химической стабильностью, диэлектрическими свойствами. В 70-е годы в… На рисунке 5 представлена структура одного из представителей галогенированных…Хлорированные бензолы (ХБ)
Рисунок 6. Структура молекулы гексахлорбензола Как правило, воздействию веществами люди подвергаются в производственных условиях, однако в последнее время достаточно…Металлы
Кадмий
Cd представляет собой серебристый, кристаллический металл, напоминающий цинк. Валентность кадмия в его кислородных соединениях: +1, +2. Чаще металл образует двухвалентные соединения, включая оксиды, гидроксиды, сульфиды, селениды, теллуриды, галлиды. В водных растворах образует с галлидами комплексные анионы.
Металл широко распространен в окружающей среде. Он встречается в природе в форме редких минералов гринокит (CdS) и отавит (CdCO4). Оба соединения обнаруживаются в цинковых и цинково-свинцовых рудах. Потребление кадмия и загрязнение им почвы, воды и воздуха в результате производственной деятельности неуклонно возрастает. Источниками большинства антропогенных загрязнений являются: выброс кадмия в сточные воды, производство и использование фосфатных удобрений, сжигание отходов, угля бензина и т.д. Однако больше всего в окружающую среду кадмий поступает в виде побочного продукта при выплавке и электролитической очистке Zn.
Таблица 10. Производства и процессы опасные в плане воздействия кадмия
| Производство (выплавка) кадмия Выплавка цинка и свинца Электроанодирование металлов Изготовление кадмиево-никилиевых батарей Переплавка анодированных кадмием металлов Производство сплавов (с медью, серебром) Производство стабилизаторов пластмасс Производство красителей Ювелирное производство Электронная промышленность |
Кадмий относится к числу высокотоксичных металлов. Он действует на самые разные органы и системы. Металл обладает очень высокой кумулятивной способностью. Пары кадмия, образуемые при плавлении, являются чрезвычайно опасными и представляют собой основную причину острых смертельных интоксикаций металлами. Установленные и подозреваемые эффекты кадмия (от гипертонии до канцерогенеза) наряду с его широким и все возрастающим использованием и накоплением в окружающей среде заставляют предположить, что этот металл представляет наивысшую угрозу человечеству, как экополлютант.
В большинстве стран отсутствует регламент на содержание Сd в пищевых продуктах. ВОЗ рекомендует максимально допустимую дозу металла, поступающую с водой и пищей Ц до 400-500 мкг/неделю, в качестве максимально допустимого уровня заражения воздуха концентрацию 10 мкг/м3 .
Токсикокинетика. Поступление кадмия per os - основной путь воздействия, не связанный с производством. Содержание Сd в различных пищевых продуктах колеблется от 0,001 до 1,3 частей на миллион (1,3 мкг/г), а суточное потребление Сd с водой и продовольствием составляет в среднем 10-30 мкг. В сильно загрязненных регионах потребление может составить до 400 мкг/сутки. Особенно много Сd содержится в печени и почках убоины, а также морепродуктах. Растительные продукты в целом содержат больше Сd, чем мясные.
Ингаляция Ц другой важный путь поступления Сd в организм. Средняя концентрация Сd в воздухе в различных регионах неодинакова: в сельской местности - 1-6 нг/м3, в городах - 5-60 нг/м3, индустриальных регионах - 20-700 нг/м3. Ежедневное поступление Сd с вдыхаемым воздухом колеблется в интервале от 0,02 мкг/сут до 2 мкг/сутки. Таким образом, даже в сильно загрязненной местности пища и вода Ц основной источник поражения населения кадмием.
Дополнительный источник поступления кадмия в организм Ц курение. Дело в том, что табак активно кумулирует кадмий, содержащийся в загрязненной почве. Установлено, что курильщик ежедневно выкуривающий пачку сигарет дополнительно ингалирует около 2 мкг Сd/сутки.
Абсорбция кадмия в первую очередь зависит от пути поступления, а затем уже от строения соединения. Большинство солей кадмия плохо абсорбируются в желудочно-кишечном тракте. По расчетам лишь около 5% вещества, попавшего в желудочно-кишечный тракт, всасывается в кровь, хотя ряд факторов, таких как характер пищи и железодефицитная анемия, могут усиливать поступление вещества. Время прохождения металла по желудочно-кишечному тракту достаточно продолжительно, вероятно, вследствие захвата его клетками слизистой оболочки.
Абсорбция в дыхательной системе проходит достаточно полно. В зависимости от степени растворимости в воде ингалированных соединений всасывается до 90% вещества проникшего в глубокие отделы дыхательной системы.
Поступивший в кровь кадмий быстро связывается эритроцитами и альбуминами плазмы. Связавшийся с плазмой металл быстро переходит в различные ткани и органы, преимущественно печень и почки (до 50% поступившего в организм Сd).
Кадмий очень медленно выводится из организма. Период его полувыведения из организма человека составляет по современным оценкам 25-30 лет. Первоначально Сd в неизмененном состоянии выделяется через почки. Однако после развития нефропатии происходит значительное увеличение выведения элемента с мочой в комплексе с металлотионеином.
Примерно 95% Сd, попавшего в желудочно-кишечный тракт, выделяется с калом в силу плохой всасываемости металла.
Токсикодинамика.Кадмий и его соединения представляют реальную опасность, как при остром, так и хроническом воздействии.
Острая интоксикация может развиться как при ингаляционном, так и алиментарном поступлении Сd в организм. Однако для этого нужны достаточно высокие дозы и концентрации. Так, для крыс ЛД50 при внутрижелудочном введении CdO равна 72 мг/кг, CdSO3 - 88 мг/кг, CdCl2 - 94 мг/кг, CdSO4 - 2425 мг/кг. При вдыхании в течение получаса крысами аэрозоля CdO, образующегося при сжигании Cd на пламени электрической дуги, ЛК50, составляет 45 мг/м3.
Хроническое поражение людей зараженной Сd водой, которую использовали для ирригации рисовых полей, проявлялось, в частности, в форме болезни Итай-итай (Япония).
Проявления хронического воздействия кадмия наиболее отчетливо прослеживаются со стороны дыхательной системы и почек. Поражение легких возникает исключительно при ингаляционном способе воздействия, в то время как почки страдают при поступлении кадмия в организм всеми возможными способами.
Другими эффектами хронического действия металла являются поражения опорно-двигательного аппарата, нарушение функций сердечно-сосудистой системы. Длительное введение металла экспериментальным животным (крысы) сопровождается некрозом нервных клеток чувствительных ганглиев и аксональной дегенерацией и демиелинизацией периферических нервных стволов.
Иммуносупрессивное действие кадмия может быть причиной канцерогенеза, встречающегося у работников, контактирующих с металлом.
Данные, полученные на животных свидетельствуют о том, что Сd может быть сильным канцерогеном. Однако проведенные эпидемиологические обследования не привели к получению однозначных результатов. Так, в ходе эпидемиологических исследований, проведенных Waalkes и Oberdorster (1990), не удалось зарегистрировать абсолютную связь между действием Сd и канцерогенезом, хотя в опытах на грызунах было установлено, что хроническое воздействие кадмия приводит к развитию аденокарциномы легких. С другой стороны, установлено, что профессиональное воздействие смеси токсикантов, среди которых был и Сd, приводит к значительному росту числа опухолей почек (Kolonel, 1976). Тем не менее до настоящего времени Сd не рассматривается как безусловный канцероген для человека.
Тератогенное действие Сd выявляется в опытах на животных. У человека тератогенное действие Сd не зарегистрировано.
Заключение
Основные практические результаты в экотоксикологии получаются в настоящее время в ходе эмпирических исследований в реальных полевых условиях и лабораториях. В будущем необходимо продолжить работы, направленные на установление основных феноменов этой науки. Среди них следует отметить следующие направления:
-выявление видов живых организмов (прежде всего среди определяющих благополучие человеческой популяции), обладающих повышенной чувствительностью к наиболее опасным экополлютантам;
-изучение закономерностей взаимодействий ксенобиотиков с абиотическими элементами окружающей среды, приводящих к формированию экотоксических эффектов;
-раскрытие закономерностей формирования неблагоприятных эффектов при сочетанном действии веществ, составляющих ксенобиотический профиль среды, влияние на экотоксичность стрессоров нехимической природы;
- выявление молекулярных и клеточных маркеров, позволяющих выявлять токсическое действие ксенобиотиков на экосистемы, до их проявления на уровне популяций и т.д
ГЛАВА 8.2. СИНДРОМ НЕСПЕЦИФИЧЕСКОЙ ПОВЫШЕННОЙ ХИМИЧЕСКОЙ ВОСПРИИМЧИВОСТИ
Состояние проблемы
Токсикология, как наука, изучающая неблагоприятное действие веществ на биологические системы, отвечает за определение условий, при которых… Дивергенция отношения к химической опасности научного сообщества и населения… Этой дивергенции способствуют и ошибки, периодически возникающие (и неизбежные в процессе познания) в ходе научных…Неспецифическая повышенная химическая восприимчивость, как заболевание
У большинства больных с синдромом ПХВ отсутствуют специфические проявления интоксикаций или заболеваний, диагностируемых клиническими или… - заболевание появляется после воздействия того или иного токсиканта или смеси… - симптомы заболевания провоцируются химическими веществами, действующими в дозах, не вызывающих эффектов у…Клиническая экология
В США и странах Европы развитие клинической экологии сопровождалось рождением многочисленных научных обществ, появлением журнальных публикаций и… Экологические болезни, как утверждалось, являются следствием неспособности… Была сделана попытка обосновать эти представления с позиций иммунологии (см. раздел УИммунотоксичностьФ). Так, по…Диагностика СПХВ
Эти исследования проводят в специальных камерах. В атмосферу камеры помещают вещество и фиксируют (методом опроса) состояние обследуемого. Наиболее… Клинические экологи, прежде всего, обращают внимание на субъективную оценку…Лечение синдрома ПХВ
Перед началом лечения необходимо убедиться в отсутствии реальной соматической патологии. Другая важная задача, стоящая перед врачом - добиться того,…ЛИТЕРАТУРА ПО ТЕМЕ
Акрилонитрил. // Гигиенические критерии состояния окружающей среды. 28. - Женева: ВОЗ, 1987. - 114 с.
Аничков С.В. и соавт. Здравоохранение в условиях химической обороны. Пособие для врачей. - М.-Л.: Гос. Мед. изд., 1931. - 648 с.
Аничков С.В., Лихачев А.А., Предтеченский Б.И. Медико-санитарные основы военно-химического дела. - М.-Л.: Медгиз, 1933. - 155 с.
Бадюгин И.С. (Ред.). Военная токсикология, радиология и защита от оружия массового поражения. - М.: Воен. изд., 1992. - 334 с.
Бадюгин И.С. Токсикология ядохимикатов. - Казань: Татарское книжное издательство, 1976. - 112 с.
Баженов С.В. Ветеринарная токсикология. - Л.: Колос, 1964. - 375 с.
Барбье М. Введение в химическую экологию. - М.: Мир, 1978. - 229 с.
Барышников И.И., Лойт А.О., Савченков М.Ф. Экологическая токсикология. 1 часть. 11 часть. - Изд. Иркутского университета, 1991. - 282 с.
Бережной Р.В. Судебно-медицинская экспертиза отравлений техническими жидкостями. - М.: Медицина, 1977. - 206 с.
Бережной Р.В., Смусин Я.С., Томилин В.В., Ширинский П.П. (Ред.). Руководство по судебно-медицинской экспертизе отравлений. - М.: Медицина, 1980. - 424 с.
Ганжара П.С., Новиков А.А. Учебное пособие по клинической токсикологии. - М.: Медицина, 1979. - 335 с.
Гембицкий Е.В., Алексеев Г.И. (Ред.). Военно-полевая терапия. - Л.: ВМА, 1987. - 342 с.
Глазова О.И. Отравления и первая помощь при них. (Краткий справочник) - М.: Медгиз, 1952. - 163 с.
Глинчиков В.И. Клиника и терапия газоотравленных. - М.: Гос. воен. изд., 1925. - 159 с.
Голиков С.Н. (Ред.). Неотложная помощь при острых отравлениях. Справочник по токсикологии. - М.: Медицина, 1977. - 311 с.
Голиков С.Н. (Ред.). Руководство по токсикологии отравляющих веществ. - М.: Медицина, 1972. - 471 с.
Голиков С.Н., Саноцкий И.В., Тиунов Л.А. Общие механизмы токсического действия. - Л.: Медицина, 1986. - 279 с.
Головко А.И. и соавт. Токсикология ГАМК-литиков. - СПб.: НИВА, 1996. - 141 с.
Головко А.И., Куценко С.А., Ивницкий Ю.Ю. и др. Экотоксикология. - СПб.: НИИХВ СПбГУ, 1999. - 124 с.
Грушко Я.М. Вредные неорганические соединения в промышленных выбросах в атмосферу. Справочник. - Л.: Химия, 1987. - 191 с.
Гусынин И.А. Токсикология ядовитых растений. - М.: Госиздат с/х литературы, 1951. - 295 с.
Демидов А.В. Авиационная токсикология (избранные разделы). - М.: Медицина, 1967. - 143 с.
Досон Р., Эллиот Д., Эллиот У., Джонс К. Справочник биохимика. Пер. с англ. - М.: Мир, 1991. - 544с.
Елизарова О.Н., Жидкова Л.В., Кочеткова Т.А. Пособие по токсикологии для лаборантов. - М.: Медицина, 1974. - 168 с.
Жоголев Д.Т., Келлер А.А. Опасные животные моря и некоторых районов суши. - М.: Воениздат, 1984. - 160 с.
Измеров Н.Ф. (Ред.). Профилактическая токсикология. Сборник учебно-методических материалов. Т.1. - М.: Центр Международных проектов ГКНТ, 1984. - 380 с.
Иличкин В.С. Токсичность продуктов горения полимерных материалов. Принципы и методы определения. - СПб.: Химия, 1993. - 133 с.
Исидоров В.А. Введение в курс химической экотоксикологии. Учебное пособие. - СПб.: Изд. СПб. Университета, 1997. - 88 с.
Исидоров В.А. Введение в химическую экотоксикологию. Учебное пособие. - СПб.: Химиздат, 1999. - 142 с.
Каган Ю.С. Общая токсикология пестицидов. - Киев: Здоровье, 1981. - 174 с.
Каган Ю.С. Токсикология фосфорорганических пестицидов. - М.: Медицина, 1977. - 296 с.
Калоянова-Симеонова Ф. Пестициды. Токсическое действие и профилактика. Пер. с болгарского. - М.: Медицина, 1980. - 304 с.
Карасик В.М. Исторический очерк учения о противоядиях. // Природа, 1939. - N 7.- С. 90 - 94.
Карасик В.М. Противоядия. // Руководство по фармакологии. Т.2 - Л.: Медгиз, 1962. - С. 436 - 452.
Каспаров А.А., Саноцкий И.В. (Ред.). Токсикометрия химических веществ, загрязняющих окружающую среду. - М.: Центр международных проектов ГКНТ, 1986. - 426 с.
Катцунг Б.Г. Базисная клиническая фармакология. Т.1. Пер. с англ. - М.-СПб.: Бином. Невский Диалект, 1998. - 611 с.
Катцунг Б.Г. Базисная клиническая фармакология. Т.2. Пер. с англ. - М.-СПб.: Бином. Невский Диалект, 1998. - 669 с.
Косоротов Д.П. Краткий учебник токсикологии. - СПб.: Типогр. Я. Трея, 1907. - 264 с.
Крылов С.С. и соавт. Клиническая токсикология лекарственных средств. Холинотропные препараты. - СПб.: Изд. Лань, 1999. - 157 с.
Курляндский Б.А., Филов В.А. (Ред.). Вредные химические вещества. Азотсодержащие органические соединения. Справочник. - Л.: Химия, 1992. - 432 с.
Кушнева В.С., Горшкова Р.Б. (Ред.). Справочник по токсикологии и гигиеническим нормативам (ПДК) потенциально опасных химических веществ. - М.: ИздАТ, 1999. - 272 с.
Лазарев Н.В. Основы промышленной токсикологии. - Л.: Медгиз, 1938. - 184 с.
Лазарев Н.В. Эволюция фармакологии. - Л.: Изд. Воен.-Морск. Мед. акад., 1947. - 276 с.
Лазарев Н.В., Гадаскина И.Д. (Ред.). Вредные вещества в промышленности. 111. Неорганические и элементорганические соединения. Справочник для химиков, инженеров и врачей. - Л.: Химия, 1977. - 607 с.
Лазарев Н.В., Гадаскина И.Д. (Ред.). Вредные вещества в промышленности. 11. Органические вещества. Справочник для химиков, инженеров и врачей. - Л.: Химия, 1976. - 623 с.
Лазарев Н.В., Левина Э.Н. (Ред.). Вредные вещества в промышленности. 1. Органические вещества. Справочник для химиков, инженеров и врачей. - Л.: Химия, 1976. - 590 с.
Левина Э.Н. Общая токсикология металлов. - Л.: Медицина, 1972. - 184 с.
Линдеман В. Токсикология химических боевых веществ. Пер. с польского. - М.: Изд. Наркомздрава РСФСР, 1928. - 406 с.
Лойт А.О. Профилактическая токсикология. Раздел 9. Первичная токсикологическая оценка химических веществ. - СПб.: Теза, 1996. - 36 с.
Лужников Е.А. Клиническая токсикология. - М.: Медицина, 1982. - 368 с.
Лужников Е.А. Клиническая токсикология. - М.: Медицина, 1994. - 255 с.
Маркова И.В., Афанасьев В.В., Цыбулькина Э.К. (Ред.). Клиническая токсикология детей и подростков. Часть 2. - СПб.: Интермедика, 1999. - 400 с.
Маркова И.В., Афанасьев В.В., Цыбулькина Э.К., Неженцева М.В. (Ред.). Клиническая токсикология детей и подростков. Часть 1. - СПб.: Интермедика, 1998. - 304 с.
Могош Г. Острые отравления. Диагноз. Лечение. - Бухарест: Мед. изд., 1984. - 579 с.
Монов А. Шоковые состояния при острых токсических и аллергических заболеваниях. - София: Медицина и физкультура, 1982. - 237 с.
Морган Д.Э., Михаил М.С. Клиническая анестезиология. Пер. с нгл. - М.-СПб.: Бином. Невский Диалект, 1998. - 430 с.
Мышьяк // Гигиенические критерии состояния окружающей среды. 18. - Женева: ВОЗ, 1990. - 185 с.
Мясников В.В. (Ред.). Защита от оружия массового поражения. - М.: Воен. изд., 1989. - 398 с.
Новиков В.С. (Ред.). Программированная клеточная гибель. - СПб.: Наука, 1996. - 275 с.
Оксигендлер Г.И. Яды и организм. Проблемы химической опасности. - СПб.: Наука, 1991. - 317 с.
Орлов Б.Н., Гелашвили Д.Б. Зоотоксинология (ядовитые животные и их яды). - М.: Высшая школа, 1985. - 280 с.
Орлов Б.Н., Гелашвили Д.Б., Ибрагимов А.К. Ядовитые животные и растения СССР. - М.: Высшая школа, 1990. - 272 с.
Павловский Е.Н. Ядовитые животные средней Азии и Ирана. Ташкент: Госиздат УзССР, 1942. - 116 с.
Парк Д. Биохимия чужеродных соединений. Пер. с англ. - М.: Медицина, 1973. - 288 с.
Пеликан Е.В. (Ред.). Руководство к токсикологии. Составлено по Рабюто. - СПб., 1878. - 471 с.
Пигулевский С.В. Ядовитые животные. Токсикология беспозвоночных. - Л.: Медицина, 1975. - 375 с.
Пигулевский С.В. Ядовитые животные. Токсикология позвоночных. - Л.: Медицина, 1966. - 386 с.
Пиотровски Е. Использование кинетики метаболизма и выведения токсичных веществ в решении проблем промышленной токсикологии. Пер. с англ. - М.: Медицина, 1976. - 195 с.
Плате Н.А., Васильев А.В. Физиологически активные полимеры. - М.: Химия, 1986. - 294 с.
Правдин Н.С. Руководство по промышленной токсикологии. Выпуск 1. - М.-Л.: Биомедгиз, 1934. - 259 с.
Предтеченский Б.И. Цлаф Я.Б. (Ред.) Пособие по санитарно-химической защите. М.-Л.: Медгиз, 1940. - 518 с.
Принципы изучения болезней предположительно химической этиологии и их профилактика. // Гигиенические критерии состояния окружающей среды. 72. - Женева: ВОЗ, 1990. - 76 с.
Прозоровский В.Б., Саватеев Н.В. Неантихолинэстеразные механизмы действия антихолинэстеразных средств. - Л.: Медицина, 1976. - 160 с.
Розенгарт В.И., Шерстобитов О.Е. Избирательная токсичность фосфорорганических инсектицидов. _ Л.: Наука, 1978. - 174 с.
Рэмсден Э.Н. Начала современной химии. Пер. с англ. - Л.: Химия, 1989. - 784 с.
Саватеев Н.В. (Ред.). Военная токсикология, радиология и медицинская защита. - Л.: ВМА, 1987. - 355 с.
Савицкий Н.Н. (Ред.). Первая помощь и лечение при промышленных отравлениях. Справочник для врачей медсанчастей и здравпунктов. - Л.: Медгиз, 1952. - 84 с.
Сергеев П.В., Шимановский Н.Л. Рецепторы физиологически активных веществ. - М.: Медицина, 1987. - 399 с.
Скарлато О.А. (Ред.). Биотестирование в решении экологических проблем. Сборник научных работ. - СПб.: Рос. АН, 1991. - 135 с.
Сондерс Б. Химия и токсикология органических соединений фосфора и фтора. Пер. с англ. - М.: Изд. иностранной литературы, 1961. - 424 с.
Софронов Г.А., Баринов В.А., Александров М.В. Некоторые вопросы корабельной токсикологии. - СПб.: ВМА, 1998.- 53 с.
Султанов М.Н. Укусы ядовитых животных. Клиника, патогенез, лечение и профилактика укусов змей и других ядовитых животных. - М.: Госиздат мед. лит., 1963. - 152 с.
Тараховский М.Л., Каган Ю.С., Мизюкова И.Г. и др. Лечение острых отравлений. - Киев: Здоровье, 1982. - 232 с.
Титан // Гигиенические критерии состояния окружающей среды. 72. - Женева: ВОЗ, 1986. - 59 с.
Тиунов Л.А., Кустов В.В. Токсикология окиси углерода. - М.: Медицина, 1980. - 286 с.
Толоконцев Н.А., Филов В.А. (Ред.). Основы промышленной токсикологии (руководство). - Л.: Медицина, 1976. - 303 с.
Филов В.А. Определение ядохимикатов в биологических средах. - М.-Л.: Наука, 1964. - 251 с.
Филов В.А., Мусийчук Ю.И., Ивин Б.А. (Ред.). Вредные химические вещества. Природные органические соединения. Т.7. - СПб.: Изд. СПХФА, НПО УМир и Семья-95Ф, 1998. - 504 с.
Филов В.А., Тиунов Л.А. (Ред.). Вредные химические вещества. Галоген- и кислородсодержащие органические соединения. Справочник. - СПб.: Химия, 1994. - 688 с.
Флюри Ф., Церник Ф. Вредные газы. Пер. с нем. - М.: Ред. химической литературы, 1938. - 846 с.
Франке З. Химия отравляющих веществ. Т.1. Пер. с нем. - М.: Химия, 1973. - 436 с.
Худолей В.В., Мизгирев И.В. Экологически опасные факторы. - СПб.: АОЗТ УПФФ, 1996. - 186 с.
Черкес А.И., Луганский Н.И., Родионов П.В. (Ред.). Руководство по токсикологии отравляющих веществ. - Киев: Здоровье, 1964. - 464 с.
Чумаков В.В. и соавт. Токсикологический справочник для врачей Военно-морского флота. - СПб.: МО РФ, 1996. - 130 с.
Шанин В.Ю. Клиническая патофизиология. - СПб.: Специальная литература, 1998. - 569 с.
Шицкова А.П., Рязанова Р.А. Гигиена и токсикология пестицидов. - М.: Медицина, 1975. - 191 с.
Штаркенштейн Э., Рост Э., Поль И. Токсикология. Руководство для врачей, студентов, фармацевтов и судебных работников. Выпуск 1 - М.-Л.: Гос. Мед. изд., 1931. - 222 с.
Штаркенштейн Э., Рост Э., Поль И. Токсикология. Руководство для врачей, студентов, фармацевтов и судебных работников. Выпуск 2 - М.-Л.: Гос. Мед. изд., 1933. - 292 с.
Шустов В.Я. (Ред.). Профессиональные болезни. - Изд. Саратовского университета, 1980. - 297 с.
Эдере Ш. Истен М. Химическое оружие и его токсическое действие. - М.: Гос. Воен. изд., 1938. - 510 с.
Ahrens G. Die Giftprufung. - Leipzig: Johann Ambrosius Barth, 1971. - 214 s.
Bassus W. Gifte im Tierreichen. - Wittenberg, Lutherstadt: A. Ziemsen Verlag, 1963. - 104 s.
Bosshard E. Review on skin and mucous-membrane irritation tests and their application// Fd. Chem. Toxic., 1985. - V. 23, N 2. - pp. 149 - 154.
Cockerham L.G., Shane B.S. (Ed.). Basic Environmental Toxicology. - Boca Raton, Fl.: CRC Press, 1994. - 627 p.
Ecobichon D.J. The Basis of Toxicity Testing. - Boca Raton, Fl.: CRC Press, 1992. - 329 p.
Filov V.A., Golubev A.A., Lublina E.I., Tolokontsev N.A. Quantitative toxicology. - John Wiley & Sons, 1979.- 462 p.
Friemel H., Brock J. Grundlagen der Immunologie. - Berlin: Akademie-Verlag, 1976. - 177 s.
Graumann W. (Editor). Histo- and Cytochemistry as Tool in Environmental Toxicology. - Stuttgart-New York: Gustav Fischer Verlag, 1991. - 415 s.
Hauschild F. Pharmakologie und Grundlagen der Tjxikologie. - Leipzig: VEB Georg Thieme, 1973. - 1251 c.
Hayes A.W. (Ed.). Principles and methods of Toxicology. 2nd ed. - New York: Raven Press, 1989. - 929 p.
Hodgson E., Levi P.E. (Ed.). Introduction to Biochemical Toxicology. 2nd ed. - Norwalk, CT: Appltone & Lange, 1994. - 588 p.
Hodgson E., Levi P.E. Textbook of modern toxicology. - Appleton and Lang, 1997. - 496 p.
Jorgenson S.E. (Ed.). Modeling in Ecotoxicology. - Amsterdam, Oxford, New York, Toktyo: Elsevier, 1990. - 353 p.
Kruger M. Chemische Kampfstoffe (C-Waffen). Teil 2// Dermatosen, 1991. - V. 39, N. 6. - pp. 179 - 193.
Landis W.G., Yu M-H. Introduction to Environmental Toxicology. - Boca Raton, Fl.: Lewis Publishers, 1995. - 328 p.
Liebenow H., Liebenow K. Giftpflanzen. Vademekum fur Tierarzte, Humanmediziner, Biologen und Landwirte. - Jena: VEB Gustav Fischer, 1973. - 213 s.
Loomis T.A., Hayes A.W. Essentials of Toxicology. 4th ed. - San Diego: Academic Press, 1966. - 282 p.
Lu F.C. Basic Toxicology. 2nd ed. Washington: Hemisphere, 1991. - 361 p.
Ludewig R., Lohs K., Akute Vergiftungen. - Jena: VEB Gustav Fischer, 1974. - 633 s.
Paracelsus. Von der Bergsuch und anderen Bergkrankheiten. // Four Treatises of Teophrastus von Hohenheim calld Paracelsus. - Baltimore: Jons Hopkins Press, 1941.
Rang H.P., Bevan S., Dray A. Chemical activation of nociceptive peripheral neurons// British. Medicall Bulletin, 1991. - V. 47, N 3. - pp. 534 - 548.
Trevan J.W. The error of determinaton of toxicity // Proc. R. Soc. Lond., 1927/ - 101 B. - P. 483 - 514.