КАК РИСУЮТ ОРГАНИЧЕСКУЮ МОЛЕКУЛУ

Среди многочисленных разделов химического знания органическая химия больше всех нуждается в символическом языке для обозначения объектов изучения. Химическая формула любого вещества — это его молекулярное «удостоверение личности», в котором отражены основные черты внешнего облика, внутреннего устройства и характера.
На протяжении 200-летней истории развития органической химии учёные, как начинающие художники, учились искусству воссоздания «портретов» молекул — совершенствовали их химические формулы. Самые первые из них появились уже на заре становления науки о соединениях углерода — в начале XIX в. Их предложил шведский химик Якоб Берцелиус — основоположник органической химии и создатель метода элементного анализа вещества. Поскольку такие формулы составлялись исходя из соотношения элементов в соединении, т. е. выводились из данных элементного анализа, их сразу назвали эмпирическими (от греч. «эмпириа» — «опыт»), или брутто-формулами (ит. brutto — «грубый»). При записи использовались символы элементов и индексы, обозначающие количество тех или иных атомов в молекуле. Правда, первые эмпирические формулы немного отличались от современных — индексы было принято писать вверху, после химического символа:
СН4, СН2О2, С2Н6О, C3H8N. Теперь они выглядят так: СН4, СН2О2, G2H6O, C3H8N.
Однако эмпирические формулы указывают только на число атомов различных элементов в молекуле и не дают никакой информации о её строении.
Очень скоро выяснилось, что совершенно разные по физическим и химическим свойствам вещества имеют одинаковые эмпирические формулы. В 1824 г. ученики Берцелиуса

Фридрих Вёлер и Юстус Либих, исследуя состав и свойства цианата и фульмината серебра (AgNCO, AgCNO), открыли явление изомерии. Оказалось, что существуют вещества, которые имеют одну и ту же эмпирическую формулу, т. е. одинаковы по составу, но обладают разными свойствами.
Вслед за открытием Вёлером и Либихом неорганических изомеров французский химик Жан Дюма в 1831 г. обнаружил изомеры среди органических веществ и распространил представление об изомерии на органическую химию. Совместные исследования Либиха и Дюма в 30-х гг. XIX в. привели к созданию первой теории строения органических веществ — теории сложных радикалов. Она дала химикам новые, более подробные полуэмпирические формулы, в которых молекулы веществ представлялись как комбинации радикалов — различных атомов и атомных групп:
СН3Сl, С2Н5ОН, (СН3)2О, C3H7NH2,
C6H5OH, CH3CHO, CH3COOH.
И всё же, несмотря на прогресс в области изучения строения органических молекул, на составление более точных набросков их молекулярных «портретов», внутреннее устройство радикалов и групп атомов по-прежнему было неясным. Невидимая молекула вещества оставалась таинственной «вещью в себе».
Дело в том, что в первой половине XIX в. отсутствовало чёткое понятие о валентности атомов и никто из учёных не мог толком объяснить, каким образом они соединяются в молекулы.
Научные изыскания в этом направлении продолжались, и в 1861 г. появилась теория химического строения, предложенная Александром Михайловичем Бутлеровым. Русский химик ввёл понятие строения органической молекулы как порядка связей между её атомами с учётом их валентностей.
Теория Бутлерова стала настоящей путеводной звездой в «дремучем лесу» органических соединений, а химики получили мощное орудие научного предсказания свойств органических веществ — графические формулы.
Первые такие формулы были очень подробными и громоздкими. В них с помощью валентных штрихов указывались все связи между атомами молекулы. Развёрнутые графические изображения до сих пор используют в учебниках для начинающих химиков.
Очень скоро графические формулы превратились в более удобные — сокращённые, в которых валентными штрихами указывались только связи внутри углеводородного каркаса молекулы и его связи с функциональными группами:
CH3—CH2—OH CH3—O—CH3
При этом, с учётом четырёхвалентности углерода, каждому его атому приписывалось столько одновалентных атомов водорода, сколько необходимо для полного насыщения всех валентностей.
Главным недостатком таких формул было плоскостное изображение органических молекул, среди которых лишь некоторые линейные и циклические действительно были плоскими (ацетилен, ароматические циклы).
В 1874 г. Якоб Вант-Гофф сформулировал основные положения теории пространственного расположения атомов в молекулах органических соединений, что позволило учёным составлять трёхмерные графические формулы.
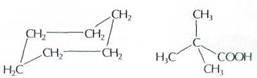
Для многих органических веществ природного происхождения, имеющих сложно устроенные молекулы, и эти графические изображения оказались слишком громоздкими. Их пришлось заменить краткими записями графических формул, где углеродный каркас молекулы обозначается