График зависимости температуры кипения алканов, спиртов, альдегидов и карбоновых кислот с неразветвлённой цепью от числа атомов углерода в молекуле.
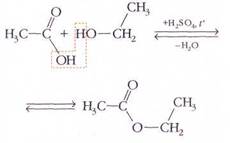
Реакция образования сложных эфиров носит название этерификации (от греч. «этер» — «эфир»). Обычно её проводят в присутствии минеральной кислоты, играющей роль катализатора. При нагревании сложный эфир (или вода, если эфир кипит при температуре выше 100 °С) отгоняется из реакционной смеси, и равновесие смещается вправо. Так, из уксусной кислоты и этилового спирта получают этилацетат — растворитель, входящий в состав многих видов клея:
Многие сложные эфиры представляют собой бесцветные жидкости с приятным запахом. Так, изоамилацетат пахнет грушей, этилбутират — ананасом, изоамилбутират — абрикосом, бензилацетат — жасмином, а этилформиат — ромом. Многие сложные эфиры используются в качестве
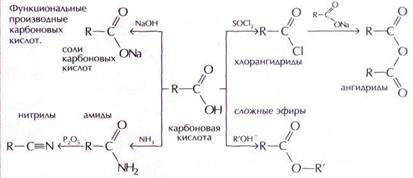
вкусовых добавок при изготовлении различных напитков, а также в парфюмерии. Особенно нежный запах у производных 2-фенилэтилового спирта: эфир этого спирта и фенилуксусной кислоты пахнет мёдом и гиацинтами. А аромат эфира муравьиной кислоты заставляет вспомнить благоухание букета роз и хризантем. В присутствии щёлочи сложные эфиры могут быть гидролизованы — разложены на исходный спирт и соль карбоновой кислоты. При гидролизе жиров (сложных эфиров глицерина и высших карбоновых кислот) образуются основные компоненты мыла — пальмитат и стеарат натрия,
НАЗВАНИЯ НЕКОТОРЫХ КАРБОНОВЫХ КИСЛОТ И ИХ СОЛЕЙ

*Этилацетат— бесцветная нерастворимая в воде жидкость с приятным эфирным запахом (tкип =77,1 °C), смешивается с этиловым спиртом и другими органическими растворителями.
**Названия сложных эфиров образованы из названий соответствующих спиртов и кислот: этилацетат — эфир этилового спирта и уксусной кислоты (уксусноэтиловый эфир), изоамилформиат — эфир изоамилового спирта и муравьиной кислоты (муравьиноизоамиловый эфир).
ЛЕДЯНАЯ КИСЛОТА

В уксусе, который образуется при прокисании вина, содержится около 5% уксусной кислоты (столовым уксусом называют 3—15-процентный раствор). Перегонкой такого уксуса получают уксусную эссенцию — раствор с концентрацией уже 70—80%. А чистая (100-процентная) уксусная кислота выделяется в результате воздействия концентрированной серной кислоты на ацетаты: CH3COOHNa+H2SO4 (конц.)= CH3COOH+NaHSO4.
Такая чистая уксусная кислота, не содержащая воды, при охлаждении до 16,8 °С превращается в прозрачные кристаллы, напоминающие лёд. Вот почему её иногда называют ледяной.
Сходство не только внешнее: в кристаллах молекулы уксусной кислоты,
