Гидроксид-ионов: CH3NH2+Н2О=CH3NH3++ОН-.
При взаимодействии большинства алифатических аминов с водой концентрация гидроксильных ионов возрастает настолько, что помещённый в раствор индикатор показывает щелочную среду.
При алкилировании (введении в органическую молекулу углеводородного радикала) первичных и вторичных аминов атомы водорода при азоте последовательно замещаются на различные группы:

При действии на алкиламмониевую соль щёлочью выделяется свободный амин:
[(CH3)3NH]+Br+КОН=(CH3)3N+KBr+Н2О.
Конечным продуктом алкилирования является соль четвертичного аммониевого основания:
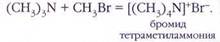
В живом организме четвертичные аммониевые соли играют важнейшую роль в передаче нервных импульсов.
В реакциях аминов с карбоновыми кислотами или их функциональными производными (ангидридами, хлорангидридами) образуются амиды — производные аммиака, в которых при атоме азота находится карбонильная группа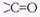 .
.
Ацилирование (введение ацильной группы RC(O)) анилина уксусным ангидридом приводит к ацетанилиду, который препятствует сворачиванию крови и поэтому называется антифибрином (от лат. fibra — «волокно»). Его производное -- пара-гидроксиацетанилид используется в медицине в качестве болеутоляющего и жаропонижающего средства парацетамола.

Амидная группа входит в состав таких необходимых для живых организмов соединений, как пептиды, белки, нуклеиновые кислоты (см. статьи «Азбука живой материи. Белки», «Хранитель наследственной информации. ДНК»),
УРОТРОПИН
В 1860 г. А. М. Бутлеров обнаружил, что взаимодействие водных растворов аммиака и формальдегида приводит к образованию белого кристаллического вещества — уротропина (гексаметилентетрамина C6H12N4):
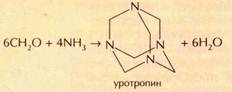
Атомы углерода и азота в молекуле уротропина расположены в пространстве так же, как атомы углерода в элементарной ячейке алмаза.
Это вещество используется как «сухое горючее» (так называемый твёрдый спирт), а также входит в состав некоторых лекарств.